2. 盐城师范学院江苏省农业养殖污染治理与资源化工程研究中心, 盐城 224007;
3. 中国科学院南京土壤研究所中国科学院土壤环境与污染修复重点实验室, 南京 210008
2. Jiangsu Province Engineering Research Center of Agricultural Breeding Pollution Control and Resource, Yancheng Teachers University, Yancheng 224007, China;
3. Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China
四环素类抗生素(TCs)包括四环素、土霉素、金霉素和强力霉素等, 广泛用于医药、畜牧业和水产养殖等行业[1].摄入动物和人体内的TCs代谢程度低, 约有60% ~ 90%的TCs以原形或活性中间体的形式随代谢产物进入环境[2].环境中的抗生素不仅影响生态系统中微生物群落结构与功能, 还会诱导病原菌微生物产生耐药性[3], 引起较严重的环境问题.近年来, 抗生素污染控制已成为人们关注重点之一[4 ~ 6].
目前物理、化学和生物技术均已被广泛用于抗生素污染控制领域.其中, 吸附技术因操作简单和成本低廉等优点, 在去除有机污染物方面应用广泛[7].近年来, 生物炭因吸附性能好、成本低廉、原料易得和生态安全等优点, 已成为环境科学领域的研究热点之一[8 ~ 10].生物炭制备原料和制备条件等对其比表面积、孔隙结构、表面官能团和元素组成等理化性质有较大影响, 并决定其吸附性能和应用前景.目前, 畜禽粪便、花生壳、木屑、果壳和作物秸秆等农业废弃物被制备成生物炭并用于水中污染物的吸附去除[11 ~ 13].然而, 在缺氧或无氧条件下将生物质直接裂解炭化制得的生物炭吸附能力有限, 难以达到高效去除污染物的要求[14].通过对原始生物炭进行氧化、还原及负载物质等方式改性, 可以改变其表面官能团种类及数目、改善孔隙结构并提高比表面积, 从而显著提升其吸附性能[15 ~ 19].有研究发现, 800 ~ 1000 ℃的高温物理活化或硫酸、氢氧化钾、高锰酸钾和碳酸钾等化学试剂改性均可提高生物炭的吸附性能[14, 20].但大多研究只关注改性剂类型、改性剂用量、活化时间和高活化温度等因素对生物炭结构和吸附性能的影响, 而关于“化学试剂改性、中低温活化”两步优化法对改性生物炭吸附性能影响的研究较少.
农作物秸秆具有较大的制备生物炭潜力, 也是我国农业领域实现碳减排的有效利用途径之一[24, 25].为此, 本文以玉米秸秆为原料, 首先制备不同炭化温度的热解生物炭(BC), 采用氢氧化钾对BC进行改性制得KBC, 并选择具有最佳吸附性能的KBC在不同温度下进行二次热解活化处理, 最终制得AKBC.以代表性四环素类抗生素——盐酸土霉素(OTC)为目标污染物, 比较BC、KBC和AKBC对水中OTC的吸附性能差异, 探讨AKBC对OTC的吸附特性、机制及溶液初始pH和腐殖酸的影响, 以期为改性秸秆生物炭高效去除环境中四环素类抗生素提供理论依据.
1 材料与方法 1.1 药品与试剂盐酸土霉素(纯度 > 97%, 分子式C22H24N2O9∙HCl, 简称OTC)、腐殖酸(AR), 购自百灵威科技有限公司.氢氧化钾、氢氧化钠和盐酸均为AR级, 购自国药集团化学试剂有限公司.乙腈为色谱纯, 购自阿拉丁试剂有限公司.
1.2 改性生物炭的制备与吸附性能测试 1.2.1 改性生物炭的制备以玉米秸秆为原料, 参考文献[13]采用限氧控温炭化法制备400、500和600℃时的热解玉米秸秆生物炭(BC400、BC500和BC600).
BC的改性:采用最佳碱炭质量比为2∶1的氢氧化钾对3种BC进行碱改性处理, 称取5 g BC于烧杯中, 加入100 mL浓度为100 g·L-1的KOH, 搅拌均匀后超声30 min, 静置12 h后置于烘箱105℃烘干, 制得KBC400、KBC500和KBC600.
KBC的活化:选择KBC400进行二次热解活化处理, 将KBC400置于氮气氛炉内, 以10℃·min-1的速率升温至不同温度(400、500和600℃)活化2 h后, 经酸洗、水洗、105℃烘干后, 最终制得改性玉米秸秆生物炭(AKBC400、AKBC500和AKBC600).
1.2.2 吸附性能测试分别称取0.050 g的BC、KBC和AKBC于150 mL具塞锥形瓶中, 加入50 mL浓度为100 mg·L-1的OTC溶液(用1.0 mol·L-1的盐酸溶液或氢氧化钠溶液调节pH = 7.0), 将锥形瓶密封后放置在恒温振荡器(DHZ-DA, 太仓实验设备厂)内以150 r·min-1转速, 25℃恒温振荡24 h后, 取样过0.45 μm滤膜, 通过高效液相色谱仪(e2695, 美国waters公司)测定吸附液中OTC的浓度, 比较吸附性能差异.
1.3 改性生物炭的表征改性生物炭表面形貌特征通过场发射扫描电子显微镜(JEOL JEM-1400 plus, 日本JEOL公司)进行分析;采用全自动气体吸附分析仪(Autosorb-iQ, 美国Quantachrome公司)测定生物炭表面性质参数;生物炭的C、H、N含量采用元素分析仪(2400 II, 美国PE公司)测定;采用傅里叶变换红外光谱仪(VERTEX 80, 德国Bruker公司)对生物炭表面官能团进行分析.
1.4 批量吸附实验 1.4.1 吸附动力学实验称取0.050 g生物炭于150 mL具塞锥形瓶中, 加入50 mL浓度为200 mg·L-1的OTC溶液(pH = 7.0), 将锥形瓶置于恒温振荡器中, 150 r·min-1转速、25℃下恒温振荡, 于设定时间点取样测定吸附液中OTC的浓度.
1.4.2 等温吸附实验称取0.050 g生物炭于150 mL具塞锥形瓶中, 加入50 mL浓度分别为50、100、150、200和250 mg·L-1的OTC溶液(pH = 7.0), 将锥形瓶置于恒温振荡器中, 温度依次设置为15、25、35和45℃, 转速为150 r·min-1, 恒温振荡24 h后, 取样测定OTC的浓度.
1.4.3 pH对生物炭吸附OTC的影响称取0.050 g生物炭于150 mL具塞锥形瓶中, 加入50 mL浓度为200 mg·L-1的OTC溶液, 用1.0 mol·L-1的盐酸溶液或氢氧化钠溶液调节pH值分别为3.0、5.0、7.0、9.0和11.0, 在25℃、150 r·min-1条件下, 振荡24 h后, 取样测定OTC的浓度.
1.4.4 腐殖酸对生物炭吸附OTC的影响称取0.050 g生物炭于150 mL具塞锥形瓶中, 加入50 mL含不同浓度腐殖酸的OTC溶液(200 mg·L-1, pH = 7.0), 25℃、150 r·min-1条件下, 恒温振荡24 h后, 取样测定OTC的浓度.
1.4.5 再生吸附性能将吸附饱和后的生物炭用0.5 mol·L-1氢氧化钠溶液超声脱附再生、水洗、烘干后, 用于重复利用实验.OTC溶液浓度为100 mg·L-1(pH = 7.0), 生物炭用量为0.050 g, 在25℃下恒温振荡24 h后, 取样测定OTC的浓度.
1.5 OTC分析与数据处理OTC测试条件:高效液相色谱仪配置150 mm×4.6 mm C18柱, 柱温为30℃, 流动相为乙腈∶水(0.01 mol·L 1磷酸) = 50∶50(体积比), 流速为1.0 mL·min-1, 紫外检测器波长为360 nm.
生物炭对OTC的吸附量由式(1)计算:
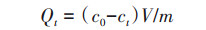
|
(1) |
式中, Qt为t时刻生物炭对OTC的吸附量(mg·g-1), ct为t时刻溶液中OTC的浓度(mg·L-1), c0为OTC初始浓度(mg·L-1), V为OTC溶液体积(L), m为生物炭的质量(g).
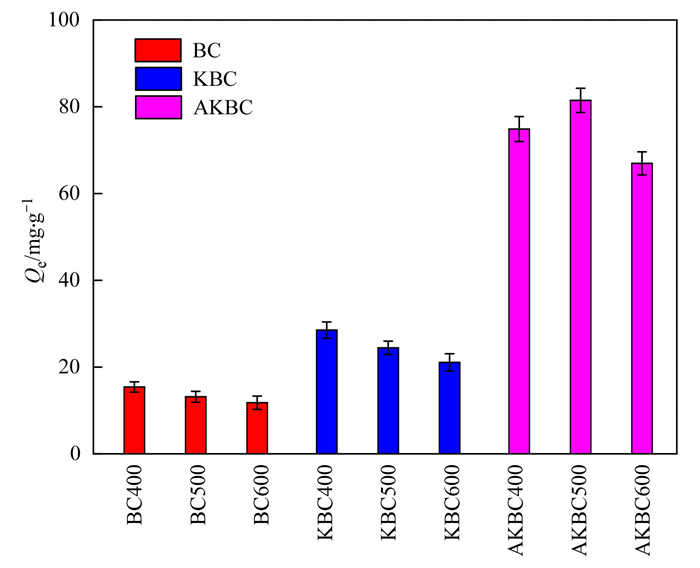
2 结果与讨论 2.1 不同处理生物炭对OTC的吸附性能比较炭化温度和改性方式对生物炭的性质有显著影响, 进而影响其对污染物的吸附性能.BC、KBC和AKBC对OTC的吸附性能比较如图 1所示.由图 1可知, BC400、BC500和BC600对OTC的吸附量分别为15.41、13.15和11.78 mg·g-1, BC400吸附量最大, 但总体而言, 直接热解玉米秸秆炭对OTC的吸附容量较低.KBC400、KBC500和KBC600对OTC的吸附量分别为28.53、24.43和21.08 mg·g-1, 表明热解玉米秸秆炭经氢氧化钾改性后, 可在一定程度上提高其吸附容量, 但吸附性能提升效果不佳.而AKBC400、AKBC500和AKBC600对OTC吸附量分别为74.8、81.48和66.96 mg·g-1, 吸附量是KBC400的2.35 ~ 2.86倍, 吸附性能显著提升.
|
图 1 不同类型玉米秸秆生物炭对OTC的吸附性能 Fig. 1 Adsorption performance of OTC by biochars |
通过分析BC、KBC和AKBC的比表面性质参数(表 1), 进一步探讨了不同处理方式对生物炭吸附OTC性能的影响.由表 1可知, BC400、BC500和BC600的比表面积为8.978 ~ 13.58 m2·g-1, 总孔体积为0.031 3 ~ 0.039 5 cm3·g-1, 表明直接热解制备的玉米秸秆生物炭表面性质参数较差.当BC经氢氧化钾改性后, 所制备的KBC比表面积、总孔体积和微孔体积均有所增加, 故吸附量有所增大.将KBC400继续在400℃和500℃活化后制得的AKBC400和AKBC500的比表面积分别为385.7 m2·g-1 和510.2 m2·g-1, 微孔体积分别为0.217 8 cm3·g-1和0.288 7 cm3·g-1, 表明中低温活化可显著增加其比表面积和微孔体积.而继续升高活化温度至600℃时, AKBC600比表面积和微孔体积反而减小至312.7 m2·g-1和0.172 8 cm3·g-1, 这可能是因为活化温度过高时, BC400与KOH反应过于剧烈, 所形成的部分微孔壁塌陷, 出现“扩孔”现象[21], 从而减小了其比表面积和微孔体积.对比3种AKBC表面性质可知, AKBC500具有最大的比表面积、总孔体积和微孔体积, 这与AKBC500具有最大的吸附容量结果一致.本实验结果表明, 玉米秸秆生物炭经2∶1碱炭比的氢氧化钾改性、500℃活化处理, 可以显著提升其对OTC的吸附性能.后续实验选择AKBC为吸附剂, 对其进行进一步表征, 并以BC400为对照, 探讨3种AKBC对OTC的吸附特性和机制.
|
|
表 1 玉米秸秆生物炭的表面性质参数 Table 1 Surface properties of biochars |
2.2 生物炭的表征 2.2.1 SEM表征分析
图 2为BC400和AKBC的SEM照片.由图 2(a)可知, 改性活化前BC400表面较光滑;而由图 2(b) ~ 2(d)可知, 经KOH改性后的AKBC表面变得十分粗糙, 且不同温度活化后的AKBC形成了不同的孔隙结构.活化温度由400℃升至500℃时, AKBC的孔隙结构更为丰富, 而活化温度继续升至600℃时, 反而不利于孔隙的形成.在KOH活化BC400过程中, BC400与其表面均匀分布的KOH反应并形成微孔, 所产生的微孔作为继续反应的界面, 在一定范围内提高活化温度, 有利于促进更多微孔的形成[26];而活化温度过高时, 会不断促进活化反应的进行, 从而导致所形成的微孔逐渐减少, 从而减小其比表面积.SEM结果表明, BC400经KOH改性、500℃活化, 可以显著改善其表面形貌和孔结构.

|
图 2 玉米秸秆生物炭的SEM照片 Fig. 2 SEM images of BC400 and AKBC |
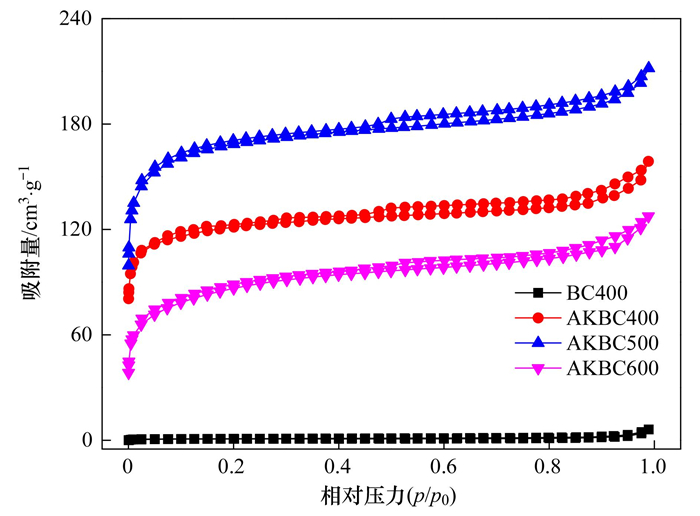
BC400和AKBC的N2吸附-脱附曲线如图 3所示, 在p/p0 < 0.1范围内, 吸附曲线均迅速上升, 说明存在较丰富的微孔, p/p0在0.1 ~ 1.0范围内上升缓慢, 表明在高相对压力区对N2吸附量较小.根据IUPAC分类可知, 该N2等温线符合Ⅰ型等温线特征[17].3种AKBC的N2吸附-脱附曲线在p/p0 > 0.4时, 出现脱附滞后现象, 形成H4型滞后环, 说明AKBC样品中存在一定的中孔结构;而当p/p0 > 0.9时, N2吸附曲线仍在上升, 说明也存在一定数量的大孔[14].
|
图 3 玉米秸秆生物炭的N2吸附-脱附等温线 Fig. 3 N2 adsorption-desorption isotherm curves of BC400 and AKBC |
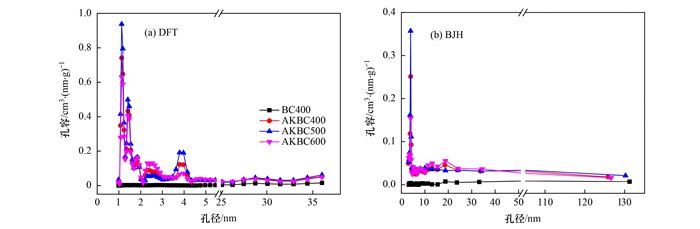
为进一步明确改性前后BC400的孔径变化情况, 采用DFT法和BJH法分析了BC400和AKBC的孔径分布, 结果见图 4.由图 4(a)可知, AKBC的孔分布主要集中在1 ~ 2 nm微孔和2 ~ 5 nm中孔范围内;由图 4(b)可知, 在10 ~ 25 nm范围内有少量的中孔分布, 而大于50 nm的大孔分布较少.由表 1可知, AKBC500的平均孔径最小, 表明BC400经2∶1碱炭比的氢氧化钾改性、500℃活化处理, 其孔隙结构改善效果最佳.
|
图 4 玉米秸秆生物炭的孔径分布 Fig. 4 Pore size distribution of BC400 and AKBC |
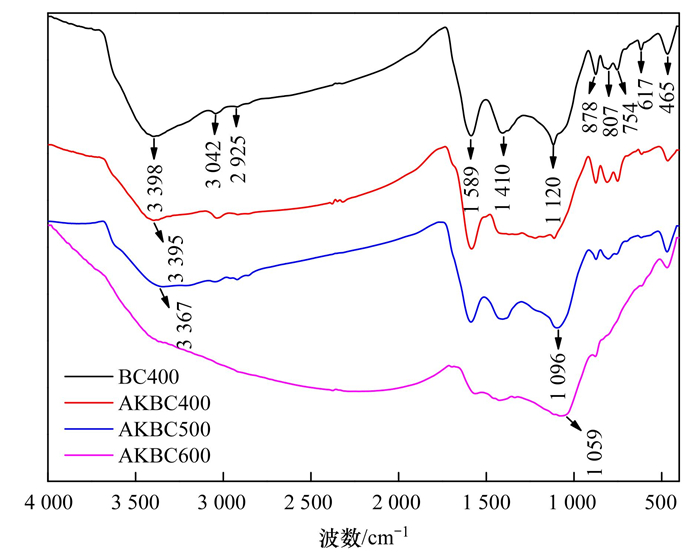
BC400经氢氧化钾改性及不同温度活化前后的FT-IR如图 5所示, 其表面官能团性质发生明显变化.改性前BC400在3 398 cm-1处的特征峰对应为—OH或—NH、—NH2的伸缩振动峰, 在2 925 cm-1的吸收峰为饱和C—H伸缩振动峰;在1 589 cm-1处的吸收峰为芳香环C=C或C=O伸缩振动、N—H变形振动峰[27], 在1 120 cm-1处的吸收峰为脂肪族化合物C—O伸缩振动峰.与BC400相比, AKBC在3 398 cm-1处的特征峰随着活化温度的升高逐渐发生红移, 且吸收峰强度明显减弱, 在2 925 cm-1和1 589 cm-1处的特征峰基本消失, 说明经氢氧化钾改性及不同温度活化后, BC400中的部分有机官能团被分解, AKBC芳香化程度增加[28].
|
图 5 玉米秸秆生物炭的FT-IR图 Fig. 5 FT-IR spectra of BC400 and AKBC |
BC400和AKBC的元素分析如表 2所示.由表 2可知, BC400经KOH改性活化后, 元素含量发生了较大变化.当活化温度由400℃升高到600℃时, C含量由61.36%增加至72.58%, 而N、H和O含量均降低, 表明BC400的改性活化过程是有机组分富碳、去极性官能团的过程[29, 30].对比3种AKBC的原子比可知, (O+N)/C、O/C和H/C值均随着活化温度的升高而减小, 表明随着活化温度升高, AKBC的极性和亲水性下降, 而芳香性增强[31], 这与FT-IR分析结果一致.
|
|
表 2 玉米秸秆生物炭的元素分析 Table 2 Element analysis of BC400 and AKBC |
2.3 吸附动力学
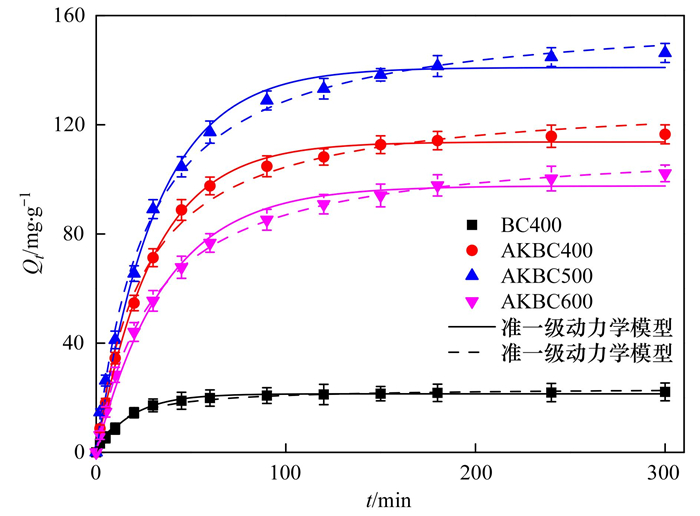
BC400和AKBC对OTC的吸附动力学曲线如图 6所示.由图 6可知, BC400对OTC吸附量在前60 min基本达吸附平衡, 而AKBC400、AKBC500和AKBC600在前60 min内急剧增加, 150 min后基本达吸附平衡, 平衡吸附量显著高于BC400, 且AKBC500吸附量最大, 这与3种AKBC的表面性质参数相对应.
|
图 6 玉米秸秆生物炭吸附OTC动力学曲线 Fig. 6 Adsorption kinetics of OTC on BC400 and AKBC |
分别采用准一级动力学模型[式(2)]、准二级动力学模型[式(3)]、颗粒内扩散模型[式(4)]和膜扩散模型[式(5)][32 ~ 34]对吸附动力学数据进行拟合:
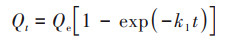
|
(2) |
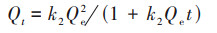
|
(3) |
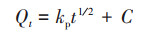
|
(4) |
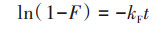
|
(5) |
式中, t为吸附时间(min), Qe为平衡吸附量(mg·g-1), Qt为t时刻吸附量(mg·g-1), k1(min-1)、k2(mg·g-1·min-1)、kp(mg·g-1·min-1/2)和kF(mg1-(1/n)·g-1·L1/n)均为相应模型的吸附速率常数, C为反应边界层效应(mg·g-1), F为Qt与Qe的比值(L·g-1).
BC400和AKBC对OTC的吸附动力学拟合曲线见图 6, 扩散模型拟合曲线见图 7, 拟合数据结果见表 3和表 4.由表 3可知, 与准一级动力学模型(R12值为0.977 3 ~ 0.982 6)相比, 准二级动力学模型(R22值为0.990 8 ~ 0.993 8)的拟合系数更高, 说明准二级动力学模型可以更好地拟合BC400和AKBC对OTC的吸附过程.表明BC400和AKBC对OTC的吸附过程不是简单的物理扩散过程, 而是物理吸附与化学吸附密切相关的过程[22, 23, 35].AKBC对OTC的吸附速率常数k2和理论饱和吸附量Qe均显著高于BC400, 且AKBC500的k2和Qe值最大.
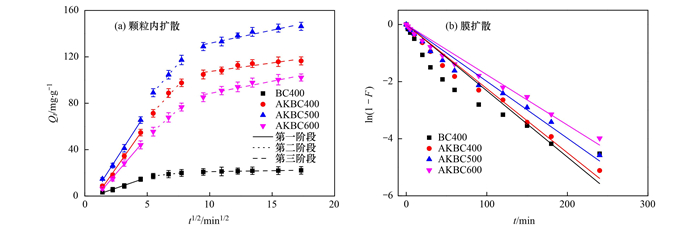
|
(a) 颗粒内扩散, (b) 膜扩散 图 7 颗粒内扩散和膜扩散模型拟合曲线 Fig. 7 Fitting curves of intra-particle diffusion and film diffusion model |
|
|
表 3 准一级和准二级动力学模型拟合参数1) Table 3 Pseudo-first-order and pseudo-second-order kinetic parameters |
|
|
表 4 颗粒内扩散和膜扩散动力学拟合参数1) Table 4 Intra-particle and film diffusion kinetic parameters |
由图 7(a)和表 4可知, 整个控制过程可分为3个阶段, 第一阶段为OTC迅速扩散到BC和AKBC表面的过程, kp1值较高;第二阶段为OTC在BC400和AKBC颗粒内大孔扩散过程, kp2值略有减小;第三阶段为OTC向BC400和AKBC颗粒内中孔和微孔扩散过程[20], 此时BC400和AKBC对OTC基本达吸附平衡, 且kp3值最小, 表明第三阶段为主要控速过程[34].此外, 3个阶段的拟合曲线均不通过原点, 表明颗粒内扩散作用并不是唯一的控速步骤, BC400和AKBC对OTC的吸附过程较为复杂[13, 36].对比3个阶段的kp值可知, AKBC颗粒内扩散速率均显著高于BC400, 且AKBC500的kp值均最大, 这可能是因为AKBC500具有最大的比表面积和最丰富的孔隙结构所致.图 7(b)为膜扩散模型拟合曲线, 其拟合系数RF2值为0.848 2 ~ 0.978 2(表 4), kF(BC400) > kF(AKBC400) > kF(AKBC500) > kF(AKBC600), 表明BC400表面的膜扩散速率更快, AKBC表面膜扩散速率随着生物炭活化温度的升高反而减小, 这可能是因为活化温度越高, 生物炭中的有机官能团被分解的程度越大, 越不利于OTC在生物炭表面膜扩散过程的进行.
2.3 吸附等温线BC400和AKBC对OTC的吸附等温线如图 8所示, 随着温度的升高, 对OTC的吸附量均增加, 表明升高温度有利于生物炭对OTC的去除.与BC400相比, AKBC对OTC的吸附量显著增大, 主要是因为BC400经氢氧化钾改性进而刺激热解活化后, 显著改善了其孔隙结构并增加了比表面积, 可以为OTC提供更多的吸附位点[13].
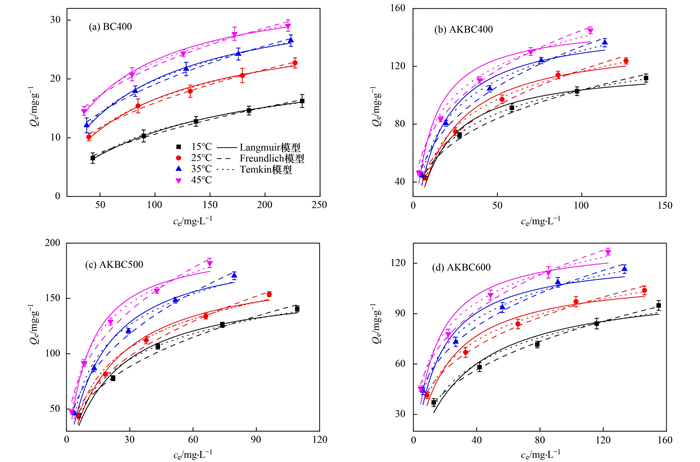
|
图 8 玉米秸秆生物炭对OTC的吸附等温线 Fig. 8 Adsorption isotherms of OTC on BC400 and AKBC |
采用Langmuir[式(6)]、Freundlich[式(7)]和Temkin[式(8)]模型[13]对吸附等温线进行拟合:
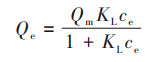
|
(6) |
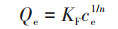
|
(7) |
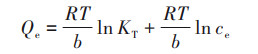
|
(8) |
式中, Qe为达平衡时的吸附量(mg·g-1), ce为吸附平衡时浓度(mg·L-1), Qm为理论饱和吸附量(mg·g-1), KL为Langmuir模型吸附常数(L·mg-1), KF为Freundlich模型吸附常数(mg1-(1/n)·L1/n·g-1), n为异质性因素, KT为Temkin模型平衡结合常数(L·g-1), b为Temkin模型常数, R为气体常数, T为热力学温度(K).3种模型拟合曲线见图 8, 拟合结果见表 5.
|
|
表 5 玉米秸秆生物炭对OTC的等温吸附拟合参数 Table 5 Isotherm equation parameters of OTC on BC400 and AKBC |
由表 5可知, Langmuir模型和Freundlich模型的拟合系数分别为0.970 5 ~ 0.989 6(RL2)和0.982 8 ~ 0.998 4(RF2), 均能较好地拟合吸附等温线, 说明BC400和AKBC对OTC的吸附过程不是简单的单分子层吸附, 吸附机制较复杂, 这可能与生物炭表面官能团及表面性质有关[13].由Langmuir模型拟合的Qm值可知, 318 K时, AKBC500对OTC的最大理论饱和吸附量可达192.1 mg·g-1.Freundlich模型的KF与吸附剂吸附容量呈正相关.由表 5可知, BC400和AKBC的KF值均随着温度的升高而增大, 表明升高温度有利于吸附的进行;n值均大于1, 表明BC400和AKBC对OTC的吸附过程为优惠吸附.Temkin模型拟合系数RT2为0.968 1 ~ 0.999 0, 表明强静电作用或离子交换作用存在于BC400和AKBC对OTC的吸附过程中[2].
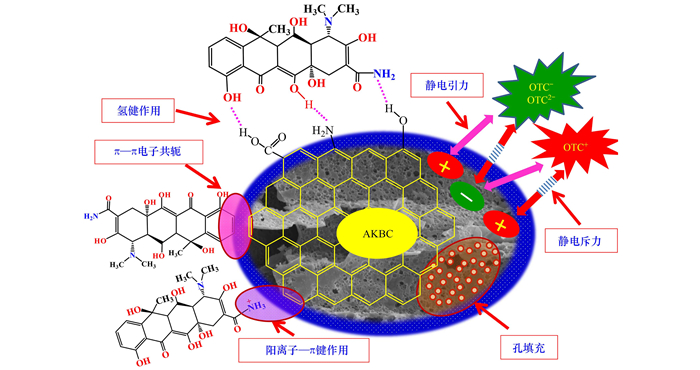
2.4 吸附热力学吸附热力学参数能够反映吸附过程驱动力和能量变化.BC400和AKBC对OTC的吸附热力学参数焓变ΔHθ(kJ·mol-1)、熵变ΔSθ(J·K-1·mol-1)和吉布斯自由能变ΔGθ(kJ·mol-1)通过式(9)和式(10)[13]计算:
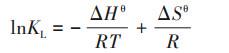
|
(9) |
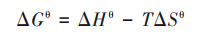
|
(10) |
式中, R为气体常数, T为热力学温度(K), KL为Langmuir方程常数(L·mg-1).
由表 6可知, ΔHθ均为大于0, 说明吸附过程吸热.不同温度时, ΔGθ值均小于0, 说明BC400和AKBC对OTC的吸附是自发的过程;且ΔGθ值随着温度的升高而减小, 表明升高温度有利于吸附的进行.此外, AKBC400、AKBC500和AKBC600的ΔGθ值均小于-20 kJ·mol-1, 说明AKBC对OTC的吸附过程存在化学吸附作用[13, 37].ΔSθ均为正值, 说明OTC吸附到BC400和AKBC过程中固-液两相界面的自由度增大[22].
|
|
表 6 玉米秸秆生物炭对OTC的吸附热力学参数 Table 6 Thermodynamic parameters of OTC on BC400 and AKBC |
2.5 pH的影响
溶液pH影响生物炭的表面电荷, 并决定吸附质的电离程度, 在吸附过程中起着重要作用[37, 38].OTC具有—OH和—NH2等极性基团, 3个pKa值分别为3.27、7.32和9.11[39], 在不同pH范围内, 分别以OTC+(pH < 3.27)、两性离子OTC0(3.27 ≤ pH < 7.32)、OTC-(7.32 ≤ pH < 9.11)及OTC2-(pH ≥ 9.11)形式存在[40, 41].不同pH对AKBC吸附OTC的影响如图 9所示.由图 9可知, 当pH值为3.0时, AKBC的吸附量较低, 此时溶液中OTC主要以OTC+阳离子形态存在, 不利于吸附的进行.而当pH值由3.0增加至4.0 ~ 7.0时, AKBC对OTC的吸附量增加, 此时主要以中性分子OTC0形式存在, 其与AKBC间的静电引力或斥力作用最小, 有利于OTC的吸附去除.而当pH继续增加至9.0 ~ 11.0时, OTC逐渐解离成负离子形态的OTC-和OTC2-, 此时生物炭表面的—OH和—COOH等基团发生去质子化而带有负电荷, 两者间存在较强的静电斥力[42], 从而导致AKBC对OTC的吸附作用减弱, 吸附量减小.
|
图 9 pH对AKBC吸附OTC的影响 Fig. 9 Effect of pH on adsorption of OTC by AKBC |
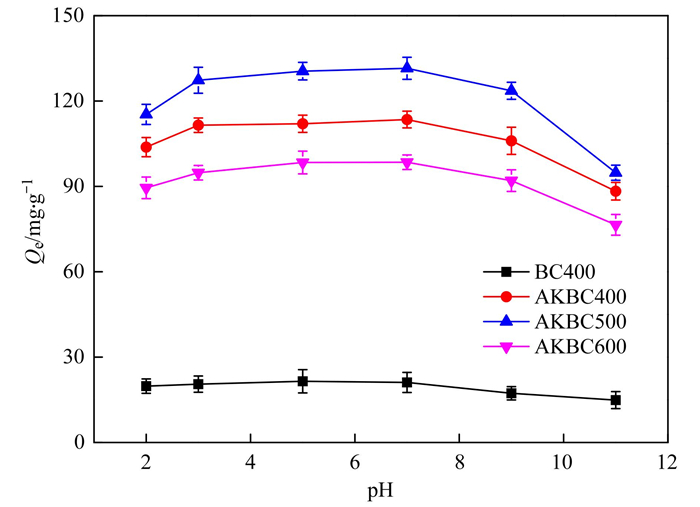
腐殖酸在水和废水中普遍存在并影响污染物的吸附去除.不同浓度腐殖酸对AKBC吸附OTC的影响如图 10所示.由图可知, 加入5 ~ 10 mg·L-1的腐殖酸后, AKBC400和AKBC500对OTC的吸附量略有增加, 而AKBC600对OTC的吸附量变化不大;当腐殖酸浓度继续增加至15 ~ 25 mg·L-1时, 3种AKBC对OTC的吸附量均减小.这可能是因为腐殖酸是大分子有机质, 体系中浓度过高时, 会占据AKBC表面吸附位点并堵塞其孔隙[43], 与污染物产生竞争吸附[44], 从而不利于AKBC对OTC的吸附.由3种AKBC元素分析结果可知, 相对于AKBC600而言, AKBC400和AKBC500表面—OH和—NH2等官能团含量更为丰富, 能通过氢键或静电引力吸附腐殖酸[45], 而吸附在AKBC表面的腐殖酸又可以与OTC分子中的—OH和—NH2等基团形成氢键, 使得AKBC400和AKBC500表面形成新的吸附位点[46].因此, 加入较低浓度的腐殖酸时, 有利于AKBC400和AKBC500对OTC的吸附.
|
图 10 腐殖酸对AKBC吸附OTC的影响 Fig. 10 Effect of humic acid on adsorption of OTC by AKBC |
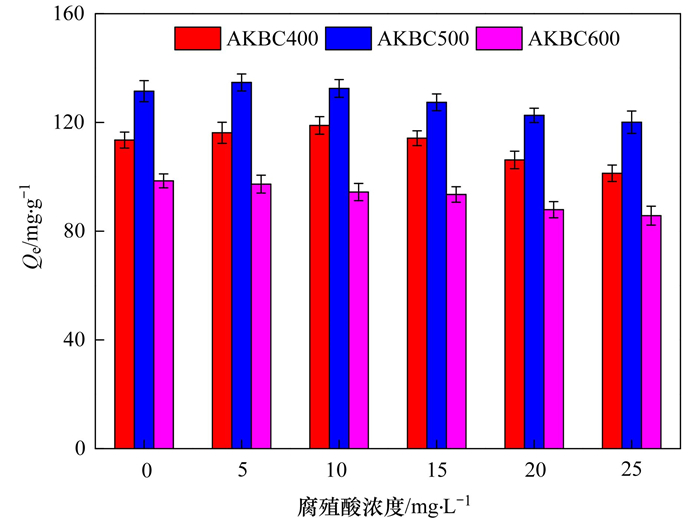
AKBC具有较高的比表面积和较丰富的孔隙结构, 同时表面有较丰富的—OH、—NH2和—COOH等基团, 由吸附实验结果可知, 其吸附机制比较复杂, 所推测的AKBC与OTC间的作用机制见图 11.首先, 溶液中的OTC迅速扩散到AKBC表面, 发生膜扩散作用, 并继续向AKBC的大孔、中孔和微孔内进行扩散填充[13, 39].AKBC表面含有较丰富的—OH、—NH2和—COOH等基团, OTC分子有—OH、—NH2和—C=O等基团, 两者均既可作为氢键受体, 又可作为氢键供体而发生强烈的氢键相互作用[41].同时, AKBC具有一定的芳香性, 其芳环可以与OTC的苯环和氨基发生π—π共轭和阳离子—π键作用[22, 39].此外, 在不同的pH条件下, OTC以不同的形态存在, AKBC表面也带有电荷, 在吸附过程中还存在一定强静电作用[2].
|
图 11 推测的AKBC与OTC作用机制示意 Fig. 11 Imagined interactions between AKBC and OTC |
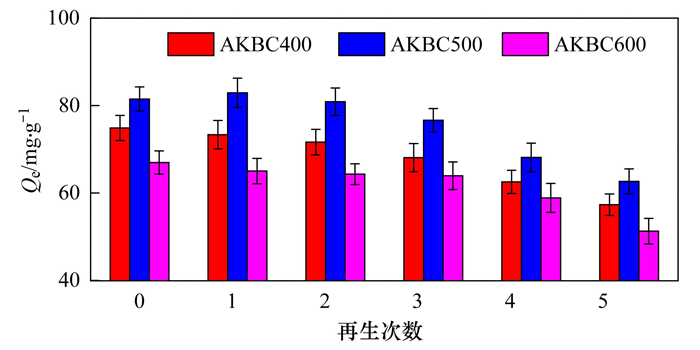
生物炭再生吸附性能决定其实际应用前景.3种吸附饱和后的AKBC经0.5 mol·L-1 NaOH溶液脱附再生后, 对OTC的5次再生吸附性能见图 12.由图可知, 3种AKBC经2次再生后对OTC的吸附性能基本与原始吸附性能相当, 第3 ~ 5次再生后吸附性能存在一定程度的降低.总体而言, 经过5次再生循环使用后, AKBC400、AKBC500和AKBC600对OTC的去除率仍能分别达到原始吸附去除率的76.6%、80.9%和75.1%, 表明AKBC具有良好的再生吸附性能和重复使用价值.
|
图 12 玉米秸秆生物炭对OTC的再生吸附性能 Fig. 12 Reusability of AKBC for OTC adsorption |
经氢氧化钾改性、500℃中温活化后制得的玉米秸秆生物炭AKBC, 比表面积增加、孔隙结构显著改善, 芳香性增强, 对水溶液中OTC的吸附性能显著提升.AKBC对OTC的吸附动力学过程符合准二级动力学模型, 颗粒内扩散和膜扩散均为吸附过程的控速步骤.其对OTC的吸附量随着温度的升高而增大, Langmuir、Freundlich和Temkin模型均可较好地拟合吸附等温线, 且吸附过程自发、吸热和熵增加.溶液初始pH大于9时, 或腐殖酸浓度高于10 mg·L-1时, 均不利于AKBC对OTC的吸附.吸附过程存在孔填充、氢键、π—π共轭、阳离子—π键和强静电作用等机制.AKBC对OTC有良好的再生吸附性能, 在四环素类抗生素污染治理方面具有良好的应用潜力.
| [1] | Xu L Y, Zhang H, Xiong P, et al. Occurrence, fate, and risk assessment of typical tetracycline antibiotics in the aquatic environment: a review[J]. Science of the Total Environment, 2021, 753. DOI:10.1016/j.scitotenv.2020.141975 |
| [2] |
张娟香, 赵保卫, 马锋锋, 等. 造纸污泥生物炭对四环素的吸附特性及机理[J]. 中国环境科学, 2020, 40(9): 3821-3828. Zhang J X, Zhao B W, Ma F F, et al. Adsorption characteristics and mechanism of tetracycline by biochars derived from paper industry sludge[J]. China Environmental Science, 2020, 40(9): 3821-3828. |
| [3] | Zhuang M, Achmon Y, Cao Y P, et al. Distribution of antibiotic resistance genes in the environment[J]. Environmental Pollution, 2021, 285. DOI:10.1016/j.envpol.2021.117402 |
| [4] | Leichtweis J, Vieira Y, Welter N, et al. A review of the occurrence, disposal, determination, toxicity and remediation technologies of the tetracycline antibiotic[J]. Process Safety and Environmental Protection, 2022, 160: 25-40. DOI:10.1016/j.psep.2022.01.085 |
| [5] | Scaria J, Anupama K V, Nidheesh P V. Tetracyclines in the environment: an overview on the occurrence, fate, toxicity, detection, removal methods, and sludge management[J]. Science of the Total Environment, 2021, 771. DOI:10.1016/j.scitotenv.2021.145291 |
| [6] |
闵炳坤, 李坤权. 高比表面硫脲改性花生壳炭的制备及对四环素和铜的吸附[J]. 环境科学, 2023, 44(3): 1528-1536. Min B K, Li K Q. Preparation of high specific surface thiourea modified peanut shell carbon and adsorption of tetracycline and copper[J]. Environmental Science, 2023, 44(3): 1528-1536. |
| [7] | Ullah F, Ji G Z, Irfan M, et al. Adsorption performance and mechanism of cationic and anionic dyes by KOH activated biochar derived from medical waste pyrolysis[J]. Environmental Pollution, 2022, 314. DOI:10.1016/j.envpol.2022.120271 |
| [8] | Haider F U, Wang X K, Zulfiqar U, et al. Biochar application for remediation of organic toxic pollutants in contaminated soils; An update[J]. Ecotoxicology and Environmental Safety, 2022, 248. DOI:10.1016/j.ecoenv.2022.114322 |
| [9] | Danesh P, Niaparast P, Ghorbannezhad P, et al. Biochar production: recent developments, applications, and challenges[J]. Fuel, 2023, 337. DOI:10.1016/j.fuel.2022.126889 |
| [10] |
徐智, 郭朝晖, 徐锐, 等. 控氧热解过程中污染稻草生物炭的组分特性及其重金属累积特征[J]. 环境科学, 2023, 44(2): 1051-1062. Xu Z, Guo Z, Xu R, et al. Component properties and heavy metal accumulation characteristics of contaminated rice straw biochar during oxygen-controlled pyrolysis[J]. Environmental Science, 2023, 44(2): 1051-1062. |
| [11] | Cho S H, Lee S, Kim Y, et al. Applications of agricultural residue biochars to removal of toxic gases emitted from chemical plants: a review[J]. Science of the Total Environment, 2023, 868. DOI:10.1016/j.scitotenv.2023.161655 |
| [12] |
龚沛云, 孙丽娟, 宋科, 等. 农业废弃物基生物炭对水溶液中镉的吸附效果与机制[J]. 环境科学, 2022, 43(6): 3211-3220. Gong P Y, Sun L J, Song K, et al. Adsorption capacity and mechanism of biochar derived from typical agricultural wastes for cadmium in aqueous solutions[J]. Environmental Science, 2022, 43(6): 3211-3220. |
| [13] |
刘总堂, 邵江, 李艳, 等. 碱改性小麦秸秆生物炭对水中四环素的吸附性能研究[J]. 中国环境科学, 2022, 42(8): 3736-3743. Liu Z T, Shao J, Li Y, et al. Adsorption performance of tetracycline in water by alkali-modified wheat straw biochars[J]. China Environmental Science, 2022, 42(8): 3736-3743. |
| [14] | Jiang Z H, Chen M, Lee X, et al. Enhanced removal of sulfonamide antibiotics from water by phosphogypsum modified biochar composite[J]. Journal of Environmental Sciences, 2023, 130: 174-186. DOI:10.1016/j.jes.2022.10.023 |
| [15] | Amalina F, Abd Razak A S, Krishnan S, et al. Biochar production techniques utilizing biomass waste-derived materials and environmental applications–A review[J]. Journal of Hazardous Materials Advances, 2022, 7. DOI:10.1016/j.hazadv.2022.100134 |
| [16] | Ambika S, Kumar M, Pisharody L, et al. Modified biochar as a green adsorbent for removal of hexavalent chromium from various environmental matrices: Mechanisms, methods, and prospects[J]. Chemical Engineering Journal, 2022, 439. DOI:10.1016/j.cej.2022.135716 |
| [17] | Mariana M, Mistar E M, Alfatah T, et al. High-porous activated carbon derived from Myristica fragrans shell using one-step KOH activation for methylene blue adsorption [J]. Bioresource Technology Reports, 2021, 16. DOI:10.1016/j.biteb.2021.100845 |
| [18] |
林鹏程, 尹华, 刘晓菲, 等. 锰铝双氧化物改性生物炭减缓土壤重金属对黑麦草的毒性作用[J]. 环境科学, 2023, 44(2): 975-983. Lin P C, Yin H, Liu X F, et al. Mn/Al-layered double oxide-loaded biochar reduced the toxic effects of heavy metals on ryegrass in soil[J]. Environmental Science, 2023, 44(2): 975-983. |
| [19] |
韦婧, 刘昳晗, 涂晨, 等. 铁修饰生物炭的制备及在砷污染土壤修复中的应用[J]. 环境科学, 2023, 44(2): 965-974. Wei J, Liu Y H, Tu C, et al. Preparation of iron-modified biochar and its application in arsenic contaminated soil remediation[J]. Environmental Science, 2023, 44(2): 965-974. |
| [20] | Kalak T, Kaczmarek M, Nowicki P, et al. Preparation of nitrogen-enriched pine sawdust-based activated carbons and their application for copper removal from the aquatic environment[J]. Wood Science and Technology, 2022, 56(6): 1721-1742. DOI:10.1007/s00226-022-01423-9 |
| [21] |
吴有龙, 徐嘉龙, 马中青, 等. KOH活化法制备气化稻壳活性炭及其吸附性能[J]. 生物质化学工程, 2021, 55(1): 31-38. Wu Y L, Xu J L, Ma Z Q, et al. Preparation of activated carbon from gasified rice husk char activated by KOH and its adsorption properties[J]. Biomass Chemical Engineering, 2021, 55(1): 31-38. |
| [22] |
余剑, 丁恒, 张智霖, 等. 改性菱角壳生物炭吸附水中土霉素性能与机理[J]. 中国环境科学, 2021, 41(12): 5688-5700. Yu J, Ding H, Zhang Z L, et al. Sorption characteristics and mechanism of oxytetracycline in water by modified biochar derived from chestnut shell[J]. China Environmental Science, 2021, 41(12): 5688-5700. |
| [23] |
莫贞林, 曾鸿鹄, 林华, 等. 高锰酸钾改性桉木生物炭对Pb(II)的吸附特性[J]. 环境科学, 2021, 42(11): 5440-5449. Mo Z L, Zeng H H, Lin H, et al. Adsorption characteristics of Pb(II) on eucalyptus biochar modified by potassium permanganate[J]. Environmental Science, 2021, 42(11): 5440-5449. |
| [24] |
杨传文, 邢帆, 朱建春, 等. 中国秸秆资源的时空分布、利用现状与碳减排潜力[J]. 环境科学, 2023, 44(2): 1149-1162. Yang C W, Xing F, Zhu J C, et al. Temporal and spatial distribution, utilization status, and carbon emission reduction potential of straw resources in China[J]. Environmental Science, 2023, 44(2): 1149-1162. |
| [25] |
于滨杭, 姬建梅, 王丽学, 等. 中国主粮作物生物炭产量效应的Meta分析[J]. 环境科学, 2023, 44(1): 520-530. Yu B H, Ji J M, Wang L X, et al. Meta analysis on yield effect of biochar for staple crops in China[J]. Environmental Science, 2023, 44(1): 520-530. |
| [26] | Vakili A, Zinatizadeh A A, Rahimi Z, et al. The impact of activation temperature and time on the characteristics and performance of agricultural waste-based activated carbons for removing dye and residual COD from wastewater[J]. Journal of Cleaner Production, 2023, 382. DOI:10.1016/j.jclepro.2022.134899 |
| [27] | Chen J, Yu Q F, Li M, et al. Preparation of high specific surface area activated carbon fiber by high-temperature vacuum activation and its superior water vapor adsorption for air humidity control[J]. Journal of Materials Science, 2023, 58(6): 2469-2493. DOI:10.1007/s10853-023-08205-z |
| [28] | Samiyammal P, Kokila A, Arul Pragasan L, et al. Adsorption of brilliant green dye onto activated carbon prepared from cashew nut shell by KOH activation: studies on equilibrium isotherm[J]. Environmental Research, 2022, 212. DOI:10.1016/j.envres.2022.113497 |
| [29] | Chen M, Wang D J, Xu X Y, et al. Biochar nanoparticles with different pyrolysis temperatures mediate cadmium transport in water-saturated soils: Effects of ionic strength and humic acid[J]. Science of the Total Environment, 2022, 806. DOI:10.1016/j.scitotenv.2021.150668 |
| [30] | Sellaoui L, Gómez-Avilés A, Dhaouadi F, et al. Adsorption of emerging pollutants on lignin-based activated carbon: Analysis of adsorption mechanism via characterization, kinetics and equilibrium studies[J]. Chemical Engineering Journal, 2023, 452. DOI:10.1016/j.cej.2022.139399 |
| [31] | Xu Z B, Xu X Y, Zhang Y, et al. Pyrolysis-temperature depended electron donating and mediating mechanisms of biochar for Cr(VI) reduction[J]. Journal of Hazardous Materials, 2020, 388. DOI:10.1016/j.jhazmat.2019.121794 |
| [32] | Zhou X, Yang Y, Li C, et al. Environmental-friendly one-step fabrication of tertiary amine-functionalized adsorption resins for removal of benzophenone-4 from water[J]. Journal of Cleaner Production, 2018, 203: 655-663. DOI:10.1016/j.jclepro.2018.08.290 |
| [33] | Abdoul H J, Yi M H, Prieto M, et al. Efficient adsorption of bulky reactive dyes from water using sustainably-derived mesoporous carbons[J]. Environmental Research, 2023, 221. DOI:10.1016/j.envres.2023.115254 |
| [34] |
桑倩倩, 王芳君, 赵元添, 等. 铁硫改性生物炭去除水中的磷[J]. 环境科学, 2021, 42(5): 2313-2323. Sang Q Q, Wang F J, Zhao Y T, et al. Application of iron and sulfate-modified biochar in phosphorus removal from water[J]. Environmental Science, 2021, 42(5): 2313-2323. |
| [35] |
陈友媛, 李培强, 李闲驰, 等. 浒苔生物炭对雨水径流中氨氮的吸附特性及吸附机制[J]. 环境科学, 2021, 42(1): 274-282. Chen Y Y, Li P Q, Li X C, et al. Effect of Enteromorpha prolifera biochar on the adsorption characteristics and adsorption mechanisms of ammonia nitrogen in rainfall runoff [J]. Environmental Science, 2021, 42(1): 274-282. |
| [36] | Xing X Y, Zhang Y T, Zhou G Y, et al. Mechanisms of polystyrene nanoplastics adsorption onto activated carbon modified by ZnCl2 [J]. Science of the Total Environment, 2023, 876. DOI:10.1016/j.scitotenv.2023.162763 |
| [37] | Li X M, Xu J L, Shi J X, et al. Rapid and efficient adsorption of tetracycline from aqueous solution in a wide pH range by using iron and aminoacetic acid sequentially modified hierarchical porous biochar[J]. Bioresource Technology, 2022, 346. DOI:10.1016/j.biortech.2022.126672 |
| [38] | Xu J, Zhang Y, Li B, et al. Improved adsorption properties of tetracycline on KOH/KMnO4 modified biochar derived from wheat straw [J]. Chemosphere, 2022, 296. DOI:10.1016/j.chemosphere.2022.133981 |
| [39] |
孙秋楠, 张荣斌, 邓曼君, 等. 高炉水渣负载硫化纳米零价铁对水中土霉素的去除[J]. 环境科学, 2021, 42(2): 867-873. Sun Q N, Zhang R B, Deng M J, et al. Removal of oxytetracycline from water using blast furnace slag loaded sulfide nanoscale zero-valent iron[J]. Environmental Science, 2021, 42(2): 867-873. |
| [40] | Wu J Y, Wang Y H, Wu Z X, et al. Adsorption properties and mechanism of sepiolite modified by anionic and cationic surfactants on oxytetracycline from aqueous solutions[J]. Science of the Total Environment, 2020, 708. DOI:10.1016/j.scitotenv.2019.134409 |
| [41] | Li H Q, Hu J T, Meng Y, et al. An investigation into the rapid removal of tetracycline using multilayered graphene-phase biochar derived from waste chicken feather[J]. Science of the Total Environment, 2017, 603-604: 39-48. DOI:10.1016/j.scitotenv.2017.06.006 |
| [42] | Sheng X Y, Wang J K, Cui Q T, et al. A feasible biochar derived from biogas residue and its application in the efficient adsorption of tetracycline from an aqueous solution[J]. Environmental Research, 2022, 207. DOI:10.1016/j.envres.2021.112175 |
| [43] |
王光泽, 曾薇, 李帅帅. 铈改性水葫芦生物炭对磷酸盐的吸附特性[J]. 环境科学, 2021, 42(10): 4815-4825. Wang G Z, Zeng W, Li S S. Adsorption characteristics of phosphate on cerium modified water hyacinth biochar[J]. Environmental Science, 2021, 42(10): 4815-4825. |
| [44] | Liu Q, Li D M, Cheng H R, et al. High mesoporosity phosphorus-containing biochar fabricated from Camellia oleifera shells: impressive tetracycline adsorption performance and promotion of pyrophosphate-like surface functional groups (C-O-P bond) [J]. Bioresource Technology, 2021, 329. DOI:10.1016/j.biortech.2021.124922 |
| [45] | Wang J C, Li H X, Yue D B. Enhanced adsorption of humic/fulvic acids onto urea-derived graphitic carbon nitride[J]. Journal of Hazardous Materials, 2022, 424. DOI:10.1016/j.jhazmat.2021.127643 |
| [46] | Kim J E, Bhatia S K, Song H J, et al. Adsorptive removal of tetracycline from aqueous solution by maple leaf-derived biochar[J]. Bioresource Technology, 2020, 306. DOI:10.1016/j.biortech.2020.123092 |
 2024, Vol. 45
2024, Vol. 45

