2. 重庆市璧山区防汛抗旱调度中心, 重庆 402760
2. Bishan Flood Control and Drought Relief Dispatching Center of Chongqing, Chongqing 402760, China
磷是农作物生长发育必需的大量营养元素, 对作物产量和品质具有重要影响[1].但磷在土壤中极易与土壤中Al3+、Fe3+和Ca2+等离子产生化学沉淀或被土壤吸附固定[2, 3], 使得能被作物吸收利用的有效态磷在土壤中转化为不能被作物利用的无效态磷, 从而降低了磷肥的利用率.磷肥的低利用率使得土壤中的磷大量流失, 导致土壤酸化[4]、水体富营养化[5]和产生温室气体[6]等一系列环境问题.土壤全磷中有25% ~56%是有机磷[7], 但有机磷必须经过活化作用分解为无机态磷酸根离子才能被根系所利用, 因此提高土壤磷库中难溶性磷素的活化利用是提高磷肥利用率的重要途径.解磷微生物是土壤难溶性磷活化和形态转化的主要驱动者[8, 9], 其可以通过释放磷酸酶, 产生可溶性的磷酸盐供作物吸收[10], 这一功能的发挥是缓解土壤缺磷的一个有效途径[11].磷酸酶活性是反映土壤有机磷矿化潜力的一个重要指标, 根据其最适pH分为酸性磷酸酶(ACP)和碱性磷酸酶(ALP), 酸性磷酸酶的最适pH区间在4~6, 碱性磷酸酶的最适pH区间在8~10[12].目前已经克隆出了编码ACP的基因phoC[13]和编码ALP的基因phoD[14], 这些编码磷酸酶的功能基因为检测环境中微生物种类、丰度和群落结构组成提供了有效手段.因此, 深入研究植物和土壤磷酸酶活性, 以及编码基因的群落结构对提高土壤中磷素的有效性有重要的意义.
生物质炭是生物质在无氧或者部分缺氧的条件下裂解炭化形成的炭材料, 其表面丰富的多孔结构可为土壤微生物的生长提供良好的环境条件[15, 16].有学者研究了施用生物炭对土壤氮磷流失及温室气体排放的影响[17~19], 也有研究生物炭施用对土壤酶活及土壤微生物多样性的影响[20, 21].靳玉婷等[22]在连续4 a的田间定位试验发现, 常规施肥配施生物炭使得水稻季土壤磷酸酶的活性显著提高了28.54%. Tian等[23]的研究发现低磷环境下生物炭的施用增加了phoD基因多样性, 同时可提高植物对磷素的获取能力.
目前, 国内外对生物炭在土壤磷转化方面的作用大部分集中在生物炭对土壤总磷、有效磷和磷酸酶的影响, 而同时研究生物炭对根际、非根际土壤中磷酸酶及其编码基因微生物群落多样性的影响还鲜见报道.因此, 本研究以玉米秸秆和稻壳秸秆为供试材料, 通过化肥和有机肥配施生物炭, 研究柠檬根际和非根际土壤磷酸酶活性及phoC和phoD基因群落多样性, 以期为土壤磷素的高效利用提供一定的理论依据.
1 材料与方法 1.1 供试材料供试土壤为紫色潮土, 采自重庆市潼南区太安镇小岭村柠檬基地, 将采集后的土壤放置于阴凉干燥处, 经自然风干后, 去除其中的小石块、动植物残体, 再碾碎过1 cm筛, 保存备用; 再将部分过1 cm筛的土壤样品进一步碾碎过3 mm筛, 用于培养试验.初始土壤的养分基本情况: pH为5.20, ω(有机质)为8.68g ·kg-1, ω(全氮)为0.68g ·kg-1, ω(全磷)为0.22g ·kg-1, ω(碱解氮)为67.31mg ·kg-1, ω(硝态氮)为34.64mg ·kg-1, ω(有效磷)为9.14mg ·kg-1, ω(速效钾)为244.12mg ·kg-1.
供试腐熟猪粪(有机肥)和新鲜猪粪(新鲜有机肥)取自潼南温氏种猪场, 其基本性质见表 1.供试生物炭为玉米秸秆生物炭和稻壳生物炭, 由四川省久晟农业有限责任公司提供, 其分别以玉米秸秆和稻壳为原料, 在500℃高温厌氧条件下热解2 h制备, 两种生物炭养分含量见表 2.供试柠檬品种为尤力克(Eureka), 苗龄为嫁接7个月的脱毒苗, 来自重庆市潼南区国家科技农业园区智能化柠檬脱毒育苗中心.
|
|
表 1 有机肥基本性质 Table 1 Basic properties of organic fertilizer |
|
|
表 2 生物炭基本性质 Table 2 Basic properties of biochar |
1.2 试验设计
本试验共设6个处理: ①对照(CK)、②传统施肥(F)、③化肥+20t ·hm-2稻壳生物炭(FP)、④化肥+10t ·hm-2稻壳生物炭+10t ·hm-2玉米生物炭(FPM)、⑤有机肥+20t ·hm-2稻壳生物炭(PP)和⑥新鲜有机肥+20t ·hm-2稻壳生物炭(NPP), 其中传统施肥是参照当地农户的施肥量, 有机肥及生物炭的施用量则保持等氮施肥, 每个处理4次重复, 试验采取随机区组设计.称取过1 cm筛的风干土15 kg, 共24份, 分别按照上述处理加入生物炭和化肥, 柠檬幼苗单株基肥纯氮2.625 g、纯磷2.625 g和纯钾1.83 g, 将上述生物炭、有机肥和基肥充分与土混匀装入直径22 cm、高30 cm的PVC圆桶中.装盆放置15 d后定植柠檬, 每钵1株, 定植时各处理的柠檬苗保持大小基本一致, 定植后, 浇水灌透.定植后每2个月, 以基肥1/3的氮、磷和钾素的量进行追肥, 各处理保持等氮、磷和钾的输入.平日进行适时适量浇水管理, 以防止肥料流失.种植9个月后破坏性采集根际和非根际土壤样品, 分析土壤无机磷、有机磷、有机磷形态、土壤理化性质、酶活性和微生物群落结构等指标, 阐明生物炭对柠檬根际土壤有机磷转化的微生物机制.传统施肥使用的氮、磷和钾肥品种分别为尿素(N 46%)、过磷酸钙(P2 O512%)和氯化钾(K2 O 60%).微肥来自北美农大集团生产的硼锌锰铁镁钙硅复合微量元素水溶肥料, 各元素含量: B、Zn、Mg、Si、Ca、Mn和Fe均大于12%, pH 6.0.除CK处理外, 各处理保持等氮的输入处理(表 3).
|
|
表 3 各试验处理施肥量 Table 3 Fertilizer amount of each experimental treatment |
1.3 测定方法
土壤样品采集为破坏性采样, 先打开定植盆, 取出带土试验苗, 去除黏附在根系上的较大颗粒土, 并用细毛刷轻轻刷下黏附在须根上的根际土, 将其收集在无菌自封塑料袋中封好, 同时收集等量的非根际土, 一部分采用MoBio PowerSoil DNA Isolation Kit试剂盒提取土壤总DNA, 另一部分土壤用于测量磷酸酶活性和微生物群落多样性.同时将新鲜植株根收集在无菌自封塑料袋中封好.
1.3.1 磷酸酶活性测定土壤酸性磷酸酶(ACP)活性和碱性磷酸酶(ALP)活性测定均采用分光光度法测定, 具体操作按照苏州科铭生物技术有限公司生产的土壤酸性磷酸酶活性测定试剂盒说明书和土壤碱性磷酸酶活性测定试剂盒说明书进行.
1.3.2 末端限制性片段长度多态性(T-RFLP)分析T-RFLP分析各功能基因采用不同的引物、扩增体系和程序, 其中每对引物的正向引物都带有FAM荧光标记.
phoC和phoD基因扩增所需引物见表 4, phoC和phoD基因扩增体系和程序见表 5.
|
|
表 4 phoC和phoD基因荧光定量PCR引物 Table 4 The phoC and phoD gene fluorescence quantitative PCR primers |
|
|
表 5 phoC和phoD基因T-RFLP分析的PCR体系和程序 Table 5 PCR system and procedures for T-RFLP analysis of phoC and phoD genes |
phoC和phoD基因扩增产物的酶切. phoC基因和phoD基因扩增的PCR产物分别利用HhaⅠ、MspⅠ限制性内切酶进行单酶切.在37℃的恒温培养箱中放置14~16 h, 然后再在80℃的恒温烘箱中放置30 min使其失活.最后送生工生物工程股份有限公司(上海)利用ABI Prism 3100基因分析仪进行T-RFLP分析.
1.4 数据处理采用Excel 2019和SPSS 23.0进行数据处理和图表绘制, 表中数据均为平均值±标准偏差, 不同处理之间的多重比较采用LSD最小显著差异法, 图表中的不同字母表示显著性差异(P<0.05).
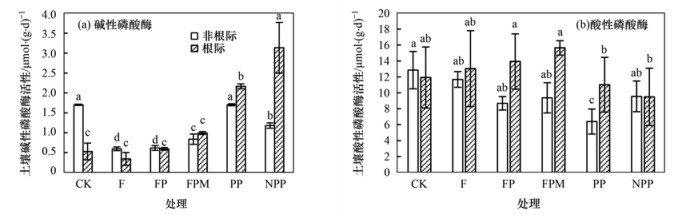
2 结果与分析 2.1 化肥和有机肥配施生物炭对土壤磷酸酶活性的影响不同处理土壤磷酸酶酶活变化特征如图 1所示.对于碱性磷酸酶, 在非根际土壤中, 其活性在0.62~1.7μmol ·(g ·d)-1之间, 与CK处理相比, 施肥的各处理的碱性磷酸酶酶活均有所降低, 其中以F处理的碱性磷酸酶活性最低, 仅为0.62μmol ·(g ·d)-1, 施加化肥会显著降低非根际土壤碱性磷酸酶活性(P<0.05).根际土壤的碱性磷酸酶活性在0.34~3.13 μmol ·(g ·d)-1之间, F处理略小于CK处理的碱性磷酸酶活性, 配施生物炭后, 根际土壤的碱性磷酸酶酶活性明显增加, 其中生物炭和有机肥配施的PP和NPP处理的酶活性显著增加, NPP处理的碱性磷酸酶酶活性最高, 达3.13μmol ·(g ·d)-1, 较CK处理的酶活性增加了4.91倍.对于酸性磷酸酶, 非根际土壤中其活性的变化范围在6.4~12.85μmol ·(g ·d)-1之间, 其中CK处理的酶活性最高, 施肥后土壤中酸性磷酸酶活性降低, 配施生物炭后, 其活性进一步降低, 其中PP处理中的酸性磷酸酶活性最低, 其酶活较CK处理降低了50.19%.根际土壤中酸性磷酸酶的酶活变化范围在9.5~15.64μmol ·(g ·d)-1之间, 但是可以看出F、FP和FPM处理根际土壤的酸性磷酸酶酶活较CK处理有所上升, 而有机肥配施生物炭处理的PP和NPP处理的酸性磷酸酶活性较其他处理更低, 说明有机肥配施生物炭降低了根际土壤酸性磷酸酶活性. 不同小写字母表示不同处理下土壤磷酸酶活性差异显著(P < 0.05)
|
图 1 不同施肥处理下土壤碱性磷酸酶和酸性磷酸酶活性 Fig. 1 Soil alkaline phosphatase and acid phosphatase activities under different fertilization treatments |
各处理柠檬根磷酸酶活性如表 6所示, 与土壤中酸性磷酸酶占主导地位不同, 植株根中碱性磷酸酶占主导地位.植株根碱性磷酸酶活性变化范围在47.57~424.29μmol ·(g ·min)-1之间, 其中F处理的碱性磷酸酶活性最高, 达424.29μmol ·(g ·min)-1, 显著高于其他处理(P<0.05), FPM和PP处理的碱性磷酸酶活性最低, 分别为47.57μmol ·(g ·min)-1和48.79μmol ·(g ·min)-1.柠檬根的酸性磷酸酶活性的变化范围在2.64~10.95μmol ·(g ·min)-1之间, 其中CK处理酸性磷酸酶活性最低, 仅为2.64μmol ·(g ·min)-1, FPM处理酸性磷酸酶活性最高, 是CK处理的4.15倍.
|
|
表 6 柠檬根碱性磷酸酶活性和酸性磷酸酶活性1)/μmol ·(g ·min)-1 Table 6 Plant root alkaline phosphatase activity and acid phosphatase activity /μmol ·(g ·min)-1 |
2.3 化肥和有机肥配施生物炭对土壤phoC和phoD基因微生物群落结构的影响 2.3.1 对土壤phoC基因的影响
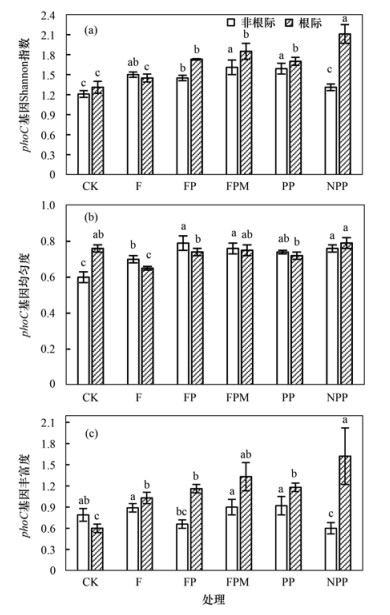
不同施肥处理下土壤中phoC基因微生物多样性分析如图 2所示.香农指数(Shannon指数)用来反映样品的多样性程度, 其值越高表明群落物种的多样性越高[24].不同处理下, 非根际土壤中Shannon多样性指数的变化范围在1.21~1.61之间, 其中CK处理的Shannon多样性指数最低, 仅为1.21; 根际土壤中Shannon多样性指数的变化范围在1.31~2.11之间, 除F处理外, Shannon指数较非根际均有所增加, 各处理中仍以CK处理的Shannon多样性指数最低, 配施生物炭后, 根际、非根际各处理的phoC基因Shannon多样性指数均有显著提升(P<0.05), 即配施生物炭显著增加了非根际和根际土壤中phoC基因的多样性.就均匀度而言, 非根际土壤的数值范围在0.60~0.79之间, CK处理的均匀度最低, 其余所有处理均匀度均高于CK, 即化肥配施生物炭处理和有机肥配施生物炭处理均提高了非根际土中phoC基因的均匀度; 根际土壤的均匀度数值范围在0.65~0.79之间, 以F处理的均匀度指数最低, 除NPP处理外, 其余处理phoC基因的均匀度均低于CK.就丰富度而言, 各处理非根际土壤的数值变化范围在0.60~0.92之间, 根际土壤的数值变化范围在0.60~1.62之间, NPP处理非根际土壤中丰富度的值最低, 仅为0.60, 但在根际土壤中, NPP处理的丰富度最高, 达到1.62, 施加肥料可以显著提升根际土壤phoC基因的丰富度指数(P<0.05).
|
不同小写字母表示不同处理下土壤phoC基因群落多样性差异显著(P < 0.05) 图 2 不同处理下土壤phoC基因的多样性、均匀度和丰富度 Fig. 2 Diversity, uniformity, and richness of soil phoC genes under different treatments |
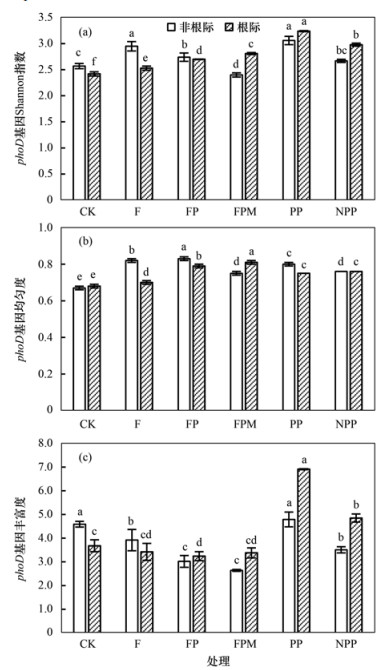
不同施肥处理下土壤中phoD基因微生物多样性分析如图 3所示, 就phoD基因的Shannon多样性指数而言, 各处理非根际土壤的数值范围为2.40~3.06之间, 根际土壤的数值变化范围在2.42~3.24之间, 施肥显著提升了非根际和根际土中phoD基因的Shannon多样性指数(P<0.05).非根际土壤中, F处理的Shannon多样性指数提升幅度最大, 其次是腐熟有机肥配施生物炭的PP处理, 根际土壤中, 各个处理间均有显著性的差异, 施用生物炭后, 进一步提升了phoD基因的Shannon多样性指数, 其中以有机肥和生物炭配施的PP和NPP处理提升的幅度最大.就phoD基因的均匀度指数而言,各处理非根际土壤的数值范围在0.67~0.83之间, 根际土壤的数值变化范围在0.68~0.81之间, 同样表现为各种施肥处理均增加了根际、非根际土壤中的phoD基因均匀度.就phoD细菌的丰富度指数而言, 各处理非根际土壤的数值范围在2.64~4.79之间, 根际土壤的数值范围在3.24~6.91之间, 非根际和根际土壤的phoD基因的丰富度指数都是PP处理最高.综上所述, 施肥能增加根际、非根际土中phoD细菌的Shannon多样性指数和均匀度指数, 有机肥配施生物炭(PP和NPP处理)对phoD基因的Shannon多样性指数和丰富度指数的提升最为显著(P<0.05).本试验土壤中phoD基因的Shannon多样性指数和丰富度指数均明显高于phoC基因.
|
(a)Shannon指数, (b)均匀度, (c)丰富度; 不同小写字母表示不同处理下土壤phoD基因群落多样性差异显著(P < 0.05) 图 3 不同处理下土壤phoD基因的多样性、均匀度和丰富度 Fig. 3 Diversity, uniformity, and richness of soil phoD genes under different treatments |
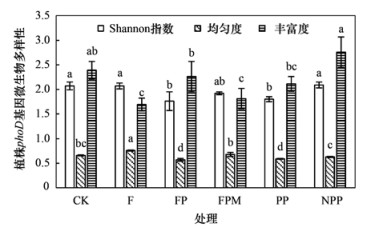
不同施肥处理下植株phoD基因生物群落的多样分析如图 4所示, 植株phoD基因微生物群落的Shannon多样性指数的变化范围在1.76~2.09之间, 其中以NPP处理最高, FP处理最低, 除NPP处理外, 其余处理Shannon多样性指数较CK均降低; 均匀度指数在0.57~0.76之间, 其中以F处理最高, FP处理最低, 除F和FPM处理外, 其余3种处理均匀度较CK均降低; 丰富度指数在1.69~2.76之间, 其中以NPP处理最高, F处理最低, 与多样性类似, 除NPP处理外, 其余处理丰富度较CK均降低.整体趋势表现为化肥和有机肥配施生物炭后, 植株根的phoD基因微生物多样性有一定程度地降低.
|
不同小写字母表示不同处理下植株phoD基因群落多样性差异显著(P < 0.05) 图 4 不同处理下植株phoD基因的多样性、均匀度和丰富度 Fig. 4 Diversity, uniformity, and richness of phoD genes in plants under different treatments |
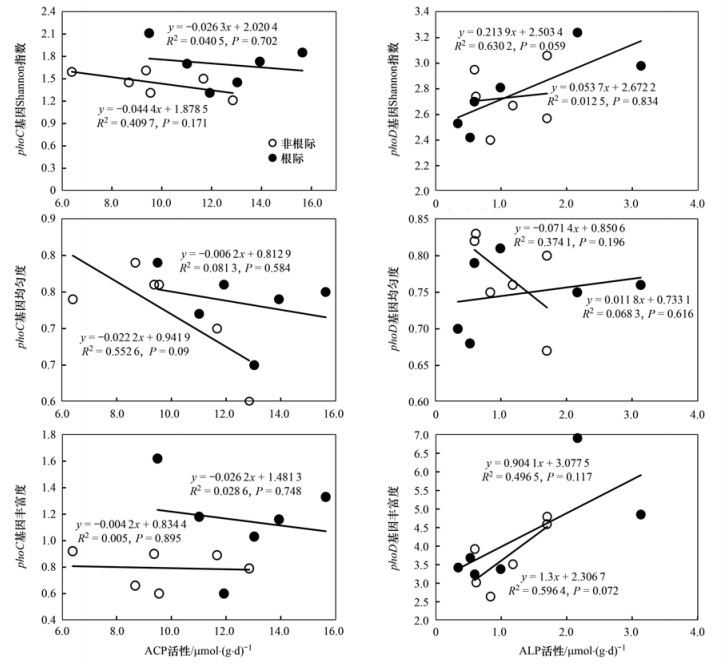
对非根际土、根际土中磷酸酶活性和两种基因的Shannon指数、均匀度和丰富度进行线性回归分析, 其结果见图 5.可以看出, 对于酸性磷酸酶来说, 非根际和根际土壤中ACP活性与编码ACP的基因phoC之间均呈负相关关系, 且这种线性关系不显著(P>0.05), 即随着ACP活性的增加, phoC基因的多样性、均匀度和丰富度减少, 其中相关性相对最大的是非根际土壤中phoC基因均匀度55.26%的变化是由ACP活性的变化引起, 而无论是非根际土还是根际土, 其基因丰富度受酸性磷酸酶活性的影响都很小.对于碱性磷酸酶来说, 除非根际土壤中ALP活性与phoD基因均匀度呈负相关以外, 其余均呈正相关, 即随着ALP活性的增加, 土壤中phoD基因的多样性、均匀度和丰富度均增加, 但增加的不显著.其中根际土壤中phoD基因的Shannon指数与ALP活性相关性最大, 拟合优度达0.630 2.
|
图 5 非根际土、根际土中磷酸酶活性与两种基因多样性、均匀度和丰富度的相关性 Fig. 5 Correlation of phosphatase activity in non-rhizosphere soil and rhizosphere soil with the diversity, uniformity, and richness of the two genes |
在本研究中, 根际土壤和非根际土壤中碱性磷酸酶活性范围在0.34~3.13μmol ·(g ·d)-1, 酸性磷酸酶活性范围是6.40~15.64 μmol ·(g ·d)-1.土壤中酸性磷酸酶活性远大于碱性磷酸酶活性, 这是因为磷酸酶活性和pH值密切相关, 在酸性土壤中, 较酸的环境更有利于酸性磷酸酶的酶促反应的发生, 而不利于碱性磷酸酶, 所以酸性酶促反应在酸性土壤中更为强烈.本试验使用的土壤是酸性紫色土, pH范围主要在4.51~6.29之间, 属于酸性磷酸酶的适合区间, 因此, 酸性磷酸酶在本研究土壤中起主导作用[22].与土壤中酸性磷酸酶占主导地位不同, 植株根中碱性磷酸酶占主导地位, 且所有处理酸性磷酸酶活性均显著高于CK, 这可能是因为施肥、有机肥和生物炭加入, 促进了植株根的生长, 进而其中的微生物活性增大.
碱性磷酸酶活性的变化趋势表现为, 在非根际土壤中, 与F处理相比, 各处理都减少了碱性磷酸酶活性, 这与Du等[25]的研究结果一致, 其中以有机肥和生物炭配施的PP处理和NPP处理减少的相对较少, 而化肥和生物炭配施的处理则明显减少碱性磷酸酶的活性, 这可能是因为化肥中的磷(P2 O5)含量高于有机肥, 而随着施磷量的增加, 根际碱性磷酸酶活性减弱[26].在根际土壤中, 各处理均增加了土壤中碱性磷酸酶的活性, 其中以添加有机肥处理(PP和NPP)下酶活增加得最明显, 分别是CK的4.09倍和5.92倍.究其原因, 主要是因为配施生物炭可以增加土壤的pH值.有研究也表明, 在酸性土壤中, 土壤酸度的降低会显著地增加土壤中碱性磷酸酶活性[27], 同时有研究认为, 土壤碱性磷酸酶主要源自土壤细菌、真菌和其它的土壤微生物[28, 29].Yoo等[30]的研究认为, 土壤碱性磷酸酶活性增加是因为微生物增殖造成的, 而生物炭的施用会促进根际土壤中微生物的生长和繁殖, 加大对磷素的需求, 从而增加了根际土壤中碱性磷酸酶活性.而PP和NPP处理下根际土壤碱性磷酸酶大幅增加, 是由于有机肥本身含有大量的微生物, 并且拥有丰富的有机碳源[31], 对提高土壤酶活性以及增加微生物数量等方面有着重要的促进作用[32].所以这两个处理能够最为显著地增加根际土壤中碱性磷酸酶的活性.
酸性磷酸酶在土壤有机磷的分解矿化过程中有相当重要的作用, 可以促进有机磷化合物上酯磷键的水解, 转化成相关的醇和无机磷[33].本研究中, 在非根际土壤中, 与CK处理相比, 配施生物炭后非根际土壤中酸性磷酸酶活性降低, 其中以PP处理活性最低, 仅为CK处理酶活性的一半.非根际土壤受柠檬根系分泌物的影响减小, 由于本试验原始土壤为酸性土壤, 含磷量较低, ω(全磷)仅有0.27g ·kg-1.Helal[34]的研究表明, 缺磷条件会刺激植物根系的酸性磷酸酶活性显著提高, 从而增加植物对土壤中有机磷的利用能力, 殷全玉等[35]的研究也表明酸性磷酸酶是微生物和植物应对低磷环境而获取有效磷素的重要媒介.施肥之后增加了土壤中的有效磷含量, 缓解了微生物和植物的磷饥饿, 从而减少对酸性磷酸酶的分泌, 降低了土壤中酸性磷酸酶的活性, 所以CK处理的酸性磷酸酶活性最高, 施肥会降低其活性, 而配施生物炭会使土壤中酸性磷酸酶活性再次降低, 这可能是因为生物炭的施用增加了土壤的pH值所致[33].在本研究中, 与非根际土壤相比, 根际土壤的酸性磷酸酶活性普遍更高.有研究表明, 酸性磷酸酶主要由植物释放和合成[36, 37], 因此根际土壤中有比非根际土壤中更高的酸性磷酸酶活性[38], 这和植物的生理活动密切相关, 土壤中的酸性磷酸酶主要是由植物根系分泌[39], 以促使根系周围的有机磷矿化, 从而增加土壤中的无机磷含量供其吸收利用, 同时土壤中根系分泌物也会促进根际微生物繁殖[40], 增加对磷素的需求, 从而有利于增加根际土壤中的酶活性[41].所以距离植物根系越近的土壤, 酸性磷酸酶活性也就相对更高.也有研究表明[42], 距离植物根系越近的土壤, 酸性磷酸酶活性会变得更高.所以在根际土壤中, F处理、FP处理和FPM处理的酸性磷酸酶活性均增加, 而PP处理和NPP处理的酶活性降低, 这可能是因为腐熟有机肥和新鲜有机肥均呈碱性, 相比较化肥配施生物炭, 有机肥配施生物炭增加了土壤环境的pH, 使得酸性磷酸酶活性降低.
3.2 化肥和有机肥配施生物炭对土壤phoC和phoD基因多样性的影响多样性指数是评价微生物群落的重要指标, 多样性指数越高表明土壤中微生物种类越丰富, 土壤微生态系统越复杂, 功能越稳定[43].在本研究中, 配施生物炭后, 显著增加了非根际和根际土壤中phoC基因和phoD基因微生物群落的Shannon多样性指数和非根际土壤中两种基因的均匀度指数, 显著增加了phoC基因根际土壤中的丰富度指数.说明生物炭输入有利于微生物繁殖, 提高磷酸酶相关基因群落结构多样性和功能多样性, 从而使土壤微生态系统更加稳定, 这和江琳琳[44]的研究结果一致.Doan等[45]也在试验中发现, 在施用化学肥料和生物有机肥时配施生物炭, 显著增加了土壤细菌数量, 土壤细菌群落结构Shannon指数和丰富度指数都得到增加.生物炭能够促进土壤微生物繁殖的原因, 主要有两个方面, 一是生物炭的碳骨架有较好的持水性和通气性, 能够为微生物的繁衍提供更良好的生存环境, 二是生物炭中含有一定的养分, 可以为微生物的生存繁殖提供营养物质, 进而增加了微生物的丰度[46].所以, 在本研究各处理中, 配施生物炭增加了土壤中phoC和phoD基因的多样性.
本研究大部分处理根际土壤的Shannon多样性指数、均匀度指数和丰富度指数都高于非根际土壤, 表现出了明显的根际效应.植物能量和物质代谢最活跃的区域就是根际, 根系释放的各种分泌物可以选择性地刺激微生物种群生长, 因此, 根际土壤形成了独特的微生物群落, 可以为微生物提供营养来源, 从而使微生物富集在根际土壤中.有研究已表明根际土壤微生物丰度和活性远高于非根际土壤[47, 48], 其中解磷微生物的分布表现出强烈的根际效应[49, 50], 植物的根系分泌物能够增强根际微生物的解磷功能[10].另外, 本研究得出酸性磷酸酶活性与phoC基因多样性、均匀度和丰富度均呈负相关关系, 这与陈海燕等[51]的研究结果相反, 可能是因为本研究配施的是生物炭, pH升高的环境不利于酸性磷酸酶的同时又增加了土壤中微生物多样性, 此外, 土壤酶的实际表达水平要通过综合基因组学和蛋白质组学来阐明, 要全面了解酸性磷酸酶活性对化肥、有机肥配施生物炭的响应, 就需要对不同处理中的phoC 转录本进行量化[52].编码碱性磷酸酶的基因phoD与碱性磷酸酶活性呈正相关关系, 是因为生物炭的特殊性质有利于碱性磷酸酶生存的同时又增加其微生物多样性, 这也与Fraser等[53]的研究结果一致.
4 结论(1) 在非根际土壤中, 各处理ALP和ACP活性较CK均降低; 根际土壤中, 各处理ALP活性显著增加, PP和NPP两个处理ACP活性降低, 生物炭显著提高了酸性土壤中碱性磷酸酶的活性.根际土壤的ACP活性高于非根际土壤, 表现出明显的根际效应.
(2) 配施生物炭显著增加了根际和非根际土壤中phoC和phoD基因群落的多样性(P < 0.05), 根际土壤中微生物群落的多样性和丰富度高于非根际, 表现出明显的根际效应; 同时phoD基因微生物群落的Shannon指数和丰富度均远高于phoC基因.
(3) ACP活性与phoC基因微生物群落均呈负相关关系, 除非根际土中ALP活性与phoD基因均匀度呈负相关关系, 其余ALP活性与phoD微生物群落均呈正相关关系.
| [1] |
黄洋, 胡学玉, 曹坤坤, 等. 调理剂对磷镉富集土壤中两种元素交互作用的影响[J]. 环境科学, 2021, 42(6): 3028-3036. Huang Y, Hu X Y, Cao K K, et al. Interaction and mechanism between conditioning agents and two elements in the soil enriched with phosphorus and cadmium[J]. Environmental Science, 2021, 42(6): 3028-3036. |
| [2] | Rutkowska B, Szulc W, Sosulski T, et al. Soil micronutrient availability to crops affected by long-term inorganic and organic fertilizer applications[J]. Plant Soil and Environment, 2014, 60(5): 198-203. DOI:10.17221/914/2013-PSE |
| [3] | Gao Y J, Wang X W, Shah J A, et al. Polyphosphate fertilizers increased maize (Zea mays L.) P, Fe, Zn, and Mn uptake by decreasing P fixation and mobilizing microelements in calcareous soil[J]. Journal of Soils and Sediments, 2020, 20(1): 1-11. DOI:10.1007/s11368-019-02375-7 |
| [4] | Bolan N S, Hedley M J, White R E. Processes of soil acidification during nitrogen cycling with emphasis on legume based pastures[J]. Plant and Soil, 1991, 134(1): 53-63. DOI:10.1007/BF00010717 |
| [5] | Yu C Q, Huang X, Chen H, et al. Managing nitrogen to restore water quality in China[J]. Nature, 2019, 567(7749): 516-520. DOI:10.1038/s41586-019-1001-1 |
| [6] | Xiong W, Lin E D, Ju H, et al. Climate change and critical thresholds in China's food security[J]. Climatic Change, 2007, 81(2): 205-221. DOI:10.1007/s10584-006-9123-5 |
| [7] | 徐明岗, 张文菊, 黄绍敏, 等. 中国土壤肥力演变[M]. ((第二版)). 北京: 中国农业科学技术出版社, 2015: 102-103. |
| [8] |
田江, 彭霞薇, 李霞, 等. 重金属抗性解磷细菌的磷溶解特性研究[J]. 环境科学, 2014, 35(6): 2334-2340. Tian J, Peng X W, Li X, et al. Isolation and characterization of two bacteria with heavy metal resistance and phosphate solubilizing capability[J]. Environmental Science, 2014, 35(6): 2334-2340. |
| [9] | Li H Z, Bi Q F, Yang K, et al. D2O-isotope-labeling approach to probing phosphate-solubilizing bacteria in complex soil communities by single-cell Raman spectroscopy[J]. Analytical Chemistry, 2019, 91(3): 2239-2246. DOI:10.1021/acs.analchem.8b04820 |
| [10] |
滕泽栋, 李敏, 朱静, 等. 解磷微生物对土壤磷资源利用影响的研究进展[J]. 土壤通报, 2017, 48(1): 229-235. Teng Z D, Li M, Zhu J, et al. Research advances in effect of phosphate-solubilizing microorganisms on soil phosphorus resource utilization[J]. Chinese Journal of Soil Science, 2017, 48(1): 229-235. |
| [11] | Sharma S B, Sayyed R Z, Trivedi M H, et al. Phosphate solubilizing microbes: sustainable approach for managing phosphorus deficiency in agricultural soils[J]. SpringerPlus, 2013, 2(1). DOI:10.1186/2193-1801-2-587 |
| [12] |
莫雪, 陈斐杰, 游冲, 等. 黄河三角洲不同植物群落土壤酶活性特征及影响因子分析[J]. 环境科学, 2020, 41(2): 895-904. Mo X, Chen F J, You C, et al. Characteristics and factors of soil enzyme activity for different plant communities in Yellow River delta[J]. Environmental Science, 2020, 41(2): 895-904. |
| [13] | Fraser T D, Lynch D H, Gaiero J R, et al. Quantification of bacterial non-specific acid (phoC) and alkaline (phoD) phosphatase genes in bulk and rhizosphere soil from organically managed soybean fields[J]. Applied Soil Ecology, 2017, 111: 48-56. DOI:10.1016/j.apsoil.2016.11.013 |
| [14] | Sakurai M, Wasaki J, Tomizawa Y, et al. Analysis of bacterial communities on alkaline phosphatase genes in soil supplied with organic matter[J]. Soil Science and Plant Nutrition, 2008, 54(1): 62-71. DOI:10.1111/j.1747-0765.2007.00210.x |
| [15] |
杨彩迪, 宗玉统, 卢升高. 不同生物炭对酸性农田土壤性质和作物产量的动态影响[J]. 环境科学, 2020, 41(4): 1914-1920. Yang C D, Zong Y T, Lu S G. Dynamic effects of different biochars on soil properties and crop yield of acid farmland[J]. Environmental Science, 2020, 41(4): 1914-1920. |
| [16] |
刘杰云, 邱虎森, 王聪, 等. 生物质炭对双季稻田土壤反硝化功能微生物的影响[J]. 环境科学, 2019, 40(5): 2394-2403. Liu J Y, Qiu H S, Wang C, et al. Influence of biochar amendment on soil denitrifying microorganisms in double rice cropping system[J]. Environmental Science, 2019, 40(5): 2394-2403. |
| [17] | Huang R, Wang Y Y, Liu J, et al. Variation in N2O emission and N2O related microbial functional genes in straw-and biochar-amended and non-amended soils[J]. Applied Soil Ecology, 2019, 137: 57-68. DOI:10.1016/j.apsoil.2019.01.010 |
| [18] | Huang R, Gao X S, Wang F H, et al. Effects of biochar incorporation and fertilizations on nitrogen and phosphorus losses through surface and subsurface flows in a sloping farmland of Entisol[J]. Agriculture, Ecosystems & Environment, 2020, 300. DOI:10.1016/j.agee.2020.106988 |
| [19] | Qi L, Pokharel P, Chang S X, et al. Biochar application increased methane emission, soil carbon storage and net ecosystem carbon budget in a 2-year vegetable-rice rotation[J]. Agriculture, Ecosystems & Environment, 2020, 292. DOI:10.1016/j.agee.2020.106831 |
| [20] |
冯慧琳, 徐辰生, 何欢辉, 等. 生物炭对土壤酶活和细菌群落的影响及其作用机制[J]. 环境科学, 2021, 42(1): 422-432. Feng H L, Xu C S, He H H, et al. Effect of biochar on soil enzyme activity & the bacterial community and its mechanism[J]. Environmental Science, 2021, 42(1): 422-432. |
| [21] |
吴丹, 孙萍, 路鹏展, 等. 浒苔生物炭对滨海盐碱土壤改良的效果及途径[J]. 环境科学, 2020, 41(4): 1941-1949. Wu D, Sun P, Lu P Z, et al. Effect and approach of Enteromorpha prolifera biochar to improve coastal saline soil[J]. Environmental Science, 2020, 41(4): 1941-1949. |
| [22] |
靳玉婷, 李先藩, 蔡影, 等. 秸秆还田配施化肥对稻-油轮作土壤酶活性及微生物群落结构的影响[J]. 环境科学, 2021, 42(8): 3985-3996. Jin Y T, Li X F, Cai Y, et al. Effects of straw returning with chemical fertilizer on soil enzyme activities and microbial community structure in rice-rape rotation[J]. Environmental Science, 2021, 42(8): 3985-3996. |
| [23] | Tian J H, Kuang X Z, Tang M T, et al. Biochar application under low phosphorus input promotes soil organic phosphorus mineralization by shifting bacterial phoD gene community composition[J]. Science of the Total Environment, 2021, 779. DOI:10.1016/j.scitotenv.2021.146556 |
| [24] |
方丹丹, 张立志, 王强. 超顺磁性纳米材料对镉污染稻田土壤微生物和酶的影响[J]. 环境科学, 2021, 42(3): 1523-1534. Fang D D, Zhang L Z, Wang Q. Effects of superparamagnetic nanomaterials on soil microorganisms and enzymes in cadmium-contaminated paddy fields[J]. Environmental Science, 2021, 42(3): 1523-1534. |
| [25] | Du Z L, Wang Y D, Huang J, et al. Consecutive biochar application alters soil enzyme activities in the winter wheat-growing season[J]. Soil Science, 2014, 179(2): 75-83. DOI:10.1097/SS.0000000000000050 |
| [26] |
彭琪, 何红花, 张兴昌. 低磷环境下接种丛枝菌根真菌促进紫花苜蓿生长和磷素吸收的机理[J]. 植物营养与肥料学报, 2021, 27(2): 293-300. Peng Q, He H H, Zhang X C. Mechanisms of increasing alfalfa growth and phosphorus uptake by inoculation with arbuscular mycorrhizal fungal under low phosphorus application level[J]. Journal of Plant Nutrition and Fertilizers, 2021, 27(2): 293-300. |
| [27] | Masto R E, Kumar S, Rout T K, et al. Biochar from water hyacinth (Eichornia crassipes) and its impact on soil biological activity[J]. Catena, 2013, 111: 64-71. DOI:10.1016/j.catena.2013.06.025 |
| [28] | Jin Y, Liang X Q, He M M, et al. Manure biochar influence upon soil properties, phosphorus distribution and phosphatase activities: a microcosm incubation study[J]. Chemosphere, 2016, 142: 128-135. DOI:10.1016/j.chemosphere.2015.07.015 |
| [29] | Romanyà J, Blanco-Moreno J M, Sans F X. Phosphorus mobilization in low-P arable soils may involve soil organic C depletion[J]. Soil Biology and Biochemistry, 2017, 113: 250-259. DOI:10.1016/j.soilbio.2017.06.015 |
| [30] | Yoo G, Kang H. Effects of biochar addition on greenhouse gas emissions and microbial responses in a short-term laboratory experiment[J]. Journal of Environmental Quality, 2012, 41(4): 1193-1202. DOI:10.2134/jeq2011.0157 |
| [31] |
李东坡, 武志杰, 陈利军. 有机农业施肥方式对土壤微生物活性的影响研究[J]. 中国生态农业学报, 2005, 13(2): 99-101. Li D P, Wu Z J, Chen L J. Influence of fertilizing modes of organic agriculture on the soil microbial activities[J]. Chinese Journal of Eco-Agriculture, 2005, 13(2): 99-101. |
| [32] |
陶磊, 褚贵新, 刘涛, 等. 有机肥替代部分化肥对长期连作棉田产量、土壤微生物数量及酶活性的影响[J]. 生态学报, 2014, 34(21): 6137-6146. Tao L, Chu G X, Liu T, et al. Impacts of organic manure partial substitution for chemical fertilizer on cotton yield, soil microbial community and enzyme activities in mono-cropping system in drip irrigation condition[J]. Acta Ecologica Sinica, 2014, 34(21): 6137-6146. |
| [33] | Goldstein A H, Baertlein D A, McDaniel R G. Phosphate starvation inducible metabolism in Lycopersicon esculentum: II. Excretion of acid phosphatase by tomato plants and suspension-cultured cells[J]. Plant physiology, 1988, 87(3): 711-715. DOI:10.1104/pp.87.3.711 |
| [34] | Helal H M. Varietal differences in root phosphatase activity as related to the utilization of organic phosphates[J]. Plant and Soil, 1990, 123(2): 161-163. DOI:10.1007/BF00011262 |
| [35] |
殷全玉, 郭夏丽, 赵铭钦, 等. 延边地区三种类型植烟土壤酶活力、速效养分根际效应研究[J]. 土壤, 2012, 44(6): 960-965. Yin Q Y, Guo X L, Zhao M Q, et al. Study on tobacco rhizosphere effects of soil enzyme activities and available nutrients in three soil types in Yanbian[J]. Soils, 2012, 44(6): 960-965. DOI:10.3969/j.issn.0253-9829.2012.06.011 |
| [36] | Dinkelaker B, Marschner H. In vivo demonstration of acid phosphatase activity in the rhizosphere of soil-grown plants[J]. Plant and Soil, 1992, 144(2): 199-205. DOI:10.1007/BF00012876 |
| [37] | Krämer S, Green D M. Acid and alkaline phosphatase dynamics and their relationship to soil microclimate in a semiarid woodland[J]. Soil Biology and Biochemistry, 2000, 32(2): 179-188. DOI:10.1016/S0038-0717(99)00140-6 |
| [38] | Li M G, Shinano T, Tadano T. Distribution of exudates of lupin roots in the rhizosphere under phosphorus deficient conditions[J]. Soil Science and Plant Nutrition, 1997, 43(1): 237-245. DOI:10.1080/00380768.1997.10414731 |
| [39] |
郑慧芬, 吴红慧, 翁伯琦, 等. 施用生物炭提高酸性红壤茶园土壤的微生物特征及酶活性[J]. 中国土壤与肥料, 2019(2): 68-74. Zheng H F, Wu H H, Weng B Q, et al. Improved soil microbial characteristics and enzyme activities with wheat straw biochar addition to an acid tea plantation in red soil[J]. Soils and Fertilizers Sciences in China, 2019(2): 68-74. |
| [40] | Richardson A E, Barea J M, McNeill A M, et al. Acquisition of phosphorus and nitrogen in the rhizosphere and plant growth promotion by microorganisms[J]. Plant and Soil, 2009, 321(1-2): 305-339. DOI:10.1007/s11104-009-9895-2 |
| [41] |
孙海国, 张福锁. 缺磷条件下的小麦根系酸性磷酸酶活性研究[J]. 应用生态学报, 2002, 13(3): 379-381. Sun H G, Zhang F S. Effect of phosphorus deficiency on activity of acid phosphatase exuded by wheat roots[J]. Chinese Journal of Applied Ecology, 2002, 13(3): 379-381. DOI:10.3321/j.issn:1001-9332.2002.03.030 |
| [42] | Nuruzzaman M, Lambers H, Bolland M D A, et al. Distribution of carboxylates and acid phosphatase and depletion of different phosphorus fractions in the rhizosphere of a cereal and three grain legumes[J]. Plant and Soil, 2006, 281(1-2): 109-120. DOI:10.1007/s11104-005-3936-2 |
| [43] |
徐华勤, 肖润林, 邹冬生, 等. 长期施肥对茶园土壤微生物群落功能多样性的影响[J]. 生态学报, 2007, 27(8): 3355-3361. Xu H Q, Xiao R L, Zou D S, et al. Effects of long-term fertilization on functional diversity of soil microbial community of the tea plantation[J]. Acta Ecologica Sinica, 2007, 27(8): 3355-3361. DOI:10.3321/j.issn:1000-0933.2007.08.031 |
| [44] | 江琳琳. 生物炭对土壤微生物多样性和群落结构的影响[D]. 沈阳: 沈阳农业大学, 2016. |
| [45] | Doan T T, Bouvier C, Bettarel Y, et al. Influence of buffalo manure, compost, vermicompost and biochar amendments on bacterial and viral communities in soil and adjacent aquatic systems[J]. Applied Soil Ecology, 2014, 73: 78-86. DOI:10.1016/j.apsoil.2013.08.016 |
| [46] | Ameloot N, Graber E R, Verheijen F G A, et al. Interactions between biochar stability and soil organisms: review and research needs[J]. European Journal of Soil Science, 2013, 64(4): 379-390. DOI:10.1111/ejss.12064 |
| [47] | Wang C, Zhao X Q, Chen R F, et al. Aluminum tolerance of wheat does not induce changes in dominant bacterial community composition or abundance in an acidic soil[J]. Plant and Soil, 2013, 367(1-2): 275-284. DOI:10.1007/s11104-012-1473-3 |
| [48] | Castorena E V G, Gutiérrez-Castorena M D C, Vargas T G, et al. Micromapping of microbial hotspots and biofilms from different crops using digital image mosaics of soil thin sections[J]. Geoderma, 2016, 279: 11-21. DOI:10.1016/j.geoderma.2016.05.017 |
| [49] |
刘文干, 曹慧, 樊建波, 等. 一株红壤花生根际溶磷真菌的分离、鉴定及溶磷能力的研究[J]. 土壤学报, 2012, 49(5): 988-995. Liu W G, Cao H, Fan J B, et al. Isolation, identification and characterization of a phosphate-solubilizing strain of fungi in rhizosphere of peanuts growing in red soil[J]. Acta Pedologica Sinica, 2012, 49(5): 988-995. |
| [50] |
郑曼曼, 王超, 沈仁芳. 碳酸钙和根际作用对酸性红壤解磷微生物丰度的影响[J]. 土壤, 2020, 52(4): 704-709. Zheng M M, Wang C, Shen R F. Effects of calcium carbonate and rhizosphere on abundance of phosphate-solubilizing microorganisms in acidic red soil[J]. Soils, 2020, 52(4): 704-709. |
| [51] |
陈海燕, 樊霆, 张泽, 等. 不同植物修复重金属复合污染土壤对土壤中微生物数量与酶活性的影响[J]. 环境保护, 2018, 46(1): 65-69. Chen H Y, Fan T, Zhang Z, et al. Effects of four plants on soil microbial biomass and soil enzyme activity in heavy metal combined polluted soil[J]. Environmental Protection, 2018, 46(1): 65-69. DOI:10.3969/j.issn.1006-4362.2018.01.013 |
| [52] | Nannipieri P, Giagnoni L, Renella G, et al. Soil enzymology: classical and molecular approaches[J]. Biology and Fertility of Soils, 2012, 48(7): 743-762. DOI:10.1007/s00374-012-0723-0 |
| [53] | Fraser T D, Lynch D H, Bent E, et al. Soil bacterial phoD gene abundance and expression in response to applied phosphorus and long-term management[J]. Soil Biology and Biochemistry, 2015, 88: 137-147. DOI:10.1016/j.soilbio.2015.04.014 |
 2022, Vol. 43
2022, Vol. 43


