2. 自然资源部/广西岩溶动力学重点实验室, 桂林 541004
2. Key Laboratory of Karst Dynamics, Ministry of Natural Resources & Guangxi, Guilin 541004, China
地下水氮污染已成为一个全球性的生态环境问题, 引起了国内外学者的普遍关注[1, 2].长期饮用高硝酸盐(NO3-)的地下水会使人体积累过量NO3-, NO3-在体内可被还原为亚硝酸盐(NO2-), 易引起高铁血红蛋白症.NO2-与仲胺类作用可形成亚硝胺, 亚硝胺在人体积累到一定剂量可致癌、致畸和致突变, 严重危害身体健康[3].
岩溶水是重要的水资源, 在我国岩溶含水层为超过1亿人口提供饮用水源.NO3-在水环境中具有易溶性和高迁移性[4].近些年由于工农业活动、旅游活动、生活污水等导致岩溶水遭受NO3-污染的现象多有报道[5~7].岩溶区“三水”转化迅速, 不利于反硝化过程的进行, 岩溶含水层一旦遭受NO3-污染, 其作为饮用水源的安全风险更大[8].为有效防控岩溶区地下水NO3-污染, 需要对其来源及转化过程进行解析.
近些年, 水化学与硝酸盐氮氧同位素(δ15N-NO3和δ18O-NO3)相结合成功运用于示踪河流[9]、湖泊[10]、水库[11]、湿地[12]和地下水[13, 14]等水体中NO3-来源.利用δ15N-NO3与δ18O-NO3的富集比率和δ18O-NO3与δ18O-H2O之间的关系有效判别了水体中NO3-的转化过程[15, 16].SIAR同位素源解析模型的运用使定量分析水体中NO3-的来源成为可能[17].已有研究表明, 岩溶区由于人为源输入的硝酸会加速碳酸盐岩的溶解, 导致地下水中溶解无机碳碳同位素(δ13CDIC)值偏正[18], δ13CDIC与地下水中NO3-呈正相关性.目前, 利用δ13CDIC识别NO3-转化过程的研究并不多见.本研究选取八步地下河流域, 结合水化学和多同位素(δ15N-NO3、δ18O-NO3和δ18O-H2O)手段, 并尝试利用δ13CDIC来解析流域内地下水中NO3-转化过程.利用SIAR模型定量计算NO3-不同输入端的贡献比例, 以期为有效防控岩溶区地下水NO3-污染提供一定参考依据.
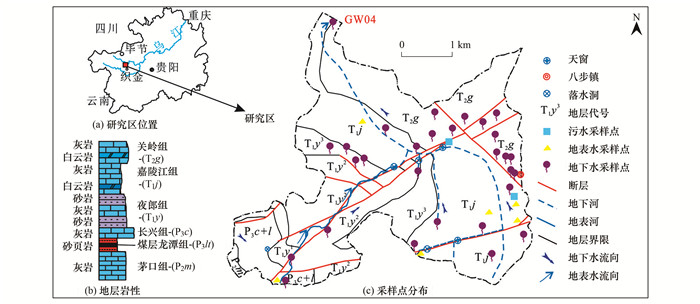
1 材料与方法 1.1 研究区概况八步地下河流域总面积18.08 km2, 属于典型的岩溶小盆地.地理坐标:105°44′~105°50′E, 26°48′~26°52′N, 位于贵州省织金县八步街道[图 1(a)].气候为亚热带季风性气候, 多年平均气温14.1℃, 多年平均降雨量1 402 mm.降雨多集中在5~10月, 占全年降雨量的83.6%.地层为浅海相沉积, 以二叠系和三叠系为主[图 1(b)], 第四系覆盖层较薄.流域内碳酸盐岩分布最广, 占总面积的83%; 碎屑岩地层为3.12 km2, 仅占总面积的17%.研究区属于裸露型岩溶环境, 岩溶裂隙、落水洞和岩溶天窗等岩溶形态发育[图 1(c)].八步地下河出口(GW04)流量在0.1~1.5 m3·s-1之间, 为八步街道的重要饮用水源地.
|
图 1 八步地下河流域水文地质示意 Fig. 1 Hydrogeological map of the Babu underground river basin |
八步地下河所在的八步街道是贵州省重点产业园区.近几年来, 随着产业园的发展, 人口由以往的1万人增至近3万人, 导致镇上污水排放量增加[19].同时蔬菜种植基地、经济林面积快速扩大, 为提高作物单产量, 化学肥料和粪肥的施用量也相应增加.
1.2 样品采集与测试2019年11月采集了29个地下水(GW01~GW29)、6个地表水(SW01~SW06)、2个污水(C01~C02)和2个雨水(R01~R02).
水体的pH、溶解氧(DO)和温度(T)用WTW3430现场测试, 精度分别为0.01、0.01 mg·L-1和0.01℃.阴离子用500 mL聚乙烯塑料瓶采集. δ18O-H2O、δ15N-NO3、δ18O-NO3和δ13CDIC样分别用50 mL棕色聚乙烯塑料瓶采集, 其中δ13CDIC样加3~5滴饱和HgCl2.取样瓶用过滤(0.45 μm滤膜)后的水润洗3~4次再装样.水样4℃冷藏待测.
NO3-和Cl-用离子色谱仪(Dionex ICS-1100)测定, 精度分别为0.05 mg·L-1和0.1 mg·L-1. NO2-和NH4+用T6新悦可见分光光度计测定, 精度分别为0.002 mg·L-1和0.02 mg·L-1. δ18O-H2O用MAT-253测定, 精度优于0.05%. δ13CDIC用MAT-253连接Gas Bench Ⅱ测定, 绝对误差<0.15‰.以上样品测定工作在自然资源部岩溶地质资源环境监督检测中心完成.δ15N-NO3和δ18O-NO3样品在中国农业科学院农业环境与可持续发展研究所测试.
1.3 SIAR同位素源解析模型SIAR模型是由Parnell等[17]开发的一个基于R统计软件的稳定同位素混合模型, 它的运用使对污染物的来源解析从定性转为定量.SIAR模型运用的前提是水体中未发生明显的反硝化作用, 其通过定义k个来源n个混合物的j个同位素, 考虑到同位素分馏作用的影响, 表示为[公式(1)]:
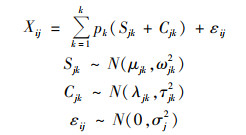
|
(1) |
式中, Xij是混合物同位素的δ值, 其中: i=1, 2, 3, …, N, j=1, 2, 3, …, J; Sjk是第k个端元的j同位素值(k=1, 2, 3, …), μjk为均值, ωjk为标准偏差; pk为端元k的贡献比例, 需要根据SIAR模型来预测; Cjk是端元k在j同位素上的分馏因子, λjk为分馏因子的均值, τjk为标准偏差; εij为剩余误差, 代表不同单个混合物间未能确定的变量, 其均值为0, 标准偏差为σj.
2 结果与分析采样点水化学和同位素测试结果列于表 1.
|
|
表 1 八步地下水、地表水、污水和雨水水化学和同位素组成1) Table 1 Hydrochemical and isotopic compositions of groundwater, surface water, sewage, and rainwater samples from Babu |
2.1 水化学特征
研究区碳酸盐岩广布, 地下水和地表水呈中至弱碱性, pH平均值分别为7.38和7.48.受到附近火电厂的影响, 雨水pH分别为5.61和5.62, 偏酸性.地下水和地表水的DO分别在1.26~8.37 mg·L-1和5.14~10.21 mg·L-1之间, 平均值分别为5.49 mg·L-1和8.29 mg·L-1, 说明研究区地下水和地表水整体上处于有氧环境, 富氧程度:地表水>地下水.污水DO分别为3.58 mg·L-1和3.67 mg·L-1, 低于地下水和地表水.地下水和地表水Cl-平均值分别为9.68 mg·L-1和10.37 mg·L-1, 地下水 < 地表水.污水中Cl-高达112.46 mg·L-1.
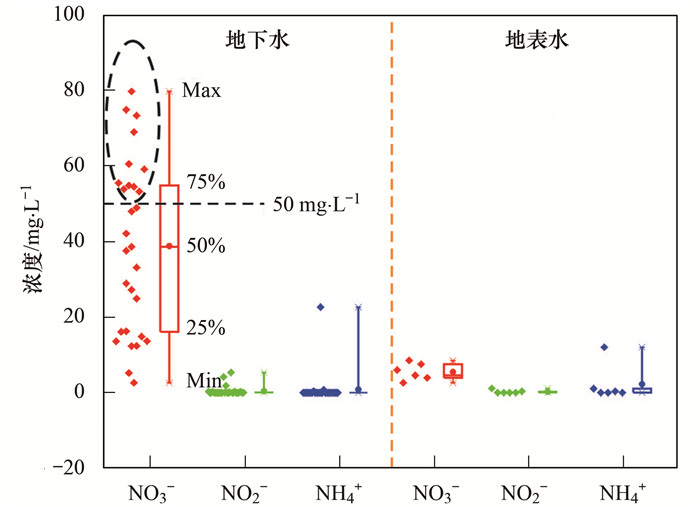
2.2 氮污染特征研究区地下水和地表水中NO3-、NO2-和NH4+分布如图 2所示.地下水中NO3-的检出率为100%, 浓度在2.59~79.72 mg·L-1之间, 平均值为38.78 mg·L-1.NO3-含量约占TN的95%以上, 近38%(11个)的样品中NO3-浓度超过了生活饮用水限值(限值50 mg·L-1, 98/83/EC).地下水中NO2-的检出率为72%(21个), 其中3个超过了限值, 最高达5.36 mg·L-1.地下水中NH4+的检出率为41%, 其中2个超过了限值(0.5 mg·L-1), 最高达22.67 mg·L-1.研究区地下水“三氮”污染严重, 部分点位NO2-超出限值10倍, NH4+超出限值近45倍.此次采集的29个泉水全部为饮用水源, 长期饮用将对流域内人体健康产生潜在的危害.
|
图 2 流域内地下水和地表水“三氮”浓度箱型图 Fig. 2 Box diagram of the "three nitrogen" concentrations of ground and surface waters in the basin |
与地下水相比, 地表水的NO3-含量较低, 浓度在2.61~8.25 mg·L-1之间.地表水中NO2-和NH4+的检出率分别为66%和83%, 平均值分别为0.39 mg·L-1和2.7 mg·L-1.地表水中NO2-和NH4+最大值分别为1.12 mg·L-1和12.03 mg·L-1, 是限值的2倍和24倍.
污水中NO2-未检出, NO3-相对较低, NH4+含量最高, NH4+分别为12.62 mg·L-1和211.2 mg·L-1.雨水中NH4+未检出, NO2-和NO3-也较低.
2.3 同位素特征地下水和地表水的δ15N-NO3平均值分别为7.52‰和7.62‰, δ18O-NO3平均值分别为6.64‰和5.89‰.与之相比, 污水有着较高的δ15N-NO3和δ18O-NO3值, 平均值分别为22.79‰和50.95‰.地下水和地表水δ18O-H2O分别在-8.83‰~-7.37‰和-7.03‰~-3.68‰之间, 均值为-8.18‰和-6.04‰.地表水较地下水富集偏重的δ18O-H2O, 可能是较强的蒸发引起同位素分馏所致.地下水中的δ13CDIC在-13.65‰~-6.76‰之间, 平均值为-10.62‰.
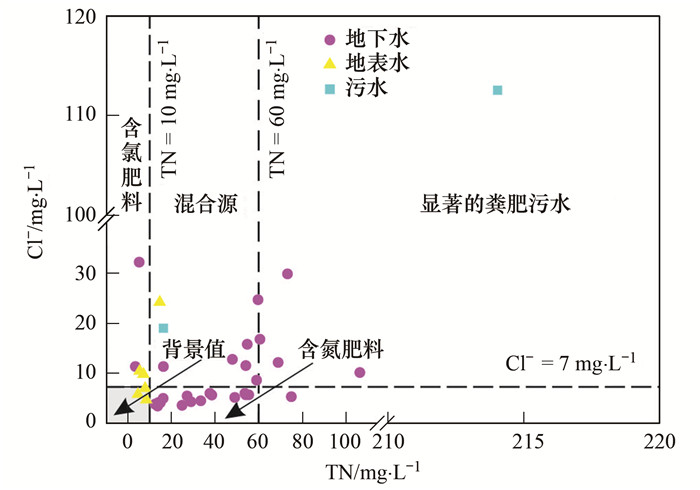
3 讨论 3.1 硝酸盐来源定性解析 3.1.1 TN-Cl法解译污染物(如污水、化肥和人类/动物排泄物)进入岩溶含水层常导致地下水中TN和/或Cl-浓度上升.Panno等[20]的研究证实TN-Cl方法是判别地下水是否受到人为影响的有效手段:①当流域内施用含氯肥料时, 地下水有高Cl-低TN特征; ②当流域内施用含氮肥料时, 地下水低Cl-高TN; ③含水层受粪肥污水强烈影响时, 地下水高Cl-高TN; ④多种来源混合时, 具有中等浓度的Cl-和TN. Panno等[21]将岩溶区地下水TN限值定在10 mg·L-1, Cl-定在15 mg·L-1, 若样品浓度超过限定值暗示着人为污染源.当TN浓度超过60 mg·L-1时, 地下水明显受到人类/动物排泄物污染.Zhang等[22]在美国中西部岩溶区发现大部分泉水Cl-浓度低于15 mg·L-1, 包括一些受到人为污染的泉水, 他们认为在这些区域应当把Cl-的限定值降低至7 mg·L-1.宋小庆等[23]在贵州采集的3 699个浅层地下水中发现Cl-背景值在3.45~6.65 mg·L-1之间, 且研究区2个雨水中的Cl-浓度分别为2.98 mg·L-1和3.61 mg·L-1.因此, 本文也尝试把Cl-值降低至7 mg·L-1.
从图 3可以看出, 研究区地下水样品皆受到了人类活动的影响, 氮和Cl-来源具有多元化, 包括含氮肥料、粪肥污水及混合源.个别点位有高Cl-低TN特征, Cl-可能来源于含氯肥料, 如流域内农作物使用的KCl等.
|
图 3 流域内水体Cl-与TN关系 Fig. 3 The Cl- vs. TN plots for water samples in the basin |
水体中NO3-除来源于含氮肥料和粪肥污水外, 还可能来源于大气沉降和土壤氮.含氮肥料包括硝态氮肥料和铵态氮肥料, 大气沉降包括雨水中的NO3-和NH4+.因研究区雨水中NH4+未检出, 暂不考虑.利用δ15N-NO3与NO3-浓度和δ15N-NO3与δ18O-NO3之间的关系有助于判别水体中NO3-的多种来源[9~12].
已有研究指出, 地下水中NO3-来源于粪肥时具有高δ15N-NO3值和高NO3-浓度的“双高特征”, 来自化肥时出现较低δ15N-NO3值和高NO3-浓度特征, 来自生活污水时出现中等δ15N-NO3值和中等NO3-浓度特征[24].研究区地下水中δ15N-NO3值在2.3‰~30.33‰之间(均值7.52‰), NO3-浓度在2.59~79.72 mg·L-1之间(均值38.78 mg·L-1), δ15NO-NO3和NO3-变化范围较大[图 4(a)], 并不具有来源唯一的特性, 说明地下水中NO3-来源复杂.

|
图 4 流域内水体NO3-与δ15N-NO3和δ15N-NO3和δ18O-NO3关系 Fig. 4 The NO3- vs. δ15N-NO3 and δ15N-NO3 vs. δ18O-NO3 plots for water samples in the basin |
从图 4(b)可以看出, 研究区地下水样几乎全部落在了铵态氮肥料、土壤氮和粪肥污水的范围内, 说明铵态氮肥料、土壤氮和粪肥污水是地下水中NO3-的主要输入源, 降雨和硝态氮肥料的影响不明显[22].地表水中NO3-的来源主要为土壤氮和粪肥污水, 铵态氮肥料次之.
3.2 硝酸盐的转化过程 3.2.1 δ18O-H2O与δ15N-NO3解译NO3-中δ15N-NO3和δ18O-NO3值不仅取决于其来源, 还受生物过程的影响, 如微生物硝化作用和反硝化作用.由于硝化细菌优先利用较轻的元素, 使得硝化作用产生的NO3-中δ15N-NO3和δ18O-NO3值偏轻, 而残留物中的元素偏重[25].硝化作用产生的NO3-中, 约2/3的氧来源于周围水体, 剩余1/3的氧来源于溶解于水体的氧气(23.5‰)[26].因此, 水体中是否发生硝化过程可由测得的δ18O-NO3值来指示[25], 即:
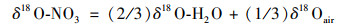
|
(2) |
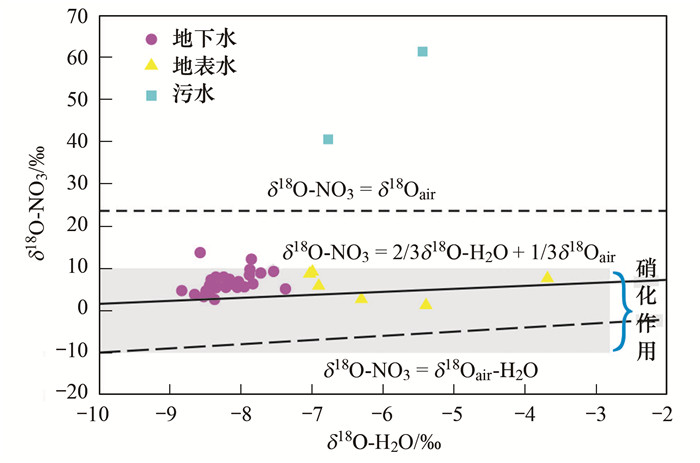
研究区地下水和地表水中大部分采样点δ18O-NO3值仅略大于理论值(图 5), 且93%的地下水和全部地表水中δ18O-NO3值落在硝化作用产生的典型δ18O-NO3值范围(-10‰~10‰)[26]内, 说明地下水和地表水中硝化作用对NO3-来源起主导作用.地下水中只有2个点位的δ18O-NO3值大于10‰, 可能是较高的δ18O-H2O大气降水输入、硝化过程中周围水体的δ18O-H2O已发生了同位素分馏或反硝化作用等导致.地下水中δ18O-NO3与δ18O-H2O虽无显著相关性(P>0.05), 但随着δ18O-H2O值增大, δ18O-NO3值仍呈增加趋势(图 5), 说明较高的δ18O-H2O值大气降水输入或δ18O-H2O同位素分馏对部分地下水样的δ18O-NO3值产生了一定影响.
|
图 5 流域内水体δ18O-H2O和δ18O-NO3关系 Fig. 5 The δ18O-H2O vs. δ18O-NO3 plots for water samples in the basin |
反硝化过程会引起显著的同位素分馏, 导致地下水残留物中富集偏重的δ15N-NO3和δ18O-NO3, δ15N-NO3与δ18O-NO3的增长速率比值通常在1.3∶1~2.1∶1之间[27, 28], 同时NO3-浓度降低.由图 4可以看出, 地下水中有2个点落在反硝化作用范围内, 其DO分别为1.26 mg·L-1和1.92 mg·L-1, 小于反硝化作用的上限(2.0 mg·L-1)[29], 可能受反硝化作用影响.其余地下水样品DO皆大于2.0 mg·L-1(均值为5.49 mg·L-1), 地表水在5.14~10.21 mg·L-1之间(均值为8.29 mg·L-1), 整体上处于富氧环境, 不利于反硝化作用进行.另外, 地下水和地表水中NO3-浓度也并未随着δ15N-NO3的增加呈降低趋势(图 4), 仅有个别点位落在反硝化用作范围内, 说明硝化作用是整个流域氮循环的主导过程.
3.2.2 δ13CDIC与δ15N-NO3和δ13CDIC与ln(NO3-)解译硝化过程是由自氧型细菌分阶段完成, 主要包括两个阶段:第一阶段为亚硝化, 即NH4+氧化为NO2-[公式(3)]; 第二阶段为硝化, 即NO2-氧化为NO3-[公式(4)].硝化作用会导致地下水中NO3-增加[公式(5)].硝化细菌在硝化的过程中吸收NH4+, 为保持电荷平衡会释放质子(H+), 地下水pH下降.硝化过程产生的酸(H+)会加速碳酸盐岩的风化[公式(5)], 使更多来自碳酸盐岩偏重的“老碳”进入地下水, 导致地下水中δ13CDIC值偏正[18, 19].如果岩溶含水层发生硝化作用, 地下水中δ15N-NO3和δ13CDIC应存在负相关性, NO3-和δ13CDIC存在正相关性.
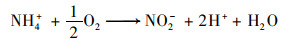
|
(3) |

|
(4) |

|
(5) |
研究区地下水中δ15N-NO3与δ13CDIC存在显著性负相关关系[图 6(a)], 再次证明硝化作用是整个流域氮循环的主要控制因素.地下水中NO3-和δ13CDIC虽不存在明显正相关性[图 6(b)], 但整体看随着δ13CDIC值增加, NO3-浓度仍有上升趋势, 也指示硝化作用的存在.NO3-和δ13CDIC之间不存在显著性正相关关系可能是硝化作用产生的NO3-受到低NO3-的补给水源稀释等作用的影响所致.
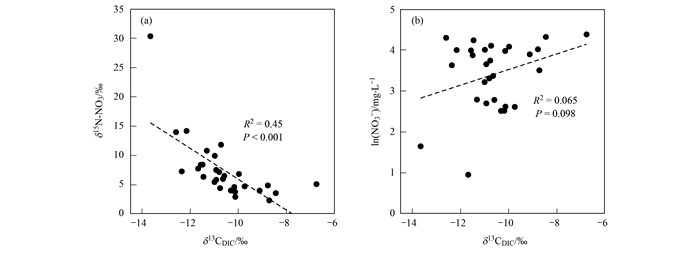
|
图 6 流域内地下水中δ13CDIC与δ15N-NO3和δ13CDIC与ln(NO3-)关系 Fig. 6 The δ13CDIC vs. δ15N-NO3 and δ13CDIC vs. ln(NO3-) plots for water samples in the basin |
前文分析知硝化作用主导着流域内水体氮循环, 反硝化作用不明显, 可利用SIAR模型定量解析水体中不同NO3-输入端的贡献比例.结合流域内的水文地质条件和人类活动情况, 在计算过程中铵态氮肥料、土壤氮和粪肥污水的同位素典型值取自文献[1], 分馏因子Cjk取0.
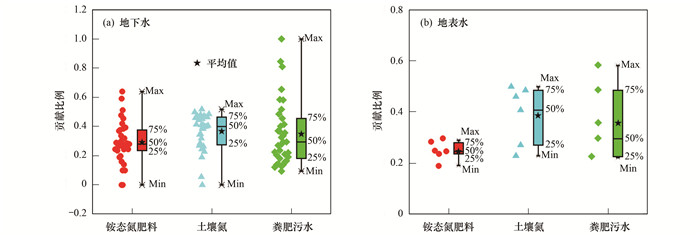
从SIAR模型计算结果看(图 7), 研究区不同端元对地下水中NO3-贡献大小为土壤氮(36.19%)>粪肥污水(33.71%)>铵态氮肥料(30.1%); 对地表水中NO3-贡献大小为土壤氮(39.15%)>粪肥污水(36.08%)>铵态氮肥料(24.77%).不同输入端元对地下水和地表水中NO3-贡献大小具有一致性:土壤氮>粪肥污水>铵态氮肥料.
|
图 7 流域内地下水中和地表水不同输入端贡献比例 Fig. 7 Potential source contributions to ground and surface water plots in the basin |
水体中高浓度的NH4+可以为硝化细菌提供物质来源, 提高硝化速率[30].流域内城镇生活污水(C01和C02)经过反硝化处理, NO3-基本去除, 但仍有高浓度的NH4+, 分别为12.62 mg·L-1和211.1 mg·L-1.污水在地表流动过程中与大气氧“掺和”[31], DO上升至3.58 mg·L-1和3.67 mg·L-1, 高于反硝化作用限值(2 mg·L-1).室内模拟实验表明岩溶含水层的反硝化作用有限[8].污水通过分散入渗或集中灌入补给岩溶含水层, 在流动的过程中发生硝化作用, 将导致地下水NO3-含量增加.研究区在污水中NO3-浓度极低的情况下, 粪肥污水对地下水和地表水NO3-贡献仍达33.71%和36.08%, 除粪肥的贡献外, 污水中硝化作用产生的NO3-不容忽视.研究区地下河出口水中DO为6.96 mg·L-1, NO3-浓度高达79.72 mg·L-1(地下水样中最大值), 证实八步地下河管道流发生了硝化作用.
调查发现, 流域内农作物施用的肥料以铵态氮肥料和粪肥为主.铵态氮肥料易于被土壤胶体吸附, 但也容易氧化产生NO3-.铵态氮肥料在岩溶区碱性环境下易于挥发损失, 而高浓度铵态氮又会造成土壤酸化, 对农作物产生危害.另外, 农作物施用的粪肥长时间堆放在农田, 在硝化作用下也会产生大量的NO3-.土壤胶体多带负电荷, 不易吸附NO3-[32], NO3-在雨水携带下极易进入含水层.岩溶含水层中颗粒物多来源于降雨对流域内土壤的冲刷, 水体中胶体也带负电荷, 这意味着岩溶含水层一旦遭受NO3-污染, 恢复治理极为困难.岩溶流域内污水处理去除NO3-的同时, 也应当去除污水中高浓度的NH4+.农业活动应加强对肥料的调控, 适当选择硝态氮肥料, 科学定量施肥, 对症追肥.
5 结论(1) 研究区29个地下水样中, 11个NO3-浓度超过生活饮用水卫生限值, 3个NO2-超过了限值, 2个NH4+超过了限值.NO3-浓度最高达79.72 mg·L-1, 部分点位NO2-超出限值10倍, NH4+超出限值近45倍.地下水“三氮”污染严重, NO3-居首位.
(2) 地下水的δ15N-NO3值介于2.3‰~30.33‰, 均值9.68‰, δ18O-NO3值介于2.65‰~13.73‰, 均值6.64‰, δ18O-H2O值介于-8.83‰~-7.37‰, 均值-8.18‰.δ15N-NO3、δ18O-NO3和δ18O-H2O同位素组成指示硝化作用主导着地下水和地表水中氮素循环.硝化作用产生的硝酸加速碳酸盐岩溶解, 导致地下水中δ13CDIC(-13.65‰~-6.76‰, 均值-10.62‰)与δ15N-NO3存在显著负相关性(P < 0.001), 说明δ13CDIC与δ15N-NO3相结合是判断岩溶水中NO3-转化的有效手段.
(3) 研究区NO3-来源主要为土壤氮、粪肥污水和铵态氮肥料, 其对地下水中的NO3-贡献率分别为36.19%、33.71%和30.1%, 对地表水贡献率分别为39.15%、36.08%和24.77%.
(4) 岩溶区污水处理时应当考虑同时去除污水中的NO3-和NH4+, 农业活动应加强对肥料的调控, 科学定量施肥, 对症追肥.
| [1] | Zhang Y, Shi P, Li F D, et al. Quantification of nitrate sources and fates in rivers in an irrigated agricultural area using environmental isotopes and a Bayesian isotope mixing model[J]. Chemosphere, 2018, 208: 493-501. DOI:10.1016/j.chemosphere.2018.05.164 |
| [2] |
梁杏, 孙立群, 张鑫, 等. 无机态氮素转化机制及水土体氮源识别方法[J]. 环境科学, 2020, 41(9): 4333-4344. Liang X, Sun L Q, Zhang X, et al. Mechanism of inorganic nitrogen transformation and identification of nitrogen sources in water and soil[J]. Environmental Science, 2020, 41(9): 4333-4344. |
| [3] |
陈建耀, 王亚, 张洪波, 等. 地下水硝酸盐污染研究综述[J]. 地理科学进展, 2006, 25(1): 34-44. Chen J Y, Wang Y, Zhang H B, et al. Overview on the studies of nitrate pollution in groundwater[J]. Progress in Geography, 2006, 25(1): 34-44. |
| [4] | Négrel P, Pauwels H. Interaction between different groundwaters in Brittany catchments (France): Characterizing multiple sources through strontium- and sulphur isotope tracing[J]. Water, Air, and Soil Pollution, 2004, 151(1-4): 261-285. DOI:10.1023/B:WATE.0000009912.04798.b7 |
| [5] | Yang P H, Li Y, Groves C, et al. Coupled hydrogeochemical evaluation of a vulnerable karst aquifer impacted by septic effluent in a protected natural area[J]. Science of the Total Environment, 2019, 658: 1475-1484. DOI:10.1016/j.scitotenv.2018.12.172 |
| [6] | Yue F J, Waldron S, Li S L, et al. Land use interacts with changes in catchment hydrology to generate chronic nitrate pollution in karst waters and strong seasonality in excess nitrate export[J]. Science of the Total Environment, 2019, 696. DOI:10.1016/j.scitotenv.2019.134062 |
| [7] | 郭芳, 王文科, 姜光辉, 等. 岩溶地下河污染物运移特征及自净能力——以广西里湖地下河为例[J]. 水科学进展, 2014, 25(3): 414-419. |
| [8] |
陈余道, 程亚平, 蒋亚萍, 等. 岩溶地下河反硝化作用的有限性——一个碳酸盐岩管道的实验研究[J]. 环境科学学报, 2016, 36(10): 3629-3635. Chen Y D, Cheng Y P, Jiang Y P, et al. Limitation of denitrification in karst subterranean river: A carbonate-conduit experimental study[J]. Acta Scientiae Circumstantiae, 2016, 36(10): 3629-3635. |
| [9] |
齐冉, 徐菲菲, 杨帆, 等. 木沥河流域氮素污染及其污染源解析[J]. 环境科学, 2020, 41(7): 3165-3174. Qi R, Yu F F, Yang F, et al. Analysis of nitrogen pollution and its pollution sources in the Muli River basin[J]. Environmental Science, 2020, 41(7): 3165-3174. |
| [10] |
殷超, 杨海全, 陈敬安, 等. 基于水化学和氮氧同位素的贵州草海丰水期水体硝酸盐来源辨析[J]. 湖泊科学, 2020, 32(4): 989-998. Yin C, Yang H Q, Chen J A, et al. Tracing nitrate sources with dual isotopes and hydrochemical characteristics during wet season in Lake Caohai, Guizhou Province[J]. Journal of Lake Sciences, 2020, 32(4): 989-998. |
| [11] |
金赞芳, 张文辽, 郑奇, 等. 氮氧同位素联合稳定同位素模型解析水源地氮源[J]. 环境科学, 2018, 39(5): 2039-2047. Jin Z F, Zhang W L, Zheng Q, et al. Contribution of nitrogen sources in water sources by combining nitrogen and oxygen isotopes and SIAR[J]. Environmental Science, 2018, 39(5): 2039-2047. |
| [12] |
孔晓乐, 王仕琴, 丁飞, 等. 基于水化学和稳定同位素的白洋淀流域地表水和地下水硝酸盐来源[J]. 环境科学, 2018, 39(6): 2624-2631. Kong X L, Wang S Q, Ding F, et al. Source of nitrate in surface water and shallow groundwater around Baiyangdian lake area based on hydrochemical and stable isotopes[J]. Environmental Science, 2018, 39(6): 2624-2631. |
| [13] |
田永著, 韩志伟, 赵然, 等. 岩溶流域不同水体硝酸盐的来源解析[J]. 环境科学, 2020, 41(7): 3157-3164. Tian Y Z, Han Z W, Zhao R, et al. Analysis of nitrate sources in different waters of a karst basin[J]. Environmental Science, 2020, 41(7): 3157-3164. |
| [14] |
段世辉, 蒋勇军, 张远瞩, 等. 岩溶槽谷区地下河硝酸盐来源及其环境效应: 以重庆龙凤槽谷地下河系统为例[J]. 环境科学, 2019, 40(4): 1715-1725. Duan S H, Jiang Y J, Zhang Y Z, et al. Sources of nitrate in groundwater and its environmental effects in karst trough valleys: A case study of an underground river system in the Longfeng trough valley, Chongqing[J]. Environmental Science, 2019, 40(4): 1715-1725. |
| [15] | Yue F J, Li S L, Liu C Q, et al. Using dual isotopes to evaluate sources and transformation of nitrogen in the Liao river, northeast China[J]. Applied Geochemistry, 2013, 36: 1-9. |
| [16] | Zheng W B, Wang S Q, Tan K D, et al. Nitrate accumulation and leaching potential is controlled by land-use and extreme precipitation in a headwater catchment in the North China Plain[J]. Science of the Total Environment, 2020, 707. DOI:10.1016/j.scitotenv.2019.136168 |
| [17] | Parnell A C, Inger R, Bearhop S, et al. Source partitioning using stable isotopes: coping with too much variation[J]. PLoS One, 2010, 5(3). DOI:10.1371/journal.pone.0009672 |
| [18] | Jiang Y J. The contribution of human activities to dissolved inorganic carbon fluxes in a karst underground river system: Evidence from major elements and (13CDIC in Nandong, southwest China[J]. Journal of Contaminant Hydrology, 2013, 152: 1-11. |
| [19] |
任坤, 潘晓东, 焦友军, 等. 贵州洪家渡盆地泉水水化学和碳同位素特征及成因[J]. 水文地质工程地质, 2019, 46(3): 9-17. Ren K, Pan X D, Jiao Y J, et al. Characteristics and controls of the hydrochemistry and carbon isotope of the spring water in the Hongjiadu Basin of Guizhou[J]. Hydrogeology & Engineering Geology, 2019, 46(3): 9-17. |
| [20] | Panno S V, Hackley K C, Hwang H H, et al. Characterization and identification of Na-Cl sources in ground water[J]. Ground Water, 2006, 44(2): 176-187. |
| [21] | Panno S V, Kelly W R, Martinsek A T, et al. Estimating background and threshold nitrate concentrations using probability graphs[J]. Ground Water, 2006, 44(5): 697-709. |
| [22] | Zhang Y, Kelly W R, Panno S V, et al. Tracing fecal pollution sources in karst groundwater by Bacteroidales genetic biomarkers, bacterial indicators, and environmental variables[J]. Science of the Total Environment, 2014, 490: 1082-1090. |
| [23] |
宋小庆, 彭钦, 王伟, 等. 贵州岩溶区浅层地下水氯化物及硫酸盐环境背景值[J]. 地球科学, 2019, 44(11): 3926-3938. Song X Q, Peng Q, Wang W, et al. Analysis of environmental background values of chloride and sulfate in shallow groundwater in karst area of Guizhou[J]. Earth Science, 2019, 44(11): 3926-3938. |
| [24] |
贺国平, 刘培斌, 慕星, 等. 永定河冲洪积扇地下水中硝酸盐来源的同位素识别[J]. 水利学报, 2016, 47(4): 582-588. He G P, Liu P B, Mu X, et al. Identification of nitrate sources in groundwater in the Yongding river alluvial fan with isotope technology[J]. Journal of Hydraulic Engineering, 2016, 47(4): 582-588. |
| [25] |
路路, 戴尔阜, 程千钉, 等. 基于水环境化学及稳定同位素联合示踪的土地利用类型对地下水体氮素归趋影响[J]. 地理学报, 2019, 74(9): 1878-1889. Lu L, Dai E F, Cheng Q D, et al. The sources and fate of nitrogen in groundwater under different land use types: Stable isotope combined with a hydrochemical approach[J]. Acta Geographica Sinica, 2019, 74(9): 1878-1889. |
| [26] | Kendall C. Tracing nitrogen sources and cycling in catchments[A]. In: Kendall C, Mcdonnell J J (Eds. ). Isotope Tracers in Catchment Hydrology[M]. Amsterdam: Elsevier Science, 1998. 519-576. |
| [27] | Xue D M, Botte J, De Baets B, et al. Present limitations and future prospects of stable isotope methods for nitrate source identification in surface- and groundwater[J]. Water Research, 2009, 43(5): 1159-1170. |
| [28] | Clague J C, Stenger R, Clough T J. Evaluation of the stable isotope signatures of nitrate to detect denitrification in a shallow groundwater system in New Zealand[J]. Agriculture, Ecosystems & Environment, 2015, 202: 188-197. |
| [29] | Gillham R W, Cherry J A. Field evidence of denitrification in shallow groundwater flow systems[J]. Water Quality Research Journal, 1978, 13(1): 53-72. |
| [30] | Zaman Di H J, Cameron K C, et al. Gross nitrogen mineralization and nitrification rates and their relationships to enzyme activities and the soil microbial biomass in soils treated with dairy shed effluent and ammonium fertilizer at different water potentials[J]. Biology and Fertility of Soils, 1999, 29(2): 178-186. |
| [31] |
任坤, 梁作兵, 于正良, 等. 重庆南山老龙洞地下河系统重金属分布、迁移及自净能力[J]. 环境科学, 2015, 36(11): 4095-4102. Ren K, Liang Z B, Yu Z L, et al. Distribution and transportation characteristics of heavy metals in Nanshan laolongdong subterranean river system and its capacity of self-purification in Chongqing[J]. Environmental Science, 2015, 36(11): 4095-4102. |
| [32] | Jiang Y J, Wu Y X, Groves C, et al. Natural and anthropogenic factors affecting the groundwater quality in the Nandong karst underground river system in Yunan, China[J]. Journal of Contaminant Hydrology, 2009, 109(1-4): 49-61. |
 2021, Vol. 42
2021, Vol. 42

