2. 中国环境科学研究院, 环境基准与风险评估国家重点实验室, 北京 100012;
3. 中国环境科学研究院, 国家环境保护地下水污染模拟与控制重点实验室, 北京 100012
2. State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;
3. State Environmental Protection Key Laboratory of Simulation and Control of Groundwater Pollution, Chinese Research Academy of Environmental Sciences, Beijing 100012, China
生活垃圾填埋场是一种非常重要的垃圾处理设施.垃圾在填埋过程中由于有机物的分解和雨水的浸淋作用, 将产生大量的垃圾渗滤液.垃圾渗滤液中含有溶解性有机物、无机盐、重金属及异质性有机物.当填埋场未铺设防渗膜或防渗膜破裂时, 渗滤液经包气带土壤进入含水层, 将造成地下水污染[1].有研究表明, 我国的河南[2]、贵州[3]、上海[4]等省市垃圾填埋场附近地下水均遭受不同程度污染.然而, 在受垃圾渗滤液污染的地下水中时有检出多环芳烃、全氟化合物、多氯联苯等疏水性强、溶解度低的有机污染物.近年来研究认为[5], 广泛存在于地下水中的溶解性有机质(DOM)含有多种疏水和亲水性官能团, 能够增强疏水性有机物的溶解度, 促进有机污染物的迁移.此外, 垃圾渗滤液或沉积物等多种来源的有机物进入地下环境后不仅能促进微生物代谢活动, 还能作为电子穿梭体促进地下矿物金属的释放, 并参与重金属元素的竞争吸附、络合和转化等过程[5, 6].因此, 研究地下水中DOM的来源、分布、组成等特征, 对阐明渗滤液在地下水的分布和转化过程, 具有非常重要意义.
目前针对地下水DOM来源及组成特征上, 国内外已有相关研究.Postma等[7]对重金属砷严重污染的孟加拉地下水研究显示, 该地区DOM主要来源于含水层中沉积物的释放, 其生物可利用性受沉积物发育时间密切相关.郭卉等[8]对我国太湖流域浅层地下水研究表明, 陆源和生物内源为地下水中DOM主要来源, 重金属Cu、Ni与小分子DOM络合紧密.Christensen等[9]对受污染地下水DOM组成研究发现, 类富里酸占总有机物的60%, 而亲水性组分和胡敏酸含量较少.于静等[10]对华北种植区受污染地下水研究发现, 新近污染的地下水DOM主要为小分子类蛋白, 其次为类富里酸物质.在研究渗滤液对地下水污染过程及受污染地下水组成特征上, 近年来基于现代光谱技术的化学法, 在地下水污染物源解析和预警上应用较为广泛.如Lapworth等[11]采用荧光技术分析了含水层中有机物来源和地下水流向.何小松等[1]的研究表明, 结合光谱技术与多元统计分析, 可识别受垃圾渗滤液污染地下水点位.鲁宗杰等[5]对通过三维荧光技术揭示了江汉平原地下水中DOM对砷迁移转化过程中的作用.
然而, 上述研究均未阐明不同填埋年限的填埋垃圾场地下水DOM组成差异, 并基于这种差异分析不同运行年限下渗滤液污染地下水特征和规律.基于此, 本研究采集了5个不同填埋年限垃圾场附近地下水样品, 在分析填埋场地下水常规理化指标及有机物来源、组成特征基础上, 阐明不同填埋年限垃圾场对地下水污染规律, 以期为填埋场地下水污染防控和预警提供依据.
1 材料与方法 1.1 采样点概况地下水样品采集于我国西南某市5座填埋场附近监测基井, 依据填埋场名称分别编号为HSZ, QJ、TL、YC及BS, 从填埋场启用日起分别运行了14、11、10、9及5 a, 设计处理规模分别为3000、200、220、400和350 t·d-1.
1.2 样品采集与分析于2017年11月对重庆市5座不同填埋年限的填埋场地下水进行布井采样分析, 其中BS、YC、TL、QJ和HSZ分别设置4、5、6、5及5个采样井, 共采集地下水样品25个.所采集样品放入加冰块的采样箱中, 于24 h内运回实验室.
水质参数pH使用pH计测定, 所有水体样品均过0.45 μm滤膜后再进行常规水质指标测定.硝酸盐氮、硫酸盐、氯化物均采用离子色谱测定(ICS-2000, Dionex USA).溶解性有机碳(DOC)采用总有机碳分析仪测定(multi N/C-2100 TOC, Analytik Jena GER).高锰酸盐指数采用高锰酸钾滴定法测定.
1.3 光谱分析紫外光谱测定采用日本岛津UV-1700型紫外分光光度计, 分析扫描波长范围设为190~700 nm, 扫面间距为1 nm.分别测定样品DOM在204、254和355 nm下的吸光度.计算样品在355 nm下的吸光系数a(355)[12].计算公式如下:

|
(1) |
式中, a(355)是355 nm处的吸收系数, m-1, A(355)为355 nm下的吸光度, l为光程路径, 0.01 m, 该值大小与DOM含量呈显著正相关.计算吸收系数比值E253/E203, 该值越大说明DOM苯环结构取代基上极性官能团含量高, 而该值越低, 显示非极性官能团含量高[13].对275~295 nm和350~400 nm处吸光度的自然对数拟合的直线斜率比值SR[14], 该值越小说明DOM分子量越大.254 nm处吸光度乘上100与DOC浓度之比计算SUVA, 该值越大表明DOM组分中芳香性越强, 苯环化合物含量越多[15].
荧光光谱测定采用日立公司生产的Hitachi F-7000型的荧光光谱检测器.激发光源为150 W氙弧灯, 光电倍增管电压为700 V, 信噪比>110.三维荧光光谱扫描在发射波长范围设为280~520 nm, 激发波长范围设为200~450 nm, 激发和发射光谱增量5 nm, 扫描速度为1200 nm·min-1, 以超纯水为空白, 将所有样品扣除空白后, 导出数据进行平行因子分析.
固定激发波长Ex为310 nm进行发射扫描波长Em为380 nm和430 nm两处荧光强度, 其比值记为BIX[16].代表陆源和微生物源的组分比例显著影响BIX值大小, 该值在0.8~1.0之间时对应为新形成的生物/微生物来源DOM.固定激发波长Ex为370 nm进行发射扫描波长Em为470 nm和520 nm两处荧光强度, 其比值计为FI, 该值小于等于1.4时说明DOM为陆源, 该值大于等于1.9时说明为微生物源[16].FI值与DOM芳香性成反比, 当FI值增加时其C/N比减少.扫描Ex为310 nm处发射光谱, 计算Em为380 nm处荧光强度与Em在420~435 nm处最强荧光强度, 其比值记为β:α, 其中β代表最近形成的DOM, 而α表示高度分解后的DOM, 因此该值越大代表所测DOM新鲜度越高[17].扫描Ex为254 nm处发射光谱, 计算发射光谱435~480 nm处峰面积与300~345 nm处峰面积, 其比值记为HIX, 该值越到大代表DOM样品腐殖化程度越高[18].DOM的腐殖化程度代表物质的形成年限及其稳定程度, 高度腐殖化的有机物较腐殖化程度低的有机物, 其一般在自然环境中存在年限较长且难以被降解.
1.4 多元数据分析对导出样品三维荧光光谱数据, 采用Barhram等[12]提出的方法扣除瑞利散射, 然后在Matlab 7.0b (Mathworks, Natick, MA)上采用DOMFluor toolbox软件包进行平行因子分析(PARAFAC).根据该一致性分析和对半检测确定荧光组分, 以及每个样品在对应组分的相对浓度得分值Fmax.基于PARAFAC组分, 计算所有类腐殖酸DOM组分Fmax和与所有类蛋白DOM组分Fmax和, 其比值记为hum:pro.计算所有陆源DOM组分Fmax之和与所有生物源DOM组分Fmax之和, 其比值记为terr:micro.
水质理化指标及光谱参数的主成分分析和相关性分析在SPSS 17.0上进行, 绘图在Origin 9.0上进行.
2 结果与讨论 2.1 地下水基本理化特征及光学性质填埋场地下水pH值在7.22~8.64之间, 整体偏碱性(表 1), 其与不同填埋年限垃圾所处发酵阶段及防渗措施存在较大关系[19].地下水高锰酸盐指数在0.72~7.75 mg·L-1, 其中两个点位超出地下水质量标准Ⅲ类(GB 14848-1993) 1.1倍、2.6倍.Cl-、SO42-及NO3--N含量分别在1.87~126、13.3~69.1和0~13.4 mg·L-1, 均未超出下水质量标准Ⅲ类.所有样品重金属铅、镉、铬、汞、砷均未检出(数据未列出).相对其它填埋场地下水, TL地下水pH值较高, 其高锰酸盐指数、Cl-及SO42-含量也呈现类似特征, 显示该填埋场地下水受渗滤液污染程度较深.在天然条件下地下水中Cl-含量较低, 通过对比不同填埋年限填埋场地下水可发现, 随着填埋年限增加Cl-呈增高趋势, 而SO42-含量并未呈现以上规律.上述结果可能与不同填埋场垃圾差异性大, 且生活垃圾中氯化钠含量较硫酸盐含量高有关.
|
|
表 1 地下水物化性质及光学参数 Table 1 Summary of groundwater sample physico-chemical properties and optical parameters |
地下水中溶解性有机碳主要包括有色和无色有机质, 两者组成受人为活动、水文地质条件及微生物活性影响最为显著[20].垃圾填埋过程中有机物经过腐殖化过程形成了大量的有色溶解性有机质, 采用光学手段示踪此类有机质变化可有效监测填埋场地下水水质状况.由表 1可知, 本研究填埋场地下水DOC含量除BS均值相对较高[(5.35±2.49)mg·L-1]外, 其它填埋场含量差异并不显著(P>0.05), 而代表有色溶解性有机质相对浓度的指标a(355)值间呈显著差异(P < 0.05), 含量大小为YC>TL>HSZ>BS>QJ, 因此需进一步分析填埋场地下水中DOM组成和分子结构差异.根据单位浓度DOM在254 nm下吸光度值SUVA可知[21], YC和QJ地下水中DOM的芳香化合物含量高, 分别位于2.08~4.19 L·(mg·m)-1和1.22~6.01 L·(mg·m)-1, 而TL、HSZ及BS地下水中DOM芳香化合物相对较低.通过有机物分子量指标SR可知[14], QJ和TL地下水DOM的分子量最大, 两者SR值位于0.17~0.58、0.28~0.74, 中位数为0.32、0.38, 均值依次为0.17、0.28.根据指示水体DOM亲疏水特性的吸光度比值E253/E203可知[22], YC和QJ地下水中DOM中羰基、羧基等极性基团含量较高, 两者E253/E203比值分别位于0.275~0.420、0.023~0.071之间, 中位数为0.408、0.029, 均值依次为0.398、0.036.综上可知, 该地区填埋场地下水虽然溶解性有机碳含量差异不明显, 但各填埋场地下水DOM组成存在显著特征.填埋场TL、HSZ及BS地下水中DOM分子量和极性官能团含量相对较低, 易被土壤吸附和阻截; 而填埋场YC和QJ地下水中DOM分子量和亲水性官能团含量高, 有利于污染物迁移和下沉, 易导致地下水质恶化.
2.2 地下水有机物种类来源、组成及分布特征荧光强度比值被广泛应用于评估陆源与微生物源对DOM的相对贡献.已有研究指出, FI值越高代表DOM结构越简单(主要为微生物源的类富里酸、类蛋白), 而FI值越低说明DOM含有越多大分子芳香组分.此外, BIX值常用于评估水体DOM自生源指标, 其值在0.6以下表明自生源贡献较少, 大于0.8代表为新生成的微生物来源有机质[18].图 1显示, 填埋场地下水中DOM的FI值绝大部分均高于1.8(均值2.10), BIX值均高于0.6.表明填埋场地下水有机物除自生陆源产生以外, 由微生物活动所贡献比重较大.进入地下水中的有机物会在地层中发生腐殖化过程, HIX与有机物的腐殖化程度密切相关.HIX值越大, 有机物腐殖化程度越高[18].图 1显示, 地下水中DOM新生度(β:α值)较高的样品, 其DOM腐殖化程度低.而填埋年限较长的垃圾场(HSZ、QJ)附近地下水DOM腐殖化程度较高, 不同采样点间地下水DOM性质较稳定差异小.填埋年限相对低的填埋场(YC、BS)地下水DOM主要为一些新生成腐殖化程度较低的组分, 不同点位差异性大.以上结果表明, 填埋场地下水中新生成的微生物来源有机物结构简单, 腐殖化程度低, 填埋年限较短的垃圾场微生物活性高, 易造成填埋场附近地下水污染.
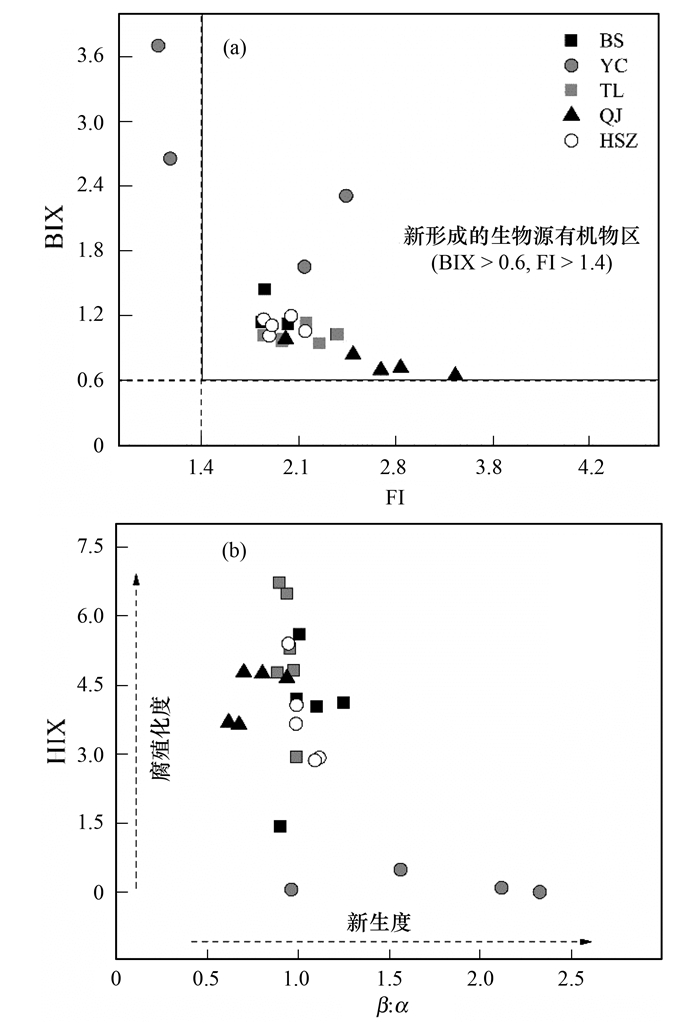
|
图 1 地下水有机物荧光参数间关系 Fig. 1 Relationship between fluorescence parameters of organic matter in groundwater samples |
对填埋场地下水样品三维荧光光谱进行平行因子分析, 可鉴定出6个荧光组分(图 2).根据已有研究显示, 组分C1~C4为类腐殖酸, 其中C1、C2和C4为陆源有机物, 而C3为生物源有机物.组分C5、C6为类蛋白物质, 由类酪氨酸、类色氨酸及结合与蛋白的氨基酸构成(表 2).Hur等[23]的研究指出, 分子结构存在聚合、缩合及大分子量的胡敏酸类有机质荧光发射波长在长波段处.因此, 本研究鉴定出来的6个组分中, 陆源组分C4和C2定义为难降解高度聚合的大分子类胡敏酸, 而类蛋白组分C5和C6为聚合程度少、易降解的荧光发色团.
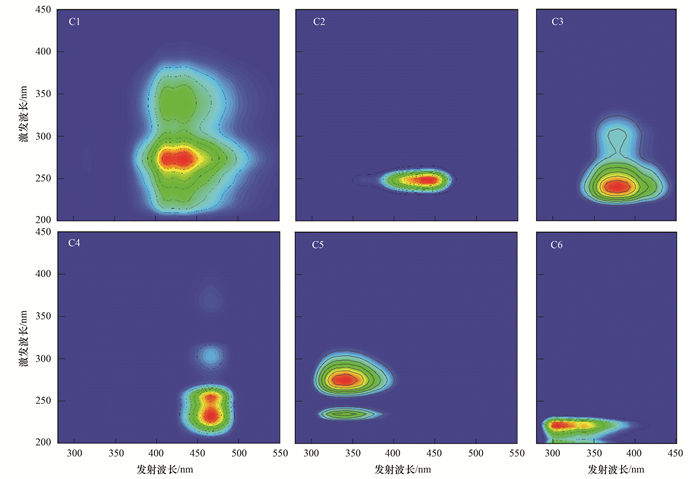
|
图 2 地下水DOM经平行因子分析法鉴定出得6个组分 Fig. 2 Six components of groundwater samples DOM identified by parallel factor analysis |
|
|
表 2 本研究平行因子鉴定组分及前人类似研究描述 Table 2 Description of PARAFAC components from this study and comparison with similar components in other studies |
由表 3可知, 大分子胡敏酸C4和C2的相对含量在填埋年限较长(TL、HSZ)的地下水DOM最高, 而在填埋时间相对较短的填埋场(YC、BS)地下水中易降解的类蛋白组分C5和C6为主要有机物质, 中等分子量的C1和C3组分在TL和QJ最高.通过分析不同荧光组分比例可发现, 中等相对分子量的C1和C3组分在不同填埋年限的地下水DOM其占总荧光有机质比例变化不大.以上现象与以往研究结果类似, He等[32]发现同一填埋场附近不同时期地下水中类富里酸和类胡敏酸含量(对应本研究组分C3和C1)变化不大.由表 3可知, 填埋场地下水中陆源和微生物源有机质比(terr:micro)随着填埋年限的增加, 呈先增加后减少的规律, 同时类腐殖质和类蛋白比(hum:pro)也呈现同样趋势.已有研究指出[33], 类色氨酸等类蛋白物质在被生物利用降解后产生其它类腐殖酸组分(对应本研究组分C3).综上可知, 垃圾填埋初期形成大量的易分解的类蛋白物质进入地下水后, 极易被微生物利用, 促进了微生物的活性, 增加了地下水中生物来源的有机质.随着填埋时间的增长, 有机质腐殖化率增高, 微生物可利用物质减少, 难降解的大分子物质逐渐累积, 微生物活性减弱, 填埋场趋向稳定对地下水影响减少.
|
|
表 3 地下水中不同组分相对浓度得分及比例 Table 3 Relative concentrations and proportions for six components in groundwater samples |
2.3 地下水有机物分子结构及动力学特征
为进一步揭示地下水DOM种类分子结构及其动力学特征, 将已鉴定出的6种荧光组分和4种光谱参数进行主成分分析, 基于变量载荷的聚类分析及不同样品因子得分, 可提取全部变量的潜在解释因子[34].经Kaiser-Meryer-Oklin(KMO值为0.8)和Bartlett的球形度检验(P < 0.001)后, 基于特征值大于1可提取3个主成分, 可解释全部变量的81.4%, 其中前两个成分(PC1、PC2)能解释全部变量的71.1%信息.根据各组分及光谱参数在PC1、PC2上的得分值绘制图 3(a), 可知各参数之间的关系及其对PC1、PC2的贡献程度; 根据不同样品降维后在PC1、PC2上的得分值绘制图 3(b), 可明确各点位样品在PC1、PC2上的特征.
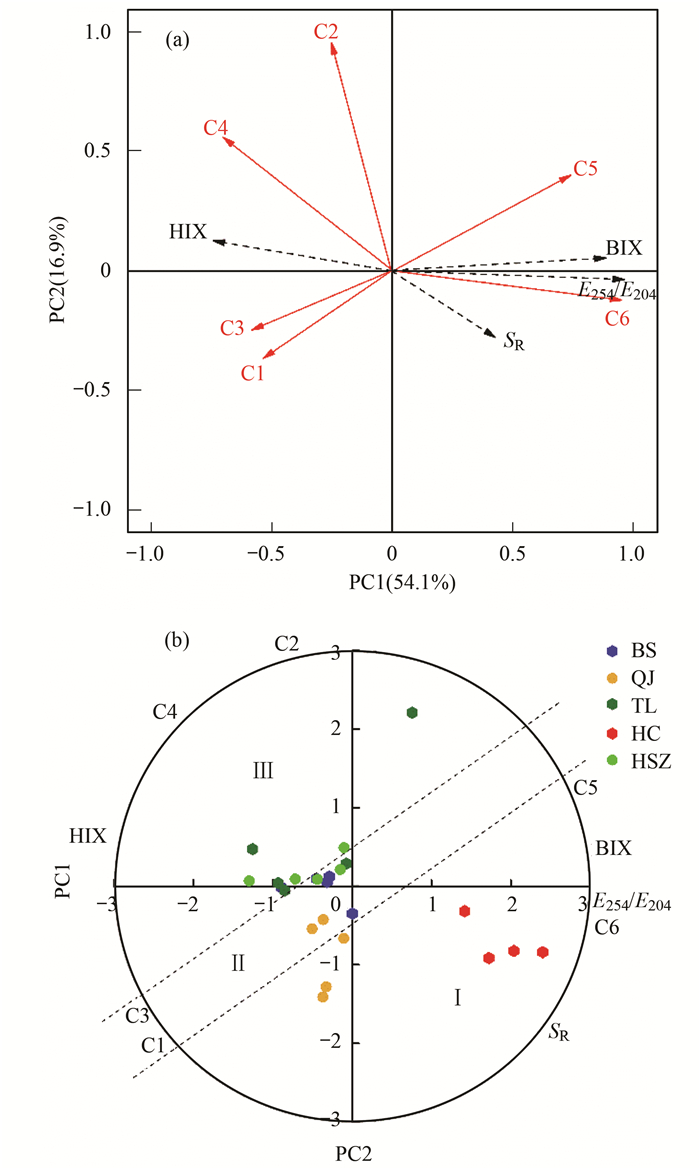
|
图 3 平行因子组分及光学参数主成分分析 Fig. 3 Principal component analysis of PARAFAC components and DOM indices from all water samples |
如图 3所示, 与PC1呈显著正载荷的为小分子类蛋白组分C5、C6、生物源指标BIX, 分子量SR及亲疏水性指标E253/E203, 而与PC2呈显著正载荷的为大分子类胡敏酸C2、C4及腐殖化率指标HIX.相比而言, 类胡敏酸/类富里酸组分C1、C3对PC2贡献较小的载荷, 而对PC1贡献中等载荷.因此, 可以对以上参数分为3类, 基于对角平行线可分为:BIX、SR、C5、C6和HIX、C2、C4, 其分别指示为低分子量生物源类蛋白(Ⅰ区)和大分子类胡敏酸有机物(Ⅲ区).在中间包括组分C1和C3的区域(Ⅱ区), 代表相对稳定的过渡性类胡敏酸物质/类富里酸.根据不同填埋场地下水样品在主成分因子得分中的分布位置[图 3(b)], 可体现不同地下水DOM来源、矿化及成岩等性质[33].沿着[图 3(b)]中平行线垂直方向可看出, 随着填埋年限的增加地下水样点逐渐从Ⅰ区转化为Ⅱ、Ⅲ区.在中间的Ⅱ区的地下水样品DOM的腐殖化率及其苯环上的极性官能团比Ⅲ区少, 显著强于Ⅰ区图 3(a), 处于Ⅱ区的地下水DOM可能为低分子量生物源有机物与大分子类胡敏酸有机物的混合物或中间产物.在实际地下水环境中, 小分子类蛋白因其具有较高的亲水性, 易随水迁移并被微生物利用[35].大分子类腐殖酸因其具备较高的腐殖化率、芳香性及疏水性, 容易被土壤吸附、包裹或发生一定的成岩作用进而较稳定[36].因此, 填埋时间相对较长的填埋场地下水DOM样品绝大部分分布在Ⅱ区, 并逐渐向Ⅲ区过渡.
地下水是个复杂的体系, 其有机物的组成和转化特征可能对无机盐组成和地下水其他理化性质具有重要影响.本研究中地下水三氮中硝态氮含量最高, 氨氮和亚硝态氮只有部分点位有检出, 且浓度较低(数据未列出).在自然条件下氨氮易被土壤黏土团粒吸附、固化, 在土壤厌氧条件下通过微生物的硝化作用转化为稳定的硝态氮进入地下水[8], 因此硝态氮在地下水中通常累积过多.对地下水中不同理化指标进行相关分析显示(表 4), 地下水中硝态氮、硫酸根离子及氯离子浓度两两间呈显著相关(P < 0.05)或极显著相关(P < 0.01), 表明这3种阴离子具有类似的迁移特性.当填埋场渗滤液中的有机物进入地下环境后, 在厌氧微生物作用下被转化为蛋白类、小分子酸及离子.表 4显示, terr:micro比值均与高锰酸盐指数、硝态氮、氯离子呈现极显著相关, 同时这些理化指标均与大分子C4、C2组分呈显著或极显著正相关, 而与小分子类蛋白C6均呈不同程度负相关.以上结果显示, 进入地下水中的有机物存在强烈的微生物转化过程, 其中易降解的类蛋白物质被逐渐消耗, 大分子相对稳定的陆源胡敏酸发生累积, 该过程与异养微生物的硝化反应密切相关.
|
|
表 4 地下水理化性质与荧光组分间相关性分析1) (n=25) Table 4 Correlation matrix between groundwater physico-chemical properties with fluorescent components (n=25) |
3 结论
采用光谱技术与多元数据分析手段, 可有效揭示常规水质检测手段难以识别的微污染填埋场地下水有机物组成、分布、结构及演化特征.填埋场地下水有机物主要为微生物来源, 在填埋前期阶段(小于10 a)其微生物来源较多, 而在填埋后期(大于10 a)微生物来源减弱.填埋年限较短的填埋场地下水DOM主要为一些新生成腐殖化程度较低的易降解类色氨酸和类酪氨酸, 促进微生物活性, 且各点位差异性较大, 应提高预警措施.填埋时间相对较长的填埋场地下水有机质腐殖化率高, 难降解的大分子物质累积, 微生物活性减弱, 填埋垃圾趋向稳定进而对地下水影响减少.
| [1] |
何小松, 余红, 席北斗, 等. 填埋垃圾浸提液与地下水污染物组成差异及成因[J]. 环境科学, 2014, 35(4): 1399-1406. He X S, Yu H, Xi B D, et al. Difference of contaminant composition between landfill leachates and groundwater and its reasons[J]. Environmental Science, 2014, 35(4): 1399-1406. |
| [2] |
仝晓霞, 宁立波, 董少刚, 等. 运行GMS模型对某垃圾场地下水污染的研究[J]. 环境科学与技术, 2012, 35(7): 197-201. Tong X X, Ning L B, Dong S G. GMS model for assessment and prediction of groundwater pollution of a garbage dumpling site in Luoyang[J]. Environmental Science & Technology, 2012, 35(7): 197-201. DOI:10.3969/j.issn.1003-6504.2012.07.042 |
| [3] |
杨元丽, 杨涛毅, 于晓红, 等. 贵州岩溶地区简易垃圾填埋场对地下水的污染研究[J]. 地下水, 2013, 35(3): 77-80. Yang Y L, Yang T Y, Yu X H, et al. Research on groundwater pollution caused by landfills in karst region in guizhou[J]. Underground Water, 2013, 35(3): 77-80. DOI:10.3969/j.issn.1004-1184.2013.03.027 |
| [4] |
田扬捷, 黄仁华, 杨虹, 等. 海滨地区垃圾填埋场渗沥液对地下水系统的污染[J]. 环境卫生工程, 2005, 13(1): 1-5. Tian Y J, Huang R H, Yang H, et al. Pollution on groundwater systems by the leachate from a seashore waste landfill site[J]. Environmental Sanitation Engineering, 2005, 13(1): 1-5. DOI:10.3969/j.issn.1005-8206.2005.01.001 |
| [5] |
鲁宗杰, 邓娅敏, 杜尧, 等. 江汉平原高砷地下水中DOM三维荧光特征及其指示意义[J]. 地球科学, 2017, 42(5): 771-782. Lu Z J, Deng Y M, Du Y, et al. EEMs characteristics of dissolved organic matter and their implication in high arsenic groundwater of Jianghan Plain[J]. Earth Science, 2017, 42(5): 771-782. |
| [6] | Wang S L, Mulligan C N. Effect of natural organic matter on arsenic release from soils and sediments into groundwater[J]. Environmental Geochemistry and Health, 2006, 28(3): 197-214. DOI:10.1007/s10653-005-9032-y |
| [7] | Postma D, Larsen F, Thai N T, et al. Groundwater arsenic concentrations in Vietnam controlled by sediment age[J]. Nature Geoscience, 2012, 5(9): 656-661. DOI:10.1038/ngeo1540 |
| [8] |
郭卉, 虞敏达, 何小松, 等. 南方典型农田区浅层地下水污染特征[J]. 环境科学, 2016, 37(12): 4680-4689. Guo H, Yu M D, He X S, et al. Pollution characteristics analysis in shallow groundwater of typical farmland area, southern China[J]. Environmental Science, 2016, 37(12): 4680-4689. |
| [9] | Christensen J B, Jensen D L, Grøn C, et al. Characterization of the dissolved organic carbon in landfill leachate-polluted groundwater[J]. Water Research, 1998, 32(1): 125-135. DOI:10.1016/S0043-1354(97)00202-9 |
| [10] |
于静, 虞敏达, 蓝艳, 等. 北方典型设施蔬菜种植区地下水水质特征[J]. 环境科学, 2017, 38(9): 3696-3704. Yu J, Yu M D, Lan Y, et al. Analysis of the characteristics of groundwater quality in a typical vegetable field, northern China[J]. Environmental Science, 2017, 38(9): 3696-3704. |
| [11] | Lapworth D J, Gooddy D C, Butcher A S, et al. Tracing groundwater flow and sources of organic carbon in sandstone aquifers using fluorescence properties of dissolved organic matter (DOM)[J]. Applied Geochemistry, 2008, 23(12): 3384-3390. DOI:10.1016/j.apgeochem.2008.07.011 |
| [12] | Bahram M, Bro R, Stedmon C, et al. Handling of Rayleigh and Raman scatter for PARAFAC modeling of fluorescence data using interpolation[J]. Journal of Chemometrics, 2006, 20(3-4): 99-105. DOI:10.1002/(ISSN)1099-128X |
| [13] | He X S, Xi B D, Wei Z M, et al. Spectroscopic characterization of water extractable organic matter during composting of municipal solid waste[J]. Chemosphere, 2011, 82(4): 541-548. DOI:10.1016/j.chemosphere.2010.10.057 |
| [14] | Helms J R, Stubbins A, Ritchie J D, et al. Absorption spectral slopes and slope ratios as indicators of molecular weight, source, and photobleaching of chromophoric dissolved organic matter[J]. Limnology and Oceanography, 2008, 53(3): 955-969. DOI:10.4319/lo.2008.53.3.0955 |
| [15] | Weishaar J L, Aiken G R, Bergamaschi B A, et al. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J]. Environmental Science & Technology, 2003, 37(20): 4702-4708. |
| [16] | McKnight D M, Boyer E W, Westerhoff P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity[J]. Limnology and Oceanography, 2001, 46(1): 38-48. DOI:10.4319/lo.2001.46.1.0038 |
| [17] | Wilson H F, Xenopoulos M A. Effects of agricultural land use on the composition of fluvial dissolved organic matter[J]. Nature Geoscience, 2009, 2(1): 37-41. DOI:10.1038/ngeo391 |
| [18] | Huguet A, Vacher L, Relexans S, et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary[J]. Organic Geochemistry, 2009, 40(6): 706-719. DOI:10.1016/j.orggeochem.2009.03.002 |
| [19] | Luo Z Y, Zhao Y C, Yuan T, et al. Natural attenuation and characterization of contaminants composition in landfill leachate under different disposing ages[J]. Science of the Total Environment, 2009, 407(10): 3385-3391. DOI:10.1016/j.scitotenv.2009.01.028 |
| [20] | Rochelle-Newall E J, Fisher T R. Chromophoric dissolved organic matter and dissolved organic carbon in Chesapeake Bay[J]. Marine Chemistry, 2002, 77(1): 23-41. DOI:10.1016/S0304-4203(01)00073-1 |
| [21] |
邵田田, 赵莹, 宋开山, 等. 辽河下游CDOM吸收与荧光特性的季节变化研究[J]. 环境科学, 2014, 35(10): 3755-3763. Shao T T, Zhao Y, Song K S, et al. Seasonal variation in the absorption and fluorescence characteristics of CDOM in downstream of Liaohe river[J]. Environmental Science, 2014, 35(10): 3755-3763. |
| [22] | Fellman J B, Hood E, Spencer R G M. Fluorescence spectroscopy opens new windows into dissolved organic matter dynamics in freshwater ecosystems:a review[J]. Limnology and Oceanography, 2010, 55(6): 2452-2462. DOI:10.4319/lo.2010.55.6.2452 |
| [23] | Hur J, Kim G. Comparison of the heterogeneity within bulk sediment humic substances from a stream and reservoir via selected operational descriptors[J]. Chemosphere, 2009, 75(4): 483-490. DOI:10.1016/j.chemosphere.2008.12.056 |
| [24] | Yamashita Y, Jaffé R, Maie N, et al. Assessing the dynamics of dissolved organic matter (DOM) in coastal environments by excitation emission matrix fluorescence and parallel factor analysis (EEM-PARAFAC)[J]. Limnology and Oceanography, 2008, 53(5): 1900-1908. DOI:10.4319/lo.2008.53.5.1900 |
| [25] | Stedmon C A, Markager S. Resolving the variability in dissolved organic matter fluorescence in a temperate estuary and its catchment using PARAFAC analysis[J]. Limnology and Oceanography, 2005, 50(2): 686-697. DOI:10.4319/lo.2005.50.2.0686 |
| [26] | Hua B, Dolan F, Mcghee C, et al. Water-source characterization and classification with fluorescence EEM spectroscopy:PARAFAC analysis[J]. International Journal of Environmental Analytical Chemistry, 2007, 87(2): 135-147. DOI:10.1080/03067310600922154 |
| [27] | Kulkarni H V, Mladenov N, Johannesson K H, et al. Contrasting dissolved organic matter quality in groundwater in Holocene and Pleistocene aquifers and implications for influencing arsenic mobility[J]. Applied Geochemistry, 2016, 77: 194-205. |
| [28] | Lu F, Chang C H, Lee D J, et al. Dissolved organic matter with multi-peak fluorophores in landfill leachate[J]. Chemosphere, 2009, 74(4): 575-582. DOI:10.1016/j.chemosphere.2008.09.060 |
| [29] | Zhang Y L, Yin Y, Feng L Q, et al. Characterizing chromophoric dissolved organic matter in Lake Tianmuhu and its catchment basin using excitation-emission matrix fluorescence and parallel factor analysis[J]. Water Research, 2011, 45(16): 5110-5122. DOI:10.1016/j.watres.2011.07.014 |
| [30] | Coble P G. Characterization of marine and terrestrial DOM in seawater using excitation-emission matrix spectroscopy[J]. Marine Chemistry, 1996, 51(4): 325-346. DOI:10.1016/0304-4203(95)00062-3 |
| [31] | He X S, Xi B D, Cui D Y, et al. Influence of chemical and structural evolution of dissolved organic matter on electron transfer capacity during composting[J]. Journal of Hazardous Materials, 2014, 268: 256-263. DOI:10.1016/j.jhazmat.2014.01.030 |
| [32] | He X S, Xi B D, Gao R T, et al. Using fluorescence spectroscopy coupled with chemometric analysis to investigate the origin, composition, and dynamics of dissolved organic matter in leachate-polluted groundwater[J]. Environmental Science and Pollution Research, 2015, 22(11): 8499-8506. DOI:10.1007/s11356-014-4029-7 |
| [33] | Chen M L, Price R M, Yamashita Y, et al. Comparative study of dissolved organic matter from groundwater and surface water in the Florida coastal Everglades using multi-dimensional spectrofluorometry combined with multivariate statistics[J]. Applied Geochemistry, 2010, 25(6): 872-880. DOI:10.1016/j.apgeochem.2010.03.005 |
| [34] | Dos Santos L M, Simões M L, De Melo W J, et al. Application of chemometric methods in the evaluation of chemical and spectroscopic data on organic matter from Oxisols in sewage sludge applications[J]. Geoderma, 2010, 155(1-2): 121-127. DOI:10.1016/j.geoderma.2009.12.006 |
| [35] | Reemtsma T, Bredow A, Gehring M. The nature and kinetics of organic matter release from soil by salt solutions[J]. European Journal of Soil Science, 1999, 50(1): 53-64. |
| [36] | Huang S B, Wang Y X, Ma T, et al. Linking groundwater dissolved organic matter to sedimentary organic matter from a fluvio-lacustrine aquifer at Jianghan Plain, China by EEM-PARAFAC and hydrochemical analyses[J]. Science of the Total Environment, 2015, 529: 131-139. DOI:10.1016/j.scitotenv.2015.05.051 |
 2018, Vol. 39
2018, Vol. 39


