2. 青岛地质工程勘察院(青岛地质勘查开发局), 青岛 266101
2. Qingdao Geo-Engineering Surveying Institute (Qingdao Geological Exploration Development Bureau), Qingdao 266101, China
塑料和塑料制品已被广泛应用于工业领域和人类的日常生活中, 惊人数量的塑料废弃物被释放到陆地、淡水和海洋环境中.进入环境的塑料在风化和降解等外界作用下逐步破碎化而形成一类新兴污染物——微塑料[1, 2].微塑料通常指直径小于5 mm的塑料微粒, 已成为日益受到关注的全球性环境问题[3, 4].目前, 微塑料已经在世界各地的水体、土壤、沉积物和生物体等基质中被检测到[5, 6], 其中土壤中微塑料的丰度约为海洋的4 ~ 23倍[7], 是微塑料重要的汇集地[8].对中国5个省份6种不同土地利用类型土壤微塑料调查发现, 微塑料广泛存在, 含量范围为2 783 ~ 6 366 items·kg-1[9].微塑料主要通过施肥、地膜破损、污水灌溉、垃圾填埋、大气沉降及地表径流等方式进入土壤[10 ~ 12].进入土壤的微塑料会对土壤理化性质、土壤功能及生物多样性产生显著影响[13], 还可与重金属、抗生素和有机氯农药等污染物结合产生复合污染效应[14, 15], 最终对人体健康和生态系统造成潜在威胁.
微塑料与各种污染物的相互作用是一个复杂的过程, 受微塑料、污染物及土壤理化性质的影响.微塑料的粒径大小、比表面积及表面特征对污染物的吸附性能起着关键的作用[16, 17].Zhou等[18]研究表明聚酰胺(PA)表面官能团(如C—O和N—H)的存在会优先与金属离子相互作用, 使得PA对Cd2+的吸附能力更强;同种微塑料对不同重金属的吸附能力也存在较大差异, Wang等[19]研究发现聚对苯二甲酸乙二醇酯(PET)对Cu和Zn的最大吸附量分别为40.3 μg·g-1和24.7 μg·g-1.另外, 微塑料可以改变土壤对污染物的吸附能力.Hüffer等[20]研究表明PE微塑料通过竞争、阻挡和稀释等作用降低了土壤对疏水性有机污染物的吸附能力而促进有机污染物的迁移;而赵雪君等[21]研究发现PA和聚甲基丙烯酸甲酯(PMMA)增强了土壤对农药异菌脲的吸附能力, 抑制了异脲在土壤中的迁移, 且使其不易被降解, 从而加剧表层土壤的污染.微塑料还可以通过改变土壤的理化性质, 进而影响到土壤中物质的迁移转化.Wen等[22]研究发现微塑料显著改变了黄棕壤的化学性质(pH、OM和CEC), 进而改变了土壤中重金属的化学形态;Yu等[23]研究表明微塑料可能通过物理吸附或者共沉淀来降低团聚体中重金属的含量, 或通过改变土壤的理化性质来影响不同重金属形态的迁移转化, 从而降低重金属的生物利用度.
长期以来重金属被认为是一种典型的土壤污染物, 受到世界各国的普遍关注.我国耕地土壤重金属点位超标率达19.4%[24], 其中Cd的点位超标率为7%, 已被确定为我国土壤的首要污染物.微塑料的存在会改变重金属在土壤中的迁移、转化及归趋, 进而影响其生态毒性.目前, 更多的研究集中在水环境中重金属在各类型微塑料上的吸附能力和机制, 尚缺乏微塑料与重金属复合污染土壤中重金属迁移特征的研究.因此, 本文选取CaCl2、NaCl为淋洗溶液, 通过土柱淋溶实验研究不同离子强度和类型下, 聚乙烯(PE)微塑料含量、粒径对土壤中Cd吸附迁移行为的影响, 以期为土壤中微塑料与重金属复合污染风险评价和防治提供理论依据.
1 材料与方法 1.1 供试材料聚乙烯(PE)是日常生活及农业生产中最常见的塑料之一, 购自东莞市樟木头华创塑胶原料商行, 选取3种不同粒径:50 μm、500 μm和1 mm.将PE微塑料置于5%的硝酸中浸泡24 h, 去除表面杂质, 然后用去离子水洗至中性后低温烘干备用.采用扫描电镜(SEM)和傅里叶红外光谱仪(FTIR)对微塑料的微观形貌和表面基团进行分析.本实验所用土壤采集于青岛市即墨蓝村镇(120°17'E, 36°42'N), 土壤类型为棕壤.采集0 ~ 20 cm表层土壤, 去除植物的根、砂石及其他杂物, 风干、碾细, 过10目筛, 备用.土壤基本理化性质如表 1所示.采用纳米粒度Zeta电位测定仪测定微塑料及土壤混合样品的Zeta电位.
|
|
表 1 供试土壤基本理化性质 Table 1 Physical and chemical properties of the tested soil |
1.2 污染土壤的制备
参考我国《土壤环境质量农用地土壤污染风险管控标准(试行)》(GB 15618-2018)及山东省农田实际污染状况[25], 设定土壤Cd污染水平为20 mg·kg-1.将浓度为500 mg·L-1的Cd(NO3)2溶液均匀地喷洒在土壤表面, 经充分混合后静置24 h.然后通过分批均匀铺洒混合的方式向土壤中添加微塑料, 为探究极限微塑料添加水平下对土壤中重金属迁移的影响, 设置添加比例分别为0%、1%、4%、7%和20%(以微塑料/土壤干重计), 依次编号为CK、T1、T2、T3和T4.最后, 将Cd与PE复合污染的土样置于温室中老化培养, 14 d后进行土柱淋溶实验.
1.3 PE微塑料对Cd的吸附实验 1.3.1 吸附动力学实验分别取0.04 g不同粒径的PE微塑料放入离心管中, 然后加入40 mL pH值为6.0, 浓度为6 mg·L-1的Cd(NO3)2溶液, 于25 ℃、转速为160 r·min-1条件下振荡0.25、0.5、1、2、5、8、10、12、24和48 h.取上清液, 过0.45 μm滤膜, 采用电感耦合等离子体发射光谱仪(ICP-OES)测定滤液中Cd2+浓度.每个处理设3个重复.微塑料对Cd2+的吸附量(Qt)由以下方程式计算:
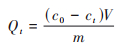
|
(1) |
式中, Qt为PE微塑料对重金属的吸附量(mg·g-1);c0为重金属的初始浓度(mg·L-1);ct为t时刻溶液中重金属离子的浓度(mg·L-1);V为加入重金属溶液的体积(L);m为加入微塑料的质量(g).
选用准一级动力学、准二级动力学和颗粒内扩散模型(Webber-Morris)对实验数据进行拟合, 表达式如下.
准一级动力学模型:
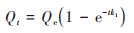
|
(2) |
准二级动力学模型:
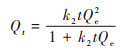
|
(3) |
Webber-Morris模型:
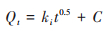
|
(4) |
式中, Qe为吸附平衡时微塑料的吸附量(mg·g-1);k1为准一级动力学反应速率常数(h-1);k2为准二级动力学吸附反应速率常数[g·(mg·h)-1];ki为颗粒内扩散模型的速率常数[mg·(g ·h1/2)-1];C为与边界层厚度有关的常数.
1.3.2 等温吸附实验配制浓度为2、4、6、8、10和15 mg·L-1的Cd(NO3)2溶液, 调节pH值为6.0, 分别将0.04 g不同粒径的微塑料添加到40 mL浓度为2 ~ 15 mg·L-1的Cd溶液中, 在25℃、转速为160 r·min-1条件下振荡48 h, 将上清液经0.45 μm的滤膜过滤后测定Cd2+浓度, 每个处理设置3个重复.
选用Langmuir和Freundlich方程来描述微塑料对重金属的等温吸附, 表达式分别如下.
Langmuir等温模型:
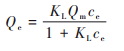
|
(5) |
Freundlich等温模型:
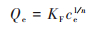
|
(6) |
式中, Qm为微塑料对重金属离子的最大吸附量(mg·g-1);KL为与吸附相关的常数(L·mg-1);ce为溶液中重金属离子的平衡浓度(mg·L-1);KF为Freundlich吸附系数(mg1–n·Ln·g-1);1/n为吸附强度.
1.4 土柱淋溶实验根据实测土壤容重1.30 g·cm-3填装土柱(容器为有机玻璃, 高度20 cm, 内径5 cm).将培养后的污染土壤分4次填装到土柱中, 以保证土壤颗粒均匀分布;不同微塑料处理的土柱中, 土壤质量相同.在土柱两端各铺一层石英砂, 以保证供液时溶液能均匀地入渗到土壤中, 避免土壤颗粒堵塞取样口.用蠕动泵作为供水装置自下而上通入去离子水对土柱进行饱和(排出柱内空气), 待饱和后调换入流方向.水流稳定后(1 mL·min-1), 通入CaCl2/NaCl溶液进行淋溶, 6 h后改用去离子水淋洗至无Cd2+流出.用自动部分收集器对流出液连续取样, 测定pH及Cd2+浓度.具体实验设置见表 2.
|
|
表 2 实验设置1) Table 2 Experimental conditions |
2 结果与讨论 2.1 PE微塑料对Cd的吸附特性 2.1.1 样品的表征
图 1(a) ~ 1(c)分别为50 μm、500 μm及1 mm的PE微塑料扫描电镜(SEM)结果, 可以观察到粒径为50 μm的PE微塑料颗粒表面比较光滑平整且存在大量的孔隙结构;粒径为500 μm和1 mm的微塑料呈不规则几何形, 表面较粗糙且有明显的褶皱和凸起.EDS分析发现[图 1(d)], 吸附Cd后的PE微塑料表面检测到Cd的存在, 且分布均匀, 说明微塑料表面对Cd2+的吸附点位较为均一, 以单层吸附为主.由于微塑料表面含氧官能团的脱质子化作用[26], 不同溶液化学条件下微塑料表面带有负电荷(-2.16 ~ -6.25 mV), 但数量较少, 少量Cd2+可通过静电吸引被微塑料吸附.

|
图 1 PE微塑料的SEM扫描图及EDS能谱图 Fig. 1 SEM scanning and EDS spectra of PE microplastics |
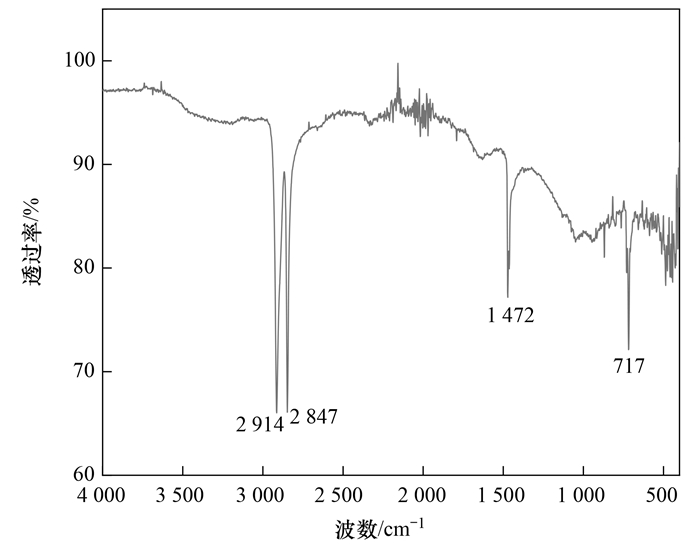
如图 2所示, PE微塑料的特征峰可以表述在2 914 cm-1 处—CH2不对称伸缩振动、2 847 cm-1处—CH2对称伸缩振动、1 472 cm-1处—CH2弯曲振动和721 ~ 717 cm-1处—CH2面内摇摆振动[27].这些官能团对Cd无显著吸附作用[28], 故物理作用在吸附过程中占主导地位.
|
图 2 PE微塑料的FTIR谱图 Fig. 2 FTIR spectra of PE microplastics |
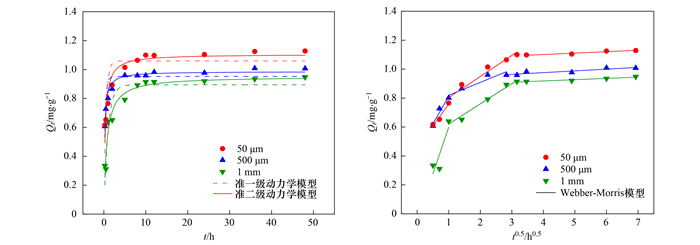
如图 3所示, PE对Cd2+的吸附过程主要分为3个阶段:第一阶段为快速吸附阶段(0 ~ 1 h), 由于吸附开始时微塑料表面吸附点位充足, Cd2+吸附速率较快, 约67%的Cd2+被吸附;第二阶段为慢速吸附阶段(1 ~ 10 h), 随着吸附反应的进行, 微塑料上的吸附点位逐渐被占满, 微塑料与溶液中Cd2+的浓度差降低, Cd2+进入微塑料表面的褶皱微孔, 吸附量增长变缓;第三阶段为平衡吸附阶段(10 ~ 48 h), 此时吸附逐渐达到平衡, 吸附量变化很小.3种粒径中50 μm微塑料因其比表面积最大, 提供的点位较多, 所以吸附容量最大.采用准一级动力学模型和准二级动力学模型对Cd2+的吸附过程进行拟合, 结果如表 3所示.准二级动力学模型的R2值(0.921 ~ 0.970)均高于准一级动力学模型(0.737 ~ 0.901), 且拟合获得的Qe更接近实测值(0.948、1.007和1.129 mg·g-1), 表明准二级动力学模型能更好地描述PE对Cd2+的吸附过程, 吸附过程受表面吸附位点、传质和颗粒内扩散等作用影响.
|
图 3 PE微塑料吸附Cd2+的动力学曲线及模型拟合 Fig. 3 Adsorption kinetics of Cd2+ fitted with kinetic models |
|
|
表 3 PE微塑料吸附Cd2+的动力学模型拟合参数 Table 3 Fitted parameters of the kinetic model of Cd2+ adsorption on PE microplastics |
为了进一步研究PE对Cd2+的吸附过程, 采用Webber-Morris模型对吸附结果进行拟合, 如图 3和表 4所示.吸附过程分为3个阶段, 分别为液膜扩散、颗粒内扩散和吸附/解吸动态平衡阶段.3个阶段的扩散速率常数大小排序为:k1 > k2 > k3, 且C值不等于0, 表明微塑料对Cd2+的吸附速率不仅受颗粒内扩散控制, 外部扩散也很重要[29].
|
|
表 4 PE微塑料吸附Cd2+的Webber-Morris模型拟合参数 Table 4 Fitted parameters of the Webber-Morris model of Cd2+ adsorption on PE microplastics |
2.1.3 吸附等温线
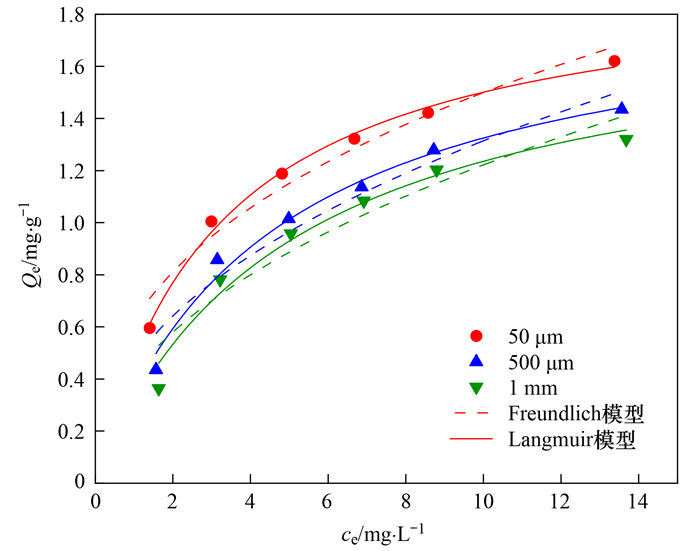
图 4为不同粒径PE微塑料对Cd2+的吸附等温线, 随着平衡液浓度的增加, PE对Cd2+的吸附量也逐渐增加.当Cd2+浓度达15 mg·L-1时, 3种粒径(50 μm、500 μm和1 mm)的微塑料对应的吸附量分别为1.620、1.435和1.320 mg·g-1, 微塑料粒径越小, 吸附量越大.采用Langmuir和Freundlich模型对Cd2+的等温吸附进行拟合(表 5), Langmuir模型的拟合结果(R2值在0.989 ~ 0.995之间)优于Freundlich模型(R2值在0.917 ~ 0.963之间), 表明PE对Cd2+的吸附是单分子层吸附[30], 微孔填充是微塑料吸附Cd2+的主要机制.Qm随粒径的减小而增大, 与本实验的结果一致, 说明Cd2+在塑料颗粒上的吸附与其尺寸大小密切相关, 这是因为较小的塑料颗粒具有较大的比表面积, 因此增加了固液接触的机会, 从而为Cd2+提供了更多的吸附位点[31].KL可用来反映微塑料对Cd2+的吸附强度, KL值越大自发反应速率也越大, 从表中可以看出, 随着微塑料粒径的减小KL增大.此外, 1/n可用于评估吸附类型, 当1/n大于1时, 吸附是化学吸附, 当1/n小于1时, 是物理吸附[32].如表 5所示, 1/n(0.381 ~ 0.462)的值均小于1, 进一步表明微塑料对Cd2+的吸附以物理吸附为主.
|
图 4 Cd2+在PE微塑料上的吸附等温线 Fig. 4 Adsorption isotherms of Cd2+ on PE microplastics |
|
|
表 5 PE微塑料吸附Cd2+的Langmuir和Freundlich拟合参数 Table 5 Fitted parameters of different isotherm models of Cd2+adsorption on PE microplastics |
2.2 PE微塑料添加量对土壤中Cd2+释放迁移的影响
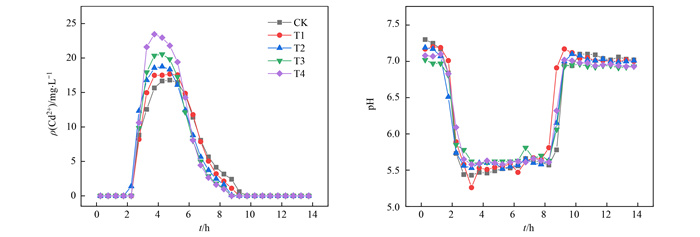
通过柱实验研究了不同微塑料处理下Cd在土壤中的迁移特征.图 5为0.1 mol·L-1 CaCl2条件下, 不同微塑料添加量土柱中Cd2+的穿透曲线.淋出液中Cd2+浓度峰值随PE添加量的增大而增大, 不同处理下(CK、T1、T2、T3和T4), ρ(Cd2+)峰值分别为16.79、17.66、18.75、20.54和23.45 mg·L-1, 且在T2、T3和T4处理下出现峰值提前现象, 说明PE微塑料使Cd在土壤中的移动性增强, 可导致Cd的生物有效性升高.微塑料的添加为Cd2+提供了吸附位点, 降低了土壤对Cd2+的吸附, 由2.1节的分析可知, 微塑料对Cd2+的吸附以物理吸附为主, 容易通过离子交换、解离等作用释放出一定含量的Cd2+[33], 从而增加了Cd2+的移动性.此外, 当微塑料进入土壤后, 微塑料与土壤颗粒相结合, 使土壤的电位增加(-4.26 mV), 进而降低了其对重金属的静电吸附[34], 促进了Cd2+的迁移.微塑料的添加量越大, 对Cd释放迁移的促进作用越强.不同微塑料处理下, Cd2+穿透曲线均出现了拖尾现象, 说明土壤/微塑料对Cd的吸附解吸受时间控制, 这与微塑料对Cd2+的动力学吸附实验结果一致.
|
图 5 不同PE微塑料添加量下Cd2+浓度和pH变化曲线 Fig. 5 Variation of Cd2+ concentration and pH under different PE additions |
从图 5可以看出, 随着CaCl2溶液的通入, pH呈现下降、趋于平稳、上升和趋于平稳的变化规律.这是因为大量Ca2+的输入把Cd2+置换出来的同时把土壤上的H+置换出来, 造成出流液pH降低, 有利于Cd2+的进一步解吸;去离子水淋洗后, 由于土壤的缓冲性及Ca2+的解吸, 溶液中的H+又被吸附, pH逐渐升高, 趋于平稳.实验过程中, pH < 8, Cd主要以Cd2+形式存在, 无Cd沉淀产生[35].另外, 不同处理土壤pH变化差异不显著, 说明PE微塑料对土壤pH影响不大, 实验条件下微塑料表面含氧官能团去质子化作用较弱.
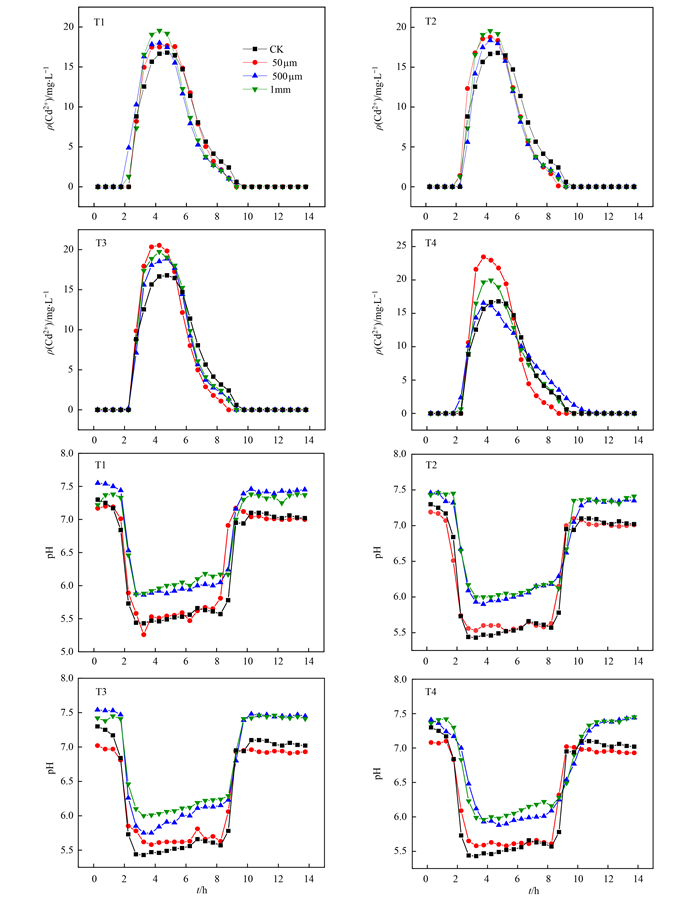
2.3 PE微塑料粒径对Cd2+释放迁移的影响图 6为不同粒径(50 μm、500 μm和1 mm)微塑料处理土壤中Cd2+淋出浓度变化曲线.从图 6中可以看出, 除粒径500 μm、添加量20%处理外, PE微塑料均对Cd的迁移有促进作用.当微塑料添加量较大时(7%、20%), 小粒径微塑料颗粒(50 μm)更有利于Cd2+的迁移, 这是因为微塑料粒径越小, 数量也就越多, 其与土壤的总接触面积越大, 土壤对Cd吸附位点越少;另外, 由吸附实验结果可知, PE粒径越小对Cd2+的吸附量越大, 被PE吸附的Cd2+容易解吸, 从而促进了Cd2+的迁移.微塑料粒径为50 μm时, 出流液pH明显低于其他粒径, 低pH有利于Cd2+的迁移.当微塑料添加量较低时(1%、4%), 微塑料对Cd吸附解吸的影响较弱, 土壤中大孔隙占比随微塑料粒径的增大而增加[36], 此时土壤中的大孔隙为影响重金属运移的主要因素, 从而导致大粒径微塑料(1 mm)对Cd2+迁移的促进作用更显著.de Souza Machado等[37]研究发现微塑料颗粒与土壤颗粒相差越大对土壤结构的影响越大, 由供试土壤的颗粒组成可以判断1 mm的微塑料对土壤结构的影响最大.另外, 大粒径微塑料的加入使得微塑料和土壤之间、微塑料和微塑料之间形成新的水流通道, 且微塑料由于本身具有疏水性会使新的水流通道的水流速度高于原有通道[38], 造成淋出液中Cd2+浓度峰值较无微塑料添加土壤提前和增大.因此, 微塑料粒径对Cd2+释放迁移的影响与其含量有关, 且微塑料含量越大, 土壤中Cd的移动性对粒径变化越敏感.
|
图 6 不同PE微塑料粒径下Cd2+浓度和pH变化曲线 Fig. 6 Variation of Cd2+ concentration and pH under different PE particle sizes |
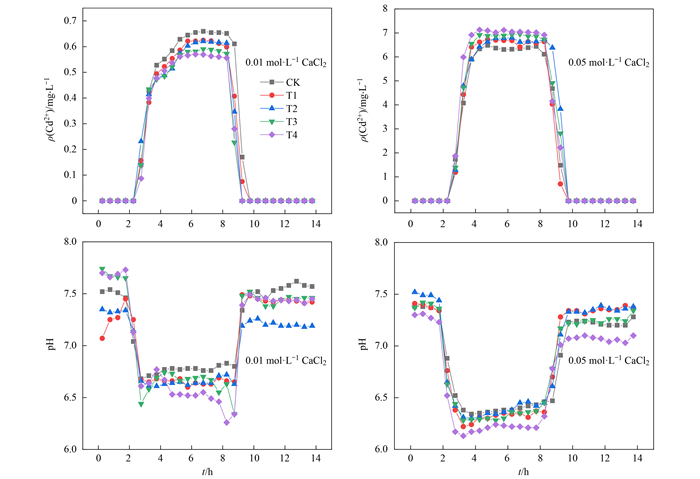
图 7为0.01 mol·L-1和0.05 mol·L-1 CaCl2条件下, 不同微塑料处理土壤中Cd2+淋出浓度变化曲线.用CaCl2溶液淋溶土柱2 h后, Cd2+浓度逐渐增大, 且维持一定水平, 去离子水淋溶2 h后Cd2+浓度逐渐下降.结合图 5可以看出, 不同处理土壤淋出液中Cd2+浓度最大峰值随离子强度的增大而升高, 从0.66 mg·L-1升高到7.05 mg·L-1和23.45 mg·L-1, 这是因为Ca2+与Cd2+竞争土壤/微塑料表面的吸附点位, 抑制固相介质对重金属的吸附, 从而促进Cd2+向下迁移, 且Ca2+浓度越高, 竞争作用越强, Cd2+淋出浓度越高.H+浓度的变化与Cd2+相似, Ca2+浓度越高, 置换出的H+浓度越高, pH越低.在CaCl2淋溶阶段, 从释放时间来看, 离子强度较大时(0.1 mol·L-1 CaCl2, 图 5), Cd2+在较短时间内被解吸出来, Cd2+出流浓度在去离子水淋洗前已达到峰值并开始下降;当离子强度较低时(0.01 mol·L-1和0.05 mol·L-1 CaCl2), 通入去离子水后, Cd2+仍保持较高的释放水平, 2 h后出流浓度逐渐降低.Cd2+淋出浓度逐渐降低直至后期不再出流, 一方面是因为土壤中大部分Cd2+在CaCl2淋溶阶段较容易以可交换态的形式解吸释放出来[39];另一方面, 在去离子水淋溶阶段淋出液pH升高, 土壤表面的含氧基团得到活化, Cd2+被络合而不易被解吸出来[40].
|
图 7 不同离子强度下Cd2+浓度和pH变化曲线 Fig. 7 Variation of Cd2+ concentration and pH under different ionic strength |
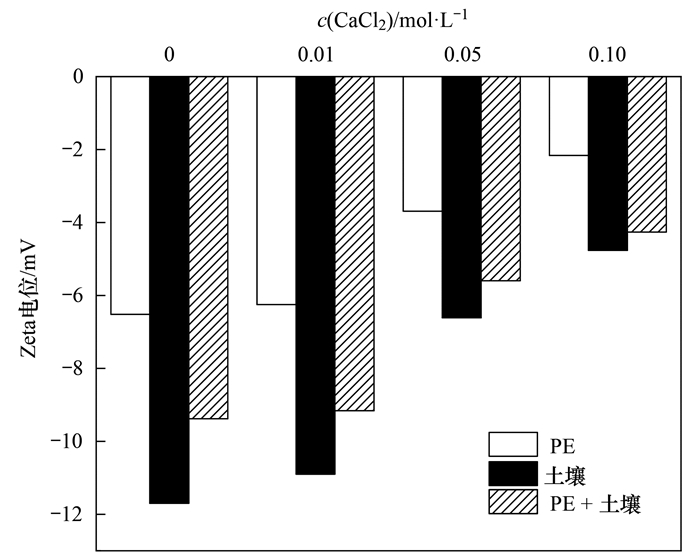
不同CaCl2浓度条件下, PE微塑料对Cd迁移的影响不同.当离子强度较低时(0.01 mol·L-1 CaCl2), PE微塑料抑制了Cd2+的迁移, 淋出液中Cd2+浓度低于未添加微塑料的土壤, 且淋出液中Cd2+浓度随PE添加量的增加从0.66 mg·L-1降低为0.57 mg·L-1.从图 7可以看出, 在较低离子强度下淋出液pH值较高, 与金属离子竞争的H+减少, 微塑料表面官能团易发生脱质子化[41], 从而导致微塑料表面的电负性(电位为-6.25 mV)和静电吸附位点增加, 使得微塑料对重金属的吸附能力提高, 而且由于Ca2+浓度较低, 对Cd2+的置换解吸作用较弱, 微塑料对Cd2+吸附滞留作用突显出来, 从而抑制了Cd2+的出流.当离子强度较高时(0.05 mol·L-1), 如2.2节所示, PE微塑料促进了Cd2+的迁移, 淋出液中Cd2+浓度高于未添加微塑料的土壤, 且淋出液中Cd2+浓度随微塑料添加量的增加从6.48 mg·L-1增大到7.12 mg·L-1.随着离子强度的增加, 淋出液pH值降低, H+与Ca2+对微塑料吸附位点的竞争加剧, 溶液中离子化学物质的活性降低以及双电层的压缩[42], 使得微塑料表面电位升高(图 8), 抑制了微塑料对重金属吸附.
|
图 8 不同离子强度下微塑料、土壤及其混合物的Zeta电位 Fig. 8 Zeta potential of microplastics, soils, and their mixtures at different ionic strengths |
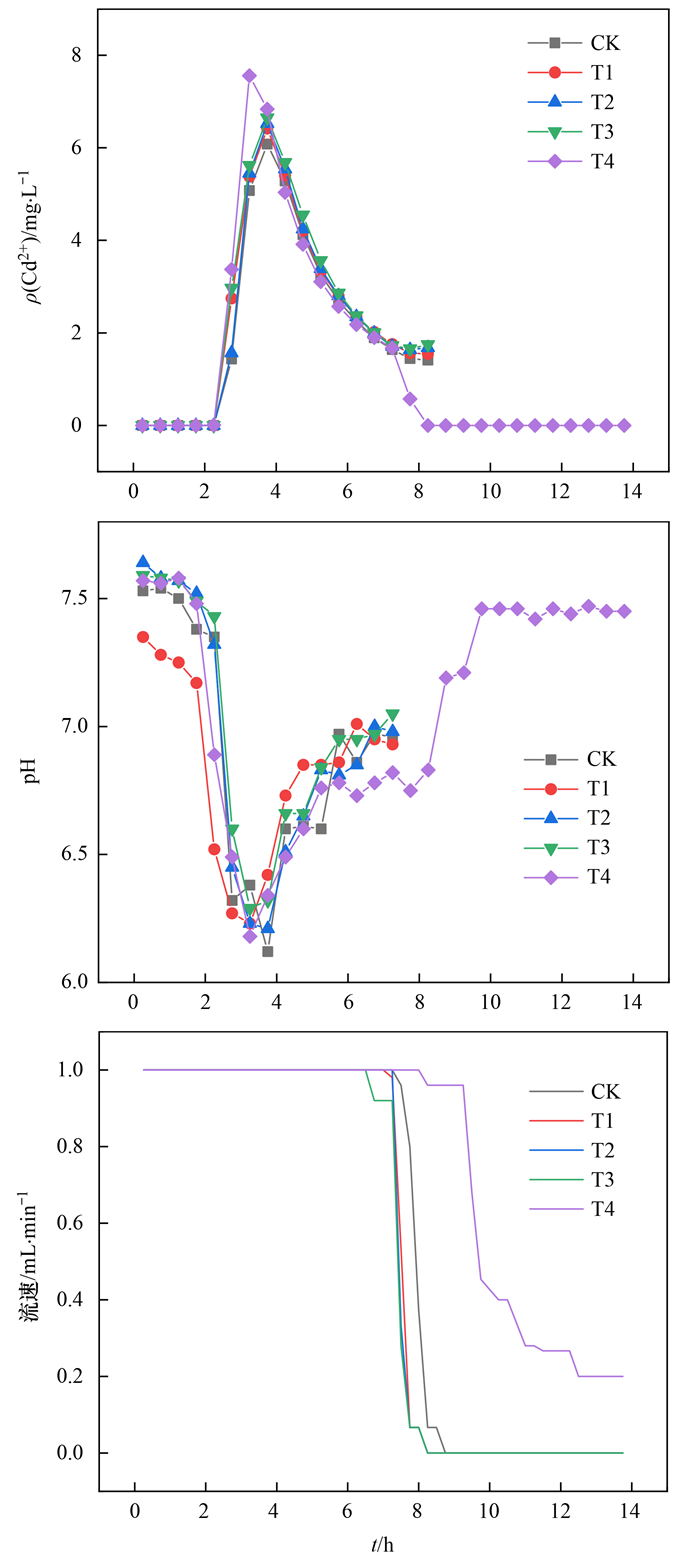
Na+为一价阳离子, 与Ca2+相比, 对Cd2+的竞争吸附及介质表面电位的影响不同.图 9为0.1 mol·L-1 NaCl条件下, 不同微塑料处理土壤中Cd2+浓度变化曲线.总体来看, 由于Na+的交换选择性系数较低[43], 交换能力较弱, 出流液中Cd2+的浓度较0.1 mol·L-1 CaCl2条件下显著下降.另外, 出流液pH高于0.1 mol·L-1 CaCl2条件下的pH值, 且降低到最低值(约6.2)后, 急剧升高, 从而抑制了Cd2+的迁移.随着Na+的不断输入, 不同微塑料处理土壤Cd2+淋出浓度均呈现先上升后下降的趋势, 除T4(20%)处理外, Cd2+的穿透曲线基本重合.在去离子水淋溶阶段, 流速变慢(图 9), 不同处理的土柱中均出现土壤颗粒流出现象.这是因为可交换性Na的含量会极大地影响土壤颗粒分散作用的强弱[44], 导致土壤团聚体分散成单个土壤颗粒, 通入去离子水后, 小颗粒被活化随溶液流出.土壤颗粒的分散可由0.1 mol·L-1 NaCl条件下微塑料和土壤颗粒的表面电位的降低来解释(微塑料、土壤及微塑料与土壤混合的电位分别为-11.1、-21.3和-22.0 mV), 电位的降低使颗粒间的静电斥力增强, 有利于颗粒分散.分散土壤颗粒紧密排列, 使土壤大孔隙数量减小[45], 出现渗透性差与无法出流的现象.而Ca2+为二价阳离子, 可在土壤颗粒之间形成桥梁, 即桥键作用, 抑制土壤的分散.
|
图 9 NaCl条件下Cd2+浓度、pH值及流速变化曲线 Fig. 9 Variation in Cd2+ concentration, pH value, and flow velocity under NaCl condition |
当微塑料无添加或添加量较小时(0%、1%、4%和7%), 用去离子水淋洗土柱2 h, 流速降为0(图 9);而T4(20%)处理下, 虽有出流但流速逐渐减低, 淋出液中有大量土壤颗粒, 这进一步说明微塑料可改变土壤结构和容重[46], 大量微塑料的存在使微塑料和土壤之间、微塑料和微塑料之间形成新的水流通道, 土壤颗粒和Cd2+可通过这些通道流出;另外, 微塑料可与土壤颗粒结合, 改变土壤团聚体大小分布, 从而改变孔隙分布, 土壤中微塑料含量越高, 这种影响越显著.
3 结论(1)微塑料对Cd2+的吸附能力随粒径的增大而降低, 以物理吸附为主;准二级动力学和Webber-Morris模型可以很好地拟合PE微塑料吸附Cd2+的动力学过程, 说明吸附过程是多个吸附阶段共同作用的结果;Langmuir模型对吸附等温线的拟合效果较好, 证实PE微塑料对Cd2+的吸附属于单层吸附.
(2)PE对Cd释放迁移的影响与CaCl2浓度有关.高离子强度下(0.05 mol·L-1和0.1 mol·L-1), 微塑料使土壤吸附位点减少、电负性降低, 导致土壤对Cd2+的吸附能力下降, 且微塑料吸附的Cd2+容易发生解吸, 从而促进了Cd2+的迁移, 微塑料的添加量越大对Cd2+迁移的促进作用越显著;低离子强度下(0.01 mol·L-1), 由于Ca2+的交换作用较弱, 且土壤/微塑料电负性较高, PE抑制了Cd2+的迁移.
(3)PE对Cd释放迁移的影响与微塑料粒径和含量有关.当PE添加量较小(1%、4%)时, 大粒径微塑料颗粒使得土壤中大孔隙所占的比例升高从而更有利于Cd2+的迁移;而当添加量较大(7%、20%)时, 微塑料对Cd2+吸附解吸的影响增强, 小粒径微塑料与土壤的接触面积较大从而减少土壤中的吸附位点, 更易促进Cd2+的迁移.此外, PE微塑料含量越高, 土壤中Cd的移动性对粒径变化越敏感.
(4)NaCl条件下, Na+显著降低了土壤的渗透性, PE对Cd的迁移无显著影响.Na+对渗透性的影响与PE的添加量有关, 20%添加量下土壤的渗透性显著增加, 说明PE改变了土壤团聚体的稳定性.
| [1] | Zhang K, Hamidian A H, Tubić A, et al. Understanding plastic degradation and microplastic formation in the environment: a review[J]. Environmental Pollution, 2021, 274. DOI:10.1016/j.envpol.2021.116554 |
| [2] |
朱宇恩, 文瀚萱, 李唐慧娴, 等. 汾河沿岸农田土壤微塑料分布特征及成因解析[J]. 环境科学, 2021, 42(8): 3894-3903. Zhu Y N, Wen H X, Li T H X, et al. Distribution and sources of microplastics in farmland soil along the Fenhe river[J]. Environmental Science, 2021, 42(8): 3894-3903. |
| [3] | Golmohammadi M, Fatemeh Musavi S, Habibi M, et al. Molecular mechanisms of microplastics degradation: a review[J]. Separation and Purification Technology, 2023, 309. DOI:10.1016/j.seppur.2022.122906 |
| [4] | Wong J K H, Lee K K, Tang K H D, et al. Microplastics in the freshwater and terrestrial environments: Prevalence, fates, impacts and sustainable solutions[J]. Science of the Total Environment, 2020, 719. DOI:10.1016/j.scitotenv.2020.137512 |
| [5] | Chen G L, Feng Q Y, Wang J. Mini-review of microplastics in the atmosphere and their risks to humans[J]. Science of the Total Environment, 2020, 703. DOI:10.1016/j.scitotenv.2019.135504 |
| [6] | Wang C H, Zhao J, Xing B S. Environmental source, fate, and toxicity of microplastics[J]. Journal of Hazardous Materials, 2021, 407. DOI:10.1016/j.jhazmat.2020.124357 |
| [7] | Horton A A, Walton A, Spurgeon D J, et al. Microplastics in freshwater and terrestrial environments: Evaluating the current understanding to identify the knowledge gaps and future research priorities[J]. Science of the Total Environment, 2017, 586: 127-141. DOI:10.1016/j.scitotenv.2017.01.190 |
| [8] | Kim S K, Kim J S, Lee H, et al. Abundance and characteristics of microplastics in soils with different agricultural practices: importance of sources with internal origin and environmental fate[J]. Journal of Hazardous Materials, 2021, 403. DOI:10.1016/j.jhazmat.2020.123997 |
| [9] | Wang J, Li J Y, Liu S T, et al. Distinct microplastic distributions in soils of different land-use types: a case study of Chinese farmlands[J]. Environmental Pollution, 2021, 269. DOI:10.1016/j.envpol.2020.116199 |
| [10] | Surendran U, Jayakumar M, Raja P, et al. Microplastics in terrestrial ecosystem: Sources and migration in soil environment[J]. Chemosphere, 2023, 318. DOI:10.1016/j.chemosphere.2023.137946 |
| [11] |
薄录吉, 李冰, 张凯, 等. 农田土壤微塑料分布、来源和行为特征[J]. 环境科学, 2023, 44(4): 2375-2383. Bo L J, Li B, Zhang K, et al. Distribution, sources, and behavioral characteristics of microplastics in farmland soil[J]. Environmental Science, 2023, 44(4): 2375-2383. |
| [12] |
郝爱红, 赵保卫, 张建, 等. 土壤中微塑料污染现状及其生态风险研究进展[J]. 环境化学, 2021, 40(4): 1100-1111. Hao A H, Zhao B W, Zhang J, et al. Research progress on pollution status and ecological risk of microplastics in soil[J]. Environmental Chemistry, 2021, 40(4): 1100-1111. |
| [13] | Yu H, Zhang Y, Tan W B, et al. Microplastics as an emerging environmental pollutant in agricultural soils: effects on ecosystems and human health[J]. Frontiers in Environmental Science, 2022, 10. DOI:10.3389/fenvs.2022.855292 |
| [14] | Feng X Y, Wang Q L, Sun Y H, et al. Microplastics change soil properties, heavy metal availability and bacterial community in a Pb-Zn-contaminated soil[J]. Journal of Hazardous Materials, 2022, 424. DOI:10.1016/j.jhazmat.2021.127364 |
| [15] | Tang Y Q, Liu Y G, Chen Y, et al. A review: research progress on microplastic pollutants in aquatic environments[J]. Science of the Total Environment, 2021, 766. DOI:10.1016/j.scitotenv.2020.142572 |
| [16] | Guo C X, Wang L L, Lang D N, et al. UV and chemical aging alter the adsorption behavior of microplastics for tetracycline[J]. Environmental Pollution, 2023, 318. DOI:10.1016/j.envpol.2022.120859 |
| [17] | Wu C, Tanaka K, Tani Y, et al. Effect of particle size on the colonization of biofilms and the potential of biofilm-covered microplastics as metal carriers[J]. Science of the Total Environment, 2022, 821. DOI:10.1016/j.scitotenv.2022.153265 |
| [18] | Zhou Y F, Yang Y Y, Liu G H, et al. Adsorption mechanism of cadmium on microplastics and their desorption behavior in sediment and gut environments: the roles of water pH, lead ions, natural organic matter and phenanthrene[J]. Water Research, 2020, 184. DOI:10.1016/j.watres.2020.116209 |
| [19] | Wang Q J, Zhang Y, Wangjin X X, et al. The adsorption behavior of metals in aqueous solution by microplastics effected by UV radiation[J]. Journal of Environmental Sciences, 2020, 87: 272-280. DOI:10.1016/j.jes.2019.07.006 |
| [20] | Hüffer T, Metzelder F, Sigmund G, et al. Polyethylene microplastics influence the transport of organic contaminants in soil[J]. Science of the Total Environment, 2019, 657: 242-247. DOI:10.1016/j.scitotenv.2018.12.047 |
| [21] |
赵雪君, 李达, 刘士领, 等. 聚酰胺和聚甲基丙烯酸甲酯微塑料对异菌脲土壤环境行为的影响[J]. 农药学学报, 2021, 23(5): 986-994. Zhao X J, Li D, Liu S L, et al. Effects of polyamide and polymethyl methacrylate microplastics on environmental behaviors of iprodione in soil[J]. Chinese Journal of Pesticide Science, 2021, 23(5): 986-994. |
| [22] | Wen X F, Yin L S, Zhou Z Y, et al. Microplastics can affect soil properties and chemical speciation of metals in yellow-brown soil[J]. Ecotoxicology and Environmental Safety, 2022, 243. DOI:10.1016/j.ecoenv.2022.113958 |
| [23] | Yu H, Hou J H, Dang Q L, et al. Decrease in bioavailability of soil heavy metals caused by the presence of microplastics varies across aggregate levels[J]. Journal of Hazardous Materials, 2020, 395. DOI:10.1016/j.jhazmat.2020.122690 |
| [24] |
庄国泰. 我国土壤污染现状与防控策略[J]. 中国科学院院刊, 2015, 30(4): 477-483. Zhuang G T. Current situation of national soil pollution and strategies on prevention and control[J]. Bulletin of Chinese Academy of Sciences, 2015, 30(4): 477-483. |
| [25] | GB 15618-2018, 土壤环境质量农用地土壤污染风险管控标准[S]. |
| [26] | Zou J Y, Liu X P, Zhang D M, et al. Adsorption of three bivalent metals by four chemical distinct microplastics[J]. Chemosphere, 2020, 248. DOI:10.1016/j.chemosphere.2020.126064 |
| [27] |
王林, 王姝歆, 曾祥英, 等. 老化作用对微塑料吸附四环素的影响及其机制[J]. 环境科学, 2022, 43(10): 4511-4521. Wang L, Wang S X, Zeng X Y, et al. Effect of aging on adsorption of tetracycline by microplastics and the mechanisms[J]. Environmental Science, 2022, 43(10): 4511-4521. |
| [28] | Wang F Y, Yang W W, Cheng P, et al. Adsorption characteristics of cadmium onto microplastics from aqueous solutions[J]. Chemosphere, 2019, 235: 1073-1080. DOI:10.1016/j.chemosphere.2019.06.196 |
| [29] | Li S S, Ma R X, Zhu X H, et al. Sorption of tetrabromobisphenol A onto microplastics: behavior, mechanisms, and the effects of sorbent and environmental factors[J]. Ecotoxicology and Environmental Safety, 2021, 210. DOI:10.1016/j.ecoenv.2020.111842 |
| [30] | Sun M, Yang Y K, Huang M L, et al. Adsorption behaviors and mechanisms of antibiotic norfloxacin on degradable and nondegradable microplastics[J]. Science of the Total Environment, 2022, 807. DOI:10.1016/j.scitotenv.2021.151042 |
| [31] | Nguyen T B, Ho T B C, Huang C P, et al. Adsorption of lead(Ⅱ) onto PE microplastics as a function of particle size: influencing factors and adsorption mechanism[J]. Chemosphere, 2022, 304. DOI:10.1016/j.chemosphere.2022.135276 |
| [32] | Huang D F, Xu Y B, Yu X Q, et al. Effect of cadmium on the sorption of tylosin by polystyrene microplastics[J]. Ecotoxicology and Environmental Safety, 2021, 207. DOI:10.1016/j.ecoenv.2020.111255 |
| [33] | Zhang S W, Han B, Sun Y H, et al. Microplastics influence the adsorption and desorption characteristics of Cd in an agricultural soil[J]. Journal of Hazardous Materials, 2020, 388. DOI:10.1016/j.jhazmat.2019.121775 |
| [34] | Huang H H, Li Z S, Wang H Y, et al. Adsorption performance of layered double hydroxides for heavy metals removal in soil with the presence of microplastics[J]. Journal of Environmental Chemical Engineering, 2022, 10(6). DOI:10.1016/j.jece.2022.108733 |
| [35] | Yu A Q, Sun X, Tang S, et al. Adsorption mechanism of cadmium on polystyrene microplastics containing hexabromocyclododecane[J]. Environmental Technology & Innovation, 2021, 24. DOI:10.1016/j.eti.2021.102036 |
| [36] |
王志超, 倪嘉轩, 张博文, 等. 聚氯乙烯微塑料对土壤水分特征曲线的影响及模拟研究[J]. 农业环境科学学报, 2022, 41(5): 983-989. Wang Z C, Ni J X, Zhang B W, et al. Simulation study to determine the influence of polyvinyl chloride microplastics on the soil water characteristic curve[J]. Journal of Agro-Environment Science, 2022, 41(5): 983-989. |
| [37] | de Souza Machado A A, Lau C W, Kloas W, et al. Microplastics can change soil properties and affect plant performance[J]. Environmental Science & Technology, 2019, 53(10): 6044-6052. |
| [38] |
刘子涵, 才璐, 赵小丽, 等. 聚乙烯残膜破碎过程对土壤水分入渗的影响[J]. 中国环境科学, 2022, 42(12): 5768-5774. Liu Z H, Cai L, Zhao X L, et al. Effect of decomposition of polyethylene residue film on soil water infiltration[J]. China Environmental Science, 2022, 42(12): 5768-5774. |
| [39] | Fan Y C, Wu Q G, Bao B L, et al. Ferrihydrite reduces the bioavailability of copper and cadmium and phosphorus release risk in hydroxyapatite amended soil[J]. Journal of Environmental Chemical Engineering, 2021, 9(6). DOI:10.1016/j.jece.2021.106756 |
| [40] | Xu J C, Ma Q, Chen C Y, et al. Cadmium adsorption behavior of porous and reduced graphene oxide and its potential for promoting cadmium migration during soil electrokinetic remediation[J]. Chemosphere, 2020, 259. DOI:10.1016/j.chemosphere.2020.127441 |
| [41] |
赵伟高, 田一梅, 赵鹏, 等. 淡水环境中微塑料与重金属的"木马效应"研究进展[J]. 环境科学, 2023, 44(3): 1244-1257. Zhao W G, Tian Y M, Zhao P, et al. Research progress on trojan-horse effect of microplastics and heavy metals in freshwater environment[J]. Environmental Science, 2023, 44(3): 1244-1257. |
| [42] | Wang X X, Zhang R X, Li Z Y, et al. Adsorption properties and influencing factors of Cu(Ⅱ) on polystyrene and polyethylene terephthalate microplastics in seawater[J]. Science of the Total Environment, 2022, 812. DOI:10.1016/j.scitotenv.2021.152573 |
| [43] |
陈春乐, 王果, 王珺玮. 3种中性盐与HCl复合淋洗剂对Cd污染土壤淋洗效果研究[J]. 安全与环境学报, 2014, 14(5): 205-210. Chen C L, Wang G, Wang J W. Leaching effect of three composite neutral salt solutions with hydrochloride acid on removing Cd from a Cd-contaminated soil[J]. Journal of Safety and Environment, 2014, 14(5): 205-210. |
| [44] | Guo Z C, Zhang J B, Fan J, et al. Does animal manure application improve soil aggregation? Insights from nine long-term fertilization experiments[J]. Science of the Total Environment, 2019, 660: 1029-1037. DOI:10.1016/j.scitotenv.2019.01.051 |
| [45] |
李慧, 林青, 徐绍辉. 咸水/微咸水入渗对土壤渗透性和盐分阳离子运移的影响[J]. 土壤学报, 2020, 57(3): 656-666. Li H, Lin Q, Xu S H. Effect of infiltration of saline water/brackish water on soil permeability and transport of salt cations in the soil[J]. Acta Pedologica Sinica, 2020, 57(3): 656-666. |
| [46] | Qiu Y F, Zhou S L, Zhang C C, et al. Soil microplastic characteristics and the effects on soil properties and biota: a systematic review and meta-analysis[J]. Environmental Pollution, 2022, 313. DOI:10.1016/j.envpol.2022.120183 |
 2024, Vol. 45
2024, Vol. 45


