2. 长安大学旱区地下水文与生态效应教育部重点实验室, 西安 710054;
3. 长安大学土地工程学院, 西安 710054
2. Key Laboratory of Subsurface Hydrology and Ecology in Arid Areas, Ministry of Education, Chang'an University, Xi'an 710054, China;
3. School of Land Engineering, Chang'an University, Xi'an 710054, China
随着工业、农业和城市的不断发展, 重金属污染日益严重, 目前我国超过80%的水体和10%的耕种土地都受到不同程度的重金属污染[1, 2].镉(Cd)是毒性最强的重金属元素之一, 人类暴露于镉污染中, 可能导致肾功能衰竭、骨疾病、神经系统疾病、嗅觉丧失、肝损伤和前列腺癌等一系列病症[3, 4].因此, 镉污染治理是一个亟待解决的问题.
生物炭是一种在限氧条件下通过生物质热化学转化获得的固体材料, 因其比表面积大、阳离子交换容量高、含富氧官能团丰富等特性, 在重金属污染治理方面具有广阔的应用潜力[5, 6].生物炭的吸附性能与生物质原料密切相关, 不同原料制备的生物炭, 其理化性质和表面结构都存在很大差异[7].因此, 炭基材料的选择至关重要.我国猕猴桃种植面积和产量均位居世界第一, 其中陕西种植面积达6.7×103 hm2, 接近全球的1/3, 已成为世界上最大的猕猴桃生产基地[8].猕猴桃属落叶藤蔓植物, 其蔓枝可长达10 m左右, 由于猕猴桃种植管理需要, 夏季和冬季都要进行疏枝修剪, 这些枝条作为农业废弃物被焚烧或堆弃, 不仅严重污染大气环境, 还容易引起病虫害.猕猴桃枝富含木质素和纤维素, 热解后往往比其他农业废弃物(如作物秸秆、畜禽粪便和果壳稻壳等)表现出更高的比表面积和更低的灰分含量[9], 且其茎叶中含有萜类、酚类、鞣质和多糖等成分, 有利于形成羟基、羧基和氨基等多种与Cd2+结合能力强的官能团.以上特性决定了猕猴桃枝可作为一种理想的生物质原料.
为了进一步提高生物炭的吸附性能, 近年来生物炭的表面改性受到越来越多的关注[10, 11].壳聚糖是自然界中最丰富的多糖, 具有良好的生物相容性、无毒无害和易化学修饰等特点.其分子长链上的羟基、氨基和酰胺基, 可借助配位键、氢键和离子键与重金属形成稳定的配合物[12].已有研究证明, 将壳聚糖负载到生物炭表面, 可显著提升生物炭表面的官能团数量、吸附位点和稳定性等.Xiang等[13]利用壳聚糖和MgCl2改性稻壳生物炭, 提高了对Cd2+的吸附能力, 并将其应用于镉污染水体和土壤的修复.Fan等[14]将壳聚糖负载在茶叶生物炭表面, 增加了生物炭表面的N/O相关官能团, 促进了对Cu2+的吸附.Zhang等[15]将壳聚糖引入到竹炭表面, 显著增加了活性吸附位点, 从而提高了对水溶液中Cr6+的去除率.Wang等[16]的研究发现壳聚糖可以与纳米FeS结合形成纳米配合物, 通过空间位阻和静电相互作用, 提高分散性, 从而提高花生壳生物炭对Pb2+的吸附能力.此外, 有研究表明壳聚糖改性生物炭的物理化学性质受生物炭的原料、制备温度和壳聚糖负载量等多种因素的影响[17].其吸附性能还会受初始吸附浓度、溶液pH、吸附剂用量以及温度等因素的影响[18].目前以树枝废弃物为原料制备壳聚糖改性生物炭的研究较少, 壳聚糖负载对生物炭理化性质和吸附特性的影响尚不明确, 对Cd2+的吸附机制也有待进一步探究.
因此, 本文以猕猴桃枝为原料, 壳聚糖为改性剂, 制备壳聚糖改性生物炭吸附材料.采用SEM-EDS、FTIR和XPS等表征方法对材料的结构和形貌进行表征分析.探讨壳聚糖的引入对生物炭结构、吸附性能和环境因素的影响机制.采用批量吸附实验探讨改性前后生物炭对水溶液中Cd2+的吸附性能和增益效果, 以期为猕猴桃枝资源化利用和Cd污染治理提供新思路.
1 材料与方法 1.1 实验材料猕猴桃枝采自陕西省周至县.壳聚糖(脱乙酰度≥90%, 粘度 < 200 mPa·s), 购自上海阿拉丁试剂有限公司. 其他化学试剂:盐酸, 氢氧化钠, 乙酸, 戊二醛50%水溶液, 氯化镉, 均为分析纯, 购自国药化学试剂有限公司.准确称取2.038 8 g的CdCl2·(5/2)H2O溶解在1 000 mL去离子水中, 制得1 g·L-1 Cd2+的储备溶液. 本研究中使用的不同浓度的Cd2+溶液通过将原液按比例稀释得到.
1.2 生物炭的制备与改性原始生物炭的制备:猕猴桃枝剪成3~5 cm小段, 用自来水清洗干净后, 去离子水冲洗3遍, 60℃干燥24 h, 粉碎后通过40目筛.将筛过的猕猴桃枝置于管式炉中(SX-G 04135型, 天津市中环实验电炉有限公司, 中国), 氮气气氛下, 以每分钟10℃升温至550℃保温2 h.待熔炉冷却至室温后, 收集样品, 研磨后通过100目筛网, 得到原始生物炭, 标记为BC.
壳聚糖改性生物炭的制备:将一定量的原始生物炭, 加入6 mol·L-1 HCl溶液中(固液比为1∶10), 室温下浸渍24 h, 过滤后, 用去离子水清洗至中性, 于烘箱中60℃烘干至恒重, 备用.准确称取1.0 g的壳聚糖溶解于300 mL, 2% 乙酸溶液中, 超声均匀分散.将酸浸后的生物炭加入壳聚糖乙酸溶液中(生物炭与壳聚糖的质量比为5∶1), 在200 r·min-1、60℃下搅拌30 min, 加入30 mL 2%的戊二醛溶液继续搅拌30 min, 滴加1 mol·L-1 NaOH调节pH至11后搅拌1 h, 抽滤、洗涤至中性, 烘干, 得到壳聚糖改性生物炭, 标记为CBC.
1.3 材料的测试与表征采用扫描电子显微镜和能谱仪(SEM-EDS, S-4800, Hitachi公司, 日本)进行改性前后生物炭的形貌特征和特定区域内元素的质量分数分析;采用傅立叶变换红外光谱仪(FTIR, Nicolet 5700, Thermo Fisher Scientific公司, 美国)测试改性前后生物炭的红外光谱;采用X射线光电子能谱仪(XPS, Escalab 250Xi, VG科学仪器公司, 英国)分析吸附Cd2+前后样品表面特定元素的状态.
1.4 批量吸附实验采用恒温振荡批处理法测定改性前后生物炭对Cd2+的吸附量.取25 mL 100 mg·L-1的Cd2+溶液于50 mL聚乙烯离心管中, 加入50 mg吸附材料, 分别在25、35和45℃的恒温振荡器中以180 r·min-1振荡24 h.然后, 在离心机中以3 000 r·min-1离心10 min, 吸取上清液过0.45 μm滤膜, 用原子吸收光谱仪(WFX-120, 北京瑞利分析仪器有限公司, 中国)测定滤液中Cd2+浓度, 根据式(1)计算吸附剂的平衡吸附容量Qe(mg·g-1), 根据式(2)计算去除率η(%).每一处理重复3次, 取平均值进行计算.
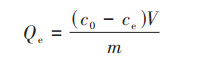
|
(1) |
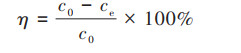
|
(2) |
式中, Qe为平衡吸附量, mg·g-1;c0和ce分别为Cd2+初始浓度和平衡浓度, mg·L-1;V为溶液体积, L;m为吸附剂质量, g;η为去除率, %.
1.5 吸附模型 1.5.1 吸附动力学模型采用Lagergren准一级动力学方程[式(3)]、Lagergren准二级动力学方程[式(4)]和颗粒内扩散模型[式(5)]对吸附动力学曲线进行拟合.
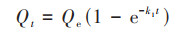
|
(3) |
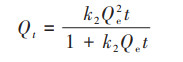
|
(4) |
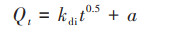
|
(5) |
式中, Qe和Qt分别为平衡吸附量和t时刻的吸附量, mg·g-1;k1为准一级动力学方程常数, h-1;k2为准二级动力学方程常数, g·(mg·h)-1;kdi为颗粒内扩散模型速率常数, mg·(g·min1/2)-1;a为颗粒吸附液膜层厚度, mg·g-1.
1.5.2 吸附等温线模型在25、35和45℃下, 采用Langmuir模型[式(6)]和Freundlich模型[式(8)]对吸附等温线进行拟合, 计算分离因子RL[式(7)]评估吸附反应发生的难易程度.
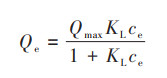
|
(6) |
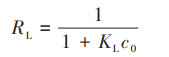
|
(7) |
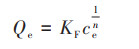
|
(8) |
式中, Qe和Qmax分别为平衡吸附量和最大吸附量, mg·g-1;ce为平衡浓度, mg·L-1;KL为Langmuir模型吸附常数, L·mg-1;KF为Freundlich模型常数, (mg·g-1)·(L·mg-1)1/n;1/n为经验常数.
1.5.3 吸附热力学采用热力学公式计算吸附过程的吉布斯自由能变∆Gθ[式(9)]、焓变∆Hθ和熵变∆Sθ[式(10)], 方程式如下:
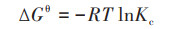
|
(9) |
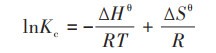
|
(10) |
式中, ∆Gθ为吉布斯自由能, kJ·mol-1;∆Hθ为标准摩尔焓变, kJ·mol-1;∆Sθ为标准摩尔熵变, J·(mol·K)-1;Kc为分配系数;R为气体常数, 8.314 J·(mol·K)-1;T为热力学温度, K.
1.6 吸附再生实验通过连续5次吸附和解吸循环实验, 测试改性前后生物炭的再生吸附性能.将50 mg饱和Cd2+的BC和CBC分别加入25 mL 0.05 mol·L-1乙二胺四乙酸钠(Na2EDTA)洗脱液中, 在25℃的恒温振荡器中以180 r·min-1振荡解吸24 h.离心后, 吸取上清液过0.45 μm滤膜, 测定滤液中Cd2+浓度.收集固体样品, 用去离子水洗至pH不变, 烘干至恒重, 进行下一次吸附.上述过程循环5次, 每个样本测量重复3次, 取平均值.
1.7 数据分析与质量控制采用Origin 8.0进行实验数据分析和绘图.所有实验设置3次重复, 实验结果用3次重复的平均值表示, 相对标准偏差小于5%.实验所用容器用3%硝酸溶液浸泡24 h后, 用去离子水冲洗3次.
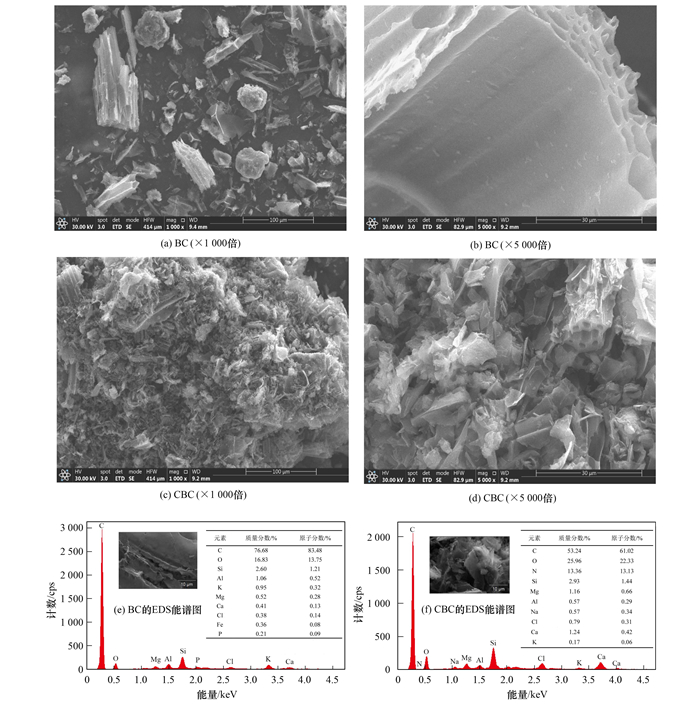
2 结果与讨论 2.1 材料的特性表征 2.1.1 扫描电镜分析(SEM-EDS)图 1(a)~ 1(d)为原始生物炭(BC)和壳聚糖改性生物炭(CBC)在1 000倍和5 000倍下的SEM分析结果.BC为多孔柱状结构, 孔隙结构明显[图 1(a)];且外表面光滑, 孔隙结构排列整齐[图 1(b)].这种外观表现出典型的木质生物炭的结构特点[18].CBC则呈致密的簇状结构, 孔隙结构不明显[图 1(c)], 材料表面粗糙, 呈白色, 有光泽[图 1(d)].这与Shi等[19]的研究结果一致, 表明改性过程中, 壳聚糖不仅包覆在生物炭表面, 而且进入生物炭的孔隙中, 改变了生物炭的孔隙结构.图 1(e)和1(f)为BC和CBC的EDS能谱图, 如图所示, 生物炭表面主要含C和O元素及少量微量元素(如K、Mg、Ca), 改性后C元素质量分数降低, O元素质量分数增加, 新增N元素谱峰, 说明壳聚糖成功包覆在生物炭表面.由于壳聚糖含有高比例羟基(—OH)和氨基(—NH2)官能团, 降低了生物炭表面C元素占比[17, 20], 提高了生物炭的极性和亲水性[9], 从而有利于其与水溶液中重金属离子的结合.
|
图 1 BC和CBC的SEM和EDS表面元素分布 Fig. 1 SEM images and EDS elemental maps of BC and CBC |
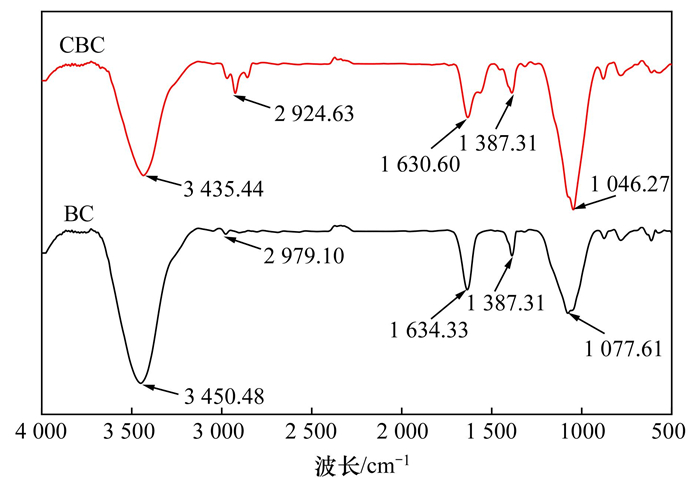
图 2为改性前后生物炭的FTIR分析结果.由图可见, BC和CBC红外光谱特征峰的位置基本相同, 但峰的振动强度有所差异.在3 435~3 450 cm-1处有宽而强的吸收带, 这是醇和羧基官能团中O—H的伸缩振动吸收峰[21].在2 920~2 979 cm-1处为脂肪性—CH2的不对称伸缩振动吸收峰[22];在1 630~1 634 cm-1为羧基和酮基中C=O的伸缩振动.在1 387 cm-1为酚羟基C—OH的伸缩振动吸收峰[14];1 046~1 077 cm-1对应于纤维素、半纤维素和木质素的C—O键的伸缩振动吸收峰[23].与BC相比, CBC在2 924.63 cm-1附近出现了甲基和亚甲基峰;在1 630.60 cm-1附近的振动峰增强, 是由于N—H键的剪式弯曲振动峰叠加所致;在1 387.31 cm-1处的振动峰强度增加, 酚羟基C—OH基团数量增加;在1 046.27cm-1附近的C—N伸缩振动带和C—O—C伸缩振动带重叠, 导致吸收峰强度增大[24].与Chen等[20]的FTIR光谱比较, 具有相似的特征峰, 表明壳聚糖成功加载到生物炭上.
|
图 2 BC和CBC的FTIR谱图 Fig. 2 FTIR spectra of BC and CBC |
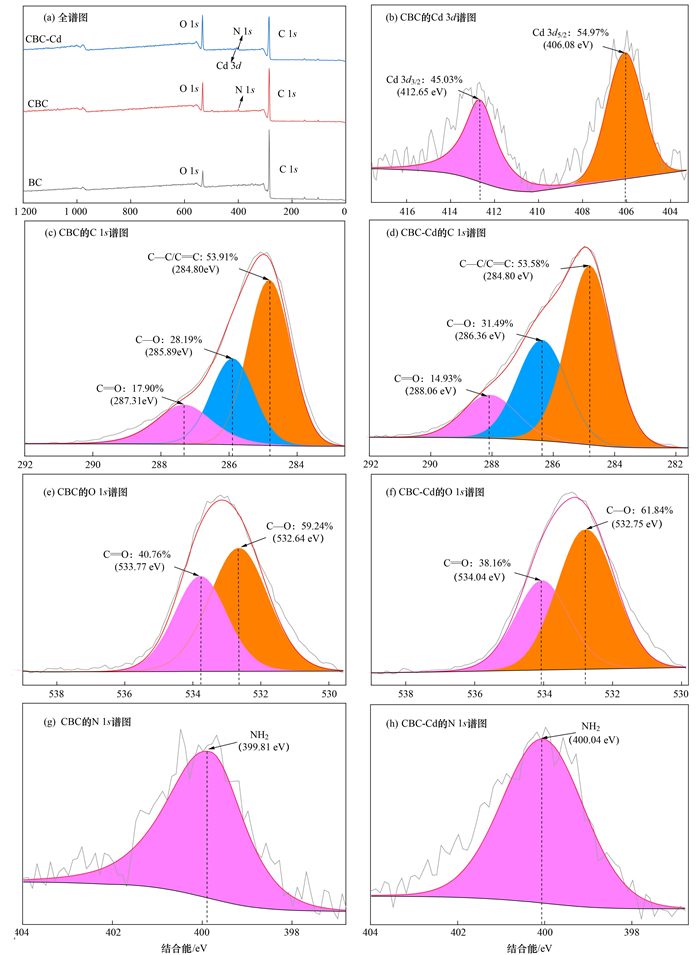
对生物炭进行X射线光电子能谱分析, 可以得到关于生物炭改性前后及吸附Cd2+后的官能团数量、特征原子的变化信息[17].图 3(a)为BC、CBC及其吸附Cd2+后CBC-Cd的XPS全谱图.与BC相比, CBC的全谱图中O 1s峰增加, C 1s峰减小, 新增N 1s峰, 证明壳聚糖成功负载到生物炭表面[25].吸附Cd2+后在406 eV出现了Cd 3d的谱峰, 高分辨率的Cd 3d光谱如图 3(b)所示, Cd 3d的两个峰分别归属于Cd 3d3/2(412.65 eV)和Cd 3d5/2(406.08 eV), 表明CBC成功吸附了Cd2+.图 4(c)为CBC的C1s谱图, 在284.80、285.89和287.31 eV有3个峰, 分别是脂肪族或芳香族中的碳原子C—C/C=C(53.91%), 羟基碳C—O(28.19%)和羰基碳C=O(17.90%).图 4(d)为CBC吸附Cd2+后的C 1s谱图, C—C/C=C的结合能没有发生变化, C—O和C=O的结合能升高为286.36 eV和288.06 eV, 表明在CBC对Cd2+的吸附过程中, C原子没有直接参与成键, 而羟基C—O和羰基C=O参与成键, O原子的核外电子分享给Cd2+, 其相邻的C原子电子云密度降低, 结合能升高.由图 3(e)和3(f)知, CBC吸附Cd2+前后C—O的电子结合能由532.64 eV变为532.75 eV, C=O的电子结合能由533.77 eV变为534.04 eV, 这是因为O原子参与了配位反应, 与Cd2+共享电子对, 使其自身的电子云密度降低, 结合能增加.图 4(g)和4(h)分别是吸附前后N 1s的XPS谱图, 吸附前结合能为399.81 eV, 吸附后结合能增加到400.04 eV, 这是因为N贡献电子给Cd2+, 其本身的电子云密度降低, 结合能增加.综上所述, 在CBC对Cd2+的吸附过程中C—O、—C=O和—NH2基团参与了配位反应.
|
图 3 BC、CBC和CBC-Cd的XPS谱图 Fig. 3 XPS spectra of BC, CBC, and CBC-Cd |
|
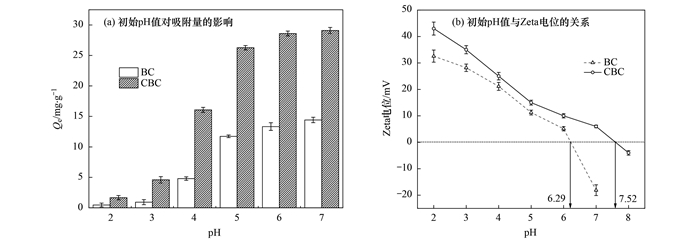
图 4 溶液初始pH对吸附量和Zeta电位的影响 Fig. 4 Effect of solution pH on the adsorption capacity and Zeta potential of BC and CBC |
溶液初始pH是一个重要的参数, 影响炭基材料的表面电荷, 官能团的形态和金属离子的电离程度[25].当pH > 7时, 溶液中OH- 浓度处于较高水平, 会与Cd2+结合生成Cd(OH)2沉淀, 干扰去除率的计算, 因此在溶液pH范围为2~7的条件下, 考察溶液初始pH对生物炭材料吸附性能的影响.由图 4(a)可见, BC和CBC对Cd2+的去除率随pH的上升而逐渐增大.在溶液初始pH为2~3范围内, 生物炭材料对Cd2+吸附量较小, 这是因为在酸性条件下, 溶液中大量的H+与Cd2+竞争吸附位点, 同时, 酸性官能团表面因质子化而带正电荷, 对Cd2+产生静电排斥[26].当pH达到3~6时, 吸附量急剧增加, BC和CBC的吸附量分别从0.93 mg·g-1和4.60 mg·g-1增加到13.33 mg·g-1和26.60 mg·g-1.这是由于随着溶液中H+浓度降低, 静电斥力和竞争作用减弱, 吸附效率显著提高[27, 28].当pH从6增加到7时, 生物炭材料对Cd2+的吸附量无明显变化.这可能是由于官能团的去质子化达到最大值.此外, pH值对吸附过程的影响也可以从吸附材料的表面电荷来解释[图 4(b)].BC和CBC吸附Cd2+的零电荷点(pHpzc)约为6.19和7.52, 当环境pH值低于pHpzc时, 吸附剂表面为正电荷, 由于静电排斥作用, 不利于对带正电荷的金属离子的吸附.然而, 值得注意的是CBC在酸性环境中对Cd2+仍表现出良好的吸附性能, 说明CBC与Cd2+之间的相互作用不单是静电作用.根据软硬酸碱理论, CBC表面的—NH2(软碱)易于与Cd2+(软酸)形成共价键.因此, 吸附容量的变化是配位作用和静电作用共同作用的结果.
综上所述, BC和CBC对Cd2+的去除率均在pH > 3时显著增加, pH为6时达到最大值.因此, 在后续实验中, 溶液的初始pH被设定为6.
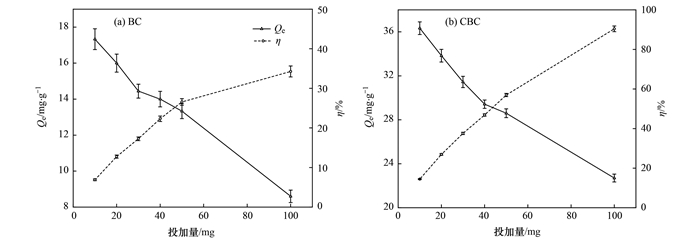
2.2.2 投加量对吸附效果的影响为了最大限度地利用吸附剂的活性位点, 需要考察吸附剂投加量对吸附量和去除率的影响, 以确定最佳投加量, 结果如图 5所示.随着投加量从10 mg增加到100 mg, BC和CBC对Cd2+的去除率分别从6.9%和14.5%增加到34.3%和90.4%, 而吸附量则分别从17.3 mg·g-1和36.3 mg·g-1下降到8.6 mg·g-1和22.7 mg·g-1.通常随着吸附剂投加量增加吸附位点和比表面积增大, 因此吸附量增大[29].然而, 投加量过大时, 过剩的吸附剂导致吸附位点的利用效率降低, 且会产生团聚现象, 造成吸附位点重叠, Cd2+扩散受阻, 因而吸附剂的单位吸附量降低.综合考虑, BC和CBC的最佳投加量确定在40 ~ 60 mg(1.6 ~ 2.4 g·L-1)左右.此外, CBC的去除率和吸附量明显高于BC, 表明壳聚糖改性可以提高生物炭对重金属的吸附性能.
|
图 5 投加量对吸附量和去除率的影响 Fig. 5 Effect of dosage on adsorption capacity and removal efficiency of BC and CBC |
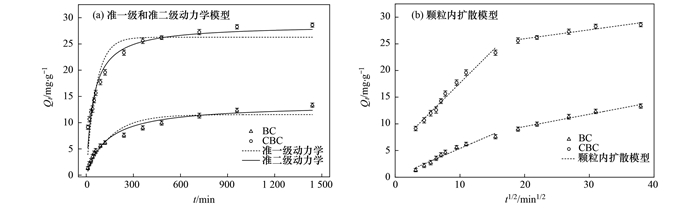
准一级和准二级动力学及颗粒内扩散模型的拟合结果如图 6所示.由图 6(a)可见, 两种生物炭吸附材料对Cd2+的吸附均分为快慢两个阶段.在快反应阶段(0~240min), Cd2+迅速占据可用的活性位点, BC和CBC对Cd2+的吸附量分别达到最大吸附量的57.1% 和81.6%.在慢反应阶段(240~1 440 min), 吸附量缓慢增加, 分别在720 min(BC)和480 min(CBC)达到吸附平衡.可见壳聚糖改性提高了吸附速率, 缩短了到达平衡的时间.由表 1可知, BC和CBC准二级动力学拟合结果的R2分别为0.975 0和0.955 6, 均高于准一级动力学拟合结果的0.925 3和0.877 5.此外, BC准一级和准二级动力学模型计算出的平衡吸附量分别为11.54 mg·g-1和13.50 mg·g-1, 后者与实验结果13.33 mg·g-1更接近;相比之下, CBC的平衡吸附量提升明显, 分别为26.28 mg·g-1和28.64 mg·g-1, 准二级动力学模型也与实验结果28.60 mg·g-1更接近.这表明准二级动力学方程能更好描述两种吸附材料对Cd2+的吸附过程, 吸附速率与吸附过程驱动力的平方成正比, 表明吸附速率主要受化学吸附过程控制[30].
|
图 6 BC和CBC对Cd2+的吸附动力学拟合 Fig. 6 Kinetic fitting curves of Cd2+ adsorption onto BC and CBC |
|
|
表 1 BC和CBC对Cd2+的吸附动力学拟合参数 Table 1 Kinetic model fitting parameters for Cd2+ adsorption on BC and CBC |
为了进一步研究吸附过程中的扩散机制和控速步骤, 采用颗粒内扩散模型对吸附结果进行拟合, 结果如图 6(b)所示, 吸附过程分为两个阶段, 第一阶段可视为陡坡阶段, 此时Cd2+迅速扩散到吸附剂外表面, 即表面扩散阶段, 由于Cd2+与吸附材料表面的强相互作用, 第一阶段的瞬时吸附非常快, 这是由于静电作用引起的物理吸附过程[31].第二阶段为缓坡阶段, Cd2+需要扩散至吸附材料内部才能与吸附位点结合, 这是一个缓慢的过程, 以配位或沉淀反应为主[32].截距(a)与边界层厚度有关, 截距(a)越大, 边界层对吸附过程的影响越大.由表 1可以看出, 第二阶段的截距比第一阶段大得多, 说明第二阶段边界层厚度对吸附速率的影响比第一阶段大.此外, 颗粒内扩散模型拟合直线不过原点, 表明BC和CBC对Cd2+的吸附受多种机制的影响.
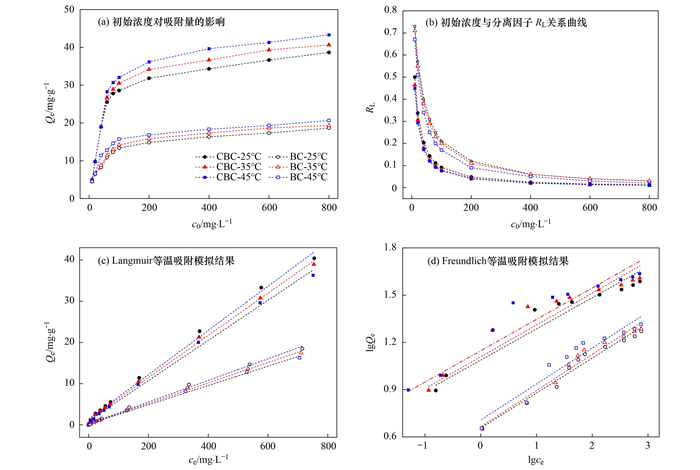
2.2.4 吸附等温线吸附等温线可以用来描述一定温度条件下, 吸附材料的吸附量与吸附质的平衡浓度的曲线关系.通过对吸附过程中吸附等温线模型的拟合, 可以进一步研究吸附机制[33, 34].图 7(a)为改性前后生物炭在25、35和45℃下的初始浓度(c0)对吸附量(Qe)的影响, 从中可知, 两种吸附材料对Cd2+的吸附量随着初始浓度的增大而增大, 直到达到饱和.在25、35和45℃下BC的最大吸附量分别为18.67、19.33和20.67 mg·g-1, 改性后的CBC吸附量达到38.67、40.67和43.33 mg·g-1, 较前者提升了107.12%、110.40%和109.63%.这一结果一方面说明, 壳聚糖的负载有利于增加生物炭对Cd2+的吸附.另一方面说明, Cd2+的吸附量随温度升高而增大, 表明升高温度可以促进Cd2+吸附.
|
图 7 BC和CBC对Cd2+的吸附等温过程 Fig. 7 Isothermal adsorption process of Cd2+ on BC and CBC at different temperatures |
采用Langmuir和Freundlich模型对25、35和45℃下的吸附等温线进行拟合[图 7(c)和7(d)], 吸附等温参数计算结果如表 2所示, Langmuir等温拟合结果的相关系数R2均高于Freundlich等温拟合结果, 且最大吸附容量与实验结果接近, 说明两种生物炭对Cd2+的吸附更符合Langmuir等温线模型, 单分子层的化学吸附起主要作用.Langmuir方程的无量纲常数分离因子RL可以预测吸附材料与Cd2+之间的亲和度[30, 35].由分离因子RL与c0的关系曲线[图 7(b)]可见, 不同吸附温度下的RL值在0.010 3~0.725 1范围内(介于0~1), 表明改性前后两种生物炭吸附材料对Cd2+的吸附均为优惠吸附(favorable), 且CBC的RL值小于BC, 表明CBC对Cd2+亲和力更强.此外, 随着初始浓度和温度的增大RL值减小, 表明增大浓度和温度对吸附过程有利.Freundlich等温吸附模型中1/n的数值在0.1~0.3之间, 远小于1, 表示被吸附离子易于吸附在吸附剂表面[36].且CBC的1/n数值均小于BC, 说明壳聚糖改性使得生物炭对Cd2+的吸附更容易进行.
|
|
表 2 BC和CBC对Cd2+的等温吸附模型拟合参数 Table 2 Isotherm fitting parameters of Cd2+ adsorption on BC and CBC |
2.2.5 吸附热力学
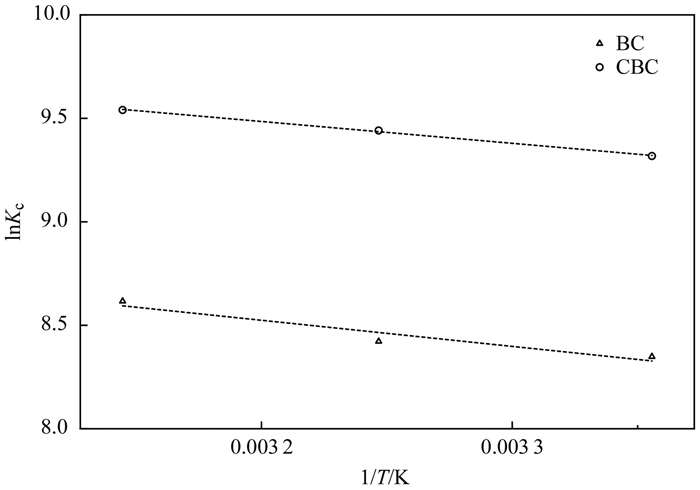
为了研究改性后生物炭的吸附热力学性质, 揭示吸附作用机制, 计算了吸附过程的热力学参数(∆Hθ, ∆Sθ和∆Gθ).图 8为lnKc对1/T的拟合直线, 根据拟合直线的斜率和截距及[式(9)和式(10)]可求出∆Hθ和∆Sθ(表 3).结果显示, 在3个温度条件下, ∆Hθ和∆Sθ均为正值, ∆Gθ均为负值.∆Hθ为正值表明BC和CBC对Cd2+吸附具有吸热性质, ∆Sθ为正值表明吸附过程中溶液和吸附剂的部分结构发生了变化, 导致生物炭/溶液界面体系的随机性增加[37].∆Gθ为负值, 吸附过程可以自发可行.而∆Gθ的绝对值随温度的升高而增大, 说明温度越高, 越有利于吸附.这是因为高温下有利于去溶剂化作用, 从而促进了Cd2+的扩散和吸附[38].
|
图 8 改性前后生物炭吸附Cd2+的 lnKc对1/T拟合直线 Fig. 8 Fitting straight line of lnKc versus 1/T for adsorption of Cd2+ by BC and CBC |
|
|
表 3 BC和CBC吸附Cd2+的热力学参数 Table 3 Thermodynamic parameters for Cd2+adsorption on BC and CBC |
2.3 吸附机制
壳聚糖分子链中的C2—NH2活性基团上的N原子具有孤对电子, 能进入金属离子的空轨道中, 发生配位反应, 对金属离子有稳定的配位作用.一级羟基(C6—OH)在空间构象上, 可较为自由地扭转, 位阻较小, 可以与其它基团结合, 从而实现将壳聚糖嫁接于支撑体(生物炭)表面, 以提高生物炭的稳定性和对重金属离子的吸附量.SEM-EDS分析结果[图 1(a)和1(b)]显示本研究所选用的猕猴桃枝生物炭(BC)具有丰富的孔隙结构和相对较大的比表面积, 这是由于猕猴桃枝中含有丰富的纤维素、木质素[9], 有助于形成多孔结构和活性基团, 为壳聚糖的负载提供了良好支撑体.改性后[图 1(c)和1(d)], 由于壳聚糖的包覆作用, 孔隙结构不明显, 比表面积降低, 而吸附容量提高[图 7(a)], 说明吸附过程受比表面积影响较小, 主要由化学吸附控制[39].元素分析结果显示改性后生物炭表面的N、O元素含量明显增加, 说明改性后生物炭表面引入了含N和含O官能团.结合图 2的FTIR分析结果, CBC中的酰胺基(NH2—C=O)和酚羟基(C—OH)吸收峰面积都有明显增加, 说明引入了具有孤对电子的基团(C=N:和C=O:), 加强了与Cd2+离子的配位作用.此外, CBC具有相对集中的芳香化结构, 具有π电子, 双键的引入加强了π电子云密度, 而Cd2+离子具有空的d轨道, 两者可以形成紧密的共价电子云结构, 即阳离子—π键作用.阳离子交换也被认为是生物炭吸附Cd2+的主要机制[40].由EDS分析结果[图 1(e)和1(f)], 改性后CBC中的Na、Mg和Ca含量较BC明显增加, 离子交换能力也有所增强[41].在XPS全谱图中, 改性后在399.81 eV新增N 1s峰[图 3(a)], 这归因于壳聚糖表面的—NH2基团[图 3(e)], 结合Zeta电位测定结果[图 4(b)], 改性后Zeta零电位点升高, 这可能是由于氨基质子化引起的, 表明生物炭表面接枝了—NH2基团, 进一步证实了壳聚糖负载成功[19].吸附Cd2+后出现了一个新的峰Cd 3d(405 eV)[图 3(b)], 表明CBC成功吸附Cd2+.在C 1s谱图中[图 3(e)], C—C/C=C基团结合能和峰面积基本不变, C—O基团峰面积增大, 而C=O基团峰面积减小, 表明在吸附Cd2+的过程中, 含氧官能团参与反应, 碳氧双键断裂, 碳氧单键形成[42].同时, C—O和C=O的结合能分别增加了0.47 eV和0.75 eV, 碳结合能的增强表明, CBC对Cd 2+的吸附受π电子离域的影响[43].在O 1s谱图中[图 3(c)和3(d)], C—O基团峰面积从59.24%增加至61.84%, 而C=O基团峰面积从40.76%减小至38.16%, 表明含氧官能团在吸附过程中起着主要作用.N 1s和O 1s结合能增加[图 3(e)~3(h)], 这表明酰胺基(N—C=O)是CBC吸附Cd2+过程中起关键作用的官能团, 形成了XN—金属配合物.此外, 吸附Cd2+后出现了Cd 3d5/2(412.65 eV)和Cd 3d3/2(406.08 eV)[图 3(b)], 对应峰面积为54.97%和45.03%, 这与Yu等[44]的研究结果相似, 表明吸附后的Cd2+以CdO和Cd(OH)2形式存在, 其中以CdO为主, 说明沉淀作用机制的存在.综上, CBC对Cd2+的吸附作用机制主要为配位作用、表面沉淀作用、离子交换作用和阳离子—π键作用.
吸附等温线和动力学实验结果表明, CBC对Cd2+的吸附符合Langmuir等温模型和准二级动力学模型, 说明吸附过程以化学吸附为主, 物理吸附为辅.改性后颗粒内扩散模型kd1增大, 表明CBC与Cd2+的结合更迅速, 最大吸附容量提高了107.12 %, 达到38.67 mg·g-1(25℃).与其它相关研究比较, 吸附容量高于KOH改性花旗松生物炭(29.0 mg·g-1)[45]、碱和磁复合改性小麦秸秆生物炭(23.44 mg·g-1)[2]和稻草秸秆生物炭(7.49 mg·g-1) [46]等吸附材料, 这主要得益于猕猴桃枝富含酚酸类和酮类等活性物质[8], 为吸附重金属离子提供了更多的吸附活性位点, 壳聚糖的负载使其吸附容量和稳定性进一步增强.由此可见, 与其它农林废弃物相比猕猴桃枝是一种有价值的生物质原料, 壳聚糖改性生物炭对Cd2+的去除具有明显优势.然而, 由于矿物含量低和比表面积较小, CBC的吸附容量低于含Fe[11, 33]、Mg[41]和S[27]等改性生物炭材料, 未来将继续探索提高CBC的吸附容量和稳定性, 及其在水体和土壤环境中的实际应用问题, 为其推广和实际应用提供理论依据.
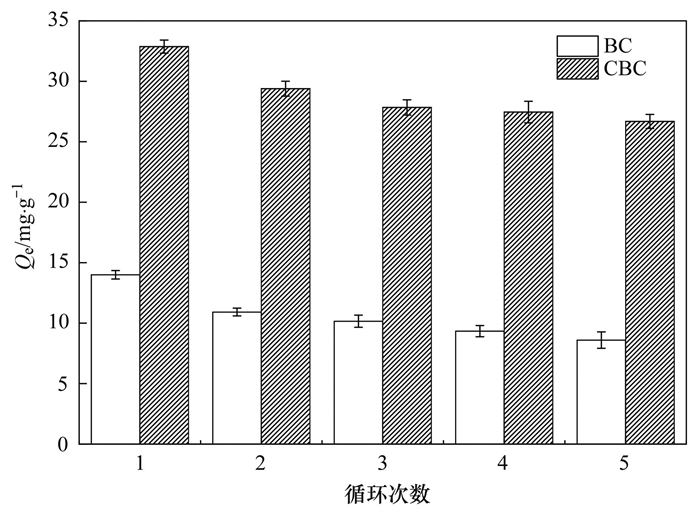
2.4 吸附再生实验为了评价改性前后生物炭的稳定性和实用性.用0.05 mol·L-1乙二胺四乙酸钠(Na2EDTA)溶液作为洗脱液进行吸附再生实验.如图 9所示, BC和CBC的吸附量在每一次连续循环中都在下降, 这可能是由于未解吸Cd2+占据了一定比例的吸附位点, 以及材料表面积和官能团强度的减少所致[35, 43].进行连续5次吸附-解吸循环后, BC和CBC对Cd2+的吸附量分别为8.60和23.54 mg·g-1, 保持在第1次吸附量的61.4%和81.2%, 可见壳聚糖的负载可以提升生物炭的重复利用性能.此外, 壳聚糖包覆还可以阻碍木质素分子的分解, 提高生物炭的稳定性.且改性过程绿色环保, 主要体现在改性剂、改性过程和改性材料的应用均不会引入二次污染.综上, 壳聚糖改性生物炭具有吸附速率快、吸附稳定性好, 且制备工艺简单、经济环保的特点, 可作为水体和土壤环境中Cd2+的高效吸附剂.
|
图 9 循环次数对改性前后生物炭吸附Cd2+的影响 Fig. 9 Effect of adsorption-desorption cycles on adsorption capacities of Cd2+ by BC and CBC |
(1) 以猕猴桃枝生物炭为基体材料, 利用壳聚糖改性, 制备了壳聚糖改性生物炭复合材料(CBC).SEM-EDS、FTIR和XPS表征分析结果证明了壳聚糖成功负载到生物炭表面, 改性后生物炭表面的氨基(—NH2)、酚羟基(—C—OH)和羧基(—COOH)等官能团可作为配体增强对Cd2+的吸附容量和吸附稳定性.
(2) 准二级动力学模型能更好描述CBC对Cd2+的吸附过程, 即吸附速率由吸附材料表面活性位点决定.颗粒内扩散模拟结果显示, 吸附过程分为外层扩散和颗粒内扩散两个阶段, 拟合直线不过原点, 说明吸附受多种机制的影响, CBC对Cd2+的主要吸附机制为配位作用、表面沉淀作用、离子交换作用和阳离子—π键作用.
(3) CBC对Cd2+的吸附过程更好地符合Langmuir等温模型, 说明单分子层的化学吸附起主要作用.分离因子RL和1/n均小于未改性生物炭(BC), 且均远小于1, 表明CBC对Cd2+的吸附反应更容易进行.在25、35和45℃下, 吸附容量较改性前提升了107.12%、110.40%和109.63%.
(4) 吸附热力学结果显示, ∆Hθ和∆Sθ均为正值, ∆Gθ均为负值, 表明CBC对Cd2+吸附过程为吸热熵增加的自发过程, 高温有利于吸附.
| [1] | 环境保护部, 国土资源部. 全国土壤污染状况调查公报[EB/OL]. http://www.gov.cn/foot/2014-04/17/content_2661768.htm, 2022-09-15. |
| [2] |
崔志文, 任艳芳, 王伟, 等. 碱和磁复合改性小麦秸秆生物炭对水体中镉的吸附特性及机制[J]. 环境科学, 2020, 41(7): 3315-3325. Cui Z W, Ren Y F, Wang W, et al. Adsorption characteristics and mechanism of cadmium in water by alkali and magnetic composite modified wheat straw biochar[J]. Environmental Science, 2020, 41(7): 3315-3325. |
| [3] |
覃建军, 唐盛爽, 蒋凯, 等. 螯合剂GLDA对象草修复镉污染农田的影响[J]. 环境科学, 2020, 41(8): 3862-3869. Qin J J, Tang S S, Jiang K, et al. Effects of chelate GLDA on the remediation of cadmium contaminated farmland by Pennisetum purpureum schum[J]. Environmental Science, 2020, 41(8): 3862-3869. |
| [4] |
王鑫宇, 孟海波, 沈玉君, 等. 改性生物炭特性表征及对冶炼厂周边农田土壤铜镉形态的影响[J]. 环境科学, 2021, 42(9): 4441-4451. Wang X Y, Meng H B, Shen Y J, et al. Characteristics of modified biochars and their immobilization effect on Cu and Cd in polluted farmland soil around smelter[J]. Environmental Science, 2021, 42(9): 4441-4451. |
| [5] |
闵炳坤, 李坤权. 高比表面硫脲改性花生壳炭的制备及对四环素和铜的吸附[J]. 环境科学, 2023, 44(3): 1528-1536. Min B K, Li K Q. Preparation of high specific surface thiourea modified peanut shell carbon and adsorption of tetracycline and copper[J]. Environmental Science, 2023, 44(3): 1528-1536. |
| [6] |
毕景望, 单锐, 韩静, 等. 改性西瓜皮生物炭的制备及其对Pb(Ⅱ)的吸附特性[J]. 环境科学, 2020, 41(4): 1770-1778. Bi J W, Shan R, Han J, et al. Preparation of modified watermelon biochar and its adsorption properties for Pb(Ⅱ)[J]. Environmental Science, 2020, 41(4): 1770-1778. |
| [7] |
龚沛云, 孙丽娟, 宋科, 等. 农业废弃物基生物炭对水溶液中镉的吸附效果与机制[J]. 环境科学, 2022, 43(6): 3211-3220. Gong P Y, Sun L J, Song K, et al. Adsorption capacity and mechanism of biochar derived from typical agricultural wastes for cadmium in aqueous solutions[J]. Environmental Science, 2022, 43(6): 3211-3220. |
| [8] |
任春燕, 郭堤, 刘翔宇, 等. 猕猴桃木生物质炭对溶液中Cd2+、Pb2+的吸附及应用研究[J]. 农业环境科学学报, 2019, 38(8): 1982-1990. Ren C Y, Guo D, Liu X Y, et al. Application of biochar derived from kiwi pruning branches for Cd2+ and Pb2+ adsorption in aqueous solutions[J]. Journal of Agro-Environment Science, 2019, 38(8): 1982-1990. |
| [9] | Fan H, Shen Z X, Wang X R, et al. Kiwi twig biochar recycling promoting the reduction of NO by a MnO2 catalyst[J]. Applied Surface Science, 2022, 596. DOI:10.1016/j.apsusc.2022.153644 |
| [10] | Hamid Y, Liu L, Usman M, et al. Functionalized biochars: synthesis, characterization, and applications for removing trace elements from water[J]. Journal of Hazardous Materials, 2022, 437. DOI:10.1016/j.jhazmat.2022.129337 |
| [11] | Chin J F, Heng Z W, Teoh H C, et al. Recent development of magnetic biochar crosslinked chitosan on heavy metal removal from wastewater-modification, application and mechanism[J]. Chemosphere, 2022, 291. DOI:10.1016/j.chemosphere.2021.133035 |
| [12] |
杨雪玲, 王明星, 徐国敏, 等. 壳聚糖改性生物炭对水稻土甲基汞生成及其稻米积累的影响[J]. 环境科学, 2021, 42(3): 1191-1196. Yang X L, Wang M X, Xu G M, et al. Effects of chitosan-modified biochar on formation of methylmercury in paddy soils and its accumulation in rice[J]. Environmental Science, 2021, 42(3): 1191-1196. |
| [13] | Xiang J X, Lin Q T, Yao X S, et al. Removal of Cd from aqueous solution by chitosan coated MgO-biochar and its in-situ remediation of Cd-contaminated soil[J]. Environmental Research, 2021, 195. DOI:10.1016/j.envres.2020.110650 |
| [14] | Fan S S, Fan X R, Wang S, et al. Effect of chitosan modification on the properties of magnetic porous biochar and its adsorption performance towards tetracycline and Cu2+ [J]. Sustainable Chemistry and Pharmacy, 2023, 33. DOI:10.1016/j.scp.2023.101057 |
| [15] | Zhang H, Xiao R, Li R H, et al. Enhanced aqueous Cr(Ⅵ) removal using chitosan-modified magnetic biochars derived from bamboo residues[J]. Chemosphere, 2020, 261. DOI:10.1016/j.chemosphere.2020.127694 |
| [16] | Wang H, Liu R R, Chen Q, et al. Biochar-supported starch/chitosan-stabilized nano-iron sulfide composites for the removal of lead ions and nitrogen from aqueous solutions[J]. Bioresource Technology, 2022, 347. DOI:10.1016/j.biortech.2022.126700 |
| [17] | Gao N, Du W Z, Zhang M Y, et al. Chitosan-modified biochar: preparation, modifications, mechanisms and applications[J]. International Journal of Biological Macromolecules, 2022, 209: 31-49. DOI:10.1016/j.ijbiomac.2022.04.006 |
| [18] | Boraah N, Chakma S, Kaushal P. Attributes of wood biochar as an efficient adsorbent for remediating heavy metals and emerging contaminants from water: a critical review and bibliometric analysis[J]. Journal of Environmental Chemical Engineering, 2022, 10(3). DOI:10.1016/j.jece.2022.107825 |
| [19] | Shi Y J, Hu H D, Ren H Q. Dissolved organic matter (DOM) removal from biotreated coking wastewater by chitosan-modified biochar: adsorption fractions and mechanisms[J]. Bioresource Technology, 2020, 297. DOI:10.1016/j.biortech.2019.122281 |
| [20] | Chen H B, Gao Y R, El-Naggar A, et al. Enhanced sorption of trivalent antimony by chitosan-loaded biochar in aqueous solutions: characterization, performance and mechanisms[J]. Journal of Hazardous Materials, 2022, 452. DOI:10.1016/j.jhazmat.2021.127971 |
| [21] | Zhang X B, Yang Y Y, Hao Ngo H, et al. Urea removal in reclaimed water used for ultrapure water production by spent coffee biochar/granular activated carbon activating peroxymonosulfate and peroxydisulfate[J]. Bioresource Technology, 2022, 343. DOI:10.1016/j.biortech.2021.126062 |
| [22] | Yang Y, Zhang Y H, Wang G Y, et al. Adsorption and reduction of Cr(VI) by a novel nanoscale FeS/chitosan/biochar composite from aqueous solution[J]. Journal of Environmental Chemical Engineering, 2021, 9. DOI:10.1016/j.jece.2021.105407 |
| [23] | Jiang L, Yi X, Yang K J, et al. Comparison of adsorption behavior of Pb(Ⅱ) by acid-alkali and chitosan modified biochar derived from kiwifruit branch[J]. Human and Ecological Risk Assessment: An International Journal, 2023, 29(2): 410-426. DOI:10.1080/10807039.2022.2098467 |
| [24] |
张瑶瑶, 姜凌, 李梦帆, 等. 氨基功能化微硅粉的制备及其对镉污染土壤的钝化效果研究[J]. 安全与环境学报, 2023, 23(4): 1270-1279. Zhang Y Y, Jiang L, Li M F, et al. Preparation of amino functionalized microsilica powder and its passivation effect on cadmium contaminated soil[J]. Journal of Safety and Environment, 2023, 23(4): 1270-1279. |
| [25] | Liu S, Li J H, Xu S, et al. A modified method for enhancing adsorption capability of banana pseudostem biochar towards methylene blue at low temperature[J]. Bioresource Technology, 2019, 282: 48-55. DOI:10.1016/j.biortech.2019.02.092 |
| [26] | Hu B W, Wang H F, Liu R R, et al. Highly efficient U(Ⅵ) capture by amidoxime/carbon nitride composites: evidence of EXAFS and modeling[J]. Chemosphere, 2021, 274. DOI:10.1016/j.chemosphere.2021.129743 |
| [27] | Wang G L, Yang R, Liu Y W, et al. Adsorption of Cd(Ⅱ) onto Auricularia auricula spent substrate biochar modiffed by CS2: characteristics, mechanism and application in wastewater treatment[J]. Journal of Cleaner Production, 2022, 367. DOI:10.1016/j.jclepro.2022.132882 |
| [28] |
肖芳芳, 张莹莹, 程建华, 等. 壳聚糖/磁性生物碳对重金属Cu(Ⅱ)的吸附性能[J]. 环境工程学报, 2019, 13(5): 1048-1055. Xiao F F, Zhang Y Y, Cheng J H, et al. Adsorption properties of chitosan/magnetic biochar for Cu(Ⅱ) removal from solution[J]. Chinese Journal of Environmental Engineering, 2019, 13(5): 1048-1055. |
| [29] |
汪存石, 何敏霞, 周峰, 等. 胺硫改性生物炭对水溶液中不同重金属离子的吸附特性及吸附稳定性[J]. 环境科学, 2021, 42(2): 874-882. Wang C S, He M X, Zhou F, et al. Heavy metal ion adsorption properties and stability of amine-sulfur modified biochar in aqueous solution[J]. Environmental Science, 2021, 42(2): 874-882. |
| [30] |
乔洪涛, 李海龙, 赵保卫, 等. 磁流体改性制备磁性肉骨生物炭及其对Cd2+的吸附特性[J]. 农业工程学报, 2021, 37(12): 199-206. Qiao H T, Li H L, Zhao B W, et al. Preparation of magnetic meat and bone meal biochar modified by magnetic fluid and its adsorption properties for Cd2+ [J]. Transactions of the Chinese Society of Agricultural Engineering, 2021, 37(12): 199-206. DOI:10.11975/j.issn.1002-6819.2021.12.023 |
| [31] | Huang Y J, Zhao W C, Zhang X, et al. Thiol-ene synthesis of thioether/carboxyl-functionalized polymers for selective adsorption of silver (I) ions[J]. Chemical Engineering Journal, 2019, 375. DOI:10.1016/j.cej.2019.121935 |
| [32] | Liu X, Sun J, Xu X T, et al. Adsorption and desorption of U(Ⅵ) on different-size graphene oxide[J]. Chemical Engineering Journal, 2019, 360: 941-950. DOI:10.1016/j.cej.2018.04.050 |
| [33] | Tian H R, Peng S C, Zhao L, et al. Simultaneous adsorption of Cd(Ⅱ) and degradation of OTC by activated biochar with ferrate: efficiency and mechanism[J]. Journal of Hazardous Materials, 2023, 447. DOI:10.1016/j.jhazmat.2022.130711 |
| [34] |
徐建玲, 张頔, 聂苗青, 等. PEI功能化秸秆生物炭对水中Cr6+的吸附性能[J]. 高等学校化学学报, 2020, 41(1): 155-161. Xu J L, Zhang D, Nie M Q, et al. Adsorption of Cr6+ on Polyethyleneimine-functionalized straw biochar from aqueous solution[J]. Chemical Journal of Chinese Universities, 2020, 41(1): 155-161. |
| [35] |
刘沁文, 丁爱中, 梁信, 等. 桉树生物炭负载绿色合成纳米零价铁去除水中Cr(Ⅵ)[J]. 环境科学, 2022, 43(12): 5657-5666. Liu Q W, Ding A Z, Liang X, et al. Removal of Cr(Ⅵ) from water using green synthesis nanoscale zero-valent iron supported on eucalyptus biochar[J]. Environmental Science, 2022, 43(12): 5657-5666. |
| [36] |
马文艳, 裴鹏刚, 高歌, 等. 微纳米粒径生物炭的结构特征及其对Cd2+吸附机制[J]. 环境科学, 2022, 43(7): 3682-3691. Ma W Y, Pei P G, Gao G, et al. Structural characteristics of micro-nano particle size biochar and its adsorption mechanism for Cd2+ [J]. Environmental Science, 2022, 43(7): 3682-3691. |
| [37] | Liu X J, Li M F, Ma J F, et al. Chitosan crosslinked composite based on corncob lignin biochar to adsorb methylene blue: Kinetics, isotherm, and thermodynamics[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2022, 642. DOI:10.1016/j.colsurfa.2022.128621 |
| [38] | Dong L J, Wu S Y, Li S B, et al. Sorption behaviors and mechanisms of Eu(Ⅲ) on rice straw-derived biochar[J]. Journal of Inorganic Materials, 2020, 35(3): 390-398. |
| [39] | Zhang L X, Tang S Y, He F X, et al. Highly efficient and selective capture of heavy metals by poly (acrylic acid) grafted chitosan and biochar composite for wastewater treatment[J]. Chemical Engineering Journal, 2019, 378. DOI:10.1016/j.cej.2019.122215 |
| [40] | Zhang J Z, Ma X F, Yuan L, et al. Comparison of adsorption behavior studies of Cd2+ by vermicompost biochar and KMnO4- modified vermicompost biochar[J]. Journal of Environmental Management, 2020, 256. DOI:10.1016/j.jenvman.2019.109959 |
| [41] | Wu J W, Wang T, Wang J W, et al. A novel modified method for the efficient removal of Pb and Cd from wastewater by biochar: enhanced the ion exchange and precipitation capacity[J]. Science of the Total Environment, 2021, 754. DOI:10.1016/j.scitotenv.2020.142150 |
| [42] | Wang T T, Sun Y C, Bai L, et al. Ultrafast removal of Cr(Ⅵ) by chitosan coated biochar-supported nano zero-valent iron aerogel from aqueous solution: application performance and reaction mechanism[J]. Separation and Purification Technology, 2023, 306. DOI:10.1016/j.seppur.2022.122631 |
| [43] | Ma W Y, Xu Y M, Zhou D M, et al. Development and optimization of high-performance nano-biochar for efficient removal Cd in aqueous: Absorption performance and interaction mechanisms[J]. Chemical Engineering Research and Design, 2023, 189: 516-529. DOI:10.1016/j.cherd.2022.11.051 |
| [44] | Yu X N, Zhou H J, Ye X F, et al. From hazardous agriculture waste to hazardous metal scavenger: tobacco stalk biochar-mediated sequestration of Cd leads to enhanced tobacco productivity[J]. Journal of Hazardous Materials, 2021, 413. DOI:10.1016/j.jhazmat.2021.125303 |
| [45] | Herath A, Layne C A, Perez F, et al. KOH-activated high surface area Douglas Fir biochar for adsorbing aqueous Cr(Ⅵ), Pb(Ⅱ) and Cd(Ⅱ)[J]. Chemosphere, 2021, 269. DOI:10.1016/j.chemosphere.2020.128409 |
| [46] |
王晓霞, 杨涛, 肖璐睿, 等. 稻草秸秆生物质炭对重金属Cd2+的吸附性能研究[J]. 环境科学学报, 2021, 41(7): 2691-2699. Wang X X, Yang T, Xiao L R, et al. Study on the adsorption performance of rice straw biomass charcoal to heavy metal Cd2+ [J]. Acta Scientiae Circumstantiae, 2021, 41(7): 2691-2699. |
 2024, Vol. 45
2024, Vol. 45


