2. 康达环保水务有限公司, 焦作 454000;
3. 中国科学院武汉植物园, 武汉 430074
2. Kangda Environmental Protection Water Co., Ltd., Jiaozuo 454000, China;
3. Wuhan Botanical Garden, Chinese Academy of Sciences, Wuhan 430074, China
2020年我国城市污水排放量为571亿m3, 处理量为557亿m3[1], 城市污水排放量占2020年全国35个主要河流代表站总径流量的3.4%[2], 超过2020年黄河年径流量(487亿m3, 花园口站)[2].生活污水是地表水环境氮和磷等营养元素的重要来源[3~5], 过量的氮磷会对地表水生态环境造成严重影响[6], 硝酸盐(NO3-)质量浓度增加造成水体富营养化, 饮用水中NO3-质量浓度过高导致高铁血红蛋白血症等疾病[5, 7].我国7.83%河流NO3-质量浓度超标(45 mg·L-1), 部分河流入海口NO3-质量浓度严重超标[5].《城镇污水处理厂污染物排放标准》(GB 18918-2002)仅针对氨氮(NH4+-N)和总氮(TN)排放标准进行限值, TN包含NH4+-N、亚硝酸盐氮(NO2--N)和硝酸盐氮(NO3--N), 以及部分有机氮(ON)[8].我国122家污水处理厂专项监测结果表明, 进水和出水ρ(NH4+-N)均值分别为27.4 mg·L-1和2.74 mg·L-1, 而ρ(TN)均值分别为39.5 mg·L-1和16.5 mg·L-1[9], TN去除率远低于NH4+-N去除率, 出水中NO3-是重要的TN组分.因此生活污水作为地表水NO3-重要来源, 其NO3-质量浓度水平是重要考量因素.
硝酸盐氮和氧同位素(δ15N-NO3-和δ18O-NO3-)已经广泛用于辨识地表水和地下水系统NO3-来源[10~12], 基于不同NO3-来源的δ15N-NO3-和δ18O-NO3-存在显著差异.例如, 生活污水和粪肥中含有大量铵盐, 铵盐挥发造成剩余铵盐氮同位素值(δ15N-NH4+)升高, 发生硝化作用后, 造成产物NO3-的δ15N-NO3-较高(7‰~20‰)[4, 13].化学肥料中NO3-的δ15N-NO3范围为0‰~3‰[13], 土壤有机氮矿化产生NO3-的δ15N-NO3-范围为-3‰~5‰[13], 大气降水中NO3-的δ15N-NO3-范围为-10‰~8‰[13].因此如果不考虑显著NO3-反硝化过程影响, 受生活污水和粪肥显著影响的水体其δ15N-NO3-普遍较高[10, 14].随着城市污水管网不断完善, 污水得到妥善处理, 大量NH4+-N转变为NO3--N.因此弄清楚污水硝酸盐同位素的受控机制, 明确污水厂出水NO3-浓度, δ15N-NO3-和δ18O-NO3-信号, 对准确解析其对河流和地下水NO3-的贡献有重要意义.我国地表水δ15N-NO3-和δ18O-NO3-特征范围分别为-23.5‰~27.0‰和-12.7‰~83.5‰[5], 生活污水处理厂出水作为地表水重要NO3-来源, 其δ15N-NO3-和δ18O-NO3-组成如表 1所示.
|
|
表 1 国内外污水处理厂出水NO3-浓度及δ15N-NO3-和δ18O-NO3-组成特征1) Table 1 Effluent nitrate concentrations and nitrogen and oxygen isotope composition characteristics in domestic and foreign WWTP |
国内外针对污水处理工艺影响δ15N-NO3-和δ18O-NO3-组成的研究不多.前人对日本东京地区污水厂研究结果表明, 从污水厂进水, 经厌氧-缺氧-好氧处理后, 铵盐的氮同位素(δ15N-NH4+)在好氧阶段显著增加[18], 但δ15N-NO3-在厌氧和缺氧阶段降低, 在好氧阶段又增加, δ18O-NO3-值在缺氧阶段逐渐增加, 在好氧阶段显著降低[18].对北京某污水处理厂的研究表明, 进水ρ(NH4+-N)均值为31.2 mg·L-1, 出水ρ(NH4+-N)均值降为2.3 mg·L-1, 但ρ(NO3--N)均值由1.1 mg·L-1增加至9.6 mg·L-1[26].进水δ15N-NO3-和δ18O-NO3-组成范围较大, 分别为2.7‰~23.5‰和3.3‰~14.0‰, 出水δ15N-NO3-和δ18O-NO3-组成相对稳定, 均值分别为14.3‰和6.7‰[26].污水处理厂处理工艺多样, 对δ15N-NO3-和δ18O-NO3-组成的影响比较复杂, 一次采样工作很难揭示其动态影响.同时生活污水水质复杂, 不同时段来水成分有所差异.针对这些问题, 在前人研究基础上, 选择目前较多污水处理厂采用的厌氧-缺氧-好氧工艺(anaerobic-anoxic-oxic, A2O), 增加采样频次, 通过长时间周期内多次采样, 试图说明污水厂处理工艺对出水NO3-浓度以及δ15N-NO3-和δ18O-NO3-组成的影响, 最后给出一个污水处理厂出水δ15N-NO3-和δ18O-NO3-组成特征, 以期在接下来的地表水NO3-来源辨识工作, 借助这一组成特征, 量化生活污水对地表水NO3-的贡献比例.
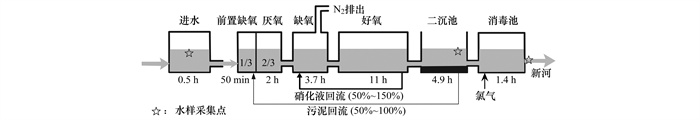
1 材料与方法 1.1 污水处理厂脱氮工艺焦作污水处理厂污水来自于城区居民生活污水, 服务人口65万人, 污水处理能力为10万m3·d-1.该污水处理厂采用A2O工艺(图 1), 去除生活污水中有机物以及含氮化合物.污水在厌氧池停留时间约为2 h, 在缺氧池停留时间约3.7 h, 在好氧池停留时间约为11 h, 经过处理后的生活污水进入二次沉淀池, 清水经消毒后达标排放(图 1).一部分污泥重新回流到厌氧池用于降解有机物, 一部分好氧池硝化液重新回流到缺氧池, 去除有机物和含氮化合物(图 1).
|
图 1 焦作市污水处理厂处理工艺流程和水样布点情况 Fig. 1 Schematic map of waste water treatment and the water sample sites in the Jiaozuo WWTP |
污水处理厂对含氮化合物的去除工艺主要有: 好氧硝化作用、厌氧氨氧化作用、厌氧异养反硝化作用和厌氧自养反硝化作用[22, 28, 29].反应方程式如式(1)~(4)所示:
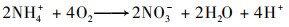
|
(1) |
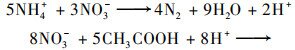
|
(2) |
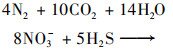
|
(3) |
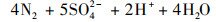
|
(4) |
污水处理厂进水含氮化合物以NH4+-N为主[26], 一部分氨氮经厌氧池和缺氧池后进入好氧池(图 1), 经过好氧硝化作用[公式(1)], 转变为NO3--N.因此在二沉池出水处应该检测到高浓度的NO3--N, 一部分NO3--N重新回流到缺氧池, 发生异养反硝化和自养反硝化, 转变为N2排入大气中(图 1).
1.2 样品收集与处理2021年12月收集污水处理厂进水口、二沉池出水口和总出水口水样(图 1), 每隔8 h在3个地点分别采集水体样品, 连续采集3 d.样品采集后, 现场测定水体温度、pH、电导率(EC)和溶解氧浓度(DO), 分别用便携式pH计、EC仪和DO仪测定(上海三信仪表厂, 型号分别为SX811, SX813和SX816), 测试精度分别优于0.1, 0.1 μS·cm-1和0.1 mg·L-1.水样经0.22 μm孔径聚醚砜滤膜(PES, 天津市津腾实验设备有限公司)过滤后, 分别置于50 mL聚丙烯塑料离心管(PP, Thermo Scientific)和10 mL棕色玻璃瓶, 分别用于测定NH4+、NO3-、δ15N-NO3-和δ18O-NO3-组成.
1.3 样品测试及分析NH4+浓度采用纳氏试剂比色法测定[30], NO3-浓度采用离子色谱法测定[31], 最低检出浓度均为0.05 mg·L-1.δ15N-NO3-和δ18O-NO3-组成采用镀铜镉粒还原+叠氮化钠化学转化法+同位素质谱仪方法测定[32], 首先确保待测液体NO3-量浓度控制在20 μmol·L-1以下, 取5 mL待测液体置于7 mL圆底离心管内, 加入约0.6 g左右的镀铜镉粒(0.3~0.8 mm, 北京朋利驰科技有限公司), 振荡反应10 h.吸取4 mL上清液置于12 mL玻璃顶空瓶内(Labco Limited, Lampeter, UK), 用高纯氦气吹扫后, 加入1 mL叠氮化钠和乙酸混合溶液, 振荡反应4 h, 加入1 mL氢氧化钠溶液(6mol·L-1)终止反应.产生的N2O气体经痕量气体预浓缩装置(Precon, Thermo Scientific, USA)导入多用途气体制备装置(Gasbench Ⅱ, Thermo Scientific, USA), 由氦气携带进入稳定同位素质谱仪(MAT253, Thermo Scientific, USA), 测定N2O的δ15N和δ18O组成.采用国际标准USGS 34(δ15N=-1.8‰, δ18O=-27.9‰), USGS 32(δ15N=180‰, δ18O=25.7‰), IAEA-NO3(δ15N=4.7‰, δ18O=25.6‰)和室内KNO3标准(CAS 7757-79-1, 上海阿拉丁生化科技股份有限公司)校准试验样品, 测试精度分别优于0.3‰和0.5‰. NH4+和NO3-浓度测定以及δ15N-NO3-和δ18O-NO3-组成测定均在河南理工大学生物遗迹与成矿过程省级重点实验室完成.
1.4 统计与分析数据统计和分析利用软件OriginPro 2021(Northampton, Massachusetts, USA)完成, 其中不同采样点测试指标之间的对比分析借助OriginPro 2021软件中单因素方差分析(ANOVA)和t检验功能完成.
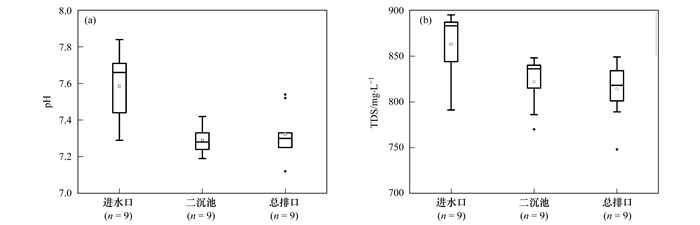
2 结果与分析 2.1 pH和TDS污水厂进水、二沉池出水以及总排口出水pH均值分别为(7.6±0.2)、(7.3±0.1)和(7.3±0.1) [图 2(a)].污水厂进水pH与二沉池出水和总排口出水pH存在显著差异(P < 0.05), 二沉池出水和总排口出水pH不存在显著差异(P > 0.05) [图 2(a)].TDS均值分别为(862±36)、(822±28)和(814±32)mg·L-1 [图 2(b)].污水厂进水TDS与二沉池出水和总排口出水TDS存在显著差异(P < 0.05) [图 2(b)], 二沉池出水TDS与总排口出水TDS不存在显著差异(P > 0.05) [图 2(b)].
|
图 2 焦作污水处理厂不同采样点水体pH和TDS变化情况 Fig. 2 Variations in pH and TDS values of water sampled at three different sites in the Jiaozuo WWTP |
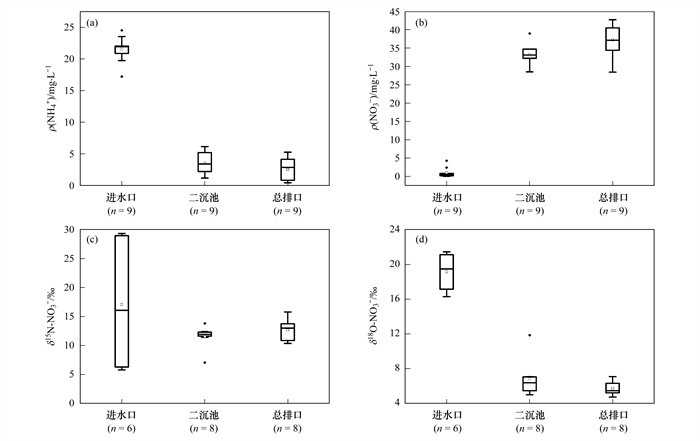
污水厂进水、二沉池出水和总排口出水ρ(NH4+)均值分别为(22.86±2.16)、(3.78±1.98)和(2.70±1.98)mg·L-1[图 3(a)].污水厂进水NH4+浓度与二沉池出水和总排口出水NH4+浓度存在显著差异(P < 0.05), 但后者之间差异不显著(P > 0.05)[图 3(a)].污水厂进水NO3-质量浓度不符合正态分布(P < 0.05), ρ(NO3-)中间值为0.62 mg·L-1, 二沉池出水以及总排口出水NO3-质量浓度符合正态分布(P>0.05), ρ(NO3-)均值分别为(33.48±3.10)和(37.20±4.34)mg·L-1 [图 3(b)].污水厂进水NO3-浓度与二沉池出水和总排口出水NO3-浓度存在显著差异(P < 0.05), 同时后者之间也存在显著差异(P < 0.05)[图 3(b)].
|
图 3 焦作污水处理厂不同采样点水体NH4+浓度和NO3-浓度以及δ15N-NO3-和δ18O-NO3-组成变化情况 Fig. 3 Variations in NH4+ concentrations, NO3- concentrations, δ15N-NO3-, and δ18O-NO3- ratios of water sampled at three different sites in the Jiaozuo WWTP |
污水厂进水δ15N-NO3-和总排口出水δ15N-NO3-符合正态分布(P>0.05), 均值分别为(17.1±10.7)‰和(12.6±1.9)‰[图 3(c)].二沉池出水δ15N-NO3-不符合正态分布(P < 0.05), 中间值为11.9‰, 三者之间不存在显著差异(P > 0.05)[图 3(c)].污水厂进水δ18O-NO3-和总排口出水δ18O-NO3-符合正态分布(P > 0.05), 均值分别为(19.2±2.2)‰和(5.7±0.8)‰[图 3(d)].二沉池出水δ18O-NO3-不符合正态分布(P < 0.05), 中间值为6.4‰, 污水厂进水δ18O-NO3-与二沉池出水和总排口出水δ18O-NO3-存在显著差异(P < 0.05), 但后者之间不存在显著差异(P>0.05)[图 3(d)].
3 讨论 3.1 污水处理厂铵盐硝化过程和硝酸盐反硝化过程焦作污水处理厂12月进水ρ(NH4+)范围为18.18~25.92 mg·L-1, 接近北京地区污水处理厂12月进水ρ(NH4+)(26.64 mg·L-1)[26].二沉池出水ρ(NH4+)范围为1.26~6.48 mg·L-1, 总排口出水ρ(NH4+)范围为0.54~5.58 mg·L-1, 与北京地区污水处理厂12月出水ρ(NH4+)(1.08 mg·L-1)接近[26].焦作污水处理厂进水NH4+去除率在88%左右, 总排口出水NH4+浓度基本符合《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准(5 mg·L-1).
污水厂进水NH4+经过A2O处理工艺后, 发生硝化作用, 大部分NH4+转变为NO3-.二沉池出水ρ(NO3-)范围为28.52~39.06 mg·L-1, 总排口出水ρ(NO3-)范围为28.52~42.78 mg·L-1, 低于北京地区污水厂12月出水ρ(NO3-)(96.72 mg·L-1)[26], 与该污水处理厂全年出水ρ(NO3-)均值(42.78 mg·L-1)相当[26].进水NH4+在好氧池发生硝化作用[公式(1)], 产生H+, 导致水体pH降低[图 2(a)].NH4+如果全部转化为NO3-, 则产生的ρ(NO3-)均值应该在78.74 mg·L-1左右, 但实际二沉池出水ρ(NO3-)均值仅为33.48 mg·L-1左右, 这与好氧池硝化液回流至缺氧池进行反硝化作用有关[公式(2)~(4), 图 1], 部分NO3-经过反硝化作用降解为N2进入大气.
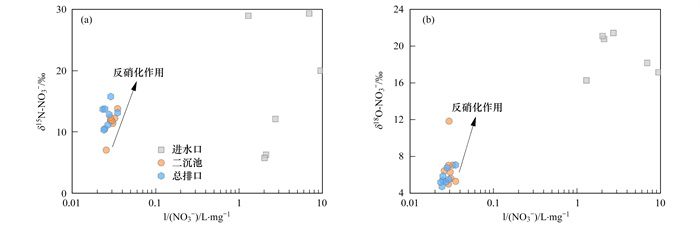
由图 4可以看出, 污水处理厂二沉池出水以及总排口出水水体经历硝酸盐反硝化过程, 随着NO3-质量浓度降低, δ15N-NO3-和δ18O-NO3-组成逐渐增加.污水处理厂进水δ15N-NO3-和δ18O-NO3-组成与之存在较大差异, 说明没有经过处理的生活污水硝酸盐δ15N-NO3-和δ18O-NO3-组成更为复杂.
|
图 4 污水处理厂不同采样点水体NO3--N浓度与δ15N-NO3-, NO3--N浓度与δ18O-NO3-关系 Fig. 4 Relations among NO3--N concentrations, δ15N-NO3-, and δ18O-NO3- ratios of waste water samples at different sites in the WWTP |
总排口出水NH4+和NO3-浓度与二沉池出水NH4+和NO3-浓度均值比较发现, ρ(NH4+)均值降低1.08 mg·L-1, 但ρ(NO3-)均值增加3.72 mg·L-1, 这说明后续消毒工序加入的氧化剂将部分NH4+氧化为NO3-.
3.2 污水处理厂δ15N-NO3-和δ18O-NO3-分馏及影响因素 3.2.1 污水处理厂硝化过程与氮同位素分馏污水处理厂作为氨硝化过程以及硝酸盐反硝化过程的典型场所, 其分馏机制是影响污水厂出水δ15N-NO3-和δ18O-NO3-组成的重要因素.硝化过程氨氧化为亚硝酸盐阶段氮同位素富集系数范围为14‰~38‰[33]; 亚硝酸盐转为硝酸盐阶段氮同位素富集系数范围为-20‰~-9‰[33], 氧同位素富集系数范围为-8‰~-1‰[34].如硝化过程氨全部转化为硝酸盐, 则氮同位素分馏程度很小, 氧同位素值与参与氧化的水氧同位素值和空气氧同位素值及其比例有关[34].本研究未测试污水厂进水δ15N-NH4+, 前人研究结果表明, 从进水到好氧池, 污水NH4+浓度呈现降低趋势, 但δ15N-NH4+呈现升高趋势[18], 这说明氨氧化过程优先利用富集14N的铵盐, 该铵盐全部转化为NO3-则导致产物δ15N-NO3-低于剩余铵盐的δ15N-NH4+[18].本研究中二沉池出水δ15N-NO3-范围为7.0‰~13.8‰, 中间值为11.9‰, 二沉池出水中仍检测到NH4+浓度, 因此笔者推测污水厂进水δ15N-NH4+均值应该高于11.9‰, 同时二沉池出水δ15N-NH4+均值应该更高, 比如前人研究好氧池中出水δ15N-NH4+高于20‰[18], 并且总排口出水δ15N-NH4+也较高(15‰左右)[18].虽然经过A2O处理后, 废水中NH4+浓度已经显著降低, 但其δ15N-NH4+较高.故如果剩余NH4+继续氧化, 则产生的NO3-具有较高的δ15N-NO3-.这一点在本研究中二沉池出水至总排口出水δ15N-NO3-变化可以验证, 因为随着NH4+浓度的持续降低, δ15N-NO3-呈现略微升高的趋势[图 3(c)].
3.2.2 污水处理厂硝化过程与氧同位素分馏好氧阶段由NH4+氧化而成的NO3-具有较低的δ18O-NO3-组成.本研究二沉池出水δ18O-NO3-范围为5.0‰~11.8‰, 中间值为6.4‰, 显著低于进水口δ18O-NO3-组成(均值为19.2‰) [图 3(d)].前述提及进水口δ18O-NO3-较高, 可能与污水在运输过程中发生反硝化过程有关.进水ρ(NO3-)均值仅为1.24 mg·L-1, 二沉池出水ρ(NO3-)均值为33.48 mg·L-1, 进水硝酸盐浓度占比仅4%左右.即使进水硝酸盐能够保持到好氧池, 对好氧池硝酸盐δ18O-NO3-组成的影响只有0.8‰的贡献.好氧池中硝化作用产生的硝酸盐的δ18O-NO3-组成主要受硝化过程中中间产物亚硝酸盐与水氧之间同位素平衡分馏, 水和空气氧参与比例及氧同位素分馏控制[22].
如果按照水和空气氧气2∶1比例进行计算的话, 研究区污水厂进水δ18O-H2O在-8‰左右(未发表数据), 空气氧气的δ18O-O2为23.5‰左右[35], 不考虑分馏, 则产物硝酸盐的δ18O-NO3-约为2.7‰.本研究二沉池出水δ18O-NO3-在6.4‰, 高于理论值2.7‰.这与前人研究结果相反[22], 前人研究结果表明污水厂出水δ18O-NO3-实测值要低于计算值, 原因与前述提及的亚硝酸盐与水氧之间的同位素平衡分馏以及亚硝酸盐到硝酸盐过程中水氧参与反应有关.最终产物硝酸盐的δ18O-NO3-可以由方程式(5)计算得出[22, 36]:
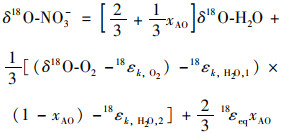
|
(5) |
式中, xAO表示与水氧进行氧平衡交换的亚硝酸盐的比例, 文献[37]报道该值为0.74. 18εk, O2与18εk, H2O, 1之和为7.5‰[37], 18εk, H2O, 2为22.5‰[37], 18εeq为13‰[37].根据上述参数, 计算得出硝化过程产生硝酸盐的δ18O-NO3-约为-7.6‰左右, 显然该计算值远低于实测二沉池出水硝酸盐的δ18O-NO3-.对计算值与实测值进行独立性t检验, 结果表明在0.05水平下, 总体均值与检验均值存在显著性差异.
3.2.3 污水处理厂反硝化过程与氧同位素分馏铵盐硝化过程产生的δ18O-NO3-在不考虑氧同位素分馏时理论值为2.7‰, 如果考虑氧同位素分馏时理论值为-7.6‰左右, 与实际二沉池出水δ18O-NO3-均值(6.4‰)存在差异, 二沉池出水δ18O-NO3-均值升高可能是反硝化作用导致.根据前述内容, 好氧池产生的硝化液回流至缺氧池, 进行反硝化作用, 结果会降低硝酸盐浓度, 而剩余硝酸盐的δ18O-NO3-会升高.硝酸盐反硝化作用造成的分馏符合瑞利分馏模型, 如公式(6)所示[22]:
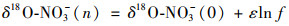
|
(6) |
式中, n表示剩余硝酸盐, 0表示初始硝酸盐, ε表示富集系数, f表示剩余硝酸盐的比例.前人对污水处理厂反硝化过程研究表明, ε范围为-0.4‰~-5.1‰, 均值为-2.9‰[22], 该值远低于自然界中已经报道的富集系数范围[22, 38], 如Kobayashi等[29]总结硝酸盐到亚硝酸盐过程氧同位素富集系数范围为-25‰~-15‰, 亚硝酸盐到氮气过程氧同位素富集系数范围为-6‰~-2‰.污水厂硝酸盐反硝化时间长度可能是影响氧同位素富集系数的重要因素[22].
本研究污水厂进水ρ(NH4+)均值为22.86 mg·L-1, 二沉池出水ρ(NH4+)均值为3.78 mg·L-1, 占比为17%.假定83%的进水NH4+全部转变为NO3-, 则好氧池内ρ(NO3-)均值为65.72 mg·L-1, 实际二沉池出水ρ(NO3-)均值33.48 mg·L-1, 则NO3-去除效率为51%.结合公式(6), 选择氧同位素富集系数为-2.9‰, 可以计算得出硝化过程产生的理论δ18O-NO3-值(-7.6‰)在经历反硝化过程后, 剩余硝酸盐的δ18O-NO3-均值应为-5.2‰左右.但如果选择自然界反硝化过程氧同位素富集系数-19‰左右, 则剩余硝酸盐的δ18O-NO3-均值为6.2‰左右, 与二沉池出水δ18O-NO3-均值(6.4‰)接近.由此可见, 污水厂反硝化过程氧同位素富集系数对剩余硝酸盐δ18O-NO3-均值影响较大.由表 1可以看出, 国内外其他地区污水处理厂出水硝酸盐的δ18O-NO3-范围为-10‰~9.3‰, 本研究结果与北京污水处理厂出水硝酸盐的δ18O-NO3-范围比较接近, 说明污水厂处理工艺对硝酸盐δ18O-NO3-的影响机制比较复杂.由于厌氧氨氧化过程[公式(2)]也会降低硝酸盐浓度, 但氧同位素富集系数仍不清楚[29].
3.3 污水处理厂出水δ15N-NO3-和δ18O-NO3-组成由图 4可以看出, 污水处理厂进水δ15N-NO3-和δ18O-NO3-组成与二沉池出水和总排口出水δ15N-NO3-和δ18O-NO3-组成存在较大差异.借助δ15N-NO3-和δ18O-NO3-组成辨识生活污水对自然水体硝酸盐贡献时, 需要明确生活污水是否经过污水处理厂处理, 因为没有经过处理的生活污水硝酸盐可能具有更高δ18O-NO3-组成, 但经过处理的生活污水中硝酸盐δ18O-NO3-组成降低.根据本研究结果, 污水处理厂排出的生活污水硝酸盐的δ15N-NO3-和δ18O-NO3-组成分别为12.6‰±1.9‰和5.7‰±0.8‰, 可以用贝叶斯同位素混合模型, 计算经过处理后的生活污水对地表水或地下水硝酸盐的贡献比例.
4 结论(1) 污水处理厂进水具有较高的氨氮含量和较低的硝态氮含量, 出水氨氮含量降低显著, 硝态氮含量升高.
(2) 污水处理厂好氧阶段硝化作用将氨氮转化为硝态氮, 引起硝态氮氧同位素值降低, 厌氧和缺氧阶段发生反硝化过程, 引起硝态氮氧同位素值升高.
(3) 污水处理厂二沉池后面的处理工序对出水硝酸盐浓度和同位素组成影响不大.污水处理厂出水硝酸盐δ15N-NO3-和δ18O-NO3-组成分别为12.6‰±1.9‰和5.7‰±0.8‰, 可以用在贝叶斯同位素混合模型中, 计算经过处理后的生活污水对地表水或地下水硝酸盐的贡献比例.
| [1] | 《净水技术》编辑部. 2020年建设统计数据(污排水部分)发布[J]. 净水技术, 2021, 40(12): 126. |
| [2] | 水利部水文司. 2020年度《中国河流泥沙公报》发布[J]. 水资源开发与管理, 2021(9): 2. |
| [3] |
赵然, 韩志伟, 田永著, 等. 岩溶流域地表水和地下水硝酸盐来源定量识别[J]. 中国环境科学, 2020, 40(4): 1706-1714. Zhao R, Han Z W, Tian Y Z, et al. Quantitative identification of nitrate source of surface water and groundwater in karst basin[J]. China Environmental Science, 2020, 40(4): 1706-1714. DOI:10.3969/j.issn.1000-6923.2020.04.038 |
| [4] |
张东, 杨伟, 赵建立. 氮同位素控制下黄河及其主要支流硝酸盐来源分析[J]. 生态与农村环境学报, 2012, 28(6): 622-627. Zhang D, Yang W, Zhao J L. Tracing nitrate sources of the Yellow River and its tributaries with nitrogen isotope[J]. Journal of Ecology and Rural Environment, 2012, 28(6): 622-627. DOI:10.3969/j.issn.1673-4831.2012.06.003 |
| [5] |
张鑫, 张妍, 毕直磊, 等. 中国地表水硝酸盐分布及其来源分析[J]. 环境科学, 2020, 41(4): 1594-1606. Zhang X, Zhang Y, Bi Z L, et al. Distribution and source analysis of nitrate in surface waters of China[J]. Environmental Science, 2020, 41(4): 1594-1606. DOI:10.3969/j.issn.1000-6923.2020.04.026 |
| [6] |
赵晨辰, 张世彦, 毛献忠. 深圳湾流域TN和TP入海年通量变化规律研究[J]. 环境科学, 2014, 35(11): 4111-4117. Zhao C C, Zhang S Y, Mao X Z. Variations of annual load of TN and TP in the deep bay watershed, Shenzhen[J]. Environmental Science, 2014, 35(11): 4111-4117. DOI:10.13227/j.hjkx.2014.11.010 |
| [7] | Hord N G. Dietary nitrates, nitrites, and cardiovascular disease[J]. Current Atherosclerosis Reports, 2011, 13(6): 484-492. DOI:10.1007/s11883-011-0209-9 |
| [8] |
刘倩. 连续流动分析法同时测定污水中总氮、氨氮、亚硝酸盐氮、硝酸盐氮[J]. 工业水处理, 2009, 29(8): 72-74. Liu Q. Simultaneous determination of the total nitrogen, ammonium-nitrogen, nitrite-nitrogen, and nitrate-nitrogen in wastewater by continuous fluxion analysis[J]. Industrial Water Treatment, 2009, 29(8): 72-74. DOI:10.3969/j.issn.1005-829X.2009.08.021 |
| [9] |
赵银慧, 李莉娜, 景立新, 等. 污水处理厂氮排放特征[J]. 中国环境监测, 2015, 31(4): 58-61. Zhao Y H, Li L N, Jing L X, et al. Study on the characteristic of the sewage plant emitting ammonia nitrogen[J]. Environmental Monitoring in China, 2015, 31(4): 58-61. DOI:10.3969/j.issn.1002-6002.2015.04.010 |
| [10] |
傅雪梅, 孙源媛, 苏婧, 等. 基于水化学和氮氧双同位素的地下水硝酸盐源解析[J]. 中国环境科学, 2019, 39(9): 3951-3958. Fu X M, Sun Y Y, Su J, et al. Source of nitrate in groundwater based on hydrochemical and dual stable isotopes[J]. China Environmental Science, 2019, 39(9): 3951-3958. DOI:10.3969/j.issn.1000-6923.2019.09.042 |
| [11] |
任坤, 潘晓东, 梁嘉鹏, 等. 碳氮氧同位素解析典型岩溶流域地下水中硝酸盐来源与归趋[J]. 环境科学, 2021, 42(5): 2268-2275. Ren K, Pan X D, Liang J P, et al. Sources and fate of nitrate in groundwater in a typical karst basin: insights from carbon, nitrogen, and oxygen isotopes[J]. Environmental Science, 2021, 42(5): 2268-2275. |
| [12] |
徐志伟, 张心昱, 于贵瑞, 等. 中国水体硝酸盐氮氧双稳定同位素溯源研究进展[J]. 环境科学, 2014, 35(8): 3230-3238. Xu Z W, Zhang X Y, Yu G R, et al. Review of dual stable isotope technique for nitrate source identification in surface-and groundwater in China[J]. Environmental Science, 2014, 35(8): 3230-3238. |
| [13] | Zhang Y, Shi P, Song J X, et al. Application of nitrogen and oxygen isotopes for source and fate identification of nitrate pollution in surface water: a review[J]. Applied Sciences, 2019, 9(1). DOI:10.3390/app9010018 |
| [14] |
金赞芳, 胡晶, 吴爱静, 等. 基于多同位素的不同土地利用区域水体硝酸盐源解析[J]. 环境科学, 2021, 42(4): 1696-1705. Jin Z F, Hu J, Wu A J, et al. Identify the nitrate sources in different land use areas based on multiple isotopes[J]. Environmental Science, 2021, 42(4): 1696-1705. |
| [15] | Chen X, Jiang C L, Zheng L G, et al. Identification of nitrate sources and transformations in basin using dual isotopes and hydrochemistry combined with a Bayesian mixing model: application in a typical mining city[J]. Environmental Pollution, 2020, 267. DOI:10.1016/j.envpol.2020.115651 |
| [16] | Zhao Y Y, Zheng B H, Jia H F, et al. Determination sources of nitrates into the Three Gorges Reservoir using nitrogen and oxygen isotopes[J]. Science of the Total Environment, 2019, 687: 128-136. DOI:10.1016/j.scitotenv.2019.06.073 |
| [17] | Yu Q B, Wang F, Li X Y, et al. Tracking nitrate sources in the Chaohu Lake, China, using the nitrogen and oxygen isotopic approach[J]. Environmental Science and Pollution Research, 2018, 25(20): 19518-19529. DOI:10.1007/s11356-018-2178-9 |
| [18] | Toyoda S, Suzuki Y, Hattori S, et al. Isotopomer analysis of production and consumption mechanisms of N2O and CH4 in an advanced wastewater treatment system[J]. Environmental Science & Technology, 2011, 45(3): 917-922. |
| [19] | Kotajima S, Koba K, Ikeda D, et al. Nitrogen and oxygen isotope signatures of nitrogen compounds during anammox in the laboratory and a wastewater treatment plant[J]. Microbes and Environments, 2020, 35(4). DOI:10.1264/jsme2.ME20031 |
| [20] | Archana A, Li L, Shuh-Ji K, et al. Variations in nitrate isotope composition of wastewater effluents by treatment type in Hong Kong[J]. Marine Pollution Bulletin, 2016, 111(1-2): 143-152. DOI:10.1016/j.marpolbul.2016.07.019 |
| [21] | Sanchez D A, Szynkiewicz A, Faiia A M. Determining sources of nitrate in the semi-arid Rio Grande using nitrogen and oxygen isotopes[J]. Applied Geochemistry, 2017, 86: 59-69. DOI:10.1016/j.apgeochem.2017.09.012 |
| [22] | Jung H, Kim Y S, Yoo J, et al. Seasonal variations in stable nitrate isotopes combined with stable water isotopes in a wastewater treatment plant: implications for nitrogen sources and transformation[J]. Journal of Hydrology, 2021, 599. DOI:10.1016/j.jhydrol.2021.126488 |
| [23] | Carrey R, Ballesté E, Blanch A R, et al. Combining multi-isotopic and molecular source tracking methods to identify nitrate pollution sources in surface and groundwater[J]. Water Research, 2021, 188. DOI:10.1016/j.watres.2020.116537 |
| [24] | Anisfeld S C, Barnes R T, Altabet M A, et al. Isotopic apportionment of atmospheric and sewage nitrogen sources in two connecticut rivers[J]. Environmental Science & Technology, 2007, 41(18): 6363-6369. |
| [25] | Lee J, Park T, Kim M S, et al. Stable isotope on the evaluation of water quality in the presence of WWTPs in rivers[J]. Environmental Science and Pollution Research, 2016, 23(18): 18175-18182. |
| [26] | Xian C F, Ouyang Z Y, Li Y M, et al. Variation in nitrate isotopic signatures in sewage for source apportionment with urbanization: a case study in Beijing, China[J]. Environmental Science and Pollution Research, 2016, 23(22): 22871-22881. |
| [27] | Lin J J, Böhlke J K, Huang S, et al. Seasonality of nitrate sources and isotopic composition in the Upper Illinois River[J]. Journal of Hydrology, 2019, 568: 849-861. |
| [28] | Van De Graaf A A, Mulder A, De Bruijn P, et al. Anaerobic oxidation of ammonium is a biologically mediated process[J]. Applied and Environmental Microbiology, 1995, 61(4): 1246-1251. |
| [29] | Kobayashi K, Makabe A, Yano M, et al. Dual nitrogen and oxygen isotope fractionation during anaerobic ammonium oxidation by anammox bacteria[J]. The ISME Journal, 2019, 13(10): 2426-2436. |
| [30] |
詹晓燕, 刘臣辉, 范海燕, 等. 水体中氨氮测定方法的比较——纳氏试剂光度法、靛酚蓝比色法[J]. 环境科学与管理, 2010, 35(11): 132-134, 131. Zhan X Y, Liu C H, Fan H Y, et al. Comparison between two N-ammoniacal measurements in water——Napierian reagent colorimetric method and Indophenol-blue colorimetric method[J]. Environmental Science and Management, 2010, 35(11): 132-134, 131. |
| [31] |
刘松韬, 张东, 李玉红, 等. 伊洛河流域河水来源及水化学组成控制因素[J]. 环境科学, 2020, 41(3): 1184-1196. Liu S T, Zhang D, Li Y H, et al. Water sources and factors controlling hydro-chemical compositions in the Yiluo River basin[J]. Environmental Science, 2020, 41(3): 1184-1196. |
| [32] |
张雯淇, 章炎麟. 大气硝酸盐中氧同位素异常研究进展[J]. 科学通报, 2019, 64(7): 649-662. Zhang W Q, Zhang Y L. Oxygen isotope anomaly (Δ17O) in atmospheric nitrate: a review[J]. Chinese Science Bulletin, 2019, 64(7): 649-662. |
| [33] | Casciotti K L, Sigman D M, Ward B B. Linking diversity and stable isotope fractionation in ammonia-oxidizing bacteria[J]. Geomicrobiology Journal, 2003, 20(4): 335-353. |
| [34] | Casciotti K L, McIlvin M, Buchwald C. Oxygen isotopic exchange and fractionation during bacterial ammonia oxidation[J]. Limnology and Oceanography, 2010, 55(2): 753-762. |
| [35] | Keeling R F. The atmospheric oxygen cycle: the oxygen isotopes of atmospheric CO2 and O2 and the O2/N2 ratio[J]. Reviews of Geophysics, 1995, 33(S2): 1253-1262. |
| [36] | Buchwald C, Santoro A E, McIlvin M R, et al. Oxygen isotopic composition of nitrate and nitrite produced by nitrifying cocultures and natural marine assemblages[J]. Limnology and Oceanography, 2012, 57(5): 1361-1375. |
| [37] | Boshers D S, Granger J, Tobias C R, et al. Constraining the oxygen isotopic composition of nitrate produced by nitrification[J]. Environmental Science & Technology, 2019, 53(3): 1206-1216. |
| [38] | Böttcher J, Strebel O, Voerkelius S, et al. Using isotope fractionation of nitrate-nitrogen and nitrate-oxygen for evaluation of microbial denitrification in a sandy aquifer[J]. Journal of Hydrology, 1990, 114(3-4): 413-424. |
 2023, Vol. 44
2023, Vol. 44

