2. 浙江工商大学环境科学与工程学院, 杭州 310012
2. School of Environmental Science and Engineering, Zhejiang Gongshang University, Hangzhou 310012, China
随着我国海洋经济的高速发展, 海洋环境尤其是近海海域中水质和沉积物指标等都引起了广泛的关注.其中近海海域的水质不仅决定海洋生物的生存和生长, 而且还影响着海水养殖和沿海观光等产业发展[1~3].近年来, 陆排废水持续进入海洋环境和海水养殖行业的兴起, 已经对我国近海海域的水质环境带了严重影响, 在我国多个近海海域都检测到了抗生素等典型的有机污染物[4~6].目前, 近海海域中的有机污染浓度低, 但在高含盐的海水体系中难以自然降解, 长时间存在对海洋生物造成严重危害, 甚至在海洋生物体内形成累积和富集作用[7~9].除了提升陆排废水的水质要求之外, 如何深度处理含有抗生素等等难降解有机污染物的海洋养殖废水, 已经成为近海海洋环境治理的关键因素[10~12].围绕着海水中低浓度难降解有机物的去除, 并结合海水中大量盐离子的特点, 研究者成功利用了多相光催化技术深度处理海水甚至其他高含盐废水中的苯酚和染料分子等有机污染物[13, 14].在前期工作中, 研究者探索了改性商用TiO2光催化剂(P25)和氧化石墨烯负载的TiO2两种光催化剂在紫外和可见光激发下对海水中苯酚和甲基橙的降解过程[14, 15], 结果发现能够有效接触或者优先吸附有机污染物分子的催化剂, 都能克服海水中盐离子的干扰, 对苯酚和甲基橙的去除率都可以达90%以上.
然而普遍认为, 纳米光催化剂粒径越小其活性越高, 如P25光催化剂粒子的粒径在25 nm左右[16~18].在海水环境治理过程中小粒径纳米颗粒物难以回收, 为此研究者提出以TiO2纳米粒子作为光催化活性组分, 用多孔材料和空心材料等作为载体制备负载型光催化剂来解决纳米粒子的回收问题[19~21].前期工作中, 本课题组利用海绵和空心有机玻璃球作为载体, 制备可以在海水中漂浮的球体光催化剂[22, 23].但是, 负载型催化剂往往牺牲小粒径TiO2纳米颗粒的大比表面, 会削弱催化剂与有机污染物分子的接触, 从而削弱了负载型光催化剂的抗盐离子干扰能力和催化活性.更重要的是, 对于海洋环境, 小粒径纳米粒子对环境和生物有潜在的纳米毒性, 这就难以将其应用于近海海域中有机污染物的去除.即使负载型催化剂也难以避免过程中纳米粒子脱落而带来的环境危害.鉴于小粒子纳米光催化剂在环境治理中难以克服的缺陷, 研究者开发了具有介孔孔隙(2~50 nm)TiO2光催化剂[24~26].催化剂内部的介孔孔道结构不仅导致催化剂具有较大比表面积, 而且孔道表面往往有丰富的活性位点, 从而具有较高的光催化活性.除此之外, 介孔TiO2光催化剂的粒径往往在200 nm以上, 可以通过过滤等手段简便地实现回收, 有效避免了光催化剂应用于海洋环境体系时潜在的纳米毒性.
在文献[14, 25, 26]和前期工作的基础上, 本文将可见光响应的手性介孔TiO2光催化剂首次用于光催化降解海水中四环素(tetracycline, TC)污染物; 而后系统探索海水中盐离子种类对光催化降解过程的影响机制, 结合自由基捕获实验和电子自旋共振(ESR)分析探索纯水和海水中手性介孔TiO2光催化剂光降解污染物的主要活性物种; 最后利用超高效液相色谱仪(UPLC)和质谱(MS)分析TC光催化降解过程中的产物, 对比纯水和海水中TC光催化降解途径的差异.
1 材料与方法 1.1 实验试剂与表征仪器实验试剂:L-谷氨酸, 肉豆蔻酰氯和3-氨基丙基三乙氧基硅烷(APES)均为分析纯, 购自国药集团化学试剂有限公司, 无需进一步纯化即可使用. 丙酮, 石油醚, 钛酸丁酯, 罗丹明B, 氢氧化钠, 浓HCl(36%), 乙酸和乙酸钠也均为分析纯, 购自上海化学试剂厂(中国上海).
表征仪器:XRD分析在日本Rigaku公司的D/max-rA转靶X射线多晶衍射仪上进行, 采用Cu Kα(λ=0.154 06 nm), 功率为1 600 W(40 kV×40 mA). 样品的X射线光电子能谱(XPS)分析在Thermo ESCALAB 250X射线光电子能谱(XPS)仪上进行. X射线激发源:单色Al Kα (hv=1 486.6 eV), 功率150 W, X射线束斑500 μm能量分析器固定透过能为30 eV. 样品的比表面积和孔径分析使用美国Quantachrome公司的Quantachrome NOVA 4200E表面积和孔径分析仪. 使用JES-X320光谱仪(JEOL, Japan) 生成电子自旋共振(ESR) 光谱检测活性自由基.将光催化剂粉末压制成片装在有积分球的TU-1901型紫外-可见分光光度计上进行光催化剂的紫外可见漫反射光谱分析.
1.2 软模板自组装法制备手性介孔TiO2光催化剂作为模板的左旋性(L型)手性表面活性剂N-酰基氨基酸C14-L-AlaA的制备过程参考文献[27]. 在120 mL去离子水和80 mL丙酮混合溶液中, 加入8.9 g L-丙氨酸和4.0 g NaOH在5℃水浴下搅拌反应, 而后加入26.8 g肉豆蔻酰氯继续反应(整个过程利用4 mg·L-1 NaOH溶液调节pH维持在12~12.5).之后用浓盐酸中和反应液直至pH=1.反应完成后, 利用去离子水将反应物洗涤至中性并用石油醚清洗5次, 利用真空干燥得到L型表面活性剂C14-L-AlaA.
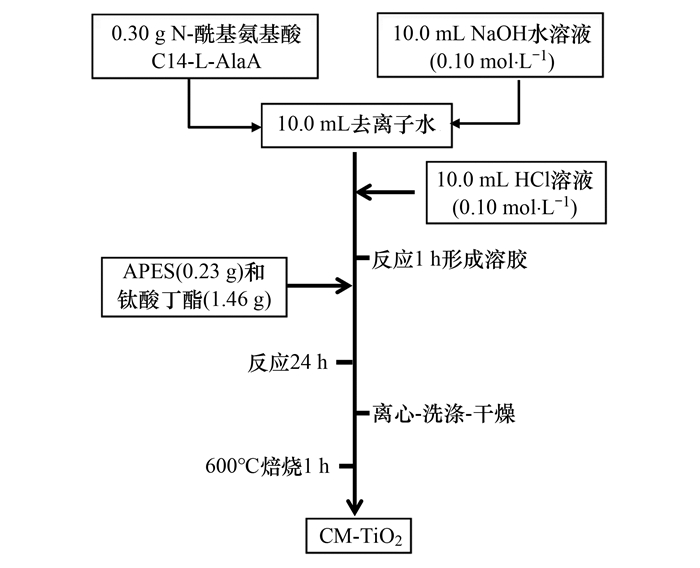
以C14-L-AlaA为表面活性剂构建软模板法制备手性介孔TiO2的过程参考文献[28], 详细的制备过程如图 1所示.得到的手性介孔TiO2催化剂记为CM-TiO2.
|
图 1 手性二氧化钛的制备过程 Fig. 1 Preparation of chiral mesoporous TiO2 |
作为对比, 选择Zhu等[29]提出的介孔TiO2材料制备方法, 制备得到非手性介孔TiO2, 记为M-TiO2.步骤如下:将Pluronic P-123作为表面活性剂, 溶于10 g的乙醇溶液中, 加入0.01 mol的四氯化钛水溶液, 置于磁力搅拌器上剧烈搅拌0.5 h后得到溶胶.将溶胶倒入开放的培养皿中在40℃的真空烘箱干燥得到粉末.而后将粉末在马弗炉400℃煅烧5 h除去P-123, 制得M-TiO2.
1.3 光催化降解实验根据文献[14, 30]配置模拟海水, 其组分为:2.5% NaCl, 1.1% MgCl2, 0.40% Na2SO4, 0.16% CaCl2.
手性介孔TiO2的光催化降解有机污染物的性能考评过程参见文献[28].以30 W的白光LED作为光源(利用滤光片去除波长小于400 nm和大于700 nm的光线), 降解400 mL纯水或者海水中四环素(初始浓度为5.0 mg·L-1). 每隔30 min进行取样, 利用可见光分光光度仪测定四环素(测定波长352 nm)的吸光度, 并根据其标准曲线计算求出其浓度变化(反应5 h).为了更清楚地探明影响介孔TiO2光催化剂可见光响应的结构特征, 实验中采用的是完全在可见光波长范围内的激发光源.
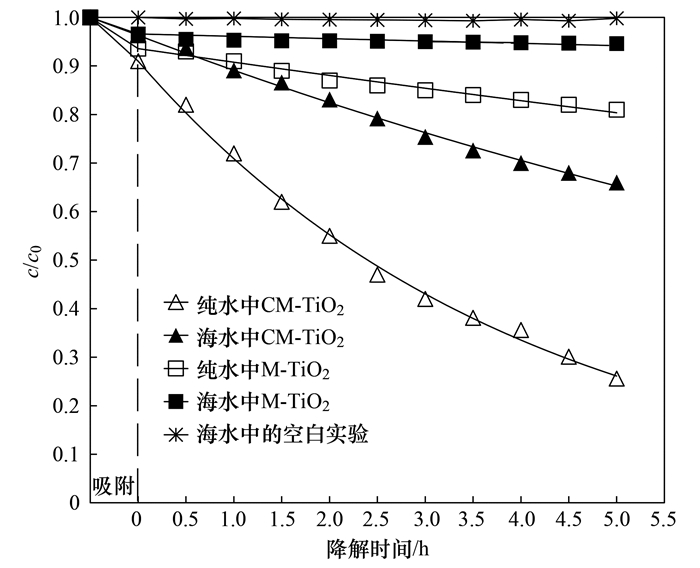
2 结果与讨论 2.1 可见光激发下手性介孔L-TiO2降解四环素的过程研究图 2是可见光激发下纯水和海水体系中两种介孔TiO2对四环素TC的降解过程, 作为对比也列出了海水体系中的空白实验.可以看出, 仅在LED光源的可见光照射下, 体系中的TC浓度不会发生任何变化, 也就是说仅可见光照射TC不会发生降解.而无论哪种催化剂在模拟海水中对TC平衡吸附率和其降解效率都明显弱于纯水中对TC的降解, 说明模拟海水中盐离子对催化剂吸附和光降解TC的过程都有显著干扰.另外, 纯水和海水体系中手性TiO2光催化剂CM-TiO2对TC降解性能要远高于非手性TiO2催化剂.为了更清楚对比两种水体系和两种催化剂对TC的降解效果, 利用一级反应动力学方程拟合得到了光降解反应速率常数, 如表 1所示.
|
图 2 可见光激发下两种水体系中不同介孔TiO2降解TC曲线 Fig. 2 Degradation curves for TC by different mesoporous TiO2 in water and seawater under irradiation of visible light |
|
|
表 1 纯水和海水体系中不同介孔TiO2降解TC的反应速率常数 Table 1 Rate constants of TC degradation by different mesoporous TiO2 in water and seawater |
表 1中数据更清楚表明, 海水体系中TC光降解过程被明显抑制, 尤其是活性较弱的非手性TiO2光催化剂M-TiO2在海水体系中几乎不能降解TC, 其反应过程也完全偏离一级动力学方程.即使在纯水中有较高活性的CM-TiO2, 其在海水中对TC的光降解反应速率也降低了70%左右.结合前期工作可知[28], 手性介孔CM-TiO2和非手性介孔M-TiO2两种催化剂不同活性是由于其结构差异而导致的.
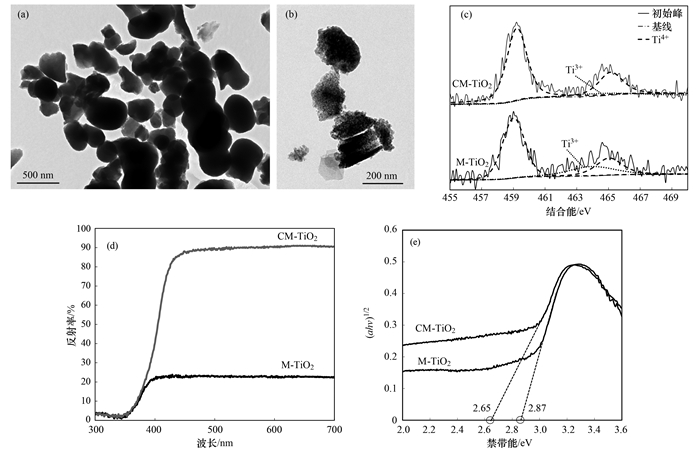
图 3对比了两种催化剂的结构, 可以发现TEM照片中都显示两种催化剂内部呈现了明显的孔隙结构.利用BET分析结果得到手性介孔CM-TiO2和非手性介孔M-TiO2的比表面积分别为77.33 m2·g-1和113 m2·g-1, 平均孔径分别为6.4 nm和8.6 nm, 进一步确定了其介孔孔隙结构.由于软模板制备过程中手性表面活性剂的结构导向作用, TEM照片呈现出CM-TiO2中存在明显手性堆积结构, 而非手性介孔M-TiO2仅仅呈现类似于圆球的形状.这种结构上的不同导致了两种催化剂中Ti3+含量的差异[图 3(c)], CM-TiO2中手性堆积结构在催化剂中引入不对称结构和大量的缺陷, 从而导致催化剂中形成丰富的Ti3+[图 3(c)], 而根据文献可知催化剂中Ti3+增加, 其可见光响应可以得到显著提升[31~33], 因此CM-TiO2的可见光响应要优于非手性M-TiO2催化剂, 图 3(e)中计算得到的CM-TiO2的禁带能要显著小于非手性M-TiO2催化剂.所以, 在可见光激发下CM-TiO2对TC的降解活性要显著高于非手性M-TiO2催化剂.
|
(a)CM-TiO2的TEM照片; (b)M-TiO2的TEM照片; (c)Ti 2p的XPS图谱; (d)紫外漫反射光谱; (e)(αhν)1/2与禁带能的关系 图 3 不同介孔TiO2的微结构 Fig. 3 Microstructures of different mesoporous TiO2 |
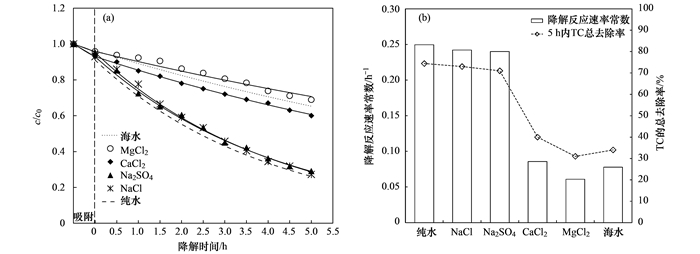
为了探明模拟海水中盐离子的影响机制, 根据模拟海水的组分及其浓度分别对应配置了单一盐离子溶液, 并在该溶液中进行CM-TiO2对TC的光降解实验, 结果如图 4所示.从中可知, 模拟海水组分中Cl-和SO42-阴离子对光催化过程的影响较少, 但不同阳离子对该催化剂的光降解过程影响差异较大. Mg2+和Ca2+对光催化过程有非常明显的抑制作用, 而Na+对光催化过程几乎没有影响.在MgCl2溶液中催化剂对TC的降解活性甚至要低于模拟海水中光降解活性, 这可能是因为模拟海水中多个离子之间存在着相互作用, 反而削弱了Mg2+和Ca2+对光催化过程的抑制作用.
|
(a)降解曲线; (b)反应速率常数和5 h内总去除率 图 4 不同盐离子对手性介孔TiO2降解TC过程的影响 Fig. 4 Effect of salt ions in seawater on TC degradation and the corresponding rate constants by CM-TiO2 |
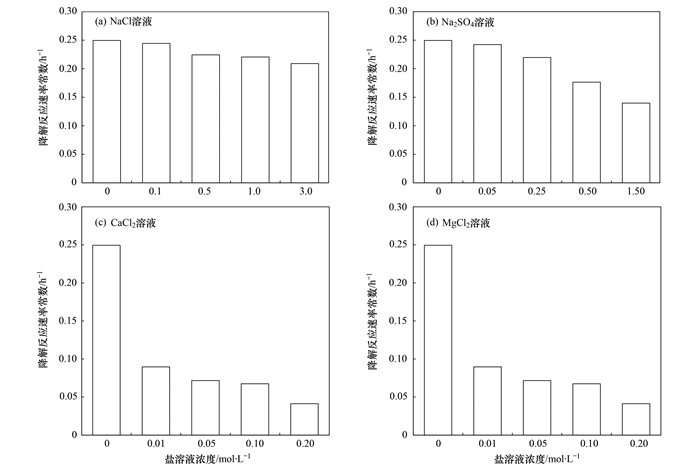
由于模拟海水中盐离子浓度有较大差异, 为了更明确不同盐离子对光催化过程的干扰作用, 进一步设计了不同量浓度4种单一盐溶液体系中催化剂对TC的光降解过程, 如图 5所示.首先发现, NaCl溶液中盐浓度变化对光催化过程影响较少, 即使浓度达到3 mol·L-1其反应速率常数也仅仅下降了10%左右.而在Na2SO4溶液中, 当盐浓度增加到0.5 mol·L-1以上时光催化过程会被少量抑制, 在1.0 mol·L-1浓度Na2SO4溶液中反应速率常数比纯水中下降了40%左右.对比图 4(a)中不同NaCl溶液体系的光催化降解过程, 由于两种溶液中Na+浓度是一样的, 因此溶液中Na2SO4对光催化过程的抑制作用是由于反应体系中存在高浓度的SO42-而导致.这可能是介孔TiO2表面带正电荷, 高浓度负二价SO42-对催化剂表面产生了一定影响, 从而抑制其光催化过程.但模拟海水中硫酸钠浓度为0.40%, 总硫酸根浓度约为0.031 mol·L-1, 远小于0.5 mol·L-1, 所以模拟海水中硫酸根阴离子对光催化过程影响较少.然而图 5(c)和5(d)显示, 含盐水体系中Mg2+和Ca2+对光催化过程的抑制作用都非常显著, 当两种离子浓度仅为0.01 mol·L-1时, 光催化反应速率就降低了60%以上, 这进一步验证了模拟海水体系中不同盐离子对光催化过程的影响结果.虽然Mg2+和Ca2+两种离子的半径等性质都有差异, 但在相同浓度下两种阳离子对CM-TiO2光降解TC的抑制作用近似, 这可能是二价阳离子的价态是抑制光降解反应的主要因素.模拟海水体系中Mg2+浓度比Ca2+离子更高, 因此Mg2+对光催化过程的抑制作用更为显著.其他阳离子或者更高价阳离子对光催化过程的影响, 则需要后续更深入的实验工作来验证.
|
图 5 不同含盐水体系中手性介孔TiO2降解TC的反应速率常数 Fig. 5 Rate constants for TC degradation by CM-TiO2 in different saline wastewaters |
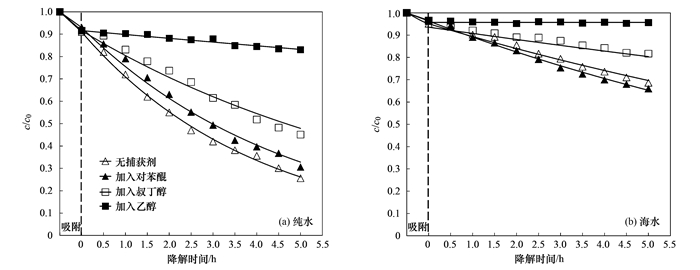
有机物的光催化降解过程首先是催化剂CM-TiO2受到可见光激发而产生光生h+和光生e-, 而后两者分别迁移到催化剂表面直接与污染物进行反应, 或者在光生空穴和电子在催化剂表面与吸附的H2O分子或者O2分子反应生成·OH或者·O2-, 而后这些活性组分攻击有机污染物分子, 进一步氧化分解有机污染物分子[34~36].因此, 本文首先通过不同自由基的捕获实验来对比分析纯水和模拟海水体系中活性组分及其变化, 结果如图 6所示.表 2也列出了按照一级动力学拟合后不同捕获剂的加入对各个光催化反应的速率常数和5 h后TC去除率的影响.从图 6和表 2的数据发现, 无论纯水还是海水体系, 3种捕获剂的加入对光催化过程的影响规律是类似的, 超氧自由基捕获剂对苯醌的加入对光催化过程影响最小,·OH捕获剂叔丁醇加入次之, 而乙醇的加入由于可以捕获全部自由基和空穴, 所以乙醇加入后光催化过程被极大地抑制[37~39].从表 2数据可以看出, 5 h光降解后纯水和海水体系中TOC去除率和通过吸光测得的去除率相当, 也就是说两种水体系中一旦发生光催化降解反应, 催化剂能够矿化TC分子, 虽然海水体系中盐离子干扰使得光催化剂降解效率显著下降.
|
图 6 捕获剂对纯水和海水体系中手性介孔TiO2降解TC过程的影响 Fig. 6 Effect of the scavenges on the TC degradation by CM-TiO2 in water and seawater |
|
|
表 2 捕获剂对纯水和海水体系中手性介孔TiO2降解TC的反应速率和去除率的影响 Table 2 Effect of the scavenges on the rate constants and removal rate for TC by CM-TiO2 in water and seawater |
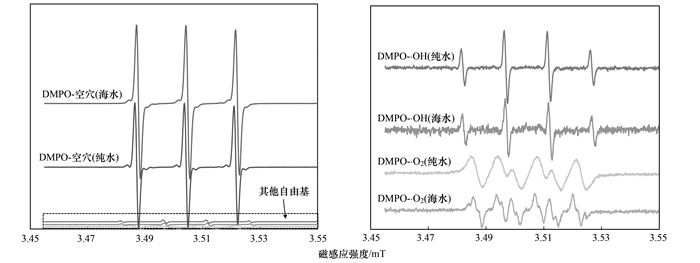
为了探明两种水体系中光降解过程产生的活性物种, 在可见光激发手性TiO2催化剂10 min后利用ESR光谱测定了反应体系的活性物种[40, 41], 如图 7所示.可以发现, 两种水体系中光激发后产生的活性物种中空穴占据主要地位, 峰强度远高于·OH和超氧自由基强度, 而且两种水体系中产生的活性物种峰的强度近似, 也就是说海水中各个盐离子不会抑制光激发CM-TiO2产生活性物种的过程.因此, 海水体系中Mg2+和Ca2+等盐离子应该是阻碍了空穴等活性物种对TC分子的攻击过程.
|
图 7 手性TiO2催化剂光降解过程中ESR光谱图 Fig. 7 ESR spectrum during photodegradation process by CM-TiO2 in water and seawater |
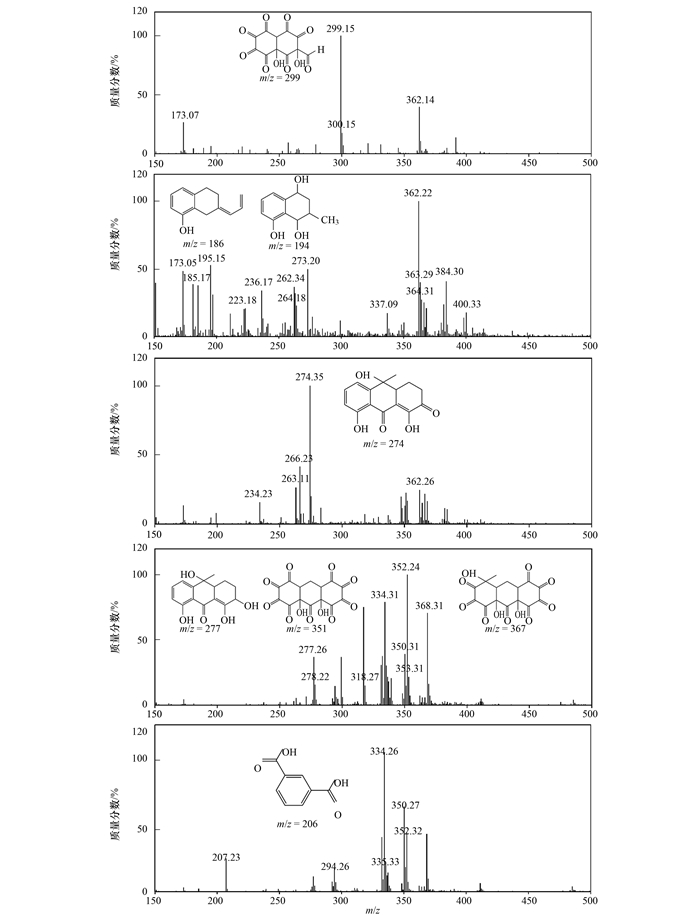
普遍认为, 空穴和·OH甚至超氧自由基都属于亲电试剂, 一般攻击有机污染物分子中的亲核原子, 也就是电负性大的原子[42].本文首先利用UPLC-MS分别分析了纯水和脱盐后海水体系中TC光催化降解30 min后体系产生的中间产物, 在两种水体系中均发现了主要中间产物的质谱图(图 8), 这说明两种水体系中都以空穴作为主要活性物种, 因此其对TC的降解路径是一致的.而后根据文献[43]利用密度泛函DFT对TC分子中各个原子的计算, 推测出可能的降解TC途径(图 9).
|
图 8 光降解10 min后海水体系中中间产物的质谱图 Fig. 8 Mass spectra of intermediates in seawater after photodegradation for 10 min |
|
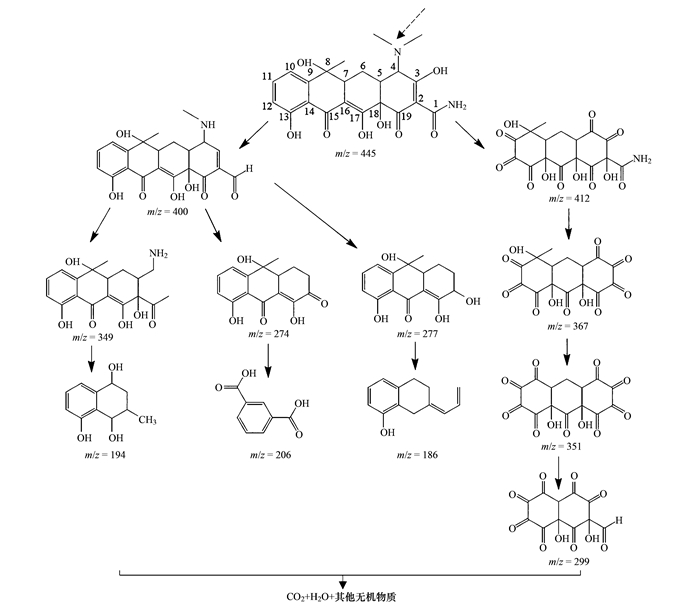
图 9 可见光激发下海水体系中手性TiO2光降解TC的路径 Fig. 9 Photodegradation pathway of TC by CM-TiO2 in seawater under visible light excitation |
根据文献[43], 四环素分子中电负性最强的分别是C21—N2键和C22—N2键.当催化剂受到可见光激发产生h+和·OH后TC受到h+的攻击, 使得负电荷最大的C21—N2键和C22—N2键最先断裂, 如图 9所示.导致TC先脱去一个甲基, 再脱去一个氮甲基, 之后在a2位置上又发生了脱酰胺反应, 得到中间产物A(m/z=400).之后在活性物质的攻击下, a环上C1—C2键上的烯醇基团脱除, 并发生开环反应, 得到产物B(m/z=349), 这与DFT理论计算的结论相符.之后a环上的C2~C19键发生脱羰基反应, 另外C8位置上的C—C键受到活性物质攻击脱去甲基.h+继续攻击不稳定的C—N键, 导致产物B的氨基基团脱除.由于不稳定的C—N键都已经断裂, 活性物质转而攻击C18—C19位置上C—C键, 导致甲基脱除, 并连续发生开环、双键断裂和羟基化等反应, 形成了产物C(m/z=194).
在海水体系中, 由于活性物种没有受到抑制, TC的光催化降解途径应该与纯水体系是一致的[44, 45].但是较多二价Mg2+和Ca2+离子可以在电负性强的原子周边富集, 不仅少量抑制手性CM-TiO2对TC的吸附过程(图 2), 而且还与空穴和自由基等亲电试剂形成竞争关系, 阻碍亲电试剂对TC分子中电负性强的原子的攻击, 从而抑制了光催化降解效率.
3 结论(1) 模拟海水体系中光降解过程被显著抑制, CM-TiO2在海水中对TC的光降解反应速率降低了70%左右, 而非手性M-TiO2光催化剂在海水体系中几乎不能降解TC.模拟海水中阴离子对光降解过程影响较小, 但不同阳离子有着不同的影响.Mg2+和Ca2+对光催化过程的抑制作用非常显著, 两种离子浓度仅为0.01 mol·L-1, TC的光催化反应速率就降低了60%以上, 但是Na+基本不影响TC的光降解过程.
(2) 在纯水和模拟海水体系中, 可见光激发后CM-TiO2产生的空穴和两种自由基数量接近, 空穴都是主要活性物种.模拟海水体系中, 盐离子不会抑制光激发CM-TiO2产生活性物种的过程, 因此TC的光催化降解途径与纯水体系是一致的.但Mg2+和Ca2+离子富集在强电负性原子周边, 不仅抑制CM-TiO2对TC的吸附, 还阻碍空穴等亲电试剂对TC分子中强电负性原子的攻击, 从而降低光催化降解效率.
| [1] |
李征, 高春梅, 杨金龙, 等. 连云港海州湾海域表层水体和沉积物中微塑料的分布特征[J]. 环境科学, 2020, 41(7): 3212-3221. Li Z, Gao C M, Yang J L, Wu L Z, et al. Distribution characteristics of microplastics in surface water and sediments of Haizhou Bay, Lianyungang[J]. Environmental Science, 2020, 41(7): 3212-3221. |
| [2] |
朱小山, 黄静颖, 吕小慧, 等. 防晒剂的海洋环境行为与生物毒性[J]. 环境科学, 2018, 39(6): 2991-3002. Zhu X S, Huang J Y, Lv X H, et al. Fate and toxicity of UV filters in marine environments[J]. Environmental Science, 2018, 39(6): 2991-3002. DOI:10.13227/j.hjkx.201709285 |
| [3] | Rodrígue J, Gallampois C M J, Haglund P, et al. Bacterial communities as indicators of environmental pollution by POPs in marine sediments[J]. Environmental Pollution, 2021, 268. DOI:10.1016/j.envpol.2020.115690 |
| [4] |
刘鹏霄, 王旭, 冯玲. 自然水环境中抗生素的污染现状、来源及危害研究进展[J]. 环境工程, 2020, 38(5): 36-42. Liu P X, Wang X, Feng L. Occurrences, resources and risk of antibiotics in aquatic environment: a review[J]. Environmental Engineering, 2020, 38(5): 36-42. DOI:10.13205/j.hjgc.202005007 |
| [5] | Huang F Y, An Z Y, Moran M J, et al. Recognition of typical antibiotic residues in environmental media related to groundwater in China (2009-2019)[J]. Journal of Hazardous Materials, 2020, 399. DOI:10.1016/j.jhazmat.2020.122813 |
| [6] | Lyu J, Yang L S, Zhang L, et al. Antibiotics in soil and water in China-a systematic review and source analysis[J]. Environmental Pollution, 2020, 266. DOI:10.1016/j.envpol.2020.115147 |
| [7] | Yang H J, Jeong H J, Bong K M, et al. Organic matter and heavy metal in river sediments of southwestern coastal Korea: Spatial distributions, pollution, and ecological risk assessment[J]. Marine Pollution Bulletin, 2020, 159. DOI:10.1016/j.marpolbul.2020.111466 |
| [8] | Farrington J W, Takada H. Persistent organic pollutants (POPs), polycyclic aromatic hydrocarbons (PAHs), and plastics: examples of the status, trend, and cycling of organic chemicals of environmental concern in the ocean[J]. Oceanography, 2014, 27(1): 196-213. DOI:10.5670/oceanog.2014.23 |
| [9] |
王金鹏, 赵阳国, 胡钰博. 磺胺甲唑对海水养殖废水处理过程中抗性细菌及抗性基因的富集作用[J]. 环境科学, 2021, 42(8): 3791-3798. Wang J P, Zhao Y G, Hu Y B. Enrichment of antibiotic resistant bacteria and antibiotic resistance genes by sulfamethoxazole in the biological treatment system of mariculture wastewater[J]. Environmental Science, 2021, 42(8): 3791-3798. |
| [10] |
杨利伟, 刘丽君, 夏训峰, 等. pg-C3N4/BiOBr/Ag复合材料的制备及其光催化降解磺胺甲唑[J]. 环境科学, 2021, 42(6): 2896-2907. Yang L W, Liu L J, Xia X F, et al. Preparation of pg-C3N4/BiOBr/Ag composite and photocatalytic degradation of sulfamethoxazole[J]. Environmental Science, 2021, 42(6): 2896-2907. |
| [11] |
高闯闯, 刘海成, 孟无霜, 等. Ag3PO4/g-C3N4复合光催化剂的制备及其可见光催化性能[J]. 环境科学, 2021, 42(5): 2343-2352. Gao C C, Liu H C, Meng W H, et al. Preparation of Ag3PO4/g-C3N4 composite photocatalysts and their visible light photocatalytic performance[J]. Environmental Science, 2021, 42(5): 2343-2352. |
| [12] |
黄文鑫, 魏虎, 蒋彩云, 等. Bi2MoO6/Bi2S3异质结光催化降解四环素-铜复合物[J]. 环境科学, 2020, 41(12): 5488-5499. Huang W X, Wei H, Jiang C Y, et al. Photocatalytic degradation of tetracycline and copper complex by Bi2MoO6/Bi2S3 heterojunction[J]. Environmental Science, 2020, 41(12): 5488-5499. |
| [13] | Shaban Y A, El Maradny A A, Al Farawati R K. Photocatalytic reduction of nitrate in seawater using C/TiO2 nanoparticles[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2016, 328: 114-121. DOI:10.1016/j.jphotochem.2016.05.018 |
| [14] | Wang T, Li B R, Pan J H, et al. Deposition of quantum-sized Ag on TiO2 through adsorbed-layer nanoreactor synthesis and its performance for photodegrading phenol in seawater under visible-light irradiation[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2018, 555: 448-456. DOI:10.1016/j.colsurfa.2018.07.024 |
| [15] | Wang T, Li Y, Pan J H, et al. Alcohol solvothermal reduction for commercial P25 to harvest weak visible light and fabrication of the resulting floating photocatalytic spheres[J]. Scientific Reports, 2019, 9(1). DOI:10.1038/s41598-019-50457-w |
| [16] | Ahmed S N, Haider W. Heterogeneous photocatalysis and its potential applications in water and wastewater treatment: a review[J]. Nanotechnology, 2018, 29(34). DOI:10.1088/1361-6528/aac6ea |
| [17] | Jing Q H, Zhang H, Huang H, et al. Ultrasonic exfoliated ReS2 nanosheets: fabrication and use as co-catalyst for enhancing photocatalytic efficiency of TiO2 nanoparticles under sunlight[J]. Nanotechnology, 2019, 30(18). DOI:10.1088/1361-6528/ab00b4 |
| [18] | Lincho J, Zaleska-Medynska A, Martins R C, et al. Nanostructured photocatalysts for the abatement of contaminants by photocatalysis and photocatalytic ozonation: an overview[J]. Science of the Total Environment, 2022, 837. DOI:10.1016/j.scitotenv.2022.155776 |
| [19] | Wang X, Wang X J, Zhao J F, et al. Solar light-driven photocatalytic destruction of cyanobacteria by F-Ce-TiO2/expanded perlite floating composites[J]. Chemical Engineering Journal, 2017, 320: 253-263. DOI:10.1016/j.cej.2017.03.062 |
| [20] | Shavisi Y, Sharifnia S, Hosseini S N, et al. Application of TiO2/perlite photocatalysis for degradation of ammonia in wastewater[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(1): 278-283. DOI:10.1016/j.jiec.2013.03.037 |
| [21] | Wang X, Wang W, Wang X J, et al. Synthesis, structural characterization and evaluation of floating B-N codoped TiO2/expanded perlite composites with enhanced visible light photoactivity[J]. Applied Surface Science, 2015, 349: 264-271. DOI:10.1016/j.apsusc.2015.05.002 |
| [22] | Xu H T, Hao Z, Feng W H, et al. The floating photocatalytic spheres loaded with weak light-driven TiO2-based catalysts for photodegrading tetracycline in seawater[J]. Materials Science in Semiconductor Processing, 2022, 144. DOI:10.1016/j.mssp.2022.106610 |
| [23] |
宋英琦, 潘家豪, 吴礼光, 等. 可见光激发降解甲基橙的光催化漂浮球的制备[J]. 纺织学报, 2020, 41(12): 102-110. Song Y Q, Pan J H, Wu L G, et al. Fabrication of photocatalytic floating spheres for degradation of methyl-orange under illumination of visible light[J]. Journal of Textile Research, 2020, 41(12): 102-110. DOI:10.13475/j.fzxb.20200306909 |
| [24] | Gabashvili A, Major D T, Perkas N, et al. The sonochemical synthesis and characterization of mesoporous chiral titania using a chiral inorganic precursor[J]. Ultrasonics Sonochemistry, 2010, 17(3): 605-609. DOI:10.1016/j.ultsonch.2009.10.019 |
| [25] | Stroyuk O L, Ermokhina N I, Korzhak G V, et al. Photocatalytic and photoelectrochemical properties of hierarchical mesoporous TiO2 microspheres produced using a crown template[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2017, 334: 26-35. DOI:10.1016/j.jphotochem.2016.10.039 |
| [26] | Li Z Z, Wang S J, Wu J X, et al. Recent progress in defective TiO2 photocatalysts for energy and environmental applications[J]. Renewable and Sustainable Energy Reviews, 2022, 156. DOI:10.1016/j.rser.2021.111980 |
| [27] | Takehara M, Yoshimura I, Takizawa K, et al. Surface active N-acylglutamate: Ⅰ. Preparation of long chain N-acylglutamic acid[J]. Journal of the American Oil Chemists Society, 1972, 49(3): 157-161. DOI:10.1007/BF02633785 |
| [28] |
付小航, 王林祥, 李瑶, 等. 可见光响应手性TiO2复合光催化剂及其降解有机污染物[J]. 环境科学学报, 2021, 41(12): 4862-4870. Fu X H, Wang L X, Li Y, et al. Chiral TiO2-based photocatalysts with visible light response and their photo-degradation of organic pollutants[J]. Acta Scientiae Circumstantiae, 2021, 41(12): 4862-4870. |
| [29] | Zhu H W, Shang Y S, Jing Y K, et al. Synthesis of monodisperse mesoporous TiO2 nanospheres from a simple double-surfactant assembly-directed method for lithium storage[J]. ACS Applied Materials & Interfaces, 2016, 8(38): 25586-25594. |
| [30] | Wang T, Xu Z Y, Zhu Y C, et al. Preparation of weak-light-driven TiO2-based catalysts via adsorbed-layer nanoreactor synthesis and enhancement of their photo-degradation performance in seawater[J]. Applied Surface Science, 2017, 423: 528-537. DOI:10.1016/j.apsusc.2017.06.177 |
| [31] | Cao Y, Xing Z P, Shen Y C, et al. Mesoporous black Ti3+/N-TiO2 spheres for efficient visible-light-driven photocatalytic performance[J]. Chemical Engineering Journal, 2017, 325: 199-207. DOI:10.1016/j.cej.2017.05.080 |
| [32] | Bad'ura Z, Naldoni A, Qin S S, et al. Light-induced migration of spin defects in TiO2 nanosystems and their contribution to the H2 evolution catalysis from water[J]. ChemSusChem, 2021, 14(20): 4408-4414. DOI:10.1002/cssc.202101218 |
| [33] | Maimaiti H, Xu B, Sun J Y, et al. Photocatalytic synthesis of urea (CO2/N2/H2O) on coal-based carbon nanotubes with the Fe-core-supported Ti3+-TiO2 composite catalyst[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(20): 6991-7002. |
| [34] | Mazierski P, Mikolajczyk A, Bajorowicz B, et al. The role of lanthanides in TiO2-based photocatalysis: a review[J]. Applied Catalysis B: Environmental, 2018, 233: 301-317. |
| [35] |
张亮, 赵朝成, 高先瑶, 等. MoS2/BiOI复合光催化剂制备及其光催化氧化还原性能[J]. 环境科学, 2019, 40(1): 281-292. Zhang L, Zhao C C, Gao X Y, et al. Fabrication of the heterojunction photocatalyst MoS2/BiOI and its investigation of its photocatalytic reduction and oxidation activities[J]. Environmental Science, 2019, 40(1): 281-292. |
| [36] | Liang Y, Huang G H, Xin X Y, et al. Black titanium dioxide nanomaterials for photocatalytic removal of pollutants: a review[J]. Journal of Materials Science & Technology, 2022, 112: 239-262. |
| [37] |
闫增元, 习海玲, 袁立永. 金属有机框架MIL-53(Fe)可见光催化还原水中U(Ⅵ)[J]. 环境科学, 2019, 40(4): 1819-1825. Yan Z Y, Xi H L, Yuan L Y. Metal organic framework MIL-53(Fe) as a photocatalyst for visible-light catalytic reduction of U(Ⅵ) in aqueous solution[J]. Environmental Science, 2019, 40(4): 1819-1825. |
| [38] | Yan Z Y, Huang W X, Jiang X R, et al. Hollow structured black TiO2 with thickness-controllable microporous shells for enhanced visible-light-driven photocatalysis[J]. Microporous and Mesoporous Materials, 2021, 323. DOI:10.1016/j.micromeso.2021.111228 |
| [39] | Chen Y, Ran M J, Zhou Z Y, et al. Lanthanum/titanium dioxide immobilized onto industrial waste with enhanced photocatalytic activity, and the degradation of dimethyl phthalate[J]. Journal of Cleaner Production, 2021, 321. DOI:10.1016/j.jclepro.2021.129014 |
| [40] |
鲍玥, 周旻昀, 邹骏华, 等. C3N4/BiOBr复合可见光催化剂的性能及其作用机制[J]. 环境科学, 2017, 38(5): 2182-2190. Bao Y, Zhou M Y, Zou J H, et al. Performance and mechanism study of visible light-driven C3N4/BiOBr composite photocatalyst[J]. Environmental Science, 2017, 38(5): 2182-2190. |
| [41] | Tzeng J H, Weng C H, Chang C J, et al. N-Schorl TiO2 nanocomposite for visible-light photocatalysis deactivation yeast exemplified by Candida albicans[J]. Chemical Engineering Journal, 2022, 435. DOI:10.1016/j.cej.2021.134294 |
| [42] | Savić T D, Čomor M I, Abazović N D, et al. Anatase nanoparticles surface modified with fused ring salicylate-type ligands (1-hydroxy-2-naphthoic acids): a combined DFT and experimental study[J]. Journal of Alloys and Compounds, 2015, 630: 226-235. |
| [43] | Yang Z F, Xia X N, Shao L H, et al. Efficient photocatalytic degradation of tetracycline under visible light by Z-scheme Ag3PO4/mixed-valence MIL-88A(Fe) heterojunctions: mechanism insight, degradation pathways and DFT calculation[J]. Chemical Engineering Journal, 2021, 410. DOI:10.1016/j.cej.2021.128454 |
| [44] | Liu L, Han C J, Ding G F, et al. Oxygen vacancies-enriched Cu/Co bimetallic oxides catalysts for high-efficiency peroxymonosulfate activation to degrade TC: Insight into the increase of Cu+ triggered by Co doping[J]. Chemical Engineering Journal, 2022, 450. DOI:10.1016/j.cej.2022.138302 |
| [45] | Zhang C Y, Chen G J, Si Y T, et al. Surface modeling of photocatalytic materials for water splitting[J]. Physical Chemistry Chemical Physics, 2022, 24(3): 1237-1261. |
 2023, Vol. 44
2023, Vol. 44


