19世纪中叶, 随着微生物领域的快速发展, 饮用水中的细菌和病毒等微生物被证实是与霍乱和伤寒等介水疾病相关的致病物种, 需要在饮用水处理过程中被去除[1].尽管包括混凝、沉淀和过滤在内的传统水处理工艺对致病菌有一定去除作用, 但消毒工艺不仅可灭活水源水中的致病微生物, 还可通过出厂水中的剩余消毒剂抑制供水管网微生物滋生, 有效保障了生活饮用水的微生物安全[2].
消毒副产物(disinfection by-products, DBPs)是在消毒过程中由消毒剂与水中存在的天然有机物(NOM)、人为污染物及卤素离子等前体物质反应生成的一类次生污染物, 其浓度水平一般在ng·L-1~μg·L-1级别[3].毒理学研究显示, 大部分已被识别的DBPs具有细胞毒性、神经毒性和遗传毒性, 且含氮消毒副产物(nitrogenous DBPs, N-DBPs)的毒性高于含碳消毒副产物(carbonaceous DBPs, C-DBPs), 此外DBPs的毒性按卤素种类大致可如下排序: 碘代DBPs>溴代DBPs≫氯代DBPs[4].流行病学研究表明, 氯消毒饮用水的长期饮用和罹患膀胱癌、结肠癌和孕妇流产之间存在一定联系[5].自21世纪初以来, 饮用水中被识别的DBPs从500余种增至700余种[6, 7], 其中约百余种DBPs的细胞毒性和遗传毒性得到了毒理学试验研究[4], 数十种DBPs被纳入各国饮用水水质标准中[8, 9].
目前有关饮用水中DBPs的研究主要集中在以下方面: ①开发及优化DBPs的定量检测方法, 甄别饮用水中新型高毒性DBPs并对其进行定性定量分析[10]; ②调研饮用水中DBPs的浓度水平和分布特征, 基于水质及工艺参数建立和优化DBPs浓度预测模型[11]; ③识别DBPs前体物质并揭示相应的DBPs生成机制[12, 13]; ④探究DBPs的毒性特征和健康风险[4, 5], 研究方法包括毒理学试验及流行病学调查; ⑤研发DBPs的控制技术, 包括源头控制、过程控制和末端控制等方式[12~14].本文聚焦于饮用水中的DBPs, 介绍了饮用水中DBPs的主要分类及研究历程, 汇总了全球多地饮用水中DBPs的浓度水平和多国水质标准对DBPs类指标管控要求, 系统梳理了DBPs的各类控制方法, 并展望了未来有关DBPs控制方法的研究方向.
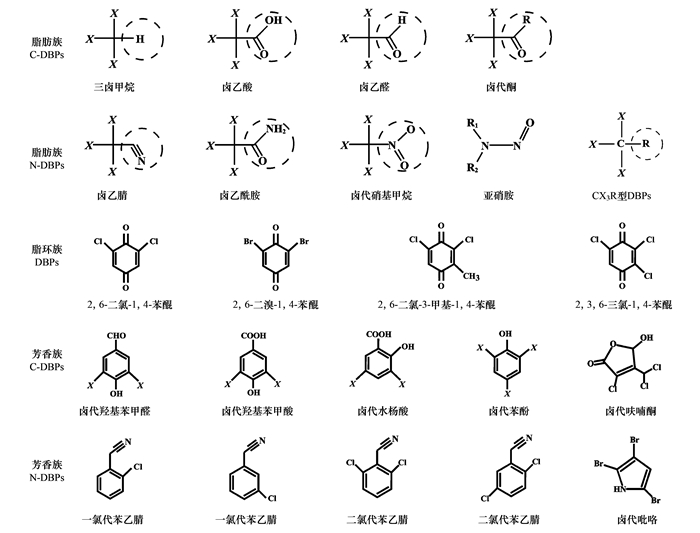
1 DBPs的主要分类和研究历程自1974年三卤甲烷(trihalomethanes, THMs)在加氯消毒的水中被发现以来[15, 16], 饮用水中的DBPs逐渐开始被人们重视, 相关领域也得到快速发展.总的看来, 常见DBPs可分为有机DBPs和无机DBPs, 目前受关注较多有机DBPs的分类及代表物质结构式如图 1所示, 其中一些已被纳入饮用水水质标准的DBPs(如THMs)和一些未被纳入标准但已知具有较高毒性的DBPs(如卤乙酰胺)皆包含CX3R的分子结构, 即在α碳位上有一个取代基和1~3个卤素原子, CX3R型DBPs由于具有毒性大、浓度高以及检出频繁的特点, 成为了一类具有代表性的DBPs[17~19].
|
X代表卤素或氢原子基团] 图 1 有机DBPs的分类及代表物质结构式 Fig. 1 Classification of organic DBPs and the structural formula of representative chemicals |
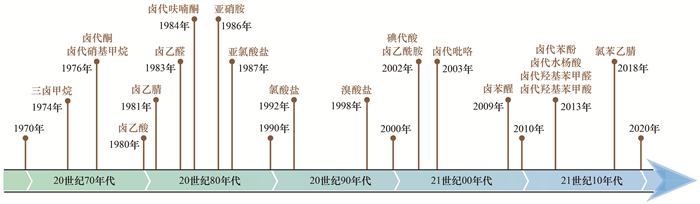
图 2展示了多类DBPs在饮用水中被发现的时间节点. 1974年, 荷兰化学家Rook[15]的研究发现氯消毒饮用水中的THMs浓度高于原水, 并猜测其是水中NOM与氯的反应产物; 同年, Bellar等[16]的研究提出, 消毒时增加氯的投量会导致饮用水中的THMs浓度升高. 1976年, 有研究者在检测饮用水厂出水中的挥发性有机物时发现卤代硝基甲烷(halonitromethanes, HNMs)类DBPs[20]; 同年, 卤代酮(haloketones, HKs)作为一类卤仿前体物在饮用水中被识别和分离[21].进入20世纪80年代后, 卤乙酸(haloacetic acids, HAAs)、卤乙腈(haloacetonitriles, HANs)和卤乙醛(haloacetaldehydes, HALs)先后在前体物消毒实验及饮用水中被检测发现[22~24]; 1984年Holmbom等[25]在氯化的造纸废水中识别出了高致诱变物质3-氯-4-二氯甲基-5-羟基-2(5氢)-呋喃酮(MX), 该团队随后于1986年在饮用水中检测到MX的存在[26]. 1986年, 加拿大开展的水质调研首次发现饮用水中也存在N-二甲基亚硝胺(N-nitrosodimethylamine, NDMA)[27].随后, 一些由替代消毒剂产生的无机DBPs相继被发现, 包括亚氯酸盐、氯酸盐和溴酸盐等[3, 28, 29].
|
图 2 饮用水中DBPs的识别历程 Fig. 2 Discovery process of DBPs in drinking water |
进入21世纪, 美国环保署(U.S. EPA)于2002年选取了全美12个典型饮用水厂展开DBPs浓度调研, 其发现了存在于饮用水中的卤乙酰胺(haloacetamides, HAMs)类DBPs和碘代酸类DBPs[30]. 2003年Richardson等[31]在以高溴水为原水的饮用水中发现卤代吡咯类DBPs. 2009年, Zhao等[32]在加拿大饮用水中首次检出一类脂环型DBPs卤苯醌, 随后对其生成机制、浓度分布及毒理效应展开了系统地研究. 2013年, Pan等[33]在氯消毒饮用水中检出了四大类芳香型DBPs, 分别是卤代苯酚、卤代水杨酸、卤代羟基苯甲酸和卤代羟基苯乙醛.时间推进至2018年, 中国饮用水中首次检出了一类芳香型N-DBPs氯苯乙腈, 其由于具有高毒性和高稳定性受到了广泛关注[34], 脂环族和芳香族类高毒性DBPs相关领域快速发展[35].
2 DBPs的浓度分布和限值要求表 1汇总了全球多地饮用水中常见DBPs的浓度水平, 总体来说, 饮用水中DBPs的浓度水平一般在ng·L-1~μg·L-1级别, 其中THMs和HAAs两大类脂肪族C-DBPs的质量浓度在不同消毒条件下均占主导地位, HALs的质量浓度水平占据第三位, 以三氯乙醛(TCAL)的浓度最高[30].对于HANs、HAMs和HNMs等脂肪族N-DBPs而言, 这几类DBPs中相较而言浓度较高且检出频率较高的物质包括: 二氯乙腈(DCAN)、二溴乙腈(DBAN)、二氯乙酰胺(DCAM)、二溴乙酰胺(DBAM)和三氯硝基甲烷(TCNM)[36].饮用水中同类脂肪族卤代DBPs的生成潜能可大致排序为: 氯代>溴氯代>溴代DBPs; 三卤代>二卤代>一卤代DBPs[37].此外, 已有的研究表明, 2, 6-二氯苯醌是卤苯醌类DBPs中检出率和浓度水平最高的一类物质[38], 另外氯苯乙腈类DBPs中检出浓度最高的物质为2-氯苯乙腈[34].
|
|
表 1 饮用水中常见DBPs的浓度水平 Table 1 Concentration levels of commonly occurring DBPs identified in drinking water |
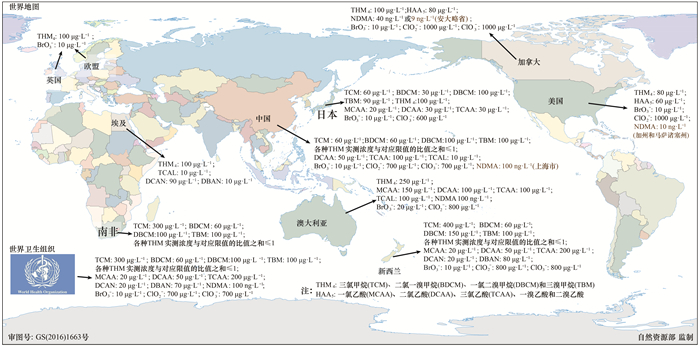
图 3展示了全球多个国家、地区及组织饮用水水质标准对DBPs指标的限值要求[9]. 总的看来, 全球多部饮用水水质标准对THMs和HAAs类C-DBPs以及溴酸盐、亚氯酸盐和氯酸盐等无机DBPs进行了限值规定, 另我国、埃及和澳大利亚将TCAL纳入了饮用水标准.除此之外, 包括NDMA和HANs在内的高风险N-DBPs日益引起关注, 我国上海市地方标准、美国加州及马萨诸塞州地方标准、加拿大国家标准、加拿大安大略省地方标准、澳大利亚国家标准和世界卫生组织(WHO)水质准则均有考虑NDMA指标, 另外埃及、新西兰和WHO为DCAN和DBAN两种HANs设置了浓度限值.
|
图 3 全球多个国家、地区和组织饮用水水质标准中DBPs指标的限值要求 Fig. 3 DBPs regulatory limits in drinking water quality standard set by various countries, regions and organizations |
饮用水中DBPs的控制方法大致可分为源头控制、过程控制、末端控制和协同控制这4大类.其中源头控制是指在消毒剂投加之前通过水源保护或饮用水厂处理工艺削减水中DBPs前体物的浓度; 过程控制即为通过改变消毒方式及优化消毒工艺等方式来减少DBPs的生成或改变DBPs的生成种类; 末端控制则是利用物理或化学方法去除一系列已生成的DBPs; 协同控制即是通过耦合源头、过程和末端控制方式以实现多类DBPs的高效控制[14].
3.1 源头控制 3.1.1 水源保护水源保护是通过降低水源水中DBPs前体物(包括NOM和卤素离子等)浓度以控制饮用水中DBPs含量.就控制NOM而言, 一方面可通过控制水源水的营养化程度以及营养物质的循环过程限制藻类的生长, 从而达到控制原水中藻源有机物的目的, 另一方面可利用河岸渗滤以及含水层储存和回采(ASR)等方式净化原水[14, 55].河岸渗滤是地表水体在进入两岸地下水系统或抽水井期间, 河床及周边含水层通过物理拦截渗透和化学生物转化等作用消减水中污染物并提升水源水质的过程.Krasner等[55]的研究发现, 河岸渗滤对总有机碳去除率约为30%, 而其对NDMA前体物的去除率可达64%.另ASR是在丰水季利用注水井将已处理的饮用水储存至合适的地下含水层中, 后续在需要时将水抽取出来并在重新消毒后输配至用户端.Singer等[56]的研究表明, ASR不仅可以去除饮用水中已生成的THMs和HAAs, 还可去除水中剩余的THMs和HAAs前体物.另就控制卤素离子而言, 首先需要防止海水或苦咸水入侵至饮用水水源, 其次需要关注水源地相关产业发展, 尤其是海产养殖业等易导致外加卤素进入水源的产业[57].
3.1.2 常规工艺和强化常规工艺DBPs的前体物特性各异, 如C-DBPs的前体物一般为疏水性、具有芳香结构的大分子物质[58], 而N-DBPs的前体物则更多是一些亲水性、富含氮元素的小分子物质[59].总的看来, 常规工艺(混凝-沉淀-砂滤)对溶解性有机碳(DOC)的去除率通常高于溶解性有机氮(DON), 期间C-DBPs前体物的控制效果优于N-DBPs.如Chu等[60]的研究显示, 混凝-沉淀-过滤对DOC和DON的平均去除率分别为47%和31%.另Zhang等[11]调研了我国太湖流域饮用水厂处理工艺对DBPs前体物的控制效果, 其中常规工艺对THMs、HAAs和HALs类C-DBPs前体物的去除率分别为30%、49%和20%, 对HANs、HNMs和HAMs类N-DBPs前体物的去除率分别为20%、33%和25%.
常规工艺主要是为了去除水中的悬浮颗粒, 而强化常规工艺可进一步改善常规工艺对溶解性有机物(DOM)的处理效果, 较显著地提高DOC和DON的去除率以及对DBPs前体物的控制效果.以聚合氯化铝作为混凝剂, Tongchang等[61]考察了粉末活性炭强化混凝对DOC和DON去除率的影响, 结果表明, 粉末活性炭强化混凝过程对DOC和DON的去除率分别可达85%和71%, 其中DOC去除率相较于非强化混凝工艺平均提升了30%.Zhao等[62]的研究发现, 以氯化铁为混凝剂进行强化混凝时DOC的去除率为57%, 而当混凝剂为聚合氯化铝时, 强化混凝工艺对THMs和HAAs前体物的去除率分别可达51%和59%.
3.1.3 预处理及深度处理工艺(1) 化学预氧化 化学预氧化是一类广泛用于饮用水厂的处理工艺, 可用于解决水中的色度及嗅味问题、去除NOM和无机离子、提高混凝工艺的效率以及处理原水中存在的藻类, 并在一定程度上控制后续消毒产生的DBPs, 常见的预氧化剂包括有氯、二氧化氯、臭氧、高锰酸钾以及高铁酸盐等[63, 64].在氯胺消毒前应用预氧化工艺可在一定程度上控制后续消毒时生成的NDMA浓度, 这是因为预氧化工艺可将NDMA前体物(如季铵盐类高分子助凝剂)转变为与氯胺反应活性较低的物质[65].Jiang等[66]考察了臭氧和高铁酸盐处理对后续氯/氯胺消毒生成DBPs的影响, 结果表明, 在该实验条件下两种预氧化处理均可控制THMs、HAAs以及HANs的生成, 但预臭氧会导致HKs和HNMs的浓度增加, 而高铁酸盐预氧化则可能会导致碘代DBPs的浓度升高.
但由于水中DBPs前体物种类繁多, 且不同前体物与各类氧化剂的反应活性、反应路径及反应产物迥异, 而预氧化剂的种类、预处理条件(预氧化剂投加量和反应pH条件等)以及对象水体的水质特征(如高藻水或高溴水)均会影响预氧化对DBPs前体物的影响, 则有关预氧化工艺对DBPs的控制效果很难得到定论.也有研究发现, 在特定前体物条件下预氧化处理也可能促进后续消毒时特定DBPs的产生[17, 64].
(2) 高级氧化 传统的高级氧化工艺(AOPs)指的是利用在环境温度和压力下原位生成的高活性羟基自由基(HO·)降解水中污染物的过程; 但随着硫酸根自由基(SO4-·)和氯自由基(Cl·)等多种自由基的相关研究不断发展, 现今的AOPs定义得到了拓展, 其它一些高活性化学自由基也被纳入范畴[67].利用AOPs控制DBPs前体物受到了广泛关注.
Ike等[68]详细综述了在氯/氯胺消毒前使用AOPs时对后续DBPs生成的影响, 提出水中DOM的特性以及AOPs产生自由基的浓度和种类均会影响实验结果.AOPs会改变DBPs前体物的性质, 当水中原有的DOM与消毒剂的反应活性较低时, 高级氧化工艺可能会导致后续消毒过程中生成的DBPs增多; 而当水中原有的DOM与消毒剂的反应活性较高时, 其与自由基的反应产物可能在消毒时生成更少DBPs.而当自由基的投加量足够致使体系发生矿化反应时, 此时原有DOM的性质不会影响实验结果, AOPs工艺可实现对有机DBPs的控制效果, 但会导致产生更多无机DBPs.而就自由基的种类而言, SO4-·相较于HO·和Cl·而言具有更高的选择性, 其对DOM中的芳香组分具有更好的降解效果, 可在整体上提高DOM的矿化率进而降低后续消毒时DBPs的生成量[68].但利用AOPs控制消毒副产物前体物时可能会致使生成更多溴酸盐、醛类物质以及卤代有机物等氧化副产物[67, 69].
(3) 离子交换 离子交换法是借助固态离子交换树脂中的离子与溶液中的离子进行可逆交换, 从而提取或去除溶液中的某些离子, 其在用于饮用水处理时可去除硝酸盐和氟离子等无机离子以及一些带电荷的有机物.根据离子交换树脂所带活性基团的性质可将其分为阳离子型、阴离子型和螯合型树脂几大类, 不同种类离子交换树脂的组成成分以及处理对象均存在差异.磁性离子交换(MIEX)树脂是一种具有磁性的以聚丙烯为骨架的大孔型强碱性阴离子交换树脂, 其功能基团为季铵基团, 可交换离子为氯离子[70].MIEX工艺被公认为是一种可高效去除原水中NOM的预处理工艺, 其具有运行灵活、占地面积小以及处理效能高等优势, 在全球多家水厂投入使用.
Bazri等[71]的研究表明, Purolite A860型强碱性阴离子交换树脂处理对腐殖质类NOM的去除率为40%~67%.而其对亲水性和非离子型NOM的去除率的去除率仅有12%~33%, 该过程中, C-DBPs前体物和N-DBPs前体物的去除率分别为13%~20%和3%~50%.此外, Gan等[72]考察了MIEX工艺对地表水中有机物以及多种DBPs前体物的控制效果, 结果显示, MIEX工艺对THMs前体物和HAAs前体物的去除率分别为39%~86%和42%~87%, 另HNMs前体物的去除率在9%~33%范围内.位于我国江苏省淮安市的北京路水厂是国内首座应用MIEX作为预处理工艺的自来水厂, 该水厂在运行过程中发现, MIEX工艺对原水中THMs前体物和HAAs前体物的去除率分别为34.4%和45.5%, 另MIEX工艺的使用还可降低后续消毒剂的投加量, 由此可知, MIEX工艺在一定程度上可实现对DBPs的控制[73, 74].但值得关注的是, 离子交换树脂已被证明是一种重要的NDMA前体物, 采用离子交换法可能导致后续消毒出水中NDMA浓度升高[72, 75].
(4) 活性炭吸附 活性炭吸附是一种有效的有机物分离工艺, 按照活性炭的形态可分为粉末活性炭(PAC)和颗粒活性炭(GAC), 其中PAC一般在应急时投加, 而以GAC作为滤料的滤池则是常见的水处理构筑物. 20世纪90年代Summers等[76]考察了GAC对于THMs前体物的去除效果, 实验结果表明, GAC具有很好的DOC去除效果以及THMs控制效果, 但GAC出水在加氯消毒时生成的THM4的溴取代系数明显高于进水; 另外Jacangelo等[77]的研究发现HAA5也有相同规律, 这是因为GAC并不能有效去除溴离子, 这一方面导致Br-与DOC的比值升高, 另一方面DOC的降低会致使消毒剂投量减小, 则此时Br-与Cl2的比值也相应升高.此外, Chili等[78]探究了GAC对于N-DBPs的控制效果, 结果发现GAC并不能有效去除N-DBPs前体物以及DON.考虑到DBPs的健康风险应结合浓度和毒性两个因素进行评价, 有学者对GAC处理后出水进行了毒性计算, 随后提出GAC对THMs及HAAs的控制效果并不适用于其它DBPs, 在应用GAC工艺时需重点关注溴代HNMs和溴代HANs这些高毒性DBPs[79, 80].
(5) 生物处理 现如今, 包括生物接触氧化以及生物活性炭滤池在内的生物处理工艺在饮用水厂受到了越来越多的应用, 一方面, 生物处理工艺生成的溶解性微生物产物和脱落的生物膜可在后续消毒工艺时充当DBPs的前体物[75]; 另一方面, 生物作用可降解或矿化DBPs前体物, 从而实现对DBPs的控制. Zhang等[81]考察了在微生物作用对20种氨基酸生成CX3R型DBPs的影响, 结果显示, 甘氨酸、精氨酸和天冬氨酸等数类氨基酸易被生物降解, 对应多类CX3R型DBPs生成潜能在生物处理后显著降低.而Bei等[82]的研究发现水中含氮有机质(如氨基酸)的微生物代谢过程会贡献重要的NDMA前体物.Liu等[83]详尽介绍了生物滤池对DBPs前体物的控制效果, 提出生物滤池可有效去除一系列卤代有机DBPs的前体物质, 但其对NDMA前体物的作用并不确定.此外, 预氧化处理、滤料种类、空床接触时间、反冲洗频率和时间、温度以及营养物质等处理方式或工艺参数均会影响生物滤池对DBPs的控制效果, 对其进行优化可实现对高浓度C-DBPs以及高毒性N-DBPs的协同控制[83].
(6) 膜滤法 膜滤法也是一种有效的有机物分离工艺, 其对于DOC和DBPs前体物的去除效果优于强化混凝工艺和GAC工艺[77].与GAC类似的是, 膜滤工艺出水在加氯消毒后产生的THM4的溴取代系数明显高于进水, 且该现象在进水DOC较低时尤为明显[76].早期的研究表明, 纳滤(NF)对THMs及HAAs前体物的去除率高达90%以上, 即使是在处理高溴水时, NF也可使DBPs生成总浓度降低[77].另外Ates等[84]同时研究了NF和超滤(UF)工艺对DBPs的控制效果, 结果显示, 在处理DOC较低的水样时, 孔径不超过1000的NF和UF可有效去除水中相对分子质量高的物质, 但对相对分子质量较小的物质(< 2 000)的去除效果较差, 且NF和UF处理均会导致Br-与DOC的比值升高, 致使生成更多溴代THMs和溴代HAAs.而在不同原水水质条件下考察NF对NDMA、THMs以及HNMs前体物去除效果的研究表明, 该过程一方面受到膜参数的影响, 另一方面还与原水水质参数有关[85].
3.1.4 组合工艺考虑到仅探究单种工艺对DBPs前体物的去除效果缺乏实际参考价值, 多位研究者通过中试实验考察了常用或新型组合工艺对饮用水中DBPs的去除效果. Hu等[86]的研究利用中试平台比较了13种常用工艺组合(包括4种预氧化方式和3种深度处理工艺)对多种DBPs及其综合毒性的控制效果, 结果显示, 针对该类原水, O3预氧化-常规工艺-O3-生物活性炭(BAC)工艺组合的出水具有最低的计算细胞毒性, 而ClO2预氧化-常规工艺-GAC(或O3-BAC)工艺组合的出水具有最低的计算遗传毒性.Andersson等[87]的研究对比了离子交换-陶瓷膜微滤-在线混凝-O3-GAC新型组合工艺与混凝-沉淀-快滤池-慢滤池常规组合工艺对DBPs前体物的去除效果, 结果表明, 新型组合工艺对THMs和总有机卤素(TOX)的控制效果优于常规组合工艺, 但新型组合工艺出水在氯化或氯胺化后生成的溴代DBPs更多.
3.2 过程控制 3.2.1 改变消毒方式常用的液氯/次钠消毒会生成较多THMs和HAAs等标准内DBPs, 为满足水质标准, 越来越多水厂开始使用其它消毒方式, 包括使用氯胺、紫外光(UV)、O3或ClO2等替代消毒剂, 或采用组合消毒方式, 如O3/氯、O3/氯胺、UV/氯和UV/氯胺等.
然而, 每种常见消毒剂的使用都会导致生成一些特定的DBPs.尽管氯胺及二氧化氯在消毒时生成的THMs、HAAs和TOX相较于氯消毒更少, 但这两种消毒剂生成的未知TOX比例更高, 且当原水中存在高浓度碘离子时, 仅利用氯胺或二氧化氯消毒可能生成较高浓度碘代DBPs, 增加饮用水的毒性风险[3, 88].此外, 氯胺的使用会造成NDMA及卤代氰生成, 而二氧化氯的使用通常会导致氯酸盐以及亚氯酸盐的产生[89].而用O3消毒时需要关注醛类物质及致癌物溴酸盐的生成[14].就组合消毒而言, 当O3与氯或氯胺联合使用时, 尽管预臭氧可去除一些DBPs的前体物(如NDMA前体物及碘离子等), 但会导致后续氯/氯胺消毒时生成更高浓度的HALs及HNMs[90]; 而当UV与氯或氯胺联用时, 由于UV会导致水中硝酸盐及亚硝酸盐的光解, 进而产生一系列活性氮物质并导致后续消毒过程中生成更多HNMs[89].需要强调的是, 在通过改变消毒方式以控制DBPs时, 消毒剂的消毒效果也是应纳入考虑的关键因素.在各类替代消毒剂中, 氯胺的氧化消毒能力较弱, 而UV和O3不能在管网中产生持续消毒效果.
3.2.2 优化消毒工艺Shah等[89]的研究提出, 相较于寻求一种不生成DBPs的消毒剂, 优化消毒方式可更高效地降低消毒后饮用水的健康风险.消毒条件(如pH和温度)及消毒剂的投加位置和投加方式等均会影响DBPs的生成种类和生成浓度.如Liang等[91]的研究发现pH值的增加会促进氯化过程中THMs的生成, 但三卤代HAAs浓度会随pH值的增加而降低; 另外碱性条件有利于HALs、HANs和HAMs等DBPs进行水解反应[92~94].与pH值类似, 水温一方面可能改变DBPs前体物与消毒剂的反应速率, 另一方面还会影响已生成DBPs的生物降解或化学去除(水解或脱羧)过程[95, 96].在通过优化消毒条件以控制DBPs的同时需关注人为调控pH值或水温带来的能耗问题, 此外出厂水的pH值及水温还会影响管网中的管材腐蚀及微生物生长情况.值得说明的是, 尽管消毒剂的投加剂量和消毒反应接触时间也会影响DBPs的生成情况[95], 但切记不可为控制DBPs忽略消毒工艺对致病微生物的灭活效果[97].
就消毒剂的投加位置而言, 考虑到GAC对芳香型卤代有机物的吸附效果优于其对NOM的吸附效果, Jiang等[98, 99]提出了一种新型的DBPs控制方法, 通过置换GAC工艺与消毒工艺的位置, 利用GAC的吸附作用去除一些氯化产生的芳香型卤代DBPs, 从而控制出水中DBPs浓度.考虑到该新型方法里GAC可将余氯耗尽, 研究者在GAC出水加入了消毒剂以保证余氯浓度, 结果显示此时出水中卤代DBPs浓度和出水的发育毒性均低于传统方法[100].
而在消毒剂的投加方式上, 陈超等[101]提出了一种新型氯化消毒工艺——顺序氯化消毒工艺, 即先加入氯进行游离氯消毒, 随后在一个较短的接触时间(< 15 min)后加入氨将游离氯转化为氯胺, 后续进行氯胺消毒.相较于传统氯消毒, 该种顺序氯化工艺被证明可有效控制DBPs的生成, 其中THMs和HAAs的生成浓度可降低50%以上[101].天然水体中存在多类耗氯物质, 为保障自由氯的消毒效果, 折点加氯工艺由此应运而生[102], 多位研究者提出折点加氯对DBPs的影响不可忽视, 尤其是具有较高健康风险的NDMA以及碘代DBPs[103~106].此外, 氯胺消毒时氯胺的投加方式(原位生成或投加预制氯胺)以及Cl2和NH3的投加顺序和比例也会影响DBPs的生成.Hayes-Larson等[107]的研究发现, 相较于预制氯胺, 相同条件下原位氯胺处理生成的HANs更多; 此外原位生成氯胺抑或采用预制氯胺还会影响高毒性碘代DBPs的生成[108, 109].考虑到二氯胺(NHCl2)是氯胺消毒时生成NDMA的主要反应物, Schreiber等[110]提出先投加Cl2再投加NH3可以防止加氯点处出现较高的氯氨比, 从而控制氯胺消毒过程中生成的NDMA.此外有研究表明, 在使用氯胺消毒时需要严格控制氯和氨的比值(4∶1或4.5∶1较宜), 这是因为当氨浓度过高时会导致给水管网中硝化细菌发生硝化反应从而引发亚硝酸盐问题, 另有研究指出当管网中发生硝化反应时, 此时的管壁生物膜会产生一些特定的DBPs前体物, 致使生成更多高毒性N-DBPs[14, 111].Charrois等[104]的研究发现相较于直接氯胺消毒, 先加入自由氯, 随后在一定接触时间后(2 h)再进行氯胺消毒可实现对NDMA的有效控制.
3.3 末端控制 3.3.1 物理法(1) 吸附法 就吸附法而言, 活性炭已被证明可通过吸附作用去除多种DBPs, 且其对某些DBPs的去除率可高达100%, 但很难吸附NDMA类强亲水性的DBPs[55, 80].Levesque等[112]考察了活性炭家用净水装置对龙头水中THMs及HAAs的去除效果, 结果显示THMs(约90%)的去除率高于HAAs(约70%).此外, 常用滤料石英砂(QS)也展示了对一系列DBPs的吸附效果, 实验结果表明, 单独使用QS对三氯乙腈的去除率可达80%[113].甘轶群[114]探究了家用净水器中常用的三级滤芯(PP棉、GAC和压缩活性炭)对7种卤代甲烷的去除效果, 结果表明, 3种吸附材料中GAC对卤代甲烷的去除率最高, 当三级滤芯串联使用时水中卤代甲烷的去除率可达81%~100%.王立伟[115]的研究发现, 不同流速条件下GAC对HAAs的去除效果均优于PP棉和压缩活性炭, 经过三级串联滤芯后, 水中7种目标HAAs类物质的去除率在16%~44%范围内.值得说明的是, 在利用吸附法去除DBPs时不能仅关注去除率, 还需考虑吸附材料的吸附容量以及DBPs的吸附动力学等参数.另外DBPs的吸附效果也会受到DBPs物化性质的影响, 如活性炭对THMs的去除率高于HAAs, 这是因为THMs的水溶性和极性更小, 更易通过吸附作用去除.
(2) 膜滤法 膜滤也是家庭净水处理中常见的一类工艺, 其可通过尺寸筛分原理去除饮用水中的微生物.现如今, 市面上家用净水器的处理工艺通常为前置三级滤芯作为预处理, 随后连接膜滤装置进行深度处理[114].由于大多数已被识别的DBPs相对分子质量较小(< 0.5×103), UF、NF以及反渗透(RO)可通过尺寸筛分及电荷排斥等机制去除一系列DBPs[116, 117].Fujioka等[118]的研究利用RO实现了对NDMA的有效去除, 去除率达71%.考虑到膜滤法的能耗较高且会产生浓水, Wang等[119]的研究尝试采用多级RO去除水中的HAAs, 结果表明5级RO对HAAs有较高的去除率(>75%), 该处理过程中水的回收率达87%.Weinberg等[120]的研究利用RO/去离子水系统去除实际龙头水中的DBPs, 结果显示, 该处理系统对THMs的去除率为48%, 对HAAs的去除率高达100%.顾昕等[121]调查了天津市两个供水区域内家用净水器(三级滤芯与滤膜联用)的使用情况和进出水水质变化, 结果表明, 该地区家用净水器中UF净水器和RO净水器分别占比70%和30%, 其中80%家用净水器对饮用水中THMs的去除率达75%以上, 另相较于UF净水器而言, RO净水器对THMs的去除率均值更高.值得说明的是, 未定期清理或更换滤芯及其它配件可能会导致家用净水膜滤装置出现微生物污染现象[112], 另有关RO会去除水中营养物质(如微量元素等)这一现象也受到广泛关注[122].
(3) 加热法 烧水是一种常用的家庭水处理技术, 对于无直饮水供应的国家及地区而言, 其是保障饮用水微生物安全最末端也是最重要的一道屏障.在水的加热过程中, 挥发性DBPs的浓度会因挥发作用而降低, 而其它部分难挥发的DBPs也可通过水解或脱羧等反应被去除[123, 124].相关研究结果表明, 在水的加热过程中, THMs的挥发作用占主导地位, 而HALs和HANs主要经历水解反应, 不同DBPs在加热过程中的去除率将受到DBPs性质(挥发性及稳定性)、水温、水中剩余消毒剂的种类和浓度以及烧水设备类型等因素影响[124].总的看来, 烧水可有效控制饮用水中DBPs, 期间THMs、HALs、HANs、HNMs和TOX浓度明显降低, 但加热过程中氯消毒饮用水中会持续生成MCAA和DCAA, 可能导致HAAs总浓度升高[125].
(4) 曝气吹脱法 U.S. EPA发布的有关控制饮用水中THMs的技术报告指出[126], 曝气法可实现THMs类DBPs的末端去除, 该过程中THM的去除效率随着物质相对分子质量的升高而降低, 即三氯甲烷(TCM)最易通过曝气法去除, 而期间三溴甲烷的去除率最低.Brooke等[127]的研究对比了扩散曝气和喷淋曝气两种方式对THMs的控制作用, 结果显示, 喷淋曝气对THMs的去除效果更好, THMs去除率受到液滴直径、液滴行进距离、水温和THM种类的影响.但值得说明的是, 曝气吹脱法只能用于去除挥发性DBPs, 而难以控制挥发性较差的DBPs[14], 另外在实际使用时采取曝气法去除DBPs也需要考虑相应的能耗问题.
(5) UV法 UV法既是一种常见的消毒工艺, 也可用于在末端去除已生成的DBPs.在利用UV法去除DBPs过程中, 一方面会发生DBPs的直接光解, 另一方面还可通过生成的HO·实现DBPs的间接光解[128].考虑到单独UV光解过程中生成的HO·有限, 则在利用UV法实现DBPs的末端控制时, 直接光解是降解DBPs的主要反应过程.除NDMA外, 一系列卤代DBPs也被发现可通过UV工艺去除, 且为基于紫外光用量的表观准一级反应速率常数呈一定规律: 三卤代DBPs>二卤代DBPs>一卤代DBPs; 碘代DBPs>溴代DBPs≫氯代DBPs[129, 130].如今, 家用净水器中常利用UV工艺在用户端去除饮用水中的致病菌, 其操作简单且不会影响饮用水的口感, 但需要考虑成本问题.
3.3.2 化学法从反应机制角度对化学法末端控制DBPs进行分类主要可以分为氧化法和还原法两类, 前者即指在氧化剂作用下去除DBPs, 常用的氧化法主要包括利用超声(US)、UV/H2O2、UV/过硫酸盐(PS)和UV/O3等AOPs, 该过程中发生的反应主要包括有氧化脱卤、脱羧及矿化; 而后者则是通过还原性物质实现DBPs的还原脱卤, 常用的还原法主要有零价铁(ZVI)及其衍生材料和工艺、亚硫酸盐处理、高级还原工艺(ARPs)和电化学法等.
3.3.2.1 氧化法(1) US工艺 US工艺在水处理中的应用受到了广泛关注, 该工艺的原理是利用空化气泡在破裂时产生的高温高压使水离解, 随即产生的具有强氧化性的HO·可用于降解污染物[131].初期有关US降解DBPs的研究主要关注THMs类物质, Guo等[132]的研究发现US对THMs有一定去除效果, 且该过程主要受到物质的自身性质(包括分子极性、蒸汽压和键离解能等)以及超声辐射声强的影响.随后相关研究得到进一步拓展, Yang等[113]的研究发现正辛醇/水分配系数对数值(lgKow)≤1.2的DBPs不可被超声去除, 而lgKow ≥ 1.97的DBPs受到超声处理时的去除率达20%以上.需要关注的是, 使用US工艺时需要考虑噪声以及能耗方面的问题, 则其在用于实际生产时可行性较低.
(2) AOPs工艺 包括UV/H2O2、UV/PS和UV/O3在内的基于UV的AOPs对DBPs具有较好的去除效果, NAs和HANs等多种DBPs在AOPs中的去除效果及反应机制以及动力学受到了广泛研究[130, 133~135].值得说明的是, 在利用这些基于UV的AOPs处理DBPs时, 一方面UV可直接光解某些DBPs, 另一方面会发生HO·或SO4-·主导的氧化反应(如使C—Cl或C—C键断裂)以及过氧离子的亲核攻击(如使腈基转变为酰胺基团)等过程[135, 136].但在考虑利用AOPs进行DBPs的末端去除时需要关注反应体系中加入的催化剂(如PS)可能造成的二次污染问题.
3.3.2.2 还原法(1) ZVI ZVI材料由于具有较强的还原性首先在地下水(受氯代有机物污染)的原位修复领域备受关注, 随后有研究者为提高ZVI效能进行了新材料制备以及反应条件优化, 由此衍生出一系列其它工艺[137].有研究发现, 单独的ZVI对HAMs、HAAs及溴酸盐等一系列DBPs具有去除效果, 而在该过程中加入金属铜则可进一步提高去除率[137~139]; 此外, 纳米零价铁材料及一系列改性或复合材料和铁系双金属材料(包括Cu/Fe和Pd/Fe)在用于处理DBPs时均展示出一定优势, 另外弱磁场条件也可改善ZVI对DBPs的去除效果[140~143].然而ZVI降解DBPs的反应速率较慢, 且该还原反应可能只是将高卤代DBPs转化成为低卤代DBPs, 则处理后饮用水的水质毒性并非一定会降低, 此外在末端控制时投加药剂材料可能引发饮用水二次污染问题, 可行性较低.
(2) 投加亚硫酸盐 亚硫酸盐是一种常用的淬灭剂, 用以淬灭水样中剩余的消毒剂从而防止DBPs在样品采集后继续生成.但亚硫酸盐具有较强的还原能力, 可使水中的DBPs发生还原脱卤反应.已有研究证明, HANs、HNMs和HAMs等DBPs均会被亚硫酸盐还原, 其中10种HAMs的降解反应动力学以及相关机制得到了深入的探究[144, 145].但该反应可能只是将高卤代DBPs转化成为低卤代DBPs, 仍需关注过程中水质毒性的变化.需要强调的是, 由于亚硫酸盐在该过程中会被氧化为硫酸盐, 而当存在较高浓度硫酸盐时可能会导致饮用水产生明显的味道, 另外还可能会腐蚀配水系统[146], 则在实际生活中利用该方法控制DBPs的可行性较低.
(3) ARPs工艺 ARPs是近几年兴起的一种水处理技术, 其是利用UV活化还原性物质(亚硫酸盐和连二亚硫酸盐等), 进而生成一系列还原性自由基用以降解污染物, 常见的还原性自由基包括有水合电子(eaq-)、氢原子(H·)和亚硫酸根自由基(SO3-·)等.利用ARPs可以有效地处理饮用水中的卤代DBPs, 包括有机DBPs(如HAMs)和无机DBPs(如溴酸盐)[147, 148].但应考虑的是饮用水厂的出厂水中需保证剩余消毒剂浓度以抑制微生物在供水管网中滋生, 则ARPs很难在水厂内应用, 而在用户端使用ARPs一方面需关注能耗和经济性问题, 另一方面还需考虑投加的化学试剂可能会造成饮用水的水质污染.
(4) 电化学工艺 电化学工艺由于具有高效低耗以及可在温和条件下进行等优势受到广泛关注, 在利用电化学法处理卤代有机物时, 相较于可能生成高毒性产物的氧化脱卤法, 电化学还原脱卤的产物通常是一些无机卤素离子和无毒有机物[149].按照主导还原物质的不同, 电化学还原脱卤反应可分为直接还原过程以及间接还原过程, 前者是通过阴极上产生的电子(e-)进行脱卤反应, 而后者则是利用一些还原性中间产物(如吸附氢Hads)[150].Li等[151]的研究利用Pd/Fe改性的碳纸电极作为阴极实现了氯代HAAs的高效去除, 发现在该过程中同时发生着两种还原过程.另外Li等[152]考察了活性炭电极材料对22种DBPs的去除效果, 在吸附和电化学的原理下, 该电极材料实现了对其中13种DBPs的高效去除, 去除率达90%以上.现如今, 电化学还原脱卤工艺在实际生产中应用的成熟度相对不够, 其中改性电极价格昂贵是制约其实现工业化应用的重要要素, 另相关反应机制和反应器设计也需进一步研究, 则现阶段较难实现在实际生活中利用电化学还原脱卤法去除饮用水中的DBPs.
3.4 协同控制饮用水中DBPs的控制方法如图 4所示, 其中源头控制、过程控制和末端控制这3种方法各有优劣.虽然源头控制不仅可降低水中DBPs前体物浓度还可降低水体的需氯量, 进而在后续消毒工艺中减少消毒剂的投加量和DBPs生成量, 但源头控制很难完全去除水中的DBPs前体物, 尤其是仅使用常规工艺的水厂对DBPs前体物的处理效果有限.就过程控制而言, 每种替代消毒剂的使用都会导致生成一些特定的DBPs, 在关注常规DBPs浓度的同时需要考虑一些更易由替代消毒剂生成的高毒性DBPs(如碘代DBPs和N-DBPs)及其对水质毒性的影响, 另通过优化消毒工艺进行DBPs的过程控制需在确保消毒效果及满足其它饮用水水质参数的前提下操作.而末端控制通常在用户端进行, 例如家用净水技术是保障饮用水安全的最后一道屏障, 由于饮用水中同时存在着剩余消毒剂和DBPs前体物, 则末端处理过程中通常也伴随着DBPs的生成与转化, 另相关能耗问题和二次污染带来的风险不容忽视.仅通过单种控制方法很难实现对各类DBPs的有效控制, 联用源头控制、过程控制和末端控制中的2~3种方法协同控制饮用水中的DBPs日益引起关注.

|
图 4 饮用水中DBPs的控制策略 Fig. 4 Strategies for DBPs control in drinking water |
Ding等[153]的研究比较了UV/H2O2预处理联合3种消毒方式(氯消毒、原位生成氯胺和先氯后氨)综合控制饮用水中DBPs浓度及毒性潜力的效果, 结果显示, 由于UV/H2O2能够破坏NOM的芳香性组分和DON成分, 该预处理工艺可致使后续消毒过程中C-DBPs生成浓度增加, 但期间N-DBPs生成浓度降低.另相较于单独氯消毒, 不论是原位生成氯胺抑或是先加氯后加氨均可降低CX3R型DBPs的总体生成浓度, 整体看来, UV/H2O2预处理协同原位氯胺处理可以使DBPs浓度和DBPs毒性潜力降至最低[153]. Chu等[154]的研究提出了一种耦合UV/PS预处理(源头控制)、消毒条件优化(过程控制)和物理曝气吹脱(末端控制)协同控制水中氯代N-DBPs的专利方法, 其中UV/PS工艺产生的强氧化性SO4-·可高效去除N-DBPs的前体物, 而针对SO4-·氧化后可能造成后续THMs类C-DBPs浓度增高的问题, 研究者调节水样pH以优化消毒条件并利用快速曝气措施去除已生成的TCM.
4 总结及展望DBPs是饮用水消毒过程中生成的一类具有潜在健康风险的次生污染物, 其浓度水平一般在ng·L-1~μg·L-1级别, 相关研究自20世纪70年代开始, 迄今已逾近50年.现如今饮用水中已被识别的DBPs超过700种, 按照化学结构对有机DBPs进行分类主要可分为脂肪族DBPs、脂环族DBPs及芳香族DBPs, 其中包含CX3R结构的一系列脂肪族DBPs由于具有毒性风险较大、浓度水平较高和检出频率较大的特点受到广泛关注.随着相关部门对DBPs的重视程度日益提高, 包括THMs、HAAs、HALs、HANs和NDMA在内的有机DBPs以及溴酸盐、亚氯酸盐和氯酸盐等无机DBPs已被纳入多个国家及组织的饮用水水质标准中.控制饮用水中的DBPs是全球饮用水安全保障领域的研究热点和难点之一, 其中常见的DBPs控制策略包括在水源或水厂削减DBPs前体物(源头控制), 改变消毒方式或优化消毒工况(过程控制), 以及通过物理法或化学法去除已生成DBPs(末端控制).但3种常见控制策略各有优劣, 如源头控制很难完全去除水中的DBPs前体物, 另每种替代消毒剂的使用都会导致生成一些特定DBPs, 而优化消毒工艺需在确保消毒效果及满足其它饮用水水质参数的前提下操作, 此外, 末端处理过程中通常也伴随着DBPs的转化与生成, 相关能耗问题和二次污染风险不容忽视.
饮用水DBPs研究发展至今, 无论是在分析识别、生成机制抑或是控制技术的研究领域中, 中国都是处于与国际接轨甚至领先的水平.但我国研究人员并不能止步于此, 未来还需要依据我国国情, 识别与我国水源水质特征和水处理工艺特点相符的、具有我国特性的高风险DBPs, 将分析检测技术、浓度调研结果、生成转化机制以及健康风险效应几部分相耦合, 提出一系列需优先控制的DBPs以纳入到我国国家以及地方饮用水水质标准之中, 对其进行有效的监管和控制.为有效降低饮用水中DBPs导致的环境和健康风险, 在此对DBPs控制方法的未来研究方向提出如下展望: ①在评价某种工艺或技术对DBPs的控制效果时, 以往研究主要考虑DBPs浓度的变化, 包括多种DBPs以及综合性指标TOX.但由于不同种类DBPs的毒性值大小各异, 可能出现DBPs总浓度明显降低但综合毒性未显著降低的情况.由此, 评估某种方法对DBPs的控制效果需要综合考虑DBPs浓度和综合毒性的变化.②考虑到常见的3类控制方法各有利弊, 未来相关研究建议关注DBPs的协同控制方法, 即耦合源头、过程及末端控制方法, 兼顾水源、水厂、管网及用户端家庭处理, 以实现对饮用水中各类DBPs的高效控制.
| [1] | Ellis K V. Water disinfection: a review with some consideration of the requirements of the third world[J]. Critical Reviews in Environmental Control, 1991, 20(5-6): 341-407. DOI:10.1080/10643389109388405 |
| [2] | Li X F, Mitch W A. Drinking water disinfection byproducts(DBPs)and human health effects: multidisciplinary challenges and opportunities[J]. Environmental Science & Technology, 2018, 52(4): 1681-1689. |
| [3] | Richardson S D, Plewa M J, Wagner E D, et al. Occurrence, genotoxicity, and carcinogenicity of regulated and emerging disinfection by-products in drinking water: a review and roadmap for research[J]. Mutation Research/Reviews in Mutation Research, 2007, 636(1-3): 178-242. DOI:10.1016/j.mrrev.2007.09.001 |
| [4] | Wagner E D, Plewa M J. CHO cell cytotoxicity and genotoxicity analyses of disinfection by-products: an updated review[J]. Journal of Environmental Sciences, 2017, 58: 64-76. DOI:10.1016/j.jes.2017.04.021 |
| [5] | Hrudey S E. Chlorination disinfection by-products, public health risk tradeoffs and me[J]. Water Research, 2009, 43(8): 2057-2092. DOI:10.1016/j.watres.2009.02.011 |
| [6] | Richardson S D. Disinfection by-products and other emerging contaminants in drinking water[J]. TrAC Trends in Analytical Chemistry, 2003, 22(10): 666-684. DOI:10.1016/S0165-9936(03)01003-3 |
| [7] | Richardson S D, Kimura S Y. Water analysis: emerging contaminants and current issues[J]. Analytical Chemistry, 2020, 92(1): 473-505. DOI:10.1021/acs.analchem.9b05269 |
| [8] | Wang X M, Mao Y Q, Tang S, et al. Disinfection byproducts in drinking water and regulatory compliance: a critical review[J]. Frontiers of Environmental Science & Engineering, 2015, 9(1): 3-15. |
| [9] |
肖融, 楚文海. 全球饮用水标准中消毒副产物管控指标对比与启示[J]. 环境科学研究, 2021, 34(6): 1328-1337. Xiao R, Chu W H. Disinfection by-products regulatory compliance in global drinking water standards: comparison and enlightenment[J]. Research of Environmental Sciences, 2021, 34(6): 1328-1337. |
| [10] | Ding S K, Chu W H. Recent advances in the analysis of nitrogenous disinfection by-products[J]. Trends in Environmental Analytical Chemistry, 2017, 14: 19-27. DOI:10.1016/j.teac.2017.04.001 |
| [11] | Zhang R H, Wang F F, Fang C, et al. Occurrence of CX3R-Type disinfection byproducts in drinking water treatment plants using DON-rich source water[J]. ACS ES & T Water, 2021, 1(3): 553-561. |
| [12] |
肖融, 楚文海. 从"源头到龙头"的前体物全过程来源分析消毒副产物的源头控制[J]. 给水排水, 2020, 46(9): 137-145. Xiao R, Chu W H. Source control of disinfection by-products in drinking water: a review from a precursor source perspective[J]. Water & Wastewater Engineering, 2020, 46(9): 137-145. |
| [13] | 高乃云, 楚文海, 徐斌. 从生成机制谈饮用水中新型消毒副产物的控制策略[J]. 给水排水, 2017, 43(2): 1-5. DOI:10.3969/j.issn.1002-8471.2017.02.001 |
| [14] | Singer P C. Control of disinfection by-products in drinking water[J]. Journal of Environmental Engineering, 1994, 120(4): 727-744. DOI:10.1061/(ASCE)0733-9372(1994)120:4(727) |
| [15] | Rook J J. Formation of haloforms during chlorination of natural waters[J]. Water Treatment Examination, 1974, 23(2): 234-243. |
| [16] | Bellar T A, Lichtenberg J J, Kroner R C. The occurrence of organohalides in chlorinated drinking waters[J]. Journal-American Water Works Association, 1974, 66(12): 703-706. DOI:10.1002/j.1551-8833.1974.tb02129.x |
| [17] | Yao D C, Chu W H, Bond T, et al. Impact of ClO2 pre-oxidation on the formation of CX3R-type DBPs from tyrosine-based amino acid precursors during chlorination and chloramination[J]. Chemosphere, 2018, 196: 25-34. DOI:10.1016/j.chemosphere.2017.12.143 |
| [18] | Fang C, Hu J L, Chu W H, et al. Formation of CX3R-type disinfection by-products during the chlorination of protein: the effect of enzymolysis[J]. Chemical Engineering Journal, 2019, 363: 309-317. DOI:10.1016/j.cej.2019.01.143 |
| [19] | Ding S K, Wang F F, Chu W H, et al. Effect of reduced sulfur group on the formation of CX3R-type disinfection by-products during chlor(am)ination of reduced sulfur compounds[J]. Chemical Engineering Journal, 2019, 361: 227-234. DOI:10.1016/j.cej.2018.12.069 |
| [20] | Hu J, Song H, Addison J W, et al. Halonitromethane formation potentials in drinking waters[J]. Water Research, 2010, 44(1): 105-114. DOI:10.1016/j.watres.2009.09.006 |
| [21] | Suffet I H, Brenner L, Silver B. Identification of 1, 1, 1-trichloroacetone(1, 1, 1-trichloropropanone)in two drinking waters: a known precursor in haloform reaction[J]. Environmental Science & Technology, 1976, 10(13): 1273-1275. |
| [22] | Norwood D L, Johnson J D, Christman R F, et al. Reactions of chlorine with selected aromatic models of aquatic humic material[J]. Environmental Science & Technology, 1980, 14(2): 187-190. |
| [23] | Miller J W, Uden P C. Characterization of nonvolatile aqueous chlorination products of humic substances[J]. Environmental Science & Technology, 1983, 17(3): 150-157. |
| [24] | Trehy M L, Bieber T I. Advances in the identification & analysis of organic pollutants in water[M]. Ann Arbor: Ann Arbor Science Publishers, 1981. |
| [25] | Holmbom B, Voss R H, Mortimer R D, et al. Fractionation, isolation and characterization of Ames-mutagenic compounds in kraft chlorination effluents[J]. Environmental Science & Technology, 1984, 18(5): 333-337. |
| [26] | Hemming J, Holmbom B, Reunanen M, et al. Determination of the strong mutagen 3-chloro-4-(dichloromethyl)-5-hydroxy-2(5H)-furanone in chlorinated drinking and humic waters[J]. Chemosphere, 1986, 15(5): 549-556. DOI:10.1016/0045-6535(86)90003-2 |
| [27] | Bond T, Huang J, Templeton M R, et al. Occurrence and control of nitrogenous disinfection by-products in drinking water-A review[J]. Water Research, 2011, 45(15): 4341-4354. DOI:10.1016/j.watres.2011.05.034 |
| [28] | Werdehoff K S, Singer P C. Chlorine dioxide effects on THMFP, TOXFP, and the formation of inorganic by-products[J]. Journal-American Water Works Association, 1987, 79(9): 107-113. DOI:10.1002/j.1551-8833.1987.tb02908.x |
| [29] | Bolyard M, Fair P S, Hautman D P. Occurrence of chlorate in hypochlorite solutions used for drinking water disinfection[J]. Environmental Science & Technology, 1992, 26(8): 1663-1665. |
| [30] | Krasner S W, Weinberg H S, Richardson S D, et al. Occurrence of a new generation of disinfection byproducts[J]. Environmental Science & Technology, 2006, 40(23): 7175-7185. |
| [31] | Richardson S D, Thruston A D, Rav-Acha C, et al. Tribromopyrrole, brominated acids, and other disinfection byproducts produced by disinfection of drinking water rich in bromide[J]. Environmental Science & Technology, 2003, 37(17): 3782-3793. |
| [32] | Zhao Y L, Qin F, Boyd J M, et al. Characterization and determination of chloro-and bromo-benzoquinones as new chlorination disinfection byproducts in drinking water[J]. Analytical Chemistry, 2010, 82(11): 4599-4605. DOI:10.1021/ac100708u |
| [33] | Pan Y, Zhang X R. Four groups of new aromatic halogenated disinfection byproducts: effect of bromide concentration on their formation and speciation in chlorinated drinking water[J]. Environmental Science & Technology, 2013, 47(3): 1265-1273. |
| [34] | Zhang D, Chu W H, Yu Y, et al. Occurrence and stability of chlorophenylacetonitriles: a new class of nitrogenous aromatic dbps in chlorinated and chloraminated drinking waters[J]. Environmental Science & Technology Letters, 2018, 5(6): 394-399. |
| [35] | Liu X Y, Chen L, Yang M T, et al. The occurrence, characteristics, transformation and control of aromatic disinfection by-products: a review[J]. Water Research, 2020, 184. DOI:10.1016/j.watres.2020.116076 |
| [36] | Mian H R, Hu G J, Hewage K, et al. Prioritization of unregulated disinfection by-products in drinking water distribution systems for human health risk mitigation: a critical review[J]. Water Research, 2018, 147: 112-131. DOI:10.1016/j.watres.2018.09.054 |
| [37] | Pressman J G, Richardson S D, Speth T F, et al. Concentration, chlorination, and chemical analysis of drinking water for disinfection byproduct mixtures health effects research: U.S. EPA's four lab study[J]. Environmental Science & Technology, 2010, 44(19): 7184-7192. |
| [38] | Zhao Y L, Anichina J, Lu X F, et al. Occurrence and formation of chloro-and bromo-benzoquinones during drinking water disinfection[J]. Water Research, 2012, 46(14): 4351-4360. DOI:10.1016/j.watres.2012.05.032 |
| [39] | Ding H H, Meng L P, Zhang H F, et al. Occurrence, profiling and prioritization of halogenated disinfection by-products in drinking water of China[J]. Environmental Science: Processes & Impacts, 2013, 15(7): 1424-1429. |
| [40] | Chu W H, Gao N Y, Yin D Q, et al. Trace determination of 13 haloacetamides in drinking water using liquid chromatography triple quadrupole mass spectrometry with atmospheric pressure chemical ionization[J]. Journal of Chromatography A, 2012, 1235: 178-181. DOI:10.1016/j.chroma.2012.02.074 |
| [41] | Wei J R, Ye B X, Wang W Y, et al. Spatial and temporal evaluations of disinfection by-products in drinking water distribution systems in Beijing, China[J]. Science of the Total Environment, 2010, 408(20): 4600-4606. DOI:10.1016/j.scitotenv.2010.06.053 |
| [42] | Chang H H, Tung H H, Chao C C, et al. Occurrence of haloacetic acids(HAAs)and trihalomethanes(THMs)in drinking water of Taiwan[J]. Environmental Monitoring and Assessment, 2010, 162(1): 237-250. |
| [43] | Kosaka K, Ohkubo K, Akiba M. Occurrence and formation of haloacetamides from chlorination at water purification plants across Japan[J]. Water Research, 2016, 106: 470-476. DOI:10.1016/j.watres.2016.10.029 |
| [44] | Nakai T, Kosaka K, Asami M, et al. Analysis and occurrence of 2, 6-dichloro-1, 4-benzoquinone in drinking water by liquid chromatography-tandem mass spectrometry[J]. Journal of Japan Society on Water Environment, 2015, 38(3): 67-73. DOI:10.2965/jswe.38.67 |
| [45] | Kawamoto T, Makihata N. Distribution of bromine/chlorine-containing disinfection by-products in tap water from different water sources in the hyogo prefecture[J]. Journal of Health Science, 2004, 50(3): 235-247. DOI:10.1248/jhs.50.235 |
| [46] | Lee K J, Kim B H, Hong J E, et al. A study on the distribution of chlorination by-products(CBPs)in treated water in Korea[J]. Water Research, 2001, 35(12): 2861-2872. DOI:10.1016/S0043-1354(00)00583-2 |
| [47] | Zhang Y P, Martinez D, Collins C, et al. Modelling of haloacetic acid concentrations in a United Kingdom drinking water system[J]. Journal of Water Supply Research and Technology-AQUA, 2011, 60(5): 275-285. DOI:10.2166/aqua.2011.047 |
| [48] | Bond T, Templeton M R, Kamal N H M, et al. Nitrogenous disinfection byproducts in English drinking water supply systems: occurrence, bromine substitution and correlation analysis[J]. Water Research, 2015, 85: 85-94. DOI:10.1016/j.watres.2015.08.015 |
| [49] | Goslan E H, Krasner S W, Bower M, et al. A comparison of disinfection by-products found in chlorinated and chloraminated drinking waters in Scotland[J]. Water Research, 2009, 43(18): 4698-4706. DOI:10.1016/j.watres.2009.07.029 |
| [50] | Villanueva C M, Castaño-Vinyals G, Moreno V, et al. Concentrations and correlations of disinfection by-products in municipal drinking water from an exposure assessment perspective[J]. Environmental Research, 2012, 114: 1-11. DOI:10.1016/j.envres.2012.02.002 |
| [51] | Samios S A, Golfinopoulos S K. Haloacetamides in the drinking water of Athens, Greece: Determination and degradation[J]. Analytical Letters, 2016, 49(7): 1091-1101. DOI:10.1080/00032719.2015.1065877 |
| [52] | Chowdhury S, Rodriguez M J, Sadiq R. Disinfection byproducts in Canadian provinces: associated cancer risks and medical expenses[J]. Journal of Hazardous Materials, 2011, 187(1-3): 574-584. DOI:10.1016/j.jhazmat.2011.01.085 |
| [53] | Simpson K L, Hayes K P. Drinking water disinfection by-products: an Australian perspective[J]. Water Research, 1998, 32(5): 1522-1528. DOI:10.1016/S0043-1354(97)00341-2 |
| [54] | Hammami B, Ben Hessin S, Bahri M, et al. Assessment of haloacetic acids in drinking water in Bizerte, Tunisia[J]. CLEAN-Soil, Air, Water, 2014, 42(8): 1052-1059. DOI:10.1002/clen.201300094 |
| [55] | Krasner S W, Mitch W A, McCurry D L, et al. Formation, precursors, control, and occurrence of nitrosamines in drinking water: a review[J]. Water Research, 2013, 47(13): 4433-4450. DOI:10.1016/j.watres.2013.04.050 |
| [56] | Singer P C, Pyne R D G, Avs M, et al. Examining the impact of aquifer storage and recovery on DBRs[J]. Journal-American Water Works Association, 1993, 85(11): 85-94. DOI:10.1002/j.1551-8833.1993.tb06106.x |
| [57] | Watson K, Farré M J, Knight N. Strategies for the removal of halides from drinking water sources, and their applicability in disinfection by-product minimisation: a critical review[J]. Journal of Environmental Management, 2012, 110: 276-298. DOI:10.1016/j.jenvman.2012.05.023 |
| [58] | Hua G H, Reckhow D A. Characterization of disinfection byproduct precursors based on hydrophobicity and molecular size[J]. Environmental Science & Technology, 2007, 41(9): 3309-3315. |
| [59] | Dotson A, Westerhoff P, Krasner S W. Nitrogen enriched dissolved organic matter(DOM)isolates and their affinity to form emerging disinfection by-products[J]. Water Science & Technology, 2009, 60(1): 135-143. |
| [60] | Chu W H, Gao N Y, Templeton M R, et al. Comparison of inclined plate sedimentation and dissolved air flotation for the minimisation of subsequent nitrogenous disinfection by-product formation[J]. Chemosphere, 2011, 83(5): 647-651. DOI:10.1016/j.chemosphere.2011.02.033 |
| [61] | Tongchang P, Kumsuvan J, Phatthalung W N, et al. Reduction by enhanced coagulation of dissolved organic nitrogen as a precursor of N-nitrosodimethylamine[J]. Journal of Environmental Science and Health, Part A, 2018, 53(6): 583-593. DOI:10.1080/10934529.2018.1428270 |
| [62] | Zhao Y M, Xiao F, Wang D S, et al. Disinfection byproduct precursor removal by enhanced coagulation and their distribution in chemical fractions[J]. Journal of Environmental Sciences, 2013, 25(11): 2207-2213. DOI:10.1016/S1001-0742(12)60286-1 |
| [63] | Camel V, Bermond A. The use of ozone and associated oxidation processes in drinking water treatment[J]. Water Research, 1998, 32(11): 3208-3222. DOI:10.1016/S0043-1354(98)00130-4 |
| [64] | Xie P C, Ma J, Fang J Y, et al. Comparison of permanganate preoxidation and preozonation on algae containing water: cell integrity, characteristics, and chlorinated disinfection byproduct formation[J]. Environmental Science & Technology, 2013, 47(24): 14051-14061. |
| [65] | Shah A D, Krasner S W, Lee C F T, et al. Trade-offs in disinfection byproduct formation associated with precursor preoxidation for control of N-nitrosodimethylamine formation[J]. Environmental Science & Technology, 2012, 46(9): 4809-4818. |
| [66] | Jiang Y J, Goodwill J E, Tobiason J E, et al. Comparison of ferrate and ozone pre-oxidation on disinfection byproduct formation from chlorination and chloramination[J]. Water Research, 2019, 156: 110-124. DOI:10.1016/j.watres.2019.02.051 |
| [67] | Miklos D B, Remy C, Jekel M, et al. Evaluation of advanced oxidation processes for water and wastewater treatment-A critical review[J]. Water Research, 2018, 139: 118-131. DOI:10.1016/j.watres.2018.03.042 |
| [68] | Ike I A, Lee Y, Hur J. Impacts of advanced oxidation processes on disinfection byproducts from dissolved organic matter upon post-chlor(am)ination: a critical review[J]. Chemical Engineering Journal, 2019, 375. DOI:10.1016/j.cej.2019.121929 |
| [69] | Lamsal R, Walsh M E, Gagnon G A. Comparison of advanced oxidation processes for the removal of natural organic matter[J]. Water Research, 2011, 45(10): 3263-3269. DOI:10.1016/j.watres.2011.03.038 |
| [70] | Levchuk I, Rueda Márquez J J, Sillanpää M. Removal of natural organic matter(NOM)from water by ion exchange - A review[J]. Chemosphere, 2018, 192: 90-104. DOI:10.1016/j.chemosphere.2017.10.101 |
| [71] | Bazri M M, Martijn B, Kroesbergen J, et al. Impact of anionic ion exchange resins on NOM fractions: Effect on N-DBPs and C-DBPs precursors[J]. Chemosphere, 2016, 144: 1988-1995. DOI:10.1016/j.chemosphere.2015.10.086 |
| [72] | Gan X J, Karanfil T, Kaplan Bekaroglu S S, et al. The control of N-DBP and C-DBP precursors with MIEXⓇ[J]. Water Research, 2013, 47(3): 1344-1352. DOI:10.1016/j.watres.2012.11.049 |
| [73] |
沈兆欢, 刘文君, 梁伟, 等. 淮安北京路净水厂MIEX树脂处理系统应用研究[J]. 给水排水, 2014, 50(4): 38-42. Shen Z H, Liu W J, Liang W, et al. Study on the application of magnetic ion exchange resin system in Beijing road water treatment plant, Huaian City[J]. Water & Wastewater Engineering, 2014, 50(4): 38-42. DOI:10.3969/j.issn.1002-8471.2014.04.008 |
| [74] |
姜春杰. 磁性离子交换技术在淮安北京路水厂的应用[J]. 中国给水排水, 2014, 30(16): 62-64, 67. Jiang C J. Application of magnetic ion exchange technique at Beijing road waterworks in Huaian City[J]. China Water & Wastewater, 2014, 30(16): 62-64, 67. |
| [75] | Ding S K, Deng Y, Bond T, et al. Disinfection byproduct formation during drinking water treatment and distribution: a review of unintended effects of engineering agents and materials[J]. Water Research, 2019, 160: 313-329. DOI:10.1016/j.watres.2019.05.024 |
| [76] | Summers R S, Benz M A, Shukairy H M, et al. Effect of separation processes on the formation of brominated THMs[J]. Journal-American Water Works Association, 1993, 85(1): 88-95. DOI:10.1002/j.1551-8833.1993.tb05925.x |
| [77] | Jacangelo J G, Demarco J, Owen D M, et al. Selected processes for removing NOM: an overview[J]. Journal-American Water Works Association, 1995, 87(1): 64-77. DOI:10.1002/j.1551-8833.1995.tb06302.x |
| [78] | Chili C A, Westerhoff P, Ghosh A. GAC removal of organic nitrogen and other DBP precursors[J]. Journal-American Water Works Association, 2012, 104(7): E406-E415. DOI:10.5942/jawwa.2012.104.0090 |
| [79] | Krasner S W, Lee T C F, Westerhoff P, et al. Granular activated carbon treatment may result in higher predicted genotoxicity in the presence of bromide[J]. Environmental Science & Technology, 2016, 50(17): 9583-9591. |
| [80] | Cuthbertson A A, Kimura S Y, Liberatore H K, et al. Does granular activated carbon with chlorination produce safer drinking water? From disinfection byproducts and total organic halogen to calculated toxicity[J]. Environmental Science & Technology, 2019, 53(10): 5987-5999. |
| [81] | Zhang R H, Wang F F, Chu W H, et al. Microbial degradation of typical amino acids and its impact on the formation of trihalomethanes, haloacetonitriles and haloacetamides during chlor(am)ination[J]. Water Research, 2019, 159: 55-64. DOI:10.1016/j.watres.2019.04.032 |
| [82] | Bei E, Li X, Wu F H, et al. Formation of N-nitrosodimethylamine precursors through the microbiological metabolism of nitrogenous substrates in water[J]. Water Research, 2020, 183. DOI:10.1016/j.watres.2020.116055 |
| [83] | Liu C, Olivares C I, Pinto A J, et al. The control of disinfection byproducts and their precursors in biologically active filtration processes[J]. Water Research, 2017, 124: 630-653. DOI:10.1016/j.watres.2017.07.080 |
| [84] | Ates N, Yilmaz L, Kitis M, et al. Removal of disinfection by-product precursors by UF and NF membranes in low-SUVA waters[J]. Journal of Membrane Science, 2009, 328(1-2): 104-112. DOI:10.1016/j.memsci.2008.11.044 |
| [85] | Ersan M S, Ladner D A, Karanfil T. The control of N-nitrosodimethylamine, Halonitromethane, and Trihalomethane precursors by Nanofiltration[J]. Water Research, 2016, 105: 274-281. DOI:10.1016/j.watres.2016.08.065 |
| [86] | Hu J L, Chu W H, Sui M H, et al. Comparison of drinking water treatment processes combinations for the minimization of subsequent disinfection by-products formation during chlorination and chloramination[J]. Chemical Engineering Journal, 2018, 335: 352-361. DOI:10.1016/j.cej.2017.10.144 |
| [87] | Andersson A, Lavonen E, Harir M, et al. Selective removal of natural organic matter during drinking water production changes the composition of disinfection by-products[J]. Environmental Science: Water Research & Technology, 2020, 6(3): 779-794. |
| [88] | Ye T, Xu B, Lin Y L, et al. Formation of iodinated disinfection by-products during oxidation of iodide-containing waters with chlorine dioxide[J]. Water Research, 2013, 47(9): 3006-3014. DOI:10.1016/j.watres.2013.03.003 |
| [89] | Shah A D, Mitch W A. Halonitroalkanes, halonitriles, haloamides, and N-nitrosamines: a critical review of nitrogenous disinfection byproduct formation pathways[J]. Environmental Science & Technology, 2012, 46(1): 119-131. |
| [90] | Krasner S W, Mitch W A, Westerhoff P, et al. Formation and control of emerging C-and N-DBPs in drinking water[J]. Journal-American Water Works Association, 2012, 104(11): E582-E595. DOI:10.5942/jawwa.2012.104.0148 |
| [91] | Liang L, Singer P C. Factors influencing the formation and relative distribution of haloacetic acids and trihalomethanes in drinking water[J]. Environmental Science & Technology, 2003, 37(13): 2920-2928. |
| [92] | Ding S K, Chu W H, Krasner S W, et al. The stability of chlorinated, brominated, and iodinated haloacetamides in drinking water[J]. Water Research, 2018, 142: 490-500. DOI:10.1016/j.watres.2018.06.024 |
| [93] | Yu Y, Reckhow D A. Kinetic analysis of haloacetonitrile stability in drinking waters[J]. Environmental Science & Technology, 2015, 49(18): 11028-11036. |
| [94] | Ma S C, Guo X Q, Chen B Y. Toward better understanding of chloral hydrate stability in water: Kinetics, pathways, and influencing factors[J]. Chemosphere, 2016, 157: 18-24. DOI:10.1016/j.chemosphere.2016.05.018 |
| [95] | Hua G H, Reckhow D A. DBP formation during chlorination and chloramination: effect of reaction time, pH, dosage, and temperature[J]. Journal-American Water Works Association, 2008, 100(8): 82-95. DOI:10.1002/j.1551-8833.2008.tb09702.x |
| [96] | Hong H C, Xiong Y J, Ruan M Y, et al. Factors affecting THMs, HAAs and HNMs formation of Jin Lan Reservoir water exposed to chlorine and monochloramine[J]. Science of the Total Environment, 2013, 444: 196-204. DOI:10.1016/j.scitotenv.2012.11.086 |
| [97] | Health Canada. Guidelines for Canadian drinking water quality-Summary Table[M]. Ottawa: Water and Air Quality Bureau, Healthy Environments and Consumer Safety Branch, 2019. |
| [98] | Jiang J Y, Zhang X R, Zhu X H, et al. Removal of intermediate aromatic halogenated DBPs by activated carbon adsorption: a new approach to controlling halogenated DBPs in chlorinated drinking water[J]. Environmental Science & Technology, 2017, 51(6): 3435-3444. |
| [99] | Jiang J Y, Zhang X R. A smart strategy for controlling disinfection byproducts by reversing the sequence of activated carbon adsorption and chlorine disinfection[J]. Science Bulletin, 2018, 63(18): 1167-1169. DOI:10.1016/j.scib.2018.07.022 |
| [100] | Jiang J Y, Li W X, Zhang X R, et al. A new approach to controlling halogenated DBPs by GAC adsorption of aromatic intermediates from chlorine disinfection: effects of bromide and contact time[J]. Separation and Purification Technology, 2018, 203: 260-267. DOI:10.1016/j.seppur.2018.04.050 |
| [101] |
陈超, 张晓健, 朱玲侠, 等. 控制消毒副产物及前体物的优化工艺组合[J]. 环境科学, 2005, 26(4): 87-94. Chen C, Zhang X J, Zhu L X, et al. Optimal process combination for control of disinfection by-products and precursors[J]. Environmental Science, 2005, 26(4): 87-94. |
| [102] | Rossum J R. A proposed mechanism for breakpoint chlorination[J]. Journal-American Water Works Association, 1943, 35(11): 1446-1449. DOI:10.1002/j.1551-8833.1943.tb18499.x |
| [103] | Amy G L, Chadik P A, King P H, et al. Chlorine utilization during trihalomethane formation in the presence of ammonia and bromide[J]. Environmental Science & Technology, 1984, 18(10): 781-786. |
| [104] | Charrois J W A, Hrudey S E. Breakpoint chlorination and free-chlorine contact time: Implications for drinking water N-nitrosodimethylamine concentrations[J]. Water Research, 2007, 41(3): 674-682. DOI:10.1016/j.watres.2006.07.031 |
| [105] | Park S H, Padhye L P, Wang P, et al. N-nitrosodimethylamine(NDMA)formation potential of amine-based water treatment polymers: effects of in situ chloramination, breakpoint chlorination, and pre-oxidation[J]. Journal of Hazardous Materials, 2015, 282: 133-140. DOI:10.1016/j.jhazmat.2014.07.044 |
| [106] | Liu Z, Lin Y Y, Xu B, et al. Formation of iodinated trihalomethanes during breakpoint chlorination of iodide-containing water[J]. Journal of Hazardous Materials, 2018, 353: 505-513. DOI:10.1016/j.jhazmat.2018.04.009 |
| [107] | Hayes-Larson E L, Mitch W A. Influence of the method of reagent addition on dichloroacetonitrile formation during chloramination[J]. Environmental Science & Technology, 2010, 44(2): 700-706. |
| [108] | Jones D B, Saglam A, Triger A, et al. I-THM formation and speciation: preformed monochloramine versus prechlorination followed by ammonia addition[J]. Environmental Science & Technology, 2011, 45(24): 10429-10437. |
| [109] | Fang C, Krasner S W, Chu W, et al. Formation and speciation of chlorinated, brominated, and iodinated haloacetamides in chloraminated iodide-containing waters[J]. Water Research, 2018, 145: 103-112. DOI:10.1016/j.watres.2018.07.074 |
| [110] | Schreiber I M, Mitch W A. Influence of the order of reagent addition on NDMA formation during chloramination[J]. Environmental Science & Technology, 2005, 39(10): 3811-3818. |
| [111] | Zeng T, Mitch W A. Impact of nitrification on the formation of N-nitrosamines and halogenated disinfection byproducts within distribution system storage facilities[J]. Environmental Science & Technology, 2016, 50(6): 2964-2973. |
| [112] | Levesque S, Rodriguez M J, Serodes J, et al. Effects of indoor drinking water handling on trihalomethanes and haloacetic acids[J]. Water Research, 2006, 40(15): 2921-2930. DOI:10.1016/j.watres.2006.06.004 |
| [113] | Yang W, Dong L L, Luo Z, et al. Application of ultrasound and quartz sand for the removal of disinfection byproducts from drinking water[J]. Chemosphere, 2014, 101: 34-40. DOI:10.1016/j.chemosphere.2013.11.018 |
| [114] |
甘轶群. 家庭常用设备对饮用水中卤代甲烷的去除研究[D]. 深圳: 哈尔滨工业大学深圳研究生院, 2015. Gan Y Q. A research of household methods for halomethane treatmen in drinking water[D]. Shenzhen: Harbin Institute of Technology Shenzhen Graduate School, 2015. |
| [115] |
王立伟. 家庭常用设备对水中卤代乙酸的去除研究[D]. 深圳: 哈尔滨工业大学深圳研究生院, 2015. Wang L W. An evaluation of household methods for haloacetic acids treatmen in water[D]. Shenzhen: Harbin Institute of Technology Shenzhen Graduate School, 2015. |
| [116] | Hua G H, Reckhow D A. Hydrophobicity and molecular size distribution of unknown TOX in drinking water[J]. Journal of Environmental Engineering, 2008, 134(3): 152-160. DOI:10.1061/(ASCE)0733-9372(2008)134:3(152) |
| [117] | Zazouli M A, Kalankesh L R. Removal of precursors and disinfection by-products(DBPs)by membrane filtration from water: a review[J]. Journal of Environmental Health Science and Engineering, 2017, 15. DOI:10.1186/s40201-017-0285-z |
| [118] | Fujioka T, Khan S J, McDonald J A, et al. N-nitrosamine rejection by nanofiltration and reverse osmosis membranes: the importance of membrane characteristics[J]. Desalination, 2013, 316: 67-75. DOI:10.1016/j.desal.2013.01.028 |
| [119] | Wang L, Sun Y N, Chen B Y. Rejection of haloacetic acids in water by multi-stage reverse osmosis: Efficiency, mechanisms, and influencing factors[J]. Water Research, 2018, 144: 383-392. DOI:10.1016/j.watres.2018.07.045 |
| [120] | Weinberg H S, Pereira V R P J, Singer P C, et al. Considerations for improving the accuracy of exposure to disinfection by-products by ingestion in epidemiologic studies[J]. Science of the Total Environment, 2006, 354(1): 35-42. DOI:10.1016/j.scitotenv.2004.12.016 |
| [121] |
顾昕, 翟洪艳, 柏慧. 饮用水中三卤甲烷健康风险和净水器净化能力评价[J]. 中国给水排水, 2020, 36(13): 31-37. Gu X, Zhai H Y, Bai H. Health risk assessment of trihalomethanes in drinking water and purification efficiency of water purifiers[J]. China Water & Wastewater, 2020, 36(13): 31-37. |
| [122] | Sedlak D L. The unintended consequences of the reverse osmosis revolution[J]. Environmental Science & Technology, 2019, 53(8): 3999-4000. |
| [123] | Wu W W, Benjamin M M, Korshin G V. Effects of thermal treatment on halogenated disinfection by-products in drinking water[J]. Water Research, 2001, 35(15): 3545-3550. DOI:10.1016/S0043-1354(01)00080-X |
| [124] | Krasner S W, Wright J M. The effect of boiling water on disinfection by-product exposure[J]. Water Research, 2005, 39(5): 855-864. DOI:10.1016/j.watres.2004.12.006 |
| [125] | Xiao R, Duan Y L, Chu W H. The effectiveness of household water treatment and safe storage in improving drinking water quality: a disinfection by-product(DBP)perspective[J]. Journal of Water Supply Research and Technology-AQUA, 2020, 69(8): 785-806. DOI:10.2166/aqua.2020.052 |
| [126] | US EPA. Treatment techniques for controlling trihalomethanes in drinking water[M]. Washington, DC: Office of Research and Development, 1981. |
| [127] | Brooke E, Collins M R. Posttreatment aeration to reduce THMs[J]. Journal-American Water Works Association, 2011, 103(10): 84-96. DOI:10.1002/j.1551-8833.2011.tb11550.x |
| [128] | Wang L, Niu R L, Chen B Y, et al. A comparison of photodegradation kinetics, mechanisms, and products between chlorinated and brominated/iodinated haloacetic acids in water[J]. Chemical Engineering Journal, 2017, 330: 1326-1333. DOI:10.1016/j.cej.2017.08.086 |
| [129] | Zhang Y Q, Xiao Y J, Zhang Y C, et al. UV direct photolysis of halogenated disinfection byproducts: experimental study and QSAR modeling[J]. Chemosphere, 2019, 235: 719-725. DOI:10.1016/j.chemosphere.2019.06.167 |
| [130] | Chuang Y H, Parker K M, Mitch W A. Development of predictive models for the degradation of halogenated disinfection byproducts during the UV/H2O2 advanced oxidation process[J]. Environmental Science & Technology, 2016, 50(20): 11209-11217. |
| [131] | Chowdhury P, Viraraghavan T. Sonochemical degradation of chlorinated organic compounds, phenolic compounds and organic dyes-a review[J]. Science of the Total Environment, 2009, 407(8): 2474-2492. DOI:10.1016/j.scitotenv.2008.12.031 |
| [132] | Guo Z B, Gu C H, Zheng Z, et al. Sonodegradation of halomethane mixtures in chlorinated drinking water[J]. Ultrasonics Sonochemistry, 2006, 13(6): 487-492. DOI:10.1016/j.ultsonch.2006.05.005 |
| [133] | Zhou C, Gao N Y, Deng Y, et al. Factors affecting ultraviolet irradiation/hydrogen peroxide(UV/H2O2)degradation of mixed N-nitrosamines in water[J]. Journal of Hazardous Materials, 2012, 231-232: 43-48. DOI:10.1016/j.jhazmat.2012.06.032 |
| [134] | Chen Z, Fang J Y, Fan C, et al. Oxidative degradation of N-Nitrosopyrrolidine by the ozone/UV process: Kinetics and pathways[J]. Chemosphere, 2016, 150: 731-739. DOI:10.1016/j.chemosphere.2015.12.046 |
| [135] | Hou S D, Ling L, Shang C, et al. Degradation kinetics and pathways of haloacetonitriles by the UV/persulfate process[J]. Chemical Engineering Journal, 2017, 320: 478-484. DOI:10.1016/j.cej.2017.03.042 |
| [136] | Ling L, Sun J L, Fang J Y, et al. Kinetics and mechanisms of degradation of chloroacetonitriles by the UV/H2O2 process[J]. Water Research, 2016, 99: 209-215. DOI:10.1016/j.watres.2016.04.056 |
| [137] | Gillham R W, O'Hannesin S F. Enhanced degradation of halogenated aliphatics by zero-valent iron[J]. Groundwater, 1994, 32(6): 958-967. DOI:10.1111/j.1745-6584.1994.tb00935.x |
| [138] | Xie L, Shang C. Effects of copper and palladium on the reduction of bromate by Fe(0)[J]. Chemosphere, 2006, 64(6): 919-930. DOI:10.1016/j.chemosphere.2006.01.042 |
| [139] | Chu W H, Li X, Bond T, et al. Copper increases reductive dehalogenation of haloacetamides by zero-valent iron in drinking water: reduction efficiency and integrated toxicity risk[J]. Water Research, 2016, 107: 141-150. DOI:10.1016/j.watres.2016.10.047 |
| [140] | Chen H F, Cao Y, Wei E Z, et al. Facile synthesis of graphene nano zero-valent iron composites and their efficient removal of trichloronitromethane from drinking water[J]. Chemosphere, 2016, 146: 32-39. DOI:10.1016/j.chemosphere.2015.11.095 |
| [141] | Zha X S, Ma L M, Liu Y. Reductive dehalogenation of brominated disinfection byproducts by iron based bimetallic systems[J]. RSC Advances, 2016, 6(20): 16323-16330. DOI:10.1039/C5RA26882F |
| [142] | Chen S H, Chu W H, Wei H B, et al. Reductive dechlorination of haloacetamides in drinking water by Cu/Fe bimetal[J]. Separation and Purification Technology, 2018, 203: 226-232. DOI:10.1016/j.seppur.2018.04.048 |
| [143] | Chen S H, Wang F F, Chu W H, et al. Weak magnetic field accelerates chloroacetamide removal by zero-valent iron in drinking water[J]. Chemical Engineering Journal, 2019, 358: 40-47. DOI:10.1016/j.cej.2018.09.212 |
| [144] | Ding S K, Wang F F, Chu W H, et al. Rapid degradation of brominated and iodinated haloacetamides with sulfite in drinking water: Degradation kinetics and mechanisms[J]. Water Research, 2018, 143: 325-333. DOI:10.1016/j.watres.2018.06.049 |
| [145] | Croue J P, Reckhow D A. Destruction of chlorination byproducts with sulfite[J]. Environmental Science & Technology, 1989, 23(11): 1412-1419. |
| [146] | WHO. Guidelines for drinking-water quality: fourth edition incorporating the first addendum[M]. Geneva: WHO, 2017. |
| [147] |
伏芝萱, 郭迎庆, 楚文海. 紫外/亚硫酸钠还原降解三氯乙酰胺的效能[J]. 环境科学, 2019, 40(5): 2271-2277. Fu Z X, Guo Y Q, Chu W H. Removal efficiency of trichloroacetamide by UV/sodium sulfite[J]. Environmental Science, 2019, 40(5): 2271-2277. |
| [148] | Xiao Q, Yu S L, Li L, et al. An overview of advanced reduction processes for bromate removal from drinking water: reducing agents, activation methods, applications and mechanisms[J]. Journal of Hazardous Materials, 2017, 324: 230-240. DOI:10.1016/j.jhazmat.2016.10.053 |
| [149] | Radjenovic J, Sedlak D L. Challenges and opportunities for electrochemical processes as next-generation technologies for the treatment of contaminated water[J]. Environmental Science & Technology, 2015, 49(19): 11292-11302. |
| [150] | Zhang M, Shi Q, Song X Z, et al. Recent electrochemical methods in electrochemical degradation of halogenated organics: a review[J]. Environmental Science and Pollution Research, 2019, 26(11): 10457-10486. DOI:10.1007/s11356-019-04533-3 |
| [151] | Li A Z, Zhao X, Hou Y N, et al. The electrocatalytic dechlorination of chloroacetic acids at electrodeposited Pd/Fe-modified carbon paper electrode[J]. Applied Catalysis B: Environmental, 2012, 111-112: 628-635. DOI:10.1016/j.apcatb.2011.11.016 |
| [152] | Li Y Q, Kemper J M, Datuin G, et al. Reductive dehalogenation of disinfection byproducts by an activated carbon-based electrode system[J]. Water Research, 2016, 98: 354-362. DOI:10.1016/j.watres.2016.04.019 |
| [153] | Ding S K, Wang F F, Chu W H, et al. Using UV/H2O2 pre-oxidation combined with an optimised disinfection scenario to control CX3R-type disinfection by-product formation[J]. Water Research, 2019, 167. DOI:10.1016/j.watres.2019.115096 |
| [154] | Chu W H, Li D M, Gao N Y, et al. Method for controlling chlorinated nitrogen-containing disinfection by-product in water[P]. United States: US 10723644B2, 2020-07-28. |
 2021, Vol. 42
2021, Vol. 42

