2. 南京大学环境纳米技术研究中心, 南京 210023
2. Research Center for Environmental Nanotechnology (ReCENT), Nanjing University, Nanjing 210023, China
市政污水深度处理与回用是解决全球水资源短缺的有效途径之一[1].市政污水二级出水中仍然存在一定量结构与组成复杂的溶解性出水有机质(dissolved effluent organic matter, dEfOM), 主要包括来自饮用水源的天然有机质(NOM)、生物处理过程中产生的微生物产物(SMPs)以及生活或工业中产生的一些微污染物[2].这些微污染物通常具有浓度低和难生物降解等特点, 且具有一定的生物毒性和致癌性[1, 2], 给再生水的回用带来不同程度的环境风险.因此, 对二级出水进行深度处理是保障再生水安全的常用技术手段.
高级氧化技术可产生氧化能力较强的自由基, 能快速高效地去除水中的众多污染物[3].在基于紫外的高级氧化技术中, 紫外/氯(UV/chlorine)高级氧化技术近年来受到了越来越多的关注[4, 5].紫外/氯技术能够高效降解有机污染物且具有一定的消毒作用[6], 该过程中可生成氧化性较强的HO·和具有选择性的含氯自由基(主要为Cl·、Cl2-·和ClO·)[7, 8]; 其中HO·可以与大部分有机污染物反应, 而含氯自由基可优先与富电子化合物反应[6, 9].这些共存的多种反应活性物种可以相互补充[10], 其对某些微污染物(如苯甲酸[11]、美托洛尔[12]和咖啡因[8]等)的降解效率甚至高于UV/H2O2技术.
目前, 有关紫外/氯技术的研究大多数是针对某种特定污染物的去除, 如布洛芬[13]、苯扎贝特[14]和卡马西平[6]等, 而对真实市政污水中dEfOM的研究关注不多.此外, 与dEfOM相关的研究往往仅利用紫外、红外或荧光等光谱法来表征简单的有机基团的组成及变化规律[15~17].然而, 由于dEfOM化学组成与结构复杂, 加上分析过程中谱线重叠等干扰, 一维光谱学研究还不能充分地反映有机物的结构信息[18].相比而言, 二维相关光谱技术(2DCOS)可以通过施加一定的外界扰动来更全面地反映有机官能团的变化规律[19], 是一种分析复杂样品的有效光谱学手段.
光谱学虽然能较好地反映出有机官能团的信息, 但还不能揭示复杂有机物体系更为精细的分子组成信息.近十多年来, 高分辨质谱的发展为dEfOM在分子水平的分析提供了可能.与较常用的飞行时间质谱和轨道阱质谱相比, 傅立叶变换离子回旋共振质谱(Fourier transform ion cyclotron resonance mass spectrometry, FT-ICR-MS)具有超高分辨率、超高质量精度和超高灵敏度等特点[1], 已广泛应用于复杂环境样品以及水处理过程中溶解性有机质的分子组成及转化规律的研究, 如混凝、生化和物化处理过程等[1, 20, 21].但目前还未见市政污水中的dEfOM在紫外/氯处理过程中分子转化规律的研究报道.此外, 由于氯的使用, 紫外/氯处理过程中不可避免地会产生一定量的氯代副产物(chlorinated byproducts, Cl-BPs).目前的大多数研究仅关注了常见Cl-BPs在紫外/氯处理过程中的浓度、生物毒性及遗传毒性的变化[22, 23], 未知Cl-BPs的分子组成和前体物-反应产物的转化信息尚不清楚.
本研究选择了两个市政污水处理厂的二级出水作为紫外/氯的处理对象, 采用紫外光谱和荧光光谱对处理前后的样品进行光谱学分析, 并对同步荧光数据采用二维相关光谱分析以探究荧光基团的先后反应顺序; 此外, 对反应前后的样品进行FT-ICR-MS分析, 以探究紫外/氯处理过程中dEfOM的分子组成及转化规律, 同时对Cl-BPs的生成进行了重点关注, 以期为市政污水二级出水中dEfOM在紫外/氯处理过程中的转化特性提供分子水平和深层次光谱学方面的信息, 同时为未知Cl-BPs的鉴别与生成机制提供基础信息.
1 材料与方法 1.1 水样的采集与预处理水样取自南京市的两个市政污水处理厂(WWTP)A和B(主体处理工艺均为A2/O)的二沉池出水.样品经0.45 μm的滤膜过滤后存放于棕色玻璃瓶中, 并在4℃低温保存.两污水处理厂二级出水的基本水质参数见表 1.
|
|
表 1 污水处理厂A和B二级出水的基本水质参数 Table 1 Water quality of secondary effluents from WWTP A and B |
1.2 紫外/氯处理二级出水
紫外/氯实验在0.9 L的圆柱形硼硅酸盐玻璃反应器内进行.采用功率为28 W的低压汞灯(ZSZ, 254 nm)进行紫外照射, 紫外灯置于配套的石英套管内, 并将其放入反应器中央.通过KI/KIO3分光光度法和低浓度H2O2的光解实验[24]分别测得该反应器在254 nm处的光通量为2.72×10-6 einsteins·s-1(1 mol光子的能量为1 einstein), 有效光程为4.51 cm, 平均光强度为1.36×10-8 einsteins·s-1·cm-2或6.42 mW·cm-2.
反应前紫外灯需提前预热15 min, 使光源工作状态保持稳定.取900 mL过滤后的二级出水, 加入到玻璃反应器中, 并将其放入恒温水浴箱中保持(25±1)℃.向反应溶液中加入一定量的次氯酸钠储备液, 使其自由氯浓度(以Cl2计)分别为0、0.1、0.3、0.5和0.7 mmol·L-1, 采用磁力搅拌, 总反应时间为30 min.反应后加入一定量的Na2SO3淬灭剂(Na2SO3与自由氯的量比为2∶1)对剩余的氧化剂进行淬灭, 测定样品处理前后的UV254和DOC.此外, 在自由氯投加量为0.5 mmol·L-1时, 分别取反应时间为0、1、3、5、7、10、15、20、25和30 min的样品进行UV254、DOC、同步荧光和自由氯浓度的测定, 并取30 min后的样品进行三卤甲烷和卤乙酸浓度的测定.
1.3 固相萃取采用安捷伦的PPL固相萃取柱(1 g, 6 mL)和默克的LiChrolut EN固相萃取柱(200 mg, 3 mL)串联, 对二级出水和紫外/氯反应30 min后的二级出水(分别用HCl将溶液的pH调至2)进行固相萃取.两种固相萃取柱分别用3倍柱体积的甲醇和3倍柱体积的酸化超纯水(pH=2的稀HCl)进行活化.将活化后的PPL柱和LiChrolut EN柱串联(LiChrolut EN柱在下、PPL柱在上)进行上样, 样品体积为400 mL, 流速约2 mL·min-1, 然后用3倍柱体积酸化超纯水淋洗固相萃取柱, 再用N2吹干柱内水分.最后, 分别用2倍柱体积的甲醇对PPL柱和LiChrolut EN柱进行洗脱, 将洗脱液放在氮吹仪上吹至5 mL, 在-20℃下避光保存待FT-ICR-MS分析.
1.4 分析方法 1.4.1 常规水质参数及荧光光谱分析样品的溶解性有机碳(DOC)及其在254 nm处的紫外吸光度(UV254)分别采用日本岛津的总有机碳分析仪(TOC-LCSH)和UV- 2600紫外可见分光光度计进行测定.样品中的4种三卤甲烷和9种卤乙酸分别通过液液萃取-气相色谱法[25]和离子色谱-电喷雾电离-串联质谱法[26]进行测定.常见阴离子使用离子色谱(ICS- 1100, Dion)进行测定, 阳离子使用电感耦合等离子体发射光谱仪(iCAP 7400, Thermo Fisher)进行测定; 采用日立F- 7000型荧光分光光度计进行同步荧光光谱分析, 在2Dshige软件中对同步荧光光谱数据进行2DCOS分析.
1.4.2 FT-ICR-MS分析(1) 仪器参数与操作步骤使用配备有15.0 T超导磁体和电喷雾电离源(ESI)的FT-ICR-MS(SolariX, Bruker)对样品中dEfOM的分子组成进行分析.样品在负离子模式下进行测试, 仪器进样方式为连续进样, 进样速度为120 μL·h-1, 毛细管入口电压为-3.8 kV, 离子累积时间为0.08 s, 相对分子质量采集范围为100~1 000, 采样点数为4 M(32位数据), 时域信号叠加300次以提高信噪比.样品检测前使用10 mmol·L-1甲酸钠溶液对仪器进行外标校正, 样品检测完成后使用已知分子式的NOM对图谱进行内标校正.经过校正后, 图谱的质量误差小于1.5×10-7.
(2) 数据处理使用Bruker DataAnalysis软件对FT-ICR-MS原始质谱数据进行校准.使用MATLAB程序对样品的分子式进行计算, 在分子式计算时仅考虑信噪比(S/N)大于5的质谱峰, 物质的元素组成及最大原子数目基于以下组合:12C1- 100 13C0- 11H1- 20016O0- 5014N0- 532S0- 331P0- 235Cl0- 3, 理论计算出的m/z与实际测得的m/z之间的误差绝对值须小于0.5×10-6.为确保分子式在化学组成上的合理性, 计算出的分子式还需满足以下条件[21, 27]:0.33≤H/C≤2.25、O/C≤1.0、N/C < 0.5、S/C < 0.2、P/C < 0.1、-10≤DBE-O≤10; 等效双键数DBE[DBE=(2C+N+P-H+2)/2]为非负整数; 还要满足偶氮规则.含氯物质需通过Bruker DataAnalysis软件进行同位素验证[28].
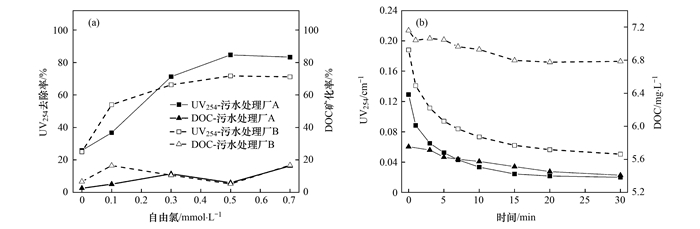
2 结果与讨论 2.1 紫外/氯处理过程中的水质参数变化紫外/氯处理前后二级出水的pH、DOC、电导率及阴阳离子浓度变化不大, 但UV254、三卤甲烷及卤乙酸的浓度均发生了较明显的变化.如图 1(a)所示, 在不同的氯投加量下, DOC一直保持较低的矿化率, 而UV254的去除率随氯投加量的增加逐渐增大, 这与Wang等[7]对紫外/氯处理NOM的研究结果类似.当氯投加量超过0.5 mmol·L-1时UV254的去除率不再明显增加, 因而后续实验均在氯投加量为0.5 mmol·L-1时进行.图 1(b)反映了氯投加量为0.5 mmol·L-1时的DOC和UV254随反应时间的变化规律, 与DOC相比, UV254呈明显的下降趋势, 说明dEfOM的整体矿化程度较低且芳香结构物质逐渐被破坏.对比Hua等[23]采用单独紫外光照、单独氯化处理和紫外/氯处理dEfOM的实验数据, 发现紫外/氯处理对UV254的去除率最高, 这表明含氯自由基对芳香族化合物的降解起着更重要的作用.
|
(a)不同氯投加量下DOC和UV254的去除效果(反应时间为30 min), (b)0.5 mmol·L-1氯投加量下DOC和UV254随时间的变化 图 1 紫外/氯处理过程中DOC和UV254的变化 Fig. 1 Variation of DOC and UV254 during UV/chlorine treatment |
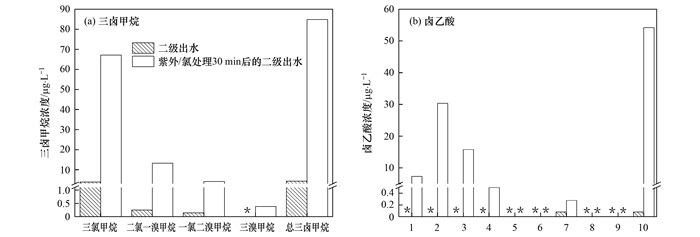
经紫外/氯处理30 min后的二级出水中的三卤甲烷和卤乙酸的浓度均明显提高.以污水处理厂A为例(图 2), 三卤甲烷中占比最高的三氯甲烷在处理后浓度提高了近20倍, 已超出《生活饮用水卫生标准》(GB 5749- 2006)中规定的限值(60 μg·L-1).而紫外/氯处理后卤乙酸的浓度更是提高了近1 000倍, 其中以氯乙酸(一氯乙酸、二氯乙酸和三氯乙酸)浓度的增加为主.二氯乙酸和三氯乙酸的浓度较高且具有潜在的致癌性[29], 在紫外/氯处理过程中需对Cl-BPs(如三氯甲烷和氯乙酸等)加以特别关注.
|
1.一氯乙酸, 2.二氯乙酸, 3.三氯乙酸, 4.一溴乙酸, 5.二溴乙酸, 6.三溴乙酸, 7.一溴一氯乙酸, 8.一溴二氯乙酸, 9.一氯二溴乙酸, 10.总卤乙酸; 氯投加量为0.5 mmol·L-1, 反应时间为30 min, *表示未检出 图 2 紫外/氯处理前后污水处理厂A的二级出水中三卤甲烷和卤乙酸的浓度 Fig. 2 Concentrations of trihalomethanes and haloacetic acids in secondary effluent from WWTP A, before and after UV/chlorine treatment |
荧光物质是dEfOM的重要组成部分, 紫外/氯处理不同时间的样品的同步荧光光谱图表明, 两个二级出水中蛋白组分含量最高(主要为酪氨酸和色氨酸), 富里酸组分次之, 而腐殖酸组分的荧光强度相对较低.随着反应时间的延长, 色氨酸、富里酸和腐殖酸组分的荧光强度均大大降低, 可见紫外/氯处理可有效破坏dEfOM中的荧光基团.与UV/H2O2技术相比, 紫外/氯过程对具有较高给电子能力的基团(如发色基团和荧光基团)的破坏能力更强[7, 23]; 酪氨酸组分变化不规律, 由于谱线产生重叠, 仅能判断出酪氨酸强度整体呈上升趋势.
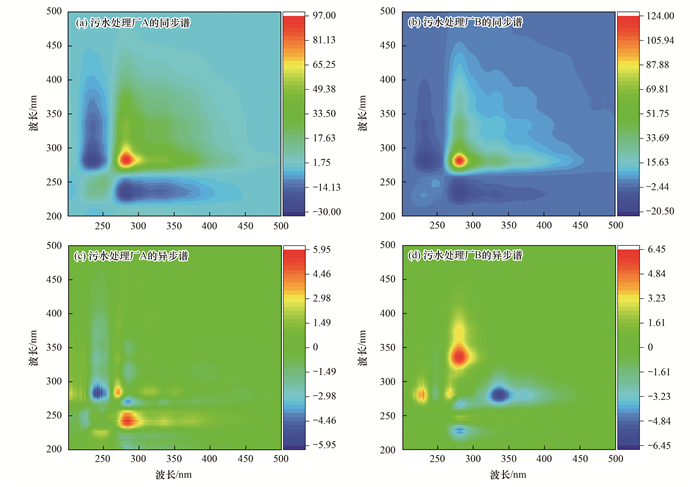
为提高光谱的分辨率, 采用二维相关同步荧光光谱进一步探究荧光基团的变化信息.如图 3所示, 230/235/250、280/285和335 nm处的荧光峰分别代表酪氨酸、色氨酸和富里酸[30, 31].污水处理厂A的同步谱图[图 3(a)]中有3个主要的自相关峰, 分别以235、250和285 nm为中心, 其中285 nm处的峰强度最大, 说明色氨酸组分反应程度最高.从同步谱的交叉峰中可以看出285 nm和335 nm处的交叉峰为正, 表明色氨酸和富里酸的强度随时间推移逐渐减小, 而235/250 nm和285 nm, 235/250 nm和335 nm处的交叉峰为负, 说明酪氨酸与色氨酸、富里酸的变化方向相反.污水处理厂B的同步谱图[图 3(b)]的结果与污水处理厂A一致.
|
以时间为扰动因子, 氯投加量为0.5 mmol·L-1; 不同颜色代表不同波长处测得光谱强度经傅里叶变换和交叉相关分析得到的二维相关光谱强度 图 3 紫外/氯处理过程中dEfOM的二维同步荧光相关光谱 Fig. 3 Two-dimensional synchronous fluorescence correlation spectrum of dEfOM during UV/chlorine treatment |
根据Noda规则[32], 同步和异步谱图中交叉峰的符号表明基团的反应先后顺序为:在污水处理厂A中, 酪氨酸先于色氨酸和富里酸反应; 而在污水处理厂B中, 色氨酸先于酪氨酸和富里酸反应.
2.3 紫外/氯处理过程中dEfOM的分子组成及转化规律本研究对紫外/氯处理前后的二级出水样品进行了FT-ICR-MS分析(氯投加量为0.5 mmol·L-1, 反应时间为30 min), 具体的分析结果如下.
2.3.1 分子组成以氧碳比(O/C)和氢碳比(H/C)作Van Krevelen图以分析不同样品dEfOM的分子组成.修正后的芳香指数(AImod)用来反映物质的芳香度情况, 计算公式如下:
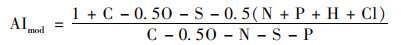
|
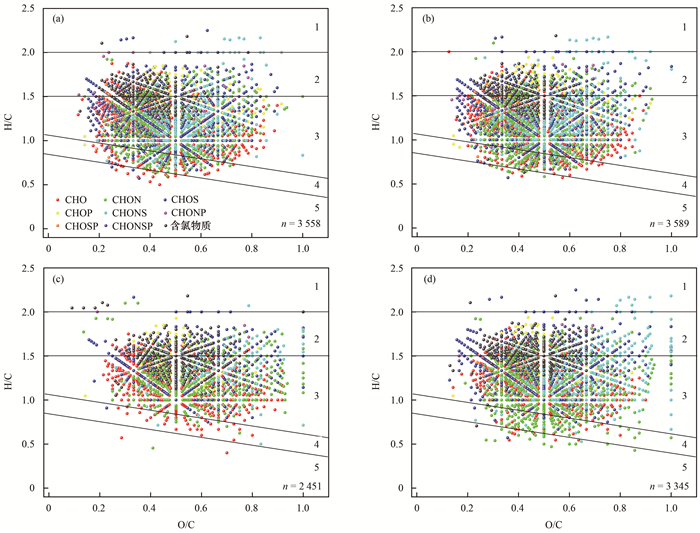
基于修正后的芳香指数和H/C将溶解性有机质分为5类[33]:稠环多环芳烃(AImod>0.66)、多酚类物质(0.5<AImod≤0.66)、高度不饱和类及酚类物质(AImod≤0.5且H/C≤1.5)、脂肪类物质(AImod≤0.5和1.5 < H/C≤2)和饱和类物质(H/C>2).如图 4所示, 二级出水中绝大部分有机物属于高度不饱和类及酚类物质、多酚类物质和脂肪类物质, 且大部分dEfOM属于CHO、CHOS和CHON类, 这与Geng等[1]的分析结果相似, 说明不同市政污水厂二级出水中dEfOM的物质组成及分子类别差别不大.从反应前后的分子总数来看, 紫外/氯处理仅矿化去除了小部分dEfOM, 而大部分dEfOM发生了转化或者未发生变化.
|
(a)和(b)污水处理厂A和B的二级出水, (c)和(d)紫外/氯处理30 min后污水处理厂A和B的二级出水; n代表样品的分子式总数; 区域1为饱和类物质, 区域2为脂肪类物质, 区域3为高度不饱和类及酚类物质, 区域4为多酚类物质, 区域5为稠环多环芳烃 图 4 紫外/氯处理前后污水处理厂A和B的二级出水的Van Krevelen图 Fig. 4 Van Krevelen diagrams of secondary effluents from WWTP A and B before and after UV/chlorine treatment |
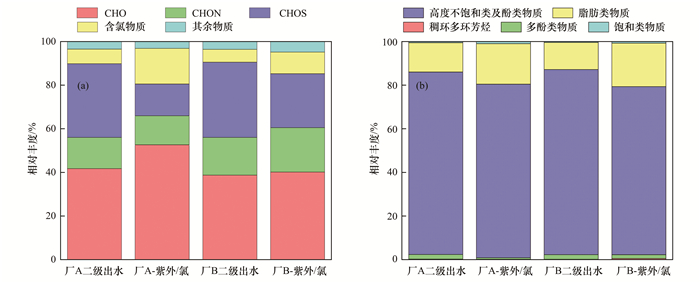
为了更清楚地反映紫外/氯处理前后分子组成的变化, 对分子式类别和物质类别进行了划分, 并在此基础上绘制了相对丰度.从图 5(a)中可以看出, dEfOM的分子式组成主要为CHO(38.74%~41.73%)、CHOS(33.84%~34.51%)、CHON(14.28%~17.29%)和含氯物质(5.90%~6.69%).紫外/氯处理后二级出水的CHO类和含氯类物质的相对丰度明显增加, 而CHOS类物质的丰度明显减少, 这表明紫外/氯处理可以使部分CHOS类物质转化为部分CHO类物质, 此外还会生成一定量的Cl-BPs.
|
(a)按分子类别划分, (b)按物质类别划分; 氯投加量为0.5 mmol·L-1, 反应时间为30 min 图 5 污水处理厂A和B的二级出水在紫外/氯处理前后分子组成的相对丰度 Fig. 5 Relative abundance of the molecular composition of secondary effluents before and after UV/chlorine treatment |
从图 5(b)中可以看出, 所有样品的物质类别中高度不饱和类及酚类物质占比最大(77.13%~84.94%), 脂肪类物质次之, 多酚类物质、稠环多环芳烃和饱和化合物相对丰度较小.而紫外/氯处理后脂肪类物质和饱和类物质的相对丰度明显增加, 高度不饱和类及酚类物质和多酚类物质的相对丰度均有所降低, 且前两类物质的增加比例与后两类物质的下降比例相近, 说明紫外/氯处理过程中发生了高度不饱和类及酚类物质和多酚类物质向脂肪类物质和饱和类物质的转化, 且高度不饱和类及酚类物质的转化对脂肪类物质相对丰度的增加贡献更大.
2.3.2 分子转化混合有机物在ESI电离时存在的离子抑制作用使得仅利用FT-ICR-MS的绝对峰强度无法进行定量分析[34], 因此, 在分析紫外/氯处理过程中的分子转化规律时, 需考虑反应前后峰强度的变化关系:
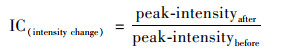
|
式中, IC为反应前后峰强度的变化倍数, peak-intensityafter为反应后的绝对峰强度, peak-intensitybefore为反应前的绝对峰强度.根据IC值大小可将反应前后的分子式分为3类:前体物(0≤IC < 0.5)、反应产物(IC>2.0)和难降解物质(0.5≤IC≤2.0)[34].
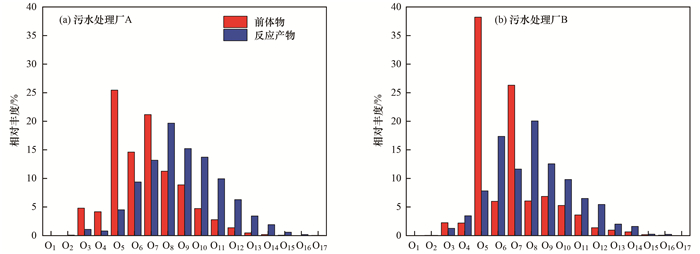
在紫外/氯处理过程中, dEfOM的分子组成发生了较大的变化, 说明该过程中发生了大量转化反应.从图 6中可以看出, Ox类物质的前体物与反应产物的相对丰度近似呈正态分布, 并且反应产物中高丰度物质的氧原子数略高于前体物, 表明在紫外/氯处理过程中存在某些加氧反应, 这应该是HO·与dEfOM发生氧化反应的结果.
|
图 6 二级出水中dEfOM在紫外/氯处理过程中前体物及反应产物的Ox类物质的相对丰度 Fig. 6 Relative abundance of Ox species of precursors and products in secondary effluents during UV/chlorine treatment |
根据不饱和度[(DBE-O)/C]和碳标称氧化态的正负值将dEfOM分为4个部分.其中, 碳标称氧化态表示为:
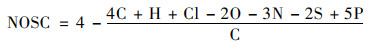
|
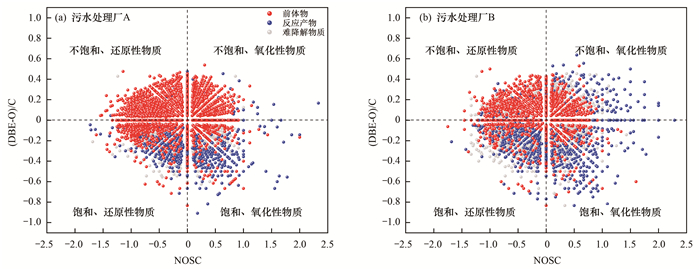
从图 7中可以看出, 前体物中不饱和及还原性物质(如烯烃和芳环)的占比最大(处理厂A: 34.74%, 处理厂B: 34.47%), 而紫外/氯处理后的大部分反应产物的(DBE-O)/C值均为负值, 并且反应后饱和及氧化性物质的增幅最大(处理厂A: 380.72%, 处理厂B: 150.71%), 说明紫外/氯反应会优先去除dEfOM中的不饱和及还原性物质, 并产生了大量的饱和及氧化性物质.
|
图 7 二级出水中dEfOM在紫外/氯处理过程中的的分子转化 Fig. 7 Molecular transformation of dEfOM in secondary effluents from WWTP A and B during UV/chlorine treatment |
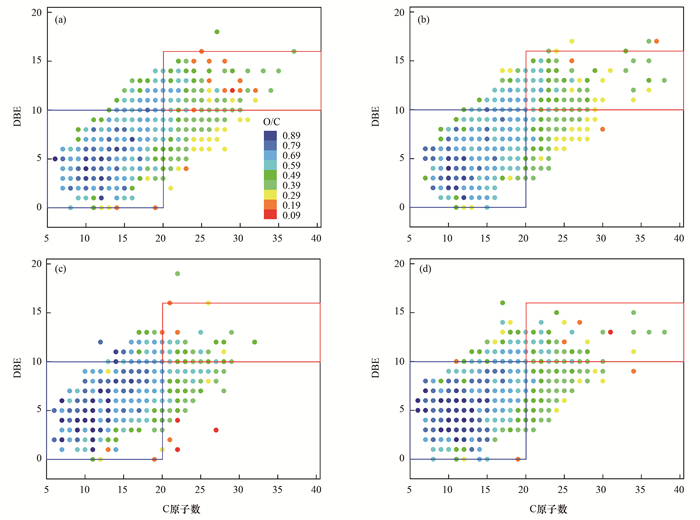
图 8更好地反映了紫外/氯处理过程中不同碳原子数与不同饱和度物质的转化规律.可以看出, 在等效双键数(DBE) < 10和5 < C原子数 < 20的范围内, 紫外/氯处理后物质的O/C明显增加, 说明这部分物质发生了加氧反应.在10 < DBE < 16的范围内有部分C原子数>20的物质在紫外/氯反应后被去除, 这表明部分大分子不饱和物质优先发生了反应, 其被降解为小分子物质或被进一步矿化.Varanasi等[35]的研究发现NOM中C原子数介于3~20的物质容易在紫外/氯处理过程中发生氧化, 同时含氯自由基会优先与NOM中分子量较大的不饱和芳香族化合物(DBE>15和C原子数>18)反应.
|
(a)和(b): 污水处理厂A和B的二级出水, (c)和(d): 紫外/氯处理30 min后污水处理厂A和B的二级出水; 圆点的颜色代表O/C的大小 图 8 等效双键数与碳原子数的分布 Fig. 8 Distribution of DBE vs. the number of carbon atoms |
在污水处理厂A和B的二级出水中分别发现了198个和191个含氯物质.这些含氯物质可能来源于进水中含氯的药物、个人护理品和含氯NOM、家用化学品与有机材料反应产生的含氯物质及SPE酸化过程中dEfOM与HCl的反应产物等[36~38].紫外/氯处理后含氯分子式的数量明显增加(处理厂A: 333个, 处理厂B: 270个), 其中新生成的Cl-BPs分别有255种和133种, 这些Cl-BPs主要由CHOCl(处理厂A: 79.21%, 处理厂B: 45.11%)和CHONCl(处理厂A: 20.78%, 处理厂B: 53.38%)组成.含氮BPs的毒性通常比含碳BPs要高[39], 因此以后的研究需要对这部分BPs的生成和去除过程加以关注.
虽然紫外/氯处理会增加Cl-BPs的形成, 但该过程同时促进了二级出水中有毒污染物的降解.在近期的研究中发现与单独氯化相比, 紫外/氯处理后的二级出水的急性毒性和遗传毒性均有所降低[23].
2.4.2 未知氯代副产物的前体物鉴别及生成机制在二级出水的氯化消毒过程中, 次氯酸与有机物的反应有3种可能的途径:氧化反应、加成反应和亲电取代反应[38].在紫外/氯反应过程中, 含氯自由基和HO·的氧化、加成和电子转移作用也是形成BPs的重要途径[40~42].
本研究基于亲电取代(-H+Cl)和加成反应(+HOCl)对未知Cl-BPs的前体物进行了鉴别.如表 2所示, 在紫外/氯处理前后的两个二级出水中共发现了12对基于亲电取代和43对基于加成反应的前体物-反应产物对, 这表明加成反应可能是紫外/氯处理过程中Cl-BPs形成的重要途径, 其可能是因为紫外/氯体系中的含氯自由基与dEfOM中的不饱和芳香族化合物的反应程度最高, 而含氯自由基又容易与芳香族化合物发生加成反应生成Cl-BPs[43].其他未检测到前体物的Cl-BPs可能是由相对分子质量大于1 000的前体物反应形成[38], 或是由于前体物发生氧化和自由基加成等多步反应生成的.
|
|
表 2 污水处理厂A和B的二级出水中Cl-BPs的前体物-反应产物配对分析结果 Table 2 Precursor-product pairs of Cl-BPs in secondary effluents from WWTP A and B |
3 结论
(1) 紫外/氯高级氧化技术易去除dEfOM中的芳香结构化合物, 且大部分物质只是发生了转化而非矿化.二维相关同步荧光光谱的分析结果表明, dEfOM中的荧光组分主要为蛋白质、类富里酸及类腐殖酸.紫外/氯高级氧化技术可以有效破坏dEfOM中的这些荧光基团, 且蛋白质比富里酸先发生反应.
(2) 两个污水处理厂二级出水中dEfOM的分子组成主要为CHO、CHOS和CHON类物质, 其物质类别主要为高度不饱和类及酚类物质、多酚类物质和脂肪类物质.紫外/氯处理会使部分CHOS类物质发生降解并生成部分CHO类物质, 该过程易使高度不饱和类及酚类物质向脂肪类物质转化.此外, dEfOM在紫外/氯处理过程中易发生一定的加氧反应, 该过程优先去除dEfOM中的大分子不饱和及还原性物质, 并生成小分子饱和及氧化性物质.
(3) 紫外/氯处理后, 三卤甲烷和卤乙酸的浓度均明显提高, dEfOM中含氯物质的数量也明显增加.在紫外/氯处理后的二级出水中分别检测到255和133种Cl-BPs, 这些Cl-BPs主要为CHOCl和CHONCl类物质.通过对Cl-BPs的前体物的鉴别, 共发现了12对基于亲电取代和43对基于加成反应的前体物-反应产物对.
| [1] | Geng C X, Cao N, Xu W, et al. Molecular characterization of organics removed by a covalently bound inorganic-organic hybrid coagulant for advanced treatment of municipal sewage[J]. Environmental Science & Technology, 2018, 52(21): 12642-12648. |
| [2] | Michael-Kordatou I, Michael C, Duan X, et al. Dissolved effluent organic matter: characteristics and potential implications in wastewater treatment and reuse applications[J]. Water Research, 2015, 77: 213-248. |
| [3] | Miklos D B, Remy C, Jekel M, et al. Evaluation of advanced oxidation processes for water and wastewater treatment- A critical review[J]. Water Research, 2018, 139: 118-131. DOI:10.1016/j.watres.2018.03.042 |
| [4] | Chuang Y H, Szczuka A, Shabani F, et al. Pilot-scale comparison of microfiltration/reverse osmosis and ozone/biological activated carbon with UV/hydrogen peroxide or UV/free chlorine AOP treatment for controlling disinfection byproducts during wastewater reuse[J]. Water Research, 2019, 152: 215-225. DOI:10.1016/j.watres.2018.12.062 |
| [5] | Guo K H, Wu Z H, Yan S W, et al. Comparison of the UV/chlorine and UV/H2 O2 processes in the degradation of PPCPs in simulated drinking water and wastewater: kinetics, radical mechanism and energy requirements[J]. Water Research, 2018, 147: 184-194. |
| [6] | Sun J L, Kong D Z, Aghdam E, et al. The influence of the UV/chlorine advanced oxidation of natural organic matter for micropollutant degradation on the formation of DBPs and toxicity during post-chlorination[J]. Chemical Engineering Journal, 2019, 373: 870-879. DOI:10.1016/j.cej.2019.05.096 |
| [7] | Wang W L, Zhang X, Wu Q Y, et al. Degradation of natural organic matter by UV/chlorine oxidation: molecular decomposition, formation of oxidation byproducts and cytotoxicity[J]. Water Research, 2017, 124: 251-258. DOI:10.1016/j.watres.2017.07.029 |
| [8] | Yang X, Sun J L, Fu W J, et al. PPCP degradation by UV/chlorine treatment and its impact on DBP formation potential in real waters[J]. Water Research, 2016, 98: 309-318. DOI:10.1016/j.watres.2016.04.011 |
| [9] | Li W T, Cao M J, Young T, et al. Application of UV absorbance and fluorescence indicators to assess the formation of biodegradable dissolved organic carbon and bromate during ozonation[J]. Water Research, 2017, 111: 154-162. |
| [10] | Gao Z C, Lin Y L, Xu B, et al. Effect of UV wavelength on humic acid degradation and disinfection by-product formation during the UV/chlorine process[J]. Water Research, 2019, 154: 199-209. DOI:10.1016/j.watres.2019.02.004 |
| [11] | Chuang Y H, Chen S, Chinn C J, et al. Comparing the UV/monochloramine and UV/free chlorine advanced oxidation processes (AOPs) to the UV/hydrogen peroxide AOP under scenarios relevant to potable reuse[J]. Environmental Science & Technology, 2017, 51(23): 13859-13868. |
| [12] | Gao Y Q, Zhang J, Li C, et al. Comparative evaluation of metoprolol degradation by UV/chlorine and UV/H2 O2 processes[J]. Chemosphere, 2020, 243. DOI:10.1016/j.chemosphere.2019.125325 |
| [13] | Cheng S S, Zhang X R, Yang X, et al. The multiple role of bromide ion in PPCPs degradation under UV/chlorine treatment[J]. Environmental Science & Technology, 2018, 52(4): 1806-1816. |
| [14] | Kong X J, Wu Z H, Ren Z R, et al. Degradation of lipid regulators by the UV/chlorine process: Radical mechanisms, chlorine oxide radical (ClO·)-mediated transformation pathways and toxicity changes[J]. Water Research, 2018, 137: 242-250. DOI:10.1016/j.watres.2018.03.004 |
| [15] | Li M, Chen Z Q, Wang Z Z, et al. Investigation on degradation behavior of dissolved effluent organic matter, organic micro-pollutants and bio-toxicity reduction from secondary effluent treated by ozonation[J]. Chemosphere, 2019, 217: 223-231. |
| [16] |
孙迎雪, 吴乾元, 田杰, 等. 污水中溶解性有机物组分特性及其氯消毒副产物生成潜能[J]. 环境科学, 2009, 30(8): 2282-2287. Sun Y X, Wu Q Y, Tian J, et al. Characteristics and chlorinated disinfection by-products formation potential of dissolved organic matter fractions in treated wastewater[J]. Environmental Science, 2009, 30(8): 2282-2287. DOI:10.3321/j.issn:0250-3301.2009.08.017 |
| [17] |
薛爽, 赵庆良, 魏亮亮. 氯化对二级处理出水中溶解性有机物结构的影响[J]. 环境科学, 2008, 29(4): 925-930. Xue S, Zhao Q L, Wei L L. Effect of chlorination on the structure of dissolved organic matters in secondary effluent[J]. Environmental Science, 2008, 29(4): 925-930. |
| [18] | Chen J, Gu B H, LeBoeuf E J, et al. Spectroscopic characterization of the structural and functional properties of natural organic matter fractions[J]. Chemosphere, 2002, 48(1): 59-68. |
| [19] | Chen W, Teng C Y, Qian C, et al. Characterizing properties and environmental behaviors of dissolved organic matter using two-dimensional correlation spectroscopic analysis[J]. Environmental Science & Technology, 2019, 53(9): 4683-4694. |
| [20] | Tseng L Y, Gonsior M, Schmitt-Kopplin P, et al. Molecular characteristics and differences of effluent organic matter from parallel activated sludge and integrated fixed-film activated sludge (IFAS) processes[J]. Environmental Science & Technology, 2013, 47(18): 10277-10284. |
| [21] | Zhang B L, Shan C, Hao Z N, et al. Transformation of dissolved organic matter during full-scale treatment of integrated chemical wastewater: Molecular composition correlated with spectral indexes and acute toxicity[J]. Water Research, 2019, 157: 472-482. |
| [22] | Zhang X R, Li W G, Blatchley Ⅲ E R, et al. UV/chlorine process for ammonia removal and disinfection by-product reduction: Comparison with chlorination[J]. Water Research, 2015, 68: 804-811. |
| [23] | Hua Z C, Li D, Wu Z H, et al. DBP formation and toxicity alteration during UV/chlorine treatment of wastewater and the effects of ammonia and bromide[J]. Water Research, 2021, 188. DOI:10.1016/j.watres.2020.116549 |
| [24] | Li X C, Ma J, Liu G F, et al. Efficient reductive dechlorination of monochloroacetic acid by sulfite/UV process[J]. Environmental Science & Technology, 2012, 46(13): 7342-7349. |
| [25] | Method 551.1, Determination of chlorination disinfection byproducts, chlorinated solvents, and halogenated pesticides/herbicides in drinking water by liquid-liquid extraction and gas chromatography with electron-capture detection[S]. |
| [26] | Cheng S, Wu Y P, Young T R, et al. Rapid determination of trace haloacetic acids in water and wastewater using non-suppressed ion chromatography with electrospray ionization-tandem mass spectrometry[J]. Science of the Total Environment, 2021, 754. DOI:10.1016/j.scitotenv.2020.142297 |
| [27] | Stubbins A, Spencer R G M, Chen H M, et al. Illuminated darkness: molecular signatures of Congo River dissolved organic matter and its photochemical alteration as revealed by ultrahigh precision mass spectrometry[J]. Limnology and Oceanography, 2010, 55(4): 1467-1477. |
| [28] | Yang M T, Zhang X R, Liang Q H, et al. Application of (LC/)MS/MS precursor ion scan for evaluating the occurrence, formation and control of polar halogenated DBPs in disinfected waters: a review[J]. Water Research, 2019, 158: 322-337. |
| [29] |
向红, 吕锡武. 饮用水中卤乙酸致癌性的研究进展[J]. 安全与环境工程, 2008, 15(1): 17-21. Xiang H, Lü X W. Study advance on carcinogenicity of haloacetic acids in drinking water[J]. Safety and Environmental Engineering, 2008, 15(1): 17-21. |
| [30] | Hur J, Jung K Y, Jung Y M. Characterization of spectral responses of humic substances upon UV irradiation using two-dimensional correlation spectroscopy[J]. Water Research, 2011, 45(9): 2965-2974. |
| [31] | Hu B, Wang P F, Wang C, et al. Investigating spectroscopic and copper-binding characteristics of organic matter derived from sediments and suspended particles using EEM-PARAFAC combined with two-dimensional fluorescence/FTIR correlation analyses[J]. Chemosphere, 2019, 219: 45-53. |
| [32] | Noda I. Techniques useful in two-dimensional correlation and codistribution spectroscopy (2DCOS and 2DCDS) analyses[J]. Journal of Molecular Structure, 2016, 1124: 29-41. |
| [33] | Hao Z N, Shi F Q, Cao D, et al. Freezing-induced bromate reduction by dissolved organic matter and the formation of organobromine compounds[J]. Environmental Science & Technology, 2020, 54(3): 1668-1676. |
| [34] | Bader T, Schulz W, Kümmerer K, et al. LC-HRMS data processing strategy for reliable sample comparison exemplified by the assessment of water treatment processes[J]. Analytical Chemistry, 2017, 89(24): 13219-13226. |
| [35] | Varanasi L, Coscarelli E, Khaksari M, et al. Transformations of dissolved organic matter induced by UV photolysis, hydroxyl radicals, chlorine radicals, and sulfate radicals in aqueous-phase UV-based advanced oxidation processes[J]. Water Research, 2018, 135: 22-30. |
| [36] | Gribble G W. The diversity of naturally produced organohalogens[J]. Chemosphere, 2003, 52(2): 289-297. |
| [37] | Lavonen E E, Gonsior M, Tranvik L J, et al. Selective chlorination of natural organic matter: identification of previously unknown disinfection byproducts[J]. Environmental Science & Technology, 2013, 47(5): 2264-2271. |
| [38] | Phungsai P, Kurisu F, Kasuga I, et al. Molecular characterization of low molecular weight dissolved organic matter in water reclamation processes using Orbitrap mass spectrometry[J]. Water Research, 2016, 100: 526-536. |
| [39] | Karanfil T, Krasner S W, Westerhoff P, et al. Disinfection by-products in drinking water: occurrence, formation, health effects, and control[M]. Washington: American Chemical Society, 2008: 36-50. |
| [40] | Xiang Y Y, Fang J Y, Shang C. Kinetics and pathways of ibuprofen degradation by the UV/chlorine advanced oxidation process[J]. Water Research, 2016, 90: 301-308. |
| [41] | Wu Z H, Fang J Y, Xiang Y Y, et al. Roles of reactive chlorine species in trimethoprim degradation in the UV/chlorine process: kinetics and transformation pathways[J]. Water Research, 2016, 104: 272-282. |
| [42] | Bulman D M, Remucal C K. Role of reactive halogen species in disinfection byproduct formation during chlorine photolysis[J]. Environmental Science & Technology, 2020, 54(15): 9629-9639. |
| [43] | Minakata D, Kamath D, Maetzold S. Mechanistic insight into the reactivity of chlorine-derived radicals in the aqueous-phase UV-chlorine advanced oxidation process: quantum mechanical calculations[J]. Environmental Science & Technology, 2017, 51(12): 6918-6926. |
 2021, Vol. 42
2021, Vol. 42


