2. 同济大学固体废物处理与资源化研究所, 上海 200092
2. Institute of Waste Treatment and Reclamation, Tongji University, Shanghai 200092, China
生活垃圾填埋场渗滤液是一类组成复杂的污水, 其水质特征随填埋龄相应变化, 主要表现为:随着填埋龄延长, 渗滤液的五日生化需氧量(biochemical oxygen demand after 5 Days, BOD5)与化学需氧量(chemical oxygen demand, COD)的比值及碳氮的质量比值均会下降.因此, 长填(埋)龄(填埋中后期)渗滤液可生物处理性降低, 其中, 特征性污染物为高浓度溶解性有机物和凯氏氮(Kjeldahl nitrogen, KN)包括有机氮(organic nitrogen, ON)和氨氮(NH4+-N)[1, 2], 须经处理达标后才可排放到受纳水体.
目前, 已有大量研究探索生活垃圾填埋场渗滤液处理组合工艺及其处理效率[3~5], 其中, 应用于工程规模的主流工艺主要为MBR与膜处理组合[6~9].MBR可通过生物作用去除渗滤液中90.3%~99.5%的NH4+-N[3, 10].此外, 由于长填龄渗滤液中的有机物以难生物降解物质为主[2], 不适用于MBR处理.膜处理可截留MBR不能去除的有机物、重金属及盐分[11~14], 通常采用纳滤(nanofiltration, NF)、反渗透(reverse osmosis, RO)或将二者串联, 其中RO处理效果最为显著, 但处理费用较高[1].近期, 已有学者探究MBR与膜处理组合工艺的运行效果.Wang等[7]的研究发现“MBR+NF”组合工艺对新鲜渗滤液总氮和COD的去除率分别为90.4%和99.9%; Chen等[8]的研究表明“MBR+RO”组合工艺对新鲜渗滤液和长填龄渗滤液混合污水的总氮和COD去除率均可达到99%以上.但是, 现有工程规模的MBR和膜处理组合工艺存在处理流程复杂且冗长, 处理成本高等问题, 而已有研究注重组合工艺的整体处理能效, 却忽视了各单元处理效能, 或是只针对某类污染物去除效果而缺乏多指标的综合评估, 或只采用COD这类总量性的有机物指标.而且, 针对长填埋龄渗滤液的处理效能评估更少.因此, 为了提供长填龄渗滤液处理设施单元设计依据, 有必要开展对其工程规模设施各单元处理效能的评估研究.
渗滤液处理效能一般采用排放标准规定水质指标评价, 其中COD是一个关键指标.Bu等[4]和Liu等[5]的研究发现渗滤液中COD的主要贡献者为溶解性有机物(dissolved organic matters, DOM).因分析便捷, 三维荧光光谱(excitation emission matrix, EEM)被广泛用于DOM分析[13, 15, 16].EEM通过结合荧光区域积分或平行因子分析(parallel factor analysis, PARAFAC)等数据处理方法, 可实现DOM的快速识别(如腐殖质、蛋白类和酚类化合物以及人造化学物等)[17, 18].其中, EEMs-PARAFAC已用于分析渗滤液处理过程中DOM变化[6], 可为探讨长填龄渗滤液DOM的去除机制提供支撑.
据此, 本文以工程规模“MBR+NF”组合工艺设施为研究对象, 监测长填龄渗滤液在该设施各单元中主要水质指标变化情况; 同时, 采用EEMs-PARAFAC追踪分析长填龄渗滤液处理过程中DOM的转化, 通过评估处理工艺各单元对长填龄渗滤液中污染物的去除效能, 以期为长填龄渗滤液处理及同类工艺的优化应用提供理论依据.
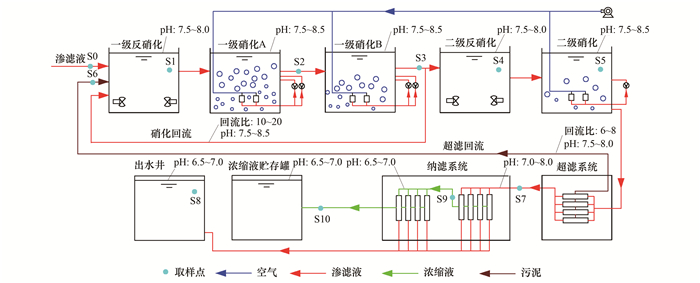
1 材料与方法 1.1 样品采集本文的研究对象为上海市某生活垃圾填埋场的渗滤液处理设施, 该填埋场已运行11 a, 日均垃圾填埋量为2×103~3×103 t·d-1.目前, 其处置垃圾的主要物理组分为有机垃圾(22.3%), 纸类和塑料类分别占23.6%和18.8%[19].长填龄渗滤液处理设施设计规模为1 000 m3·d-1, 实际处理量约为800 m3·d-1, 处理出水水质符合《GB/T 31962-2015污水排入城镇下水道水质标准》要求.渗滤液进行氨吹脱预处理, 调节氨氮浓度 <2 500 mg·L-1; 而后进主体处理工艺“MBR+NF”(工艺流程, 如图 1), 其中生物反应工艺为两段反硝化-硝化, 膜生物反应器为外置式超滤.为补充长填龄渗滤液反硝化碳源的不足, 该设施根据在线监测反硝化单元进水COD/(NH4+-N+NO3--N)值, 投加甲醇、乙酸钠和葡萄糖的复合碳源, 由于渗滤液水质存在波动, 投加的碳源也相应变化, 本研究采样期间, 一级反硝化和二级反硝化平均的投加量分别为8.2 t·d-1和1.6 t·d-1.除此之外, 为实现纳滤单元的高产水率, 一次纳滤处理后得到的浓缩液会进行二次纳滤浓缩.
|
图 1 长填龄渗滤液工程化处理流程示意 Fig. 1 Schematic diagram of engineering treatment of mature landfill leachate |
在2018年11月、2019年1月和2019年3月, 采集了3次水样, 每次采集11个水样(S0~S10), 取样点位置如图 1所示, 该工艺进水(S0)水质如表 1所示, 其sCOD和DOC浓度范围分别为2 061~3 083 mg·L-1和685~1 106 mg·L-1, 有机物含量高; B/C为0.07~0.16, 可生化性能差; 凯氮含量高(KN为1 218~1 883 mg·L-1), sCOD/DN为1.10~1.59, 与Renou等[1]归纳的长填龄渗滤液水质特征相符.样品采集后, 在室温下经过0.45 μm的聚醚砜膜过滤, 贮存于4℃冰箱中, 待进一步分析测试.
|
|
表 1 生物池进水渗滤液(S0)的水质理化特性 Table 1 Physical and chemical characteristics of landfill leachate (S0) before biological treatment |
1.2 基本理化性质分析
样品的水质分析指标包含pH、NH4+-N、KN、硝态氮(NO3--N)、溶解性氮(dissolved nitrogen, DN)、DOC、sCOD、BOD5、盐分[包括电导率(electrical conductivity, EC)、Cl-、Na+和K+][20]、重金属(As、Cr、Cd、Pb和Hg), 测试方法均参照美国水和废水标准分析方法[21].此外, 本文中提及的有机氮(organic nitrogen, ON)为KN与NH4+-N的差值.
将样品的DOC浓度(以C计)稀释至10 mg·L-1以下, 利用紫外分光光度仪(UV-1800, SHIMADZU)测定254 nm的紫外吸收光度除以对应的DOC浓度得到特定波长紫外吸收指数(special UV absorbance, SUVA254)[13].
1.3 荧光光谱分析与数据处理通过Cary Eclipse荧光分光光度仪(Varian Inc., Palo, CA, USA)扫描水样, 仪器运行操作参数设置, 参考文献[22, 23]的研究结果, 激发波长(excitation, Ex)和发射波长(emission, Em)范围分别调节至200~400 nm和280~520 nm, 扫描步长分别为10 nm和5 nm.以超纯水(Milli-Q)作为空白对照扣除, 通过除以对应样品DOC浓度对EEMs数据进行均一化[23], 利用DOMFlour toolbox[18]进行PARAFAC分析.
生物指数(biological index, BIX)是指在Ex=310 nm时, Em为380 nm和430 nm的荧光强度比值, 该指标可以反映微生物活动所形成的溶解性有机物对总溶解性有机物的贡献[24].荧光指数(fluorescence index, FI)是指当Ex=370 nm, Em为450 nm和500 nm荧光强度比值.FI指标可指示DOM与陆源、土壤源和水相生物源有机质的相似性[25].
1.4 数据处理本研究中“MBR+NF”组合工艺对长填龄渗滤液的处理效能中各单元对某污染物的去除依据遵守该单元的物料守恒原则, 去除率公式如式(1) 所示.为了体现各单元对该组合工艺处理长填龄渗滤液的贡献, 文中提及的去除贡献率如式(2).对于各单元进出水浓度变化是否显著以及两单元之间某类污染物浓度变化是否显著, 均采用T检验实现.
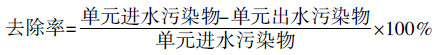
|
(1) |

|
(2) |
处理设施各单元进出水位置取样的sCOD、DOC和BOD5的测试结果见表 2, 以整个处理设施进(S0)出(S8)水为依据(见表 1), sCOD、DOC和BOD5的去除率分别为93.4%、98.7%和91.8%.因存在回流, 实际进入第一个处理单元(一级反硝化)的混合水质为S0m, 相应地上述去除率为92.4%、98.7%和69.9%.以S0m为基准, S1~S5所代表的各生物处理单元出水sCOD、DOC和BOD5没有统计意义的差异(P>0.05).可见, 处理设施的生物处理单元基本没有除碳效果, 这与长填龄渗滤液可降解有机物含量低的特性一致[2], 同时, 也说明硝酸盐氮的多点投加碳源方式中的碳源得到充分利用, 没有对除碳的宏观指标产生影响.超滤和纳滤单元对sCOD、DOC和BOD5去除率分别为69.0%、75.6%、66.7%和74.8%、94.4%、约为0, 表明MBR外置超滤单元的超滤膜在污泥反滤层协同下对DOM去除效果良好, 同时, 纳滤单元对小分子有机物处理效率高; 因少量生物易降解有机物(BOD5可测量)以更小的分子形态存在, 使纳滤单元对BOD5去除不显著.
|
|
表 2 不同处理单元sCOD、DOC和BOD5变化1)/mg·L-1 Table 2 Changes in sCOD, DOCs and BOD5 in different treatment units/mg·L-1 |
处理设施各单元进出水位置取样的不同形态氮测试结果见表 3, 以整个处理设施进(S0)出(S8)水为依据(见表 1), DN、NH4+-N、NO3--N和ON的去除率分别为98.4%、99.7%、87.4%和68.4%; 以S0m为基准则为88.9%、97.5%、43.3%和85.5%.因回流液稀释, 以S0m为基准各形态氮的去除率一般低于S0基准, 但是, 因超滤回流泥水混合物(S8)中ON浓度(105 mg·L-1)高于S0(38 mg·L-1), 使ON的去除率变化相反.除此之外, 经检测未检出NO2--N, 因生化阶段各单元进水NH4+-N最高的仅为160 mg·L-1(S0m), 硝化充分, NO2--N不易累积.
|
|
表 3 不同处理单元不同种类的氮变化1)/mg·L-1 Table 3 Changes in N of different types in different treatment units/mg·L-1 |
以S0m为基准, 生物处理各单元NH4+-N浓度单调下降, 按生物处理段浓度下降占比, 一级反硝化46.2%、一级硝化A 32.6%, 其它单元略有下降, 但没有显著性差异(P>0.20); NO3--N浓度呈波动状态, 上升最明显为一级硝化A 30.4%, 下降最明显为二级反硝化44.4%; ON浓度同样波动, 一级反硝化下降具非常显著性(P < 0.001)为36.1%.根据一级反硝化和二级反硝化的脱氮效能, 结合S1~S5各点sCOD无明显变化(P>0.972)可知, 投加的碳源已被脱氮充分利用.以S0为基准, 生物处理DN的浓度降低1 736 mg·L-1, 占处理设施浓度降低值的93.4%; 该组合工艺对DN去除贡献最大是一级反硝化(占54.6%), MBR超滤单元DN的浓度降低了51 mg·L-1, 对该工艺DN去除贡献为24.4%, 两者皆主要去除氮形态为ON和NH4+-N, 其中超滤单元可能依靠超滤膜拦截有机物和污泥反滤层吸附NH4+-N; 而纳滤单元DN浓度显著降低(P < 0.001), 去除形态以ON为主.
2.2 各单元对DOM组分处理的贡献表 4为各采样点水样SUVA254、FI和BIX的分析结果, 以整个处理设施进(S0)出(S8)水为依据, 上述三者分别提高了16.9%、19.7%和71.6%, 表明最终处理出水的DOM主要由微生物代谢活动生成, 该结果与Qiu等的描述相似[26].有研究发现与S0 SUVA254值相似的长填龄渗滤液中腐殖质类(腐殖酸和富里酸)占DOM比例约为45%~66%[12, 13], 同时, 从FI和BIX的值可知, 长填龄渗滤液中的DOM以微生物源有机物为主[9, 24], 这表明在长时间填埋过程中微生物的作用使有机物腐殖化程度增加[2, 27].
|
|
表 4 不同取样点的SUVA254、BIX和FI变化1) Table 4 Changes in SUVA254, BIX, and FI at different sampling points |
长填龄渗滤液经一级反硝化单元后, SUVA254明显下降(P < 0.05), FI和BIX无明显变化(P>0.05); 由于该单元sCOD实际去除率低(见表 2)、回流比大、污泥浓度高(约28 000 mg·L-1), 单元出水SUVA254低于各股回流液(S6和S3).这表明SUVA254下降主要受回流混合的影响, 同时, 回流污泥对出水中DOM的吸附也是改变SUVA254的因素[8]. S1~S5的各生物处理单元水样的SUVA254等3项指标没有显著变化(P>0.05), 与sCOD等宏观指标的变化浮动相似(见表 2).在超滤单元中, 与超滤回流(S6)比较, 超滤出水(S7)的SUVA254、FI和BIX都有增加, 其中SUVA254增加了1.46 L·(mg·m)-1, 表明超滤主要截留渗滤液中芳香度较低的DOM, 结合此单元sCOD和DOC浓度显著下降(P < 0.05), 推测此类DOM是长填龄渗滤液中主要的有机物类别.经过纳滤处理, 最终出水(S8)DOM的SUVA254降低了26.1%, 而FI和BIX分别增加了20.0%和93.1%, 具有微生物代谢产物的明显特征, 而芳香度低于一次浓缩液(S9)和最终浓缩液(S10)的DOM, 表明针对高芳香性的DOM, 纳滤处理更为有效[9, 28].
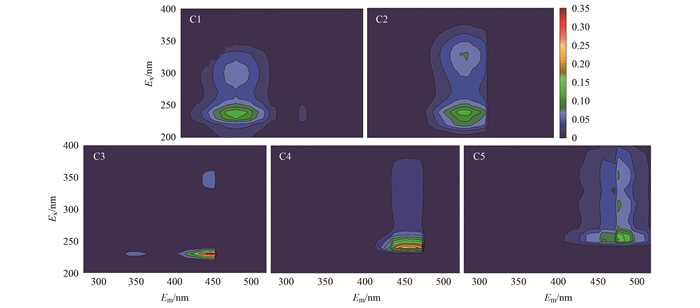
通过EEMs-PARAFAC分析得到5个荧光组分(C1~C5)如图 2所示, 其中C1为类蛋白质[29], C2为类腐殖质物质[16], C3、C4和C5为腐殖质类物质[17], 分析结果获得的组分最大荧光强度(Fmax)变化, 可判断荧光组分的去除或转化情况[15].各取样点组分Fmax相对丰度如图 3(a)所示, 在S0中C3、C4和C5三者的相对丰度和达到了67.9%, 表明长填龄渗滤液中的DOM以腐殖质类物质为主.
|
图 2 EEM-PARAFAC获得的5个组分 Fig. 2 Five components acquired by EEM-PARAFAC |
|
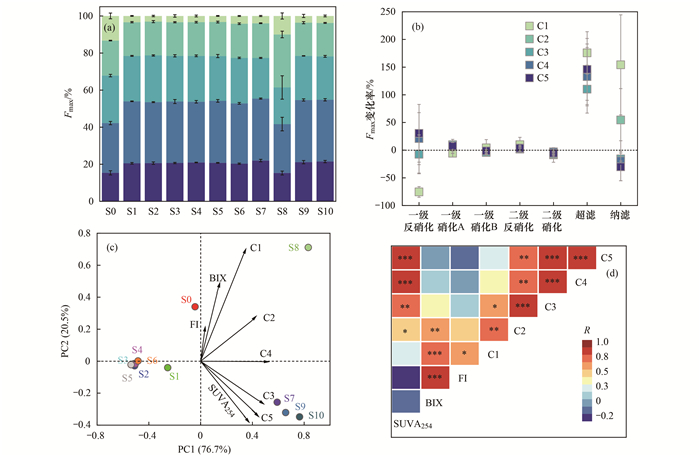
Fmax为该取样点某组分Fmax除以5个组分Fmax之和, Fmax变化率为后一处理阶段某组分Fmax减去前一阶段对应组分的Fmax之差除以前一阶段对应组分的Fmax; R为Pearson相关系数, *、**和***分别表示P < 0.05、P < 0.01和P < 0.001; (a)不同取样点荧光组分的相对丰度, (b)不同处理单元的Fmax变化率, (c)DOM特征主成分分析以及(d)DOM各类指标与DOM指标间的Pearson相关性 图 3 不同处理单元中荧光组分的特征及转化情况 Fig. 3 Characteristics and transformation of fluorescence components in different treatment units |
从图 3(b)可见, 经过一级反硝化单元后, C4和C5的荧光强度分别增加了20.8%和30.4%, 表明它们可能是由微生物代谢转化形成的新腐殖质类化合物[6], 而C1荧光强度降低了75.4%, 可见该物质可被微生物利用[29].同时, 在一级硝化A单元出水(S2)中, 腐殖化程度较高的C2~C5均增加了10%左右, 从图 3(d)可知, C2~C5与SUVA254呈正相关(R>0.95, P < 0.05), 可知通过一段缺氧和好氧处理渗滤液DOM芳香化程度加深.
超滤单元出水(S7)中C1~C5的Fmax均显著增加, 而从图 3(c)和图 3(d)可见, C1和C2与BIX呈正相关(R>0.76, P < 0.01), 同时C1还与FI呈正相关(R=0.69, P=0.02), 可见超滤单元出水中的DOM主要为微生物生长代谢产物.C3~C5的Fmax增加, 表明超滤单元难以截留高芳香类化合物.纳滤单元出水(S8)中C3、C4和C5的荧光强度分别降低了15.8%、19.1%和30.1%, 说明纳滤对腐殖化程度较强的DOM截留效果更佳.但是, 纳滤对微生物代谢衍生的类蛋白物质C1和类腐殖质C2没有截留效果[30], 最终出水DOM主要是微生物代谢产物[26].
2.3 各单元重金属及盐分变化处理设施各单元进出水位置取样的重金属测试结果见表 5, 长填龄渗滤液中重金属浓度低[1].各生物处理单元重金属浓度变化没有显著性(P>0.05).超滤单元和纳滤单元对重金属均有一定的拦截作用, 这可能是由于膜上污泥和腐殖质胶体的吸附作用[31].按测试均值计, 整个处理过程进出水的As、Cr、Hg和Pb去除率分别为66.7%、99.4%、64.5%和88.9%.
|
|
表 5 不同取样点重金属浓度变化1)/mg·L-1 Table 5 Changes in heavy metal concentrations at different sampling points units/mg·L-1 |
处理设施各单元进出水位置取样的盐分测试结果见表 6, 长填龄渗滤液具有高盐分特征EC达16.9 mS·cm-1, 该工艺对EC、Na+、K+和Cl-去除率分别49.7%、16.1%、18.0%和12.8%.盐分浓度主要在一级反硝化、超滤和纳滤环节变化.一级反硝化和超滤单元EC下降, 但Na+、K+和Cl-没有明显变化(P>0.05), 主要机制可能是pH变化沉淀和污泥反滤层吸附去除了碱土金属离子[31]; 纳滤单元EC和Na+、K+均有所降低, 但纳滤浓缩液(S10水量, 约占S7水量的4%)中Na+和K+明显富集(P < 0.001)[11].
|
|
表 6 不同取样点盐分含量变化1) Table 6 Changes in salinity concentration at different sampling points units |
2.4 各单元污染物处理效能分析
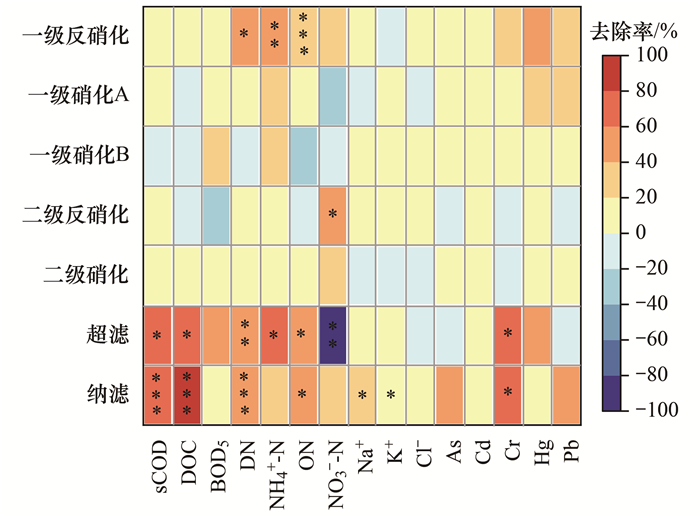
本研究中处理设施各单元污染物去除效能(以S0m为基准)如图 4所示.在脱氮除碳方面, 一级反硝化单元对长填龄渗滤液DN的去除率达到了41.7%, 具有显著的脱氮能力(P < 0.05), 去除的氮以NH4+-N和ON为主, 该单元应存在反硝化和同步硝化.依靠外加碳源, 二级反硝化单元对NO3--N去除显著(P < 0.05); 同时, 超滤和纳滤单元对DN去除均具有显著性(P < 0.01和P < 0.001), 去除率分别为41.8%和57.0%.sCOD和DOC的主要去除单元为超滤和纳滤, 它们在这两个处理单元中的去除率分别为69.7%和75.9%以及68.0%和74.7%, 但这两个单元易发生膜堵塞[1, 31].综上可知, 在工程化长填龄渗滤液处理过程中, 生物处理段的主要作用是脱氮, 主要贡献单元为反硝化, 而硝化单元作用相对不明显, 同时可能因处理流程过长, 污泥水解使ON累积而削弱脱氮作用.超滤和纳滤是主要的除碳单元, 也对DN去除的具有一定的作用, 对于长填龄渗滤液处理不可或缺; 同时, 纳滤单元还可去除重金属和盐分, 但对于重金属而言, 因原水重金属浓度较低, 对出水达标没有影响.可见, 长填龄渗滤液处理设施中生物处理段单元可简化, 建设时应设置超越管道, 根据填埋场渗滤液的阶段性特征灵活组合处理单元, 作为MBR工艺一部分的超滤单元污染物去除负荷高, 但应设置充分的防堵塞措施.
|
*、**和***分别表示P < 0.05、P < 0.01和P < 0.001 图 4 在不同处理阶段污染物的去除效率及基于T检验污染物浓度变化 Fig. 4 Removal efficiency of contaminants in different treatment units analyzed using T-test |
(1) 对sCOD、DOC和BOD5的降低率分别为93.4%、98.7%和91.8%, 其中超滤单元对sCOD和DOC的去除贡献最大分别为92.2%和93.3%, 截留的DOM以亲水性低芳香类为主; 其次是一级反硝化单元对sCOD和DOC的去除贡献为4.8%和6.0%, 去除的DOM主要为易降解物质如类蛋白物质C1; 纳滤单元对sCOD和DOC的去除贡献为2.5%和2.5%, 截留芳香化程度较高的DOM如腐殖质物质C3~C5.
(2) 该工艺对DN、NH4+-N、NO3--N和ON的去除率分别为98.4%、99.7%、87.4%和68.4%, 一级反硝化单元对DN的去除贡献最大达到了54.6%, 其次是超滤单元为24.4%, 而二级反硝化单元可显著去除NO3--N.
(3) 同时, 该工艺对重金属As、Cr、Hg和Pb去除率分别为66.7%、99.4%、64.5%和88.9%, 而对EC、Na+、K+和Cl-去除率分别为49.7%、16.1%、18.0%和12.8%, 纳滤单元为重金属和盐分去除的主要贡献者.
(4) 对于长填龄渗滤液处理而言, 反硝化是主要的脱氮单元, 对于设置多段硝化的处理设施, 可适当减小硝化单元的段数.对于除碳而言, 超滤和纳滤单元是必不可少的环节; 超滤除碳负荷最高, 但应预防堵塞.
| [1] | Renou S, Givaudan J G, Poulain S, et al. Landfill leachate treatment: review and opportunity[J]. Journal of Hazardous Materials, 2008, 150(3): 468-493. DOI:10.1016/j.jhazmat.2007.09.077 |
| [2] |
肖骁, 何小松, 席北斗, 等. 垃圾填埋水溶性有机物组成、演化及络合重金属特征[J]. 环境科学, 2017, 38(9): 3705-3712. Xiao X, He X S, Xi B D, et al. Composition, evolution, and complexation of dissolved organic matter with heavy metals in landfills[J]. Environmental Science, 2017, 38(9): 3705-3712. |
| [3] | Li H S, Zhou S Q, Sun Y B, et al. Advanced treatment of landfill leachate by a new combination process in a full-scale plant[J]. Journal of Hazardous Materials, 2009, 172(1): 408-415. DOI:10.1016/j.jhazmat.2009.07.034 |
| [4] | Bu L, Wang K, Zhao Q L, et al. Characterization of dissolved organic matter during landfill leachate treatment by sequencing batch reactor, aeration corrosive cell-Fenton, and granular activated carbon in series[J]. Journal of Hazardous Materials, 2010, 179(1-3): 1096-1105. DOI:10.1016/j.jhazmat.2010.03.118 |
| [5] | Liu Z P, Wu W H, Shi P, et al. Characterization of dissolved organic matter in landfill leachate during the combined treatment process of air stripping, Fenton, SBR and coagulation[J]. Waste Management, 2015, 41: 111-118. DOI:10.1016/j.wasman.2015.03.044 |
| [6] | Yang X F, Meng L, Meng F G. Combination of self-organizing map and parallel factor analysis to characterize the evolution of fluorescent dissolved organic matter in a full-scale landfill leachate treatment plant[J]. Science of the Total Environment, 2019, 654: 1187-1195. DOI:10.1016/j.scitotenv.2018.11.135 |
| [7] | Wang H, Cheng Z W, Sun Z Y, et al. Molecular insight into variations of dissolved organic matters in leachates along China's largest A/O-MBR-NF process to improve the removal efficiency[J]. Chemosphere, 2020, 243. DOI:10.1016/j.chemosphere.2019.125354 |
| [8] | Chen W M, Zhuo X C, He C, et al. Molecular investigation into the transformation of dissolved organic matter in mature landfill leachate during treatment in a combined membrane bioreactor-reverse osmosis process[J]. Journal of Hazardous Materials, 2020, 397. |
| [9] | Campagna M, ÇakmakcƖ M, Yaman F B, et al. Molecular weight distribution of a full-scale landfill leachate treatment by membrane bioreactor and nanofiltration membrane[J]. Waste Management, 2013, 33(4): 866-870. DOI:10.1016/j.wasman.2012.12.010 |
| [10] |
王凡, 陆明羽, 殷记强, 等. 反硝化-短程硝化-厌氧氨氧化工艺处理晚期垃圾渗滤液的脱氮除碳性能[J]. 环境科学, 2018, 39(8): 3782-3788. Wang F, Lu M Y, Yin J Q, et al. Treatment of old landfill leachate via a denitrification-partial nitritation-ANAMMOX process[J]. Environmental Science, 2018, 39(8): 3782-3788. |
| [11] | Trebouet D, Schlumpf J P, Jaouen P, et al. Stabilized landfill leachate treatment by combined physicochemical-nanofiltration processes[J]. Water Research, 2001, 35(12): 2935-2942. DOI:10.1016/S0043-1354(01)00005-7 |
| [12] | Wang H W, Wang Y N, Li X Y, et al. Removal of humic substances from reverse osmosis (RO) and nanofiltration (NF) concentrated leachate using continuously ozone generation-reaction treatment equipment[J]. Waste Management, 2016, 56: 271-279. DOI:10.1016/j.wasman.2016.07.040 |
| [13] | Zhang Q Q, Tian B H, Zhang X, et al. Investigation on characteristics of leachate and concentrated leachate in three landfill leachate treatment plants[J]. Waste Management, 2013, 33(11): 2277-2286. DOI:10.1016/j.wasman.2013.07.021 |
| [14] | Calabrò P S, Gentili E, Meoni C, et al. Effect of the recirculation of a reverse osmosis concentrate on leachate generation: a case study in an Italian landfill[J]. Waste Management, 2018, 76: 643-651. DOI:10.1016/j.wasman.2018.03.007 |
| [15] | Cheng C, Wu J, You L D, et al. Novel insights into variation of dissolved organic matter during textile wastewater treatment by fluorescence excitation emission matrix[J]. Chemical Engineering Journal, 2018, 335: 13-21. DOI:10.1016/j.cej.2017.10.059 |
| [16] | Tang G, Zheng X, Li X L, et al. Variation of effluent organic matter (EfOM) during anaerobic/anoxic/oxic (A2O) wastewater treatment processes[J]. Water Research, 2020, 178. DOI:10.1016/j.watres.2020.115830 |
| [17] | Chen W, Westerhoff P, Leenheer J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24): 5701-5710. |
| [18] | Stedmon C A, Bro R. Characterizing dissolved organic matter fluorescence with parallel factor analysis: a tutorial[J]. Limnology and Oceanography: Methods, 2008, 6(11): 572-579. DOI:10.4319/lom.2008.6.572 |
| [19] | Feng S J, Gao K W, Chen Y X, et al. Geotechnical properties of municipal solid waste at Laogang Landfill, China[J]. Waste Management, 2017, 63: 354-365. DOI:10.1016/j.wasman.2016.09.016 |
| [20] | Loncnar M, Zupančič M, Bukovec P, et al. Fate of saline ions in a planted landfill site with leachate recirculation[J]. Waste Management, 2010, 30(1): 110-118. DOI:10.1016/j.wasman.2009.09.010 |
| [21] | APHA AWWA, WPCF. Standard methods for the examination of water and wastewater[M]. Washington, DC, USA: American Public Health Association (APHA), 2005. 100-508. |
| [22] | Lu F, Chang C H, Lee D J, et al. Dissolved organic matter with multi-peak fluorophores in landfill leachate[J]. Chemosphere, 2009, 74(4): 575-582. DOI:10.1016/j.chemosphere.2008.09.060 |
| [23] | Wu J, Zhang H, He P J, et al. Insight into the heavy metal binding potential of dissolved organic matter in MSW leachate using EEM quenching combined with PARAFAC analysis[J]. Water Research, 2011, 45(4): 1711-1719. DOI:10.1016/j.watres.2010.11.022 |
| [24] | Huguet A, Vacher L, Relexans S, et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary[J]. Organic Geochemistry, 2009, 40(6): 706-719. DOI:10.1016/j.orggeochem.2009.03.002 |
| [25] | Mcknight D M, Boyer E W, Westerhoff P K, et al. Spectrofluorometric characterization of dissolved organic matter for indication of precursor organic material and aromaticity[J]. Limnol Oceanogr, 2001, 46(1): 38-48. DOI:10.4319/lo.2001.46.1.0038 |
| [26] | Qiu J J, Lü F, Zhang H, et al. Persistence of native and bio-derived molecules of dissolved organic matters during simultaneous denitrification and methanogenesis for fresh waste leachate[J]. Water Research, 2020, 175. DOI:10.1016/j.watres.2020.115705 |
| [27] | Comstock S E H, Boyer T H, Graf K C, et al. Effect of landfill characteristics on leachate organic matter properties and coagulation treatability[J]. Chemosphere, 2010, 81(7): 976-983. DOI:10.1016/j.chemosphere.2010.07.030 |
| [28] | Zhang B L, Shan C, Hao Z N, et al. Transformation of dissolved organic matter during full-scale treatment of integrated chemical wastewater: molecular composition correlated with spectral indexes and acute toxicity[J]. Water Research, 2019, 157: 472-482. DOI:10.1016/j.watres.2019.04.002 |
| [29] | Henderson R K, Baker A, Murphy K R, et al. Fluorescence as a potential monitoring tool for recycled water systems: a review[J]. Water Research, 2009, 43(4): 863-881. DOI:10.1016/j.watres.2008.11.027 |
| [30] | Francisco N C, Caixach J. Molecular characterization of dissolved organic matter through a desalination process by high resolution mass spectrometry[J]. Environmental Science & Technology, 2013, 47(17): 9619-9627. |
| [31] | Meng F G, Chae S R, Drews A, et al. Recent advances in membrane bioreactors (MBRs): membrane fouling and membrane material[J]. Water Research, 2009, 43(6): 1489-1512. DOI:10.1016/j.watres.2008.12.044 |
 2021, Vol. 42
2021, Vol. 42


