2. 重庆地质矿产研究院, 重庆 401120
2. Chongqing Institute of Geology and Mineral Resources, Chongqing 401120, China
氮是全球生态系统的重要元素, 也是许多有机、无机物的组成部分[1].磷仅次于氮, 是初级生产中第二重要的元素[2].氮和磷元素是细胞组成的必需物质, 是农作物生长必需的养分.近年来, 随着人口数量逐年增加, 全球对水稻小麦等主要粮食作物的需求量进一步扩大, 由于粮食作物产量小、质量低等情况的出现, 农业生产中施用化肥已经成为解决此类问题的重要途径, 其中氮肥与磷肥是农业生产中常用的基础肥料.但随着氮肥和磷肥施用量的增加以及人类不合理的施用方法, 不仅降低了肥料利用率, 还造成了环境破坏, 这种不对等的产投比在严重破坏自然界氮磷流动系统内部代谢与循环的同时[3], 还会导致土壤酸化[4]、水体富营养化[5~7]和产生温室气体[8]等一系列问题.因此寻找一种既具备良好的养分特性又能减轻氮磷对环境造成不良影响的物质是当前迫在眉睫要解决的问题之一.
生物质炭通常是用工农业废弃物、动植物组织等生物质在无氧或者部分缺氧及相对低温(< 700℃)的条件下裂解炭化形成的炭材料, 其表面含有丰富的含氧官能团和多孔结构[9], 可为土壤微生物的栖息和生长提高良好的环境条件[10].近些年人们发现生物炭的结构特性可通过一些物理和化学方法来进行改性[11, 12], 改性后的生物炭具有比原本生物炭更强的吸附能力[13]、更大的阳离子交换量和更高的pH[14].有研究表明, 添加小麦秸秆生物炭可改善红壤的理化性质, 在修复重金属对红壤性水稻土污染的同时可改善土壤肥力状况[15].李娇等[16]的研究发现, 与常规施肥相比, 生物炭不仅能提高作物产量和系统净初级生产力, 还能增加土壤的固碳量.
目前国内对生物炭的研究大部分集中在以农业废弃物为原材料的生物炭与化肥复合制得的生物炭基肥进行还田时对作物生长的影响, 而我国工业生产上所产生的废弃物数量也相当庞大, 对工农业废弃物制成的生物炭与化肥混合时对氨挥发和磷固定影响的研究较少.因此, 本研究利用烟沫和酒糟这两种工业废弃物以及玉米秸秆为原材料制成生物炭, 同时将烟沫生物炭进行改性处理, 来分析4种生物炭与化肥混合后在一定时间内氨挥发和磷固定的规律, 以期为工业废弃物的可持续利用和提高化肥中N、P元素的利用率提供一定的实验依据和理论指导.
1 材料与方法 1.1 供试材料以贵州省贵阳市周边的酒厂、烟厂及农场收集的酒糟、烟沫和玉米秸秆为研究对象, 对3种原料进行清理和干燥, 粉碎后放置在无氧密闭容器中, 在马弗炉内加热到450℃热解, 研磨热解产物, 用超纯水清洗若干次, 烘干, 即得到生物炭成品.酒糟、烟沫和玉米秸秆热解制成的生物炭分别记为JZ、YM和JG.取上述制备好的烟沫生物炭按4:1的比例加入硅钙镁肥(pH 8.5~10.5, SiO2 25%, CaO 40%), 放入马弗炉内混合烧制, 即得烟沫改性生物炭, 记为M-YM.供试化肥分别为尿素(含氮46.0%)、氯化钾(含钾60.0%)和磷酸二氢钾(含磷52%、含钾34%).
1.2 实验设计 1.2.1 生物炭与化肥混合后对氨的挥发实验称取过0.25 mm筛的YM、M-YM、JZ和JG这4种生物炭各15 g于500 mL广口瓶中, 分别与3种不同化肥添加水平(A1:2.25 g尿素; A2:2.25 g尿素+2.25 g氯化钾; A3:2.25 g尿素+2.25 g磷酸二氢钾)充分混匀平铺于广口瓶底部, 用喷洒的方式向混合物中加入去离子水, 保证混合物含水量为150 g·kg-1 [17], 同时设置空白对照(即不加生物炭和化肥), 所有样品在培养前均置于25℃的恒温箱中预培养一夜.次日在培养瓶内的混合物表面垫一块尼龙布, 将盛有10 mL 2%硼酸-指示剂混合液的塑料瓶放在广口瓶内作为N的吸收杯, 将培养瓶用保鲜膜封住加盖密封好并置于(28±1)℃的恒温箱中培养, 在培养的第5、10、15、20、30、45和60 d时取出吸收杯, 同时放入同样规格盛有10 mL 2%硼酸-指示剂混合液的吸收杯于培养瓶中加盖密封继续培养.将替换下来的吸收杯用标准HCl滴定, 使硼酸-指示剂混合液至淡紫色, 记录标准酸用量, 根据标准酸的用量计算混合物中N的挥发量.每个处理设置3个重复, 在整个培养期间定期采用称重法补充混合样品水分.
1.2.2 生物炭与化肥混合后对磷的固定实验称取过0.25 mm筛的YM、M-YM、JZ和JG 4种生物炭各2 g(每种生物炭需称取42份), 加入100 mL离心管中, 分别与3种不同化肥添加水平(B1:0.4 g磷酸二氢钾、B2:0.4 g磷酸二氢钾+0.3 g尿素和B3:0.4 g磷酸二氢钾+0.3 g氯化钾)充分混匀, 用喷洒的方式向混合物中加入去离子水, 保证混合物含水量为150 g·kg-1[17], 同样设置空白对照, 用保鲜膜封口置于25℃的恒温箱中培养, 在培养的第5、10、15、20、30、45和60 d时分别取出相应混合样品的离心管, 直接测定其有效磷含量.每个处理设置2个重复, 在整个培养期间定期采用称重法补充混合样品水分.
1.3 测定方法 1.3.1 生物炭性质的测定采用常规分析方法测定生物炭基本理化性质[18].其中测定pH时称取烘干过筛后的生物炭于离心管中, 按炭土比为1:20的比例加入去离子水, 置于振荡器中恒温振荡90 min, 再用离心管离心5 min, 用pH计测定上清液的pH, 重复3次; 含水量采用烘干法; 全氮采用H2SO4-H2O2消煮、靛酚蓝比色法; 全磷采用H2SO4-H2O2消煮、钒钼黄比色法; 颗粒粒径采用筛分法; 灰分含量测定时将生物炭放在马弗炉中, 调节温度为760℃, 保持6 h, 对剩余物质进行称量, 其质量即为生物炭的灰分含量.
1.3.2 混合样品的测定氨的挥发量采用2%硼酸-指示剂混合液的吸收、标准盐酸滴定法; 有效磷采用碳酸氢钠浸提-钼锑抗比色法测定.
1.4 数据处理① 氨挥发累积排放量为每次测得的氨挥发量之和; ②氨的挥发速率[mg·(kg·d)-1]=氨挥发量/培养时间; ③氨的挥发率=挥发的氨量/样品中加入的氮量×100%; ④磷的固定量=样品加入磷量-测定有效磷量; ⑤磷的固定率=(样品加入磷量-测定有效磷量)/样品加入磷×100%.
采用Excel 2010和IBM SPSS 21.0软件对数据进行处理, 不同处理之间的多重比较采用LSD最小显著差数法(P < 0.05), 所有图表采用Excel 2010及Origin 8.5绘制.
2 结果与分析 2.1 生物炭的基本性质与粒径分布 2.1.1 生物炭的基本性质4种生物炭的基本性质如表 1, 4种生物炭均呈碱性, 烟沫改性后提高了生物炭的pH值, 4种生物炭pH大小顺序为:JZ>M-YM>YM>JG. 4种生物炭中全氮及全磷的含量最高的均为JZ, 比最低的JG分别高了24.66g·kg-1和15.33g·kg-1.烟沫改性后降低了生物炭的全氮含量、提高了全磷含量.灰分是衡量生物炭中矿物质的一个重要指标, 4种生物炭灰分含量(质量分数)在25.44%~37.91%之间, 灰分含量大小顺序为:M-YM>YM>JZ>JG.另外, 烟沫改性后提高了生物炭的含水量, 在自然条件下, YM与M-YM含水量均高于JZ与JG.
|
|
表 1 4种生物炭的基本性质 Table 1 Basic physical and chemical properties of four types of biochar |
2.1.2 不同生物炭粒径分布特征
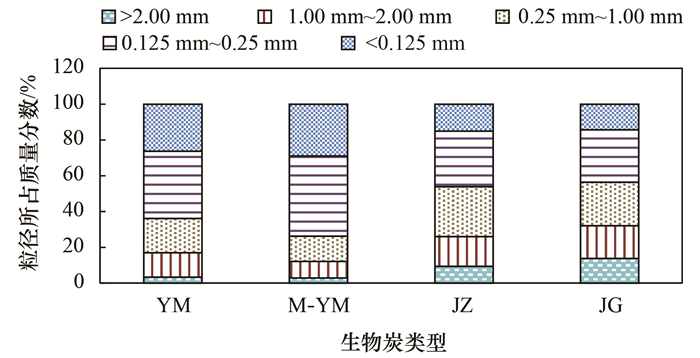
图 1表示4种生物炭在5种不同粒径范围下的分布情况.从中可知, 4种生物炭所占质量分数最多的粒径均集中在0.125~0.25 mm范围内, 其中大于2 mm的粒径在所有粒径中所占质量分数最小, YM、M-YM和JZ的粒径所占质量分数均在10%以内, 而JG较多, 所占质量分数为13.75%; 4种生物炭在>2 mm和1~2 mm粒径范围内所占质量分数的大小顺序均为:JG>JZ>YM>M-YM, 在0.25~1 mm粒径范围内时表现为JZ>JG>YM>M-YM, 而从0.125~0.25 mm和 < 0.125 mm开始, YM与M-YM的粒径所占质量分数显著增加, 此时大小顺序为:M-YM>YM>JZ>JG, 说明4种生物炭中YM与M-YM的总体粒径更小, 即YM和M-YM的比表面比JZ和JG大.
|
图 1 不同生物炭颗粒粒径分布特征 Fig. 1 Distribution characteristics of the particle size of different biochar particles |
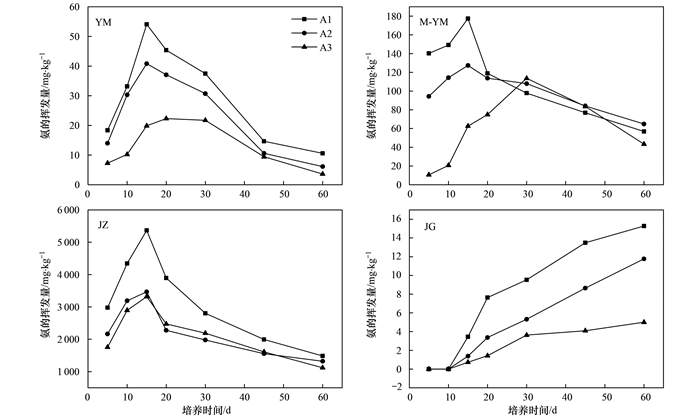
4种生物炭在不同化肥配比下各培养时间段内氨的挥发量如图 2所示, 从中可以看出:YM、M-YM和JZ在A1、A2和A3处理下, 整个培养时间内氨的挥发量均呈现先增大后减小的趋势, 而JG的3个处理下则呈缓慢上升的趋势.在培养15~30 d时间范围内, YM、M-YM、JZ这3种生物炭在3种水平下氨的挥发量达到最大值, 这是因为在该时间段内尿素不断被水解为NH4+, 而随着NH4+浓度的增加, 促进了NH4+向NH3的转化, 从而导致该时间段内氨的挥发量急剧增加, 且JZ在A1处理下, 在培养的第15 d时氨的挥发量最大, 达5366.72 mg·kg-1. JG生物炭在前10 d均未出现氨的挥发, 从第10 d开始各处理均出现少量的氨挥发, 但远远低于其余3种生物炭处理.在整个培养时间内, JG氨挥发量随着培养时间的增加而增加, 且在第60 d时出现最大值.在整个培养时间内, 4种生物炭在不同化肥配比下的氨挥发量大小均为:JZ>M-YM>YM>JG, 这与生物炭pH大小关系一致, 可见pH在生物炭对氨挥发方面的影响之大.另外, YM和JG在各培养阶段内3种化肥配比下氨挥发量的总体规律为A1>A2>A3, 说明在YM和JG混合物中添加磷酸二氢钾对氨的挥发抑制作用在整个培养过程中都比氯化钾强; 在JZ混合物中添加磷酸二氢钾和氯化钾对氨的挥发抑制作用差异不大; M-YM混合物中则在培养前30 d内, 添加磷酸二氢钾对氨的挥发抑制作用强于氯化钾, 而在培养的后30 d内, 在尿素中添加这两种肥料对氨挥发的抑制作用差异不大.
|
图 2 不同化肥配比下生物炭对氨的挥发量的影响 Fig. 2 Effect of biochar on ammonia volatilization with different fertilizer addition ratios |
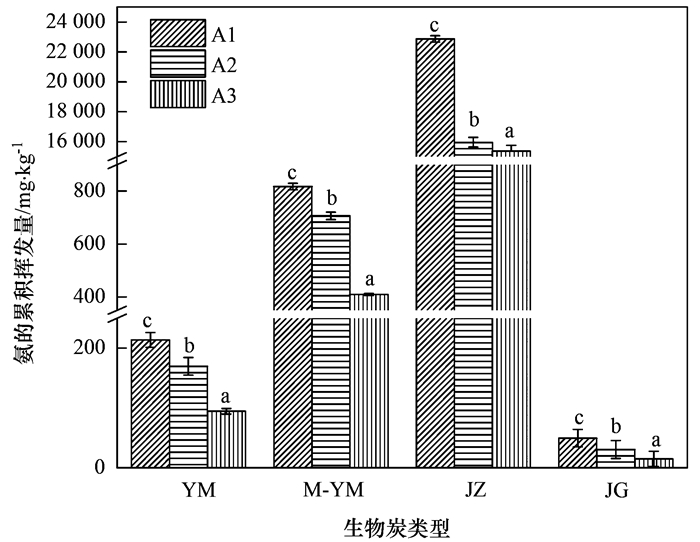
培养结束时4种生物炭在A1、A2和A3处理下氨的累积挥发量如图 3所示.YM、M-YM、JZ和JG在不同化肥配比下氨的累积挥发量差异显著(P < 0.05), 且均表现为:A1>A2>A3, 说明添加氯化钾与磷酸二氢钾降低了尿素中氨的挥发, 且添加磷酸二氢钾的抑制作用更强, 这是因为磷酸二氢钾在该过程中被水解, 水解使得其产生H+, 从而使得环境的pH降低, 进而抑制尿素水解产生的铵盐向氨气转化; 但氯化钾并不能改变环境的pH, 因此也不能很好地抑制NH4+向NH3的转化, 即会有较高的氨挥发量. 4种生物炭在所有A1、A2和A3处理下氨的累积挥发量均表现为:JZ>M-YM>YM>JG, 其中JZ在A3水平下氨的累积量分别是YM、M-YM和JG处理的162.6、37.5和1031.3倍, 这是因为JZ的pH高于其他3种生物炭, 而pH又是决定氨挥发的主要因素之一, 随着pH的增加, 环境中铵态氮的比例升高, 使得氨挥发的潜力增大[19].
|
不同小写字母表示不同化肥配比差异显著(P < 0.05) 图 3 不同化肥配比下生物炭对氨的累积挥发量的影响 Fig. 3 Effect of biochar on cumulative ammonia volatilization with different fertilizer addition ratios |
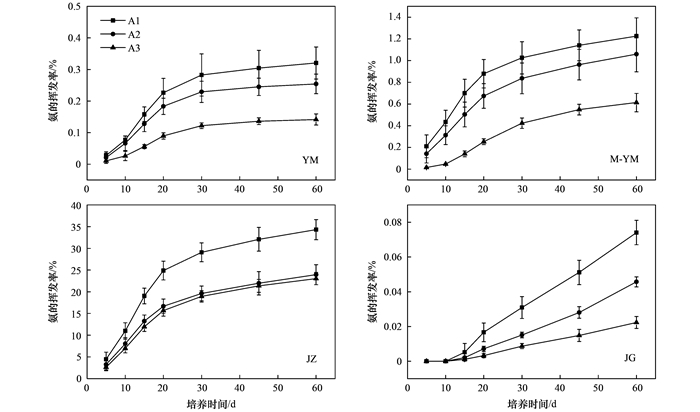
4种生物炭处理在A1、A2和A3处理下对氨的挥发率的影响如图 4所示. 4种生物炭在3种化肥配比下每个对应的培养阶段内, 不同生物炭处理氨的挥发率大小顺序均为:JZ>M-YM>YM>JG.当培养第60 d时, 氨的挥发率最大和最小分别是JZ、JG处理.从各生物炭氨的挥发率的最大值也可以得出, 在A1、A2和A3处理下, 4种生物炭处理氨的挥发率的大小均表现为:A1>A2>A3, YM、M-YM、JZ和JG的A3处理氨的挥发率分别比A1处理氨的挥发率减少了0.179%、0.612%、11.261%和0.052%, 说明磷酸二氢钾能减少生物炭与尿素混合物中的氨的挥发率, 这是因为磷酸二氢钾水解使得环境变为酸性, 而酸性条件有利于NH4+-N的固定, 减少NH3的挥发[20].在YM、M-YM和JZ处理中, 3种化肥水平下氨的挥发率均先快速增大后缓慢增大; JG处理从培养第10 d开始到培养结束氨的挥发率随时间呈线性增加的趋势.
|
图 4 不同化肥配比下生物炭对氨挥发率的影响 Fig. 4 Effect of biochar on ammonia volatilization ratio with different fertilizer addition ratios |
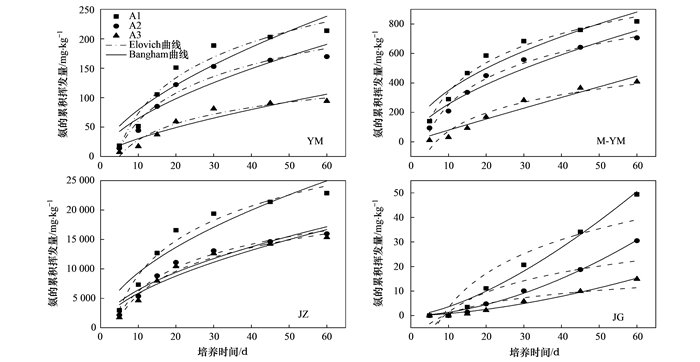
在相同培养温度下, 除JG外, YM、M-YM和JZ在不同化肥配比下氨的挥发累积量的趋势基本一致, 说明不同生物炭对氨的累积挥发量有影响, 将所有处理中氨的累积挥发量与培养时间用Elovich(y=a+blnt)与Bangham(y=At1/B)动力学方程进行拟合, 拟合结果如图 5和表 2所示.方程中, y表示氨的累积挥发量, t表示培养时间; 其中在Elovich方程中, 参数a表示第1 d氨的挥发量, 参数b为斜率, 可用来表征不同处理的NH3挥发速率; 在该方程中, 4种生物炭在不同处理间均表现出差异性, 且a和b两个参数的大小与累积氨挥发量的变化趋势一致, 除JZ外, 其余3种生物炭在A3水平下a的绝对值和b值均远低于A1和A2水平, 可见这3种生物炭在A3水平下氨挥发容量和强度均小于A1和A2水平, 说明在YM、M-YM和JG中添加磷酸二氢钾更有效抑制了氮的损失.同时根据拟合参数可知, YM、M-YM和JZ的Elovich方程相关系数(R2)在0.932~0.986之间, 均达到了极显著水平, 而Bangham方程相关系数(R2)在0.839~0.932之间, 远低于Elovich方程, 说明Elovich方程能更好地拟合YM、M-YM和JZ中氨累积挥发量的规律.JG的Bangham方程相关系数(R2)分别为0.981、0.993和0.984, 高于Elovich方程相关系数(0.805、0.734和0.761), 说明JG用Bangham方程拟合程度更好.
|
图 5 氨的累积挥发量与时间的拟合曲线 Fig. 5 Fitting curve of cumulative ammonia volatilization and ammonia volatilization time |
|
|
表 2 氨的累积挥发量与时间的拟合曲线参数 Table 2 Fitting curve parameters of cumulative ammonia volatilization and ammonia volatilization time |
2.3 不同生物炭与化肥混合对磷固定的影响 2.3.1 不同生物炭与化肥混合对磷的固定量的动态变化
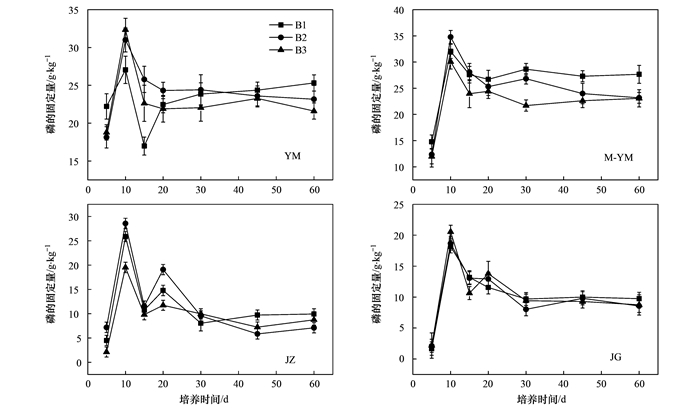
4种生物炭在B1、B2和B3处理下各培养时间段内磷的固定量的动态变化如图 6所示, 从中可以看出, 4种生物炭在不同的化肥配比下, 磷的固定量均在第10 d时达到最大值, 随后随培养时间的增加磷的固定量急剧减小, 除YM的B1处理外, 其余处理均在第15 d时出现最低值, 当培养时间从第15~20 d时, 磷的固定量急剧上升, 随后逐渐趋于平缓. 4种生物炭中, M-YM对磷的固定量最大, JG最小, 且在整个培养时间内, M-YM在B1、B2和B3处理下磷固定量最大值分别是最小值的2.17、2.82和2.51倍, JG在B1、B2和B3处理下磷固定量最大值分别是最小值的10.84、8.79和9.42倍.
|
图 6 不同化肥配比下生物炭对磷的固定量的影响 Fig. 6 Effect of biochar on phosphorus fixation with different fertilizer addition ratios |
不同生物炭与化肥混合对磷的固定率的影响如表 3所示.在所有生物炭中, 磷的固定率在16.48%~61.22%之间.YM和M-YM在B1、B2和B3处理下磷的固定率大小顺序均为:B1>B2>B3, JZ和JG在B1、B2和B3处理下磷的固定率大小顺序则均为:B1>B3>B2;通过显著性分析可知, YM中B1处理与B3处理差异显著(P < 0.05), 而B2处理与两者之间差异均不显著(P < 0.05), M-YM处理B1处理与其余两种处理间差异显著(P < 0.05), 但B2与B3两种处理间无显著差异, JZ与JG的所有处理间差异均不显著(P < 0.05).这表明氯化钾的添加会降低磷肥与YM的混合物中磷的固定率, 而尿素对混合物无影响; 氯化钾与尿素的加入均会降低磷肥与M-YM混合物中磷的固定率, 但两者之间的效果无显著差异; 而氯化钾与尿素的添加对JZ和JG两种生物炭与磷肥的混合物在磷固定中无较大影响.在B1、B2和B3处理下, 4种生物炭对磷的固定率大小顺序均为:M-YM>YM>JG>JZ, 且3种化肥配比下M-YM比JZ固定率分别高出40.91%、37.70%和30.33%.
|
|
表 3 不同化肥配比下生物炭对磷的固定率的影响1)/% Table 3 Effect of biochar on the fixed ratio of phosphorus with different fertilizer addition ratios/% |
3 讨论 3.1 不同生物炭与化肥混合对氨的挥发量与累积挥发量的影响
尿素分解受外界水分、pH以及微生物的影响较大[21], 在本研究中, YM、M-YM和JZ在不同化肥配比下, 在培养前期氨的挥发量剧增, 这主要是由于此阶段尿素与混合物中的水分接触, 促使尿素发生水解反应, 产生氨气, 同时有一部分原因是由于生物炭呈碱性, 而碱性环境会使尿素中的氮向氨气转化, 对氨的挥发有促进作用, 这也与Schomberg等[22]的研究结果类似.在此3种生物炭的培养后期, 氨的挥发率逐渐减小, 出现这种现象的原因可能是由于在前期尿素水解过程中会生成一些酸性物质(如氨基甲酸铵), 使培养环境的pH减小, 同时由于此时培养环境趋于稳定, 生物炭内的官能团逐渐活跃, 对尿素中氮的吸收固持量增加, 减少了氨的挥发.成功等人[23]利用静态暗箱-气相色谱原位研究小麦-玉米轮作系统条件下添加不同量生物炭对土壤碳氮排放、作物产量的影响, 发现添加生物炭的处理使得整个小麦-玉米轮作农田土壤系统中氮素的吸附显著增加了27.6%~38.7%, 这也与本研究的结果类似.
JG与其余3种生物炭结果不同, 在前10 d内均无法测出氨的挥发, 且培养后期氨的挥发量也远远低于其余3种生物炭, 这与以往理论研究有较大的差别, 笔者推测可能是由于JG中大颗粒粒径较多, 自身的浸润性较强, 而较强的浸润性会紧紧包裹住外界添加的水分, 使水分无法与尿素等肥料接触, 导致无氨气的挥发, 且由于添加水量不多, 与水分结合的生物炭只有少数, 所以虽然生物炭呈碱性, 但无液体作为其中介质, pH对尿素的作用缓慢, 这也是后期JG中氨挥发量低的主要原因.
本研究结果显示, 4种生物炭在不同化肥配比下氨的累积挥发量差异显著(P < 0.05)且均表现为:A1>A2>A3, 这表示尿素中添加氯化钾与磷酸二氢钾均降低氨的累积挥发量, 且在YM、M-YM和JG中添加磷酸二氢钾对氨挥发的抑制作用强于氯化钾, 而在JZ混合物中添加这两者对氨挥发的抑制作用差异不大.有研究认为, 钾离子与氯离子能与尿素分子通过相互作用形成离子-分子缔合物, 这也是导致混合物中氨的挥发量减少的原因之一[24].尿素处理土壤且加入磷酸二氢钾后氨的挥发量最低, 这很有可能是由于磷酸二氢钾水解呈酸性, 酸性环境会使铵根离子持留在样品中, 氨气的挥发减少.在本研究中将4种生物炭氨的累积挥发量进行对比, 发现在所有化肥配比水平上生物炭的大小顺序均为:JZ>M-YM>YM>JG, 这与4种生物炭的pH大小关系一致, 其中JZ在A1水平下氨的挥发比同期其他3种生物炭A1水平下都强, 这是因为JZ的pH(10.86)高于其他3种生物炭, 在相同NH4+-N水平下, pH每升高一个单位, 氨挥发量增加10倍[25].同时, 由于改性后的生物炭具有比原本生物炭更大的阳离子交换量和更高的pH[14], 使得M-YM具有比YM更高的pH, 导致当生物炭与化肥混合后, M-YM与化肥混合后的氨挥发量、累积挥发量和挥发率均高于YM.因此在实际应用中, 当与化肥混合时, 应尽量选取未改性生物炭, 这样可降低氨的挥发率, 进而增大肥料利用率.
另外还与生物炭的自身官能团、孔隙结构等有极大的关系.易从圣等[26]的研究认为, 不同原材料对生物炭与化肥混合后对氮的缓释性能影响较大, 在稻壳炭、油茶壳炭制成的两种生物炭中, 稻壳炭的效果更好, 这可能是因为稻壳炭比油茶壳炭孔隙结构更发达, 表面积更大, 对尿素的吸附和负载能力更强.因此为减少氮肥中氨的挥发, 在生物炭与氮肥混合时, 应尽量选择JG和YM, 因为这两种生物炭在提高工农业废弃物利用率的同时又可明显降低氨的挥发, 且在这两种混合物中添加磷酸二氢钾对氨挥发具有更强的抑制作用, 从而大大减少氮的损失, 提高氮利用率; 而JZ由于与氮肥混合后具有较大的氨挥发量, 因此在实际应用中不宜在氮肥中添加.
3.2 不同生物炭与化肥混合对磷固定量的动态变化及磷固定率的影响由于磷肥的快速性, 将生物炭与磷肥混合后施入土壤, 利用生物炭对养分的固持作用使磷素缓慢释放到环境中, 延长磷肥的有效性.在本研究中, 4种生物炭在整个培养时间内均对磷有一定的固定作用, 但每个阶段内的固定量有所差别.在前5 d内, 磷的固定量极低, 而在培养第10 d时, 磷的固定量最大, 这可能是在前期时混合物中的磷素主要以游离态存在, 混合物中的生物炭及水分无较大的作用.在5~10 d期间, 磷的固定量急剧上升, 此时混合物中的水分在蒸气压的推动下与磷酸二氢钾混合, 形成饱和溶液[27], 由于生物炭的原因混合物环境呈碱性, 而从前人研究成果可知生物炭在pH为9左右时对磷的吸附最好[28], 所以在此阶段生物炭将饱和溶液中的磷快速固定.在10~15 d期间, 磷的固定量逐渐下降, 这可能是由于磷溶解的原因, 有研究认为磷的固定机制是不断溶解-沉淀的结果[29].在第30~60d时, 磷的固定量差别不大, 此时生物炭由于自身的吸持特性及混合物中的环境已达到一个相对稳定的系统, 磷的固定量在一个较小的范围内波动, 此阶段下也可以推断生物炭在实际应用中的最大固定量.
M-YM生物炭对磷的固定率最高, 且4种生物炭对磷固定量的大小顺序与生物炭粒径 < 0.125 mm所占质量分数的大小顺序一致, 即M-YM>YM>JZ>JG, 其中在M-YM混合物中添加尿素和氯化钾均会降低对磷的固定, 但二者之间降低效果无显著差异; YM混合物中添加氯化钾会降低对磷的固定, 但尿素对其无影响; 而在JZ和JG混合物中添加氯化钾和尿素对磷的固定均无较大影响.另外, 可以推断出生物炭对磷的固定率可能与生物炭自身的粒径大小有关.孟庆瑞等[30]的研究表明生物炭巨大的比表面积和多孔结构, 以及丰富的官能团为其吸附磷提供了载体结构基础.宋小宝等[31]通过一步共沉淀法制备的2-La-MHTC具有更大的比表面, 同时其对磷的固定作用更强, 具有高效的除磷能力, 最大吸附量可达100.25 mg·g-1.这些与本研究结果类似, 当生物炭中粒径较小时, 生物炭与化肥的接触比表面积更大, 作用点位更多, 而磷固定过程的实质是与生物炭发生物理或化学反应的过程, 接触面积越大, 反应越充分, 因此小粒径的生物炭相较于大粒径的生物炭对磷的固定作用更强.同时, 生物炭改性提高了生物炭本身的比表面积, 使得其与化肥的接触面积更大, 化肥中的磷酸根更易被改性生物炭吸附, 从而导致改性生物炭在一定程度上降低了磷的生物有效性.因此当生物炭与磷肥混合时, 为降低生物炭对磷的固定, 宜选择JG和JZ, 且在这两种生物炭与磷肥混合物中无需添加氯化钾或尿素, 以免造成化肥资源的浪费; 另外, 若可供添加的生物炭中只有M-YM可选择, 为了减少其对磷的固定, 可在M-YM与磷肥的混合物中添加尿素或氯化钾, 也可通过增大M-YM的粒径来提高磷的生物有效性.
4 结论(1) 4种生物炭在A1、A2和A3处理下氨的挥发量、累积挥发量和挥发率均表现为:JZ>M-YM>YM>JG; 尿素中添加氯化钾与磷酸二氢钾可在一定程度上抑制氨挥发; Elovich方程能更好地拟合YM、M-YM和JZ的所有处理中氨的累积挥发量与培养时间的变化趋势, 而JG用Bangham方程拟合程度更好.
(2) 在B1、B2和B3化肥配比下, 4种生物炭对磷的固定率的大小顺序均为:M-YM>YM>JG>JZ; 所有处理下磷的固定量均先增加后减小, 随后逐渐稳定, 且在培养的第10 d达到最大值.
(3) 当生物炭与氮磷肥混合时, 考虑到生物炭会同时导致氨挥发和磷固定而使得氮磷元素的生物有效性降低, 在实际应用中, 若在氮磷肥中添加M-YM, 则不需添加氯化钾、添加JG时与M-YM一样但需适当多施磷肥、添加YM时则需加入适量氯化钾以及适当增加磷肥用量, 这样可在减少氨挥发和磷固定的同时又最大限度地减少化肥的投入, 但因JZ不能同时提高氮磷的利用率而使得其不可与氮磷肥混合施用.
| [1] | Sabovljević M, Vukojević V, Sabovljević A, et al. Determination of heavy metal deposition in the county of Obrenovac (Serbia) using mosses as bioindicators. Ⅲ. Copper (Cu), Iron (Fe) and Mercury (Hg)[J]. Archives of Biological Sciences, 2007, 59(4): 351-361. |
| [2] |
孙宏洋.贡嘎山垂直梯度带土壤微生物特征及其与磷的关系[D].北京: 中国科学院大学, 2014. Sun H Y. Soil microbial communities and its relationship with phosphorus along altitudinal gradient of Gongga mountain[D]. Beijing: University of Chinese Academy of Sciences, 2014. |
| [3] |
刘毅, 陈吉宁. 滇池流域磷循环系统的物质流分析[J]. 环境科学, 2006, 27(8): 1549-1553. Liu Y, Chen J N. Substance flow analysis on phosphorus cycle in Dianchi Basin, China[J]. Environmental Science, 2006, 27(8): 1549-1553. |
| [4] | Bolan N S, Hedley M J, White R E. Processes of soil acidification during nitrogen cycling with emphasis on legume based pastures[J]. Plant and Soil, 1991, 134(1): 53-63. |
| [5] | Gupta S, Gupta R, Sharma S. Impact of pesticides on plant growth promotion of Vigna radiata and non-target microbes:comparison between chemical-and bio-pesticides[J]. Ecotoxicology, 2014, 23(6): 1015-1021. |
| [6] | Riah W, Laval K, Laroche-Ajzenberg E, et al. Effects of pesticides on soil enzymes:a review[J]. Environmental Chemistry Letters, 2014, 12(2): 257-273. |
| [7] | Yu C Q, Huang X, Chen H, et al. Managing nitrogen to restore water quality in China[J]. Nature, 2019, 567(7749): 516-520. |
| [8] | van Kessel C, Venterea R, Six J, et al. Climate, duration, and N placement determine N2O emissions in reduced tillage systems:a meta-analysis[J]. Global Change Biology, 2013, 19(1): 33-44. |
| [9] |
杨彩迪, 宗玉统, 卢升高. 不同生物炭对酸性农田土壤性质和作物产量的动态影响[J]. 环境科学, 2020, 41(4): 1914-1920. Yang C D, Zong Y T, Lu S G. Dynamic effects of different biochars on soil properties and crop yield of acid farmland[J]. Environmental Science, 2020, 41(4): 1914-1920. |
| [10] |
刘杰云, 邱虎森, 王聪, 等. 生物质炭对双季稻田土壤反硝化功能微生物的影响[J]. 环境科学, 2019, 40(5): 2394-2403. Liu J Y, Qiu H S, Wang C, et al. Influence of biochar amendment on soil denitrifying microorganisms in double rice cropping system[J]. Environmental Science, 2019, 40(5): 2394-2403. |
| [11] | Guo Y P, Rockstraw D A. Activated carbons prepared from rice hull by one-step phosphoric acid activation[J]. Microporous and Mesoporous Materials, 2007, 100(1-3): 12-19. |
| [12] | Genuino D A D, de Luna M D G, Capareda S C. Improving the surface properties of municipal solid waste-derived pyrolysis biochar by chemical and thermal activation:Optimization of process parameters and environmental application[J]. Waste Management, 2018, 72: 255-264. |
| [13] | Qian K Z, Kumar A, Zhang H L, et al. Recent advances in utilization of biochar[J]. Renewable and Sustainable Energy Reviews, 2015, 42: 1055-1064. |
| [14] | Inyang M, Gao B, Pullammanappallil P, et al. Biochar from anaerobically digested sugarcane bagasse[J]. Bioresource Technology, 2010, 101(22): 8868-8872. |
| [15] |
郭碧林, 陈效民, 景峰, 等. 施用生物炭对红壤性水稻土重金属钝化与土壤肥力的影响[J]. 水土保持学报, 2019, 33(3): 298-304. Guo B L, Chen X M, Jing F, et al. Effects of biochar application on heavy metal passivation and soil fertility in the red paddy soil[J]. Journal of Soil and Water Conservation, 2019, 33(3): 298-304. |
| [16] |
李娇, 田冬, 黄容, 等. 秸秆及生物炭还田对油菜/玉米轮作系统碳平衡和生态效益的影响[J]. 环境科学, 2018, 39(9): 4338-4347. Li J, Tian D, Huang R, et al. Effects of straw and biochar addition on soil carbon balance and ecological benefits in a rape-maize rotation planting system[J]. Environmental Science, 2018, 39(9): 4338-4347. |
| [17] |
郑杰炳, 王子芳, 高明, 等. 含硅熔渣对磷的吸附与解吸特征研究[J]. 植物营养与肥料学报, 2007, 13(3): 504-511. Zheng J B, Wang Z F, Gao M, et al. Study on the characteristics of phosphorus adsorption and desorption in slag containing silicon[J]. Plant Nutrition and Fertilizer Science, 2007, 13(3): 504-511. |
| [18] | 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. |
| [19] |
靳红梅, 常志州, 郭德杰, 等. 追施猪粪沼液对菜地氨挥发的影响[J]. 土壤学报, 2012, 49(1): 86-95. Jin H M, Chang Z Z, Guo D J, et al. Effect of topdressing with digested pig slurry on ammonia volatilization in vegetable fields[J]. Acta Pedologica Sinica, 2012, 49(1): 86-95. |
| [20] | Ndegwa P M, Hristov A N, Arogo J, et al. A review of ammonia emission mitigation techniques for concentrated animal feeding operations[J]. Biosystems Engineering, 2008, 100(4): 453-469. |
| [21] |
刘遵奇, 孟军, 陈温福. 玉米秸秆生物炭对尿素分解的影响[J]. 农业环境科学学报, 2015, 34(6): 1142-1148. Liu Z Q, Meng J, Chen W F. Effect of corn stalk biochar on urea hydrolysis[J]. Journal of Agro-Environment Science, 2015, 34(6): 1142-1148. |
| [22] | Schomberg H H, Gaskin J W, Harris K, et al. Influence of biochar on nitrogen fractions in a coastal plain soil[J]. Journal of Environmental Quality, 2012, 41(4): 1087-1095. |
| [23] |
成功, 陈静, 刘晶晶, 等. 秸秆/生物炭施用对关中地区小麦-玉米轮作系统净增温潜势影响的对比分析[J]. 环境科学, 2017, 38(2): 792-801. Cheng G, Chen J, Liu J J, et al. Comparative analysis on effect of wheat straw and its biochar amendment on net global warming potential under wheat-maize rotation ecosystem in the Guanzhong plain[J]. Environmental Science, 2017, 38(2): 792-801. |
| [24] | Hong J, Capp M W, Anderson C F, et al. Preferential interactions in aqueous solutions of urea and KCl[J]. Biophysical Chemistry, 2003, 105(2-3): 517-532. |
| [25] | Martines A M, Nogueira M A, Santos C A, et al. Ammonia volatilization in soil treated with tannery sludge[J]. Bioresource Technology, 2010, 101(12): 4690-4696. |
| [26] |
易从圣, 宗同强, 杜衍红, 等. 生物炭基复混肥缓释特性研究[J]. 广州化学, 2018, 43(3): 60-64. Yi C S, Zong T Q, Du Y H, et al. Study of sustained-release property of compound fertilizers based on biochar[J]. Guangzhou Chemistry, 2018, 43(3): 60-64. |
| [27] | Shaviv A, Raban S, Zaidel L. Modeling controlled nutrient release from polymer coated fertilizers:Diffusion release from single granules[J]. Environmental Science & Technology, 2003, 37(10): 2251-2256. |
| [28] |
许润, 石程好, 唐倩, 等. 氢氧化镧改性介孔稻壳生物炭除磷性能[J]. 环境科学, 2019, 40(4): 1834-1841. Xu R, Shi C H, Tang Q, et al. Phosphate removal using rice husk biochars modified with lanthanum hydroxide[J]. Environmental Science, 2019, 40(4): 1834-1841. |
| [29] |
廖艳妮.生物质灰渣的农业化学行为研究[D].重庆: 西南大学, 2013. Liao Y N. Study on agrochemistry behavior of biomass ash[D]. Chongqing: Southwest University, 2013. |
| [30] |
孟庆瑞, 崔心红, 朱义, 等. 载氧化镁水生植物生物炭的特性表征及对水中磷的吸附[J]. 环境科学学报, 2017, 37(8): 2960-2967. Meng Q R, Cui X H, Zhu Y, et al. Characterization of MgO-loaded aquatic plants biochar and its adsorption capacity of phosphorus in aqueous solution[J]. Acta Scientiae Circumstantiae, 2017, 37(8): 2960-2967. |
| [31] |
宋小宝, 何世颖, 冯彦房, 等. 载镧磁性水热生物炭的制备及其除磷性能[J]. 环境科学, 2020, 41(2): 773-783. Song X B, He S Y, Feng Y F, et al. Fabrication of La-MHTC composites for phosphate removal:adsorption behavior and mechanism[J]. Environmental Science, 2020, 41(2): 773-783. |
 2021, Vol. 42
2021, Vol. 42


