2. 中国环境科学研究院水环境治理研究室, 北京 100012
2. Department of Water Environment Treatment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China
湖泊作为重要的地表水资源, 与人类生产生活密切相关[1].然而, 随着湖泊资源的开发和利用, 以及外源营养盐大量输入, 湖泊富营养化及其带来的生态环境问题日益严重, 甚至已成为全球湖泊面临的主要问题之一, 是当前国际水资源和水生态领域的研究热点[2].近年来, 随着外源营养盐输入得到有效控制, 长期输入累积的内源营养物质的释放已经成为一些湖泊富营养化及蓝藻水华暴发营养盐重要来源之一.例如滇池、巢湖和太湖等湖泊, 由于历史上大量的外源输入, 导致沉积物中营养物大量富集, 累积在沉积物中的营养物质会释放至上覆水体, 沉积物中营养盐由“汇”转换成“源”, 形成内源污染, 由此通过湖泊沉积物中营养盐分析可以间接反映出湖泊水体污染情况[3].沉积物中营养盐的控制削减对降低湖泊水体富营养化和维持水生态系统健康十分重要.因此, 研究湖泊沉积物中氮、磷和有机质的含量及其形态分布特征, 评价湖泊污染状况, 对控制湖泊水体富营养化和建立健康水生态系统具有重要意义.
国内外现已开展很多关于湖泊沉积物中的营养盐分布特征及污染评价的相关研究, 并取得了一些研究成果[3~10].衡水湖作为华北平原上第一个国家级湿地自然保护区, 加强衡水湖湿地的建设和保护对维护华北平原内陆淡水湿地生态系统、调节周边乃至京津地区气候环境具有重要作用[11, 12].近年来, 国家和地方各级政府针对衡水湖的生态环境保护开展了大量的工作, 衡水湖水生态环境质量得到较好的改善, 但衡水湖历史上曾有过一段污染较重的时期, 对整个衡水湖生态环境的不利影响至今仍然存在, 尤其是沉积物中富集的营养盐可通过内源释放进入上覆水体, 形成内源污染.近年来, 衡水湖水体中氮磷超标现象时有发生, 湖泊富营养化趋势明显, 而沉积物形成的内源污染更是加剧了水体富营养化状态.目前关于衡水湖营养盐方面的研究较少且年代久远, 相关研究鲜见报道, 针对衡水湖沉积物中营养盐分布特征及污染评价研究更是极为缺乏, 为更有效地保护衡水湖生态环境, 提高衡水湖生态治理与环境保护工作的针对性, 本研究对衡水湖表层沉积物中营养盐形态分布特征进行解析并对其污染程度进行评价, 以期为衡水湖水生态环境保护和富营养化控制提供理论支撑.
1 材料与方法 1.1 研究区域概况衡水湖自然保护区位于河北省衡水市境内, 地跨桃城、冀州两区, 2003年被评为国家级自然保护区, 保护区总面积163.65 km2, 湖泊蓄水总面积75 km2(冀州境内57 km2, 桃城区境内18 km2), 分为东、西两湖, 最大蓄水能力为1.88×108m3.现如今只有东湖常年蓄水, 水源补给主要为定期黄河引水.衡水湖是南水北调中线工程丹江口—北京的必经之路, 亦是“南水北调”调蓄工程的枢纽[13, 14].
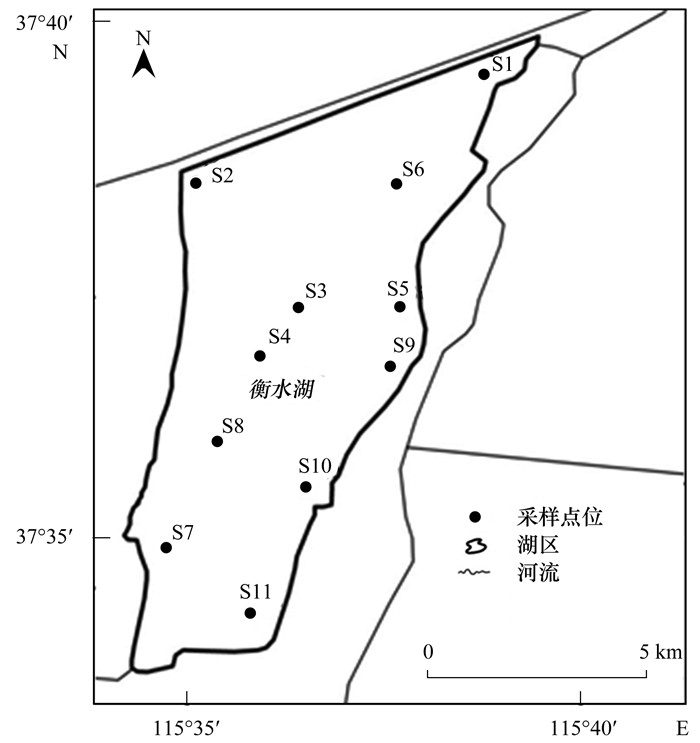
1.2 点位布设与样品采集基于衡水湖湖区功能划分、水动力特征及污染源分布等因素, 在衡水湖湖区设置11个采样点(图 1), 采样点编号及地理位置信息如表 1所示(S9、S10和S11为小湖区, 其余为大湖区). 2019年3月使用抓斗式采样器采集该11个点位的表层沉积物(0~10 cm), 密封保存于聚乙烯自封袋中, 低温储存.
|
图 1 衡水湖沉积物采样点分布示意 Fig. 1 Map of sediment sampling sites in Hengshui Lake |
|
|
表 1 衡水湖沉积物采样点分布地理位置信息表 Table 1 Geographic location information of sediment sampling sites in Hengshui Lake |
1.3 样品的处理及测定
沉积物样品经冷冻后, 剔除沙石、动植物碎片等, 并混合均匀.进一步采用玛瑙研钵研磨后过100目尼龙筛, 装入聚乙烯塑料自封袋, 放入冰箱中冷冻保存备用.
采用烧失量法[15]将冷冻干燥后沉积物样品, 称取0.2~0.5 g, 在550℃下将样品置于马弗炉中干烧3 h, 根据质量差法测定沉积物样品中有机质(TOC)含量.
采用SMT法[16]提取沉积物样品中总磷(TP)、无机磷(IP)和有机磷(OP).采用基于Rydin[17]改进的连续提取法对沉积物中无机磷形态进行连续分级提取, 依次获得弱吸附态磷(NH4Cl-P)、金属氧化物结合态磷(Al-P)、可还原态磷(Fe-P)、钙结合态磷(Ca-P)和残渣磷(Res-P).经过适当稀释后采用磷钼蓝法[18]对提取液中各形态磷进行定量分析.
采用过硫酸盐氧化法[19]测定沉积物中总氮(TN).采用化学连续提取法[20]对沉积物中可转化态氮(TTN)进行连续分级提取, 依次获得离子交换态氮(IEF-N)、弱酸可提取态氮(WAEF-N)、强碱可提取态氮(SAEF-N)、强氧化剂可提取态氮(SOEF-N), 各提取液经过适当稀释后参照文献[21], 分别采用纳氏试剂分光光度法和重氮偶合分光光度法测定稀释液中的NH4+-N和NO2--N, 通过Zn-Cd还原后采用重氮偶合分光光度法[22]测定NO3--N.最后残渣态氮(Res-N)以总氮(TN)与其他各提取态氮差值获得[23].
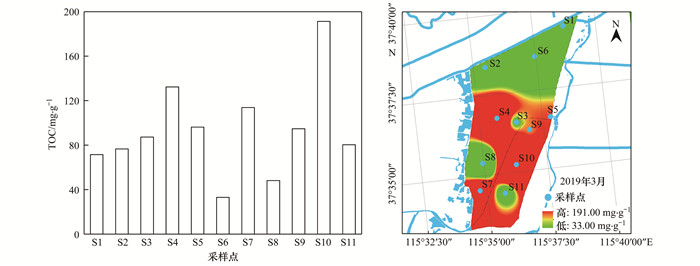
2 结果与讨论 2.1 沉积物有机质含量及其分布特性碳不仅是沉积物中的重要营养元素之一, 也是氮、磷迁移转化的重要载体, 对水体富营养化有着重要的影响[24].而沉积物中的TOC作为自然界中一种重要胶体, 能够与重金属和有机物等发生一系列复杂的物理和化学反应, 是反映水体沉积物营养程度的重要标志[25].衡水湖沉积物中TOC含量范围为33.014~191.350 mg·g-1, 其平均含量为93.226 mg·g-1(图 2), 可以看出衡水湖沉积物TOC含量空间差异较大, 就空间分布而言, S6和S8的沉积物TOC含量较低, 分别为33.014 mg·g-1和48.208 mg·g-1, 低于平均值, S4和S10的沉积物TOC含量较高, 分别为132.340 mg·g-1和191.350 mg·g-1, 其整体分布呈现中部区高, 北部区低的特征.
|
图 2 衡水湖TOC含量空间分布 Fig. 2 Spatial distribution of TOC content in Hengshui Lake |
有研究表明, TOC对释放TN有较大的影响, 沉积物中TOC含量越高, 所释放TN的量也就越大.通常情况下, 表层沉积物中有机物质含量较高时, 有机氮和氨氮是表层沉积物中氮的主要存在形式.因此, TOC在湖泊沉积物中的沉积可能成为湖泊氮的重要来源[26, 27].可知, 衡水湖沉积物TOC在S6、S8湖区含量比较低, 其潜在氮源较小, 其他湖区TOC含量较高, 其潜在氮源较大.衡水湖TOC平均含量高于滇池[28, 29], 且远高于太湖、巢湖和鄱阳湖等[30]我国典型湖泊, 可能是衡水湖湖区水生高等植物偏多, 沉积物中亦包含大量腐烂植物根茎及底栖生物残体, 其有机物尚未矿化, 含有较高的TOC.
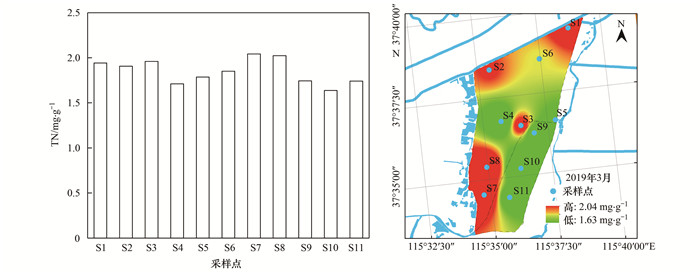
2.2 沉积物不同形态氮含量及其分布特性衡水湖沉积物中TN含量为1.638~2.042 mg·g-1, 其平均含量为1.850 mg·g-1(图 3), 其中, S7点位沉积物TN值最高, 为2.042 mg·g-1, S10点位沉积物TN值最低, 为1.638 mg·g-1, 其整体分布呈现西部区和北部区高, 东部区低的特征.
|
图 3 衡水湖TN含量空间分布 Fig. 3 Spatial distribution of TN content in Hengshui Lake |
S7和S8处TN含量相对较大, 这可能与S7湖区是道安寺, 旅游污染贡献率大, 接受外源氮的总量多, 且S7和S8点位附近从未进行过沉积物清淤有关. TN空间分布差异较小, 从总体平均值来看, 大湖区污染比小湖区严重, 推测大湖区受外源输入的影响比小湖区大.根据EPA制定的分类标准, 衡水湖湖区TN平均值在1~2 mg·g-1之间[31], 属中度污染.可知, 衡水湖沉积物受到一定程度的氮污染.
可转化态氮(TTN)是表层沉积物氮素中最“活跃”的形态, 受物理、化学、生物及地质等多方面影响, TTN不仅直接参与氮循环, 还可能通过早期成岩作用转化为颗粒物中相对惰性的氮[32]. TTN根据结合强度分为离子交换态氮(IEF-N)、弱酸可提取态氮(WAEF-N)、强碱可提取态氮(SAEF-N)和强氧化剂可提取态氮(SOEF-N).一般情况, IEF-N是所有可转化态氮中结合能力最弱的, 最容易被释放并参与湖泊系统氮循环; WAEF-N的结合能力相当于碳酸盐的结合能力, 其释放能力稍低于IEF-N; SAEF-N的结合能力相当于铁锰氧化物的结合能力, 稍高于WAEF-N, 故其释放能力稍低于WAEF-N.即3种无机形态的可转化态氮释放能力为IEF-N>WAEF-N>SAEF-N. SOEF-N也称为可转化态有机氮和其它惰性氮, 主要是有机形态的氮和强结合态氮, 其释放能力比可转化态无机氮的释放能力弱, 是4种可转化态氮中最弱的, 也是最难被释放参与氮循环的形态[27].
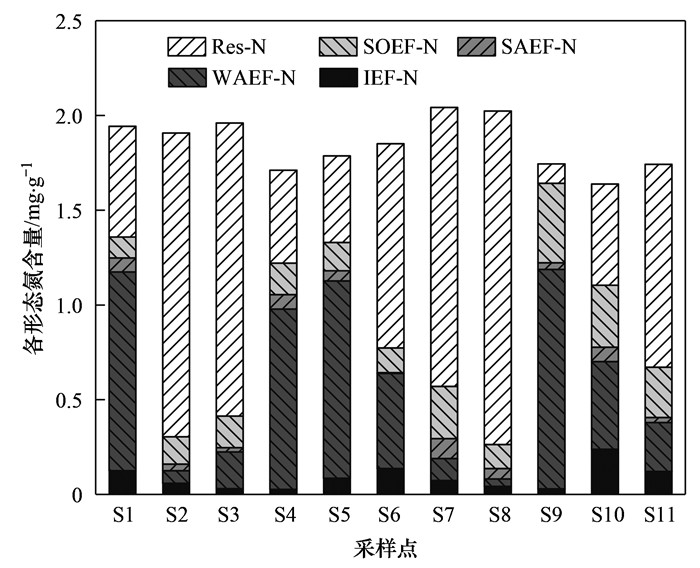
衡水湖沉积物中各种氮形态的平均含量及其在TN占比依次为: Res-N(0.973 mg·g-1, 52.57%)>WAEF-N(0.531 mg·g-1, 28.69%)>SOEF-N(0.208 mg·g-1, 11.23%)>IEF-N(0.088 mg·g-1, 4.77%)>SAEF-N(0.051 mg·g-1, 2.75%), 如图 4所示. TTN含量差异较大, WAEF-N含量最高, SAEF-N含量最小.各形态氮的空间分布差异较大, 可能与各点位自身性质及周围环境条件有关, 其中S9点位WAEF-N的含量高于其他点位; SAEF-N的含量分布较为复杂, S7点位的含量明显高于其他点位; S9点位SOEF-N的含量相对高于其他点位.衡水湖沉积物中TTN在TN的平均占比47.43%, 约占TN的一半, 说明沉积物氮释放风险较强, TTN中含量最高的较活泼的WAEF-N在TN的平均占比28.69%, TTN中最活泼的IEF-N在TN的平均占比4.77%, 同时结合温度和水体营养盐浓度等环境条件研究, 进一步说明衡水湖沉积物氮释放风险较大.
|
图 4 衡水湖沉积物中各形态氮含量分布 Fig. 4 Content of different N forms in the sediments from Hengshui Lake |
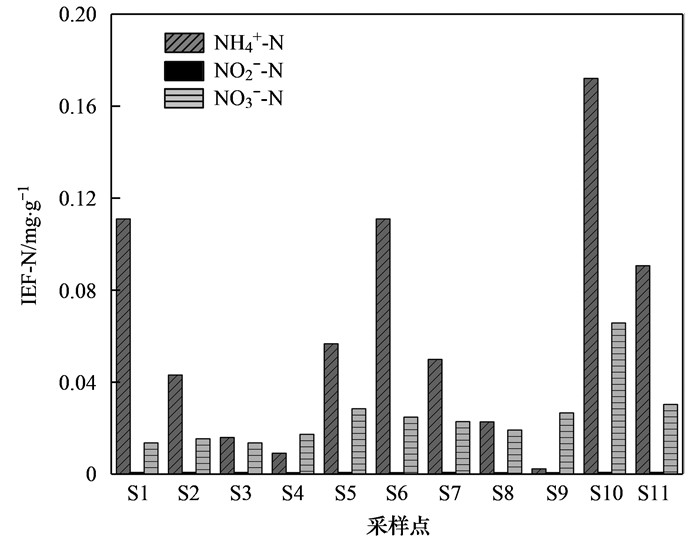
离子交换态氮结合能力最差, 相较于其他形态氮, 更易与水体发生相互作用, 直接参与到生物的生命活动中[32].主要由NH4+-N和NO3--N组成, 其中NH4+-N的含量范围在0.002~0.172 mg·g-1之间, 平均值为0.062 mg·g-1, NO2--N的含量极少, 平均值为0.001 mg·g-1, NO3--N的含量范围在0.014~0.065 mg·g-1之间, 平均值为0.025 mg·g-1; NH4+-N在IEF-N中占主导地位, NO3--N次之(图 5).
|
图 5 沉积物离子交换态氮中NH4+-N、NO2--N和NO3--N的分布特征 Fig. 5 Distribution of NH4+-N, NO2--N, and NO3--N in the IEF-N of sediments |
IEF-N中NH4+-N和NO3--N的成岩机制存在着一定的差异:NH4+-N主要受到TOC含量、氧化还原环境的影响; NO3--N的分布与水体密切相关[32].无机形态的可提取态氮中NH4+-N对上覆水体中氮最具潜在影响.蓝藻暴发时水体中的NH4+-N被大量利用, 浮游植物最先吸收利用NH4+-N, 此外, 沉积物中NH4+-N的释放将有可能促进藻类的进一步大量生长[23].
衡水湖沉积物IEF-N中NH4+-N占主导地位, NO2--N和NO3--N的含量很低, 可能与沉积物中TOC含量高且处于强还原性环境(Eh<0 mV)有关, 其中S10点位NH4+-N含量明显高于其他点位, 氮污染风险较大, S9点位NH4+-N含量明显低于其他点位, 氮污染风险较小, IEF-N中NH4+-N空间分布不均衡.
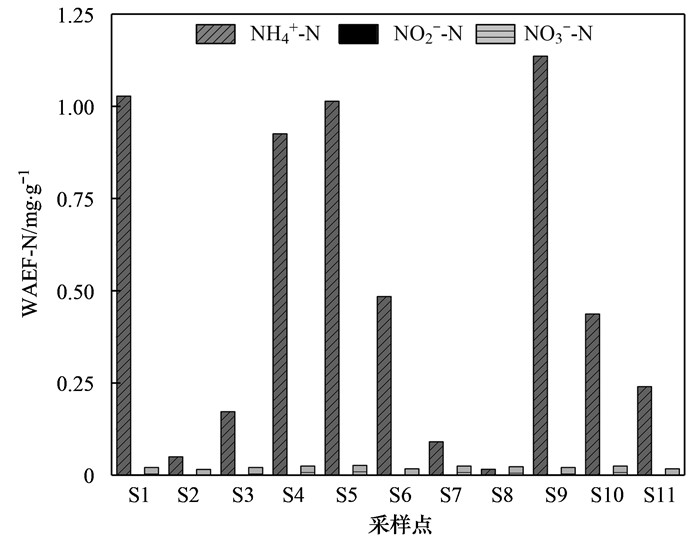
2.2.2 弱酸可提取态氮(WAEF-N)弱酸可提取态氮也称碳酸盐结合态氮(CF-N), 是溶解性有机物结合的有机氮及碳酸盐结合的无机氮[32].主要由NH4+-N和NO3--N组成, 其中NH4+-N的含量范围在0.016~1.136 mg·g-1之间, 平均值为0.508 mg·g-1, NO2--N的含量极少, 平均值为0.001 mg·g-1, NO3--N的含量范围在0.015~0.027 mg·g-1之间, 平均值为0.021 mg·g-1, NH4+-N在WAEF-N中占主导地位, NO3--N次之(图 6).有研究表明, WAEF-N也是易释放态氮, 其产生与分布主要取决于沉积物的碳酸盐和有机质含量, 同时与pH值密切相关[23].随着碳酸盐与有机质含量的增加, WAEF-N亦相应增加[27].
|
图 6 沉积物弱酸可提取态氮中NH4+-N、NO2--N和NO3--N的分布特征 Fig. 6 Distribution of NH4+-N, NO2--N, and NO3--N in the WAEF-N of sediments |
衡水湖沉积物WAEF-N中NH4+-N占主导地位, NO2--N和NO3--N的含量很低, 可能与沉积物中强还原性环境有关, 其中S1、S4、S5和S9点位NH4+-N含量明显高于其他点位, 氮污染风险较大, S8点位NH4+-N含量明显低于其他点位, 氮污染风险较小, WAEF-N中NH4+-N空间分布不均衡. WAEF-N作为TN中占比(28.69%)最大的一种可转化态氮形态, 可能是衡水湖所在区域属于我国北方的石灰性土壤, 沉积物碳酸盐含量高, 从而沉积物中WAEF-N含量占绝对优势.
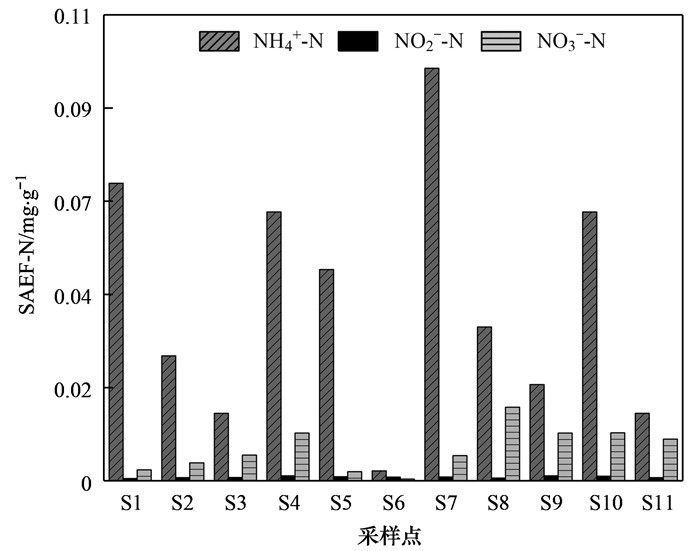
2.2.3 强碱可提取态氮(SAEF-N)强碱可提取态氮也称铁锰氧化态氮(IMOF-N), 在敏感的氧化条件下与铁锰化合物结合的氮形态, 其结合能力与铁锰氧化物的结合能力不相上下[32].其中NH4+-N的含量范围在0.002~0.097 mg·g-1之间, 平均值为0.042 mg·g-1, NO2--N的含量极少, 平均值为0.001 mg·g-1, NO3--N的含量范围在0.001~0.017 mg·g-1之间, 平均值为0.007 mg·g-1, NH4+-N在SAEF-N中占主导地位, NO3--N次之(图 7).
|
图 7 沉积物强碱可提取态氮中NH4+-N、NO2--N和NO3--N的分布特征 Fig. 7 Distribution of NH4+-N, NO2--N and NO3--N in the SAEF-N of sediments |
SAEF-N是一种对氧化还原环境敏感的氮形态, 该形态氮与铁锰化合物的结合能力与沉积物环境氧化还原特性有关, 沉积物的还原性越强, SAEF-N含量可能越低[27]. SAEF-N在沉积物-水界面pH值升高及氧化还原电位降低时易释放于上覆水体.
衡水湖沉积物SAEF-N中NH4+-N占主导地位, 其次为NO3--N, NO2--N含量最低, 这可能与沉积物中强还原性环境有关, 其中S7点位NH4+-N含量明显高于其他点位, 氮污染风险较大, S6点位NH4+-N含量明显低于其他点位, 氮污染风险较小, SAEF-N中NH4+-N空间分布不均衡.而衡水湖沉积物中SAEF-N含量最低, 且沉积物Eh<0mV, 为强还原性条件, 进一步反映由于衡水湖沉积物处于强还原性环境, 导致SAEF-N易释放于水体, 使沉积物中SAEF-N含量低.
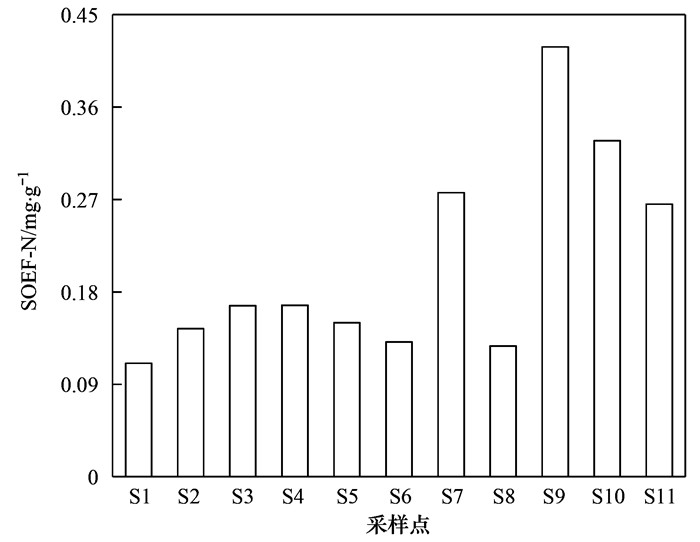
2.2.4 强氧化剂可提取态氮(SOEF-N)强氧化剂可提取态氮也称有机物与硫化物结合态氮(OSF-N), 主要指的是与有机质和硫化物结合的可转化态氮, 其结合能力最强, 最难被释放[32].其中NO3--N的含量范围在0.111~0.419 mg·g-1之间, 平均值为0.208 mg·g-1, NO3--N在SOEF-N中占主导地位. SOEF-N可在微生物和其他环境条件的作用下分解释放, 是水体氮的一个重要来源[23]. SOEF-N含量的多少与沉积物来源有关, 此外氧化还原环境及TOC的释放速度、沉积物自身的吸附均会对SOEF-N分布特征造成一定影响[32].一般来说, TOC含量高的沉积物, SOEF-N也越高[27].
衡水湖沉积物SOEF-N中NO3--N占主导地位, 其中S9和S10点位NO3--N含量明显高于其他点位, 氮污染风险较大, S1点位NO3--N含量明显低于其他点位, 氮污染风险较小, 且SOEF-N中NO3--N空间分布不均衡(图 8). SOEF-N在TN占比为11.23%, 占比较高, 在可转化态氮中仅次于WAEF-N, 可在侧面反映衡水湖沉积物TOC的高含量.
|
图 8 沉积物强氧化剂可提取态氮中NO3--N的分布特征 Fig. 8 Distribution of NO3--N in the SOEF-N of sediments |
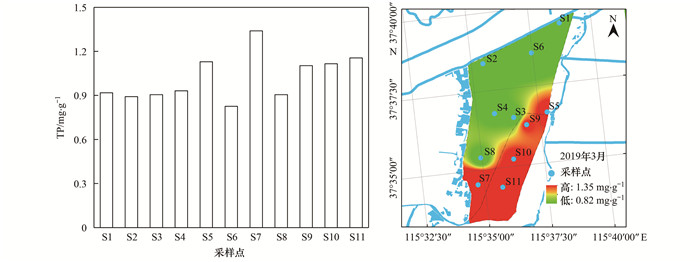
衡水湖沉积物中TP含量为0.826~1.340 mg·g-1, 其平均含量为1.020 mg·g-1.其中S7点位沉积物TP值最高, 为1.340 mg·g-1, S6点位沉积物TP值最低, 为0.826 mg·g-1(图 9), 其整体分布呈现东南部区高, 西北部区低的特征.其中, S7处TP含量较大, 而S6处, TP的含量较小, 可能是S6附近历史上曾经进行过沉积物清淤而S7附近历史上未曾进行过清淤. TP呈现出空间分布, 按总体平均值来说, 小湖区TP含量仍高于大湖区, 说明小湖区磷污染比大湖区严重.根据总磷的含量沉积物的污染水平分为三级, 重污染水平:TP>1.3 mg·g-1; 中等污染水平:0.5 mg·g-1<TP<1.3 mg·g-1; 轻度污染水平:TP<0.5 mg·g-1[33], 衡水湖沉积物中总磷含量处于中等污染水平, 属中度污染.可知, 衡水湖沉积物受到一定程度的磷污染.
|
图 9 衡水湖TP含量空间分布 Fig. 9 Spatial distribution of TP content in Hengshui Lake |
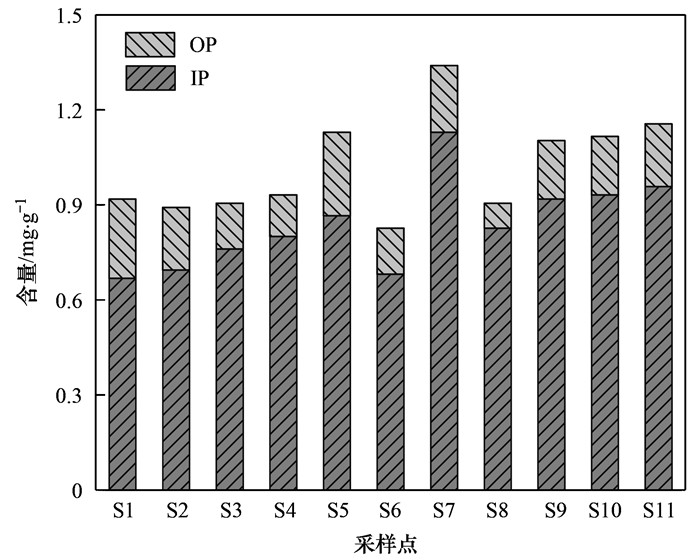
衡水湖沉积物中IP的含量为0.668~1.129 mg·g-1, 平均含量为0.839 mg·g-1, 占TP含量的82.27%; OP在衡水湖沉积物中的含量为0.079~0.264 mg·g-1, 平均为0.181 mg·g-1, 占TP含量的17.73%(图 10).
|
图 10 衡水湖IP和OP含量空间分布 Fig. 10 Spatial distribution of IP and OP content in Hengshui Lake |
有研究表明, 湖泊沉积物中近50%~60%的有机磷(OP)可被降解或水解为生物可利用磷形态, 具有部分的活性, 是湖泊系统中重要的“磷蓄积库”[34].在厌氧释放过程中, 存在有机磷向无机磷转化, 铁磷、铝磷向钙磷、闭蓄态磷转化的趋势, 从而使沉积物中总磷含量不断减少[35].总体而言, 衡水湖沉积物受到一定程度的磷污染, 沉积物中的磷主要以无机磷形式存在, S6点位IP含量最低, S7点位IP含量较高, IP空间分布差异较大, OP含量很低.
2.3.1 弱吸附态磷(NH4Cl-P)NH4Cl-P即松散吸附的磷, 当沉积物环境发生变化或受到扰动时, 沉积物中弱吸附态的活性磷最容易进入上层水体中, 并被生物吸收利用.尽管弱吸附态磷在沉积物中的含量相对较小, 但却是活性最大的一种磷形态[34].衡水湖沉积物中NH4Cl-P的含量较低, 为0.028~0.034 mg·g-1, 平均为0.030 mg·g-1, 约占无机磷总量的3.58%.
2.3.2 可还原态磷(Fe-P)和金属氧化物结合态磷(Al-P)Fe-P和Al-P具有很强的释放活性, 也是内源污染负荷的重要来源之一.当沉积物中的氧化还原环境变化时, 沉积物中的Fe-P与Al-P可转化为可溶性磷, 并通过间隙水进入上覆水体, 对湖泊水质产生很大影响[34].衡水湖沉积物中Fe-P和Al-P总含量为0.142~0.193 mg·g-1, 平均为0.169 mg·g-1, 占无机磷的20.14%.与水体富营养化息息相关的Fe-P和Al-P在衡水湖沉积物中较高的含量和比例分布, 不但揭示了沉积物中较大的潜在磷源, 同时也说明了衡水湖近年来存在潜在污染, 易发生磷污染.
2.3.3 钙结合态磷(Ca-P)Ca-P又称为酸提取磷, 主要指与自生磷灰石、湖泊沉积碳酸钙以及生物骨骼等的含磷矿物有关的沉积磷存在形态.由于Ca-P很稳定且很难被分解或转化为磷酸盐, 基本上对间隙水和上覆水中磷酸盐的富集没有贡献[34]. Ca-P含量为0.358~0.618 mg·g-1, 平均含量0.440 mg·g-1, 平均占无机磷的52.44%. Ca-P是无机磷中含量比例最大的一种形态, 其原因可能为衡水湖所在区域属于我国北方的石灰性土壤, 沉积物有碎屑磷灰石存在, 从而决定了沉积物中钙结合态磷含量占绝对优势.
2.3.4 残渣磷(Res-P)Res-P主要指禁锢于矿物氧化物和矿物晶格中的磷, 由于难以转化为溶解磷而释放到上覆水中, 对水体富营养化几乎没有贡献, 是最稳定的一种磷[34]. Res-P含量为0.107~0.297 mg·g-1, 平均含量0.200 mg·g-1, 平均占无机磷的23.84%.
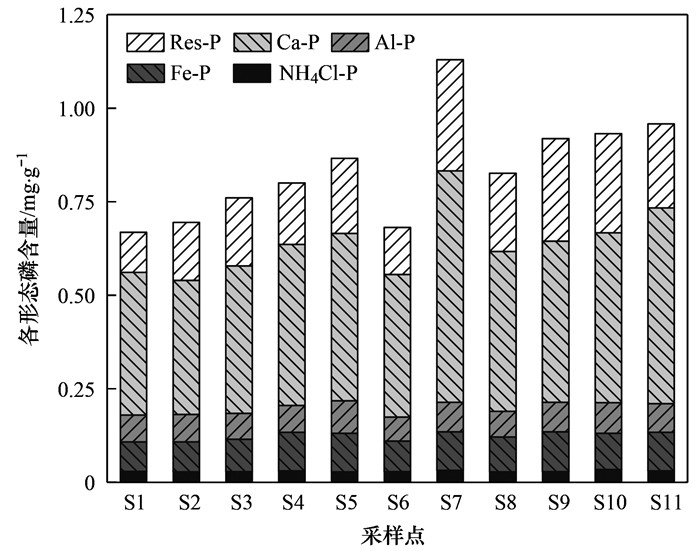
由图 11可知, 衡水湖沉积物中IP各形态含量差异较大, Ca-P含量最高, NH4Cl-P含量最小.其中各点位NH4Cl-P、Fe-P和Al-P的含量空间分布差异较小, Ca-P含量空间分布差异较大, S7点位Ca-P的含量明显高于其他位点.衡水湖沉积物各形态磷的相对比例与其已有研究结果大体一致[36].衡水湖沉积物中较活泼IP形态的平均占比为23.97%, 约占IP的1/5, 说明沉积物磷释放风险较弱. IP形态中含量最高的较稳定的Ca-P与最稳定的Res-P在IP的平均占比76.03%, 而IP形态中最活泼的NH4Cl-P在IP的平均占比为3.59%, 同时结合pH和溶解氧等环境条件研究, 进一步说明衡水湖沉积物磷释放风险较小.
|
图 11 衡水湖沉积物中各形态磷含量分布 Fig. 11 Content of different P forms in the sediments from Hengshui Lake |
衡水湖沉积物中C/N分布见表 2, 沉积物中C/N为20.8~136.3, 平均值为60.2, 空间分布差异极大.沉积物中C/N可以反映有机质的来源:通常情况水生生物为2.8~3.4;浮游动物一般小于7;浮游植物为6~14;藻类为5~14;高等植物为14~23;维管束陆生植物通常大于20;而陆生禾本科或莎草科植物可以高达45~50[24, 37].衡水湖湖体与岸边生长有大量的芦苇蒲草, 沉积物中含有大量腐烂芦苇等植物根茎, 该类型植物可以从水体和底泥中吸收碳、氮和磷等营养物质, 并同化为自身结构组成物质, 在植物死亡后释放出这些营养物质[38].因此, 衡水湖沉积物中有机质可能主要是来自陆生高等植物, 芦苇蒲草等植物凋谢后残体可能是衡水湖沉积物中有机质的主要来源.
|
|
表 2 衡水湖沉积物营养盐相互关系 Table 2 Relationship between nutrients in sediments of Hengshui Lake |
C/P在一定程度上可以反映沉积物中有机碳和磷化合物的分解速率, 一般来说表层沉积物中P比C分解速度快[39].衡水湖沉积物中C/P分布见表 2, 沉积物中C/P为103.2~442.9, 平均值为233.1, 空间分布差异极大, 表明衡水湖表层沉积物中P比C分解速度快, 与文献[24, 39]的观点一致.
沉积物中N、P含量及比值通常可以综合反映水中N、P聚积和沉积及沉积物溶出与释放两种动态过程, 在某种程度上反映了水体中营养化状态[39].衡水湖沉积物中N/P分布见表 2, 沉积物中N/P为3.2~5.0, 空间分布上大湖区高于小湖区, 全湖平均值为4.1, 小于Redfield比(C:N:P=106:16:1)[40], 表明衡水湖沉积物中磷可能主要受陆源输入的影响.同时, 衡水湖每年引入的黄河水中可能输入大量含磷物质[41], 据此推断衡水湖沉积物中磷主要以外源为主.
2.4.2 沉积物各营养盐相关性分析由表 3可知, 沉积物中TOC、TN和TP三者之间无显著性相关, 表明三者的来源可能有差异. TN与Res-N的含量呈极显著正相关(r=0.744, P < 0.01), 且Res-N占TN含量的52.57%, Res-N对TN含量贡献率很大.各形态氮之间基本无显著相关, 表明各形态氮来源多样性与复杂性. TP与IP的含量呈极显著正相关(r=0.942, P < 0.01), 且IP占TP含量的82.27%, IP对TP含量贡献率很大. TP和IP都与Fe-P、Al-P、Ca-P和Res-P呈显著或极显显著相关关系, 其中Ca-P与TP和IP呈极显著正相关(r=0.901, P < 0.01; r=0.939, P < 0.01), 且Ca-P在TP和IP占比分别为43.21%和52.59%, Ca-P对磷含量贡献率很大, 结合之前分析研究进一步说明衡水湖沉积物中磷释放风险较小.同时Fe-P、Al-P、Ca-P和Res-P之间互相呈显著或极显著相关, 反映其具有一定来源转化关系; NH4Cl-P与TOC的含量呈极显著正相关(r=0.811, P < 0.01), 表明NH4Cl-P与TOC具有一定同源性.总的来看, 衡水湖沉积物中碳、氮和磷之间相关性较弱, 各形态磷之间的相关性强于各形态氮.
|
|
表 3 衡水湖沉积物中不同形态氮磷及有机质的相关系数矩阵1) Table 3 Pearson correlation coefficient matrix for nitrogen, phosphorus forms and total organic carbon in sediments |
2.5 衡水湖沉积物污染状况评价
由于沉积物污染状况评价未有统一评价标准, 结合文献[42]的报道与衡水湖表层沉积物的实际情况, 利用有机指数和有机氮来评价衡水湖沉积物营养盐污染情况.有机指数常用来评价水域沉积物的环境状况, 有机氮则是衡量湖泊表层沉积物是否遭受氮污染的重要指标, 其计算方法如下:
有机指数=有机碳(%)×有机氮(%)
有机碳(%)=有机质(%)/1.724
有机氮(%)=总氮(%)×0.95
|
|
表 4 沉积物有机指数评价标准 Table 4 Evaluation standards of organic index in sediments |
|
|
表 5 沉积物有机氮评价标准 Table 5 Evaluation standards of organic nitrogen in sediments |
按照沉积物有机指数和有机氮评价标准, 衡水湖沉积物污染状况评价结果如表 6, 可知衡水湖各点位沉积物的有机指数在0.337~1.727之间, 平均值为0.934, 为Ⅳ级标准, 湖泊沉积物环境状况为有机污染, 其中, S6点位相对较轻, 为尚清洁, 其余各点位均为有机污染.各点位沉积物的有机氮在0.156%~1.194%之间, 平均值为0.176%, 均为Ⅳ级标准, 湖泊表层沉积物均遭受氮污染.可以看出衡水湖沉积物营养盐污染程度严重, 已达到Ⅳ级标准, 全湖氮污染严重.可能是衡水湖四周与水中均含有丰富的芦苇等挺水植物, 水下亦有大量腐烂植物与动物残体, 形成生物残留沉积, 导致衡水湖沉积物营养盐污染程度严重.建议今后加强对衡水湖底质沉积物清淤工作的力度, 定期对湖中动植物残体进行清除.
|
|
表 6 衡水湖沉积物营养盐污染状况评价 Table 6 Evaluation of nutrient pollution in sediments of Hengshui Lake |
3 结论
(1) 衡水湖沉积物中TOC平均含量为93.226 mg·g-1, TOC含量较高, 导致潜在氮源污染风险较大. TN平均含量为1.850 mg·g-1, 属中度污染; 各种氮形态平均含量及TN占比依次为: Res-N(0.973 mg·g-1, 52.57%)>WAEF-N(0.531 mg·g-1, 28.69%)>SOEF-N(0.208 mg·g-1, 11.23%)>IEF-N(0.088 mg·g-1, 4.77%)>SAEF-N(0.051 mg·g-1, 2.75%), 衡水湖沉积物氮释放风险相对较高. TP平均含量为1.020 mg·g-1, 其中IP平均含量为0.839 mg·g-1, 占TP含量的82.27%, 属中度污染; 各种磷形态平均含量及IP占比依次为: Ca-P(0.440 mg·g-1, 52.44%)>Res-P(0.200 mg·g-1, 23.84%)>Fe-P和Al-P(0.169 mg·g-1, 20.14%)>NH4Cl-P(0.030 mg·g-1, 3.58%), 衡水湖沉积物磷释放风险相对较小.
(2) C/N、C/P和N/P特征分析结果表明, 衡水湖沉积物中有机质主要是来自陆生禾本科和莎草科陆生高等植物, 沉积物中磷主要受陆源输入的影响.各营养盐相关性分析结果表明, 衡水湖沉积物中碳、氮、磷之间相关性较弱, 三者的来源可能不同; 各形态磷之间的相关性强于各形态氮, 各形态磷具有很好的同源性, 而各形态氮来源多样且复杂.
(3) 污染状况评价结果表明, 衡水湖沉积物营养盐污染程度严重, 达到Ⅳ级标准, 全湖氮污染严重, 推测与大量腐烂植物与动物残体, 形成生物残留沉积有关, 建议加强沉积物清淤工作的力度, 并定期清除湖中动植物残体.
| [1] | 裘知, 王睿, 李思亮, 等.中国湖泊污染现状与治理情况分析[A].见: 湖泊湿地与绿色发展-第五届中国湖泊论坛论文集[C].长春: 中国科学技术协会学会学术部, 2015.207-211. |
| [2] |
魏丽萍, 梁美生. 我国湖泊富营养化问题概述[J]. 化工文摘, 2008(6): 38-40. Wei L P, Liang M S. A summary of the problem of lake eutrophication in China[J]. China Chemicals, 2008(6): 38-40. |
| [3] |
张光贵, 黄博. 洞庭湖表层沉积物营养盐污染特征与评价[J]. 环境工程技术学报, 2016, 4(6): 514-519. Zhang G G, Huang B. Pollution characteristics and evaluation of surface sediment nutrients in Dongting Lake[J]. Journal of Environmental Engineering Technology, 2016, 4(6): 514-519. |
| [4] |
熊春晖, 张瑞雷, 吴晓东, 等. 滆湖表层沉积物营养盐和重金属分布及污染评价[J]. 环境科学, 2016, 37(3): 925-934. Xiong C H, Zhang R L, Wu X D, et al. Distribution and pollution assessment of nutrient and heavy metals in surface sediments from Lake Gehu in Southern Jiangsu Province, China[J]. Environmental Science, 2016, 37(3): 925-934. |
| [5] |
甘树, 卢少勇, 秦普丰, 等. 太湖西岸湖滨带沉积物氮磷有机质分布及评价[J]. 环境科学, 2012, 33(9): 3064-3069. Gan S, Lu S Y, Qin P F, et al. Spatial distribution and evaluation of nitrogen, phosphorus and organic matter in surface sediments from Western Lakeside Belt of Lake Taihu[J]. Environmental Science, 2012, 33(9): 3064-3069. |
| [6] | Shan J L, Zhu W Q, Pan M, et al. Characteristics and evaluation for nitrogen pollution in water and surface sediments of Xixi Wetland[A]. In: Proceedings of the 20133rd International Conference on Intelligent System Design and Engineering Applications[C]. Hong Kong, China: IEEE, 2013. |
| [7] | Wang S R, Zhao Y L, Jiao L X, et al. Characteristics of soluble organic nitrogen composition and sources in sediments from Erhai Lake in China and the effect on the water quality[J]. Environmental Earth Sciences, 2015, 74(5): 3849-3856. DOI:10.1007/s12665-015-4107-2 |
| [8] | Ni Z K, Wang S R. Historical accumulation and environmental risk of nitrogen and phosphorus in sediments of Erhai Lake, Southwest China[J]. Ecological Engineering, 2015, 79: 42-53. DOI:10.1016/j.ecoleng.2015.03.005 |
| [9] | Liu W B, Wang S R, Zhang L, et al. Phosphorus release characteristics of sediments in Erhai Lake and their impact on water quality[J]. Environmental Earth Sciences, 2015, 74(5): 3753-3766. DOI:10.1007/s12665-015-4715-x |
| [10] | Ni Z K, Wang S R, Wang Y M. Characteristics of bioavailable organic phosphorus in sediment and its contribution to lake eutrophication in China[J]. Environmental Pollution, 2016, 219: 537-544. DOI:10.1016/j.envpol.2016.05.087 |
| [11] |
王乃姗, 张曼胤, 崔丽娟, 等. 河北衡水湖湿地汞污染现状及生态风险评价[J]. 环境科学, 2016, 37(5): 1754-1762. Wang N S, Zhang M Y, Cui L J, et al. Contamination and ecological risk assessment of mercury in Hengshuihu Wetland, Hebei Province[J]. Environmental Science, 2016, 37(5): 1754-1762. |
| [12] |
黎聪, 李晓文. 衡水湖湿地恢复预案空间模拟及生态风险评价[J]. 环境科学学报, 2010, 30(6): 1312-1321. Li C, Li X W. Modeling the scenarios of restoring the wetland in Hengshui Lake national nature reserve and assessing their ecological risk[J]. Acta Scientiae Circumstantiae, 2010, 30(6): 1312-1321. |
| [13] |
张嘉雯, 魏健, 吕一凡, 等. 衡水湖沉积物中典型持久性有机污染物污染特征与风险评估[J]. 环境科学, 2020, 41(3): 1357-1367. Zhang J W, Wei J, Lü Y F, et al. Occurrence and ecological risk assessment of typical persistent organic pollutants in Hengshui Lake[J]. Environmental Science, 2020, 41(3): 1357-1367. |
| [14] |
刘利, 张嘉雯, 陈奋飞, 等. 衡水湖底泥重金属污染特征及生态风险评价[J]. 环境工程技术学报, 2020, 10(2): 205-211. Liu L, Zhang J W, Chen F F, et al. Pollution characteristics and ecological risk assessment of heavy metals in the sediment of Hengshui Lake[J]. Journal of Environmental Engineering Technology, 2020, 10(2): 205-211. |
| [15] |
胡彩莉, 马玉贞, 郭超, 等. 烧失量法测定土壤有机质含量的实验条件探究[J]. 地球与环境, 2016, 44(1): 110-118. Hu C L, Ma Y Z, Guo C, et al. Optimization of the experiment conditions for estimating organic matter content with loss-on-ignition method[J]. Earth and Environment, 2016, 44(1): 110-118. |
| [16] | Pardo P, Rauret G, López-Sánchez J F. Shortened screening method for phosphorus fractionation in sediments:a complementary approach to the standards, measurements and testing harmonised protocol[J]. Analytica Chimica Acta, 2004, 508(2): 201-206. DOI:10.1016/j.aca.2003.11.005 |
| [17] | Rydin E. Potentially mobile phosphorus in Lake Erken sediment[J]. Water Research, 2000, 34(7): 2037-2042. DOI:10.1016/S0043-1354(99)00375-9 |
| [18] | HJ632-2011, 土壤总磷的测定碱熔-钼锑抗分光光度法[S]. |
| [19] | 钱君龙, 张连弟, 乐美麟. 过硫酸盐消化法测定土壤全氮全磷[J]. 土壤, 1990, 22(5): 258-262. |
| [20] |
马红波, 宋金明, 吕晓霞, 等. 渤海沉积物中氮的形态及其在循环中的作用[J]. 地球化学, 2003, 32(1): 48-54. Ma H B, Song J M, Lü X X, et al. Nitrogen forms and their functions in recycling of the Bohai sea sediments[J]. Geochimica, 2003, 32(1): 48-54. |
| [21] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002. |
| [22] |
张勇, 程祥圣, 吴月英, 等. 锌-镉还原-分光光度法测定地表水中硝酸盐[J]. 理化检验-化学分册, 2008, 44(2): 139-141. Zhang Y, Cheng X S, Wu Y Y, et al. Spectrophotometric determination of nitrate in surface water after reduction with Zinc metal in Cd(Ⅱ) solution[J]. Physical Testing and Chemical Analysis (Part B:Chemical Analysis), 2008, 44(2): 139-141. |
| [23] |
朱元荣, 张润宇, 吴丰昌. 滇池沉积物中氮的地球化学特征及其对水环境的影响[J]. 中国环境科学, 2011, 31(6): 978-983. Zhu Y R, Zhang R Y, Wu F C. Geochemical characteristics and influence to overlying water of nitrogen in the sediments from Dianchi Lake[J]. China Environmental Science, 2011, 31(6): 978-983. |
| [24] |
黄廷林, 刘飞, 史建超. 水源水库沉积物中营养元素分布特征与污染评价[J]. 环境科学, 2016, 37(1): 166-172. Huang T L, Liu F, Shi J C. Distribution characteristics and pollution status evaluation of sediments nutrients in a drinking water reservoir[J]. Environmental Science, 2016, 37(1): 166-172. |
| [25] |
卢少勇, 许梦爽, 金相灿, 等. 长寿湖表层沉积物氮磷和有机质污染特征及评价[J]. 环境科学, 2012, 33(2): 393-398. Lu S Y, Xu M S, Jin X C, et al. Pollution characteristics and evaluation of nitrogen, phosphorus and organic matter in surface sediments of Lake Changshouhu in Chongqing, China[J]. Environmental Science, 2012, 33(2): 393-398. |
| [26] |
罗玉红, 苏青青, 高婷, 等. 底泥泥质与污染物释放量的关系[J]. 三峡大学学报(自然科学版), 2012, 34(1): 19-22. Luo Y H, Su Q Q, Gao T, et al. Relationship between sediment quality and pollutant release quantity[J]. Journal of China Three Gorges University (Natural Sciences), 2012, 34(1): 19-22. |
| [27] | 焦立新.浅水湖泊表层沉积物氮形态特征及在生物地球化学循环中的功能[D].呼和浩特: 内蒙古农业大学, 2007. |
| [28] |
韩秀秀, 黄晓虎, 余丽燕, 等. 滇池沉积物有机质沉积特征与来源解析[J]. 环境科学, 2017, 38(1): 78-86. Han X X, Huang X H, Yu L Y, et al. Sedimentary characteristics and sources of organic matter in sediments of Dianchi Lake[J]. Environmental Science, 2017, 38(1): 78-86. |
| [29] |
陈云增, 杨浩, 张振克, 等. 相平衡分配法在滇池沉积物环境质量评价中的应用研究[J]. 环境科学学报, 2006, 26(9): 1545-1552. Chen Y Z, Yang H, Zhang Z K, et al. Application of equilibrium partitioning approach to the assessment of sediment quality in Dianchi Lake[J]. Acta Scientiae Circumstantiae, 2006, 26(9): 1545-1552. |
| [30] |
房吉敦, 熊永强, 吴丰昌, 等. 中国典型淡水湖泊沉积物中生物标志物组成特征及源解析[J]. 环境污染与防治, 2017, 39(8): 822-828. Fang J D, Xiong Y Q, Wu F C, et al. Composition and source identification of biomarkers in surface sediments from typical freshwater lakes in China[J]. Environmental Pollution and Control, 2017, 39(8): 822-828. |
| [31] |
向速林, 朱梦圆, 朱广伟, 等. 太湖东部湖湾水生植物生长区底泥氮磷污染特征[J]. 沉积学报, 2014, 32(6): 1083-1088. Xiang S L, Zhu M Y, Zhu G W, et al. Pollution characteristics of nitrogen and phosphorus in sediment of the Eastern Bays of Lake Taihu with aquatic macrophytes[J]. Acta Sedimentologica Sinica, 2014, 32(6): 1083-1088. |
| [32] | 周美玲.七里海潟湖沉积物氮赋存形态分布特征及污染评价[D].石家庄: 河北师范大学, 2018. |
| [33] |
金晓丹, 吴昊, 陈志明, 等. 长江河口水库沉积物磷形态、吸附和释放特性[J]. 环境科学, 2015, 36(2): 448-456. Jin X D, Wu H, Chen Z M, et al. Phosphorus fractions, sorption characteristics and its release in the sediments of Yangtze Estuary Reservoir, China[J]. Environmental Science, 2015, 36(2): 448-456. |
| [34] | 邢友华.东平湖表层沉积物中磷的形态特征及对富营养化的影响研究[D].泰安: 山东农业大学, 2011. |
| [35] |
王晓蓉, 华兆哲, 徐菱, 等. 环境条件变化对太湖沉积物磷释放的影响[J]. 环境化学, 1996, 15(1): 15-19. Wang X R, Hua Z Z, Xu L, et al. The effects of the environmental conditions on phosphorus release in lake sediments[J]. Environmental Chemistry, 1996, 15(1): 15-19. |
| [36] |
刘芳, 李占臣, 秦哲, 等. 衡水湖沉积物磷形态特征分析[J]. 安徽农业科学, 2015, 43(5): 215-217, 230. Liu F, Li Z C, Qin Z, et al. Phosphorus forms and its characteristic in sediments of Hengshui Lake[J]. Journal of Anhui Agricultural Sciences, 2015, 43(5): 215-217, 230. |
| [37] |
邱祖凯, 胡小贞, 姚程, 等. 山美水库沉积物氮磷和有机质污染特征及评价[J]. 环境科学, 2016, 37(4): 1389-1396. Qiu Z K, Hu X Z, Yao C, et al. Pollution characteristics and evaluation of nitrogen, phosphorus and organic matter in sediments of Shanmei Reservoir in Fujian, China[J]. Environmental Science, 2016, 37(4): 1389-1396. |
| [38] |
种云霄, 胡洪营, 钱易. 大型水生植物在水污染治理中的应用研究进展[J]. 环境污染治理技术与设备, 2003, 4(2): 36-40. Chong Y X, Hu H Y, Qian Y. Advances in utilization of macrophytes in water pollution control[J]. Techniques and Equipment for Environmental Pollution Control, 2003, 4(2): 36-40. |
| [39] |
卓海华, 邱光胜, 翟婉盈, 等. 三峡库区表层沉积物营养盐时空变化及评价[J]. 环境科学, 2017, 38(12): 5020-5031. Zhuo H H, Qiu G S, Zhai W Y, et al. Evaluation of temporal and spatial variation characteristics of nutrients in surface sediment in the Three Gorges Reservoir Area[J]. Environmental Science, 2017, 38(12): 5020-5031. |
| [40] |
李强, 霍守亮, 王晓伟, 等. 巢湖及其入湖河流表层沉积物营养盐和粒度的分布及其关系研究[J]. 环境工程技术学报, 2013, 3(2): 147-155. Li Q, Huo S L, Wang X W, et al. Distribution and correlation of nutrients and particle size in surface sediments of Lake Chaohu and its Inflow Rivers[J]. Journal of Environmental Engineering Technology, 2013, 3(2): 147-155. |
| [41] | 丁二峰. 衡水湖水环境特征分析及改善对策[J]. 地下水, 2015, 37(4): 84-86. |
| [42] |
隋桂荣. 太湖表层沉积物中OM、TN、TP的现状与评价[J]. 湖泊科学, 1996, 8(4): 319-324. Sui G R. Statement and evaluation of organic matter, total nitrogen and total phosphate in surface layer sediments in Taihu Lake[J]. Journal of Lake Sciences, 1996, 8(4): 319-324. |
 2020, Vol. 41
2020, Vol. 41


