2. 北京市市政工程设计研究总院有限公司, 北京 100082;
3. 哈尔滨工业大学城市水资源与水环境国家重点实验室, 哈尔滨 150090
2. Beijing General Municipal Engineering Design & Research Institute Co., Ltd., Beijing 100082, China;
3. State Key Laboratory of Urban Water Resource and Environment, Harbin Institute of Technology, Harbin 150090, China
砷是饮用水中毒性最强且致癌的天然污染物之一, 长期引用高砷水会引起皮肤损害、肌无力等症状, 严重可造成皮肤、内脏器官等的癌变[1].在中国, 高砷水遍布11个省市和自治区, 涉及234多万人, 其中饮用水中砷含量大于50 μg ·L-1的地区人口已达到52万人[2].由于对人类健康的巨大威胁, WHO、中国和日本等已将砷的饮用水标准含量限值由50 μg ·L-1修订为10 μg ·L-1, 这对除砷工艺提出更为严格的要求.
目前除砷的主要技术有吸附法、离子交换法、混凝沉淀法和膜过滤法等, 其中吸附法因其具有经济环保、操作简单和处理效果好等优点, 得到广泛应用.吸附技术的关键是吸附剂的选择.因此, 寻找高效、廉价的吸附剂成为当前含砷水处理的热点.
有研究表明, 生物除铁锰滤池反冲洗泥(铁锰泥)中, 含有大量Fe(Ⅲ)(氢)氧化物和Mn(Ⅳ)氧化物, 使用铁锰泥进行吸附除砷实验, 得到了很好的除砷效果, As(Ⅴ)的最大吸附量可高达40.98~77mg ·g-1[3, 4].由于水厂废弃的铁锰泥为粉末态, 应用于水体除砷后泥水分离困难, 处理不当又会带来新的环境问题.将粉末制粒, 克服了粉末形态吸附剂在水处理方面操作复杂、不易用于固定床等固有瓶颈.本课题组采用高温烘焙法和包埋法, 其中包埋采用烘干和冻干两种干燥方式以铁锰泥为原料制备颗粒吸附剂, 对除砷性能进行比较, 并通过表征、静态实验等手段分析其原因并力求找到充分利用铁锰泥的最佳方法.
1 材料与方法 1.1 主要试剂与仪器 1.1.1 主要试剂作为原料的铁锰泥由中国哈尔滨松北水处理厂提供.该水厂的生物除铁除锰滤池稳定运行5 a以上, 进水铁和锰浓度分别为15 mg ·L-1和0.8~1.2 mg ·L-1[5].收集除铁除锰滤池的反冲洗废水, 静沉数日, 将沉积在底部的污泥取出, 自然风干, 用研钵磨碎后过100目筛置于干燥处备用.
本实验所用硼氢化钾、氢氧化钠、硫脲、乙酸均为优级纯; Na2HAsO4 ·H2O、葡萄糖、海藻酸钠、氨水、盐酸均为分析纯. As(Ⅴ)储备液(1 000 mg ·L-1)由Na2HAsO4 ·H2O制备而成.根据需要用去离子水或超纯水配制使用溶液.以上试剂均由天津福晨化学试剂厂提供.壳聚糖为中等黏度(200~400 mPa ·s), 购自中国上海麦克林生化公司.
1.1.2 主要仪器磁力搅拌器, 电子分析天平, DHG-9070A电热鼓风干燥箱, AFS-8230原子荧光分光光度计, pHSJ-3F型pH计, THZ-82恒温振荡箱, TL3014陶瓷纤维马弗炉.
1.2 制备方法 1.2.1 GA的制备将适量的铁锰泥粉末、海藻酸钠和葡萄糖均匀混合, 其重量比为10 :0.5 :2, 混匀后加入适量水制备成泥状, 制成粒径为1.0~2.0 mm的颗粒.将颗粒陈化24 h自然风干, 然后放入马弗炉中焙烧, 在180℃下预热20 min, 350℃下焙烧60 min, 以速率为10℃ ·min-1升温.待焙烧后的颗粒冷却后, 使用去离子水冲洗多次后于100℃烘干至恒重, 得到新型除砷颗粒吸附剂GA.
1.2.2 H-GA的制备称取适量的壳聚糖粉末, 溶于5%乙酸, 搅拌约6~7 h至壳聚糖粉末全部溶解.将铁锰泥粉末加入壳聚糖溶液中搅拌至均匀, 其中铁锰泥粉末质量为壳聚糖的4倍.使用分液漏斗将混合溶液均匀分散滴加到NH4OH溶液(50%, 体积分数)中剧烈搅拌, 制成粒径2.0 mm的凝胶珠, 得到的凝胶珠在NH4OH溶液中稳定过夜.将凝胶珠从NH4OH溶液中分离出来, 用去离子水多次洗涤.在55℃下干燥至重量不再发生变化(约36 h), 得到烘干颗粒吸附剂(H-GA).
1.2.3 D-GA的制备将上述从NH4OH中分离出的凝胶珠多次清洗后放入真空冷冻干燥机中静置8 h.待经干燥的颗粒恢复室温后, 即可得到冻干颗粒吸附剂(D-GA).
1.3 吸附实验等温线吸附实验和pH影响实验均在250 mL锥形瓶中进行, 吸附动力学实验是在1 000 mL聚乙烯塑料瓶进行.在25℃, 等温吸附实验和动力学实验用0.1 mol ·L-1盐酸或氢氧化钠调整pH值稳定在6.5±0.1, 以150 r ·min-1的转速振荡.
1.3.1 等温吸附实验将颗粒吸附剂(1g ·L-1)加入100 mL As(Ⅴ) (0.02~50mg ·L-1)溶液中, 恒温振荡24 h, 实验结束后测定其残余As(Ⅴ)浓度.
1.3.2 吸附动力学实验称取0.7 g吸附剂置于700 mL初始为1mg ·L-1的As(Ⅴ)溶液, 恒温振荡0~50 h内设置时间间隔取样, 测定砷浓度.
1.3.3 pH影响实验称取0.1 g吸附剂加入100 mL浓度为1 mg ·L-1的As(Ⅴ)溶液, 用HCl和NaOH调节初始pH(1.0~13.0), 恒温振荡24 h, 测定砷浓度, 考察不同pH对As(Ⅴ)吸附效果的影响.
1.4 测砷方法As(Ⅴ)浓度采用原子分光光度计测定, 所有样品测定前都过0.45 μm滤膜过滤和加酸预处理.颗粒吸附剂对As(Ⅴ)的吸附量计算公式如下:
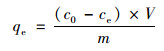
|
(1) |
式中, qe为吸附平衡时的吸附量(mg ·g-1), c0和ce分别为初始时和平衡时砷的浓度(mg ·L-1), V为反应溶液的体积(L), m为颗粒吸附剂的投加量(g).
1.5 表征方法采用扫描电镜(Hitachi S-4800, 日本)和能量色散光谱分析仪对颗粒吸附剂表面形貌进行表征.采用X射线衍射仪(BRUCKERD8, 德国)对颗粒吸附剂物相组成进行分析.采用物理吸附分析仪(ASAP 2460, 美国)进行氮气吸附/解吸等温线测定, BET法测定比表面积.
1.6 pHpzc的测定方法将0.05 g颗粒吸附剂加到100 mL的0.1 mol ·L-1的NaNO3溶液中, 初始pH在4.0~10.0之间, 振荡24 h, 测量溶液最终pH, 并绘制初始pH所对应的ΔpH的线形图.曲线与ΔpH为0的交叉点处的pH是颗粒吸附剂的pHpzc.
2 结果与讨论 2.1 颗粒吸附剂表面特性对比 2.1.1 表面宏观特征所制备的3种颗粒吸附剂及其原料铁锰泥如图 1所示.原始的反冲洗泥因含有铁而呈现出棕黄色, 其本身为粉末状. GA为红棕色颗粒, 粒径分布不均, 在1~2 mm之间, 焙烧之后机械强度增加. H-GA为颜色接近于原始铁锰泥的球型颗粒, 机械强度良好, 粒径为1.6~1.8 mm. D-GA与H-GA颜色类似, 但形状不规则, 较为扁平.如图 1所示, 3种颗粒相较于原始的铁锰泥, 均克服了粉末难以从处理后的水中分离的缺点, 但从颜色上相比, GA与原始铁锰泥相差较大, 可能是高温制备过程中铁氧化物物质结构发生变化, 导致宏观颜色的改变.

|
图 1 铁锰泥、GA、H-GA和D-GA的颗粒形态 Fig. 1 Granule morphology of iron and manganese sludge, GA, H-GA, and D-GA |
图 2显示了铁锰泥、GA、H-GA和D-GA的扫描电镜SEM照片.由图 2铁锰泥的SEM图可知, 铁锰泥结构比较松散, 周围有很多细小的碎片颗粒.上述由铁锰泥制备的3种颗粒表面均有凸起的大小颗粒, 使得表面粗糙不平.由图 2中GA的SEM所示, GA表面有众多大小不一的颗粒团聚, 由于颗粒团聚而形成了众多通道, 这些通道之间互相贯通相连, 增加了颗粒表面利用率, 有利于砷的去除, 而在H-GA和D-GA表面颗粒团聚较少, 但也可以发现存在孔径, 这是因为加入的壳聚糖作为粘结剂将粉末铁锰泥小颗粒粘结在一起, 在干燥过程中形成了大部分的孔隙, 这些孔隙使颗粒比表面积增大, 并且使砷离子很容易扩散到吸附剂内部.

|
图 2 铁锰泥、GA、H-GA和D-GA的扫描电镜照片 Fig. 2 SEM of iron and manganese sludge, GA, H-GA, and D-GA |
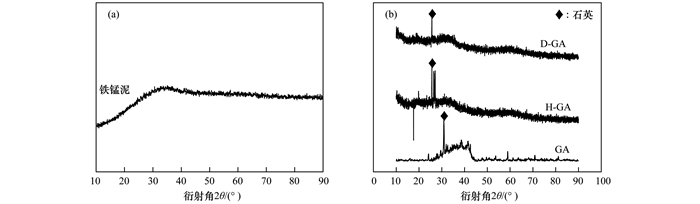
图 3为铁锰泥及3种新型颗粒吸附剂的XRD图谱.铁锰泥的XRD图谱没有明显的晶体衍射峰, 表明铁锰泥以非晶的无定型形式存在. 3种颗粒吸附剂则都存在尖锐的衍射峰是由于石英引起的, 在反冲洗过程中会不可避免地冲出滤料碎片, 而石英砂是滤池的滤料主要组成成分, 3种颗粒在制备过程中, 结晶程度增强, 图谱中出现了石英结晶体, 铁锰泥的图谱在该位置宽峰明显, 但结晶程度不高.除石英晶体外, H-GA和D-GA的XRD图谱未显示明显峰值, 说明二者均具有非晶质的特性.作为主要原料的铁锰泥主要成分是无定型结构的γ-FeOOH[6], H-GA和D-GA的XRD图谱与铁锰泥类似, 可推测其组成成分为γ-FeOOH. GA的XRD图谱在2θ为35°~45°的范围内出现了赤铁矿的峰值, 说明GA在制备过程中伴随着晶体的转换, 无定形的γ-FeOOH部分转换为具有晶型结构的赤铁矿.曾辉平等[7]的研究也表明, 高温条件下, 羟基铁通过脱羟基等一系列反应转化为赤铁矿, 但这种转变并不利于吸附, 有研究表明赤铁矿对As(Ⅴ)的吸附效果远不如γ-FeOOH[8].外界条件如温度、pH和湿度发生改变时, 不同形态结构的铁氧化物之间可能会发生转化[9].吴鹍[10]发现当温度较低(60℃)时, 铁氧化物主要由无定形铁组成, 而当温度高于300℃时, 铁氧化物则由无定形转变为具有晶型结构的赤铁矿.
|
图 3 铁锰泥、GA、H-GA和D-GA的XRD图谱 Fig. 3 XRD patterns of iron and manganese sludge, GA, H-GA, and D-GA |
比表面积是影响吸附材料性能的一个重要因素, 因为高比表面积为吸附过程提供了更多吸附位点, 吸附效率得到提高, 从而吸附容量增大.有研究表明制备方法、干燥方式等对天然的以及合成的铁锰氧化吸附剂比表面积会产生明显影响[11]. 表 1是铁锰泥及3种颗粒吸附剂的BET分析结果, 铁锰泥因其粉末形态和其非晶的无定型形式, 具有较高的比表面积. H-GA与D-GA的孔结构分析比较相似, 相较于GA, 比表面积明显升高, 这表明包埋法比高温焙烧法显著提高了吸附剂的比较面积, 这也暗示了H-GA与D-GA可能吸附效果优于GA.
|
|
表 1 铁锰泥、GA、H-GA和D-GA孔结构分析 Table 1 Analysis of pore structure for iron and manganese sludge, GA, H-GA, and D-GA |
2.1.5 表面电性分析
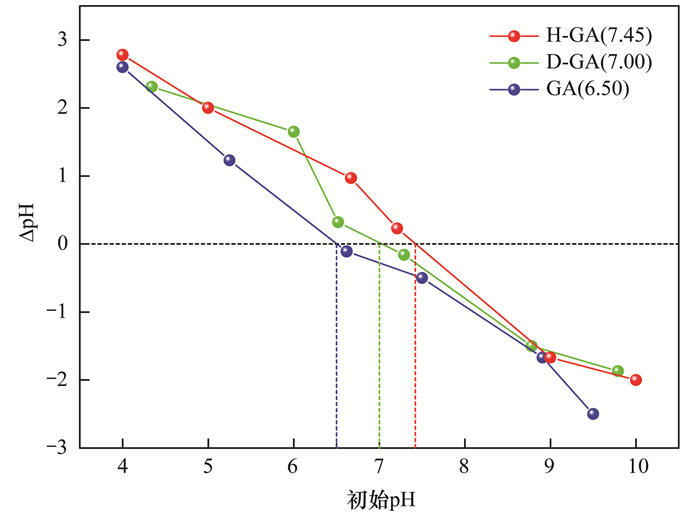
pHpzc是吸附剂的一个重要参数, 图 4显示了颗粒吸附剂在不同初始pH中充分反应后, 溶液pH的变化情况.其中可以确定H-GA、D-GA和GA吸附剂的pHpzc分别为7.45、7.00和6.50.
|
图 4 pHpzc测定曲线 Fig. 4 The pHpzc determination curve |
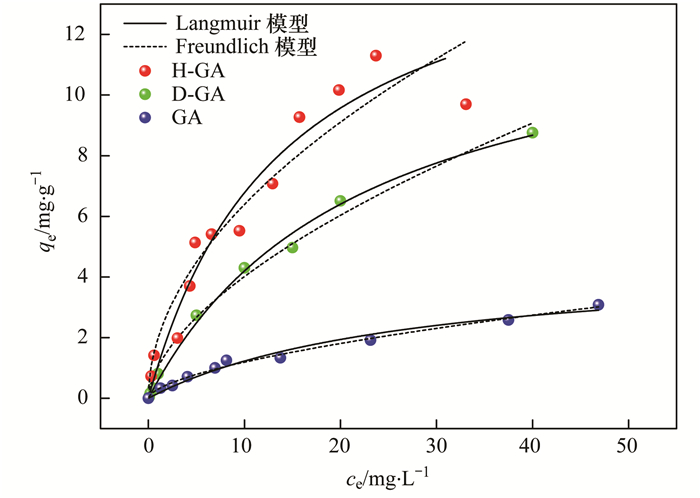
图 5为3种新型颗粒吸附剂对As(Ⅴ)的吸附等温线.总体来说, 三者的吸附等温线具有相似的特点, 吸附容量随平衡浓度升高而逐渐增加, 在低浓度时, 吸附容量增加较为迅速, 随着浓度逐渐升高, 吸附反应速度逐渐减缓直至趋于平衡.从图 5中可看出, 使用3种颗粒吸附剂分别对As(Ⅴ)进行去除时, 对于GA, 平衡浓度为23.12 mg ·L-1时所对应的砷吸附量为1.91 mg ·g-1; 对于H-GA, 平衡浓度为20 mg ·L-1, 砷吸附量为10.162 mg ·g-1; 对于D-GA, 当平衡浓度达到20 mg ·L-1时, 砷吸附量可以达到6.51 mg ·g-1.以上数据比较表明H-GA对砷的吸附能力最强, 其次是D-GA, 而GA吸附能力最弱.
|
图 5 GA、H-GA和D-GA去除As(Ⅴ)的吸附等温曲线 Fig. 5 Adsorption isotherms of As(Ⅴ) onto GA, H-GA, and D-GA |
为了确定3种颗粒吸附剂最适的等温线模型, 采用Langmuir和Freundlich模型对吸附等温线数据进行拟合. Langmuir模型[式(2)]适用于均匀表面的单层吸附.
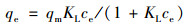
|
(2) |
式中, qm为吸附剂的最大吸附容量(mg ·g-1), qe为吸附平衡时吸附剂对砷的吸附容量(mg ·g-1), ce为吸附平衡时的溶液砷浓度(mg ·L-1), KL为与吸附能力相关的常数(L ·mg-1).
Frendlich模型[式(3)]主要用于描述吸附剂表面的非均质性的多分子层吸附:
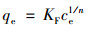
|
(3) |
式中, KF为吸附容量常数, 1/n为吸附强度常数.
本研究的吸附等温线数据拟合计算得到相关参数列于表 2中.其中的相关系数(R2)比较可得知, H-GA和D-GA的实验数据用Langmuir模型拟合更合适, GA的实验数据用Freundlich模型拟合更适合.根据Langmuir模型可计算得GA、H-GA和D-GA对As(Ⅴ)的最大吸附量理论值分别为5.05、14.95和13.45 mg ·g-1.此外, Freundlich模型的反应常数1/n小于1, 说明反应易发生, 若1/n大于2, 则说明反应难以发生. 表 2中3种颗粒吸附剂的1/n数据均小于1, 说明As(Ⅴ)在颗粒表面的吸附反应容易进行. Freundlich模型的KF值能够间接说明吸附剂的吸附能力, 从表 2中三者的比较来说, H-GA、D-GA和GA吸附能力逐次降低, 这与Langmuir模型推算出的最大吸附容量也是一致的. 3种新型颗粒吸附剂同文献中报道的其他种类颗粒吸附剂相比(表 3), 也均具有较高的吸附量, 表明铁锰泥制粒有较强的应用前景.
|
|
表 2 GA、H-GA和D-GA去除As(Ⅴ)的吸附等温线模型参数 Table 2 Parameters of Langmuir and Freundlich isotherms for the removal As(Ⅴ) by GA, H-GA, and D-GA |
|
|
表 3 本研究与已有报道的吸附剂除砷性能比较 Table 3 Comparison of adsorption capacity of adsorbents in this study and others reported in the literature |
2.2.2 吸附动力学
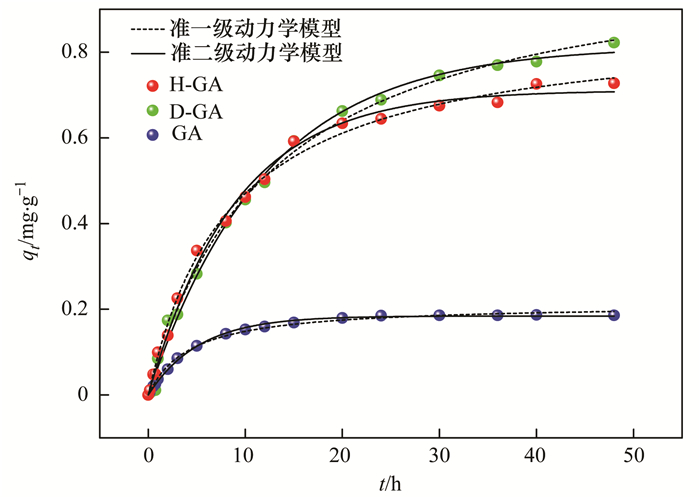
图 6显示了3种颗粒吸附剂对As(Ⅴ)的吸附动力学特征.从中可知, GA、H-GA和D-GA分别在10、20和20 h后达到吸附平衡.实验初始阶段, 颗粒吸附剂吸附量随时间显著增加, 这是因为前期吸附剂表面吸附位点数量远大于溶液中砷离子数量, 砷离子容易与吸附位点结合被吸附去除.随着吸附进一步进行, 吸附速率减缓直至达到平衡, 此时吸附位点也接近饱和.
|
图 6 GA、H-GA和D-GA去除As(Ⅴ)的吸附动力学模型曲线 Fig. 6 Kinetics of arsenic adsorption on the GA, H-GA, and D-GA |
为研究3种吸附材料在除砷过程中的动力学特征, 分别用准一级动力学、准二级动力学模型对动力学实验数据进行拟合.两种模型的数学形式分别为式(5)和式(6).
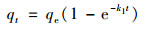
|
(5) |
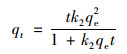
|
(6) |
式中, qe和qt分别为平衡状态下每单位质量吸附剂吸附的As(Ⅴ)量和时刻t吸附的As(Ⅴ)量(mg ·g-1); k1和k2分别为吸附过程的准一级速率常数(h-1)和准二级速率常数[g ·(mg ·h)-1)], t为吸附反应时间(h).
3种颗粒吸附剂对As(Ⅴ)的吸附动力学拟合参数见表 4.准一级动力学与准二级动力学模型的相关系数R2均大于0.99, 说明两种模型都适合描述颗粒吸附剂对砷的吸附过程.由于准一级动力学模型基于扩散速率为决定反应速度的控制步骤, 准二级动力学模型基于化学反应为决定反应速度的控制步骤, 因此, 可推测, 颗粒吸附剂表面砷吸附反应速度受化学吸附和扩散的双重影响.
|
|
表 4 GA、H-GA和D-GA去除As(Ⅴ)的吸附动力学参数 Table 4 Parameters of kinetic models for the removal As(Ⅴ) by GA, H-GA, and D-GA |
2.3 pH对颗粒吸附剂的影响
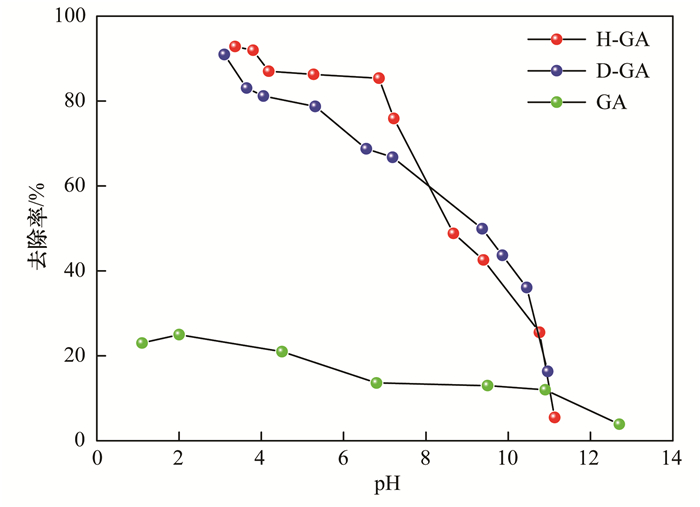
溶液的pH值是影响砷去除效率的关键因素, 因为溶液的pH值会影响官能团的离子化程度、金属离子的化学形态和一些化学反应等[18].溶液pH值对3种颗粒吸附剂除砷效率的影响如图 7所示. 3种颗粒吸附剂在不同pH溶液环境中, 呈现相同的趋势, 在酸性条件下, 砷去除率最高, H-GA和D-GA的砷去除率高达90%以上; 随着pH值的增加, 去除率逐渐降低直至吸附过程几乎不再进行. As(Ⅴ)在水环境中主要以H3AsO4和H2AsO4-的形式存在[19, 20].在酸性范围内, 颗粒吸附剂的表面带正电, 这增强了静电吸引力.在高碱性pH下, 吸附剂被去质子化并带负电, 这增强了吸附剂和砷离子之间的排斥力.因此, As(Ⅴ)吸附容量随pH的升高而降低.虽然酸性条件有利于砷的吸附, 但由壳聚糖作为黏合剂组成的H-GA和D-GA在pH小于3.5时会解体, GA虽吸附能力远远不如前两者, 但它在强酸条件下不会发生解体.含砷的地下水的正常pH值在6.0~7.5之间[21], 因此H-GA和D-GA完全可以满足实际工程应用的需要.
|
图 7 溶液pH对吸附剂除砷效率的影响 Fig. 7 Effect of pH on arsenic adsorption |
粉末状铁锰泥不易从水中分离, 增加了水处理成本, 本实验采用高温烘焙制粒的方法制备GA, 但与原始铁锰泥的除砷效果相差甚远, 杨宏等[6]的研究表明高温让铁锰泥内部的大部分结晶水被去除, 孔容和比表面积均有所下降, 物相结构也发生了变化.因此, 改变制粒条件, 选用温和的方式制粒是提高吸附剂吸附效果的最直接的方式.包埋法制粒条件温和, 使用液体黏合剂将微粒相连接形成复合结构, 黏合剂通常采用干燥冷却或颗粒基质与黏合剂发生反应而转化为稳定固相.本实验采用烘干和冻干的干燥稳定方式, H-GA是在较为低温条件(55℃)下采用壳聚糖包埋制粒, 避免了高温对原材料的影响, 吸附效果相比于GA有所提升, 但从吸附效果来看, 最大吸附容量仅达到了铁锰泥的二分之一, BET分析表明制粒后比表面积(110.30 mg ·g-1)相比于粉末形态(253.150 mg ·g-1)大大减少. D-GA是选用另一种干燥稳定的方式, 在冻干过程中将孔内水冻结并通过升华的方式去除, 但从实验数据来看, 两种颗粒吸附剂吸附效果相差不大.张艺钟[22]采用热烘干和真空冷冻干燥将粉末水合氧化铁进行制粒, 真空冷冻材料的饱和吸附容量为61.80 mg ·g-1, 仅比热烘干材料的吸附容量(56.39 mg ·g-1)高5 mg ·g-1左右.
壳聚糖虽然有诸多优点, 材料本身较密实[23~25], 作为黏合剂制粒时, H-GA和D-GA表面的孔隙不够丰富, 并且制粒过程中需要采用碱性溶液, 易造成污染.而海藻酸钠是从海带或海藻中提取的天然高分子物质, 可以和溶液中Ca2+产生凝胶, 制粒过程简便, 但其凝胶强度较低, 需要进一步加强吸附剂稳定性[26~28].因此下一步可以考虑制备基于铁锰泥的壳聚糖/海藻酸钠复合凝胶颗粒吸附剂.
3 结论(1) 采用高温焙烧和包埋两种方法将铁锰泥粉末制备为颗粒吸附剂, 其中包埋法制备的H-GA和D-GA吸附容量分别达到14.95 mg ·g-1和13.45 mg ·g-1, 大于高温烘焙制备的GA的吸附容量5.05 mg ·g-1.包埋法制备条件温和, 避免了高温改变铁氧化物物质结构, 提高了高温制粒的比表面积, 从而具备较高吸附容量.
(2) 包埋法选用烘干和冻干两种干燥方式制粒, 所制备的H-GA和D-GA, 从物化特征到吸附特性, 均无较大差别.
| [1] | 李昱秀, 张焕祯, 李海燕. 负载铁氧化物吸附剂水处理除砷研究进展[J]. 水处理技术, 2017, 43(7): 5-11. |
| [2] |
郭华明, 倪萍, 贾永锋, 等. 原生高砷地下水的类型、化学特征及成因[J]. 地学前缘, 2014, 21(4): 1-12. Guo H M, Ni P, Jia Y F, et al. Types, chemical characteristics and genesis of geogenic high-arsenic groundwater in the world[J]. Earth Science Frontiers, 2014, 21(4): 1-12. |
| [3] | Ociński D, Jacukowicz-Sobala I, Mazur P, et al. Water treatment residuals containing iron and manganese oxides for arsenic removal from water-Characterization of physicochemical properties and adsorption studies[J]. Chemical Engineering Journal, 2016, 294: 210-221. DOI:10.1016/j.cej.2016.02.111 |
| [4] |
赵运新, 曾辉平, 吕育锋, 等. 生物除铁除锰滤池反冲洗铁锰泥除As(Ⅴ)研究[J]. 中国给水排水, 2017, 33(11): 1-6. Zhao Y X, Zeng H P, Lyu Y F, et al. As(Ⅴ) Removal with iron and manganese oxide sludge from biological iron and manganese removal filter[J]. China Water & Wastewater, 2017, 33(11): 1-6. |
| [5] | Li X K, Chu Z R, Liu Y J, et al. Molecular characterization of microbial populations in full-scale biofilters treating iron, manganese and ammonia containing groundwater in Harbin, China[J]. Bioresource Technology, 2013, 147: 234-239. DOI:10.1016/j.biortech.2013.08.008 |
| [6] |
杨宏, 李冬, 张杰, 等. 生物固锰除锰机理与生物除铁除锰技术[J]. 中国给水排水, 2003, 19(6): 1-5. Yang H, Li D, Zhang J, et al. Mechanism of Biological Manganese Fixation and Removal and Biological Iron and Manganese Removal Technology from Ground Water[J]. China Water & Wastewater, 2003, 19(6): 1-5. DOI:10.3321/j.issn:1000-4602.2003.06.001 |
| [7] |
曾辉平, 赵运新, 吕育锋, 等. 水厂反冲洗铁锰泥热处理产物结构及除砷变化[J]. 中国环境科学, 2017, 37(8): 2986-2993. Zeng H P, Zhao Y X, Lü Y F, et al. Adsorption behaviors towards As and structural change of iron and manganese oxide sludge by thermal treatment[J]. China Environmental Science, 2017, 37(8): 2986-2993. DOI:10.3969/j.issn.1000-6923.2017.08.022 |
| [8] | Wang J, Zhang S J, Pan B C, et al. Hydrous ferric oxide-resin nanocomposites of tunable structure for arsenite removal:Effect of the host pore structure[J]. Journal of Hazardous Materials, 2011, 198: 241-246. DOI:10.1016/j.jhazmat.2011.10.036 |
| [9] | Sharma S K, Petrusevski B, Schippers J C. Characterisation of coated sand from iron removal plants[J]. Water Supply, 2002, 2(2): 247-257. DOI:10.2166/ws.2002.0070 |
| [10] | 吴鹍.吸附凝聚除砷的中试与工程应用研究[D].北京: 中国科学院研究生院, 2011. |
| [11] | Crosby S A, Glasson D R, Cuttler A H, et al. Surface areas and porosities of iron(Ⅲ)-and iron(Ⅱ)-derived oxyhydroxides[J]. Environmental Science & Technology, 1983, 17(12): 709-713. |
| [12] | Miller S M, Zimmerman J B. Novel, bio-based, photoactive arsenic sorbent:TiO2-impregnated chitosan bead[J]. Water Research, 2010, 44(19): 5722-5729. DOI:10.1016/j.watres.2010.05.045 |
| [13] | Yin H B, Kong M, Gu X H, et al. Removal of arsenic from water by porous charred granulated attapulgite-supported hydrated iron oxide in bath and column modes[J]. Journal of cleaner Production, 2017, 166: 88-97. DOI:10.1016/j.jclepro.2017.08.026 |
| [14] | Zhou Z, Liu Y G, Liu S B, et al. Sorption performance and mechanisms of arsenic(Ⅴ) removal by magnetic gelatin-modified biochar[J]. Chemical Engineering Journal, 2017, 314: 223-231. DOI:10.1016/j.cej.2016.12.113 |
| [15] | Wu K, Liu T, Lei C, et al. Evaluation of Al-based nanoparticle-impregnated sawdust as an adsorbent from byproduct for the removal of arsenic(Ⅴ) from aqueous solutions[J]. Environmental Progress & Sustainable Energy, 2017, 36(5): 1314-1322. |
| [16] | Gupta A, Chauhan V S, Sankararamakrishnan N. Preparation and evaluation of iron-chitosan composites for removal of As(Ⅲ) and As(Ⅴ) from arsenic contaminated real life groundwater[J]. Water Research, 2009, 43(15): 3862-3870. DOI:10.1016/j.watres.2009.05.040 |
| [17] |
吴昆明, 郭华明, 魏朝俊. 天然磁铁矿化学改性及其在水体除砷中的应用[J]. 岩矿测试, 2017, 36(1): 32-39. Wu K M, Guo H M, Wei C J. Chemical modification of natural magnetite and its application in arsenic removal from a water environment[J]. Rock and Mineral Analysis, 2017, 36(1): 32-39. |
| [18] | Lee C G, Alvarez P J J, Nam A, et al. Arsenic(Ⅴ) removal using an amine-doped acrylic ion exchange fiber:kinetic, equilibrium, and regeneration studies[J]. Journal of Hazardous Materials, 2017, 325: 223-229. DOI:10.1016/j.jhazmat.2016.12.003 |
| [19] | Ma M D, Wu H, Deng Z Y, et al. Arsenic removal from water by nanometer iron oxide coated single-wall carbon nanotubes[J]. Journal of Molecular Liquids, 2018, 259: 369-375. DOI:10.1016/j.molliq.2018.03.052 |
| [20] | Veličković Z, Vuković G D, Marinković A D, et al. Adsorption of arsenate on iron(Ⅲ) oxide coated ethylenediamine functionalized multiwall carbon nanotubes[J]. Chemical Engineering Journal, 2012, 181-182: 174-181. DOI:10.1016/j.cej.2011.11.052 |
| [21] |
李冬, 曾辉平, 张杰. 饮用水除铁除锰科学技术进展[J]. 给水排水, 2011, 37(6): 7-13. Li D, Zeng H P, Zhang J. Review of iron and manganese removal technology in drinking water[J]. Water & Wastewater Engineering, 2011, 37(6): 7-13. DOI:10.3969/j.issn.1002-8471.2011.06.002 |
| [22] | 张艺钟.壳聚糖负载水合氧化铁凝胶球的制备及其吸附As(Ⅲ)研究[D].西安: 长安大学, 2017. |
| [23] |
付军, 范芳, 李海宁, 等. 铁锰复合氧化物/壳聚糖珠:一种环境友好型除磷吸附剂[J]. 环境科学, 2016, 37(12): 4882-4890. Fu J, Fan F, Li H N, et al. Fe-Mn binary oxide impregnated chitosan bead (FMCB):an environmental friendly sorbent for phosphate removal[J]. Environmental Science, 2016, 37(12): 4882-4890. |
| [24] |
陶虎春, 李硕, 张丽娟, 等. 一种新型磁性壳聚糖/海藻酸钠复合凝胶球的制备与性能研究[J]. 北京大学学报(自然科学版), 2018, 54(4): 899-906. Tao H C, Li S, Zhang L J, et al. Preparation and optimization of a novel magnetic chitosan/sodium alginate composite gel bead[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2018, 54(4): 899-906. |
| [25] | Pandey S, Tiwari S. Facile approach to synthesize chitosan based composite:characterization and cadmium(Ⅱ) ion adsorption studies[J]. Carbohydrate Polymers, 2015, 134: 646-656. DOI:10.1016/j.carbpol.2015.08.027 |
| [26] |
吴洁, 丁师杰, 陈静, 等. 凹凸棒黏土对壳聚糖/海藻酸钠微球释放性能的影响[J]. 高校化学工程学报, 2014, 28(3): 648-653. Wu J, Ding S J, Chen J, et al. Effects of attapulgite on sustained release performance of chitosan/sodium alginate microspheres[J]. Journal of Chemical Engineering of Chinese Universities, 2014, 28(3): 648-653. DOI:10.3969/j.issn.1003-9015.2014.03.033 |
| [27] | Vijaya Y, Popuri S R, Boddu V M, et al. Modified chitosan and calcium alginate biopolymer sorbents for removal of nickel (Ⅱ) through adsorption[J]. Carbohydrate Polymers, 2008, 72(2): 261-271. DOI:10.1016/j.carbpol.2007.08.010 |
| [28] | Papageorgiou S K, Kouvelos E P, Katsaros F K. Calcium alginate beads from Laminaria digitata for the removal of Cu+2 and Cd+2 from dilute aqueous metal solutions[J]. Desalination, 2008, 224(1-3): 293-306. DOI:10.1016/j.desal.2007.06.011 |
 2019, Vol. 40
2019, Vol. 40

