2. 西安扬水源环境科技有限公司, 西安 710075
2. Xi'an Jumping Water Environment Technology Co., Ltd., Xi'an 710075, China
近年来, 微污染水源水中产生的嗅味问题[1]引起了人们的广泛关注.水中异味破坏了饮用水的感官性状, 常引起自来水用户怀疑与投诉, 已成为供水行业不可忽视的问题[2, 3].此外, 嗅味物质还可积累于水生生物体内影响水产品的品质[4], 损害了水产养殖业的经济利益.土霉味被认为是淡水水体中存在最广泛且最难闻的一种嗅味, 其中以2-甲基异莰醇(2-methylisoborneol, 2-MIB)与土臭素(geosmin, GSM)最常见, 为水体中典型嗅味.这种泥土味主要为蓝藻(水环境)和丝状放线菌(土壤环境)的代谢产物[5].水中典型嗅味严重超标时浓度可达约800 ng·L-1[6, 7], 而常规水处理工艺对这两种典型致嗅物质难以有效去除.因此研究一种高效经济的除嗅技术对保证饮用水质量和提升水产品品质具有重要的现实意义.
学者们相继提出了吸附技术[8]、化学氧化技术[9]、生物处理技术[10]、以及组合工艺[11]等手段去除水中2-MIB和GSM等典型嗅味.但活性炭等吸附剂回收困难不宜长期使用, 生物处理受限于去除周期长, 而二氧化氯、高锰酸盐等传统氧化剂去除率极低.高级氧化技术具有反应速率快, 简单可控等优点受到广泛关注, 其依赖于反应体系中产生的羟基自由基(·OH)和硫酸根自由基(·SO4-)等活性物质降解大分子有机污染物和痕量有害化学物质.近年来通过高级氧化技术去除嗅味污染的研究主要有光催化氧化(紫外/臭氧、紫外/氯、紫外/二氧化钛、紫外/过硫酸盐等)、电化学氧化、类芬顿氧化等技术[12~16].过硫酸盐可以通过热、碱、过渡金属、紫外等手段断裂过氧基(O—O)形成高活性硫酸根自由基, 利用硫酸根自由基的强氧化性降解有机物, 在有机废水处理和地下水原位修复等方面己成为高级氧化领域发展的热点[17, 18].这是由于过硫酸盐有良好的水溶性, 在室温下稳定存在且成本低, 其活化生成的硫酸根自由基具有极高的氧化还原电位(2.5~3.1 V)和较长的存在时间(3×10-5~4×10-5 s)[19], 在理想条件下能氧化分解绝大多数有机物.
超声技术在微污染原水、难降解高浓度有机废水以及饮用水灭菌消毒等方面已被广泛研究[20], 其具有反应速率快、设施简单等优点.超声在水中诱导空化气泡的形成和生长, 气泡破裂时造成局部点的高温(约5 000 K)、高压(约1×108 Pa), 同时此极端条件下水被热解产生·OH与·H, 为有机物降解提供了独特的物理化学环境.高频超声(850 kHz)已被研究在渔业养殖循环水中降解GSM和2-MIB有巨大的应用潜力[4], 但单独超声处理降解效果差、动力成本高等问题无法忽视.魏红等[21]的研究发现过硫酸钾单独处理对诺氟沙星的去除率为27.17%, 而超声活化后去除率高达88.64%. Wang等[22]的研究也发现超声辐射过硫酸盐降解卡马西平有显著的协同作用.但目前超声活化过硫酸盐高级氧化技术研究主要集中在有机废水处理方面, 在嗅味污染控制方面鲜见报道.
本文以固定超声频率为40 kHz的条件下, 研究了超声活化过硫酸盐高级氧化技术对典型致嗅物质2-MIB和GSM的氧化效果和影响因素, 初步探究了嗅味降解的机制, 以期超声/过硫酸盐联用工艺在异味突发时对饮用水保障和渔业养殖的实际应用提供参考.
1 材料与方法 1.1 实验材料 1.1.1 仪器与设备气相色谱质谱联用仪(7890A/7000B, 美国Agilent); 吹扫捕集浓缩仪(Stratum PTC, 美国Tekmar); 超纯水系统(pure-lab Option R7+Ultra Genetic, 英国ELGA); 超声波清洗仪(KQ500DE, 昆山超声仪器有限公司, 超声功率500 W, 频率40 kHz); 电动搅拌机(HD2004W, 上海司乐仪器有限公司); pH计(HQ30d, 美国HACH); 总有机碳分析仪(TOC-L, 日本岛津).
1.1.2 标准物质与试剂2-甲基异莰醇(2-methylisoborneol, 2-MIB) &土臭素(geosmin, GSM):Sigma-Aldrich公司, 混标100 μg·mL-1; 腐殖酸钠:Sigma-Aldrich公司, 溶于去离子水后经0.45 μm玻璃纤维膜过滤得到储备溶液; 过硫酸钾(优级纯), 甲醇(色谱纯), 叔丁醇、磷酸二氢钠、磷酸氢二钠(分析纯, 天津市科密欧化学试剂有限公司).
1.2 实验装置采用自制长方体有机玻璃反应器, 反应器置于超声清洗仪固定位置(图 1).本实验开始时同步开启电动搅拌桨, 确保实验过程中溶液混合均匀, 附加循环水浴以保证反应在室温下进行.
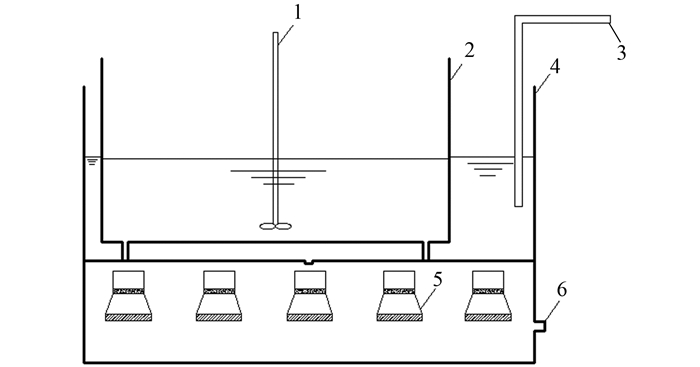
|
1.电动搅拌桨;2.反应器外壁;3.恒温循环水入口;4.超声仪外壁;5.超声换能器;6.恒温循环水出口 图 1 实验装置示意 Fig. 1 Schematic diagram of the experimental set-up |
反应前超声清洗仪提前开启预热15 min, 以保证反应过程中的超声稳定性.用去离子水配制一定浓度的致嗅物质混标溶液1 L, 根据不同的实验条件投加一定浓度物质后搅拌均匀.固定反应时间为15 min, 分别取反应0、2.5、5、7.5、10、15 min时水样20 mL测定致嗅物质浓度.
溶液的pH值均使用2mmol·L-1的磷酸盐缓冲溶液调节, 如无特殊说明反应体系pH值均维持在7.05±0.05.过硫酸钾浓度采用碘量法[23]测定; 超声波浴的声强用量热法[24]进行校准, 即假定进入反应器的所有声能都作为热量消散.
1.4 仪器设置条件典型致嗅物质的定量分析使用吹扫捕集-气相色谱质谱联用法进行测定.
吹扫捕集条件:六通阀温度50℃, 传输线温度115℃, 样品吹扫温度60℃; 吹扫时间11 min, 流量40 mL·min-1; 解吸温度250℃, 时间3 min; 烘烤温度280℃, 时间2 min, 流量200 mL·min-1.
色谱、质谱条件:色谱柱型号AglientHP-5MS; 进样口温度280℃; 进样采用分流模式, 分流比5:1;柱箱升温程序:50℃保持1 min, 以10℃·min-1升到200℃, 保持1 min, 以20℃·min-1升到220℃保持1 min. EI离子源温度为230℃, 四级杆温度150℃, 使用选择离子监测(SIM)模式测定, 2-MIB的监测离子为95和107, GSM的监测离子为112和125.
1.5 方法检出限和加标回收率将嗅味混标溶液稀释为5 ng·L-1, 重复测定6次, 得到2-MIB和GSM的方法检出限分别为1.63 ng·L-1和1.08 ng·L-1; 在加标浓度分别为100、200、400 ng·L-1的条件下平行实验6次, 得到2-MIB和GSM的平均加标回收率分别为91.4%~107.3%和90.8%~105.5%.
2 结果与讨论 2.1 单独PS、单独US和US/PS联用工艺比较考察了单独超声(US)、单独过硫酸盐(PS)、超声/过硫酸盐(PS/US)联用技术对2-MIB和GSM的去除效果.具体实验条件:典型嗅味混标初始浓度为400 ng·L-1, PS浓度2mmol·L-1, US声强为0.53W·cm-2, 结果如图 2所示.
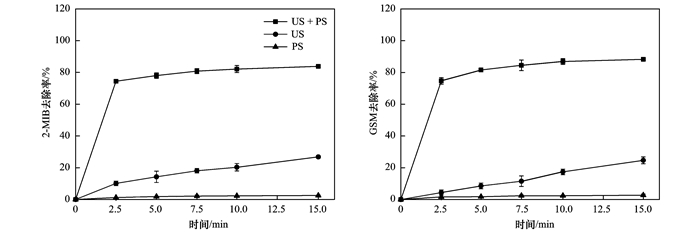
|
图 2 不同氧化条件下2-MIB和GSM的降解效果 Fig. 2 Efficiency of the removal of 2-MIB and GSM under different oxidation conditions |
单独PS处理对2-MIB与GSM几乎没有去除效果, 表明典型致嗅物质难以被过硫酸盐直接氧化; 单独US辐射处理对2-MIB和GSM的去除率分别为26.81%和24.65%, 该结果与Nam-Koong等[4]的研究低频超声(20 kHz)处理循环养殖水中典型嗅味所得的结论相类似.有学者通过羟基自由基清除剂实验表明, 单独超声(640 kHz)降解典型嗅味主要为超声诱导的热解作用而非自由基贡献[25].
同条件下, US/PS联用处理对2-MIB和GSM的去除率分别为83.80%和88.28%, 与单独超声处理相比, 去除率分别提高了57.0%和63.6%.整个反应体系中超声辐射会导致局部温度和压力骤升, 从而激活了过硫酸盐, 且在均相系统中引起强烈机械效应增强溶液中的传质作用, 加速PS分解和·SO4-生成, ·SO4-在一定条件下转化生成·OH, 如反应方程式(1)~(3)所示[26, 27].可以看出单一过硫酸盐体系和单一超声系统之间发生协同效应, 这可能是反应体系中生成了强氧化性的自由基(·SO4-、·OH)使嗅味快速降解.
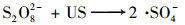
|
(1) |
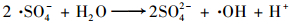
|
(2) |

|
(3) |
已知甲醇(MeOH)和叔丁醇(TBA)都是典型的自由基清除剂, 但甲醇和叔丁醇与·OH和·SO4-反应速率不同, 如反应方程式(4)~(7)所示[13].
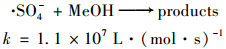
|
(4) |
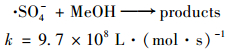
|
(5) |
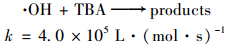
|
(6) |
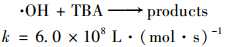
|
(7) |
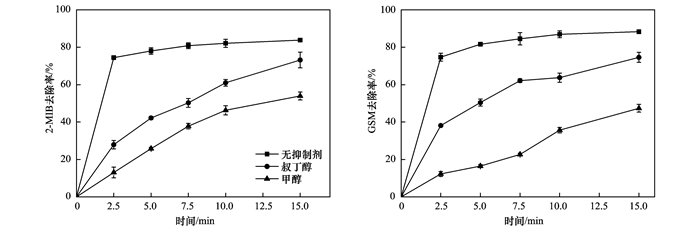
因此反应体系中分别加入甲醇和叔丁醇可探究US/PS联用工艺两种自由基对2-MIB与GSM的降解机制.在典型嗅味混标浓度400 ng·L-1, PS浓度2mmol·L-1, 超声声强0.53W·cm-2, pH为7.05条件下, 研究分别加入甲醇(2mmol·L-1)和叔丁醇(2mmol·L-1)时, 降解嗅味的效果如图 3所示.
|
图 3 超声/过硫酸盐体系下不同自由基清除剂对2-MIB和GSM的降解影响 Fig. 3 Effect of different free radical scavengers on the degradation of 2-MIB and GSM using the US/PS system |
当叔丁醇加入反应体系中, 竞争消耗·OH使2-MIB与GSM降解受到抑制, 去除率从83.80%和88.82%降为73.17%和74.56%;当甲醇加入后抑制效果更为明显, 因为甲醇同时捕捉体系中的·OH和·SO4-, 嗅味降解速率减慢, 使去除率降为53.95%和47.36%.但对比单独US处理, US/PS体系中加入叔丁醇和甲醇后2-MIB与GSM去除率仍保持较高水平, 可能是自由基清除剂量不足以将·OH和·SO4-完全淬灭.马京帅等[28]研究热激活过硫酸盐降解普萘洛尔时也发现乙醇和叔丁醇在低浓度(60mmol·L-1)条件下对体系中自由基抑制效果不明显.以上结果分析可得US/PS体系中典型嗅味的降解为·OH和·SO4-共同作用. GSM比2-MIB降解抑制效果更明显, 即GSM更容易被自由基破坏降解, 其与自由基有较高的反应速率, 这是由于2-MIB化学结构比GSM稳定[12].
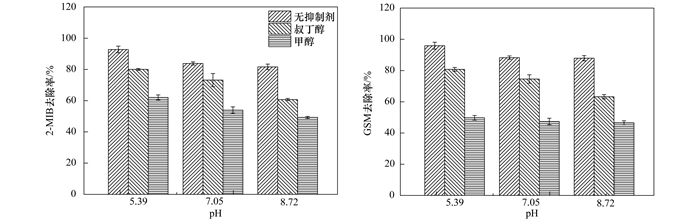
相同实验条件下改变反应体系中pH值分别为5.39、7.05、8.72, 研究不同pH条件下致嗅物质的降解效果以及甲醇(2mmol·L-1)和叔丁醇(2mmol·L-1)加入后对嗅味去除的的影响, 结果如图 4所示.
|
图 4 不同pH条件下超声/过硫酸盐体系中存在不同的自由基清除剂 Fig. 4 Different free radical scavengers in ultrasonic/persulfate systems at different pH conditions |
自由基清除剂未加入时, 酸性条件下比碱性条件下2-MIB和GSM的去除率分别高11.13%和8.01%.当甲醇存在时, 在pH为5.39、7.05和8.72的条件下2-MIB去除率分别为62.08%, 53.95%和49.30%, 同条件下叔丁醇存在时2-MIB去除率分别为80.01%, 73.17%和60.76%. GSM的降解也得到类似结果.不同pH条件下, 两种自由基清除剂加入体系中嗅味分解均被明显抑制, 且甲醇抑制作用始终高于叔丁醇, 这与Xie等[13]的研究紫外活化过硫酸盐降解典型致嗅物质结果相一致.叔丁醇在pH为8.72条件下抑制嗅味降解更为明显, 这表明US/PS体系中羟基自由基在碱性条件下为主要活性物质, 而硫酸根自由基主要存在于酸性和中性条件下.
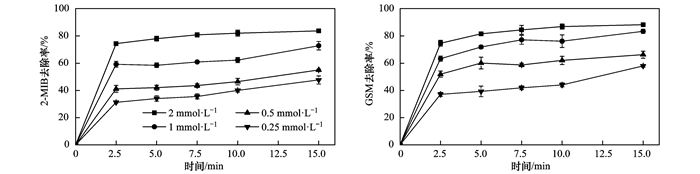
2.3 影响US/PS降解嗅味物质的因素 2.3.1 过硫酸盐浓度的影响作为活性自由基源的过硫酸盐浓度是评价氧化过程效率的重要因素.在控制反应体系2-MIB和GSM浓度为400 ng·L-1, 超声声强为0.53W·cm-2条件下, 分别考察了初始PS浓度为0.25、0.5、1、2mmol·L-1时致嗅物质的降解效果, 结果如图 5所示.
|
图 5 不同过硫酸盐浓度下2-MIB和GSM的去除效果 Fig. 5 Efficiency of the removal of 2-MIB and GSM under different persulfate concentrations |
结果显示, 随着过硫酸盐剂量从0.25mmol·L-1增加到2mmol·L-1, 2-MIB和GSM去除率分别从47.69%和58.02%增加到83.80%和88.28%.这表明较高的过硫酸盐浓度被超声激活产生了更多的·SO4-加快了嗅味降解, 与Chen等[29]研究超声活化过硫酸盐去除废水中二硝基甲苯得到的结论相一致.但过硫酸盐投加量过大会导致水体中硫酸根离子增多, 在实际应用中应在保证出水水质嗅味达标的前提下, 选择合理的过硫酸盐投加量.
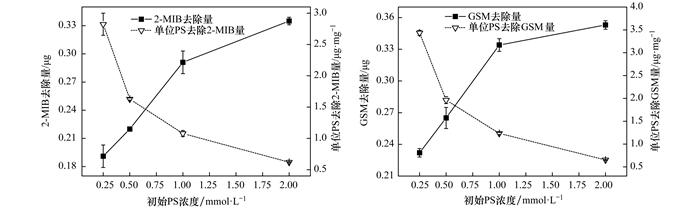
图 6显示了初始过硫酸盐浓度变化对嗅味总去除量和单位质量过硫酸盐降解典型嗅味的影响.随着初始PS浓度的增加, 2-MIB和GSM总去除量增加.初始PS浓度为0.25mmol·L-1时, 每单位PS的2-MIB和GSM平均去除质量为2.82 μg·mg-1和3.43 μg·mg-1, 而当PS浓度为2mmol·L-1时, 平均去除质量为0.62 μg·mg-1和0.65 μg·mg-1.随着PS初始浓度增加, US/PS体系中·SO4-产率降低.这可能由于硫酸根自由基发生重组、两种自由基与过量PS反应被消耗, 如反应方程式(8)~(10)所示[30].
|
图 6 初始过硫酸盐浓度对GSM和2-MIB去除量的影响以及单位过硫酸盐的去除量 Fig. 6 Effect of the initial persulfate concentration on the quantity of GSM and 2-MIB removed and the quantity removed per unit persulfate |
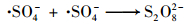
|
(8) |

|
(9) |

|
(10) |
在控制典型嗅味混标初始浓度为400 ng·L-1, PS浓度2mmol·L-1, 分别考察超声输入功率为500、400、300、200 W条件下2-MIB和GSM的降解效果, 量热法校正后对应的声强分别为0.53、0.47、0.36、0.33W·cm-2, 结果如图 7所示.随着声强增大, 2-MIB和GSM的去除率分别由69.92%和72.37%增加到83.80%和88.28%, 说明增大超声声强可以促进致嗅物质的降解.声音强度由振动幅度的大小决定, 有研究表明较高超声振幅更容易激活PS产生较多的自由基[31], 同时在均相体系中引起更为剧烈的机械作用可以增强溶液中的传质效果来促进嗅味降解.
|
图 7 超声波功率对2-MIB和GSM去除效果的影响 Fig. 7 Effect of ultrasonic power input on the removal efficiency of 2-MIB and GSM |
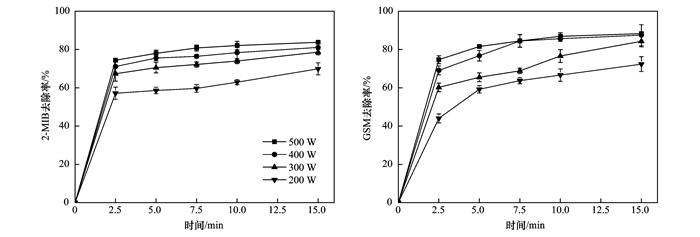
在湖库水源水及水产养殖中, 典型致嗅物质受水华等影响不同季节浓度变化较大.在体系中PS浓度2mmol·L-1, 超声声强为0.53W·cm-2, 考察了US/PS联用工艺分别对典型嗅味混标初始浓度为100、200、400、600、800 ng·L-1条件下的去除效果, 结果如图 8所示.在100~800 ng·L-1范围内US/PS高级氧化技术均有良好的降解效果, 初始嗅味在低浓度时有更高的去除率.初始嗅味浓度为100 ng·L-1时2-MIB和GSM去除率可达88.73%和93.32%, 而800 ng·L-1时去除率为76.69%和84.64%.而这可能是因为低浓度条件下自由基生成率高于2-MIB与GSM降解的消耗率, 导致更高的去除率.而高浓度嗅味初始嗅味浓度去除率较低, 可能是由于反应位点的数量有限和反应体系中自由基的有限可用性.
|
图 8 不同嗅味初始浓度下2-MIB与GSM的降解效果 Fig. 8 Degradation of 2-MIB and GSM at different initial concentrations of the odors |
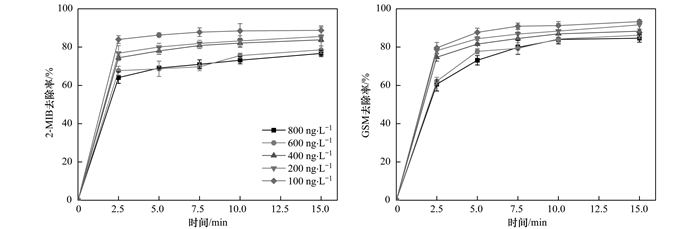
天然有机物在原水中广泛存在, 主要为腐殖酸, 其存在对水处理效能有一定影响[32].在控制2-MIB和GSM混标溶液初始浓度为400 ng·L-1, PS浓度2mmol·L-1, 超声声强为0.53 W·cm-2条件下, 分别研究反应体系中投加1、2、4和8 mg·L-1的腐殖酸(相应TOC值分别为0.60、0.89、1.48和2.39 mg·L-1)时对典型致嗅物质去除效果的影响, 如图 9所示.随着腐殖酸浓度的增加, 2-MIB和GSM的去除率减小, 当腐殖酸浓度为8 mg·L-1时, 2-MIB和GSM的去除率下降11.18%和10.91%.这是由于腐殖酸的存在会竞争消耗自由基, 抑制了嗅味降解.对比孙昕等[33]研究真空紫外激活过硫酸盐去除水中典型嗅味, US/PS体系受水体中的天然有机物影响较小, 这是因为腐殖酸色度显著影响紫外的穿透性从而削弱了过硫酸盐激活效果, 而超声几乎不受色度影响, 激活过硫酸盐效果好.此外, 有学者研究表明循环养殖水中有机与无机负荷存在对超声降解典型致嗅物质影响极小[4].
|
图 9 不同腐殖酸浓度条件下2-MIB和GSM的去除效果 Fig. 9 Removal efficiency of 2-MIB and GSM in the presence of different humic acid concentrations |
(1) 单独过硫酸盐处理基本不能去除水中典型致嗅物质, 单独超声(40 kHz)处理去除效果较差, 但采用US/PS高级氧化技术在短时间对典型嗅味有较理想的去除效果.
(2) US/PS联用工艺处理低浓度(100 ng·L-1)典型致嗅物质有更高的去除率, 且体系中增加过硫酸盐投加量和超声波声强可提高反应速率, 此外原水中的腐殖酸会抑制典型致嗅物质降解但影响效果较小.在实际工艺运行中可通过调整适宜条件使嗅味降解效果达到最优.
(3) 超声活化过硫酸盐高级氧化技术中, 对致嗅物质的去除主要为硫酸根自由基和羟基自由基共同作用的结果, 其中硫酸根自由基在酸性和中性条件下降解典型嗅味起主导作用.
| [1] | Su M, Yu J W, Zhang J Z, et al. MIB-producing cyanobacteria (Planktothrix sp.) in a drinking water reservoir:distribution and odor producing potential[J]. Water Research, 2015, 68: 444-453. DOI:10.1016/j.watres.2014.09.038 |
| [2] |
张旭东, 张学博, 刘畅, 等. 天津滨海新区自来水嗅味事件成因分析及应急处理[J]. 中国给水排水, 2017, 33(13): 46-49. Zhang X D, Zhang X B, Liu C, et al. Cause for odor problem and its emergent treatment in Tianjin Binhai New Area[J]. China Water & Wastewater, 2017, 33(13): 46-49. |
| [3] | Dietrich A M, Phetxumphou K, Gallagher D L. Systematic tracking, visualizing, and interpreting of consumer feedback for drinking water quality[J]. Water Research, 2014, 66: 63-74. DOI:10.1016/j.watres.2014.08.007 |
| [4] | Nam-Koong H, Schroeder J P, Petrick G, et al. Removal of the off-flavor compounds geosmin and 2-methylisoborneol from recirculating aquaculture system water by ultrasonically induced cavitation[J]. Aquacultural Engineering, 2016, 70: 73-80. DOI:10.1016/j.aquaeng.2015.10.005 |
| [5] | Lee J, Rai P K, Jeon Y J, et al. The role of algae and cyanobacteria in the production and release of odorants in water[J]. Environmental Pollution, 2017, 227: 252-262. DOI:10.1016/j.envpol.2017.04.058 |
| [6] | Qi M, Chen J, Sun X X, et al. Development of models for predicting the predominant taste and odor compounds in Taihu Lake, China[J]. PLoS One, 2012, 7(12): e51976. DOI:10.1371/journal.pone.0051976 |
| [7] |
焦洁, 陆纳新, 王海湧, 等. 太湖原水藻类代谢产物中嗅味物质的去除技术研究[J]. 中国给水排水, 2016, 32(11): 64-67. Jiao J, Lu N X, Wang H Y, et al. Removal of odorous substances from algae metabolites in raw water of Taihu Lake[J]. China Water & Wastewater, 2016, 32(11): 64-67. |
| [8] | Yu J W, Yang F C, Hung W N, et al. Prediction of powdered activated carbon doses for 2-MIB removal in drinking water treatment using a simplified HSDM approach[J]. Chemosphere, 2016, 156: 374-382. DOI:10.1016/j.chemosphere.2016.05.010 |
| [9] |
翁皓琳, 肖冠芳, 葛孝新, 等. 高密孚日水厂化学预氧化法去除嗅味物质研究[J]. 环境科学与技术, 2016, 39(S1): 247-250, 289. Weng H L, Xiao G F, Ge X X, et al. Removal effect of taste and odor for chemical preoxidation of sunvim water plant in Gaomi[J]. Environmental Science & Technology, 2016, 39(S1): 247-250, 289. |
| [10] | Azaria S, Nir S, Van Rijn J. Combined adsorption and degradation of the off-flavor compound 2-methylisoborneol in sludge derived from a recirculating aquaculture system[J]. Chemosphere, 2017, 169: 69-77. DOI:10.1016/j.chemosphere.2016.11.051 |
| [11] | Kim C, Lee S Ⅱ, Hwang S, et al. Removal of geosmin and 2-methylisoboneol (2-MIB) by membrane system combined with powdered activated carbon (PAC) for drinking water treatment[J]. Journal of Water Process Engineering, 2014, 4: 91-98. DOI:10.1016/j.jwpe.2014.09.006 |
| [12] | Antonopoulou M, Evgenidou E, Lambropoulou D, et al. A review on advanced oxidation processes for the removal of taste and odor compounds from aqueous media[J]. Water Research, 2014, 53: 215-234. DOI:10.1016/j.watres.2014.01.028 |
| [13] | Xie P C, Ma J, Liu W, et al. Removal of 2-MIB and geosmin using UV/persulfate:contributions of hydroxyl and sulfate radicals[J]. Water Research, 2015, 69: 223-233. DOI:10.1016/j.watres.2014.11.029 |
| [14] | Yaparatne S, Tripp C P, Amirbahman A. Photodegradation of taste and odor compounds in water in the presence of immobilized TiO2-SiO2 photocatalysts[J]. Journal of Hazardous Materials, 2018, 346: 208-217. DOI:10.1016/j.jhazmat.2017.12.029 |
| [15] | Bu L J, Zhou S Q, Shi Z, et al. Removal of 2-MIB and geosmin by electrogenerated persulfate:performance, mechanism and pathways[J]. Chemosphere, 2017, 168: 1309-1316. DOI:10.1016/j.chemosphere.2016.11.134 |
| [16] | Park J A, Nam H L, Choi J W, et al. Oxidation of geosmin and 2-methylisoborneol by the photo-Fenton process:kinetics, degradation intermediates, and the removal of microcystin-LR and trihalomethane from Nak-Dong River water, South Korea[J]. Chemical Engineering Journal, 2017, 313: 345-354. DOI:10.1016/j.cej.2016.12.086 |
| [17] | Wacławek S, Lutze H V, Grübel K, et al. Chemistry of persulfates in water and wastewater treatment:a review[J]. Chemical Engineering Journal, 2017, 330: 44-62. DOI:10.1016/j.cej.2017.07.132 |
| [18] | Matzek L W, Carter K E. Activated persulfate for organic chemical degradation:a review[J]. Chemosphere, 2016, 151: 178-188. DOI:10.1016/j.chemosphere.2016.02.055 |
| [19] | Ghanbari F, Moradi M, Gohari F. Degradation of 2, 4, 6-trichlorophenol in aqueous solutions using peroxymonosulfate/activated carbon/UV process via sulfate and hydroxyl radicals[J]. Journal of Water Process Engineering, 2016, 9: 22-28. DOI:10.1016/j.jwpe.2015.11.011 |
| [20] |
蒋昊琳, 刘立新, 杨明全, 等. 超声波在水处理中的应用与研究现状[J]. 化工进展, 2017, 36(S1): 464-468. Jiang H L, Liu L X, Yang M Q, et al. Application and research status of ultrasound in water treatment[J]. Chemical Industry and Engineering Progress, 2017, 36(S1): 464-468. |
| [21] |
魏红, 史京转, 李佳霖, 等. 超声、过硫酸钾协同去除水中诺氟沙星的效果[J]. 环境科学, 2015, 36(11): 4121-4126. Wei H, Shi J Z, Li J L, et al. Norfloxacin solution degradation under ultrasound, potassium persulfate collaborative system[J]. Environmental Science, 2015, 36(11): 4121-4126. |
| [22] | Wang S L, Zhou N. Removal of carbamazepine from aqueous solution using sono-activated persulfate process[J]. Ultrasonics Sonochemistry, 2016, 29: 156-162. DOI:10.1016/j.ultsonch.2015.09.008 |
| [23] | Liang C J, Huang C F, Mohanty N, et al. A rapid spectrophotometric determination of persulfate anion in ISCO[J]. Chemosphere, 2008, 73(9): 1540-1543. DOI:10.1016/j.chemosphere.2008.08.043 |
| [24] | Chakma S, Moholkar V S. Investigations in synergism of hybrid advanced oxidation processes with combinations of sonolysis+Fenton process+UV for degradation of bisphenol A[J]. Industrial & Engineering Chemistry Research, 2014, 53(16): 6855-6865. |
| [25] | Song W H, O'Shea K E. Ultrasonically induced degradation of 2-methylisoborneol and geosmin[J]. Water Research, 2007, 41(12): 2672-2678. DOI:10.1016/j.watres.2007.02.041 |
| [26] | Darsinou B, Frontistis Z, Antonopoulou M, et al. Sono-activated persulfate oxidation of bisphenol A:kinetics, pathways and the controversial role of temperature[J]. Chemical Engineering Journal, 2015, 280: 623-633. DOI:10.1016/j.cej.2015.06.061 |
| [27] | Ji Y F, Dong C X, Kong D Y, et al. Heat-activated persulfate oxidation of atrazine:Implications for remediation of groundwater contaminated by herbicides[J]. Chemical Engineering Journal, 2015, 263: 45-54. DOI:10.1016/j.cej.2014.10.097 |
| [28] |
马京帅, 吕文英, 刘国光, 等. 热活化过硫酸盐降解水中的普萘洛尔[J]. 环境化学, 2017, 36(2): 221-228. Ma J S, Lyu W Y, Liu G G, et al. Degradation of propranolol in aqueous solution by heat-activated persulfate[J]. Environmental Chemistry, 2017, 36(2): 221-228. |
| [29] | Chen W S, Su Y C. Removal of dinitrotoluenes in wastewater by sono-activated persulfate[J]. Ultrasonics Sonochemistry, 2012, 19(4): 921-927. DOI:10.1016/j.ultsonch.2011.12.012 |
| [30] | Monteagudo J M, El-Taliawy H, Durán A, et al. Sono-activated persulfate oxidation of diclofenac:degradation, kinetics, pathway and contribution of the different radicals involved[J]. Journal of Hazardous Materials, 2018, 357: 457-465. DOI:10.1016/j.jhazmat.2018.06.031 |
| [31] | Peng L P, Wang L, Hu X T, et al. Ultrasound assisted, thermally activated persulfate oxidation of coal tar DNAPLs[J]. Journal of Hazardous Materials, 2016, 318: 497-506. DOI:10.1016/j.jhazmat.2016.07.014 |
| [32] | Sillanpää M, Ncibi M C, Matilainen A. Advanced oxidation processes for the removal of natural organic matter from drinking water sources:a comprehensive review[J]. Journal of Environmental Management, 2018, 208: 56-76. |
| [33] |
孙昕, 史路肖, 张燚, 等. 真空紫外/过二硫酸盐去除饮用水中嗅味物质[J]. 环境科学, 2018, 39(5): 2195-2201. Sun X, Shi L X, Zhang Y, et al. Removal of odorants in drinking water using VUV/persulfate[J]. Environmental Science, 2018, 39(5): 2195-2201. |
 2019, Vol. 40
2019, Vol. 40

