2. 浙江工业大学环境学院, 杭州 310032;
3. 山东建筑大学市政与环境工程学院, 济南 250101
2. College of Environment, Zhejiang University of Technology, Hangzhou 310032, China;
3. College of Municipal and Environmental Engineering, Shandong Jianzhu University, Ji'nan 250101, China
水体富营养化现已成为当今世界所面临的重大水环境问题, 而磷浓度过高则是引起水体富营养化的主要因素[1~3].水体中磷的来源分为外源输入和内源释放[4].当外源输入得到有效控制之后, 研发内源磷释放控制技术已经成为近年来备受关注的研究课题[5].最近, 许多方法被开发用于底泥内源磷释放的控制, 包括底泥疏浚[6]、铝盐钝化法[7]、曝气供氧[8]、水生植物修复[9]、硝酸盐原位处理[10]以及固态活性材料原位覆盖/改良[11~13]等.其中, 固态活性材料原位覆盖/改良, 受到国内外研究人员的广泛关注.目前, 已经受到国内外学者关注的固态活性材料有镧改性膨润土[11~13]、富含钙黏土矿物[14]、给水处理厂铁铝泥[15]、水化硅酸钙[16]、铝改性沸石[17]、镧改性沸石[18]以及锆基钝化剂[19~22]等.其中, 锆基钝化剂是将锆负载到价格低廉的天然矿物上制备得到的固态材料, 因其具有安全、高效且经济的特点而受到国内外学者的较多关注[19~22].
膨润土是一种以蒙脱石为主要矿物成分的层状黏土矿物, 具有阳离子交换容量高、比表面积大、来源广泛和价格低廉等特点, 适合作为锆的载体[23].文献[21]已经报道了锆改性膨润土适合作为一种底泥改良剂控制河道内源磷的释放.但是, 锆改性膨润土投加到底泥中后很难回收, 这就会增加成本, 也不符合可持续发展的理念, 并且吸附磷后的锆改性膨润土仍然位于底泥中, 当外界环境发生改变时这部分磷可能会发生再次释放, 这就降低了它的控磷效率.而如果将锆改性膨润土进一步改性为磁性锆铁改性膨润土, 就能很好地解决这一问题, 因为磁性材料不仅具有良好的吸附磷的能力, 而且还可以通过磁分离的方式被回收进行再次利用[24].
揭示磁性锆铁改性膨润土对水中磷酸盐的吸附特征与机制, 对于确定磁性锆铁改性膨润土活性覆盖/改良技术控制底泥磷释放的效果, 是非常重要的.先前的研究发现, 膨润土中可交换钙离子含量对锆改性膨润土吸附水中磷酸盐起到重要的作用, 可交换钙离子含量越高, 锆改性膨润土对水中磷酸盐的吸附能力越强[25].由此可以推测, 如果膨润土中可交换钙离子含量越高, 磁性锆铁改性膨润土对水中磷酸盐的吸附能力预计越强.阳离子交换反应是增加膨润土中可交换钙离子量的常见方法[25].如果采用钙离子对膨润土进行预处理, 所获得的磁性锆铁改性钙预处理膨润土(ZrFeCaBT)对水中磷酸盐的吸附能力预计强于磁性锆铁改性原始膨润土(ZrFeRBT), 即钙预处理预计提高了磁性锆铁改性膨润土对水中磷酸盐的吸附能力.揭示钙预处理对磁性锆铁改性膨润土吸附水中磷酸盐的影响, 有助于弄清膨润土中可交换钙离子对磁性锆铁改性膨润土吸附水中磷酸盐所起的作用, 进而有助于阐明磁性锆铁改性膨润土对水中磷酸盐的吸附特征与机制.但是, 目前国内外关于钙预处理对磁性锆铁改性膨润土吸附水中磷酸盐的影响, 还鲜见报道.
为此, 本研究首先制备2种不同类型的磁性锆铁改性膨润土, 即ZrFeRBT和ZrFeCaBT, 再通过批量实验对比考察ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附等温线和吸附动力学, 然后考察溶液pH值、共存阳离子、共存阴离子和反应温度对吸附的影响, 最终揭示钙预处理对磁性锆铁改性膨润土吸附水中磷酸盐的影响, 以期为应用磁性锆铁改性膨润土控制底泥磷释放提供科学依据.
1 材料与方法 1.1 实验材料本实验所用的CaCl2、FeCl3·6H2O、FeSO4·7H2O、NaOH、ZrOCl2·8H2O、HCl、KH2PO4、NaNO3、NaHCO3、Na2SO4、NaCl、KCl和MgCl2等化学药剂采购于中国国药集团化学试剂有限公司, 均为分析纯.实验所用的原始膨润土购于上海试四赫维化工有限公司.实验所用的水均为去离子水.采用KH2PO4和去离子水配制磷酸盐储备液, 再通过稀释的方式获得磷酸盐使用液.磷酸盐使用液的浓度均以元素磷计.
1.2 材料制备和表征ZrFeCaBT的制备步骤为:将10 g膨润土和100 mL的1 mol·L-1 CaCl2溶液倒入锥形瓶中, 将此锥形瓶放入温度为25℃、转速为150 r·min-1的振荡器中振荡24 h后离心分离, 即可得到钙预处理过的膨润土, 再用100 mL的去离子水将钙预处理过的膨润土转移至1 L的锥形瓶中; 称取5.99 g的FeSO4·7H2O和11.6 g的FeCl3·6H2O分别溶于100 mL的去离子水中, 再将它们与钙预处理的膨润土进行混合; 将锥形瓶置于可控温磁力搅拌器上, 当反应液温度达到70℃后, 缓慢滴加1 mol·L-1的NaOH溶液, 直至反应液pH值达到10, 再稳定1 h; 之后, 等锥形瓶中的混合液冷却后, 加入100 mL的50 g·L-1八水氧氯化锆(ZrOCl2·8H2O)溶液; 随后, 继续缓慢滴加1 mol·L-1的NaOH溶液, 直至反应液pH值达到10;然后采取磁分离的方式用去离子水将锥形瓶中的固体材料清洗5遍, 再将获得的固体材料置于35℃烘箱中烘干, 并研磨成粉末状, 装入自封袋中备用. ZrFeRBT的制备步骤, 除了没有采用钙离子对原始膨润土进行预处理外, 其余步骤都与ZrFeCaBT的制备步骤相同.
采用的X射线衍射仪(XRD, D8 ADVANCE, 布鲁克公司, 德国)对ZrFeRBT和ZrFeCaBT的相结构进行分析.采用X射线荧光光谱仪(XRF, XRF-1800, 岛津公司, 日本)对ZrFeRBT和ZrFeCaBT的化学成分进行测定.
1.3 批量吸附实验采用批量吸附实验探究了ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附等温线和吸附动力学, 接着探究溶液pH值、共存阳离子、共存阴离子和反应温度对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响.具体的吸附实验步骤为: ①首先配置一定质量浓度的磷酸盐溶液, 其中吸附等温线实验中, 磷初始质量浓度分别为2、4、6、8、10、15、20、25、30、35和40 mg·L-1, 其它实验的磷初始质量浓度均为20 mg·L-1, 在共存阴阳离子影响实验中, 磷酸盐溶液中所加入的共存电解质(NaCl、KCl、MgCl2、CaCl2、NaHCO3、Na2SO4或NaNO3)浓度分别为0、2、6和10 mmol·L-1, 其它实验则不需要加入共存电解质; ②采用0.1 mol·L-1 NaOH和HCl来调节磷酸盐溶液的pH值, 其中溶液pH值影响实验中, 磷酸盐溶液的pH值分别为4、5、6、7、8、9、10和11, 其它实验的磷酸盐溶液的pH值均为7; ③再称取一定质量的吸附剂材料与25 mL磷酸盐溶液一起置于50 mL的锥形瓶中, 其中吸附动力学实验中吸附剂的投加量为40 mg, 其他实验的吸附剂投加量均为25 mg; ④然后将锥形瓶放置在恒温水浴振荡器(150 r·min-1)中控制一定的温度(对于温度影响实验, 温度控制在20、30和40℃; 对于其他实验, 温度控制在25℃)进行振荡, 反应一定的时间, 其中吸附动力学的反应时间范围为15~1 440 min, 其它实验的反应时间均为24 h; ⑤将锥形瓶取出, 进行离心分离, 最后采用磷钼蓝分光光度法测定上清液中的磷酸盐浓度.需要指出的是, 在共存阴阳离子影响实验中, 共存电解质的磷溶液配制方法为:向容量瓶中加入磷酸盐溶液与某一电解质溶液, 再定容后制备得到.
1.4 数据处理ZeFeRBT和ZrFeCaBT对水中磷酸盐的平衡单位吸附量(qe, mg·g-1)和t时刻单位吸附量(qt, mg·g-1)可以分别通过公式(1)和(2)进行计算.
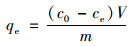
|
(1) |
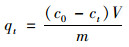
|
(2) |
式中, c0、ce和ct分别是初始时刻、平衡时刻和t时刻溶液中磷酸盐质量浓度(mg·L-1); V为溶液的体积(L); m为吸附剂材料的投加量(g).
初始时刻ZeFeRBT和ZrFeCaBT对水中磷酸盐的平均吸附速率[v, mg·(g·min)-1]可以通过公式(3)进行计算.
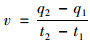
|
(3) |
式中, t1和t2为反应时间(min); q1和q2分别为对应t1和t2的单位吸附量(mg·g-1).
采用3种等温线模型对等温线数据进行拟合分析, 这3种模型为Langmuir、Freundlich和Dubinin-Radushkevich(D-R)等温线模型.
Langmuir等温吸附模型假设吸附质被吸附到均相吸附剂表面上形成单分子层覆盖, 它的线性方程表达式为[26]:
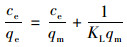
|
(4) |
式中, qe为吸附剂对水中吸附质的单位吸附量(mg·g-1); ce为平衡时刻水中吸附质的质量浓度(mg·L-1); qm为吸附剂对水中吸附质的最大单层单位吸附量(mg·g-1); KL为Langmuir吸附常数(L·mg-1).
Freundlich等温吸附模型假定的是吸附质被吸附到不均匀吸附剂表面上, 用线性方程表达的公式为[27]:
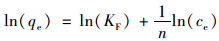
|
(5) |
式中, KF为Freundlich吸附常数[mg(1-1/n)·L(1/n)·g-1]; 1/n是与吸附强度有关的非均质因子.
D-R等温线模型的线性表达式为[28]:
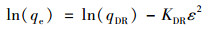
|
(6) |
式中, qDR为吸附剂对水中吸附质的最大单位吸附量(mmol·g-1); KDR为与吸附自由能有关的D-R等温吸附模型常数(mol2·kJ-2); ε是波兰尼势, ε=RT ln(1+1/ce), 其中, R为理想气体常数[8.314 J·(mol·K)-1]; T为反应温度(K).
吸附的平均自由能(E, kJ·mol-1)是指将1 mol的吸附质从水溶液转移至吸附剂表面所需要的能量, 它的计算公式为[28]:
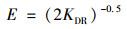
|
(7) |
通过E值可以确定吸附过程是化学吸附还是物理吸附.当E值的取值范围为0~8 kJ·mol-1时, 则是物理吸附过程; 当E值的取值范围为8~16 kJ·mol-1时, 则是化学吸附过程[28].
采用准二级动力学模型和颗粒内扩散模型对吸附动力学数据进行拟合分析.
准二级动力学模型[29]:
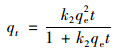
|
(8) |
颗粒内扩散模型[29]:
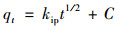
|
(9) |
式中, t为反应时间(min); qt和qe分别为t时刻和平衡时刻吸附剂对水中吸附质的单位吸附量(mg·g-1); k2 [g·(mg·min)-1]是准二级动力学的吸附速率常数; kip (mg·g-1·min-0.5)是颗粒内扩散常数; C (mg·g-1)是与边界层厚度有关的纵坐标截距, 并且C值越大, 则边界层越厚.如果qt和t0.5拟合成的曲线为线性且经过原点, 那么吸附剂对吸附质的吸附过程只受到颗粒内扩散的影响[29].但是, 如果qt和t0.5拟合成的曲线为线性但不经过原点, 那么吸附过程则受到颗粒内扩散和膜扩散的共同影响[29].
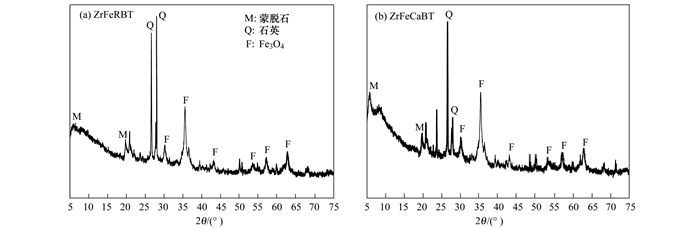
2 结果与讨论 2.1 材料表征XRD分析表明, 原始膨润土含蒙脱石和石英这2种矿物成分[21]. 图 1为ZrFeRBT和ZrFeCaBT的XRD图谱.从中可见, ZrFeRBT和ZrFeCaBT同样含蒙脱石和石英这2种矿物成分.这说明采用锆铁或锆铁钙对膨润土进行改性, 并不会改变膨润土中蒙脱石和石英的相结构.另外, 从图 1中发现, ZrFeRBT和ZrFeCaBT还包含Fe3O4.这意味着, 采用本研究所用的改性方法成功地将Fe3O4结合进了锆铁改性膨润土中, 使得本研究所制备的锆铁改性膨润土具备磁性. ZrFeRBT和ZrFeCaBT的磁分离特性可以进一步从图 2中得到证实.从中可见, 将ZrFeRBT或ZrFeCaBT与去离子水混合后, 再将一块磁铁靠近样品瓶中的混合物, 发现样品瓶中的ZrFeRBT或ZrFeCaBT很快被磁铁吸引到一边, 瓶中的悬浮液由原先的混浊状态变为澄清状态.这证实了ZrFeRBT和ZrFeCaBT具有良好的磁分离能力. 表 1为ZrFeRBT和ZrFeCaBT的化学元素组成.原始膨润土仅仅含少量的Fe(3.18%), 且不含Zr[21]. ZrFeRBT和ZrFeCaBT中Fe所占质量分数则远远高于原始膨润土, 并且ZrFeRBT和ZrFeCaBT中Zr所占质量分数分别高达9.31%和10.25%.这说明, 本研究采用锆铁或锆铁钙对原始膨润土进行改性, 已经成功地将锆和铁结合进磁性锆铁改性膨润土中.此外, 从表 1中还可以看出, ZrFeCaBT中Ca所占质量分数远高于ZrFeRBT.这说明采用钙对原始膨润土进行预处理, 显著地提高了磁性锆铁改性膨润土中可交换Ca离子的含量.
|
图 1 ZrFeRBT和ZrFeCaBT的XRD图谱 Fig. 1 XRD patterns of ZrFeRBT and ZrFeCaBT |

|
图 2 ZrFeRBT和ZrFeCaBT的磁分离效果 Fig. 2 Efficiency of the magnetic separation of ZrFeRBT and ZrFeCaBT in aqueous solution under the action of a magnet |
|
|
表 1 ZrFeRBT和ZrFeCaBT的化学元素组成/% Table 1 Chemical compositions of ZrFeRBT and ZrFeCaBT/% |
2.2 吸附等温线
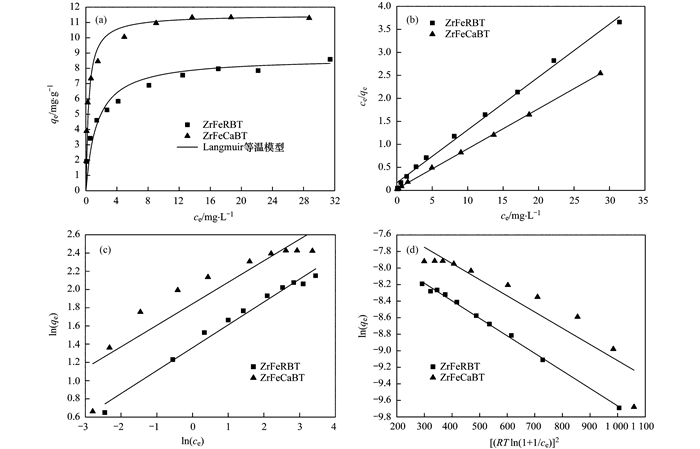
通过改变初始磷浓度获得了ZrFeRBT和ZrFeCaBT对水中磷酸盐吸附等温线, 结果见图 3(a).从中可以看出, 当初始磷浓度增加时, ZrFeRBT和ZrFeCaBT对水中磷酸盐的单位吸附量首先不断增加, 当初始磷浓度达到一定的数值时, 对磷酸盐的单位吸附量曲线就会趋于平缓, 即达到最大值.此外, 当溶液的初始磷质量浓度位于4~40 mg·L之间时, ZrFeCaBT对水中磷酸盐的吸附效果要明显优于ZrFeRBT.
|
(a)吸附量的实验值和预测值与吸附平衡浓度的关系; (b)线性Langmuir图; (c)线性Freundlich图; (d)线性D-R图 图 3 ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附等温线 Fig. 3 Adsorption isotherms of phosphate onto ZrFeRBT and ZrFeCaBT |
通过Langmuir、Freundlich和D-R等温模型对实验数据进行进一步的分析拟合, 线性拟合曲线见图 3(b)~3(d), 根据线性拟合曲线计算得出的各项参数见表 2.从中可见, ZrFeRBT对水中磷酸盐的吸附等温数据可以较好地采用Langmuir、Freundlich和D-R等温模型进行描述, 且Langmuir(R2=0.995)和D-R(R2=0.997)模型的拟合效果优于Freundlich(R2=0.982)模型.与此不同的是, Langmuir(R2=0.999)等温吸附模型对ZrFeCaBT吸附水中磷酸盐实验数据的拟合效果, 明显优于Freundlich(R2=0.835)和D-R(R2=0.879)等温吸附模型.
|
|
表 2 ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的吸附等温模型参数 Table 2 Fitting results of isotherms for phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
通过Langmuir等温模型可知, ZrFeRBT和ZrFeCaBT对水中磷酸盐的最大吸附量分别为8.70 mg·g-1和11.5 mg·g-1, 非常接近于最大的实验值, 这证明了使用Langmuir等温模型来预测磁性锆铁改性膨润土的最大饱和吸附容量是可靠的. ZrFeCaBT的磷酸盐最大单分子层饱和吸附容量要高于ZrFeRBT.这进一步说明了采用钙离子对原始膨润土进行预处理, 显著提高了磁性锆铁改性膨润土对水中磷酸盐的吸附能力.根据D-R等温吸附模型计算得到的ZrFeRBT和ZrFeCaBT的E值分别为16.3 kJ·mol-1和24.1 kJ·mol-1, 都高于8 kJ·mol-1.这说明, 当初始磷酸盐溶液pH值为7和反应温度为25℃时, ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附过程为化学吸附.
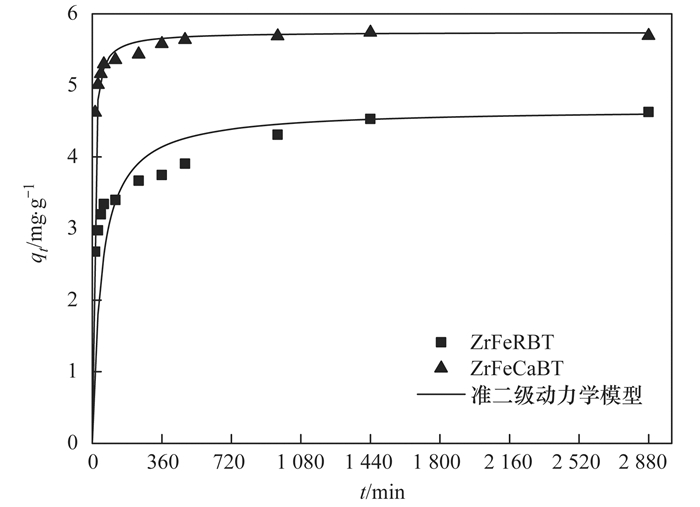
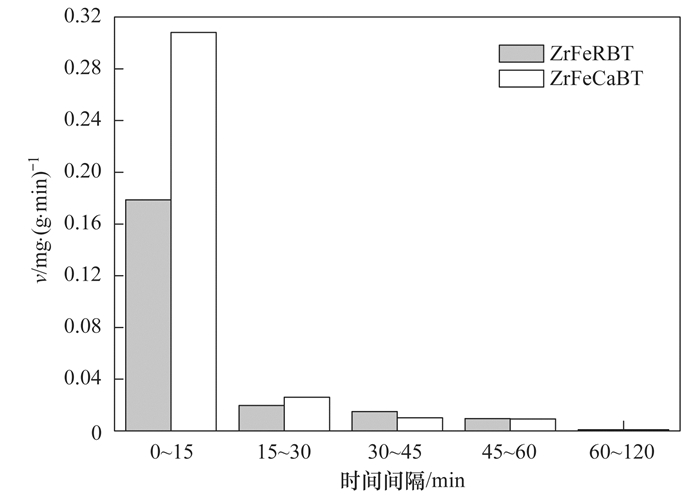
2.3 吸附动力学图 4为ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附动力学拟合曲线.根据图 4实验数据计算得到的初始吸附阶段ZrFeRBT和ZrFeCaBT对水中磷酸盐的平均吸附速率, 详见图 5.从中可见, ZrFeRBT和ZrFeCaBT对水中磷酸盐的单位吸附量随时间的增加而增加, 直至达到吸附平衡; 在吸附的早期阶段, 由于吸附剂材料表面存在着大量的活性点位, 所以ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附速率很大, 单位吸附量随着反应时间的增加而快速增加; 在经过最初的快速吸附之后, 由于吸附剂材料表面的活性点位大量减少, 所以ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附速率变得较小, 单位吸附量则随着反应时间的增加而缓慢增加, 最后到达吸附平衡.此外, 从图 4中还可以看出, 当反应时间相同时, ZrFeCaBT对水中磷酸盐的单位吸附量要高于ZrFeRBT.这一现象表明, 与ZrFeRBT相比, ZrFeCaBT对水中磷酸盐有着更高的亲和力.另外, 从图 5中还可以看出, 在早期的吸附阶段, ZrFeCaBT的平均吸附速率要远远高于ZrFeRBT, 随后二者的差距急剧减少.由此可见, 在早期的吸附阶段, ZrFeCaBT比ZrFeRBT能够更快地去除水中磷酸盐.
|
图 4 ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附动力学曲线 Fig. 4 Kinetics for phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
|
图 5 吸附前期ZrFeRBT和ZrFeCaBT对水中磷酸盐的平均吸附速率 Fig. 5 Average adsorption rate of phosphate onto ZrFeRBT and ZrFeCaBT during the earlier adsorption stage |
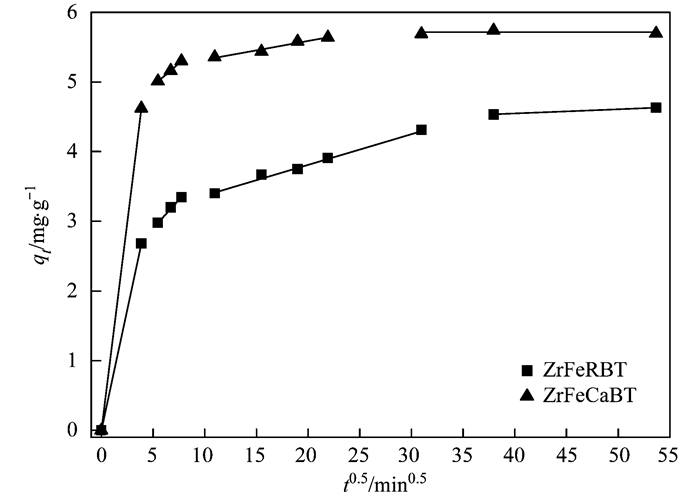
为了进一步探究吸附剂材料的吸附机制, 并确定它的吸附速率, 本文采用准二级动力学模型和颗粒内扩散模型来对图 4动力学数据进行拟合分析.颗粒内扩散模型的拟合曲线见图 6.准二级动力学模型和颗粒内扩散模型对图 4中实验数据的拟合结果见表 3.从中可见, 准二级动力学模型对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐动力学实验数据的拟合相关系数(R2)非常高, 分别为0.998和0.999.这说明ZrFeRBT和ZrFeCaBT与磷酸盐之间产生的是化学吸附[30], 这一结论与上文中根据D-R等温线模型E值所得到的结果是相一致的.从表 3中还可见, 计算得到的ZrFeCaBT吸附水中磷酸盐的初始时刻速率(h), 明显大于ZrFeRBT.这说明, 采用钙离子对原始膨润土进行预处理, 可以极大地增加磁性锆铁改性膨润土对水中磷酸盐的初始吸附速率.这与根据图 5所获得的结论是一致的.
|
图 6 ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的qt和t0.5曲线 Fig. 6 Plot of qt versus t0.5 for phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
|
|
表 3 ZrFeRBT和ZrFeCaBT吸附磷酸盐的准二级动力学和颗粒内扩散动力学模型参数 Table 3 Parameters of pseudo-second-order and intra-diffusion kinetic models for phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
从图 6可以看出, ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的动力学过程可以分为3个阶段, 即:快速表面吸附阶段、逐渐吸附阶段以及最终平衡阶段.在快速表面吸附阶段, 水中的磷酸盐会穿过吸附剂周围的边界层快速地被吸附, 该阶段的速率限制步骤主要是膜扩散[23, 29].在逐渐吸附阶段, 颗粒内扩散是该阶段的速率限制步骤; 考虑到该阶段的拟合曲线不通过原点, 故该阶段的吸附速率限制步骤不仅仅只是颗粒内扩散, 而是颗粒内扩散和膜扩散的共同作用[23, 29].在最终平衡阶段, 吸附剂表面上空闲的活性位点的数量已经非常少了, 所以该阶段的吸附速率非常慢[23, 29].
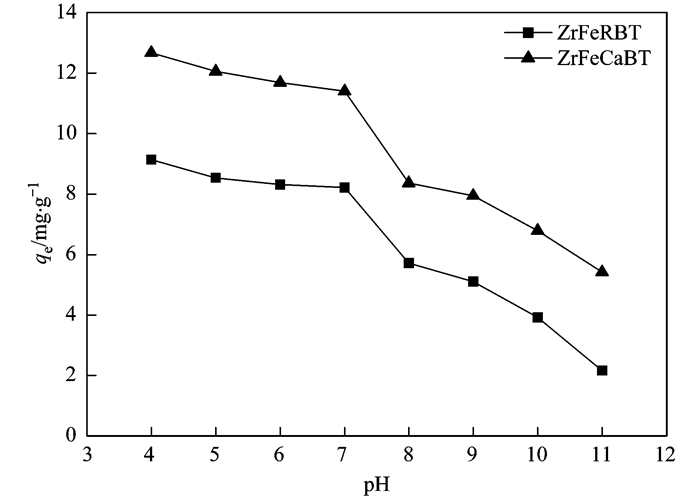
2.4 pH值对吸附的影响溶液pH值可能是影响金属氧化物或氢氧化物吸附磷酸盐的一个重要参数, 这可能是因为溶液pH值不仅能够改变溶液中磷酸盐的存在形式, 而且会改变吸附剂表面的官能基团的种类和数量.为此, 本文通过改变初始溶液pH值, 来探索ZrFeRBT和ZrFeCaBT对磷酸盐的吸附随pH值的改变而变化的情况, 结果见图 7.从中可见, 当初始溶液pH值为4时, ZrFeRBT和ZrFeCaBT均有着对水中磷酸盐最大的吸附容量; 当初始溶液pH值从4增加到11时, ZrFeRBT和ZrFeCaBT对磷酸盐的吸附容量均逐渐下降.这说明, 磁性锆铁改性膨润土对水中磷酸盐的吸附能力依赖于溶液pH值, pH值越高, 越不利于其对水中磷酸盐的吸附.
|
图 7 溶液pH值对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响 Fig. 7 Effect of solution pH on phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
先前的研究已经发现, 锆改性膨润土吸附水中磷酸盐的机制主要是: ①首先, 吸附剂中锆与水中磷酸盐之间发生配位体交换, 释放出OH-; ②然后, 被吸附到吸附剂表面上的磷酸盐与锆之间形成了内层络合物[21, 25]. Fe3O4基吸附剂吸附水中磷酸盐的一个主要机制是:与铁结合的表面羟基基团与磷酸盐之间发生配位体交换, 进而形成了内层络合物(Fe-O-P)[31].另外, 根据吸附等温线和动力学研究已经确定, 磁性锆铁改性膨润土对水中磷酸盐的吸附, 主要是化学吸附反应.因此, 磁性锆铁改性膨润土吸附水中磷酸盐的主要机制应该是:吸附剂中与铁锆结合的表面羟基基团和水中磷酸盐之间的配位体交换作用, 以及内层络合物的形成.
溶液pH值对磁性锆铁改性膨润土的影响, 可以解释为: ①当初始溶液pH值从4增加至11时, 溶液从以H2PO4-的形式存在为主转变为以HPO42-的形式存在为主, 而且H2PO4-比HPO42-更有利于配位体交换, 从而导致通过配位体交换和内层络合物形成机制被ZrFeRBT/ZrFeCaBT所吸附的磷酸盐量的降低[32]; ②随着初始溶液pH值逐渐增加, 吸附剂表面的正电荷减少而负电荷增加, 因此吸附剂和磷酸盐之间的静电吸引作用减弱而静电排斥作用增强, 这都不利于ZrFeRBT和ZrFeCaBT对磷酸盐的吸附[23]; ③在强碱性条件下, 更多的OH-与磷酸盐竞争吸附剂表面的活性位点, 从而导致ZrFeRBT和ZrFeCaBT对磷酸盐的吸附容量降低.
从图 7中还可以看出, 在不同pH值条件下, ZrFeCaBT对水中磷酸盐的吸附能力均明显强于ZrFeRBT.这说明, 采用钙离子对原始膨润土进行预处理, 可以显著增强磁性锆铁改性膨润土对水中磷酸盐的吸附能力.
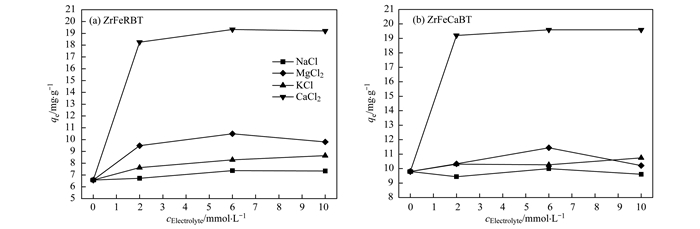
2.5 共存阳离子和阴离子对吸附的影响天然水体中往往存在共存Na+、K+、Mg2+和Ca2+等阳离子, 同时也往往存在Cl-、HCO3-、SO42-和NO3-等阴离子, 它们可能会对磁性锆铁改性膨润土吸附水中磷酸盐产生影响.为此, 本文首先考察了溶液共存NaCl、KCl、MgCl2和CaCl2对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响, 结果见图 8.溶液共存的NaCl略微促进了ZrFeRBT对水中磷酸盐的吸附, 当NaCl浓度由0增加到10 mmol·L-1时, ZrFeRBT对磷酸盐的单位吸附量由6.57逐渐增加到7.34 mg·g-1.但是, 溶液共存NaCl对ZrFeCaBT吸附水中磷酸盐的影响却很小.先前的研究发现[30, 32], 如果吸附剂通过静电吸引作用去除水中的磷酸盐, 那么离子强度会降低吸附剂对水中磷酸盐的吸附去除; 如果吸附机制为配位体交换和内层络合物形成, 那么离子强度则对吸附无影响或者促进吸附.溶液共存NaCl对ZrFeRBT和ZrFeCaBT吸附磷酸盐的影响规律, 这证实了配位体交换和内层络合物形成是磁性锆铁改性膨润土吸附水中磷酸盐的主要机制.这也意味着溶液共存的Na+和Cl-对磁性锆铁改性膨润土吸附水中磷酸盐无负面影响.由图 8还可见, 溶液共存的KCl、MgCl2和CaCl2均会促进ZrFeRBT和ZrFeCaBT对水中磷酸盐的吸附, 但CaCl2的促进作用远远大于KCl和MgCl2.这说明, 溶液共存Ca2+、Mg2+和K+促进了磁性锆铁改性膨润土对水中磷酸盐的吸附, 并且Ca2+的促进作用远远大于Mg2+和K+. Ca2+对磁性锆铁改性膨润土吸附磷酸盐的促进作用, 与先前文献报道的Ca2+对水合氧化锆[33, 34]、锆改性沸石[35]和锆改性膨润土[25]的影响是类似的.
|
cElectrolyte为溶液中共存电解质的浓度,下同 图 8 共存NaCl、KCl、MgCl2和CaCl2对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响 Fig. 8 Effect of coexisting NaCl, KCl, MgCl2, and CaCl2 on phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
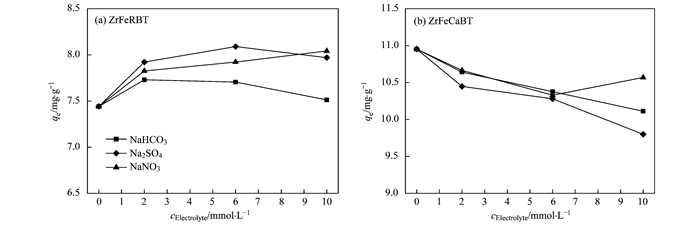
本文进一步考察了NaHCO3、Na2SO4和NaNO3对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响, 结果见图 9.从中可见, NaHCO3、Na2SO4和NaNO3对ZrFeRBT吸附水中磷酸盐有略微的促进作用, 但与之略微不同的是, 这些电解质对ZrFeCaBT吸附水中磷酸盐有略微的抑制作用.考虑到Na+略微促进了ZrFeRBT对水中磷酸盐的吸附, 所以HCO3-、SO42-和NO3-等阴离子对ZrFeRBT吸附水中磷酸盐不会产生抑制作用.考虑到Na+对ZrFeRBT吸附水中磷酸盐无影响, 所以HCO3-、SO42-和NO3-等阴离子略微抑制了ZrFeRBT对水中磷酸盐的吸附.从总体而言, 溶液中存在的HCO3-、SO42-和NO3-等阴离子对磁性锆铁改性膨润土吸附水中磷酸盐的影响可以忽略不计.
|
图 9 共存NaHCO3、Na2SO4和NaNO3对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响 Fig. 9 Effect of coexisting NaHCO3, Na2SO4, and NaNO3 on phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
从图 8和图 9中还可以看出, 在共存NaCl、KCl、NaHCO3、Na2SO4和NaNO3等电解质的条件下, ZrFeCaBT吸附水中磷酸盐的能力仍然要明显强于ZrFeRBT.这说明, 采用钙离子对原始膨润土进行预处理, 可以显著地提高磁性锆铁改性膨润土对水中磷酸盐的吸附能力.
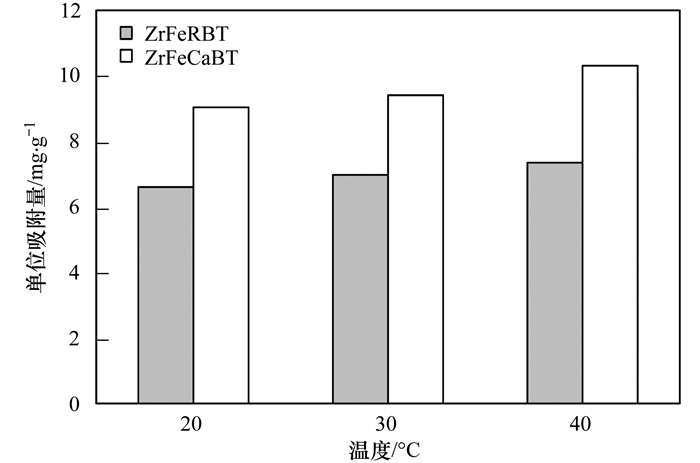
2.6 反应温度对吸附的影响图 10为温度对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响.从中可见, 当反应温度由20逐渐增加到40℃时, ZrFeRBT和ZrFeCaBT对水中磷酸盐的单位吸附量分别由6.63 mg·g-1逐渐增加到7.36 mg·g-1和由9.06 mg·g-1逐渐增加到10.3 mg·g-1.这说明, 反应温度越高, 越有利于磁性锆铁改性膨润土对水中磷酸盐的吸附.此外, 在不同的反应温度条件下, ZrFeCaBT吸附水中磷酸盐的能力均明显强于ZrFeRBT.这同样说明了采用钙离子对膨润土进行预处理, 可以明显提高磁性锆铁改性膨润土对水中磷酸盐的吸附能力.
|
图 10 温度对ZrFeRBT和ZrFeCaBT吸附水中磷酸盐的影响 Fig. 10 Influence of reaction temperature on phosphate adsorption onto ZrFeRBT and ZrFeCaBT |
图 11为吸附磷酸盐后磁性锆铁改性膨润土的磁分离效果.从中可见, 通过外加磁场的作用, 可以很容易地将吸附磷酸盐后的磁性锆铁改性膨润土从溶液中分离出来, 从而方便地实现了对磁性锆铁改性膨润土的回收.

|
图 11 吸附磷酸盐后磁性锆铁改性膨润土的磁分离效果 Fig. 11 Efficiency of the magnetic separation of phosphate-adsorbed zirconium/iron-modified bentonites in aqueous solution under the action of a magnet |
文献[34]发现, 溶液共存Ca2+极大地促进了水合氧化锆对水中磷酸盐的吸附, 其促进机制为: ① Ca2+首先与溶液中磷酸盐形成CaHPO40, 然后CaHPO40被吸附到水合氧化锆表面上, 形成Zr(OPO)(O2H)Ca+; ②磷酸盐首先被吸附到水合氧化锆表面上, 形成Zr(OPO)(O2H)-, Ca2+再被吸附到水合氧化锆表面上形成Zr(OPO)(O2H)Ca+, 这降低了已吸附磷酸盐与未吸附磷酸盐之间的静电排斥力, 从而增强了水合氧化锆对水中磷酸盐的吸附.另一先前的文献发现[25], 锆改性膨润土中可交换Ca2+离子对其吸附水中磷酸盐起到非常重要的作用, Ca2+含量越大, 其吸附去除水中磷酸盐的能力越强; 通过阳离子交换作用从锆改性膨润土中交换出来的Ca2+, 会与水中的磷酸盐形成了CaHPO40, 而CaHPO40更容易被锆改性膨润土所吸附, 从而可以促进锆改性膨润土对水中磷酸盐的吸附; 另外, 吸附到锆改性膨润土表面上所形成的Zr(OPO)(O2H)Ca+, 降低了已吸附磷酸盐与未吸附磷酸盐之间的静电排斥力, 从而也可以促进锆改性膨润土对水中磷酸盐的吸附.与锆改性膨润土类似的是, 通过阳离子交换作用从磁性锆铁改性膨润土中释放出来的Ca2+, 同样可以促进磁性锆铁改性膨润土中锆对水中磷酸盐的吸附. ZrFeCaBT中Ca2+含量明显高于ZrFeRBT, 所以从前者中释放出来的Ca2+的促进作用大于了后者, 从而导致前者的吸磷能力大于了后者.因此, 钙预处理增强了磁性锆铁改性膨润土对水中磷酸盐的吸附, 这主要归功于钙预处理增加了磁性锆铁改性膨润土中可交换Ca2+含量.
综上所示, 磁性锆铁改性膨润土与水中磷酸盐之间的相互作用可以通过以下的公式加以描述[25, 34~38]:
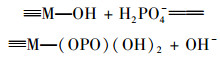
|
(10) |
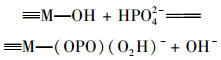
|
(11) |
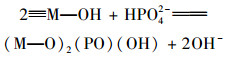
|
(12) |
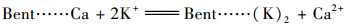
|
(13) |
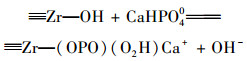
|
(14) |
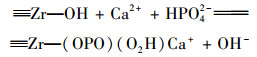
|
(15) |
式中, M是指Zr或Fe; Bent是指膨润土.
3 结论(1) 磁性锆铁改性膨润土对水中磷酸盐吸附平衡实验数据可以很好地采用Langmuir等温吸附模型加以描述, 动力学实验数据可以很好地采用准二级动力学模型和颗粒内扩散模型进行描述.吸附等温线与吸附动力学的研究结果表明, 磁性锆铁改性膨润土吸附水中磷酸盐的过程属于化学吸附.
(2) 溶液pH对磁性锆铁改性膨润土吸附水中磷酸盐具有非常重要的影响, 随着pH值的增加, 对应的吸附效果逐渐降低.当溶液共存Cl-、HCO3-、SO42-、NO3-、Na+、K+、Mg2+和Ca2+等阴阳离子时, 磁性锆铁改性膨润土对水中磷酸盐的吸附具有很好的选择性, 并且溶液共存的Ca2+会极大地促进了吸附剂对水中磷酸盐的吸附.
(3) 采用Ca2+对膨润土进行预处理, 极大地提高了磁性锆铁改性膨润土对水中磷酸盐的吸附能力.
| [1] |
秦伯强. 长江中下游浅水湖泊富营养化发生机制与控制途径初探[J]. 湖泊科学, 2002, 14(3): 193-202. Qin B Q. Approaches to mechanisms and control of eutrophication of shallow lakes in the middle and lower reaches of the Yangze River[J]. Journal of Lake Sciences, 2002, 14(3): 193-202. DOI:10.3321/j.issn:1003-5427.2002.03.001 |
| [2] |
曹金玲, 许其功, 席北斗, 等. 我国湖泊富营养化效应区域差异性分析[J]. 环境科学, 2012, 33(6): 1777-1783. Cao J L, Xu Q G, Xi B D, et al. Regional heterogeneity of lake eutrophication effects in China[J]. Environmental Science, 2012, 33(6): 1777-1783. |
| [3] | Smith V H, Tilman G D, Nekola J C. Eutrophication:impacts of excess nutrient inputs on freshwater, marine, and terrestrial ecosystems[J]. Environmental Pollution, 1999, 100(1-3): 179-196. DOI:10.1016/S0269-7491(99)00091-3 |
| [4] |
张志斌, 周光军, 魏垒垒, 等. 主要理化因子对南四湖底泥磷释放的影响[J]. 山东建筑大学学报, 2010, 25(6): 637-641. Zhang Z B, Zhou G J, Wei L L, et al. Effect of main physicochemical factors on the release of phosphorus from Nansi Lake sediment[J]. Journal of Shandong Jianzhu University, 2010, 25(6): 637-641. DOI:10.3969/j.issn.1673-7644.2010.06.016 |
| [5] |
黎睿, 王圣瑞, 肖尚斌, 等. 长江中下游与云南高原湖泊沉积物磷形态及内源磷负荷[J]. 中国环境科学, 2015, 35(6): 1831-1839. Li R, Wang S R, Xiao S B, et al. Sediments phosphorus forms and loading in the lakes of the mid-lower reaches of the Yangtze River and Yunnan Plateau, China[J]. China Environmental Science, 2015, 35(6): 1831-1839. DOI:10.3969/j.issn.1000-6923.2015.06.028 |
| [6] | Yu J H, Ding S M, Zhong J C, et al. Evaluation of simulated dredging to control internal phosphorus release from sediments:Focused on phosphorus transfer and resupply across the sediment-water interface[J]. Science of the Total Environment, 2017, 592: 662-673. DOI:10.1016/j.scitotenv.2017.02.219 |
| [7] | Rydin E, Welch E B. Aluminum dose required to inactivate phosphate in lake sediments[J]. Water Research, 1998, 32(10): 2969-2976. DOI:10.1016/S0043-1354(98)00055-4 |
| [8] |
林建伟, 朱志良, 赵建夫. 曝气复氧对富营养化水体底泥氮磷释放的影响[J]. 生态环境, 2005, 14(6): 812-815. Lin J W, Zhu Z L, Zhao J F. Effect of aeration on release of nitrogen and phosphorus from sediments in eutrophic waterbody[J]. Ecology and Environment, 2005, 14(6): 812-815. DOI:10.3969/j.issn.1674-5906.2005.06.002 |
| [9] |
张云, 王圣瑞, 段昌群, 等. 滇池沉水植物生长过程对间隙水氮、磷时空变化的影响[J]. 湖泊科学, 2018, 30(2): 314-325. Zhang Y, Wang S R, Duan C Q, et al. Spatial-temporal variations of nitrogen and phosphorus forms in sediment porewater as affected by submerged plant in Lake Dianchi[J]. Journal of Lake Sciences, 2018, 30(2): 314-325. |
| [10] | Yamada T M, Sueitt A P E, Beraldo D A S, et al. Calcium nitrate addition to control the internal load of phosphorus from sediments of a tropical eutrophic reservoir:microcosm experiments[J]. Water Research, 2012, 46(19): 6463-6475. DOI:10.1016/j.watres.2012.09.018 |
| [11] |
朱广伟, 李静, 朱梦圆, 等. 锁磷剂对杭州西湖底泥磷释放的控制效果[J]. 环境科学, 2017, 38(4): 1451-1459. Zhu G W, Li J, Zhu M Y, et al. Efficacy of phoslock® on the reduction of sediment phosphorus release in West Lake, Hangzhou, China[J]. Environmental Science, 2017, 38(4): 1451-1459. |
| [12] | Meis S, Spears B M, Maberly S C, et al. Sediment amendment with Phoslock® in Clatto Reservoir (Dundee, UK):investigating changes in sediment elemental composition and phosphorus fractionation[J]. Journal of Environmental Management, 2012, 93(1): 185-193. DOI:10.1016/j.jenvman.2011.09.015 |
| [13] | Wang Y, Ding S M, Wang D, et al. Static layer:A key to immobilization of phosphorus in sediments amended with lanthanum modified bentonite (Phoslock®)[J]. Chemical Engineering Journal, 2017, 325: 49-58. DOI:10.1016/j.cej.2017.05.039 |
| [14] | Yin H B, Han M X, Tang W Y. Phosphorus sorption and supply from eutrophic lake sediment amended with thermally-treated calcium-rich attapulgite and a safety evaluation[J]. Chemical Engineering Journal, 2016, 285: 671-678. DOI:10.1016/j.cej.2015.10.038 |
| [15] | Wang C H, He R, Wu Y, et al. Bioavailable phosphorus (P) reduction is less than mobile P immobilization in lake sediment for eutrophication control by inactivating agents[J]. Water Research, 2017, 109: 196-206. DOI:10.1016/j.watres.2016.11.045 |
| [16] | Li C J, Yu H X, Tabassum S, et al. Effect of calcium silicate hydrates (CSH) on phosphorus immobilization and speciation in shallow lake sediment[J]. Chemical Engineering Journal, 2017, 317: 844-853. DOI:10.1016/j.cej.2017.02.117 |
| [17] | Gibbs M, Özkundakci D. Effects of a modified zeolite on P and N processes and fluxes across the lake sediment-water interface using core incubations[J]. Hydrobiologia, 2011, 661(1): 21-35. DOI:10.1007/s10750-009-0071-8 |
| [18] |
李佳, 林建伟, 詹艳慧. 镧改性沸石活性覆盖控制重污染河道底泥溶解性磷酸盐和铵释放研究[J]. 环境科学, 2013, 34(11): 4266-4274. Li J, Lin J W, Zhan Y H. Evaluation of in situ capping with lanthanum-modified zeolite to control phosphate and ammonium release from sediments in heavily polluted river[J]. Environmental Science, 2013, 34(11): 4266-4274. |
| [19] | Yang M J, Lin J W, Zhan Y H, et al. Immobilization of phosphorus from water and sediment using zirconium-modified zeolites[J]. Environmental Science and Pollution Research, 2015, 22(5): 3606-3619. DOI:10.1007/s11356-014-3604-2 |
| [20] | Yang M J, Lin J W, Zhan Y H, et al. Adsorption of phosphate from water on lake sediments amended with zirconium-modified zeolites in batch mode[J]. Ecological Engineering, 2014, 71: 223-233. DOI:10.1016/j.ecoleng.2014.07.035 |
| [21] | Lin J W, Wang H, Zhan Y H, et al. Evaluation of sediment amendment with zirconium-reacted bentonite to control phosphorus release[J]. Environmental Earth Sciences, 2016, 75(11): 942. DOI:10.1007/s12665-016-5744-9 |
| [22] |
王虹, 林建伟, 詹艳慧, 等. 锆改性高岭土原位改良技术控制重污染河道底泥磷释放效果[J]. 环境科学, 2015, 36(10): 3720-3729. Wang H, Lin J W, Zhan Y H, et al. Efficiency of sediment amendment with zirconium-modified kaolin clay to control phosphorus release from sediments in heavily polluted rivers[J]. Environmental Science, 2015, 36(10): 3720-3729. |
| [23] |
姜博汇, 林建伟, 詹艳慧, 等. 不同锆负载量锆改性膨润土对水中磷酸盐吸附作用的对比[J]. 环境科学, 2017, 38(6): 2400-2411. Jiang B H, Lin J W, Zhan Y H, et al. Comparison of phosphate adsorption onto zirconium-modified bentonites with different zirconium loading levels[J]. Environmental Science, 2017, 38(6): 2400-2411. |
| [24] | Funes A, del Arco A, álvarez-Manzaneda I, et al. A microcosm experiment to determine the consequences of magnetic microparticles application on water quality and sediment phosphorus pools[J]. Science of the Total Environment, 2017, 579: 245-253. DOI:10.1016/j.scitotenv.2016.11.120 |
| [25] | Lin J W, Jiang B H, Zhan Y H. Effect of pre-treatment of bentonite with sodium and calcium ions on phosphate adsorption onto zirconium-modified bentonite[J]. Journal of Environmental Management, 2018, 217: 183-195. |
| [26] | Langmuir I. The constitution and fundamental properties of solids and liquids. Part Ⅰ. Solids[J]. Journal of the American Chemical Society, 1961, 38(11): 2221-2295. |
| [27] | Freundlich H. Colloid & capillary chemistry[M]. London: Methuen & Co. Ltd, 1926. |
| [28] | D'Arcy M, Weiss D, Bluck M, et al. Adsorption kinetics, capacity and mechanism of arsenate and phosphate on a bifunctional TiO2-Fe2O3 bi-composite[J]. Journal of Colloid and Interface Science, 2011, 364(1): 205-212. DOI:10.1016/j.jcis.2011.08.023 |
| [29] | Tan K L, Hameed B H. Insight into the adsorption kinetics models for the removal of contaminants from aqueous solutions[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 74: 25-48. DOI:10.1016/j.jtice.2017.01.024 |
| [30] | Su Y, Cui H, Li Q, et al. Strong adsorption of phosphate by amorphous zirconium oxide nanoparticles[J]. Water Research, 2013, 47(14): 5018-5026. DOI:10.1016/j.watres.2013.05.044 |
| [31] | Cai R, Wang X, Ji X H, et al. Phosphate reclaim from simulated and real eutrophic water by magnetic biochar derived from water hyacinth[J]. Journal of Environmental Management, 2017, 187: 212-219. |
| [32] | Wang Z, Xing M C, Fang W K, et al. One-step synthesis of magnetite core/zirconia shell nanocomposite for high efficiency removal of phosphate from water[J]. Applied Surface Science, 2016, 366: 67-77. DOI:10.1016/j.apsusc.2016.01.059 |
| [33] |
王星星, 林建伟, 詹艳慧, 等. 不同沉淀pH值条件下制备的水合氧化锆对水中磷酸盐的吸附作用[J]. 环境科学, 2017, 38(5): 1936-1946. Wang X X, Lin J W, Zhan Y H, et al. Adsorption of phosphate from aqueous solution on hydrous zirconium oxides precipitated at different pH values[J]. Environmental Science, 2017, 38(5): 1936-1946. |
| [34] | Lin J W, Zhan Y H, Wang H, et al. Effect of calcium ion on phosphate adsorption onto hydrous zirconium oxide[J]. Chemical Engineering Journal, 2017, 309: 118-129. DOI:10.1016/j.cej.2016.10.001 |
| [35] | Lin J W, Zhang Z, Zhan Y H. Effect of humic acid preloading on phosphate adsorption onto zirconium-modified zeolite[J]. Environmental Science and Pollution Research, 2017, 24(13): 12195-12211. DOI:10.1007/s11356-017-8873-0 |
| [36] | Zhan Y H, Zhang H H, Lin J W, et al. Role of zeolite's exchangeable cations in phosphate adsorption onto zirconium-modified zeolite[J]. Journal of Molecular Liquids, 2017, 243: 624-637. DOI:10.1016/j.molliq.2017.08.091 |
| [37] | Xiong W P, Tong J, Yang Z H, et al. Adsorption of phosphate from aqueous solution using iron-zirconium modified activated carbon nanofiber:performance and mechanism[J]. Journal of Colloid and Interface Science, 2017, 493: 17-23. DOI:10.1016/j.jcis.2017.01.024 |
| [38] | Zach-Maor A, Semiat R, Shemer H. Adsorption-desorption mechanism of phosphate by immobilized nano-sized magnetite layer:interface and bulk interactions[J]. Journal of Colloid and Interface Science, 2011, 363(2): 608-614. DOI:10.1016/j.jcis.2011.07.062 |
 2019, Vol. 40
2019, Vol. 40


