2. 中国科学院广州地球化学研究所, 有机地球化学国家重点实验室, 广州 510640;
3. 南开大学环境科学与工程学院, 环境污染过程与基准教育部重点实验室, 天津 300350
2. State Key Laboratory of Organic Geochemistry, Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, Guangzhou 510640, China;
3. Key Laboratory of Pollution Processes and Environment Criteria, Ministry of Education, College of Environmental Science and Engineering, Nankai University, Tianjin 300350, China
全氟和多氟烷基化合物(perfluoroalkyl and polyfluoroalkyl substances, PFASs)是一类人工合成的化合物, 因其良好的疏水、疏油特性而被广泛应用于纺织、造纸、化工和灭火剂等生产领域[1].全氟辛烷磺酸(perfluorooctane sulfonate acid, PFOS)和全氟辛酸(perfluorooctanoic acid, PFOA)是两种应用最广泛的PFASs, 具有较强的毒性及潜在的致癌性, 可对生物体造成急性和亚慢性毒性作用[2]. 2006年, 美国环保署联合全球8家PFOA生产公司承诺到2015年停止PFOA的生产[3]. 2009年, 斯德哥尔摩缔约方大会将PFOS及其盐类列入附件B并在全球限制使用[4], 之后在2015年通过了PFOA及其盐类和相关化合物的附件D审查(POPs特性筛选), 认为PFOA符合附件D筛选标准, 决定在其附件E审查时应纳入可降解为PFOA的盐类和相关化合物[5]. C8被禁用后, 一些具有较低的生物富集性[6]和毒性[7, 8]的替代品受到广泛关注[9], 如全氟己酸(perfluorohexanoic acid, PFHxA)[6]、全氟醚基烷酸(perfluoroalkyl ether sulfonic acids, PFESAs)[10]、三氟乙酸(trifluoroacetic, TFA)和全氟聚醚类[perfluoropolyethers, PFPEs:CF3O(CF2)3OCHFCF2COOH(ADONA)和CF3(CF2)2OCF(CF3)COOH(HFPO-DA)], 目前已在多个流域的水环境中检出[10~12].
截止到2004年, 直接或间接释放到环境中的PFASs含量为3 200~7 300 t[13]. PFASs在大气[4]、水体[13]、沉积物[14]、土壤[15]及生物体[16]等多种环境介质中均有不同程度的检出.由于具有较高的水溶性、较低的蒸气压和较强的表面活性, 离子型的全氟烷酸(PFAAs)多分布在水环境中[13].进入水体的PFASs可被水生生物摄入体内转移至食物网并随食物链累积[17].河流不仅在全球地球化学循环中起着关键作用, 也为人类生存提供必须的水资源.它是人类排污的主要场所, 是将污染物从大陆向海洋输送的重要途径[18].因此, 了解PFASs在河流中的分布特征及污染来源极为重要.黄河是华北地区重要的饮用水、农业用水和工业用水水源, 黄河渭南—郑州段流经人类活动密集的中原城市群.随着流域内经济的快速发展, 工业化程度提高, 黄河每年接纳的废水量为9.23亿m3, 以有机污染物为主[19].本研究分析了黄河渭南—郑州段表层水体水相及颗粒相中的28种PFASs, 阐述PFASs的分布特征, 并估算了流域通量.
1 材料与方法 1.1 试剂与药品甲醇(色谱级)、丙酮(色谱级)、氢氧化铵(25%, 体积比)购自德国Merck公司, 玻璃纤维滤膜(glass fibre filter, GFF, GF/C, Φ 47 mm, 1.2 μm)购自美国Whatman公司. 28种目标化合物包含PFCAs(TFA、PFPrA、PFBA、PFPeA、PFHxA、PFHpA、PFOA、PFNA、PFDA、PFUnA和PFDoDA)、PFSAs(PFBS、PFHxS和PFOS)、FTCAs(3:3、5:3、7:3、6:2和8:2 FTCA)、FTUCAs(6:2和8:2 FTUCA)、PFESAs(Cl-6:2和Cl-8:2 PFESA)、PFPEs(ADONA和HFPO-DA)和diPAP(6:2、8:2和10:2 diPAP), 和9种同位素标记内标(internal standard, IS)的具体信息见表 1.所有标准物质购自加拿大Wellington实验室, 纯度大于98%. HPLC级水购自美国Fisher公司. Millipore水由Milli-Q PLUS 185系统(德国)制备. Oasis系列弱阴离子交换柱(WAX, 150 mg, 6 mL, 30 μm)购自美国Waters公司. Envi-Carb柱(3 mL, 0.25 g)购自Supelco公司.
|
|
表 1 目标化合物和内标化合物全称、缩写及特征离子 Table 1 Full names, abbreviations and characteristic ion of the target compound and standard chemicals |
1.2 样品采集
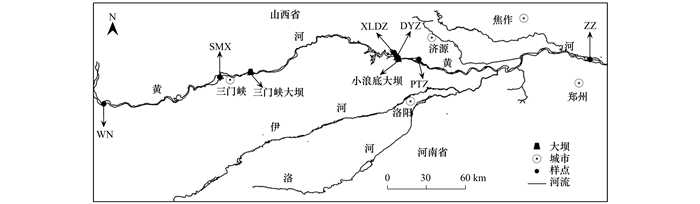
2016年4月, 在渭南(WN, 110°19′35.05″E, 34°36′17.00″N)、三门峡(SMX, 111°07′54.95″ E, 34°47′27.53″ N)、小浪底镇(XLDZ, 112°20′33.07″ E, 34°57′40.52″ N)、大峪镇(DYZ, 112°21′27.54″ E, 34°56′17.70″ N)、坡头镇(PTZ, 112°30′52.23″ E, 34°54′51.55″ N)和郑州(ZZ, 113°42′09.03″, 34°54′48.64″ N)布设6个采样点(见图 1), 每个样点采集3个体积为1 L的表层水样(0~1 m), 共18个样品.河水使用甲醇预洗的不锈钢采水器采集, 收集在甲醇预洗的聚丙烯(polypropylene, PP)瓶中, -20℃下保存至进一步处理.
|
图 1 黄河渭南—郑州段样点分布示意 Fig. 1 Sampling stations in the Weinan-Zhengzhou section of the Yellow River |
利用抽滤装置将颗粒相截留在GFF上.水相使用固相萃取法(solid-phase extraction, SPE)提取PFASs.萃取柱使用前用10 mL的甲醇和10 mL的Millipore水活化.样品萃取前加载5 ng (500 μg·L-1, 10 μL)内标, 由改造的分液漏斗控制流速1~2滴·s-1, 依靠重力富集到SPE柱上.分别用5 mL甲醇和5 mL 0.1%氢氧化铵甲醇溶液洗脱萃取柱, 洗脱液氮吹浓缩至150 μL.滤膜使用前在马弗炉中450℃灼烧12 h.加载样品后的滤膜在-50℃下冷冻干燥72 h, 之后置于PP离心管超声萃取.离心管中加入10 mL甲醇和5 ng(500 μg·L-1, 10 μL)IS, 于摇床振荡20 min后超声15 min.在4 000 r·min-1条件下离心10 min, 转移上清液至50 mL的PP管中, 重复两次.萃取液氮吹(>99.99%)浓缩至2 mL, 经10 mL甲醇活化的Envi-Carb柱净化, 氮吹浓缩至150 μL.仪器分析前添加13C2-8:2 FTUCA(5 ng)作为进样内标.
1.4 仪器分析分析仪器为安捷伦1260液相色谱仪串联安捷伦6460三重四级杆质谱联用仪(HPLC-MS/MS, Agilent Technologies, 美国). C2~C4-PFCAs使用RSpak JJ-50 2D离子交换柱(150 mm×2 mm, 5 μm, CNW, 德国)进行分离.进样体积为10 μL, 流动相为体积比1:4的20% pH=9的50 mmol·L-1 CH3COONH4与甲醇混合溶液.流动相的流速是250 μL·min-1. C5~C12-PFCAs、PFSAs、FTCAs、FTUCAs、PFESAs、PFPEs及diPAPs使用X-terra MS C18色谱柱(150 mm×2.1 mm, 5 μm; Waters, 爱尔兰)进行分离.进样体积为10 μL.流动相分别为含2.5 mmol·L-1醋酸铵缓冲剂的Millipore水(A)和含2.5 mmol·L-1醋酸铵缓冲剂的甲醇(B).梯度洗脱:起始流动相为10%B, 0~0.8 min逐渐升至60%B, 0.8~12.8 min逐渐升至100%B, 12.8~14.3 min逐渐恢复到初始状态.质谱条件为电喷雾离子源(electrospray ionisation, ESI), 负离子化多反应监测模式(multiple reaction monitoring, MRM), 雾化器电压、温度和气流流速分别为-4 500 V、350℃和10 L·min-1, 气帘流速为8 L·min-1, 停留时间为15 ms[4].质谱的特征离子见表 1.
1.5 加标回收率向1 L的HPLC级水中加入5 ng目标化合物标准品(PFCAs、PFSAs、FTCAs、FTUCAs、PFESAs、PFPEs和diPAPs)和IS(13C-标记的C2-、C4-和C8-PFCAs、C8-PFSA、8:2 FTUCA、HFPO-DA、6:2和8:2 diPAPs、18O-标记的C6-PFSA)进行加标回收率方法实验, 分别为水样萃取前加入目标化合物标准品和IS(前加标), 水样测定前加入目标化合物标准品和IS(后加标)及水样萃取前只加IS(不加标), 每组实验设3个平行样, 目标化合物的回收率计算公式如下:
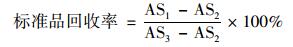
|
(1) |
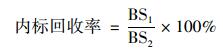
|
(2) |
式中, AS1、AS2和AS3分别为前加标、不加标和后加标组中标准品的响应面积. BS1和BS2分别为前加标和后加标组中内标的响应面积. 28种目标化合物的方法回收率在45%±15%(8:2 diPAP)~108%±13%(PFHxS)之间, 具体数值见表 2, 内标的方法回收率在36%±22%(13C3-8:2 diPAP)~116%±19%(18O2-PFHxS)之间.
|
|
表 2 目标化合物的IQLs、MQLs及回收率 Table 2 IQLs, MQLs, and recoveries of target analytes |
1.6 质量控制和质量保证
本实验器皿均采用玻璃和PP材质, 但玻璃材质容易吸附PFASs[20], 应尽可能地避免使用, 对于无法避免的玻璃材质的过滤装置应在250℃下烘烤12 h, 使用前用Millipore水和甲醇润洗内壁, 过滤后用少量Millipore水和甲醇淋洗并收集. PP材质器皿事先用甲醇与水的混合液超声30 min, 然后用甲醇溶液超声30 min, 接触样品前用甲醇淋洗内壁3次.在采样过程中设置3个野外空白, 在样品处理过程中设置3个过程空白.标准曲线的浓度梯度为0、0.5、1、2、5、10、20、50、100和200 μg·L-1, 在标准曲线浓度范围内, 线性相关系数均大于0.993.仪器定量限(instrument quantification limits, IQLs)利用3倍的信噪比确定.方法定量限(method quantification limits, MQLs)利用10倍的信噪比确定.水相及颗粒相中28种PFASs的IQLs和MQLs列于表 2. C3~C4-PFCAs、C6~C7-PFCAs和PFSAs在颗粒相及水相空白中检出, 含量(以干重计)分别为 < MQL~0.9 ng·L-1和 < MQL~0.3 ng·g-1(以干重计), C2-PFCAs在空白中检出含量较高, 分别为10 ng·L-1及7 ng·g-1, 所有实验结果为经过空白修正后再使用内标校正法进行定量分析.
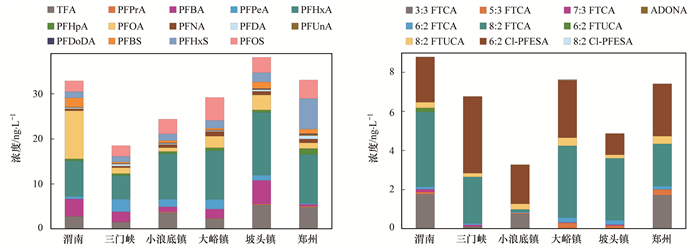
2 结果与讨论 2.1 PFASs的含量、组成及空间分布 2.1.1 水相中的PFASs水相中有24种PFASs检出, 其中TFA、PFHxA、PFOA、PFNA、PFDA、PFHxS、PFOS、8:2 FTUCA和Cl-6:2PFESA的检出率为100%. Σ28PFASs的浓度为18.4~56.9ng·L-1, 平均值为(35.8±9.51)ng·L-1(表 2). Σ28PFASs最高浓度在坡头镇(PTZ)检出[(43.0±12.2)ng·L-1]. PFHxA是水相中的主要污染物, 浓度为(9.82±3.87)ng·L-1, 占总浓度的27%(图 2), 其作为C8的替代品广泛应用于服装、地毯及家具等产品中[21, 22].新型PFASs在水相中均有检出. 6:2和8:2 Cl-PFESA的浓度分别为(2.49±1.62)ng·L-1和(0.005 19±0.011 4)ng·L-1. 6:2和8:2 Cl-PFESA是铬雾抑制剂F-53B的主要成分, 多应用于电镀行业[23].本研究中6:2 Cl-PFESA浓度与PFOA[(3.31±3.57)ng·L-1]和PFOS[(3.44±1.70)ng·L-1]的浓度处于同一水平, 由此可见, 电镀行业的兴盛和发展带来的PFASs污染问题应当引起重视[24].该河段6:2/8:2 Cl-PFESA的比值为264±98.4, 显著高于商品中两种同系物的比值(12.9±2.6)[8], 这可能与不同PFESAs在环境中的物理化学性质及环境行为的差异有关[8]. ADONA和HFPO-DA可作为全氟辛酸铵(ammonium perfluorooctanoate, APFO)的替代物用作氟聚物工业生产过程中的乳化剂[25].本研究ADONA和HFPO-DA的浓度均低于检出限, 显著低于德国阿尔兹河中ADONA的浓度[(0.32~6.2)μg·L-1][26]和我国小清河中HFPO-DA的浓度(n.d.~3.1 μg·L-1)[25], 表明流域内氟聚物工业生产过程中的乳化剂的排放处于较低水平.
|
图 2 黄河渭南—郑州段水相中PFASs的浓度和组成 Fig. 2 Concentrations and compositions of PFASs in the water phase from the Weinan-Zhengzhou section of the Yellow River |
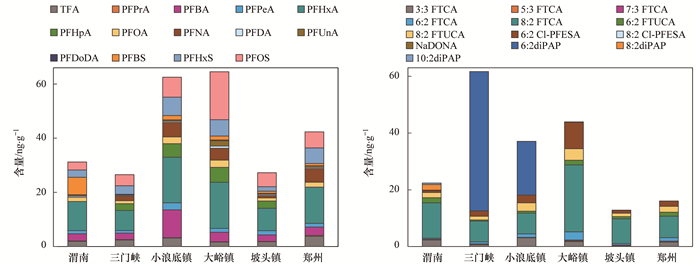
颗粒相中27种PFASs均有检出, TFA、PFPrA、PFBA、PFPeA、PFHxA、PFOA、PFUnA、PFHxS、PFOS、8:2 FTCA和8:2 FTUCA的检出率为100%. Σ28PFASs的含量(以干重计, 下同)为26.8~164 ng·g-1, 平均值为(74.7±35.9)ng·g-1(见表 2), 高于大连湾中Σ17PFASs的含量(3.5~22.2 ng·g-1)[27]. Σ28PFASs最高值在大峪镇检出(DYZ, 108±49.8 ng·g-1). DYZ位于小浪底水库中, 可能接受了上游河流的输入.河水进入库区后, 流速降低, 大粒径颗粒沉降, 颗粒物以富含有机质的小粒径悬浮颗粒物为主[28, 29], 有利于PFASs的吸附[30].
颗粒相中PFHxA是主要污染物, 含量为(12.2±7.77)ng·g-1, 占总含量的16%(图 3).前体物FTCA及一些新型PFASs在颗粒相中均有检出.大峪镇(DYZ)8:2 FTCA的含量[(23.6±5.99)ng·g-1]较高. FTCAs没有直接排放源, 来自于前体物FTOHs的降解[31, 32]. Ellis等[33]报道大气中FTOHs降解的中间产物(FTCAs等)可附着在大气颗粒上, 而后沉降到河流中, 是离子型PFASs的间接源[13].三门峡(SMX)和小浪底镇(XLDZ)检出较高含量的6:2 diPAP, 分别为(49.1±16.0)ng·g-1和(18.9±6.85)ng·g-1. diPAPs主要应用于与食品接触的纸质包装材料及润湿剂中, 在污水处理厂及纸纤维中检测到diPAPs的存在[34].分布在河南省的多家包装材料生产厂家可能是diPAP的主要污染源[35]. 6:2 Cl-PFESA和8:2 Cl-PFESA的检出含量为(2.91±3.90)ng·g-1和(0.036 3±0.110)ng·g-1. 6:2/8:2 Cl-PFESA的比值为31.4±30.5, 低于水相中的结果, 这可能是因为PFASs的疏水性随碳链长度增加而增强[8].
|
图 3 黄河渭南—郑州段段颗粒相中PFASs的含量和组成 Fig. 3 Contents and compositions of PFASs in the particle phase from the Weinan-Zhengzhou section of the Yellow River |
本研究发现黄河呼和浩特段水相中Σ7PFASs(PFHpA、PFOA、PFNA、PFDA、PFDoDA、PFHxS和PFOS)浓度为(1.8±0.15)ng·L-1, 山西境内为(4.8±1.8)ng·L-1[36], 低于本研究中相同的7种PFASs的浓度[(11.2±4.50)ng·L-1]. 2011年, Zhao等[14]分析了黄河中下游水相中的11种PFASs污染水平, 短链PFASs(PFBS、PFBA、PFPeA、PFHxA和PFHpA)和长链PFASs(PFOS、PFOA、PFNA、PFDA、PFUnA和PFDoDA)的浓度分别为44.7 ng·L-1和1.52 μg·L-1, 均高于本研究水相中相同PFASs短链[(15.3±4.84)ng·L-1]和长链[(8.05±3.56) ng·L-1]的浓度(表 3).本研究水相中PFOA浓度范围是0.459~12.7 ng·L-1[(3.32±3.67)ng·L-1], 与莱茵河PFOA的浓度处于同一水平[(4.8±1.0)ng·L-1][25], 但低于辽河(12.0 ng·L-1)[37]、海河(15 ng·L-1)[38]、长江(2.0~260 ng·L-1)[39]和多瑙河(25 ng·L-1)[40]流域中PFOA的浓度.本研究水相中PFOS浓度为1.21~6.05 ng·L-1[(3.45±1.33)ng·L-1], 显著低于黄河河口(82.30~261.8 ng·L-1)[41]和塞纳河(97 ng·L-1)[40]水相中PFOS的浓度.
|
|
表 3 水相和颗粒相中PFASs的含量 Table 3 Contents of the target compounds in the water and particle phases |
Zhao等[14]分析黄河中下游颗粒相中11种PFASs的污染水平, 短链PFASs(PFBS、PFBA、PFPeA、PFHxA和PFHpA)含量为3.44 ng·g-1, 长链PFASs(PFOS、PFOA、PFNA、PFDA、PFUnA和PFDoDA)含量为14.7 ng·g-1, 均低于本研究颗粒相中的短链[(22.3±14.8)ng·g-1]及长链[(13.1±11.7)ng·g-1]的含量.黄河渭南—郑州段颗粒相中PFOA含量范围是0.663~4.97 ng·g-1[(2.73±1.33)ng·g-1], 低于辽河(30 ng·g-1)和太湖(13 ng·g-1)[37]中PFOA的含量, 但与大连湾(1.8 ng·g-1)[27]及黄河[(2.78±1.43)ng·g-1][14]中PFOA的含量处于同一水平.本研究颗粒相中PFOS含量为1.19~33.6 ng·g-1[(7.20±7.75)ng·g-1], 高于大连湾(3.3 ng·g-1)[27]和黄河[(0.252±0.178)ng·g-1]颗粒相中PFOS的含量, 但低于太湖中PFOS的含量(23 ng·g-1)[37].
2.3 PFASs在水-颗粒相中的分配污染物在水相和颗粒相的分配系数Kd可由如下公式计算:
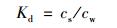
|
(3) |
式中, cs(ng·kg-1)是PFASs在颗粒相中的含量, cw(ng·L-1)是PFASs在水相中的含量. Kd(L·kg-1)为污染物在水相和颗粒相的分配系数.
由表 4可知, 水体主要PFASs的lgKd变化范围为2.95±0.553(PFPeA)~3.85±0.237(8:2 FTUCA). PFOA的lgKd值为2.89±0.524, 高于海河中PFOA的lgKd值(2.1±0.4)[38]. PFOS的lgKd值为3.21±0.363高于辽河(3.06±0.56)中PFOS的lgKd值[42]. PFOS比PFOA高0.32个lg单位, PFBS比PFBA高0.04个lg单位, 表明磺酸基团的存在是影响PFASs在颗粒物上吸附的重要因素[9]. n :3 FTCA、n:2 FTCA及n:2 FTUCA呈现随碳链长度的增加而增加的趋势. 6:2 Cl-PFESA和ADONA的lgKd值为3.03±0.488和3.23±0.659, 分别与TFA(3.01±0.538)和PFOS(3.21±0.363)的lgKd值接近. PFCAs的lgKd值没有呈现随碳链长度增加而增加的趋势, 且lgKd与lgKow值没有显著相关. PFASs在水相和颗粒相的分配受颗粒物粒径及有机碳含量的影响[42]; 水体的pH值、Ca2+、盐度、水温及电导率也会影响PFASs的分配[9].
|
|
表 4 PFASs在水和颗粒相间的lgKd和lgKow值 Table 4 The lgKd and lgKowvalues of PFASs between water and particle phase |
2.4 通量
PFASs的年通量的计算方程如下[44]:
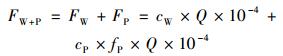
|
(4) |
式中, FW+P、FW和FP分别是水体、水相及颗粒相中PFASs的年通量(t·a-1), cW(ng·L-1)和cP(ng·g-1)是水相和颗粒相中PFASs的含量, fP(g·L-1)指颗粒物的含量, Q(亿m3)是河水年径流量[45].
由表 5可知, PFASs的年通量呈现先下降后上升的趋势.渭南[WN, (0.773±0.151)t·a-1]到三门峡[SMX, (0.573±0.128)t·a-1]的F值呈下降趋势.渭南以西河段有渭河和汾河汇入, 分别为黄河第一和第二大支流.两条河流流经陕西省和山西省, 常年接纳大量的纺织、造纸废水及城市污水[46, 47], 是水中PFASs的主要来源[48].三门峡到郑州[ZZ, (0.866±0.184)t·a-1]的F值呈上升趋势.该河段通量的增加主要来自于支流的汇入[49].洛阳市工业发达, 沿岸有消防药剂厂、污水处理厂及造纸厂等企业分布, 流经洛阳市的洛河接收PFASs并输入黄河.渭南到三门峡的PFASs通量呈现降低趋势, 这可能是由于水库阻碍了PFASs的输送, 导致部分PFASs被截留在水库段[50].水相中的PFASs通量大于颗粒相, 主要是因为PFASs多分布在溶解相[51].
|
|
表 5 黄河渭南—郑州段cw、cp、fp、Q及水相和颗粒相中PFASs的年通量 Table 5 The cw, cp, fp, Q, and the flux of PFASs in the water and particles phases in the Weinan-Zhengzhou section of the Yellow River |
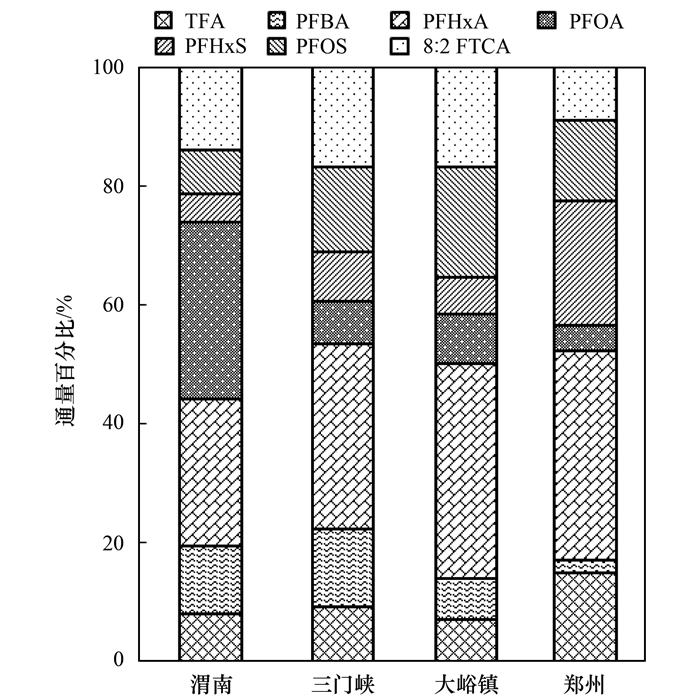
由图 4可知黄河渭南—郑州段PFASs通量以PFHxA[(0.167±0.054 4)t·a-1]为主, 高于本研究PFOA[(0.067 9±0.066 2)t·a-1]和PFOS[(0.069 9±0.029 6)t·a-1]的通量, 且高于易北河[(71±37)kg·a-1][52]和双台子河(17.9 kg·a-1)[51]的PFHxA通量. PFOA低于双台子河[(83±36)kg·a-1][51]的PFOA通量.渭南PFASs通量以PFOA(0.178 t·a-1)为主, 而其他样点均以PFHxA为主要输入污染物.
|
图 4 黄河中游7个主要的PFASs物质(水相+颗粒相)年通量的百分比 Fig. 4 Percentage of the annual flux of each site for the seven major PFASs (water+particle phase) in the middle of the Yellow River |
(1) 水相和颗粒相中Σ28PFASs的含量分别为18.4~56.9 ng·L-1和26.8~164 ng·g-1(以干重计).
(2) 水相和颗粒相中均以PFHxA为主要污染物.
(3) ADONA、PFESAs及diPAPs在颗粒相均有检出.
(4) 黄河渭南—郑州段的上游及支流对该河段PFASs的通量贡献较大.
| [1] | Ahrens L, Barber J L, Xie Z Y, et al. Longitudinal and latitudinal distribution of perfluoroalkyl compounds in the surface water of the Atlantic Ocean[J]. Environmental Science & Technology, 2009, 43(9): 3122-3127. |
| [2] | Kennedy G L, Butenhoff J L, Olsen G W, et al. The toxicology of perfluorooctanoate[J]. Critical Reviews in Toxicology, 2004, 34(4): 351-384. DOI:10.1080/10408440490464705 |
| [3] | EPA. 2010/15 PFOA stewardship program: guidance on reporting emissions and product content[R]. EPA-HQ-OPPT-2006-0621, U.S.: Office of Pollution Prevention and Toxics, Environmental Protection Agency, 2006. |
| [4] | Zhao Z, Tang J H, Mi L J, et al. Perfluoroalkyl and polyfluoroalkyl substances in the lower atmosphere and surface waters of the Chinese Bohai Sea, Yellow Sea, and Yangtze River estuary[J]. Science of the Total Environment, 2017, 599-600: 114-123. DOI:10.1016/j.scitotenv.2017.04.147 |
| [5] | Wang Y, Sun Y Z. The causes of the scientific and regulatory gap in the listing of new persistent organic pollutants into the stockholm convention[J]. Environmental Science & Technology, 2016, 50(12): 6117-6118. |
| [6] | Conder J M, Hoke R A, de Wolf W, et al. Are PFCAs bioaccumulative? A critical review and comparison with regulatory criteria and persistent lipophilic compounds[J]. Environmental Science & Technology, 2008, 42(4): 995-1003. |
| [7] | Kleszczyński K, Gardzielewski P, Mulkiewicz E, et al. Analysis of structure-cytotoxicity in vitro relationship (SAR) for perfluorinated carboxylic acids[J]. Toxicology in Vitro, 2007, 21(6): 1206-1211. DOI:10.1016/j.tiv.2007.04.020 |
| [8] | Ruan T, Lin Y F, Wang T, et al. Identification of novel polyfluorinated ether sulfonates as PFOS alternatives in municipal sewage sludge in China[J]. Environmental Science & Technology, 2015, 49(11): 6519-6527. |
| [9] | Higgins C P, Luthy R G. Sorption of perfluorinated surfactants on sediments[J]. Environmental Science & Technology, 2006, 40(23): 7251-7256. |
| [10] | Chen H, Han J B, Zhang C, et al. Occurrence and seasonal variations of per-and polyfluoroalkyl substances (PFASs) including fluorinated alternatives in rivers, drain outlets and the receiving Bohai Sea of China[J]. Environmental Pollution, 2017, 231(Pt 2): 1223-1231. |
| [11] | Chen H, Wang X M, Zhang C, et al. Occurrence and inputs of perfluoroalkyl substances (PFASs) from rivers and drain outlets to the Bohai Sea, China[J]. Environmental Pollution, 2017, 221: 234-243. DOI:10.1016/j.envpol.2016.11.070 |
| [12] | Labadie P, Chevreuil M. Partitioning behaviour of perfluorinated alkyl contaminants between water, sediment and fish in the Orge River (nearby Paris, France)[J]. Environmental Pollution, 2011, 159(2): 391-397. DOI:10.1016/j.envpol.2010.10.039 |
| [13] | Prevedouros K, Cousins I T, Buck R C, et al. Sources, fate and transport of perfluorocarboxylates[J]. Environmental Science & Technology, 2006, 40(1): 32-44. |
| [14] | Zhao P J, Xia X H, Dong J W, et al. Short-and long-chain perfluoroalkyl substances in the water, suspended particulate matter, and surface sediment of a turbid river[J]. Science of the Total Environment, 2016, 568: 57-65. DOI:10.1016/j.scitotenv.2016.05.221 |
| [15] | Zhang L L, Lee L S, Niu J F, et al. Kinetic analysis of aerobic biotransformation pathways of a perfluorooctane sulfonate (PFOS) precursor in distinctly different soils[J]. Environmental Pollution, 2017, 229: 159-167. DOI:10.1016/j.envpol.2017.05.074 |
| [16] | Pignotti E, Casas G, Llorca M, et al. Seasonal variations in the occurrence of perfluoroalkyl substances in water, sediment and fish samples from Ebro Delta (Catalonia, Spain)[J]. Science of the Total Environment, 2017, 607-608: 933-943. DOI:10.1016/j.scitotenv.2017.07.025 |
| [17] | Ding G H, Peijnenburg W J G M. Physicochemical properties and aquatic toxicity of poly-and perfluorinated compounds[J]. Critical Reviews in Environmental Science and Technology, 2013, 43(6): 598-678. DOI:10.1080/10643389.2011.627016 |
| [18] | Viers J, Dupré B, Gaillardet J. Chemical composition of suspended sediments in World Rivers:new insights from a new database[J]. Science of the Total Environment, 2009, 407(2): 853-868. DOI:10.1016/j.scitotenv.2008.09.053 |
| [19] |
刘昕宇, 冯玉君, 刘玲花, 等. 黄河重点河段水环境有毒有机物污染现状浅析[J]. 水资源保护, 2004, 20(2): 37-38, 56. Liu X Y, Feng Y J, Liu L H, et al. Current situation of toxic organism induced pollution in water environment of critical section of Yellow River[J]. Water Resources Protection, 2004, 20(2): 37-38, 56. DOI:10.3969/j.issn.1004-6933.2004.02.011 |
| [20] | Ahrens L. Polyfluoroalkyl compounds in the aquatic environment:a review of their occurrence and fate[J]. Journal of Environmental Monitoring, 2011, 13(1): 20-31. |
| [21] | Klaunig J E, Shinohara M, Iwai H, et al. Evaluation of the chronic toxicity and carcinogenicity of perfluorohexanoic acid (PFHxA) in Sprague-Dawley rats[J]. Toxicologic Pathology, 2015, 43(2): 209-220. DOI:10.1177/0192623314530532 |
| [22] | Lu Z B, Song L N, Zhao Z, et al. Occurrence and trends in concentrations of perfluoroalkyl substances (PFASs) in surface waters of eastern China[J]. Chemosphere, 2015, 119: 820-827. DOI:10.1016/j.chemosphere.2014.08.045 |
| [23] | Wang S W, Huang J, Yang Y, et al. First report of a Chinese PFOS alternative overlooked for 30 Years:its toxicity, persistence, and presence in the environment[J]. Environmental Science & Technology, 2013, 47(18): 10163-10170. |
| [24] | Zhang L, Liu J G, Hu J X, et al. The inventory of sources, environmental releases and risk assessment for perfluorooctane sulfonate in China[J]. Environmental Pollution, 2012, 165: 193-198. DOI:10.1016/j.envpol.2011.09.001 |
| [25] | Heydebreck F, Tang J H, Xie Z Y, et al. Alternative and legacy perfluoroalkyl substances:differences between european and Chinese River/Estuary systems[J]. Environmental Science & Technology, 2015, 49(14): 8386-8395. |
| [26] | Fromme H, Wöckner M, Roscher E, et al. ADONA and perfluoroalkylated substances in plasma samples of German blood donors living in South Germany[J]. International Journal of Hygiene and Environmental Health, 2017, 220(2 Pt B): 455-460. |
| [27] | Ding G H, Xue H H, Yao Z W, et al. Occurrence and distribution of perfluoroalkyl substances (PFASs) in the water dissolved phase and suspended particulate matter of the Dalian Bay, China[J]. Chemosphere, 2018, 200: 116-123. DOI:10.1016/j.chemosphere.2018.02.093 |
| [28] |
张智, 曾晓岚, 王利利, 等. 泥沙沉降对水库富营养化指标的影响[J]. 中国环境科学, 2007, 27(2): 213-216. Zhang Z, Zeng X L, Wang L L, et al. The influence of sediment subsiding on the index of the reservoir eutrophication[J]. China Environmental Science, 2007, 27(2): 213-216. DOI:10.3321/j.issn:1000-6923.2007.02.015 |
| [29] | Ran X B, Yu Z G, Yao Q Z, et al. Silica retention in the Three Gorges Reservoir[J]. Biogeochemistry, 2013, 112(1-3): 209-228. DOI:10.1007/s10533-012-9717-0 |
| [30] | Zhao X F, Zhang H J, Fan J F, et al. Dioxin-like compounds in sediments from the Daliao River Estuary of Bohai Sea:distribution and their influencing factors[J]. Marine Pollution Bulletin, 2011, 62(5): 918-925. DOI:10.1016/j.marpolbul.2011.02.054 |
| [31] | Eriksson U, Kärrman A. World-wide indoor exposure to polyfluoroalkyl phosphate esters (PAPs) and other PFASs in household dust[J]. Environmental Science & Technology, 2015, 49(24): 14503-14511. |
| [32] | Zhao L J, Folsom P W, Wolstenholme B W, et al. 6:2 Fluorotelomer alcohol biotransformation in an aerobic river sediment system[J]. Chemosphere, 2013, 90(2): 203-209. DOI:10.1016/j.chemosphere.2012.06.035 |
| [33] | Ellis D A, Martin J W, de Silva A O, et al. Degradation of fluorotelomer alcohols:a likely atmospheric source of perfluorinated carboxylic acids[J]. Environmental Science & Technology, 2004, 38(12): 3316-3321. |
| [34] | Gebbink W A, Ullah S, Sandblom O, et al. Polyfluoroalkyl phosphate esters and perfluoroalkyl carboxylic acids in target food samples and packaging-method development and screening[J]. Environmental Science and Pollution Research, 2013, 20(11): 7949-7958. DOI:10.1007/s11356-013-1596-y |
| [35] | 国家质量监督检验检疫总局.河南省食品相关产品行业生产及产品质量检测状况调研报告[EB/OL]. http://www.aqsiq.gov.cn/xxgk_13386/zxxxgk/201401/t20140110_393632.htm, 2014-01-10. |
| [36] | Wang T Y, Khim J S, Chen C L, et al. Perfluorinated compounds in surface waters from Northern China:comparison to level of industrialization[J]. Environment International, 2012, 42: 37-46. DOI:10.1016/j.envint.2011.03.023 |
| [37] | Chen X W, Zhu L Y, Pan X Y, et al. Isomeric specific partitioning behaviors of perfluoroalkyl substances in water dissolved phase, suspended particulate matters and sediments in Liao River Basin and Taihu Lake, China[J]. Water Research, 2015, 80: 235-244. DOI:10.1016/j.watres.2015.04.032 |
| [38] | Li F S, Sun H W, Hao Z N, et al. Perfluorinated compounds in Haihe River and Dagu Drainage Canal in Tianjin, China[J]. Chemosphere, 2011, 84(2): 265-271. DOI:10.1016/j.chemosphere.2011.03.060 |
| [39] | So M K, Miyake Y, Yeung W Y, et al. Perfluorinated compounds in the Pearl River and Yangtze River of China[J]. Chemosphere, 2007, 68(11): 2085-2095. DOI:10.1016/j.chemosphere.2007.02.008 |
| [40] | Loos R, Gawlik B M, Locoro G, et al. EU-wide survey of polar organic persistent pollutants in European river waters[J]. Environmental Pollution, 2009, 157(2): 561-568. DOI:10.1016/j.envpol.2008.09.020 |
| [41] | Wang S L, Wang H, Deng W J. Perfluorooctane sulfonate (PFOS) distribution and effect factors in the water and sediment of the Yellow River Estuary, China[J]. Environmental Monitoring and Assessment, 2013, 185(10): 8517-8524. DOI:10.1007/s10661-013-3192-5 |
| [42] |
陈欣维.全氟化合物支链/直链异构体在水体多界面分配行为的研究[D].天津: 南开大学, 2014. Chen X W. Distribution and partitioning behaviors of perfluoroalkyl substances and typical isomers in water[D]. Tianjin: Nankai University, 2014. |
| [43] | Hu G Z, Wang H T, Fan X G, et al. Mathematical model of coalbed gas flow with Klinkenberg effects in multi-physical fields and its analytic solution[J]. Transport in Porous Media, 2009, 76(3): 407-420. DOI:10.1007/s11242-008-9254-4 |
| [44] | Wang J Z, Guan Y F, Ni H G, et al. Polycyclic aromatic hydrocarbons in riverine runoff of the pearl river delta (China):concentrations, fluxes, and fate[J]. Environmental Science & Technology, 2007, 41(16): 5614-5619. |
| [45] | 水利部黄河水利委员会.黄河泥沙公报[EB/OL]. http://www.yellowriver.gov.cn/nishagonggao/2016/index.html#p=1, 2016. |
| [46] |
李英杰, 张振文, 王亚萍, 等. 渭河关中段水污染状况与防治对策[J]. 人民黄河, 2015, 37(6): 53-55, 59. Li Y J, Zhang Z W, Wang Y P, et al. Water pollution condition and prevention countermeasures in guanzhong section of weihe river[J]. Yellow River, 2015, 37(6): 53-55, 59. DOI:10.3969/j.issn.1000-1379.2015.06.014 |
| [47] | 张引栓. 汾河运城段水质评价及排污口排放标准分析[J]. 人民黄河, 2010, 32(7): 54-55. DOI:10.3969/j.issn.1000-1379.2010.07.023 |
| [48] |
陈清武, 张鸿, 柴之芳, 等. 深圳市沿岸表层海水中全氟化合物的残留特征及其分布规律[J]. 环境科学, 2012, 33(6): 1795-1800. Chen Q W, Zhang H, Chai Z F, et al. Residue characteristics and distributions of perfluorinated compounds in surface seawater along Shenzhen coastline[J]. Environmental Science, 2012, 33(6): 1795-1800. |
| [49] |
王丽伟, 樊引琴, 王霞, 等. 黄河三门峡至高村河段入河排污状况调查研究[J]. 人民黄河, 2007, 29(12): 45-46. Wang L W, Fan Y Q, Wang X, et al. Survey and study on unloading status of sanmenxia-gaocun section of the Yellow River[J]. Yellow River, 2007, 29(12): 45-46. DOI:10.3969/j.issn.1000-1379.2007.12.022 |
| [50] | Devault D A, Gérino M, Laplanche C, et al. Herbicide accumulation and evolution in reservoir sediments[J]. Science of the Total Environment, 2009, 407(8): 2659-2665. DOI:10.1016/j.scitotenv.2008.12.064 |
| [51] | Shao M H, Ding G H, Zhang J, et al. Occurrence and distribution of perfluoroalkyl substances (PFASs) in surface water and bottom water of the Shuangtaizi Estuary, China[J]. Environmental Pollution, 2016, 216: 675-681. DOI:10.1016/j.envpol.2016.06.031 |
| [52] | Zhao Z, Xie Z Y, Tang J H, et al. Seasonal variations and spatial distributions of perfluoroalkyl substances in the rivers Elbe and lower Weser and the North Sea[J]. Chemosphere, 2015, 129: 118-125. DOI:10.1016/j.chemosphere.2014.03.050 |
 2019, Vol. 40
2019, Vol. 40


