2. 中国科学院陆地表层格局与模拟重点实验室, 北京 100101;
3. 中国科学院大学, 北京 100049;
4. 南昌大学资源环境与化工学院, 南昌 330038
2. Key Laboratory of Land Surface Pattern and Simulation, Chinese Academy of Sciences, Beijing 100101, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. School of Resources Environmental & Chemical Engineering, Nanchang University, Nanchang 330038, China
石油化工、焦化煤气等工业企业活动遗留大量有机污染场地, 往往具有污染物种类复杂、污染面积大、污染程度深、修复困难等特点, 对人体健康和生态环境造成严重威胁[1, 2].复合有机污染场地中的典型污染物主要包括多环芳烃(polycyclic aromatic hydrocarbons, PAHs)、石油烃、苯系物和含氯有机物等[3, 4].其中, 多环芳烃是一类含有两个或两个以上苯环的碳氢化合物, 具有高毒、致癌和持久性等特点, 美国环保署和欧盟均将其列为优先污染物[5].而石油烃是由链烷烃、环烷烃和芳香烃等各种碳氢化合物组成的复杂混合物, 一定程度上能引起癌变, 在我国48种危险废物中位于前列[6].因此, 针对工矿场地及其周边的复合有机污染土壤研发高效的修复技术成为国内外学者研究的热点.
化学氧化修复技术是当前有机污染场地修复中应用最广泛的修复技术之一, 具有反应强度大、适用范围广、修复效率高、反应迅速等特点[7].其中, 活化过硫酸盐是近来发展起来的一种新型氧化技术, 其氧化还原电位高、在土体中存留时间长、稳定性强, 受到国内外学者的广泛关注[8, 9].过硫酸盐常见的活化方式具体包括热活化、过渡金属离子活化、紫外光活化、碱活化等[10].其中, 亚铁离子是应用最广泛的过渡金属离子活化剂, 其通常与螯合剂柠檬酸联用以实现过硫酸盐的持续活化[11].近年来还出现了一些新型、高效的过硫酸盐活化技术, 具体包括含铁活化材料(如零价铁、铁基双金属材料、铁复合材料)、含碳活化材料(如活性炭、糖类)和含醌活化材料(如腐殖酸)[12~14].其中, 含碳物质(如糖类)和含醌天然有机物(如腐殖酸)等大分子材料因具有节能、廉价和环境友好等优势, 具有广泛的应用前景[13, 14].
本研究以多环芳烃、石油烃典型复合有机污染土壤为对象, 基于前人的研究[15]选取了合适的氧化剂剂量和活化剂配比开展过硫酸盐氧化修复实验, 重点比较和分析了固定氧化剂、活化剂浓度下不同活化过硫酸盐体系(糖类、腐殖酸联合亚铁离子、柠檬酸螯合铁等)对土壤有机污染物的降解效果、氧化机制和稳定程度, 以期为复合有机污染场地的实际修复工程提供理论参考和科学依据.
1 材料与方法 1.1 供试土壤供试土壤采自南京某煤制气厂(118°50′47.59″E, 32°6′57.73″N), 采样深度0~50 cm.采样后去除土壤表面覆盖物及石块、植物残根等, 将土样置于室温条件下风干, 混匀后放入密封的自封袋, 待用.经测定, 土壤密度为1.76 g·cm-3, 孔隙率为48.1%, 含水率为18.05%, 渗透系数为8.09×10-7 cm·s-1.土壤中总石油烃(total petroleum hydrocarbons, TPHs)含量为17.45 mg·g-1, 总多环芳烃含量为196.34 mg·kg-1.
1.2 实验试剂PAHs标准品购于国家标准物质中心; 过硫酸钠、柠檬酸、腐殖酸、葡萄糖、蔗糖和可溶性淀粉、硫酸亚铁、无水硫酸钠、硅胶均为分析纯, 正己烷、二氯甲烷等溶剂为色谱纯试剂, 购于国药集团化学试剂北京有限公司.
1.3 过硫酸盐活化方法筛选实验取800 g污染土壤置于2 L的烧杯中, 水土比设置为0.6:1.实验共设置8个处理, 氧化剂为过硫酸钠, 活化剂包括单聚糖(葡萄糖)、双聚糖(蔗糖)和多聚糖(可溶性淀粉)、腐殖酸、硫酸亚铁和柠檬酸6种, 每个处理3个重复, 具体见表 1.按实验各处理中设定量加入去离子水使其充分搅拌均匀, 再按设定量缓慢加入氧化剂和活化剂, 在25℃、400 r·min-1条件下搅拌20 min, 停止搅拌后对处理后土壤进行养护, 并于搅拌后0、1、2、4、8、16 d时采集土壤样品, 冷冻干燥后待测土壤中的TPHs和PAHs含量.土壤理化性质于0、2、4、8、12、16、24 h和2、4、8、12、16 d时进行采样测定.
|
|
表 1 实验处理 Table 1 Experimental treatments |
1.4 分析方法
土壤中的TPHs采用紫外分光光度法进行测定.取0.5 g土壤样品装入10 mL顶空瓶中, 加入5 mL二氯甲烷, 用压盖器压紧密封, 置于恒温水浴振荡器中, 20℃, 150 r·min-1下振荡30 min后, 静置, 直接移取上清液或取一定量在比色管中稀释至10 mL, 以紫外分光光度计在229 nm处测定吸光度, 代入标准曲线确定土壤中的TPHs含量(mg·g-1)[16].标准曲线的制作:准确称取0.5 g柴油(0号)置于100 mL容量瓶中, 加入二氯甲烷溶解并稀释, 得到5000 mg·L-1的柴油溶液.用移液管准确移取1 mL此溶液于100 mL容量瓶中定容, 得到50 mg·L-1的标准油品. 7个10 mL的具塞比色管中分别加入1、2、3、4、5、6、8 mL前面配制的50 mg·L-1的标准油, 用二氯甲烷稀释至10 mL标线, 得到5、10、15、20、25、30、40 mg·L-1的系列油标准溶液.在最大吸收波长229 nm处, 用10 mm石英比色皿, 以二氯甲烷为空白测定其吸光度, 经空白校正后, 以吸光度-含量做线性回归, 得到标准曲线.实验所用紫外可见光分光光度计购于尤尼柯(上海)仪器有限公司, 型号UV-2800/2802/2802S.
土壤中的PAHs(包括NAP、ANY、ANE、FLE、PHE、ANT、FLA、PYR、BaA、CHR、BbF、BkF、BaP、DahA、IcdP和BghiP16种美国环保署列为优先检测污染物的多环芳烃)采用超声萃取法进行提取.土样经冷冻干燥后, 取2 g, 加10 mL二氯甲烷, 超声提取1 h, 离心, 取2 mL上清液过硅胶柱, 收集洗脱液, 在旋转蒸发仪上蒸至约0.5 mL, 用正己烷定容至1 mL待测[10]. PAHs采用GC-MS(Agilent6890)进行测定.分析条件: HP-5MS 30 m×0.25 mm毛细色谱柱, 载气为氦气, 柱前压0.03 MPa, 线速度37 cm·s-1, 进样口温度300℃, 初始温度60℃, 以5℃·min-1速度升至300℃, 保留20 min至样品完全流出.
土壤pH、Eh直接使用pH、Eh计进行测定.
1.5 质量保证和质量控制现场空白和试剂空白: TPHs和PAHs测试过程中, 每12个样品加一个现场空白样品和一个试剂空白样品, 所有空白样品中均无目标化合物检出.
重现性实验和仪器校正: TPHs检测时, 每2个样品检测前均用空白试剂调零. PAHs上机测定时, 每运行12针样品, 加一针250 ng·mL-1的含有18种目标物(16种多环芳烃和2种替代标准物)的混合标样, 并对仪器进行一次质量校正, 分析完所有样品后, 标准样品定量结果的相对偏差范围为0.45%~1.79%, 说明仪器具有良好的重现性, 测试的数据较为准确.
回收率: TPHs采用标准柴油作基质回收率标准, 在加标水平为250 mg·kg-1时, 基质加标回收率为88.3%~110.9%. PAHs采用对三联苯-d14和2-氟联苯标准品作回收率替代标准, 在加标水平为250 μg·kg-1时, 替代标准的回收率均在66.2%~115.9%范围内.最终结果经回收率校正.
平行性:所有平行处理中污染物含量的相对偏差均小于15%.
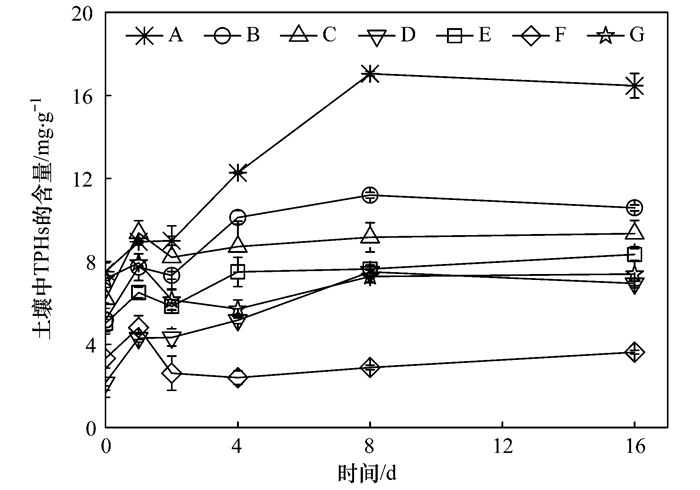
2 结果与分析 2.1 不同过硫酸盐活化系统对土壤中总石油烃的降解效果不同过硫酸盐活化处理后土壤中总石油烃的含量变化如图 1所示.从中可知, 在搅拌结束0 h时不同处理后土壤中TPHs的含量从大到小依次为: CK(A)>柠檬酸螯合铁活化(G)>双糖活化(C)>单糖活化(B)>多糖加亚铁离子活化(E)>腐殖酸加亚铁离子活化(F)>多糖活化(D).其中, 多糖活化过硫酸钠对TPHs的降解效果最佳, 土壤中TPHs的残留含量仅为2.17 mg·g-1, 去除率可达87.56%;腐殖酸联合亚铁离子活化过硫酸盐降解效果次之, 土壤中TPHs的残留含量仅为3.32 mg·g-1, 去除率可达80.97%.比较氧化处理后不同时间下土壤中TPHs含量变化发现, 过硫酸盐氧化降解后土壤中TPHs含量均发生一定程度的反弹现象, 并于反应结束的第8 d逐渐趋于平稳.其中, 腐殖酸联合亚铁离子活化过硫酸盐处理的TPHs反弹现象最小, 氧化后土壤中残留的TPHs含量最低, 为3.63 mg·g-1, 柠檬酸螯合铁处理的反弹也较弱, TPHs的残留含量为7.39 mg·g-1.多糖、多糖联合亚铁离子、双糖、单糖这4种活化处理下土壤中TPHs含量变化规律相似, 呈现先增加后稳定的趋势, 截至反应后16 d, 土壤中残留TPHs含量分别为6.94、8.33、9.34和10.58 mg·g-1.而CK处理反弹幅度最大, TPHs含量从7.51 mg·g-1升至16.47 mg·g-1.
|
图 1 不同过硫酸盐活化处理后土壤中TPHs的含量变化 Fig. 1 Content of TPHs in soils treated with different activated persulfate |
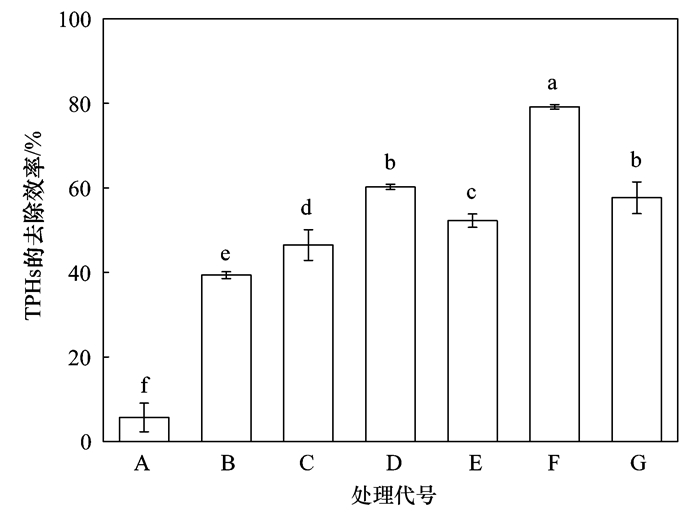
16 d时不同过硫酸盐活化处理后土壤中TPHs的去除率见图 2.腐殖酸联合亚铁离子活化过硫酸盐(F)对TPHs的氧化降解效果最好, 可达79.21%.多糖活化过硫酸盐(D)和柠檬酸螯合铁活化过硫酸盐(G)氧化效果相近, 分别为60.23%和57.66%.多糖加亚铁离子活化过硫酸盐(E)降解效果次之, 土壤中TPHs去除率为52.25%.而双糖(C)和单糖(B)活化过硫酸盐的降解效果较差, TPHs去除率在39.37%~46.47%之间. CK对照组(A)中TPHs氧化降解效果最差, 仅为5.66%.
|
小写字母表示各处理去除率间的显著性差异(P < 0.05), 两处理字母相同代表两个处理的去除率无显著性差异, 字母不同代表两个处理的去除率达到显著性差异 图 2 第16 d不同过硫酸盐活化处理后土壤中TPHs的去除率 Fig. 2 Removal efficiency of TPHs in soils treated with different activated persulfate in 16 d |
不同过硫酸盐活化处理后, 土壤中多环芳烃的残留含量及去除率如表 2所示.从中可知, 土壤中PAHs去除率由大到小依次为:腐殖酸联合亚铁离子活化(F)>多糖活化(D)>柠檬酸螯合铁活化(G)>多糖加亚铁离子活化(E)>双糖活化(C)>单糖活化(B)>CK对照组(A).各处理下, 土壤中PAHs的去除率在19.90%~79.89%之间.其中, 腐殖酸联合亚铁离子活化过硫酸盐处理后PAHs降解效率最高, 土壤中接近80%PAHs已被去除, 残留含量仅为39.49 mg·kg-1±4.73 mg·kg-1.
|
|
表 2 不同过硫酸盐活化处理后土壤中多环芳烃的残留含量及去除率1) Table 2 Residual content and removal efficiency of PAHs in soils treated with different activated persulfate |
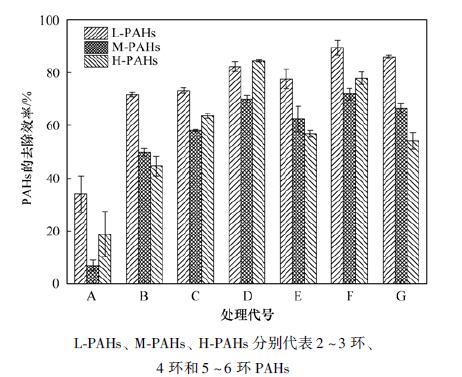
不同过硫酸盐活化处理对土壤中16种多环芳烃的去除率如图 3所示.从中可知, 不同环数多环芳烃降解效果基本呈现出低环>中环>高环的趋势.不同过硫酸盐活化系统对土壤中低环多环芳烃(low-ring PAHs, L-PAHs)均表现出较高的氧化效果, 去除率在34.04%~89.42%之间.其中, 腐殖酸联合亚铁离子活化过硫酸盐(F)对L-PAHs降解效率最高, 接近90%.比较土壤中中环多环芳烃(middle-ring PAHs, M-PAHs)的降解规律可知, 腐殖酸联合亚铁离子活化过硫酸盐(F)和多糖活化过硫酸盐(D)能够有效降解土壤中的M-PAHs, 去除率分别达71.88%和69.94%, 其他氧化处理M-PAHs的降解效率在6.94%~66.46%之间.对于难降解的高环多环芳烃(high-ring PAHs, H-PAHs)而言, 多糖活化过硫酸盐(D)表现出最佳的氧化效果, H-PAHs去除率可达84.37%, 腐殖酸联合亚铁离子活化过硫酸盐(F)次之, 能够去除土壤中77.96%的H-PAHs, 其他氧化处理下H-PAHs的降解效率在18.86%~63.59%之间.综上所述, 腐殖酸联合亚铁离子活化过硫酸盐系统和多糖活化过硫酸盐系统能够有效降解土壤中的PAHs.
|
图 3 不同过硫酸盐活化处理后土壤中低环、中环和高环多环芳烃的去除效果 Fig. 3 Removal efficiency of L-PAHs, M-PAHs and H-PAHs in soils treated with different activated persulfate |
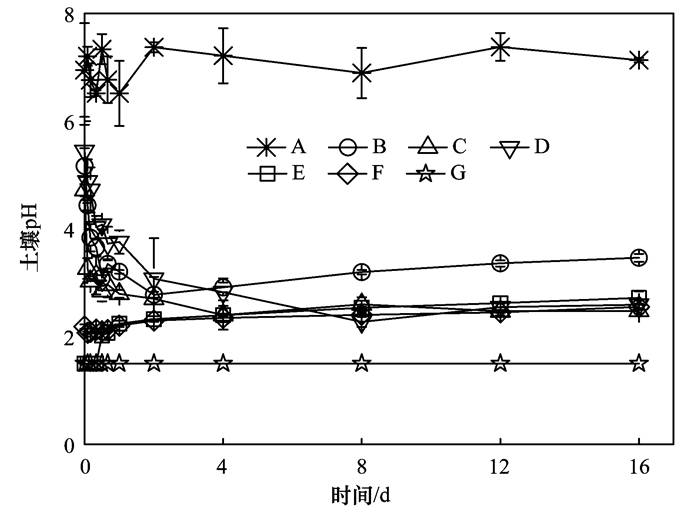
不同过硫酸盐活化系统氧化后土壤pH随时间的变化如图 4所示.从中可知, 土壤自身的pH为7.01, 而不同过硫酸盐活化处理后土壤pH均呈现酸性.其中, 柠檬酸螯合铁活化(G)处理后土壤的酸性最大, pH约为1.50, 而其他处理后土壤的pH均在2~4之间.从pH的变化上看, 不同糖类处理后pH在前期的波动性较大, 随后趋向平稳, 而其他处理后土壤pH均较为稳定.
|
图 4 不同过硫酸盐活化系统氧化后土壤中pH随时间的变化 Fig. 4 The pH in soils treated with different activated persulfate |
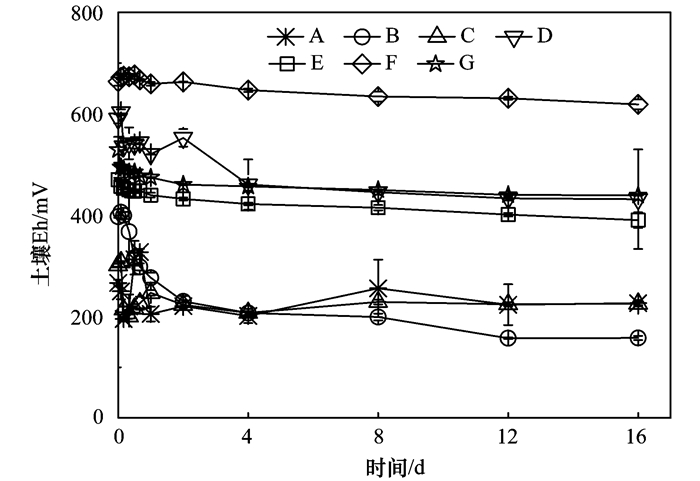
不同过硫酸盐活化系统氧化后土壤Eh变化情况差异显著, 如图 5所示.不同处理后土壤Eh从大到小依次为:腐殖酸加亚铁离子活化(F)>柠檬酸螯合铁活化(G)>多糖活化(D)>多糖加亚铁离子活化(E)>CK(A)>双糖活化(C)>单糖活化(B).其中, 腐殖酸联合亚铁离子活化(F)处理后土壤中的Eh最高, 可达676.27 mV.多糖活化(D)、多糖联合亚铁离子活化(E)和柠檬酸螯合铁活化(G)处理后Eh接近, 在390.07~438.97 mV之间.单糖活化(B)、双糖活化(C)和CK对照组(A)处理后土壤中的Eh较低, 在157.73~226.37 mV范围内.从Eh总体变化趋势来看, 糖类物质活化过硫酸盐处理后, 土壤Eh在前期波动较大, 随后趋于稳定, 而腐殖酸、多糖和柠檬酸等物质联合亚铁离子活化过硫酸盐等系统中, 土壤Eh均较为稳定.
|
图 5 不同过硫酸盐活化系统氧化后土壤中Eh随时间的变化 Fig. 5 Eh in soils treated with different activated persulfate |
不同方式活化过硫酸盐处理后土壤中的TPHs在后期均发生一定程度的含量反弹现象, 这与前人的研究结果相吻合[17]. Mcguire等[18]在长年监测59个修复后的氯代烃污染场地时发现, 多数场地发生了污染物含量回升, 有7个场地的污染物降解率从修复完成后的90%下降到1 a后的78%.这种现象的出现可能是由于修复后残留在土壤中难解吸污染物的缓慢质移造成的, 也可能是源于污染物在含水层中的缓慢平流传输等.此外, 氧化剂通常会氧化土壤中的天然有机质, 而天然有机质的氧化会导致吸附态污染物的释放, 进而导致污染物的反弹[19].本研究结果显示, 腐殖酸联合亚铁离子活化过硫酸盐处理后土壤中石油烃的反弹含量最小, 降解效果最稳定, 表明该体系对TPHs能实现较好的精准修复.
不同过硫酸盐活化系统氧化降解土壤有机污染物效果差异显著.本研究中, 腐殖酸联合亚铁离子活化系统和多糖活化系统是最有效的两种活化方式, 尤其对于疏水性强、难降解的石油烃及高环PAHs, 获得较高的去除效率.其中, 腐殖酸联合亚铁离子活化过硫酸盐对污染土壤中的TPHs和PAHs去除率接近80%, 多糖活化过硫酸盐系统对TPHs和PAHs的去除率分别达到60%和78%, 优于柠檬酸螯合铁活化过硫酸盐降解效果(58% TPHs和71% PAHs).而先前部分研究表明, TPHs和PAHs类有机污染物难以氧化降解.吴昊等[20]的研究显示, 柠檬酸螯合铁活化、碱活化、过氧化氢活化和热活化处理仅分别去除土壤中35.4%~40.8%、21.4%~35.2%、20%和0.1%~15.6%的TPHs. Yen等[21]的研究中指出, 在420 mmol·g-1过硫酸盐的剂量下, 亚铁离子活化处理仅降解土壤中55%的TPHs.吉红军等[22]的研究也表明, 柠檬酸螯合铁活化过硫酸盐(0.5 mmol·g-1)仅对土壤中的PAHs实现了65%的去除效率.各活化系统对低环多环芳烃的降解效果显著优于中、高环多环芳烃, 这是因为高环多环芳烃水溶性差、辛醇-水分配系数高、苯环数量多、结构复杂, 极难被氧化降解[15, 23].土壤中Eh能够显著影响反应系统中产生的自由基数量及土壤中污染物的降解效果, 反应体系Eh越高, 氧化活性越强, 污染物去除效果越显著[24].本研究中, 腐殖酸联合亚铁离子活化处理后土壤中的Eh最高, 多糖次之, 这与污染物氧化降解规律一致.过硫酸盐氧化后土壤中的pH显著降低, 这是因为在过硫酸盐氧化有机物的过程中, 向环境中加入了SO42-和H+, 导致土壤的pH下降.李鸿炫等[25]的研究发现, 过硫酸盐氧化后土壤的pH从6.04下降到2.56. Huang等[26]的研究也表明, 过硫酸盐氧化后含水层会酸化, pH会降低2.8~6个单位.但相比于柠檬酸螯合铁活化系统, 腐殖酸联合亚铁离子活化及糖类活化处理后土壤的酸性相对较弱, 在一定程度上提高了修复后土壤的安全性.
腐殖酸联合亚铁离子能够有效活化过硫酸盐促进污染物的降解, 这与前人的研究结果相吻合. Fang等[13]在研究腐殖酸活化过硫酸盐机制时发现, 醌类是腐殖酸中活化过硫酸盐的重要部分, 其研究还表明, 苯醌/过硫酸盐的系统中2, 4, 4′-三氯联苯(PCB28)的降解效率可以达到88%, 而单一的过硫酸盐与苯醌(BQ)系统中污染物的降解率分别只有20%与9%. Leng等[14]在研究含醌结构物质活化过硫酸盐时也发现, 随着聚苯乙烯基氢醌的加入, 罗丹明B的降解速率从0.0091 min-1明显上升到了0.0219 min-1, 其研究还发现, 醌类物质的存在成功建立起了Fe(Ⅲ)/Fe(Ⅱ)的循环和半醌(SQ)/醌的循环, 两个循环促使系统产生了更多的Fe(Ⅱ)与SO4·-, 继而提高了污染物的降解率.腐殖酸内含有醌类基团, 能够在Fe2+存在条件下加速生成醌基自由基, 以活化过硫酸盐释放SO4·-和·OH, 进而分解土壤中的疏水性有机污染物[13, 27, 28].同时, 腐殖酸中含有抗氧化特性的酚类基团, 能够减缓腐殖酸中其他基团的氧化转换, 以增加它们在氧化环境中的抗性, 降低活化剂与污染物竞争消耗氧化剂的能力[29, 30].
糖类物质能够促进过硫酸盐对有机污染物的降解, 该结论在相关研究报告中也有验证(未发表), 其指出, 当糖类(CH)与过硫酸盐(SP)摩尔比为0.003:1时即可显著增强过硫酸盐的活化效果及降解效率.而在糖类物质中, 多糖活化过硫酸盐降解效果显著优于单糖和双糖, 这可能是因为多糖具有抗氧化性, 不会与污染物竞争消耗氧化剂[31], 而单糖和双糖极性更强, 不利于有机污染物的增溶与洗脱[32].多糖加亚铁离子活化系统中污染物的去除效果低于多糖直接活化过硫酸盐系统, 这可能是由于多糖不具备螯合亚铁离子的作用, 使系统中的亚铁离子与污染物发生自由基的竞争消耗, 从而导致效率降低[11].
4 结论腐殖酸联合亚铁离子活化过硫酸盐降解土壤中总石油烃和多环芳烃的效果最好, 处理后石油烃的反弹含量最小, 氧化效果最稳定.腐殖酸联合亚铁离子活化和多糖活化过硫酸盐对难降解的高环多环芳烃去除效果最佳, 各处理后土壤Eh以腐殖酸联合亚铁离子活化过硫酸盐最高, 多糖处理次之, 表明大分子材料活化过硫酸盐系统的氧化性能更好.相比于柠檬酸螯合铁活化过硫酸盐系统, 腐殖酸联合亚铁离子活化过硫酸盐系统处理后土壤酸性较弱, 土壤氧化的安全性得到一定提高.
| [1] |
马妍, 董彬彬, 杜晓明, 等. 挥发及半挥发性有机物污染场地异位修复技术的二次污染及其防治[J]. 环境工程, 2017, 35(4): 174-178. Ma Y, Dong B B, Du X M, et al. Secondary pollution and its prevention of VOC/SVOC-contaminated sites with ex situ remediation technologies[J]. Environmental Engineering, 2017, 35(4): 174-178. |
| [2] |
杨宾, 李慧颖, 伍斌, 等. 污染场地中挥发性有机污染工程修复技术及应用[J]. 环境工程技术学报, 2013, 3(1): 78-84. Yang B, Li H Y, Wu B, et al. Engineering remediation techniques and its application for volatile organic compounds-contaminated sites[J]. Journal of Environmental Engineering Technology, 2013, 3(1): 78-84. DOI:10.3969/j.issn.1674-991X.2013.01.014 |
| [3] |
金鑫, 林玉锁, 徐建, 等. 某有机废弃场地土壤化学分析与生态毒性诊断研究[J]. 农业环境科学学报, 2008, 27(6): 2216-2221. Jin X, Lin Y S, Xu J, et al. Chemical analysis and eco-toxicity diagnosis on organics contaminated soil from an abandoned site[J]. Journal of Agro-Environment Science, 2008, 27(6): 2216-2221. DOI:10.3321/j.issn:1672-2043.2008.06.016 |
| [4] |
付高阳, 谯华, 彭伟, 等. 溶解性有机质对土壤中典型有机污染物迁移转化的影响[J]. 化学与生物工程, 2016, 33(7): 61-63, 67. Fu G Y, Qiao H, Peng W, et al. Effect of dissolved organic matters on migration and transformation of typical organic pollutants in soil[J]. Chemistry & Bioengineering, 2016, 33(7): 61-63, 67. DOI:10.3969/j.issn.1672-5425.2016.07.015 |
| [5] | Domingo J L, Nadal M. Human dietary exposure to polycyclic aromatic hydrocarbons:A review of the scientific literature[J]. Food and Chemical Toxicology, 2015, 86: 144-153. DOI:10.1016/j.fct.2015.10.002 |
| [6] | Wu H, Sun L N, Wang H, et al. Persulfate oxidation for the remediation of petroleum hydrocarbon-contaminated soils[J]. Polish Journal of Environmental Studies, 2016, 25(2): 851-857. DOI:10.15244/pjoes/60857 |
| [7] | Huling S. In situ chemical oxidation[R]. Washington, DC: US EPA, 2006. |
| [8] | Ranc B, Faure P, Croze V, et al. Selection of oxidant doses for in situ chemical oxidation of soils contaminated by polycyclic aromatic hydrocarbons (PAHs):A review[J]. Journal of Hazardous Materials, 2016, 312: 280-297. DOI:10.1016/j.jhazmat.2016.03.068 |
| [9] | Wang J L, Wang S Z. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants[J]. Chemical Engineering Journal, 2018, 334: 1502-1517. DOI:10.1016/j.cej.2017.11.059 |
| [10] | Zhao D, Liao X Y, Yan X L, et al. Effect and mechanism of persulfate activated by different methods for PAHs removal in soil[J]. Journal of Hazardous Materials, 2013, 254-255: 228-235. DOI:10.1016/j.jhazmat.2013.03.056 |
| [11] | Matzek L W, Carter K E. Activated persulfate for organic chemical degradation:A review[J]. Chemosphere, 2016, 151: 178-188. DOI:10.1016/j.chemosphere.2016.02.055 |
| [12] | Li H X, Wan J Q, Ma Y W, et al. Influence of particle size of zero-valent iron and dissolved silica on the reactivity of activated persulfate for degradation of acid orange 7[J]. Chemical Engineering Journal, 2014, 237: 487-496. DOI:10.1016/j.cej.2013.10.035 |
| [13] | Fang G D, Gao J, Dionysiou D D, et al. Activation of persulfate by quinones:Free radical reactions and implication for the degradation of PCBs[J]. Environmental Science & Technology, 2013, 47(9): 4605-4611. |
| [14] | Leng Y Q, Guo W L, Shi X, et al. Degradation of Rhodamine B by persulfate activated with Fe3O4:Effect of polyhydroquinone serving as an electron shuttle[J]. Chemical Engineering Journal, 2014, 240: 338-343. DOI:10.1016/j.cej.2013.11.090 |
| [15] |
赵丹, 阎秀兰, 廖晓勇, 等. 不同化学氧化剂对焦化污染场地苯系物的修复效果[J]. 环境科学, 2011, 32(3): 849-856. Zhao D, Yan X L, Liao X Y, et al. Chemical oxidants for remediation of BTEX-contaminated soils at coking sites[J]. Environmental Science, 2011, 32(3): 849-856. |
| [16] |
蒋瑞萍, 孙丽丽, 解开治, 等. 采用紫外分光光度法评价石油烃降解菌的降解能力[J]. 石化技术与应用, 2015, 33(1): 70-74. Jiang R P, Sun L L, Xie K Z, et al. Evaluation of degrading ability of petroleum hydrocarbon degrading bacteria by ultraviolet spectrophotometry[J]. Petrochemical Technology & Application, 2015, 33(1): 70-74. DOI:10.3969/j.issn.1009-0045.2015.01.017 |
| [17] | Mundle K, Reynolds D A, West M R, et al. Concentration rebound following in situ chemical oxidation in fractured clay[J]. Ground Water, 2007, 45(6): 692-702. DOI:10.1111/gwat.2007.45.issue-6 |
| [18] | Mcguire T M, Mcdade J M, Newell C J. Performance of DNAPL source depletion technologies at 59 chlorinated solvent-impacted sites[J]. Ground Water Monitoring & Remediation, 2006, 26(1): 73-84. |
| [19] | Liang C J, Bruell C J, Marley M C, et al. Thermally activated persulfate oxidation of trichloroethylene (TCE) and 1, 1, 1-trichloroethane (TCA) in aqueous systems and soil slurries[J]. Soil and Sediment Contamination:An International Journal, 2003, 12(2): 207-228. DOI:10.1080/713610970 |
| [20] |
吴昊, 孙丽娜, 李玉双, 等. 活化过硫酸钠去除长期污染土壤中的TPH[J]. 环境工程学报, 2016, 10(9): 5231-5237. Wu H, Sun L N, Li Y S, et al. Application of persulfate to remediatiate long-term TPH contaminated soils[J]. Chinese Journal of Environmental Engineering, 2016, 10(9): 5231-5237. |
| [21] | Yen C H, Chen K F, Kao C M, et al. Application of persulfate to remediate petroleum hydrocarbon-contaminated soil:Feasibility and comparison with common oxidants[J]. Journal of Hazardous Materials, 2011, 186(2-3): 2097-2102. DOI:10.1016/j.jhazmat.2010.12.129 |
| [22] |
吉红军, 龙涛, 陈墙, 等. Tween 80强化-活化过硫酸钠氧化修复多环芳烃污染土壤[J]. 化工学报, 2016, 67(9): 3879-3887. Ji H J, Long T, Chen Q, et al. Tween 80 enhanced-activated sodium persulfate oxidation of PAHs contaminated soil[J]. CIESC Jorunal, 2016, 67(9): 3879-3887. |
| [23] | de Souza e Silva P T, da Silva V L, de Barros Neto B, et al. Potassium permanganate oxidation of phenanthrene and pyrene in contaminated soils[J]. Journal of Hazardous Materials, 2009, 168(2-3): 1269-1273. DOI:10.1016/j.jhazmat.2009.03.007 |
| [24] | 赵丹.过硫酸盐氧化修复多环芳烃污染场地的关键机理及其生态环境风险[D].北京: 中国科学院大学, 2013. |
| [25] |
李鸿炫, 胡金星, 林伟, 等. 重金属-有毒有机物复合污染土壤的过硫酸盐氧化修复模拟研究[J]. 环境科学学报, 2017, 37(9): 3553-3560. Li H X, Hu J X, Lin W, et al. Remediation of soils contaminated with heavy metals and toxic organic pollutants by persulfate oxidation:A lab-scale study[J]. Acta Scientiae Circumstantiae, 2017, 37(9): 3553-3560. |
| [26] | Huang K C, Zhao Z Q, Hoag G E, et al. Degradation of volatile organic compounds with thermally activated persulfate oxidation[J]. Chemosphere, 2005, 61(4): 551-560. DOI:10.1016/j.chemosphere.2005.02.032 |
| [27] | Ma J H, Song W J, Chen C C, et al. Fenton Degradation of organic compounds promoted by dyes under visible irradiation[J]. Environmental Science & Technology, 2005, 39(15): 5810-5815. |
| [28] | Duesterberg C K, Waite T D. Kinetic modeling of the oxidation of p-Hydroxybenzoic acid by Fenton's reagent:Implications of the role of quinones in the redox cycling of iron[J]. Environmental Science & Technology, 2007, 41(11): 4103-4110. |
| [29] | Rimmer D L, Smith A M. Antioxidants in soil organic matter and in associated plant materials[J]. European Journal of Soil Science, 2009, 60(2): 170-175. DOI:10.1111/ejs.2009.60.issue-2 |
| [30] | Rimmer D L, Abbott G D. Phenolic compounds in NaOH extracts of UK soils and their contribution to antioxidant capacity[J]. European Journal of Soil Science, 2011, 62(2): 285-294. DOI:10.1111/ejs.2011.62.issue-2 |
| [31] |
周林珠, 杨祥良, 周井炎, 等. 多糖抗氧化作用研究进展[J]. 中国生化药物杂志, 2002, 23(4): 210-212. Zhou L Z, Yang X L, Zhou J Y, et al. Advances of the antioxidative activities research of polysaccharides[J]. Chinese Journal of Biochemical Pharmaceutics, 2002, 23(4): 210-212. DOI:10.3969/j.issn.1005-1678.2002.04.028 |
| [32] | Kang S, Xing B S. Phenanthrene sorption to sequentially extracted soil humic acids and humins[J]. Environmental Science & Technology, 2005, 39(1): 134-140. |
 2018, Vol. 39
2018, Vol. 39


