2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
磷(P)通常是海洋初级生产的限制性营养元素, 影响海洋浮游植物生长、群落结构和生物固氮能力[1, 2].大气沉降是海洋外源性P的重要来源, 尽管在全球尺度上河流输入海洋的P通量高于大气沉降[3], 但河流输入影响的区域有限, 在河口以外的海域、尤其是开阔大洋, 海洋表层P的补充主要来自大气P沉降[1].因此, 为评估大气P沉降对海洋生态系统的影响, 对大气气溶胶中P的浓度水平、存在形态及来源等的研究是很有必要的.
大气气溶胶中的P来源于自然源和人为源, 自然源包括地壳源、海盐源、一次生物源和火山源等, 人为源包括生物质燃烧、化石燃料燃烧、农业化肥释放等[3~6].一直以来普遍认为, 地壳源是大气P的最主要来源[3], 但最近的研究发现燃煤排放对大气P也有重要贡献[6].大气P沉降入海后, 由于矿物气溶胶在海洋真光层中的停留时间较短, 因此能被海洋生物所利用的主要是大气沉降中的溶解态P(DP)[7]. DP包括溶解态无机P(DIP)和溶解态有机P(DOP).目前关于DP的研究绝大多数仅分析了DIP[8], 这是由于人们普遍认为仅DIP可直接被海洋生物所利用, 且其在DP中占主导[3].但已有研究发现DOP通过酶介反应也可以转化为生物可利用P[9].尽管Izquierdo等[10]的研究指出地中海近岸大气沉降中DOP对DP的贡献仅为6%, 但也有研究报道在全球海洋大气沉降中DOP的贡献为20%~83%[11].因此, 研究大气气溶胶中的P, 不仅应考虑总P(TP), 还应考虑DP及其中的DIP和DOP.
目前, 有关大气气溶胶中P浓度的观测数据还很缺乏, 在西北太平洋和中国近海鲜见报道.另外, 由于夏季海洋层化现象严重, 大气P沉降对海洋表层水体中P营养盐补充的相对贡献在夏季可能最为重要[12].因此, 本文利用2016年夏季在黄海近岸城市(青岛市)采集的总悬浮颗粒物(TSP)样品, 分析其中TP、DP、DIP和DOP的浓度分布特征及来源, 并估算了大气不同形态P的沉降通量, 以期为正确评价大气沉降P的生物可利用性及其对海洋初级生产的贡献提供有效的数据参考.
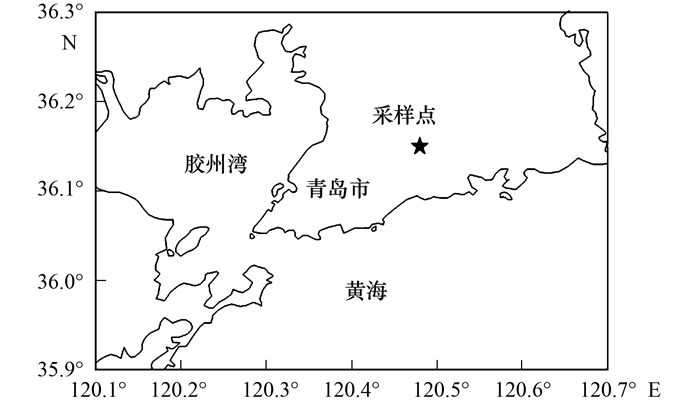
1 材料与方法 1.1 样品采集于2016年6月20日~2016年7月20日在青岛采集TSP样品28个.采集地点位于中国海洋大学崂山校区内(36°9'N, 120°29'E), 附近多绿地、无明显工业污染源, 距离海岸线约7 km(图 1). TSP样品采用KC-1000型大流量采样器(青岛崂山电子公司)采集, 采样流量为1.05 m3·min-1, 每个样品采集时间约为24 h, 采样体积约为1 500 m3.采样膜为预先酸洗处理的Whatman 41纤维滤膜.采样结束后, 在超净台中小心取下样品膜, 对折后放入洁净的聚乙烯封口袋中, 于-20℃冷冻保存至分析.采样期间, 记录气温、相对湿度、风向、风速等气象参数.
|
图 1 青岛近岸采样点的位置示意 Fig. 1 Aerosol sampling site at Qingdao |
裁取一定面积样品膜(8 cm2)放入高压消解罐的聚四氟乙烯内胆中, 加入4 mL 70%的HNO3和1 mL 49%的HF, 密封消解罐, 于180℃烘箱中消解48 h, 冷却后取出内胆置于180℃电热板上加热使酸完全挥发, 至近干时取下冷却至室温, 用超纯水把消解罐内胆中样品多次润洗转移并定容至25 mL, 用于测定TP.裁取一定面积样品膜(48 cm2)放入萃取瓶中, 加入15 mL超纯水在0℃下超声萃取20 min, 萃取液经0.45 μm滤膜过滤后转移至容量瓶中, 重复提取步骤, 后润洗样品膜3次, 定容至50 mL, 取其中25 mL测定DIP.另取10 mL上述萃取液, 加入2.5 mL过硫酸钾氧化剂(0.375 mol·L-1 NaOH+0.185 mol·L-1 K2S2O8+0.484 mol·L-1 H3BO3混合溶液), 于120℃下消解30 min, 冷却后取出定容至25 mL用于测定DP. DOP由DP和DIP差减计算得到.
不同形态P浓度采用磷钼蓝比色法进行测定, 在上述样品预处理后的溶液中, 加入2.5 mL显色剂(硫酸+钼酸铵+抗坏血酸+酒石酸锑钾混合溶液), 摇匀.显色15 min后, 采用紫外分光光度计(北京普析通用T6新世纪), 在880 nm波长处, 用5 cm比色皿进行测定.该方法检出限为0.07 μmol·L-1, 测定精密度为<3%. TP消解实验中, 为检验样品中P的消解效率, 取一定量的土壤成分分析标准物质(GBW07408, 地球物理地球化学勘查研究所.因无气溶胶标准样, 以土壤标准样代替)与样品膜相同方法消解, TP的回收率为95%~105%.样品处理过程中所用试剂均为优级纯, 所用器皿均预先经过酸洗以去除可能的干扰.
样品中Al、Mn、Fe、Ba、Sr、V、Ni、Cu、As、Cd、Pb等其他微量元素采用Agilent 7500c ICP-MS分析, 水溶性离子(Na+、K+、Mg2+、NH4+、Ca2+、Cl-、NO3-、SO42-)采用Dionex ICS-3000离子色谱仪分析, 样品的分析方法及质量控制等详见文献[13].
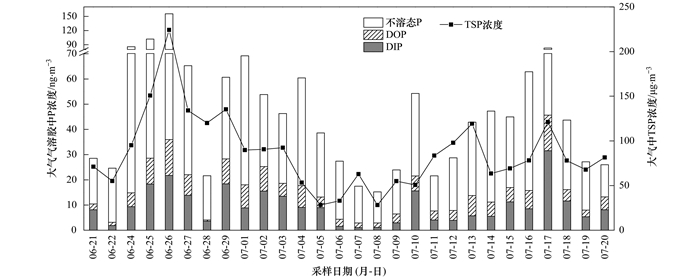
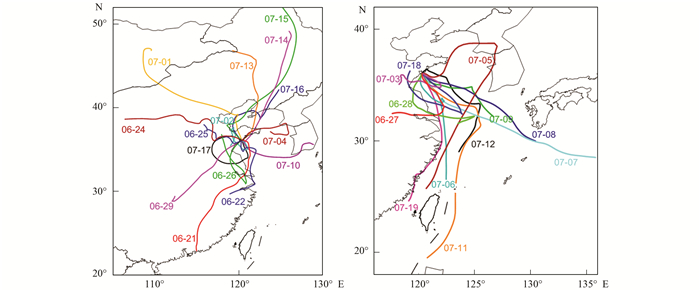
2 结果与讨论 2.1 青岛大气气溶胶中TP及DP的浓度采样期间, 青岛大气中TSP浓度为28.1~224.3 μg·m-3, 平均为(86.8±42.0) μg·m-3.气溶胶中TP浓度为15.2~155.5 ng·m-3, 平均浓度为(49.3±30.6) ng·m-3, DP浓度为2.9~45.7 ng·m-3, 平均为(15.5±10.4) ng·m-3(图 2).青岛气溶胶中TP浓度与夏季东海花鸟岛气溶胶中14~115 ng·m-3的TP浓度相当[14], 但高于夏季南海观测的气溶胶中(36±22) ng·m-3的TP浓度[15], DP则与夏季亚喀巴湾观测的18.6 ng·m-3 DP浓度接近[16].观测期间青岛气溶胶中TP浓度的最大值出现在6月26日采集的样品中, 最小值出现在7月7日和8日的样品中; 而DP浓度的最大值出现在7月17日的样品中, 最小值出现在7月7日和7月8日采集的样品中.分析每个样品采集期间气团72h后向轨迹(HYSPLIT 4, http://www.arl.noaa.gov/, 图 3), 发现影响6月26日样品的气团主要来自南方陆源, 该样品中TSP浓度和代表地壳源的元素Al浓度也最高, 而代表海洋源的Na+和Cl-的浓度相对较低, 且气象参数显示, 采样期间风向为南风, 大气能见度低, 为雾天; 影响7月7日和7月8日样品的气团主要来自海洋源, 这两个样品中TSP浓度和地壳元素(Al、Mn、Fe和Ba)及人为源的指示元素(Ni、As、Cd和Pb)浓度均较低, 而代表海洋源的Na+和Cl-浓度相对较高, 采样期间风向为东南风, 能见度较高, 为晴天; 影响7月17日样品的气团也主要来自南方陆源, 该样品中人为源元素Ni、As、Cd和Pb等浓度均较高且水溶性离子NO3-和SO42-浓度与其他样品相比最高, 采样期间风向也为南风, 大气能见度低, 为雾天.这些结果表明青岛大气气溶胶中TP及DP的浓度分布与采样期间气团的来源及迁移路径有很大的关系, 受陆源影响的气溶胶中P的浓度明显高于受海洋源影响的气溶胶.
|
图 2 青岛大气气溶胶中不同形态磷浓度及TSP浓度 Fig. 2 Atmospheric concentrations of different forms of P and TSP in aerosols collected from Qingdao |
|
图 3 青岛大气气溶胶样品采集期间气团72 h后向轨迹(500 m高度) Fig. 3 The 72 h air mass back trajectories for aerosols collected in Qingdao (500 m above ground level) |
青岛大气气溶胶中DP对TP的贡献为12.9%~54.9%, 平均为30.9%±11.0%(图 2).这与新加坡大气气溶胶中38%的TP是溶解态的结果相近[17], 但高于东海花鸟岛大气气溶胶中DP的贡献为0.6%~63%(中位值为15%)的结果[14], 这可能与东海观测期间出现了沙尘天气有关.观测期间, 青岛气溶胶中DP对TP的贡献在7月17日样品中最大, 在6月22日和7月6~8日样品中的最小, 气团的后向轨迹分析显示, 前者主要受到陆源的影响, 后者不同程度受到海洋源气团的影响(图 3).有研究报道, 地中海大气中受撒哈拉沙尘影响的气溶胶中DP在TP中的比例为2%~20%, 平均为10%, 而受混合了人为源气团影响的气溶胶中DP的比例为30%~79%, 平均为50%[18]; 在大西洋东西断面上, 观测样品中DP的比例平均约为32%, 其中受沙尘影响的气溶胶中约为8%, 而受南美陆源气团影响的气溶胶中达87%[19, 20].可见, 受不同来源气团影响的气溶胶中DP对TP的贡献不同.
2.2 青岛大气气溶胶中DIP和DOP的浓度青岛大气DIP浓度为1.0~31.6 ng·m-3, 平均浓度为(9.6±7.1) ng·m-3, DOP浓度为0.5~14.3 ng·m-3, 平均为(5.9±3.6) ng·m-3(图 2).青岛气溶胶中DIP浓度略低于夏季南海观测的气溶胶中(16±12) ng·m-3的DIP浓度[15], 也低于夏季亚喀巴湾观测的(12.4±6.2) ng·m-3 DIP浓度[16].已有研究中关于大气气溶胶中DOP较少, Chen等[16]研究了亚喀巴湾大气气溶胶中DOP浓度为(6.2±3.1) ng·m-3, 与本研究中DOP浓度相近.
青岛大气气溶胶中DP以DIP占主导, 其对DP的贡献为35.4%~88.9%, 平均为59.2%±13.0%(图 2).但DOP也有重要贡献, 为DP的11.1%~64.6%, 平均为40.8%±13.0%, 这一结果高于亚喀巴湾大气气溶胶中DOP对DP的贡献为31%的结果[16], 但与黄渤海气溶胶中DOP对DP的贡献为41.1%±8.6%的结果相近[21].有研究报道当气团携带的海洋气溶胶增多时, 气溶胶样品中DOP对DP的贡献增大, 这可能是由于海洋气团中人为源贡献的DIP比例降低, 使得DOP在DP中的比例相对升高, 也可能是由于海洋生物活动释放DOP的结果[22].因此, 大气气溶胶中DOP的贡献不能忽略, 尤其是在海洋气溶胶中, 不包括DOP贡献的DP浓度可能被低估30%~40%.
2.3 青岛大气气溶胶中不同形态P的来源 2.3.1 相关性分析分析不同形态P与微量元素及水溶性离子的相关关系(表 1), 结果显示夏季青岛气溶胶中的TP与Al、Mn、Fe和Sr等地壳元素显著相关(r>0.8, P<0.01), 表明大气P主要来源于地壳源.大气气溶胶中TP还与Cu、As、Cd和Pb等人为源元素有一定相关性(r>0.4, P<0.05), 表明大气P还有部分来自人为源的贡献.另外, 气溶胶中TP还与K+、NH4+、NO3-和SO42-等水溶性离子有相关关系, K+被认为是生物质燃烧的指示性元素[23], 大气中NH4+主要是由农业活动和生物释放的NH3转化形成的, 而NO3-和SO42-主要是由化石燃料燃烧排放的NOx和SO2转化而来[24, 25], 这表明大气P还可能受到生物质燃烧、农业施肥以及化石燃料燃烧源的影响. Al是典型的地壳元素, 以Al作为地壳源参比元素, 根据地壳中P/Al的比值为0.013[26]估算青岛气溶胶中来自地壳源的P对大气TP的贡献约为37%, 则人为源P的贡献最大约为63%. Mahowald等[3]基于模式和观测结果指出, 在全球尺度上, 地壳源是大气P的主要来源, 贡献约为82%, 而人为源的贡献约为5%.但最近Wang等[27]的研究认为, 化石燃料燃烧和生物质燃烧排放贡献了全球大气P的50%. Srinivas等[8]的研究则发现印度洋北部孟加拉湾大气气溶胶中75%的P来源于与农业化肥和生物质燃烧排放有关的人为源.
|
|
表 1 青岛大气气溶胶中不同形态P与微量元素及水溶性离子的相关关系1) Table 1 Correlation of different forms of P with trace elements and water-soluble ions in aerosols collected from Qingdao |
气溶胶中DP与地壳源及人为源元素均有显著的相关关系, 表明DP可能受到地壳源与人为源的共同影响. DP与水溶性离子NO3-和SO42-也呈显著相关关系, 表明DP浓度可能受到大气酸过程的影响.来自地壳源的P主要以磷灰石类矿物的形式存在, 少部分P与铁氧矿物结合[28], 这些矿物态P很难溶解, Nenes等[29]模拟大气酸化过程(pH=2的H2SO4溶液)的实验显示, 酸化后的撒哈拉表层土壤和沙尘气溶胶中DP浓度升高了10~40倍. Hsu等[30]在研究东海气溶胶时也发现溶解态P与NO3-和SO42-存在显著相关关系, 这些结果表明在大气传输过程中气溶胶P受到大气酸过程的影响, 从而提高了DP浓度.与地壳源P相比, 人为源中的DP对TP的贡献更大[18~20], 表明人为源P可能更容易溶解, 青岛气溶胶中DP相比于TP与人为源元素有更好的相关关系也说明了这一点.
与DP类似, 青岛气溶胶中DIP和DOP与地壳元素Al、Mn、Fe、Ba、Sr和人为源元素Ni、Cu、As、Cd、Pb等均呈显著相关, 表明DIP和DOP受地壳源和人为源的共同影响.另外, DIP和DOP还与水溶性离子K+、NH4+、NO3-和SO42-等有显著相关关系, 表明其可能来自于生物质燃烧, 农业施肥以及大气酸化过程等.总之, 青岛气溶胶中不同形态P与微量元素和水溶性离子均有一定相关关系, 表明大气中不同形态P的来源复杂, 受到多种因素的共同影响.
2.3.2 正矩阵因子(PMF)分析采用PMF(EPA PMF 5.0)对青岛气溶胶中的不同形态P及其它化学成分谱进行定量的来源解析.经多次分析比较, 发现当解析因子为6时各特征源谱指示明显, 各组分模型模拟值与实测值一致, 除Ba和As模型模拟值与实测值的R2约为0.7外, 其他组分模型模拟值与实测值的R2均为>0.8, 模型模拟结果可以反映各组分的真实信息.
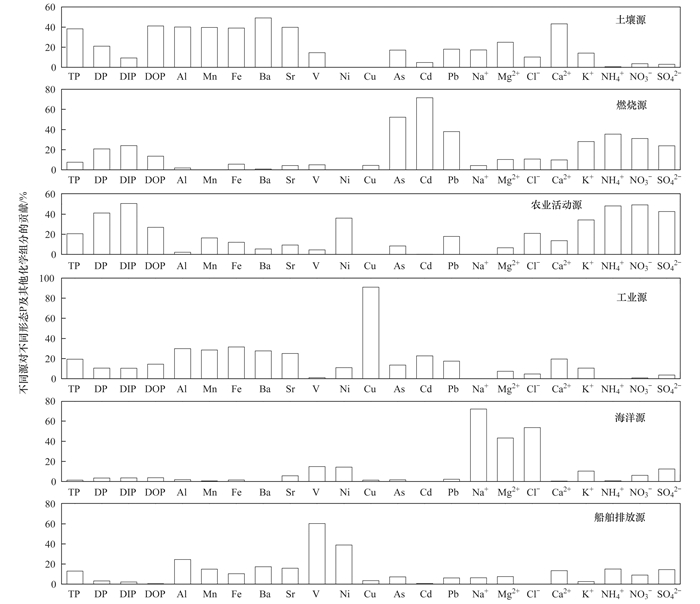
PMF模型分析结果显示, 青岛大气气溶胶中P主要受到6个因子影响(图 4).因子1中地壳源的代表元素Al、Mn、Fe、Ba、Sr及Ca2+的载荷较高, 贡献了其总量的43%~50%, 因此确定因子1为土壤源; 因子2中, 机动车燃油排放的代表性元素Cd和Pb[31]的载荷最高, 分别贡献其总量的72%和38%, 且NO3-的载荷也较高, 贡献其总量的31%, NO3-主要是由机动车燃油排放的NOx转化而来[25], 此外, 化石燃料燃烧的产物As及SO42-也有较高的负载, 贡献其总量的52%和24%, 因此确定因子2为燃烧源; 因子3中NH4+的载荷最高, 贡献其总量的48%, NH4+主要来自于农业活动和生物释放[24, 25], 此外, 生物质燃烧(农业秸秆的燃烧)的指示元素K+[23]的载荷也较高, 贡献其总量的34%, 且Ni等重金属、水溶性离子NO3-及SO42-的载荷也较高, 有研究表明农田土壤中Ni等重金属的含量较高[32], NO3-及SO42-可能是由秸秆燃烧过程中释放的NOx以及SO2[33]在大气中氧化生成的, 因此确定因子3为农业活动源; 因子4中Cu的载荷最大, 贡献其总量的91%, Cu常被认为是金属冶炼废气排放的标志性元素[31], 且Mn、Fe、Ba、Sr等的载荷也较高, 贡献其总量的30%左右, 因此因子4确定为工业源; 因子5中, 海盐标志性组分Na+、Cl-和Mg2+的载荷最高, 分别贡献了其总量的72%、54%和43%, 因此因子5代表海洋源; 因子6中, 船舶排放的重油燃烧产物V和Ni[34]的载荷最高, 分别贡献其总量的60%和39%, 因此确定因子6为船舶排放源.
|
图 4 青岛大气气溶胶PMF解析的源轮廓 Fig. 4 Source profiles of Qingdao aerosols from PMF |
分析气溶胶中不同源对不同形态P的贡献, 发现TP主要来自土壤源的贡献, 为38%, 这与依据地壳中P/Al比值估算的结果一致; 其次是农业活动源、工业源、船舶排放源以及燃烧源, 分别贡献其总量的21%、19%、13%和8%;海洋源对TP的贡献最小, 为1%. DIP主要来自农业活动源的贡献, 为51%;其次是燃烧源, 为24%.农业活动源和燃烧源中酸性物质NO3-和SO42-均有较高载荷, 这些组分的酸化作用可使气溶胶中不溶态P转化为溶解态P; 工业源和土壤源对DIP的贡献相当, 分别为10%和9%;海洋源和船舶排放源的贡献较小, 分别为4%和2%.而对于DOP, 土壤源是其主要来源, 其贡献为41%, 有研究发现土壤中的细菌、真菌孢子、昆虫及植物残体等对气溶胶中DOP有重要贡献[12, 35], 土壤源释放的有机P中有10%是溶解态的[34]; 其次是农业活动源, 其贡献为27%;燃烧源和工业源的贡献相当, 约为14%;海洋源的贡献较小, 只有4%, 船舶排放源基本无贡献.
2.4 不同形态P的干沉降通量及其对海洋初级生产力的贡献估算黄海近岸大气P的干沉降通量[F, μg·(m2·d)-1], 利用方程F=0.864×(c×V)计算, 式中, c为气溶胶中不同形态的P浓度(ng·m-3), V为气溶胶中不同形态P的干沉降速率(cm·s-1).由于气溶胶中TP和DP的粒径分布不同, 而不同粒径颗粒物的沉降速率不同, 根据文献中TP更多分布在粗粒子上而DP更多分布在细粒子上的分布特征, 取TP的沉降速率为1.2 cm·s-1、DP的为0.9 cm·s-1[13].
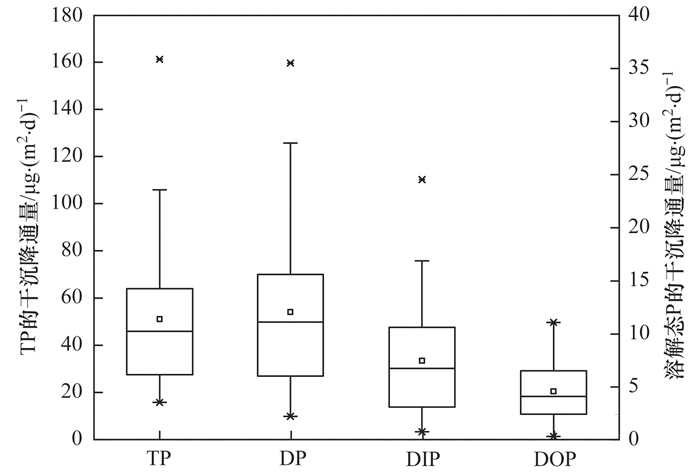
青岛大气中TP的干沉降通量为15.8~161.2 μg·(m2·d)-1, 平均为51.7 μg·(m2·d)-1(图 5), 与东海非沙尘天气下大气P沉降通量为42 μg·(m2·d)-1的结果相近[13]. DP的干沉降通量为2.2~35.5 μg·(m2·d)-1, 平均为12.1 μg·(m2·d)-1, 其中DIP的沉降通量为0.8~24.5 μg·(m2·d)-1, 平均为7.5 μg·(m2·d)-1; DOP的沉降通量为0.4~11.1 μg·(m2·d)-1, 平均为4.6 μg·(m2·d)-1.青岛大气DIP的沉降通量略高于东海大气非沙尘天气下5.2 μg·(m2·d)-1的沉降通量[13], 但低于黄海大气春季非沙尘天气下(10±6) μg·(m2·d)-1的沉降通量[12].已有研究中关于大气DOP的沉降通量鲜见报道, Zamora等[36]的研究显示迈阿密大气中DOP的湿沉降通量为(4.6±2.8) μg·(m2·d)-1, DOP对DP湿沉降通量的贡献为>50%, 高于青岛大气DOP对DP干沉降通量约40%的贡献.
|
图 5 青岛大气不同形态P的干沉降通量 Fig. 5 Atmospheric dry deposition fluxes of different forms of P in Qingdao |
大气P沉降入海后, 只有溶解态部分可直接被浮游植物吸收利用, 从而影响海洋的初级生产.夏季青岛大气TP干沉降通量的23.2%±8.2%是溶解态的.若大气沉降的DP能被海洋浮游植物完全利用, 由Redfield比值估算大气沉降的DP可支持黄海(0.5±0.3) mg·(m2·d)-1的浮游植物碳的生产.据报道黄海的年平均新生产力为68.4 mg·(m2·d)-1[37], 因此夏季大气沉降的DP可以支持黄海约1%的新生产力.有研究指出夏季大气P的干沉降通量最小, 其他季节通常为夏季的2~4倍[38], 尤其在沙尘天气下[12, 13], 大气P对海洋的输入明显增多.另外, 大气P沉降以湿沉降为主, DIP的干沉降在总沉降通量中仅占<20%[39].因此, 本研究估算的大气P沉降对海洋初级生产的贡献可能明显低估了其实际贡献, 今后需要进一步对不同季节大气P的干、湿沉降通量开展研究才能准确评价大气P沉降对海洋初级生产的贡献.
3 结论(1) 夏季青岛大气气溶胶中TP的浓度为15.2~155.5 ng·m-3, 平均为49.3 ng·m-3, 约30%的TP以溶解态的形式存在, 其中DIP的浓度为(9.6±7.1) ng·m-3, DOP的浓度为(5.9±3.6) ng·m-3, 不包括DOP贡献的溶解态P浓度可能被低估30%~40%.
(2) 青岛气溶胶中不同形态P与微量元素和水溶性离子均存在一定相关关系. TP主要来源于土壤源, 其贡献为38%, 其次是农业活动源和工业源, 分别贡献20%左右; DIP的51%来自农业活动源的贡献, 燃烧源的贡献为24%; DOP主要来自土壤源的贡献, 为41%, 其次是农业活动源的贡献, 为27%.
(3) 观测期间, 大气TP的干沉降通量为(51.7±31.7) μg·(m2·d)-1, 其中的23%以DP的形式沉降入海.在DP的沉降通量中, DOP贡献了40%.大气DP的干沉降通量可支持黄海(0.5±0.3) mg·(m2·d)-1的浮游植物碳的生产, 对新生产力的贡献约为1%.
| [1] | Paytan A, McLaughlin K. The oceanic phosphorus cycle[J]. Chemical Reviews, 2007, 107(2): 563-576. DOI:10.1021/cr0503613 |
| [2] | Peñuelas J, Poulter B, Sardans J, et al. Human-induced nitrogen-phosphorus imbalances alter natural and managed ecosystems across the globe[J]. Nature Communications, 2013, 4: 2934. DOI:10.1038/ncomms3934 |
| [3] | Mahowald N, Jickells T D, Baker A R, et al. Global distribution of atmospheric phosphorus sources, concentrations and deposition rates, and anthropogenic impacts[J]. Global Biogeochemical Cycles, 2008, 22(4). |
| [4] | Anderson L D, Faul K L, Paytan A. Phosphorus associations in aerosols:what can they tell us about P bioavailability?[J]. Marine Chemistry, 2010, 120(1-4): 44-56. DOI:10.1016/j.marchem.2009.04.008 |
| [5] | Tipping E, Benham S, Boyle J F, et al. Atmospheric deposition of phosphorus to land and freshwater[J]. Environmental Science:Processes & Impacts, 2014, 16(7): 1608-1617. |
| [6] | Weinberger R, Weiner T, Angert A. Isotopic signature of atmospheric phosphate emitted from coal combustion[J]. Atmospheric Environment, 2016, 136: 22-30. DOI:10.1016/j.atmosenv.2016.04.006 |
| [7] | Mackey K R M, Roberts K, Lomas M W, et al. Enhanced solubility and ecological impact of atmospheric phosphorus deposition upon extended seawater exposure[J]. Environmental Science & Technology, 2012, 46(19): 10438-10446. |
| [8] | Srinivas B, Sarin M M. Atmospheric deposition of phosphorus to the northern Indian Ocean[J]. Current Science, 2015, 108(7): 1300-1305. |
| [9] | Mackey K R M, Mioni C E, Ryan J P, et al. Phosphorus cycling in the red tide incubator region of Monterey Bay in response to upwelling[J]. Frontiers in Microbiology, 2012, 3: 33. DOI:10.3389/fmicb.2012.00033 |
| [10] | Izquierdo R, Benítez-Nelson C R, Masqué P, et al. Atmospheric phosphorus deposition in a near-coastal rural site in the NE Iberian Peninsula and its role in marine productivity[J]. Atmospheric Environment, 2012, 49: 361-370. DOI:10.1016/j.atmosenv.2011.11.007 |
| [11] | Kanakidou M, Duce R A, Prospero J M, et al. Atmospheric fluxes of organic N and P to the global ocean[J]. Global Biogeochemical Cycles, 2012, 26(3): GB3026. DOI:10.1029/2011GB004277 |
| [12] | Myriokefalitakis S, Nenes A, Baker A R, et al. Bioavailable atmospheric phosphorous supply to the global ocean:a 3-D global modeling study[J]. Biogeosciences, 2016, 13(24): 6519-6543. DOI:10.5194/bg-13-6519-2016 |
| [13] | Shi J H, Zhang J, Gao H W, et al. Concentration, solubility and deposition flux of atmospheric particulate nutrients over the Yellow Sea[J]. Deep Sea Research Part Ⅱ:Topical Studies in Oceanography, 2013, 97: 43-50. DOI:10.1016/j.dsr2.2013.05.004 |
| [14] | Guo L, Chen Y, Wang F J, et al. Effects of Asian dust on the atmospheric input of trace elements to the East China Sea[J]. Marine Chemistry, 2014, 163: 19-27. DOI:10.1016/j.marchem.2014.04.003 |
| [15] | Hsu S C, Gong G C, Shiah F K, et al. Sources, solubility, and acid processing of aerosol iron and phosphorous over the South China Sea:East Asian dust and pollution outflows vs. Southeast Asian biomass burning[J]. Atmospheric Chemistry and Physics Discussions, 2014, 14(15): 21433-21472. DOI:10.5194/acpd-14-21433-2014 |
| [16] | Chen Y, Mills S, Street J, et al. Estimates of atmospheric dry deposition and associated input of nutrients to Gulf of Aqaba seawater[J]. Journal of Geophysical Research, 2007, 112(D4): D04309. DOI:10.1029/2006JD007858 |
| [17] | He J, Balasubramanian R, Burger D F, et al. Dry and wet atmospheric deposition of nitrogen and phosphorus in Singapore[J]. Atmospheric Environment, 2011, 45(16): 2760-2768. DOI:10.1016/j.atmosenv.2011.02.036 |
| [18] | Herut B, Collier R, Krom M D. The role of dust in supplying nitrogen and phosphorus to the Southeast Mediterranean[J]. Limnology and Oceanography, 2002, 47(3): 870-878. DOI:10.4319/lo.2002.47.3.0870 |
| [19] | Baker A R, French M, Linge K L. Trends in aerosol nutrient solubility along a west-east transect of the Saharan dust plume[J]. Geophysical Research Letters, 2006, 33(7): L07805. DOI:10.1029/2005GL024764 |
| [20] | Baker A R, Jickells T D, Witt M, et al. Trends in the solubility of iron, aluminium, manganese and phosphorus in aerosol collected over the Atlantic Ocean[J]. Marine Chemistry, 2006, 98(1): 43-58. DOI:10.1016/j.marchem.2005.06.004 |
| [21] |
张瑞峰, 祁建华, 丁雪, 等. 青岛近海及黄渤海大气气溶胶中不同形态氮磷质量浓度及组成特征[J]. 环境科学, 2018, 39(1): 38-48. Zhang R F, Qi J H, Ding X, et al. Concentrations and compositions of different forms of nitrogen and phosphorus in atmospheric aerosols in the Qingdao coastal region and over the Yellow and Bohai Sea[J]. Environmental Science, 2018, 39(1): 38-48. |
| [22] | Chen H Y, Fang T H, Presto M R, et al. Characterization of phosphorus in the aerosol of a coastal atmosphere:using a sequential extraction method[J]. Atmospheric Environment, 2006, 40(2): 279-289. DOI:10.1016/j.atmosenv.2005.09.051 |
| [23] | Lim J M, Lee J H, Moon J H, et al. Source apportionment of PM10at a small industrial area using Positive Matrix Factorization[J]. Atmospheric Research, 2010, 95(1): 88-100. DOI:10.1016/j.atmosres.2009.08.009 |
| [24] | Paerl H W, Dennis R L, Whitall D R. Atmospheric deposition of nitrogen:implications for nutrient over-enrichment of coastal waters[J]. Estuaries, 2002, 25(4): 677-693. DOI:10.1007/BF02804899 |
| [25] | Zhao X, Yan X Y, Xiong Z Q, et al. Spatial and temporal variation of inorganic nitrogen wet deposition to the Yangtze River Delta Region, China[J]. Water, Air, and Soil Pollution, 2009, 203(1-4): 277-289. DOI:10.1007/s11270-009-0011-2 |
| [26] | Taylor S R. Abundance of chemical elements in the continental crust:a new table[J]. Geochimica et Cosmochimica Acta, 1964, 28(8): 1273-1285. DOI:10.1016/0016-7037(64)90129-2 |
| [27] | Wang R, Balkanski Y, Boucher O, et al. Significant contribution of combustion-related emissions to the atmospheric phosphorus budget[J]. Nature Geoscience, 2015, 8(1): 48-54. DOI:10.1038/ngeo2324 |
| [28] | Hudson-Edwards K A, Bristow C S, Cibin G, et al. Solid-phase phosphorus speciation in Saharan Bodélé Depression dusts and source sediments[J]. Chemical Geology, 2014, 384: 16-26. DOI:10.1016/j.chemgeo.2014.06.014 |
| [29] | Nenes A, Krom M D, Mihalopoulos N, et al. Atmospheric acidification of mineral aerosols:a source of bioavailable phosphorus for the oceans[J]. Atmospheric Chemistry and Physics, 2011, 11(13): 6265-6272. DOI:10.5194/acp-11-6265-2011 |
| [30] | Hsu S C, Wong G T F, Gong G C, et al. Sources, solubility, and dry deposition of aerosol trace elements over the East China Sea[J]. Marine Chemistry, 2010, 120(1-4): 116-127. DOI:10.1016/j.marchem.2008.10.003 |
| [31] |
杨卫芬, 银燕, 魏玉香, 等. 霾天气下南京PM2.5中金属元素污染特征及来源分析[J]. 中国环境科学, 2010, 30(1): 12-17. Yang W F, Yin Y, Wei Y X, et al. Characteristics and sources of metal elements in PM2.5 during hazy days in Nanjing[J]. China Environmental Science, 2010, 30(1): 12-17. |
| [32] | Nicholson F A, Smith S R, Alloway B J, et al. An inventory of heavy metals inputs to agricultural soils in England and Wales[J]. Science of the Total Environment, 2003, 311(1-3): 205-219. DOI:10.1016/S0048-9697(03)00139-6 |
| [33] |
陆炳, 孔少飞, 韩斌, 等. 2007年中国大陆地区生物质燃烧排放污染物清单[J]. 中国环境科学, 2011, 31(2): 186-194. Lu B, Kong S F, Han B, et al. Inventory of atmospheric pollutants discharged from biomass burning in China continent in 2007[J]. China Environmental Science, 2011, 31(2): 186-194. |
| [34] | Sholkovitz E R, Sedwick P N, Church T M. Influence of anthropogenic combustion emissions on the deposition of soluble aerosol iron to the ocean:empirical estimates for island sites in the North Atlantic[J]. Geochimica et Cosmochimica Acta, 2009, 73(14): 3981-4003. DOI:10.1016/j.gca.2009.04.029 |
| [35] | Kanakidou M, Duce R A, Prospero J M, et al. Atmospheric fluxes of organic N and P to the global ocean[J]. Global Biogeochemical Cycles, 2012, 26(3): GB3026. DOI:10.1029/2011GB004277 |
| [36] | Zamora L M, Prospero J M, Hansell D A, et al. Atmospheric P deposition to the subtropical North Atlantic:sources, properties, and relationship to N deposition[J]. Journal of Geophysical Research:Atmospheres, 2013, 118(3): 1546-1562. DOI:10.1002/jgrd.50187 |
| [37] |
李杰, 吴增茂, 万小芳. 黄海冷水团新生产力及微食物环作用分析[J]. 中国海洋大学学报, 2006, 36(2): 193-199. Li J, Wu Z M, Wan X F. Modelling study of the new production and the contribution of the microbial food loop in the Yellow Sea cold water mass[J]. Periodical of Ocean University of China, 2006, 36(2): 193-199. |
| [38] | Luo J, Wang X R, Yang H, et al. Atmospheric phosphorus in the northern part of Lake Taihu, China[J]. Chemosphere, 2011, 84(6): 785-791. DOI:10.1016/j.chemosphere.2011.01.043 |
| [39] | Zhang G S, Zhang J, Liu S M. Characterization of nutrients in the atmospheric wet and dry deposition observed at the two monitoring sites over Yellow Sea and East China Sea[J]. Journal of Atmospheric Chemistry, 2007, 57(1): 41-57. DOI:10.1007/s10874-007-9060-3 |
 2018, Vol. 39
2018, Vol. 39


