2. 四川文理学院化学化工学院, 达州 635000
2. School of Chemistry and Chemical Engineering, Sichuan University of Arts and Science, Dazhou 635000, China
氧化铁和有机质是土壤/沉积物的重要活性组分, 它们在自然环境中常相互胶结形成复合物[1~4].氧化铁-有机质复合物对土壤的结构和理化性质有显著影响, 是土壤团聚体的核心物质, 也是土壤肥力的物质基础[5~9].土粒的颗粒尺寸和稳定性能影响土壤的抗蚀性, 土壤有机质可以显著增强土粒间的黏结力, 极大地提高土粒的抗冲蚀性能[10~12].氧化铁-有机质复合物具有结构稳定和表面活性强等特性, 对土壤团聚体的形成、结构和性质有重要影响.深入了解氧化铁-有机质复合物的微观结构、结合机制及其稳定性, 可为水土保持、土壤肥力培育、环境修复等方面提供基础数据和科学依据.
土壤氧化铁颗粒细小、比表面积较大, 表面功能团主要是两性铁羟基(≡Fe—OH)和边缘配位不饱和的Fe原子[13~15].针铁矿是土壤中最常见的晶质氧化铁.在我国南方山地土壤和黄棕壤中, 针铁矿是主要的土壤黏粒氧化物, 在红壤和砖红壤中也有一定含量的针铁矿存在.腐殖质是土壤有机质的主体成分, 根据酸碱提取过程可将其划分为富啡酸、胡敏酸和胡敏素这3种组分.胡敏酸是土壤腐殖质的主体部分, 其表面具有丰富的活性官能团, 易与营养元素和污染物相互作用形成稳定性的络合物[16~19].当悬浮液中同时存在针铁矿和腐殖酸时, 多种微观作用力可导致两种颗粒胶结复合.静电作用被认为是二者胶结复合的重要机制之一, 当表面带正电荷的针铁矿靠近带负电荷的胡敏酸时, 其表面双电层在一定程度上重叠形成二元复合物[6].针铁矿表面Fe原子与胡敏酸结构中的羧酸等官能团之间的配位络合作用被认为是二者之间的主要化学作用机制[6, 20, 21].
关于氧化铁与腐殖酸之间胶结形成复合物的研究较多, 但这类研究多集中于复合物的表面性质及其与污染物的作用特性[22~26].有关氧化铁与胡敏酸的胶结机制及二元复合物的微观结构和稳定性方面的报道却较少.土壤类型多样, 各种土壤的物质组成千差万别, 不同土壤的团聚体对维持和提升土壤质量存在较大的地域差异.然而, 土壤团聚体的胶结核心物质主要为活性金属氧化物、腐殖质、铝硅酸盐矿物等.因此, 以针铁矿和胡敏酸为前驱物, 探讨它们的胶结机制及其复合物的微观结构和稳定性, 以期为土壤团聚体形成、土壤质量提升、水土流失防治等方面提供基础资料.
1 材料与方法 1.1 实验试剂所用试剂均为分析纯试剂, 超纯水由超纯水机(HK-UP-11-20, 成都浩康科技有限公司)制备.腐殖酸购自阿拉丁试剂(上海)有限公司, 胡敏酸组分的主要提取步骤为:用0.1 mol·L-1 NaOH溶液将腐殖酸悬浮液调至pH=10.0, 搅拌至悬浮液溶解, 静置2 h, 倒出棕褐色溶液, 弃去不溶物.将所得溶液继续静置2 h, 取上层棕褐色溶液, 重复操作3次.用0.1 mol·L-1HCl溶液将所得棕褐色溶液调节至pH=1.0, 静置1 d, 弃去上清液, 沉淀物用超纯水洗涤并离心两次, 所得胡敏酸50℃真空干燥、研磨待用.
1.2 样品的制备 1.2.1 针铁矿的制备根据文献[27]中的方法合成针铁矿, 主要步骤为:取50 mL 1 mol·L-1 Fe(NO3)3溶液于1 L塑料烧杯中, 搅拌条件下迅速加入90 mL 5 mol·L-1 NaOH溶液, 加超纯水至总体积为1 000 mL, 用保鲜膜将烧杯密封, 置于70℃油浴中老化60 h.将所得样品悬浮液冷却至室温, 充分搅拌悬浮液, 并将其分成两份.一份用超纯水洗涤并离心2次, 沉淀物50℃真空干燥、研磨, 用于样品表征测试.另一份悬浮液用于合成针铁矿-胡敏酸复合物.
1.2.2 针铁矿-胡敏酸复合物的制备取胡敏酸0.9 g于50 mL超纯水中, 用0.1 mol·L-1 NaOH溶液调节至pH=12.0, 搅拌至胡敏酸全部溶解.将1.2.1节中针铁矿悬浮液超声分散处理10 min, 磁力搅拌状态下将胡敏酸溶液缓慢滴加到针铁矿悬浮液中, 继续搅拌2 h, 并用0.1 mol·L-1HCl和NaOH溶液调节悬浮液至pH=4.0, 室温静置2 d, 离心分离.沉淀物即为针铁矿-胡敏酸复合物, 50℃真空干燥、研磨, 用于样品的检测分析.
1.3 样品的表征样品的X-射线衍射(XRD)分析采用粉末压片法, X射线衍射仪为岛津XRD-7000型, 测试条件:Cu Kα辐射, 工作电压40 kV、工作电流30 mA, 步长为0.01°, 扫描速度为8(°)·min-1.样品的透射电镜(TEM)分析在JEM-1400型透射电镜仪上进行.样品的红外光谱(IR)分析在傅里叶红外光谱分析仪Nicolet iS5(Thermo Fisher Scientific)上进行, 测试范围为4 000~400 cm-1, 分辨率为4 cm-1.样品热重(TG/DTG)分析在热重仪(SⅡTG/DTA6300) 上进行, 氩气氛围下测试, 温度范围为40~800℃, 升温速率为20℃·min-1.样品的粒径分布在马尔文激光粒度仪(Malven 2 000 mu)上进行, 测试条件:样品浓度为0.02 g·L-1, 背景溶液为0.01 mol·L-1 NaCl溶液, pH=4.0, 超声分散频率为80 kHz, 分散处理时间分别为10、20和40 min.
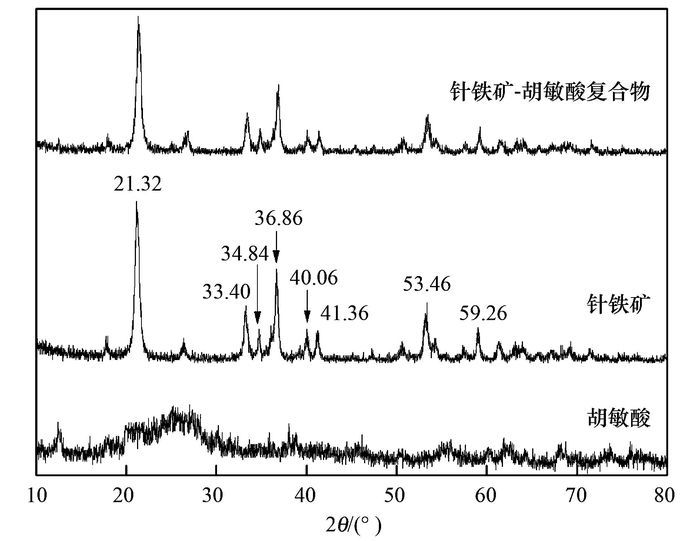
2 结果与分析 2.1 X-射线衍射分析样品的X-射线衍射(XRD)分析见图 1.针铁矿单体的XRD图谱中, 在2θ为21.32°、33.4°、34.84°、36.86°、40.06°、41.36°、53.46°和59.26°处分别出现了强弱不同的衍射峰, 这些峰对应的角度和相对强度与针铁矿标准卡片(PDF#810462) 的XRD衍射数据比较吻合, 表明针铁矿单体的纯度较高、结晶度良好.胡敏酸的XRD图谱中出现了一系列强度很弱的衍射峰, 说明胡敏酸试样中混有少量的晶质盐.针铁矿-胡敏酸复合物的主要衍射峰均可归属于针铁矿, 而没有出现其它的新衍射峰.与针铁矿单体比较, 复合物XRD衍射峰的2θ角度没有明显变化, 但其强度略微减弱, 其原因可归属为复合物中部分胡敏酸颗粒包被在针铁矿表面.
|
图 1 样品的XRD图谱 Fig. 1 X-Ray diffraction patterns of the samples |
样品的透射电镜(TEM)图像见图 2.胡敏酸为形貌不规则的纳米颗粒物, 且颗粒间相互连接成网状或链条状, 见图 2(a); 针铁矿单体颗粒为典型的针棒状形貌, 且表面为较光滑的裸露状态, 见图 2(b); 复合物中一些形貌不规则的胡敏酸颗粒物附着在针铁矿表面, 且没有发现脱离针铁矿表面而独立存在的胡敏酸颗粒, 见图 2(c).可见, 复合物中针铁矿与胡敏酸并非简单的机械混合, 而是部分胡敏酸颗粒包被在针铁矿表面形成了二元复合物, 这与XRD的分析结果一致.

|
(a)、(b)和(c)分别为胡敏酸、针铁矿单体和针铁矿-胡敏酸复合物 图 2 样品的TEM图像 Fig. 2 Transmission electron micrographs of the samples |
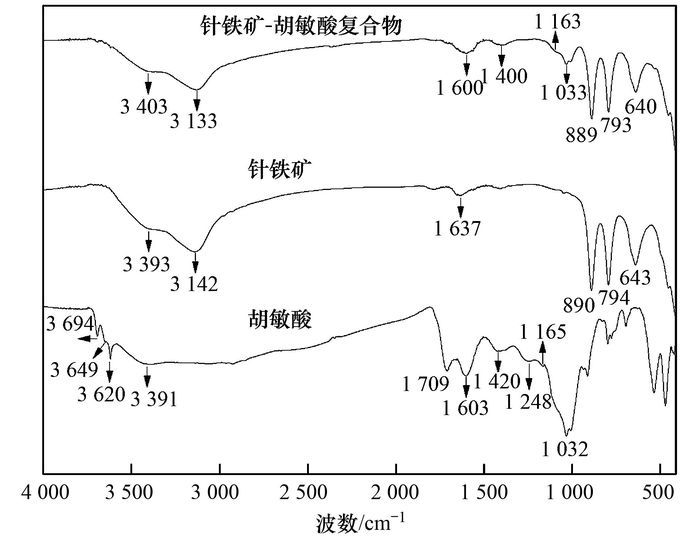
样品的红外光谱(IR)图谱见图 3.胡敏酸的IR图谱中, 在3 694、3 649、3 620、3 391、1 709、1 603、1 420、1 248、1 165、1 032 cm-1等处出现了一系列官能团振动吸收带.针铁矿单体的IR图谱中, 在3 142、890、794、643 cm-1等处出现了不同强度的振动吸收带.根据文献[18, 20, 27~30], 将针铁矿单体和胡敏酸两种样品的IR吸收带的归属列于表 1.针铁矿-胡敏酸复合物中, 胡敏酸分子中缔合羟基(H—O…H—O)伸缩振动带由3 391 cm-1向高波数漂移至3 403 cm-1, 而羧酸根(COO-)反对称伸缩振动带由1 603 cm-1向低波数漂移至1 600 cm-1, COO-的对称伸缩振动带由1 420 cm-1漂移至1 400 cm-1, 酚类C—O伸缩振动带由1 165 cm-1漂移至1 163 cm-1, 醇类C—O伸缩振动带没有明显变化, 羧酸C—O和羧酸羟基(OCOH)、酚羟基(ArOH)、醇羟基(ROH)等游离羟基的吸收带基本消失.复合物中出现了针铁矿单体的所有特征吸收带, 其中铁羟基(≡Fe—OH)和铁氧键(≡Fe—O)的伸缩振动带分别向低波数漂移至3 133 cm-1和640 cm-1附近, 其它振动吸收带没有明显变化.
|
图 3 样品的IR图谱 Fig. 3 IR spectra of the samples |
|
|
表 1 胡敏酸、针铁矿的红外吸收带归属 Table 1 IR absorption band assignments of the samples |
胡敏酸单体的IR图谱中, 各类C—O振动吸收带[醇类C—O伸缩振动吸收带(1 032 cm-1)、酚类C—O振动吸收带(1 165 cm-1)和羧酸C—O振动吸收带(1 248 cm-1)]、各类游离羟基振动吸收带[OCOH伸缩振动吸收带(3 620 cm-1)、ArOH伸缩振动吸收带(3 649 cm-1)和ROH伸缩振动吸收带(3 694 cm-1)]、羧酸羰基C=O振动吸收带(1 709 cm-1)、COO-反对称振动吸收带(1 603 cm-1)以及COO-的对称振动吸收带(1 420 cm-1)明显.复合物中出现了明显的醇类C—O振动吸收带(1 033 cm-1)、酚类C—O振动吸收带(1 163 cm-1)和COO-反对称及对称伸缩振动吸收带(1 603 cm-1和1 400 cm-1), 而没有出现C=O、羧酸C—O和各类游离羟基的振动吸收带.这些差异的主要原因可解释为:① 复合物形成过程中羧基中O原子可与针铁矿表面Fe原子发生配位作用, 导致C=O的键力常数降低, 而羧酸C=O的键力常数升高, 因此复合物中C=O和羧酸C—O的振动吸收带消失, 同时COO-和≡Fe—O的伸缩振动带都明显向低频率漂移; ② 酚类C—O中O原子与针铁矿表面Fe原子发生配位作用, 降低了酚类C—O的键力常数, 导致复合物中酚类C—O的振动频率降低; ③ 复合物中游离羟基与≡Fe—OH间形成了氢键, 羟基由游离态变为了缔合态, 因此复合物中游离羟基的吸收带消失, 而缔合羟基的吸收带变强, 同时≡Fe—OH的振动吸收带向低波数方向移动.
根据文献[18, 28], 有机羧酸-金属离子复合体系中COO-反对称伸缩振动吸收带与对称伸缩振动吸收带的波数差达到200 cm-1时, 说明羧酸官能团与金属离子之间是以单齿配位而作用; 当COO-反对称伸缩振动吸收带与对称伸缩振动吸收带的波数差为160 cm-1附近时, 说明羧酸官能团与金属离子之间的作用以双齿配位为主.本研究中, 复合物中COO-反对称伸缩振动吸收带与对称伸缩振动吸收带的波数差Δν≈200, 这表明针铁矿表面Fe原子与胡敏酸中羧酸官能团以单齿配位而复合, 这与文献[30]报道的结果相一致.
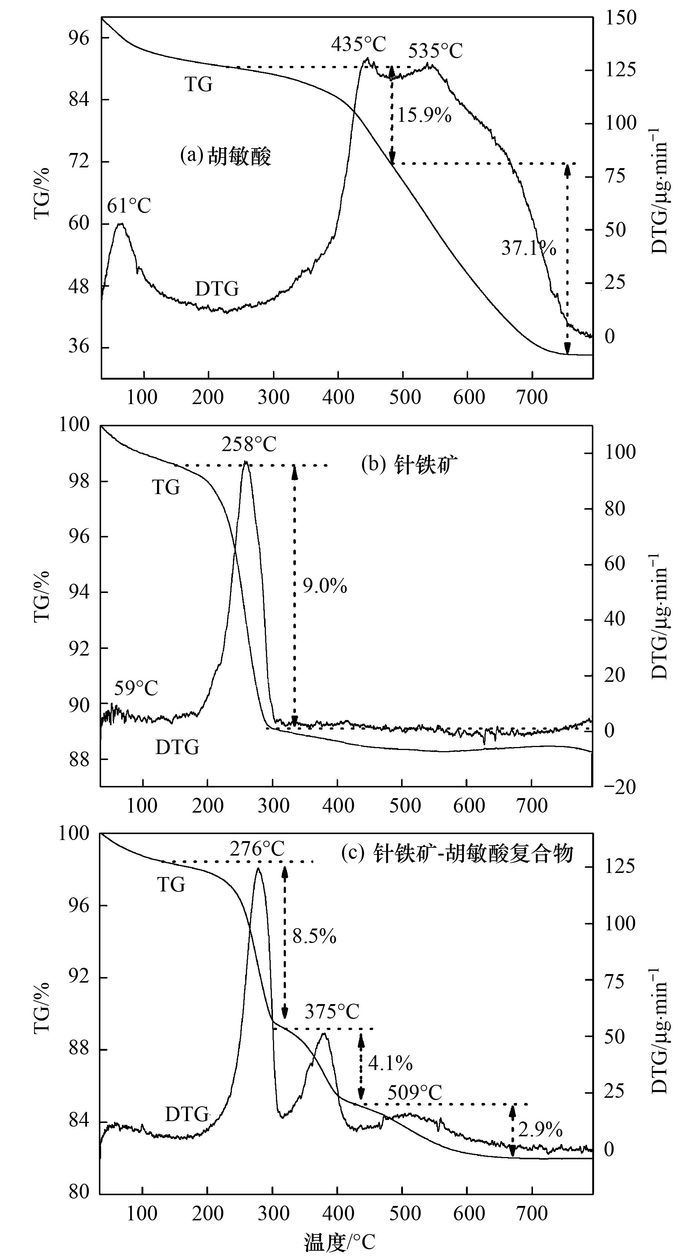
2.4 稳定性分析 2.4.1 热稳定性样品的热重(TG/DTG)曲线见图 4.可见, 胡敏酸单体的失重主要集中在两个温度范围内.温度为40~170℃时, 在61℃处出现了一个较小的失重峰, 失重量为8.5%, 这可归属于样品表面物理吸附水的损失; 温度在230~800℃时, 在435℃和535℃处出现了两个失重峰, 失重量分别为15.9%和37.1%, 这可分别归属于胡敏酸单体中脂肪族组分和芳香族组分的损失[31].在针铁矿单体的TG/DTG曲线中, 物理吸附水的损失发生在59℃左右, 其失重量为1.5%;温度在180~305℃时, 在258℃处出现了一个明显的失重峰, 失重量为9.0%, 这可归属于针铁矿结构羟基的损失[32].随着温度进一步升高至800℃时, 针铁矿的总失重量达11.8%.
|
图中虚线表示失重温度区间及相应失重量 图 4 样品的TG/DTG曲线 Fig. 4 TG/DTG curves of the samples |
针铁矿-胡敏酸复合物的TG/DTG曲线主要表现为4个明显的失重台阶.物理吸附水在温度<115℃时损失, 失重量约为1.5%.复合物中针铁矿结构羟基的损失发生在185~315℃间, 失重峰在276℃, 失重量为8.5%;胡敏酸中脂肪族组分和芳香族组分的损失分别发生在315~430℃和465~620℃间, 失重峰分别在375℃和509℃, 失重量分别为4.1%和2.9%.
Kang等[33]的研究表明, 腐殖酸中脂肪族组分与金属氧化物的亲和力强于芳香族组分.本研究中, 胡敏酸单体中脂肪族组分和芳香族组分的失重量分别是15.9%和37.1%, 而针铁矿-胡敏酸复合物中两种组分的失重量分别是4.1%和2.9%.可见, 复合物中脂肪族组分与芳香族组分的含量比明显高于胡敏酸单体中两种组分的含量比, 说明胡敏酸中脂肪族组分更易结合针铁矿形成复合物, 这与Kang等[33]的研究结果一致.与针铁矿单体比较, 复合物中针铁矿的结构羟基失重峰的温度升高了18℃, 表明胡敏酸的包被作用明显提高了复合物中针铁矿的热稳定性.与胡敏酸单体比较, 复合物中胡敏酸脂肪族组分和芳香族组分失重峰的温度分别降低了60℃和26℃.这可能是由于复合物形成过程中分子量小、热稳定性差的胡敏酸组分更易与针铁矿结合, 而分子量大、热稳定性强的胡敏酸组分难以被针铁矿吸附.可见, 复合物中针铁矿和胡敏酸组分的热力学特性明显不同于两种单体.
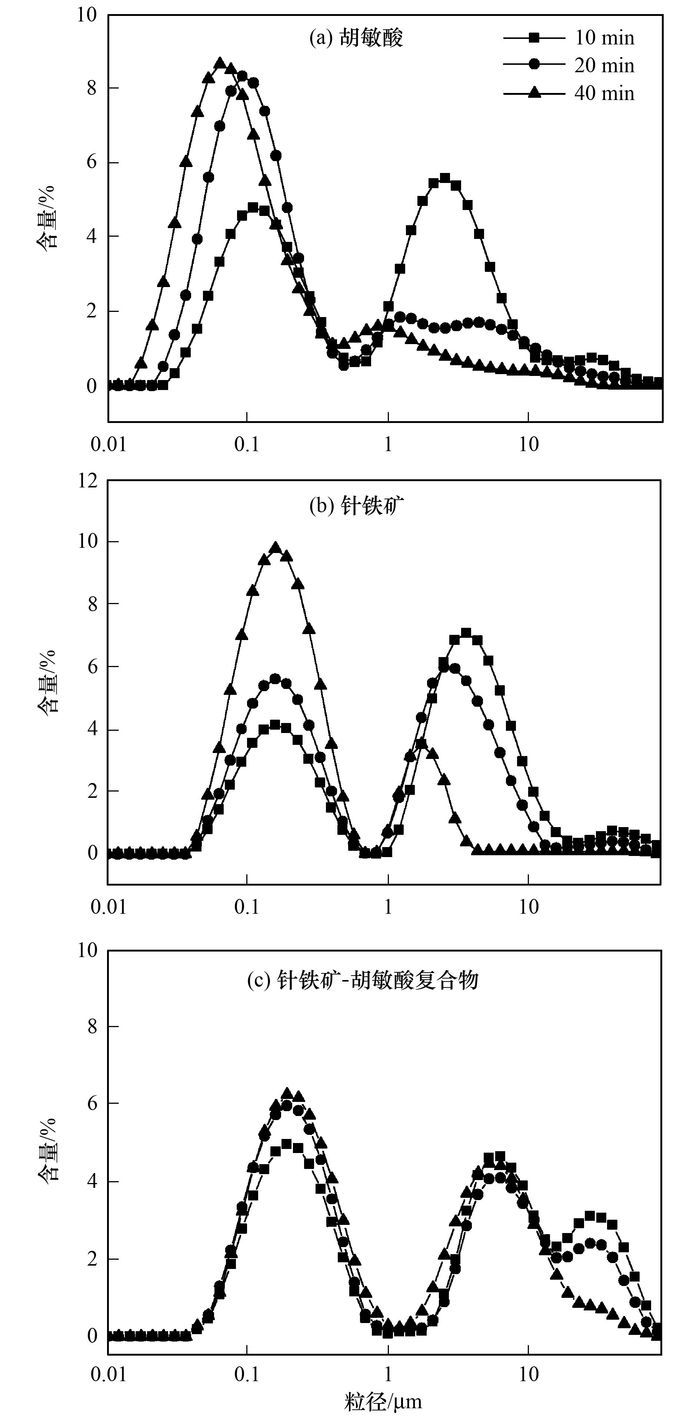
2.4.2 机械稳定性样品悬浮液超声分散处理后的粒径分布曲线和数据分别见图 5和表 2.胡敏酸单体悬浮液超声分散处理10 min时, 在粒径范围0.03~0.57、0.57~19.05和19.05~100 μm间分别出现了两个强的粒径分布峰和一个弱的分布峰, 其含量(质量分数)分别为44.22%、53.09%和3.94%, 峰位分别在0.11、2.51和27.54 μm附近.分散处理20 min时, 72.09%的颗粒分布在粒径0.02~0.48 μm间, 峰位在0.09 μm附近; 26.56%的颗粒分布在0.48~15.85 μm间, 其中在2.51 μm和4.36 μm处有两个较弱的分布峰; 此外, 有2.52%的颗粒分布在粒径15.85 μm以上.当分散处理40 min时, 83.34%的颗粒分布在0.01~0.48 μm间, 峰位在0.06 μm附近; 粒径大于0.48 μm的颗粒含量为17.26%, 其中在1.74 μm处有一个较弱的分布峰.可见, 随着超声分散时间的延长, 胡敏酸单体的粒径不断减小, 尤其是粒径大于1.00 μm的颗粒含量明显减小.
|
图 5 样品的粒径分布 Fig. 5 Particle size distributions of the samples |
|
|
表 2 样品的粒径分布数据 Table 2 Data for the particle size distributions of the samples |
针铁矿单体悬浮液超声分散处理10 min时, 粒径分布曲线由3部分组成.粒径在0.04~0.69 μm间有一个较强的分布峰, 其颗粒含量为34.78%, 峰位在0.16 μm附近; 在1.00~22.91 μm间有一个最强的分布峰, 其含量为61.39%, 峰位在3.63 μm附近; 在22.9~100 μm间有一个微弱的分布峰, 其含量为4.19%, 峰位在39.81 μm附近.分散处理20 min时, 粒径分布曲线中有两个强的分布峰, 其粒径范围分别为0.04~0.69 μm和0.69~15.85 μm, 含量分别为47.20%和50.49%, 峰位分别在0.16 μm和2.51 μm处; 粒径大于15.85 μm的颗粒含量为2.61%, 且没有出现明显的分布峰.分散处理40 min时, 粒径在0.04~0.69 μm间有一个很强的分布峰, 其含量达82.23%, 峰位在0.16 μm附近; 粒径在0.69~4.36 μm间有一个弱的分布峰, 其含量为16.54%, 峰位在1.74 μm附近; 粒径在4.36 μm以上的颗粒含量为1.33%.根据文献[34, 35], 粒径≤0.69 μm的颗粒为分散的针铁矿单粒, 粒径在1.00~22.91 μm和22.91~100 μm间的颗粒可分别归属于针铁矿的微团聚体和大团聚体.可见, 分散时间从10 min延长至40 min时, 针铁矿的大团聚体逐渐减少直至消失, 微团聚体的含量不断降低、粒径不断减小, 单粒的含量随分散时间的延长而明显升高.
针铁矿-胡敏酸复合物悬浮液超声分散处理10 min时, 44.00%的颗粒分布在粒径0.04~1.00 μm间, 峰位在0.19 μm附近; 36.76%的颗粒分布在1.00~15.85 μm间, 峰位在6.31 μm附近; 粒径大于15.85 μm的颗粒含量为21.65%, 峰位在27.54 μm附近.分散处理20 min时, 在0.04~1.00、1.00~15.85和15.85~100 μm间出现了3个粒径分布峰, 其颗粒含量分别为52.99%、33.26%和15.98%, 峰位分别在0.19、6.31和27.54 μm附近.分散处理40 min时, 粒径分布曲线中只出现了两个强的粒径分布峰, 其中57.15%颗粒分布在粒径0.04~1.20 μm间, 40.52%的颗粒在1.20~22.91 μm间, 峰位分别在0.19 μm和5.25 μm附近; 粒径大于22.91 μm的颗粒含量为3.48%.可见, 分散时间从10 min延长至40 min时, 复合物中大团聚体含量显著减少, 粒径在6 μm附近的微团聚体含量没有显著变化, 粒径在0.2 μm附近的颗粒含量略有增加.
样品的粒径分布数据表明, 针铁矿和胡敏酸两种单体的团聚体机械稳定性差, 随着超声处理时间的延长均显著解离成粒径更小的颗粒.针铁矿-胡敏酸复合物的机械稳定性则不同于两种单体:① 复合物的大团聚体含量较高, 但随着超声处理时间的延长大团聚体显著分解; ② 复合物微团聚体表现出了较高的稳定性, 随着超声处理时间的延长其含量变化不明显; ③ 复合物的各粒径分布峰位均大于针铁矿单体相应的粒径分布峰位, 且随超声时间的延长, 在粒径为0.19 μm和6.31 μm附近的颗粒含量变化较小.这表明复合物中针铁矿与胡敏酸确实发生了明显的界面胶结作用, 且超声分散处理不易破坏这类胶结作用.可见, 自然环境中氧化铁与腐殖酸之间的胶结作用, 有利于提高土壤黏粒之间的胶结力和土壤团聚体的稳定性.
3 结论酸性条件下, 胡敏酸可包被于针铁矿表面形成二元复合物.与针铁矿单体比较, 复合物中颗粒间的团聚更明显.针铁矿与胡敏酸交互作用后, COO-反对称伸缩振动和FeOH的红外振动带向低频率方向漂移, 表面缔合羟基的振动频率升高, 羧基C—O键和游离羟基的红外振动吸收带基本消失.与针铁矿和胡敏酸两种单体比较, 复合物中FeOH的失重峰温度明显升高, 而脂肪族和芳香族有机质的失重峰温度都明显降低了, 且复合物中脂肪族与芳香族有机质的失重量之比明显增大.随着样品悬浮液超声分散处理时间的延长, 胡敏酸和针铁矿两种单体中大颗粒(>2 μm)的含量都明显减少, 而复合物中大颗粒的峰位和含量却变化较小.复合物中针铁矿与胡敏酸之间确实发生了胶结作用, 且胡敏酸组分中热稳定性较差的脂肪族组分更容易与针铁矿胶结复合, 其中针铁矿表面Fe原子与胡敏酸结构中羧基官能团之间的单齿配位以及羟基之间的氢键都是二者胶结的重要机制.复合物中胡敏酸的包被作用增强了针铁矿的热稳定性; 复合物微团聚体的机械稳定性较强, 不易受到超声分散处理的破坏, 有利于提高土壤的抗冲蚀性能.
| [1] | Chen K Y, Chen T Y, Chan Y T, et al. Stabilization of natural organic matter by short-range-order iron hydroxides[J]. Environmental Science & Technology, 2016, 50(23): 12612-12620. |
| [2] | Tang Z, Zhao X L, Zhao T H, et al. Magnetic nanoparticles interaction with humic acid:in the presence of surfactants[J]. Environmental Science & Technology, 2016, 50(16): 8640-8648. |
| [3] | Conroy N A, Zavarin M, Kersting A B, et al. Effect of natural organic matter on plutonium sorption to goethite[J]. Environmental Science & Technology, 2017, 51(1): 699-708. |
| [4] | Saad E M, Sun J Y, Chen S, et al. Siderophore and organic acid promoted dissolution and transformation of Cr(Ⅲ) -Fe(Ⅲ) -(oxy) hydroxides[J]. Environmental Science & Technology, 2017, 51(6): 3223-3232. |
| [5] | Chen C M, Dynes J J, Wang J, et al. Properties of Fe-organic matter associations via coprecipitation versus adsorption[J]. Environmental Science & Technology, 2014, 48(23): 13751-13759. |
| [6] |
魏世勇, 谭文峰, 刘凡. 土壤腐殖质-矿物质交互作用的机制及研究进展[J]. 中国土壤与肥料, 2009(1): 1-6. Wei S Y, Tan W F, Liu F. Advances on the study of mineral-humus interactions in soils[J]. Soil and Fertilizer Sciences in China, 2009(1): 1-6. |
| [7] | Kebede M A, Bish D L, Losovyj Y, et al. The role of iron-bearing minerals in NO2 to HONO conversion on soil surfaces[J]. Environmental Science & Technology, 2016, 50(16): 8649-8660. |
| [8] | Jiang Y J, Goodwill J E, Tobiason J E, et al. Effect of different solutes, natural organic matter, and particulate Fe(Ⅲ) on ferrate(Ⅵ) decomposition in aqueous solutions[J]. Environmental Science & Technology, 2015, 49(5): 2841-2848. |
| [9] |
陈强, KravchenkoY S, 陈渊, 等. 少免耕土壤结构与导水能力的季节变化及其水保效果[J]. 土壤学报, 2014, 51(1): 11-21. Chen Q, Kravchenko Y S, Chen Y, et al. Seasonal variations of soil structures and hydraulic conductivities and their effects on soil and water conservation under no-tillage and reduced tillage[J]. Acta Pedologica Sinica, 2014, 51(1): 11-21. DOI:10.11766/trxb201304190189 |
| [10] |
董雪, 王春燕, 黄丽, 等. 侵蚀红壤腐殖酸组分特点及其对水稳性团聚体的影响[J]. 土壤学报, 2014, 51(1): 114-125. Dong Q, Wang C Y, Huang L, et al. Characteristics of humus fraction in erosion ultisols and their effects on water-stable aggregates[J]. Acta Pedologica Sinica, 2014, 51(1): 114-125. DOI:10.11766/trxb201302030067 |
| [11] |
邹翔, 崔鹏, 陈杰, 等. 小江流域土壤抗冲性实验研究[J]. 水土保持学报, 2004, 18(2): 71-73. Zou X, Cui P, Chen J, et al. Experiment study on anti-scouring of soil in Xiaojiang river basin[J]. Journal of Soil and Water Conservation, 2004, 18(2): 71-73. |
| [12] |
文倩, 关欣. 土壤团聚体形成的研究进展[J]. 干旱区研究, 2004, 21(4): 434-438. Wen Q, Guan X. Progress in the study on soil aggregate formation[J]. Arid Zone Research, 2004, 21(4): 434-438. |
| [13] | Cornell R M, Schwertmann U. The iron oxides:structure, properties, reactions occurences and uses (2nd ed.)[M]. Weinheim, Germany:Wiley-VCH, 2003. |
| [14] |
魏世勇, 刘凡, 冯雄汉, 等. 针铁矿-高岭石二元体的微观结构与形成机制[J]. 土壤学报, 2011, 48(2): 320-330. Wei S Y, Liu F, Feng X H, et al. Microstructure of goethite-kaolinite dyad and mechanism of its formation[J]. Acta Pedologica Sinica, 2011, 48(2): 320-330. DOI:10.11766/trxb200910210470 |
| [15] | Wei S Y, Tan W F, Zhao W, et al. Microstructure, interaction mechanisms, and stability of binary systems containing goethite and kaolinite[J]. Soil Science Society of America Journal, 2012, 76(2): 389-398. DOI:10.2136/sssaj2011.0065 |
| [16] | Gaffney J S, Marley N A, Clark S B. Humic and fulvic acids:isolation, structure, and environmental role[A]. In:Proceedings of a Symposium at the 210th American Chemical Society's National Meeting[C]. Chicago, Illinois, USA:American Chemical Society, 1995. |
| [17] | Schellekens J, Buurman P, Kalbitz K, et al. Molecular features of humic acids and fulvic acids from contrasting environments[J]. Environmental Science & Technology, 2017, 51(3): 1330-1339. |
| [18] | Hagvall K, Persson P, Karlsson T. Spectroscopic characterization of the coordination chemistry and hydrolysis of gallium(Ⅲ) in the presence of aquatic organic matter[J]. Geochimica et Cosmochimica Acta, 2014, 146: 76-89. DOI:10.1016/j.gca.2014.10.006 |
| [19] | Bollyn J, Nijsen M, Baken S, et al. Polyphosphates and fulvates enhance environmental stability of PO4-bearing colloidal iron oxyhydroxides[J]. Journal of Agricultural and Food Chemistry, 2016, 64(45): 8465-8473. DOI:10.1021/acs.jafc.6b02425 |
| [20] | Kovaács K, Czech V, Fodor F, et al. Characterization of Fe-leonardite complexes as novel natural iron fertilizers[J]. Journal of Agricultural and Food Chemistry, 2013, 61(50): 12200-12210. DOI:10.1021/jf404455y |
| [21] | Weber T, Allard T, Tipping E, et al. Modeling iron binding to organic matter[J]. Environmental Science & Technology, 2006, 40(24): 7488-7493. |
| [22] | Yang Y, Saiers J E, Barnett M O. Impact of interactions between natural organic matter and metal oxides on the desorption kinetics of uranium from heterogeneous colloidal suspensions[J]. Environmental Science & Technology, 2013, 47(6): 2661-2669. |
| [23] | Neubauer E, Köhler S J, von der Kammer F, et al. Effect of pH and stream order on iron and arsenic speciation in boreal catchments[J]. Environmental Science & Technology, 2013, 47(13): 7120-7128. |
| [24] | Xiong J, Koopal L K, Weng L P, et al. Effect of soil fulvic and humic acid on binding of Pb to goethite-water interface:linear additivity and volume fractions of HS in the Stern layer[J]. Journal of Colloid and Interface Science, 2015, 457: 121-130. DOI:10.1016/j.jcis.2015.07.001 |
| [25] | ThomasArrigo L K, Mikutta C, Byrne J, et al. Iron and arsenic speciation and distribution in organic flocs from streambeds of an arsenic-enriched peatland[J]. Environmental Science & Technology, 2014, 48(22): 13218-13228. |
| [26] | Shaker A M, Komy Z R, Heggy S E M, et al. Kinetic study for adsorption humic acid on soil minerals[J]. The Journal of Physical Chemistry A, 2012, 116(45): 10889-10896. DOI:10.1021/jp3078826 |
| [27] | Schwertmann U, Cornell R M. Iron oxides in the laboratory:preparation and characterization[M]. Weinheim:John Wiley & Sons, 2000. |
| [28] | 翁诗甫. 傅里叶变换红外光谱分析[M]. 北京: 化学工业出版社, 2010. |
| [29] |
顾志忙, 王晓蓉, 顾雪元, 等. 傅里叶变换红外光谱和核磁共振法对土壤中腐殖酸的表征[J]. 分析化学, 2000, 28(3): 314-317. Gu Z M, Wang X R, Gu X Y, et al. Characterization of humic acid extracted from different soils by Fourier transform infrared spectrometry and nuclear magnetic resonance specteoscopy[J]. Chinese Journal of Analytical Chemistry, 2000, 28(3): 314-317. |
| [30] | Karlsson T, Persson P. Complexes with aquatic organic matter suppress hydrolysis and precipitation of Fe(Ⅲ)[J]. Chemical Geology, 2012, 322-323: 19-27. DOI:10.1016/j.chemgeo.2012.06.003 |
| [31] |
刘茜. 胡敏酸-氧化铁-高岭石复合体的形成与表征[D]. 武汉: 华中农业大学, 2009. Liu Q. Interaction between humic acid, iron oxides and kaolinite, and their characteristics[D]. Wuhan:Huazhong Agricultural University, 2009. http://cdmd.cnki.com.cn/Article/CDMD-10504-2010010577.htm |
| [32] |
朱晓, 陈天虎, 颜玲, 等. 黄铁矿-针铁矿混合无氧焙烧产物物相演变和特性[J]. 硅酸盐学报, 2014, 42(11): 1435-1440. Zhu X, Chen T H, Yan L, et al. Phase evolution and performance characteristics of pyrite-goethite anaerobic roasting product[J]. Journal of the Chinese Ceramic Society, 2014, 42(11): 1435-1440. |
| [33] | Kang S, Xing B S. Humic acid fractionation upon sequential adsorption onto goethite[J]. Langmuir, 2008, 24(6): 2525-2531. DOI:10.1021/la702914q |
| [34] |
吴思源, 练有为, 郑红, 等. 制备条件对合成针铁矿的影响[J]. 环境化学, 2012, 31(10): 1625-1630. Wu S Y, Lian Y W, Zheng H, et al. Influence of preparation conditions on synthetic goethite[J]. Environmental Chemistry, 2012, 31(10): 1625-1630. |
| [35] |
方继敏. 铁(氢)氧化物的制备、负载及对HIOCs类污染物的吸附研究[D]. 武汉: 武汉理工大学, 2008. Fang J M. Research on iron (Hydr) oxide preparation and loading and adsorption of HIOCs pollutants[D]. Wuhan:Wuhan University of Technology, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10497-2009084818.htm |
 2017, Vol. 38
2017, Vol. 38


