好氧颗粒污泥(AGS)是微生物在一定的环境条件下自发凝聚、增殖形成的结构紧密、沉降性能良好的生物颗粒[1].与传统的活性污泥相比, 好氧颗粒污泥具有相对密度大、沉降速度快、污泥产率低[2, 3]、耐冲击负荷等优点[4], 同时还具有较好的脱氮除磷性能, 在废水处理领域中具有较好的应用前途.但是好氧颗粒污泥快速颗粒化及其稳定运行一直是限制其实际应用的最大瓶颈.国内外许多学者对促进好氧颗粒污泥形成因素进行了广泛研究[5~9].有研究表明, 虽然加入Zn2+、Mg2+、Ca2+等无机金属离子有利于促进污泥的颗粒化, 但是过高的金属浓度会使金属离子对微生物产生毒性, 使污泥生物活性降低.近年来一些研究表明, 一些惰性载体或者解体的颗粒污泥碎片等都可以作为好氧颗粒污泥形成的“成核”物质[10, 11].这些成核载体具有良好的表面性能, 并有效增加其抗冲击负荷能力[12], 从而能增加好氧颗粒污泥的长期稳定运行性能.
其中, 活性炭由于其具有较好的吸附性和价格低廉等优点, 投加在水体中能够促进污泥的颗粒化进程, 提高污水处理效能, 因而被广泛地应用于污水处理系统中.高阳等[13]在气升式内循环间歇式反应器(SBAR)加入了粒径为830~1 700 μm的颗粒活性炭, 研究发现加入颗粒活性炭可加速好氧颗粒污泥的颗粒化进程, 缩短颗粒化时间, 且污泥恢复活性的时间也比传统的活性污泥短, 同时也能提高反应器对总氮(TN)的去除率.高景峰等[14]研究表明在SBR系统启动初期加入一定比例的颗粒活性炭诱导AGS的形成是可行的.虽然上述研究表明污水生物处理系统中投加活性炭能促进污泥颗粒化, 提高其除污性能, 但是目前关于不同粒径活性炭对污泥颗粒化进程的影响报道不多; 并且, 如何对生物污泥系统中加入的活性炭回收重复利用又是一大难题.因此, 本论文基于好氧颗粒污泥“成核假说”以及“微磁场生物效应”的基本原理, 并从外加磁场对磁性材料加以分离重复利用角度考虑, 在SBR系统中投加不同粒径的磁性活性炭, 以单独的活性污泥系统为对照, 从污泥形态变化、粒径分布特征、沉降性能等方面评价不同粒径磁性活性炭对AGS形成的影响, 探讨磁性活性炭基好氧颗粒污泥的形成机制, 以期为推进好氧颗粒污泥进一步实际工程应用提供可靠的理论和实验依据.
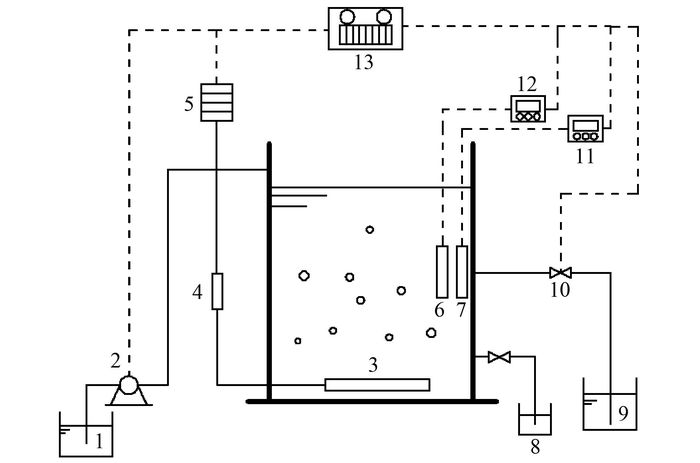
1 材料与方法 1.1 实验材料 1.1.1 实验装置及运行方式采用5个相同的序批式活性污泥反应器(SBR)(图 1), 高径比为2:1, 有效容积为1.5 L, 空气压缩机通过砂芯曝气头提供曝气, 并通过气体转子流量计控制气体流量. 1号反应器为单独的活性污泥系统(对照组), 其他4个反应器分别在活性污泥反应器内投加1.5 g·L-1的80目(2号)、140目(3号)、200目(4号)和300目(5号)的磁性活性炭.反应器均置于30℃的恒温水浴锅中运行, 通过气体转子流量计调节曝气量为300mL·min-1左右(DO约为4.0 mg·L-1). 1 d运行2个周期, 每个周期为12 h, 包括进水0.5 h, 曝气8 h, 沉淀时间(20~1 min)(根据运行时间逐步缩短), 排水0.5 h, 剩余时间为静置, 每次排水为反应器容积的50%.
|
1.进水箱; 2.进水泵; 3.曝气盘; 4.气体流量计; 5.曝气泵; 6、7.pH计、DO仪探头; 8.排泥箱; 9.出水箱; 10.出水控制阀; 11.溶解氧仪; 12.pH计; 13.自动控制箱 图 1 实验装置流程示意 Fig. 1 Schematic diagram of experiment apparatus |
实验所用接种污泥取自成都科雅污水处理厂二期曝气池中的污泥, 反应器中的污泥接种量约为反应器有效容积的40%, 接种后的污泥浓度(MLSS)为4.279 g·L-1, 污泥体积指数(SVI)为202.2 mL·g-1.
1.1.2 磁性活性炭的制备[15]分别将不同粒径的活性炭浸没在HNO3溶液中搅拌, 洗涤过滤后于105℃下在干燥箱中干燥过夜, 得到改性活性炭.称取改性活性炭分散于Fe(NO3)3·9H2O水溶液中超声溶解, 将所得颗粒过滤干燥; 干燥后的颗粒在纯氮气的氛围中于管式炉中煅烧, 所得样品为磁性活性炭复合材料.
1.1.3 实验用水本次实验中采用人工模拟废水为进水水质.其中葡萄糖、柠檬酸三钠提供碳源, 硫酸铵提供氮源, 磷酸二氢钾提供磷源, 同时外加少量的Fe2+, Ca2+, Cu2+等微量元素[16].进水水质:ρ(COD)为120~240 mg·L-1, ρ(TN)为40~50 mg·L-1, ρ(TP)为2~4 mg·L-1, ρ(NH4+-N)为35~45 mg·L-1, pH维持在7.0~7.2.
1.2 实验分析方法 1.2.1 水质和污泥指标分析方法水质指标COD、TN、TP、NH4+-N以及主要的污泥浓度MLSS、MLVSS和污泥体积指数SVI等的测定均采用国家标准方法[17]; 污泥的形态外观用相机进行观察, EPS的提取采用离心方法, PN采用修正的Lowry法测定[18], PS采用蒽酮-硫酸法测定[19].
1.2.2 污泥粒径分析采用高斯正态分布计算污泥的平均粒径与标准偏差[20].
高斯函数拟合公式为:
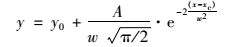
|
式中, y为粒径分布函数; y0为y轴偏移量; A为常数项; x为污泥的粒径; xc为污泥平均粒径; w为标准偏差, 反映了拟合后的曲线分布宽度.
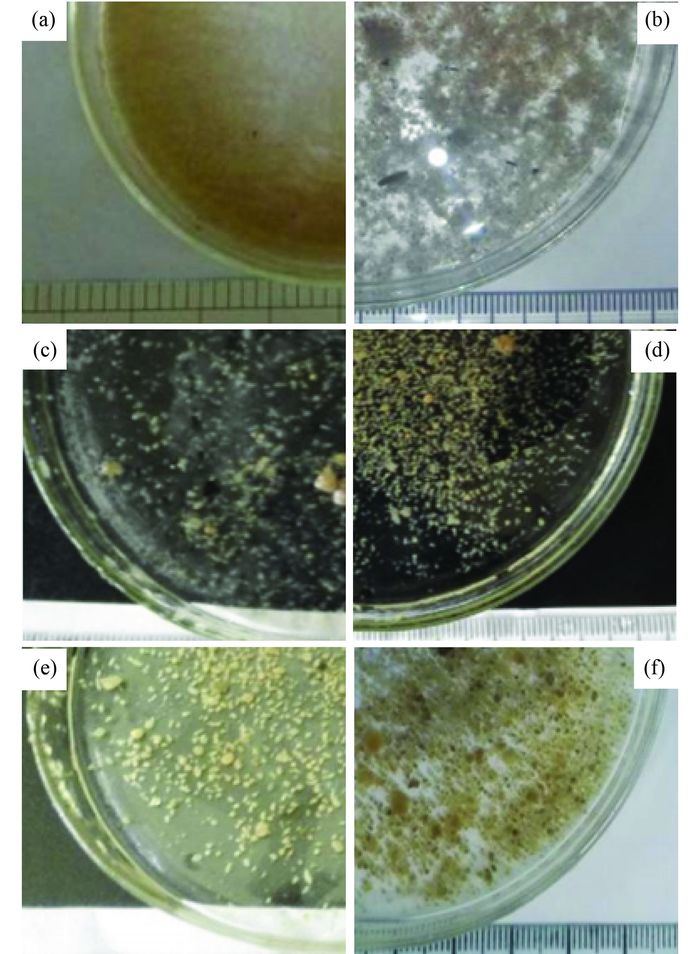
2 结果与讨论 2.1 污泥指标变化 2.1.1 污泥形态变化反应器接种污泥为絮状, 黄褐色[图 2(a)].运行30 d后各反应器相继出现污泥聚集形成颗粒污泥的现象. 1号反应器中污泥沉降性能较接种污泥好, 开始聚集成团, 但形成的团状污泥结构较松散[图 2(b)]. 2号反应器的污泥出现了少量结构紧密的颗粒污泥[图 2(c)], 但通过对反应器内部观察, 发现2号反应器投加的磁性活性炭的粒径相对较大, 部分沉于反应器底部, 不利于活性污泥将其作为“晶核”而快速形成颗粒污泥.而投加140目和200目磁性活性炭的3号和4号反应器中形成了明显的好氧颗粒污泥, 其结构较紧密, 形成的颗粒污泥直径大多数在0.6~0.8 mm之间, 沉降性能最好[图 2(d)和图 2(e)].而投加300目磁性活性炭的5号反应器中, 污泥颗粒化程度比1号反应器高, 但明显低于3号和4号反应器[图 2(f)].因此, 从反应器内污泥颗粒化程度来看, 投加磁性活性炭的反应器均高于1号反应器.同时, 投加不同粒径的磁性活性炭对污泥颗粒化程度的影响也有明显的不同. 80目的磁性活性炭由于其粒径太大, 易沉降在反应器底部, 不利于作为污泥颗粒化“成核”载体; 300目的磁性活性炭由于粒径过小, 部分活性炭容易漂浮在水面上, 初始排水时易被排走; 而140目和200目的磁性活性炭, 很容易以其为“晶核”形成好氧颗粒污泥, 并且形成的颗粒污泥结构紧密, 沉降速率快.
|
(a)接种污泥; (b)~(f)分别是1、2、3、4和5号反应器运行第30 d的污泥 图 2 污泥拍照外观形态 Fig. 2 Morphological observation of the sludge |
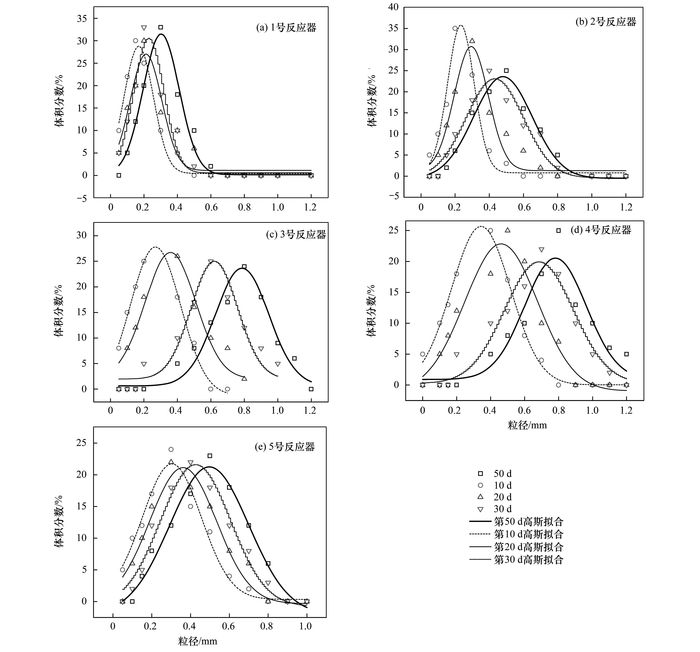
污泥的粒径分布是评价污泥颗粒化程度的一个重要指标.采用高斯正态分布来分析各反应器颗粒化进程中污泥的粒径分布特征(图 3).在各反应器启动运行的前10 d内, 污泥的粒径大部分在0.2 mm以下, 污泥呈絮状, 沉降性能差.随着各反应器的运行, 反应系统内污泥的粒径分布开始出现不同的分布情况.第30 d时, 1号反应器内小于0.2 mm粒径的污泥仍然占多数; 相对于对照组, 2号反应器内的污泥粒径有所增加, 多集中于0.3~0.6 mm之间; 而投加140目和200目磁性活性炭的3号和4号反应器内, 污泥粒径多集中在0.6~0.8 mm之间, 与此同时, 5号反应器内污泥粒径多集中于0.4~0.7 mm之间.可见, 相对于其他反应器, 3号和4号反应器的污泥平均粒径稍大一点, 且这两个系统内颗粒污泥所占的体积分数较大, 污泥颗粒化程度较高, 表明该粒径范围内的磁性活性炭对污泥的颗粒化有较好的促进作用.当反应器运行到第50 d时, 3号和4号两反应器内污泥粒径大都达到0.8 mm以上, 污泥颗粒化已基本完成.
|
图 3 各反应器内污泥粒径分布及高斯拟合 Fig. 3 Characteristics of particle size distribution and Gaussian distribution |
各反应器运行阶段污泥粒径分布的高斯拟合及参数结果如图 3和表 1所示. 1号反应器运行10 d时污泥平均粒径xc为168.4 μm, 反应进行50 d时, 污泥平均粒径xc有所增大, 为302.7 μm, 标准偏差w也由第10 d的174.5 μm变为第50 d的216.2 μm; 2号反应器, xc由第10 d时的233.8 μm增加到第50 d时的479.9 μm, w由155.3 μm变到342.9 μm; 3号反应器, xc由268.8 μm增加至786.6 μm, w由301.2 μm增至318.9 μm; 4号反应器, xc由343.6 μm增至781.5 μm, w由347.7 μm增至362.3 μm; 5号反应器, 污泥平均粒径xc由303.9 μm增至496.8 μm, w由303.6 μm增至406.7 μm.可见投加磁性活性炭反应器内的污泥的平均粒径均高于1号反应器, 同时投加不同粒径磁性活性炭反应器的污泥粒径分布也有一定差别.将50 d时各反应器内的污泥粒径进行比较, 发现3号和4号反应器内的污泥平均粒径均在780 μm左右, 高于其他反应器, 而两反应器的标准偏差分别为318.9 μm和362.3 μm, 相对于其他投加磁性活性炭的2号和5号反应器内的标准偏差较小, 说明3号和4号反应器内形成的颗粒污泥粒径较均匀, 颗粒污泥较稳定.
|
|
表 1 高斯曲线描述粒径分布拟合参数/μm Table 1 Size distribution of aerobic granules fitted using the Gauss function/μm |
2.1.3 污泥SVI指标
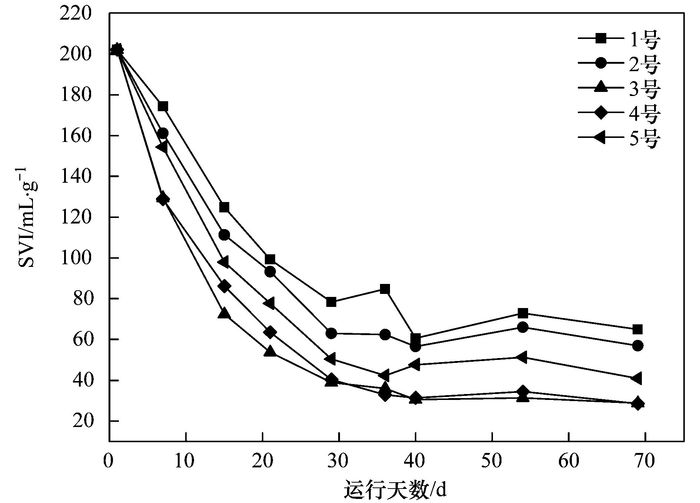
污泥体积指数(SVI)是对污泥沉降性能评价的一个重要指标, SVI值越低, 表明污泥的沉降性能就越好.本实验中, 各反应器运行过程中SVI的变化如图 4所示.各反应器接种污泥的污泥体积指数SVI均为202.2 mg·L-1, 随着各反应器不断运行, 前30 d内, 反应系统中污泥体积指数SVI都呈明显下降趋势; 相对于1号、2号和5号反应器, 3号和4号反应器内污泥体积指数SVI下降幅度最大, 第30 d时, 3号、4号反应器内的污泥的SVI值分别降到了40.32mL·g-1与38.9 mL·g-1, 污泥的沉降性能较其他反应器的好, 这和前面3号与4号反应器内的污泥形态变化结果一致, 即投加140目与200目的磁性活性炭能明显提高污泥的沉降性能, 加快污泥颗粒化进程.在反应器运行到第70 d时, 3号、4号反应器内污泥SVI值分别为28.5 mL·g-1与28.8 mL·g-1, 明显低于其他反应器.
|
图 4 污泥体积指数SVI变化 Fig. 4 Changes in the SVI during operation of the reactor |
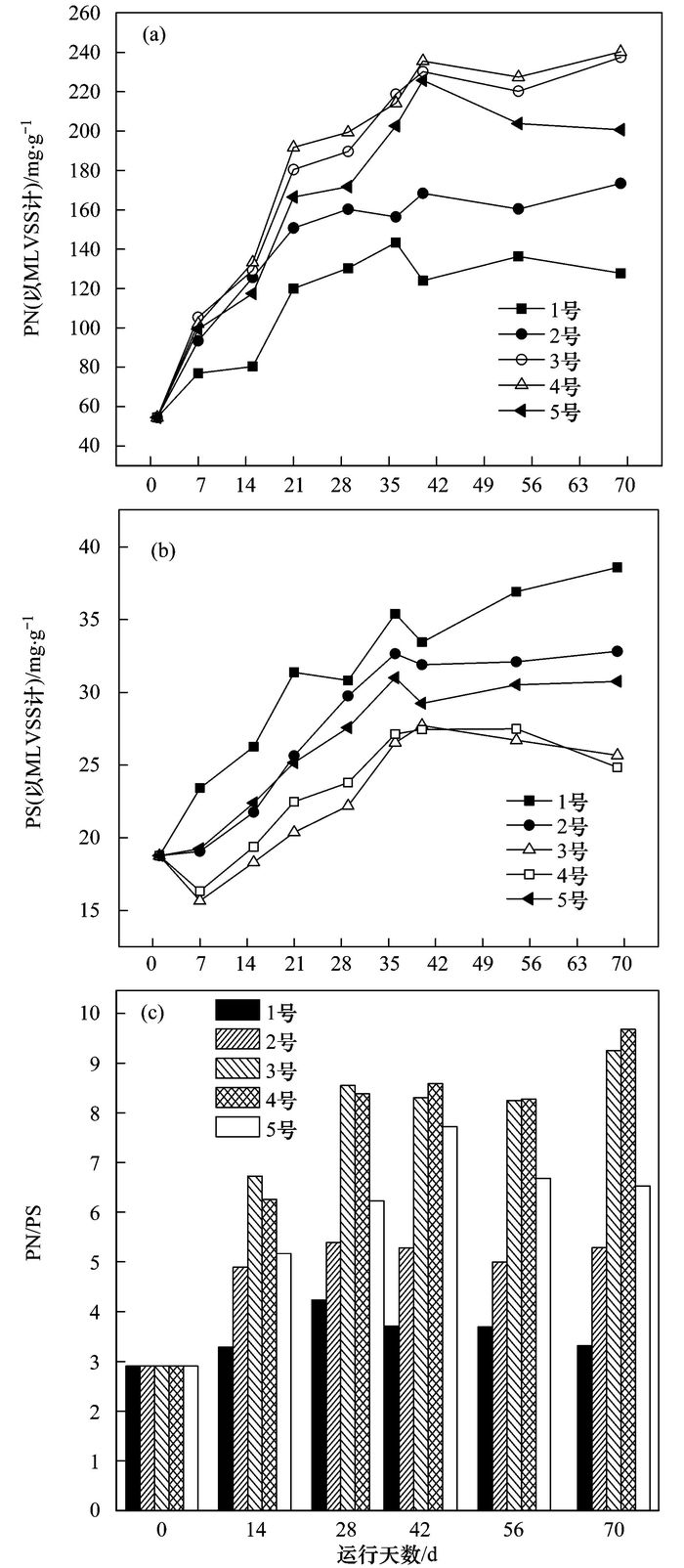
胞外聚合物(EPS)是微生物在新陈代谢过程中分泌的高分子有机物, 主要包括胞外蛋白质(PN)和胞外多糖(PS).本实验中, 各反应器内污泥的PN、PS含量以及PN/PS比值的变化如图 5所示.接种污泥的PN含量为54.55 mg·g-1, 随着反应时间的进行, 各反应器内的PN都呈逐渐升高的趋势, 投加磁性活性炭的各SBR系统中污泥的PN均高于1号反应器.反应器运行到第30 d时, 1、2、3、4和5号反应器污泥PN含量分别为130.28、160.37、189.65、199.37和171.78 mg·g-1.并且, 污泥中的PN含量随着投加磁性活性炭粒径的减小呈先增加明显, 后增加缓慢的趋势[图 5(a)].各反应器接种污泥的PS为18.77 mg·g-1, 随着各反应器的运行, 各反应器内污泥的PS也呈逐步升高的趋势, 但是增加幅度不是很大, 第30 d时, 投加140目和200目磁性活性炭的3号和4号的反应器内污泥PS的含量分别为22.19和23.78 mg·g-1, 低于其他3个反应器[图 5(b)].通过进一步对各反应器PN/PS的比值[图 5(c)]分析发现, 随着反应器的不断运行, 颗粒化程度明显的3号和4号反应器的PN/PS的比值均高于其他3个反应器, 第30 d时, 其PN/PS的比值分别为8.55和8.38, 而此时1、2和5号反应器的PN/PS值分别为4.24、5.39和6.23.实验结果表明, 一方面, 投加磁性活性炭有利于促进污泥胞外蛋白质PN, 对胞外多糖PS的含量影响不大, 合适的磁性活性炭粒径(140目和200目)更有利于污泥PN的分泌, PN含量越多, 越有利于污泥颗粒化.另一方面, PN/PS比值越高, 其对应的污泥反应器内颗粒程度越高, 说明较高的PN/PS比值有利于污泥的颗粒化及颗粒污泥的稳定维系.
|
图 5 各反应器污泥PN、PS含量及PN/PS的变化 Fig. 5 Changes of PN, PS, and PN/PS ratio |
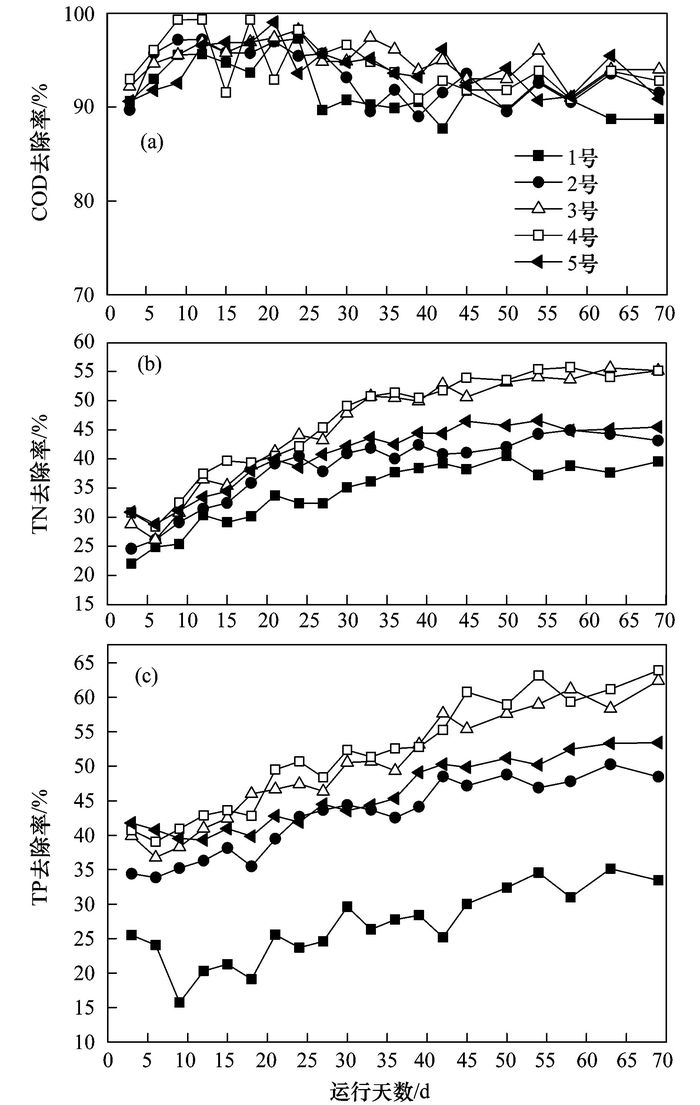
各反应器对污水中COD、TN和TP的去除效果见图 6.各反应器对COD的去除效率都很高, 反应器运行初期, 各反应器COD的去除率基本保持在90%左右, 相差不是很大[图 6(a)], 而各反应器对TN和TP的去除率相差比较明显[图 6(b)和图 6(c)].各反应器对废水TN的去除率在反应初期都比较低, 差别也不是很大, 但是随着反应器的连续运行, 各反应器对废水TN的去除率都有所上升; 同时伴随着3号和4号反应器颗粒化程度的不断提高, 第30 d后, 3号和4号反应器对废水TN的平均去除率均达到50%以上, 明显高于1号和2号反应器[图 6(b)].反应器运行刚开始时, 1号反应器对TP的去除率明显低于其他各组反应器, 这说明系统中投加了不同粒径的磁性活性炭能明显增加对污水处理系统中TP的去除率效果; 随着反应器的继续运行, 各反应器内污泥的颗粒化不同, 导致其对总磷的去除效果差别越来越明显.反应器运行末期, 3号与4号反应器对TP去除效率平均达到了60%以上, 明显高于其他反应器[图 6(c)].一定粒径磁性活性炭的加入能提高SBR系统的除污性能, 尤其是明显提高反应器去除氮、磷的性能.其原因在于:一是因为磁性活性炭的吸附和污泥微生物氧化分解的协同作用, 磁性活性炭的大量微孔吸附了废水中的污染物质, 为微生物群的生长繁殖提供了高浓度的营养源, 而微生物代谢过程中产生的酶和辅酶又被吸附和富集在磁性活性炭的孔隙中, 这样就会促使附着在磁性活性炭上的微生物和污染物质接触时间变长有利于污染的分解或转化; 二是因为以磁性活性炭为“晶核”形成的好氧颗粒污泥, 其独特的空间立体结构形成了好氧-厌氧的微观区域环境, 有利于实现同步脱氮除磷; 再者, 投加磁性活性炭组的各反应器在反应器后期均明显高于对照组1号反应器, 说明随着各反应器的不断运行, 各反应器内投加的磁性活性炭的微磁学效应发挥重要的作用, 合适的磁学效应可以加快活性污泥的硝化速率[21], 改变了反应器内关键脱氮除磷菌群的组成[22], 并有利改善颗粒污泥处理系统的稳定性[23].
|
图 6 反应器对污水中COD、TN和TP的去除效果 Fig. 6 Removal efficiency of COD, TN, and TP |
本实验中加载不同粒径磁性活性炭的反应器内污泥平均粒径均高于对照组, 呈现出较明显促进污泥颗粒化的现象.活性污泥系统中加载载体材料促进污泥颗粒化进程可用“惰性内核模型”来解释[14].投加的磁性活性炭主要从两个方面影响活性污泥.一方面, 可作为污泥颗粒化的“成核”载体, 反应器内有大量的胚胎颗粒污泥产生后, 随之反应系统内的水力条件形成的气、液、固微环境发生了变化, 胚胎颗粒污泥之间相互碰撞的机会增多; 加上污泥胞外聚合物EPS含量的增加, 会增进污泥细胞之间的相互粘连, 尤其是胞外蛋白PN的显著增加, 能改变污泥表面的相对疏水性, 从而增加污泥之间的凝聚作用, 促使胚胎颗粒污泥能更快地聚集成更大的颗粒污泥.另一方面, 磁性活性炭的投加会影响活性污泥系统中微生物的种群、活性和数量.磁性活性炭具有良好的比表面积, 有利于富集生长速率较慢的硝化细菌等脱氮菌群, 从而避免因传质阻力引起的污泥颗粒内部分裂, 可提高好氧颗粒污泥系统的稳定性; 再者, 良好的磁学效应, 能提高污泥系统微生物活性和新陈代谢作用, 从而达到提高系统脱氮除磷的处理效果.
目前, 虽然有一些关于加载惰性载体促进污泥颗粒化的研究报道[21~23], 但是关于加载不同粒径的磁性活性炭载体对污泥颗粒化的影响鲜有报道.本研究表明, 不同粒径的磁性活性炭对污泥的性能及颗粒化程度方面存在一定的差异.载体粒径过大、过小都不利于其作为好氧颗粒污泥快速成核的有效载体, 其原因在于:若粒径过大, 部分磁性活性炭会沉在反应器底部, 从而导致活性污泥与载体的接触碰撞机会减少, 不利于微生物在载体表面附着生长, 不易形成以磁性活性炭为内核的颗粒污泥.从水力学条件出发, 若加载该粒径范围的磁性活性炭, 要达到比较好的污泥颗粒化效果, 可能会通过增加曝气量、水力剪切力等途径增加污泥和载体之间的接触和碰撞, 这样势必会引起能耗的增加.若粒径过小, 在反应启动初期, 其部分载体会浮于反应器水体表面, 随着反应器的出水而流失, 加上载体粒径过小, 其比表面积越大, 微生物在其表面的生长也会受到一定的限制, 从而导致污泥颗粒化进程缓慢.
3 结论(1) SBR系统中加载磁性活性炭有利于好氧颗粒污泥的形成.磁性活性炭粒径大小对好氧颗粒污泥的形成有一定的影响; 载体粒径过大、过小都不利于其作为好氧颗粒污泥快速成核的有效载体; 粒径为140目和200目磁性活性炭有利于好氧颗粒污泥的形成.
(2) SBR系统中加载不同粒径的磁性活性炭对污泥粒径分布有一定影响.投加140目和200目磁性活性炭的3号和4号反应器内的污泥平均粒径均高于其他反应器; 两反应器的标准偏差较小, 形成的颗粒污泥粒径较均匀, 颗粒污泥较稳定.
(3) 活性污泥系统中加载磁性活性炭材料促进污泥颗粒化进程可用“惰性内核模型”来解释.一方面, 磁性活性炭可作为污泥颗粒化的“成核”载体; 另一方面, 磁性活性炭良好磁学效应能增强微生物活性和新陈代谢作用, 提高反应系统脱氮除磷性能.
| [1] |
梁梦晓, 倪晋仁. SBR中好氧颗粒污泥的培养及特性研究[J]. 应用基础与工程科学学报, 2009, 17(4): 502-512. Liang M X, Ni J R. Cultivation and characteristics of aerobic granular sludge in sequencing batch reactor[J]. Journal of Basic Science and Engineering, 2009, 17(4): 502-512. |
| [2] | Nancharaiah Y V, Venugopalan V P. Denitrification of synthetic concentrated nitrate wastes by aerobic granular sludge under anoxic conditions[J]. Chemosphere, 2011, 85(4): 683-688. DOI:10.1016/j.chemosphere.2011.06.077 |
| [3] | Lotito A M, Fratino U, Mancini A, et al. Effective aerobic granular sludge treatment of a real dyeing textile wastewater[J]. International Biodeterioration & Biodegradation, 2012, 69: 62-68. |
| [4] |
陈冉妮, 高景峰, 郭建秋, 等. 好氧颗粒污泥同步脱氮除磷的常温启动和低温维持[J]. 环境科学, 2009, 30(10): 2995-3001. Chen R N, Gao J F, Guo J Q, et al. Simultaneous nitrogen and phosphorus removal by aerobic granular sludge at normal and low temperatures[J]. Environmental Science, 2009, 30(10): 2995-3001. DOI:10.3321/j.issn:0250-3301.2009.10.030 |
| [5] | Jiang H L, Tay J H, Liu Y, et al. Ca2+ Augmentation for enhancement of aerobically grown microbial granules in sludge blanket reactors[J]. Biotechnology Letters, 2003, 25(2): 95-99. DOI:10.1023/A:1021967914544 |
| [6] |
刘绍根, 孙菁, 徐锐. Ca2+、Mg2+对好氧污泥快速颗粒化的影响研究[J]. 环境科学学报, 2015, 35(1): 168-176. Liu S G, Sun J, Xu R. Effects of Ca2+ and Mg2+ on rapid granulation of aerobic sludge[J]. Acta Scientiae Circumstantiae, 2015, 35(1): 168-176. |
| [7] |
巢少峰, 冒文娟, 郑晓英, 等. Cu2+对好氧颗粒污泥理化特性的影响分析[J]. 河海大学学报(自然科学版), 2014, 42(5): 399-403. Chao S F, Mao W J, Zheng X Y, et al. Analysis of influence of Cu2+ on physicochemical characteristics of aerobic granular sludge[J]. Journal of Hohai University (Natural Sciences), 2014, 42(5): 399-403. |
| [8] |
郑晓英, 吴颜科, 陈卫, 等. Zn(Ⅱ)长期作用对好氧颗粒污泥基本性能与污染物去除功效的影响[J]. 河海大学学报(自然科学版), 2015, 43(1): 49-53. Zhen X Y, Wu Y K, Chen W, et al. Long-term effects of Zn(Ⅱ) on properties and pollutant removal efficiencies of aerobic granular sludge[J]. Journal of Hohai University (Natural Sciences), 2015, 43(1): 49-53. |
| [9] |
金雪瓶, 邓风. Ce3+对好氧颗粒污泥培养的影响[J]. 化工环保, 2013, 33(2): 103-107. Jin X P, Deng F. Effect of Ce3+ on cultivation of aerobic granular sludge[J]. Environmental Protection of Chemical Industry, 2013, 33(2): 103-107. |
| [10] | Wang S G, Gai L H, Zhao L J, et al. Aerobic granules for low-strength wastewater treatment:formation, structure, and microbial community[J]. Journal of Chemical Technology and Biotechnology, 2009, 84(7): 1015-1020. DOI:10.1002/jctb.v84:7 |
| [11] | Zhou J H, Zhao H, Hu M, et al. Granular activated carbon as nucleating agent for aerobic sludge granulation:effect of GAC size on velocity field differences (GAC versus flocs) and aggregation behavior[J]. Bioresource Technology, 2015, 198: 358-363. DOI:10.1016/j.biortech.2015.08.155 |
| [12] | Zhou D D, Liu M Y, Gao L L, et al. Calcium accumulation characterization in the aerobic granules cultivated in a continuous-flow airlift bioreactor[J]. Biotechnology Letters, 2013, 35(6): 871-877. DOI:10.1007/s10529-013-1157-y |
| [13] |
高阳, 徐晓晨, 徐光景, 等. 活性炭为载体的好氧颗粒污泥培养及性能研究[J]. 水资源与水工程学报, 2012, 23(5): 25-28. Gao Y, Xu X C, Xu G J, et al. Research on cultivation and performance of aerobic granular sludge using activated carbon as carrier[J]. Journal of Water Resources & Water Engineering, 2012, 23(5): 25-28. |
| [14] |
高景峰, 张倩, 王金惠, 等. 颗粒活性炭对SBR反应器中好氧颗粒污泥培养的影响研究[J]. 应用基础与工程科学学报, 2012, 20(3): 345-354. Gao J F, Zhang Q, Wang J H, et al. Enhanced aerobic sludge granulation in sequencing batch reactor by granular activated carbon augmentation[J]. Journal of Basic Science and Engineering, 2012, 20(3): 345-354. |
| [15] | Shahamat Y D, Farzadkia M, Nasseri S, et al. Magnetic heterogeneous catalytic ozonation:a new removal method for phenol in industrial wastewater[J]. Journal of Environmental Health Science and Engineering, 2014, 12(1): 50. DOI:10.1186/2052-336X-12-50 |
| [16] | Xin X, Lu H, Yao L, et al. Rapid formation of aerobic granular sludge and its mechanism in a continuous-flow bioreactor[J]. Applied Biochemistry and Biotechnology, 2017, 181(1): 424-433. DOI:10.1007/s12010-016-2221-6 |
| [17] | 国家环境保护总局. 水和废水监测分析方法[M]. 第四版. 北京: 中国环境科学出版社, 2002. |
| [18] | 宁正祥. 食品成分分析手册[M]. 北京: 中国轻工业出版社, 1998. |
| [19] | Frølund B, Palmgren R, Keiding K, et al. Extraction of extracellular polymers from activated sludge using a cation exchange resin[J]. Water Research, 1996, 30(8): 1749-1758. DOI:10.1016/0043-1354(95)00323-1 |
| [20] | Su K Z, Yu H Q. Formation and characterization of aerobic granules in a sequencing batch reactor treating soybean-processing wastewater[J]. Environmental Science & Technology, 2005, 39(8): 2818-2827. |
| [21] | Tomska A, Wolny L. Enhancement of biological wastewater treatment by magnetic field exposure[J]. Desalination, 2008, 222(1-3): 368-373. DOI:10.1016/j.desal.2007.01.144 |
| [22] | Li A J, Li X Y, Yu H Q. Aerobic sludge granulation facilitated by activated carbon for partial nitrification treatment of ammonia-rich wastewater[J]. Chemical Engineering Journal, 2013, 218: 253-259. DOI:10.1016/j.cej.2012.12.044 |
| [23] | Li B, Huang W L, Zhang C, et al. Effect of TiO2 nanoparticles on aerobic granulation of algal-bacterial symbiosis system and nutrients removal from synthetic wastewater[J]. Bioresource Technology, 2015, 187: 214-220. DOI:10.1016/j.biortech.2015.03.118 |
 2017, Vol. 38
2017, Vol. 38

