2. 中国科学院大学资源与环境学院, 北京 100049
2. College of Resources and Environment, University of Chinese Academy of Sciences, Beijing 100049, China
印染废水是公认难降解的工业废水之一, 具有高色度、高化学需氧量及“三致”毒性, 对水环境产生极大的隐患[1].传统的处理方法如吸附法、好氧生物处理等, 不能有效地去除污染物, 而且易造成二次污染[2].近年来, 光催化氧化技术作为一种新型绿色的处理方法, 能快速有效地去除难降解有机污染物, 成为染料废水处理技术研究的热点.传统的光催化剂主要有金属氧化物、金属硫化物和多金属氧酸盐等[3, 4].其中, 应用最广泛的为TiO2, 但是其带隙较宽(约为3.2 eV), 仅能吸收占太阳光能量4%的紫外线[4].因此, 开发新型、高效的可见光催化材料是十分必要的.
当前, 基于贵金属纳米颗粒表面等离子体共振(plasmon)效应的光催化材料由于能高效地吸收可见光, 从而引起了人们广泛的关注.其中, 多种银系光催化体剂已被开发, 尤其是Ag/AgX(X为Cl、Br、I). Zhou等[5]利用沉积-沉淀法将Ag-AgBr均匀负载在γ-Al2O3(MA)上制备出Ag-AgBr/MA, 对氯酚类污染物具有良好的可见光催化氧化效果. Hu等[6, 7]研究发现Ag/AgI/MA不仅能高效地催化降解有机污染物, 还具有较强的杀菌消毒作用.这些催化剂的可见光催化活性显著提高, 主要是基于Ag纳米颗粒的plasmon诱导辅助机制, 在光反应过程中, Ag粒子被激发后其光生电子向AgX的导带迁移, 而自身被氧化为Ag+, 导致催化剂的稳定性极差.为了解决此类问题, Peng等[8]将Au和Ag共沉积在AgI/MA表面, 利用双贵金属纳米粒子的协同作用, 加速光催化体系电子的传递, 有效地抑制了Ag+的溶出. Shi等[9]则利用CNTs加快光反应体系的界面电子传输, 提高Ag/AgI的光催化活性和稳定性.这说明加快界面电子的传输, 能及时还原被激发的Ag粒子, 有效地抑制反应过程中Ag+的释放, 且有助于光催化活性的增强.
氮化碳(CN)作为一种有机聚合物半导体, 带隙较窄(约为2.7 eV), 且具有较高的导带位置(-1.3 eV), 常作为电子给体与其他半导体或金属进行复合[10, 11].同时, CN具有π共轭体系, 能加速体系光电子的传输, 促进界面电子-空穴的分离, 从而提高复合物的光催化性能[12, 13].因此, 本文采用沉淀法和热聚合法将AgI和CN分别负载在MA上, 并通过光还原银离子制备出Ag-AgI/CN/MA复合可见光催化剂, 利用CN增加Ag-AgI/MA体系光电子的传递, 提高催化剂的光催化活性和稳定性, 并选取不同的染料作为目标污染物, 系统研究了不同影响因素对Ag-AgI/CN/MA可见光催活性的影响.
1 材料与方法 1.1 试剂与仪器试剂:尿素, 异丙醇铝, 葡萄糖, 硝酸银, 碘化钾, 氨水(25%), 十八伯胺醋酸盐, 甲基橙, 罗丹明B, 甲基红, 亚甲基蓝等均为分析纯, 购自北京化学试剂公司.所有的溶液均使用去离子水配制.
仪器:X射线衍射仪(X'Pert PRO MPD, 荷兰帕纳科公司), X射线光电子能谱仪(Axis Ultra, 日本岛津公司), 紫外-可见分光光度计(UV-3010, 日本日立公司)等.
1.2 催化剂的制备利用蒸发诱导自组装法, 以异丙醇铝为前驱体, 葡萄糖为模板剂合成了MA[14].采用沉积-沉淀法制备了AgI/MA[6]. Ag-AgI/CN/MA复合材料的制备过程如下:称取0.5 g AgI/MA加入50 mL去离子水中, 超声搅拌30 min.将0.05 g十八伯胺醋酸盐溶解到上述悬浊液中, 向上述悬浊液中加入银氨溶液(7.9 mg的硝酸银溶于0.08 mL的氨水中), 搅拌30 min后, 加入不同质量的尿素(分别为1、2、3和4 g), 80℃搅拌蒸干.将得到的混合物在500℃下煅烧3 h, 残余物加入去离子水中光还原4 h(λ>400 nm), 即可制得催化剂, 记作Ag-AgI/CN/MA-X(其中, X为尿素的投加质量). Ag-AgI/MA的合成方法与上述步骤相似, 除了不添加尿素之外, 其他实验条件保持不变.纯CN的制备采用热聚合法, 直接将尿素置于马弗炉中, 于500℃下煅烧3 h, 即可获得样品.
1.3 光催化活性评价以质量浓度为10 mg·L-1的不同种染料的水溶液为目标物考察所制备催化剂的可见光催化性能, 其中, 甲基橙为主要降解污染物.室温下, 将一定量的催化剂加入到60 mL的染料溶液中, 于暗处搅拌30 min以达到吸附平衡.以150 W球形氙灯为光源, 在λ>420 nm的可见光下进行催化降解.每隔5 min取样1次, 每次取4 mL的溶液, 经0.45 μm的膜过滤后, 利用紫外-可见分光光度计测定各染料在最大吸收波长处的吸光度(表 1), 计算催化降解效率.使用电感耦合等离子体发射光谱仪(ICP-OES, OPTIMA 2000 Perkin Elmer Co.)测定反应过程中溶液里Ag+的质量浓度.
|
|
表 1 不同染料的最大吸收波长(λmax) Table 1 The λmax of different dyes |
2 结果与讨论 2.1 催化剂的表征
图 1为纯CN、纯MA、Ag-AgI/MA和不同CN掺量的Ag-AgI/CN/MA的X射线衍射(XRD)图谱.通过与X衍射标准谱图对比可知, 纯CN在13.1°和27.4°处有两个不同衍射峰, 分别属于(100) 和(002) 晶面, 由晶面间堆叠和共轭芳香族堆垛而形成[13].实验所制得的γ-Al2O3呈现立方晶相(JCPDS, 10-0425). Ag-AgI/MA和不同的Ag-AgI/CN/MA样品中, 明显地观察到β-AgI(JCPDS, 09-0374) 和γ-AgI(JCPDS, 09-0399) 的特征衍射峰, 且2θ为23.7°, 39.1°和46.3°处的特征峰分别对应为β-AgI的(002)、(110) 和(112) 晶面, 同时也属于γ-AgI的(111)、(220) 和(311) 晶面, 表明β-AgI和γ-AgI共存于复合材料中.随着CN掺量的增加, 不同复合样品中AgI衍射峰的峰强发生明显的变化, 并且β(100) 与β(002)/γ(111) 的峰面积比显著增加(见表 2), 说明CN与AgI发生强相互作用, 造成β-AgI的相对含量增多, 有利于加强催化剂的光催化活性[15].复合材料的XRD图谱中没有发现Ag的特征衍射峰, 可能是因为Ag的负载量太小(最大理论质量分数仅为1%), 这与之前的研究相似[6]. CN和Ag-AgI复合后, 样品中也均未观察到明显的CN衍射峰, 原因可能为复合样品中CN的含量较低且高度分散.

|
图 1 CN、MA、Ag-AgI/MA和Ag-AgI/CN/MA的XRD图谱 Fig. 1 XRD patterns of CN, MA, Ag-AgI/MA and Ag-AgI/CN/MA |
|
|
表 2 β(100) 晶面与[β(002)/γ(111)]晶面的峰面积比 Table 2 Peak area ratio of β (100) to β (002)/γ(111) |
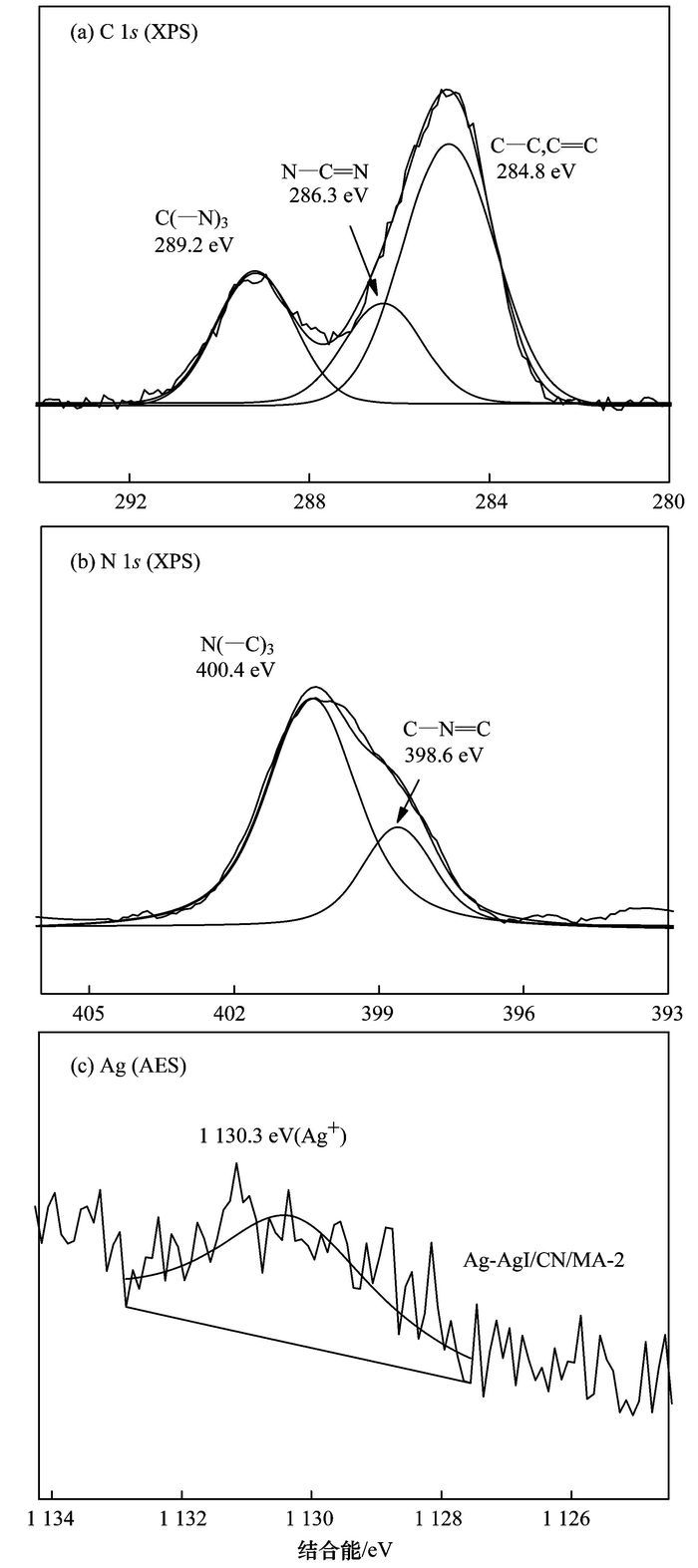
进一步, 以Ag-AgI/CN/MA-2复合材料为例, 通过XPS分析了复合材料的表面元素组成与价态(图 2). 图 2(a)为C 1s高分辨XPS图谱, 可以分出3个主峰, 284.8 eV位置的峰对应于sp2杂化的石墨相C原子(C—C或C=C), 286.3 eV位置的峰对应于含氮芳香环中sp2杂化的C原子(N—C=N), 289.2 eV位置的峰对应于sp3杂化的C原子[C(—N)3][16]. 图 2(b)为表面N元素的XPS分峰结果.可以看出, N 1s可以分出2个主峰, 结合能(BE)为398.6 eV和400.4 eV, 分别归属于C—N=C键和N(—C)3键中的N原子[17].以上结果说明复合材料中存在CN.由于Ag+和Ag0的结合能接近, 无法通过XPS峰进行区分, 所以对表面Ag元素进行了AES分析, 结果见图 2(c).可以发现, Ag的AES能谱只有一个主峰, 位于1 130.3 eV处.根据公式α(俄歇参数)=BE(Ag 3d5/2)-Auger(M4VV)+1 486.71(特征能量, eV)[18]进行计算, 其俄歇参数为724.8 eV, 说明表面Ag的主要存在形式为Ag+.同时, XPS含量分析表明, 材料表面Ag和I元素的原子百分比分别为0.72%和0.38%, 其对应的原子个数比(Ag:I=1.89) 高于AgI中Ag原子与I原子的化学计量比(Ag:I=1), 说明表面仍有Ag0的存在.
|
图 2 Ag-AgI/CN/MA-2表面C、N的XPS谱和Ag的AES谱 Fig. 2 C 1s XPS, N 1s XPS, and Ag AES spectra for Ag-AgI/CN/MA-2 |
为了观察其微观形貌结构, 对纯MA、Ag-AgI/MA和Ag-AgI/CN/MA-2复合物进行SEM结构分析, 如图 3所示.由图 3(a)可见, MA呈大颗粒状堆积体, 具有较平滑的表面.从图 3(b)中可以看出, Ag和AgI直接沉积在MA上时, 颗粒粒径较大且分布不均匀.通过热聚合的方法加入CN后, CN呈现多孔结构负载在MA表面, 且Ag和AgI颗粒相对均匀地分散在CN上.为了进一步观察复合材料的内部结构, 对Ag-AgI/CN/MA-2进行了TEM和HRTEM测定, 如图 3(d)所示.可以发现, CN呈片层状结构存在, 这与之前的报道是一致的[18].同时, 复合催化剂中Ag和AgI分散均匀, 且与CN相互结合. 图 3(d)中的插图为Ag-AgI/CN/MA-2相应的HRTEM图.通过精确地测量晶格参数, 并与JCPDS标准卡片对比后, 发现晶格间距d=0.232 nm归属于AgI(JCPDS, 09-0399) 的(220) 晶面, 而条纹间距d=0.240 nm则对应于Ag(JCPDS, 65-2871) 的(111) 晶面, 且两者晶格条纹相互交错.上述结果表明, Ag、AgI和CN相互结合并形成良好的接触, 成功地构建了复合光催化剂.

|
(a)MA的SEM图; (b)Ag-AgI/MA的SEM图; (c)Ag-AgI/CN/MA-2的SEM图; (d)Ag-AgI/CN/MA-2的TEM图(插图为相应的HRTEM图) 图 3 不同样品的的SEM图、TEM图和HRTEM图 Fig. 3 SEM, TEM, and HRTEM images of different samples |
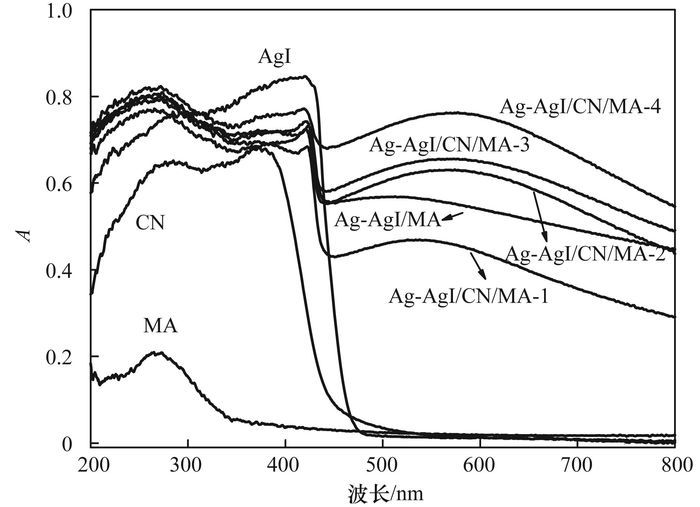
图 4是不同样品的紫外-可见漫反射光谱图.从中可知, 纯CN、AgI和MA的吸收边分别为450、460和360 nm.在460~800 nm的波长范围, Ag-AgI/MA和不同CN含量的Ag-AgI/CN/MA复合催化剂对可见光仍有强烈的吸收, 并且出现明显的吸收峰, 这是由纳米Ag的表面等离子体共振产生的, 说明了复合材料中Ag纳米颗粒的存在[19].随着CN掺杂量的增加, Ag纳米颗粒的共振吸收峰发生了一定的红移, 且光吸收能力增强.
|
图 4 不同样品的紫外-可见漫反射光谱图 Fig. 4 UV-Vis diffuse reflectance spectra of different samples |
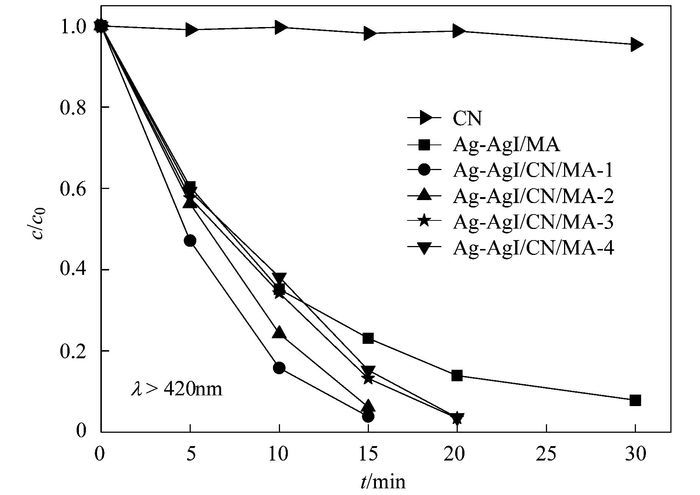
图 5为不同催化剂在可见光(λ>420 nm)照射下对MO的降解曲线.从中可以明显看出, 纯CN在可见光下对MO几乎无降解作用, 主要是因为CN可见光吸收能力有限, 且光生电子和空穴容易发生复合, 所以其光催化效率很低[16, 20]. Ag-AgI/MA对MO的可见光催化氧化反应进行得较慢, 光照30 min后, 降解率仅为92%.而CN的掺入提高了Ag-AgI/MA的光催化活性, 其中, Ag-AgI/CN/MA-1显示出最优的催化效果, 光反应15 min后其对MO的降解去除率为98%.随着复合材料中CN含量的增加, 光催化活性有所下降.当MO降解率大于95%时, Ag-AgI/CN/MA-2, Ag-AgI/CN/MA-3和Ag-AgI/CN/MA-4对应所需光反应时间分别为15、20和20 min.由此可见, 适量的CN与Ag-AgI产生耦合作用, 促进光生载流子的分离, 提高了复合催化剂可见光催化活性.
|
图 5 不同催化剂对MO的可见光催化降解(λ>420 nm) Fig. 5 Photodegradation of MO by different catalysts under visible light irriadiation (λ>420 nm) |
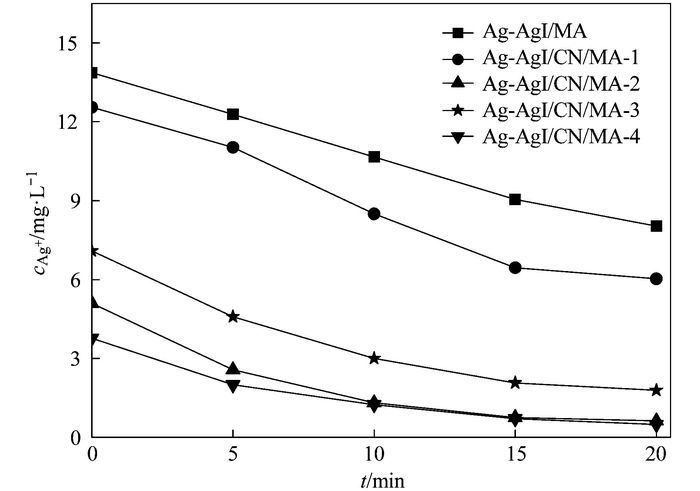
光反应过程中金属离子的溶出是考察光催化剂稳定性的一个重要指标. 图 6为不同样品在可见光催化降解MO过程中, 溶液中Ag+浓度随时间的变化曲线.可以看出, 暗反应30 min后, Ag-AgI/MA悬浮液中Ag+的质量浓度高达13.9 mg·L-1, 且随着反应的进行, 浓度不断减少至8.0 mg·L-1, 说明释放到溶液中的Ag+在反应的过程中被重新光还原到催化剂表面[21].掺入CN后, 在相同条件下, 整个反应过程中Ag+的释放量明显减少, 特别是Ag-AgI/CN/MA-2和Ag-AgI/CN/MA-4复合催化剂, 光反应20 min后, 反应液中Ag+的质量浓度约为0.5 mg·L-1, 可能是因为CN被可见光激发后将导带的光生电子传递至Ag纳米颗粒从而抑制了其被氧化腐蚀[22].根据活性评价和Ag+释放分析, 可以得出CN最优掺杂量的复合催化剂为Ag-AgI/CN/MA-2.以上结果表明, CN的掺入不仅能提高Ag-AgI/MA可见光催化降解MO的活性, 而且可以显著抑制反应过程中催化剂的光腐蚀现象发生, 从而避免对水体造成严重的二次污染.
|
图 6 不同样品可见光催化降解MO过程中体系Ag+的浓度变化 Fig. 6 Ag+ dissolution during the photodegradation of MO by different samples under visible light irradiation |
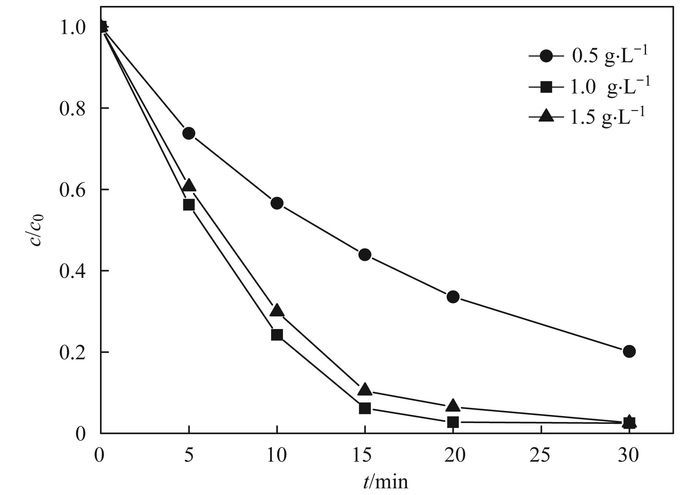
图 7为不同催化剂投加量对光催化降解MO的影响, 实验条件如下:以Ag-AgI/CN/MA-2为目标催化剂, MO的初始质量浓度为10 mg·L-1, 中性条件, 反应时间为30 min, 催化剂投加量分别为0.5、1和1.5 g·L-1.
|
图 7 不同催化剂投加量对光催化氧化MO的影响(λ>420 nm) Fig. 7 Effect of the catalyst dosage on the photocatalytic oxidation of MO (λ>420 nm) |
从图 7可知, MO的可见光催化降解效率随催化剂投加量的增加而提高, 投加量为1 g·L-1时, 光照20 min后, MO几乎被完全降解.这是由于催化剂量的增多, 增加了对可见光的吸收, 从而产生更多的光生电子和空穴, 有利于MO的降解.当催化剂投加量大于1 g·L-1时, MO的去除率反而下降, 这是因为投加量过大导致光色散增多, 一定程度上阻碍了催化剂表面对光的吸收, 同时过多的投加量也增加了光生电子和空穴的复合位点[23].
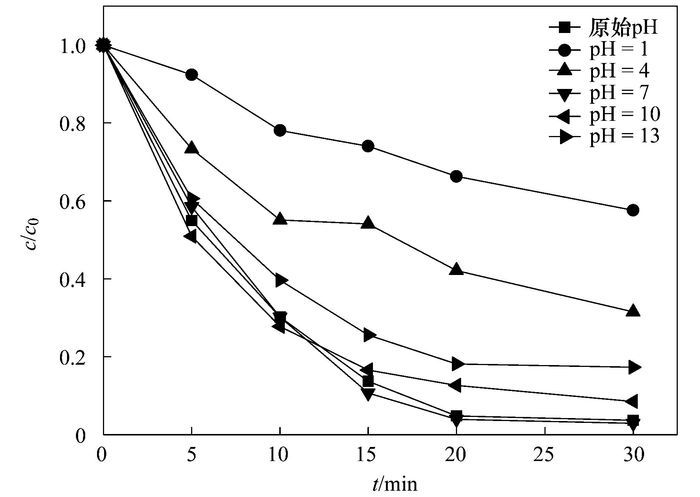
2.2.3 溶液初始pH对光催化效果的影响图 8为不同初始pH对可见光催化氧化MO的影响, 实验条件如下:选取Ag-AgI/CN/MA-2为目标催化剂, MO的初始质量浓度为10 mg·L-1, 催化剂投加量为1 g·L-1, 反应时间为30 min, 采用HNO3和NaOH将初始溶液的pH分别调至1、4、7、10和13.
|
图 8 初始溶液pH对Ag-AgI/CN/MA-2可见光催化降解MO活性的影响(λ>420 nm) Fig. 8 Effect of the initial solution pH value on the photocatalytic degradation of MO by the Ag-AgI/CN/MA-2 catalyst (λ>420 nm) |
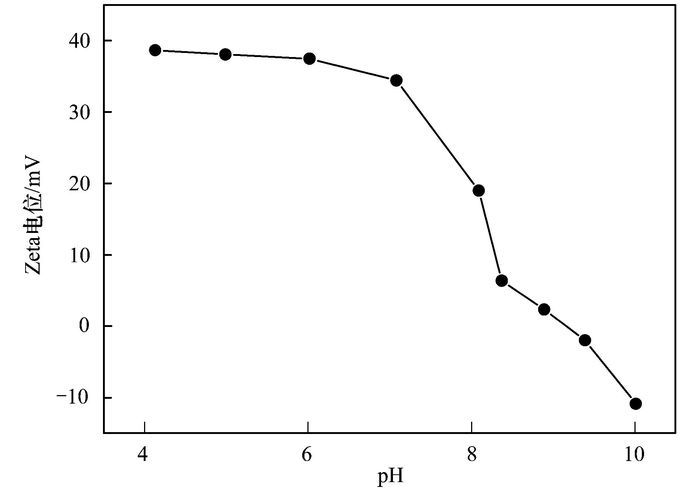
可以看出, 随着pH值的升高, 催化剂降解MO的能力先增强后减弱, 当pH=7时, 光反应20 min内, MO几乎被降解完全.碱性和中性条件有利于MO的去除, 当pH=10和13时, MO的去除率仍可达92%和84%;而酸性条件极大地抑制了MO的可见降解, 当pH=1时, MO的去除率仅为42%.这主要是因为, 溶液的pH直接影响催化剂表面所带电荷的性质和与被降解物质的结构性质[24].从图 9可知, Ag-AgI/CN/MA-2复合材料的等电点为9.15.当pH<9.15时, 催化剂表面带正电; 当pH>9.15时, 催化剂表面带负电.并且, Ag-AgI/CN/MA-2表面电荷数量也因pH不同而变化, 从而影响它的吸附和降解行为.同时, 不同pH条件下, MO呈现不同的结构与电性[25].因此, 当pH=1时, MO呈不带电的酸结构, 过多的H+可能与光生电子发生强烈的还原作用, 从而不利于O2·-等活性物种的生成, 抑制光催化反应的进行.当pH=4和7时, MO以阴离子形式存在, 催化剂表面带正电, 对MO的静电吸附作用增强, 进而加强了其催化降解能力.随着pH继续升高(pH>9.15), MO与材料表面的负电荷发生相斥作用, 同时, 其在碱性条件下的偶氮式结构更难被氧化[26], 导致催化去除效率下降.
|
图 9 Ag-AgI/CN/MA-2样品的ζ电位与pH的关系曲线 Fig. 9 Change in zeta potential of Ag-AgI/CN/MA-2 as function of pH values |
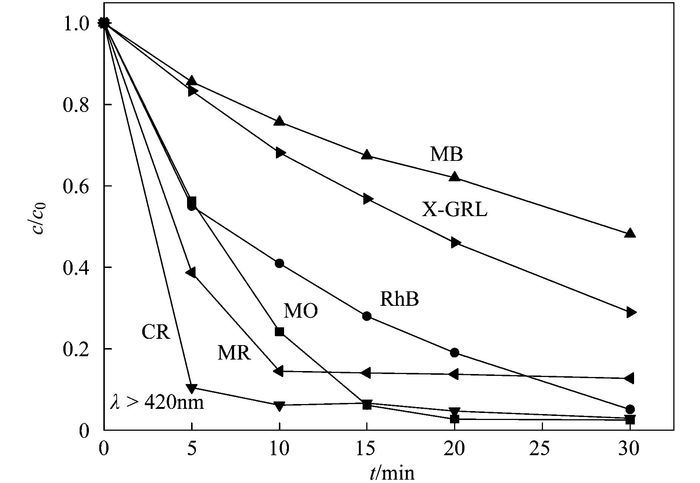
图 10为催化剂对不同染料的光催化降解曲线, 实验条件如下:以Ag-AgI/CN/MA-2为催化剂, 所选染料的质量浓度均为10 mg·L-1, 中性条件, 催化剂投加量为1 g·L-1, 反应时间为30 min, 选取目标污染物分别为MO、CR、MR、RhB、X-GRL和MB等6种不同的染料.根据染料所带电性的不同, MO、CR和MR属于阴离子染料, 而RhB、X-GRL和MB属于阳离子染料.可以发现, 在降解过程中6种染料均发生明显的脱色现象, 说明染料的结构发生了破坏.光反应30 min后, Ag-AgI/CN/MA-2对CR、MR和MO的降解效率分别为97%、87%和97%.而相同条件下, RhB、X-GRL和MB的去除率分别为95%、71%和52%.上述结果说明, 复合催化剂对电性不同的两类染料均具有优异的可见光催化降解能力, 且对阴离子染料有较好的选择性.
|
图 10 Ag-AgI/CN/MA-2对不同染料的可见光催化降解(λ>420 nm) Fig. 10 Degradation of different dyes under visible light irradiation (λ>420 nm) with Ag-AgI/CN/MA-2 |
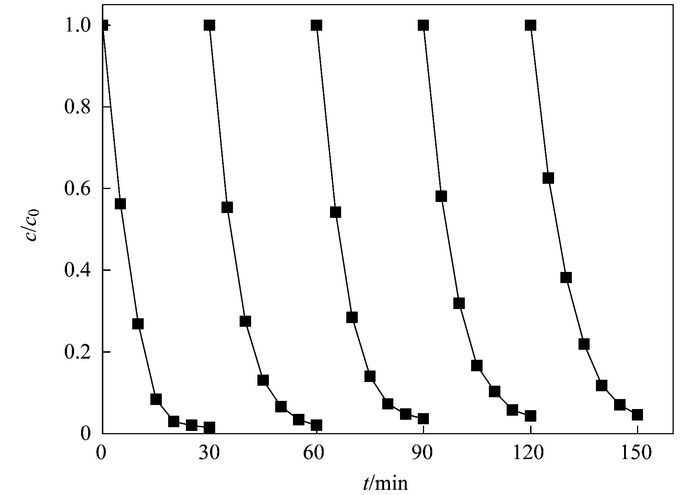
本文对Ag-AgI/CN/MA-2催化剂进行了5次可见光催化降解MO的重复实验, 如图 11所示.实验条件如下:MO的初始质量浓度为10 mg·L-1, 中性条件, 催化剂投加量为1 g·L-1, 反应时间为30 min.结果表明, 连续5次光催化降解实验之后, Ag-AgI/CN/MA-2对MO的催化氧化能力有所下降, 可能是因为在重复使用过程催化剂出现了团聚现象, 但其降解效率仍高达95%, 说明复合催化剂具备良好的稳定性, 可以重复利用.
|
图 11 Ag-AgI/CN/MA-2在可见光下循环降解MO的曲线图 Fig. 11 Cycling runs in the photodegradation of MO by Ag-AgI/CN/MA-2 in aqueous dispersion with visible light |
(1) 通过沉淀-热聚合法将AgI和CN负载在MA上, 并结合光还原法成功制备出新型的可见光催化剂Ag-AgI/CN/MA.结构表征结果表明, 表面银以Ag+和Ag0形式共存, 并且Ag和AgI均匀地分散在CN的表面.
(2) 当溶液pH值为7、催化剂投加量为1 g·L-1时, Ag-AgI/CN/MA-2显示出最优的催化性能, 光反应20 min内, MO几乎被降解完全.并且, 复合催化剂对罗丹明B(RhB)和刚果红(CR)等不同电性的染料均显示出较好的去除效果.
(3) CN的掺杂有效地抑制了Ag-AgI/MA可见光催化反应过程中Ag+的溶出, 提高了催化剂的稳定性.同时, 循环重复5次实验后, Ag-AgI/CN/MA-2对MO的可见光降解率仍高于95%.
| [1] | Aguilar Z G, Brillas E, Salazar M, et al. Evidence of Fenton-like reaction with active chlorine during the electrocatalytic oxidation of Acid Yellow 36 azo dye with Ir-Sn-Sb oxide anode in the presence of iron ion[J]. Applied Catalysis B: Environmental, 2017, 206: 44-52. DOI:10.1016/j.apcatb.2017.01.006 |
| [2] | Chakrabarti S, Dutta B K. Photocatalytic degradation of model textile dyes in wastewater using ZnO as semiconductor catalyst[J]. Journal of Hazardous Materials, 2004, 112(3): 269-278. DOI:10.1016/j.jhazmat.2004.05.013 |
| [3] | Marschall R. Semiconductor Composites: strategies for enhancing charge carrier separation to improve photocatalytic activity[J]. Advanced Functional Materials, 2014, 24(17): 2421-2440. DOI:10.1002/adfm.201303214 |
| [4] | Zhao Z F, Wang Y Z, Xu J, et al. Mesoporous Ag/TiO2 nanocomposites with greatly enhanced photocatalytic performance towards degradation of methyl orange under visible light[J]. RSC Advances, 2015, 5(73): 59297-59305. DOI:10.1039/C5RA12065A |
| [5] | Zhou X F, Hu C, Hu X X, et al. Plasmon-assisted degradation of toxic pollutants with Ag-AgBr/Al2O3 under visible-light irradiation[J]. Journal of Physical Chemistry C, 2010, 114(6): 2746-2750. DOI:10.1021/jp909697k |
| [6] | Hu C, Peng T W, Hu X X, et al. Plasmon-induced photodegradation of toxic pollutants with Ag-AgI/Al2O3 under visible-light irradiation[J]. Journal of the American Chemical Society, 2010, 132(2): 857-862. DOI:10.1021/ja907792d |
| [7] | Hu X X, Hu C, Peng T W, et al. Plasmon-induced inactivation of enteric pathogenic microorganisms with Ag-AgI/Al2O3 under visible-light irradiation[J]. Environmental Science & Technology, 2010, 44(18): 7058-7062. |
| [8] | Peng T W, Hu C, Hu X X, et al. Enhanced photodegradation of toxic pollutants on plasmonic Au-Ag-AgI/Al2O3 under visible irradiation[J]. Catalysis Letters, 2012, 142(5): 646-654. DOI:10.1007/s10562-012-0788-2 |
| [9] | Shi H X, Chen J Y, Li G Y, et al. Synthesis and characterization of novel plasmonic Ag/AgX-CNTs (X=Cl, Br, I) nanocomposite photocatalysts and synergetic degradation of organic pollutant under visible light[J]. ACS Applied Materials & Interfaces, 2013, 5(15): 6959-6967. |
| [10] | Liu L, Qi Y H, Hu J S, et al. Efficient visible-light photocatalytic hydrogen evolution andenhanced photostability of core@shell Cu2O@g-C3N4 octahedra[J]. Applied Surface Science, 2015, 351: 1146-1154. DOI:10.1016/j.apsusc.2015.06.119 |
| [11] | Zhou L, Zhang H Y, Sun H Q, et al. Recent advances in non-metal modification of graphitic carbon nitride for photocatalysis: a historic review[J]. Catalysis Science & Technology, 2016, 6(19): 7002-7023. |
| [12] | Zhu Y P, Li M, Liu Y L, et al. Carbon-doped ZnO hybridized homogeneously with graphitic carbon nitride nanocomposites for photocatalysis[J]. The Journal of Physical Chemistry C, 2014, 118(20): 10963-10971. DOI:10.1021/jp502677h |
| [13] | Su F Y, Xu C Q, Yu Y X, et al. Carbon self-doping induced activation of n-π* electronic transitions of g-C3N4 nanosheets for efficient photocatalytic H2 evolution[J]. Chemcatchem, 2016, 8(22): 3527-3535. DOI:10.1002/cctc.201600928 |
| [14] | Xu B J, Xiao T C, Yan Z F, et al. Synthesis of mesoporous alumina with highly thermal stability using glucose template in aqueous system[J]. Microporous and Mesoporous Materials, 2006, 91(1-3): 293-295. DOI:10.1016/j.micromeso.2005.12.007 |
| [15] | Wang Q, Shi X D, Liu E Q, et al. Preparation and photoelectrochemical performance of visible-light active AgI/TiO2-NTs composite with rich β-AgI[J]. Industrial & Engineering Chemistry Research, 2016, 55(17): 4897-4904. |
| [16] | Qin J Y, Huo J P, Zhang P Y, et al. Improving the photocatalytic hydrogen production of Ag/g-C3N4 nanocomposites by dye-sensitization under visible light irradiation[J]. Nanoscale, 2016, 8(4): 2249-2259. DOI:10.1039/C5NR06346A |
| [17] | Zhang S W, Li J X, Wang X K, et al. In situ ion exchange synthesis of strongly coupled Ag@AgCl/g-C3N4 porous nanosheets as plasmonic photocatalyst for highly efficient visible-light photocatalysis[J]. ACS Applied Materials & Interfaces, 2014, 6(24): 22116-22125. |
| [18] | Hu C, Lan Y Q, Qu J H, et al. Ag/AgBr/TiO2 visible light photocatalyst for destruction of azodyes and bacteria[J]. The Journal of Physical Chemistry B, 2006, 110(9): 4066-4072. DOI:10.1021/jp0564400 |
| [19] | Linic S, Christopher P, Ingram D B. Plasmonic-metal nanostructures for efficient conversion of solar to chemical energy[J]. Nature Materials, 2011, 10(12): 911-921. DOI:10.1038/nmat3151 |
| [20] |
张志贝, 李小明, 陈飞, 等. g-C3N4/Bi2S3复合物的制备及可见光催化降解MO[J]. 环境科学, 2016, 37(6): 2393-2400. Zhang Z B, Li X M, Chen F, et al. Preparation of visible-light-induced g-C3N4/Bi2S3 photocatalysts for the efficient degradation of methyl orange[J]. Environmental Science, 2016, 37(6): 2393-2400. |
| [21] |
王冉, 周雪峰, 胡学香, 等. Cu2O-Ag-AgBr/MA可见光催化剂的制备及其降解2-氯苯酚的研究[J]. 环境科学, 2014, 35(9): 3417-3421. Wang R, Zhou X F, Hu X X, et al. Synthesis of Cu2O-Ag-AgBr/MA visible photocatalyst and its performance in degradation of 2-chlorophenol[J]. Environmental Science, 2014, 35(9): 3417-3421. |
| [22] | Chen Y F, Huang W X, He D L, et al. Construction of heterostructured g-C3N4/Ag/TiO2 microspheres with enhanced photocatalysis performance under visible-light irradiation[J]. ACS Applied Materials & Interfaces, 2014, 6(16): 14405-14414. |
| [23] | Gu Q, Gao Z W, Zhao H A, et al. Temperature-controlled morphology evolution of graphitic carbon nitride nanostructures and their photocatalytic activities under visible light[J]. RSC Advances, 2015, 5(61): 49317-49325. DOI:10.1039/C5RA07284K |
| [24] |
赵雪辉, 蒋彩云, 王玉萍. PVA-I修饰介孔TiO2光催化剂对盐酸四环素的光降解[J]. 环境工程学报, 2014, 8(10): 4060-4066. Zhao X H, Jiang C Y, Wang Y P. Photocatalytic degradation of tetracycline hydrochloride using mesoporous TiO2 modified by PVA-I[J]. Chinese Journal of Environmental Engineering, 2014, 8(10): 4060-4066. |
| [25] | Smith Y R, Kar A, Subramanian V R. Investigation of physicochemical parameters that influence photocatalytic degradation of methyl orange over TiO2 nanotubes[J]. Industrial & Engineering Chemistry Research, 2009, 48(23): 10268-10276. |
| [26] | Liao J J, Lin S W, Zhang L, et al. Photocatalytic degradation of methyl orange using a TiO2/Ti mesh electrode with 3D nanotube arrays[J]. ACS Applied Materials & Interfaces, 2012, 4(1): 171-177. |
 2017, Vol. 38
2017, Vol. 38


