随着电镀、采矿、冶炼、染料等工业的快速发展, 水体中Cd2+污染越来越严重.镉的毒性较大, 被镉污染的空气和食物对人体危害严重, 常见的去除Cd2+的方法有化学沉淀法、离子交换法、膜法以及吸附等[1].其中吸附法因吸附效果好、材料易得等受到青睐.利用小麦、水稻、玉米、橡树皮、木薯杆、果壳、桔子皮等农林废弃物或制备的生物炭材料, 常被用作吸附剂去除溶液中的重金属离子[2~7].其中经过磁化改性的生物质材料易于固液分离或效率更高等优点, 近年来引起越来越多的国内外学者的关注[6~9].
磁性生物质炭的制备方法较多, 依据赋磁过程的不同, 可分为浸渍法、液相沉淀法和液相还原法[10].浸渍法是将生物质或生物炭粉末与前驱体溶液混合, 干燥后于惰性环境中高温热裂解、烧结得到磁性生物炭, 磁性颗粒是在热解过程中通过氧化还原反应形成并负载至生物炭表面[11~13]; 液相沉淀法将生物炭粉末与Fe2+/Fe3+混合盐溶液混合, 在惰性气氛下, 滴加NaOH溶液使产生沉淀, 搅拌、老化一定时间, 再经过洗涤、干燥, 得到载Fe3O4生物炭复合材料[6, 7, 14]; 液相还原法是将热解得到的生物炭与Fe2+盐溶液混合, 利用NaBH4/KBH4液相还原剂制备零价铁/生物炭复合材料[15, 16].
但关于采用生物质(小麦秸秆)直接还原菱铁矿制备磁性生物质炭的研究目前还未见报道.菱铁矿作为一种传统低品位铁矿资源主要用于钢铁冶炼, 我国菱铁矿(FeCO3)资源十分丰富, 目前已探明储量近20亿t.有关菱铁矿的工业化利用技术的研究也引起了人们的广泛关注.国外有Gallagher等[17, 18]研究了菱铁矿在真空、氮气和氧气环境下的分解特征; 国内张迎春等[19]研究了菱铁矿热解产物及其变化规律, 庞永莉等[20]和张汉泉等[21]研究了空气和氮气环境下的菱铁矿热解行为, 比较一致的结论为, 菱铁矿加热时可分解成铁氧化物, 其最终产物与气氛密切相关, 氧化性气氛下为α-Fe2O3; 惰性气氛或真空条件下为Fe3O4和FeO[18].
考虑到菱铁矿矿产资源丰富且具有较高的热化学活性, 在中温环境下即可发生热解, 本实验以小麦秸秆和天然菱铁矿为原料, 通过混合煅烧的方式制备C-Fe3O4复合材料, 考察其对Cd2+的吸附性能并与单独煅烧的小麦秸秆炭进行对比, 结合FTIR、XRD、SEM等表征技术以及吸附动力学、等温式等结果, 研究C-Fe3O4复合材料对Cd2+固化的影响因素、性能及机制, 以期开发一种经济、有效、可磁回收吸附溶液中Cd2+的材料.
1 材料与方法 1.1 材料的制备本研究所采用的天然菱铁矿取自山东乳山.将乳山菱铁矿在空气气氛下烧2 h, 得出烧失量为32.3%.剩余产物通过X射线荧光(XRF), 得出煅烧后菱铁矿的化学成分(质量分数)见表 1.小麦秸秆取自安徽省合肥市庐江县, 采用元素分析仪测得的小麦秸秆的元素含量(质量分数)见表 2.
|
|
表 1 煅烧后菱铁矿的化学成分 Table 1 Chemical composition of siderite/% |
|
|
表 2 小麦秸秆的化学成分 Table 2 Chemical composition of wheatstraw/% |
XRF和XRD结果表明乳山菱铁矿中主要矿物相为菱铁矿(FeCO3), 通过化学分析计算得到, 矿样中菱铁矿约含92.1%.将小麦秸秆破碎, 过40目筛, 在105℃下烘干, 将乳山菱铁矿破碎过200目筛, 按照2:1的质量比混合, 加入适量的去离子水搅拌0.5 h, 放入烘箱中烘干.称取约2 g的样品, 置于管式炉中以10℃·min-1的速率升至500℃, 在20 mL·min-1的低氮气气速下, 恒温碳化60 min, 待样品在炉内冷却至室温时装入样品袋保存, 制得复合材料(magnetic biomass char composition, MBC).相同条件下煅烧了单独的小麦秸秆(biomass char, BC)和菱铁矿(annealed siderite, AS), 并按照2:1的质量比将煅烧后的小麦秸秆炭和煅烧后的菱铁矿进行机械混合(mechanical biomass char and annealed siderite, MBS), 用于对照实验.
1.2 材料的表征采用通过X射线荧光光谱仪(Shimadzu XRF-1800型)测定乳山菱铁矿的化学成分.采用元素分析仪(Vario EL cube)测得的小麦秸秆的元素含量.采用比表面积及孔径分析仪(NOVA 3000e)测定MBC及BC的N2吸附-脱附等温线; 采用德国傅立叶变换红外光谱仪(VERTEX-70), 分析MBC和BC表面化学官能团差异及吸附镉前后的变化.采用英国双频磁化率仪(Bartigton MSZ型)测量磁化率; 利用日立制造场发射扫描电镜(SU8020) 分析MBC和BC吸附镉前后表面形貌和元素组成的变化; 采用日本理学X射线衍射仪(D/max-rB型)分析MBC、BC、AS、MBS的物相; 利用X射线光电子能谱仪(ESCALAB 250Xi)得到MBC吸附前Cd2+后的XPS图谱.
1.3 吸附实验 1.3.1 吸附动力学研究MBC、BC、AS、MBS对Cd2+的吸附动力学特性.分别称取0.1 g的4种材料放入100 mL离心管中, 加入20 mg·L-1的硝酸镉溶液100 mL, 置于数显翻转器上(50 r·min-1), 分别在1 min、5 min、10 min、15 min、30 min、1 h、2 h、4 h、8 h、24 h取样, 经0.22 μm的滤膜过滤后, 检测Cd2+浓度, 镉浓度按照GB/T 7475-87原子吸收分光光度法来测定.将所得数据利用准一级吸附动力学、准二级吸附动力学模型来拟合.
准一级动力学方程[22]:
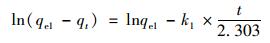
|
(1) |
式中, qe1、qt分别表示吸附平衡和t时刻的吸附容量, mg·g-1; t为反应时间, min; k1为准一级动力学吸附速率常数, min-1; 用t/qt对t作图, 由斜率和截距可得出k2和qe2.
准二级动力学方程[23]:
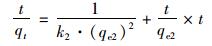
|
(2) |
式中, qe2、qt分别表示吸附平衡和t时刻的吸附容量, k2为准二级动力学常数, g·(mg·min)-1; 用t/qt对t作图, 由斜率和截距可得出k2和qe2.
1.3.2 等温吸附模型为获取复合材料(MBC)对Cd2+的饱和吸附容量.分别取10、20、40、60、80mg·L-1(Cd2+)的硝酸镉溶液10 mL, 加入10 mg的MBC, 置于数显翻转器上, 翻转24 h后取样测定镉的含量, 每个实验做两组, 计算平均吸附容量.实验数据用Langmuir等温吸附模型和Freundlich等温吸附模型进行拟合.
Langmuir方程[24]:
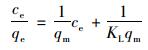
|
(3) |
式中, ce为平衡时的液相中Cd2+浓度, 单位是mg·L-1, qe为平衡时固相中(吸附剂)Cd2+的浓度, mg·g-1; qm为单层最大吸附容量, mg·g-1; KL为吸附作用的平衡常数, L·mg-1; KL值越大, 则表示吸附能力越强.
Freundlich方程[25]:
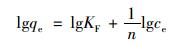
|
(4) |
式中, n为Freundlich平衡参数, 其值的大小表示浓度对吸附容量影响的强弱, 1/n越小, 吸附性能越好; KF为吸附平衡常数, 可视为单位浓度时的吸附量, mg·g-1.
1.3.3 pH及离子强度对Cd2+的吸附及解吸量的影响吸附实验:在初始pH影响实验中, 分别用1、10、100 mmol·L-1的NaCl溶液配制了20mg·L-1的Cd2+溶液, 调节初始pH为3~9范围, 考察了不同的离子强度及初始pH下对MBC吸附Cd2+的影响.
解吸实验:吸附实验完成后, 离心过膜, 测定上清液中镉含量.用去离子水洗涤MBC两次, 高速(10 000 r·min-1)离心后倒去上清液, 一组分别加入50 mL(10 mmol·L-1 NaCl)溶液, 调节pH为4、5、6、7、8、9, 反应24 h测定pH对解析量的影响; 另一组分别加入50 mL(1、10、100 mmol·L-1)的NaCl溶液, 测定离子强度对解吸量的影响.
2 结果与讨论 2.1 材料表征 2.1.1 比表面积和孔结构对小麦秸秆炭(BC)和复合材料(MBC)进行77 K N2吸附-脱附等温线的实验, 由NOVAWin2软件分析, 采用BET模型得到样品的比表面积, H-K模型得到微孔容和微孔分布[26], BJH模型得到中孔容, DFT模型得到全孔径分布[27].
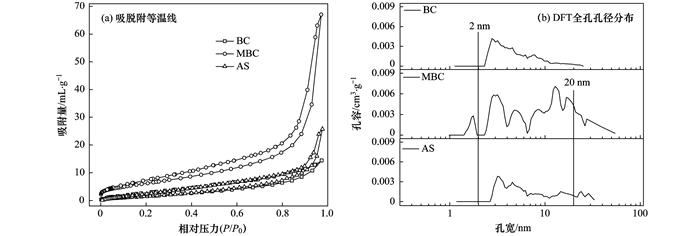
图 1为BC、MBC和AS的氮气吸脱附等温线及全孔径分布图.从图 1(a)可以看出, BC、MBC和AS的吸附等温线都属于BBDT的5种类型中的Ⅳ型, 且存在明显生物滞后环, 表明3种材料孔径以介孔(2~50 nm)为主; BC和AS的吸附等温线起始纵坐标低于MBC, 说明BC和AS的微孔和中孔的数量要比MBC的少[28~29].由图 1(b)可以看出BC孔径大部分分布在2~10 nm之间; AS的孔径分布较均匀, 主要由3~25 nm的中孔组成; MBC的孔径分布主要在2~7 nm、10~30 nm之间, MBC的孔容大于BC和AS, 也说明了其中孔的数量多于BC和AS, 与氮气吸脱附等温线的结果相对应.
|
图 1 BC、MBC和AS的吸脱附等温线及DFT全孔孔径分布 Fig. 1 N2 adsorption isotherms and pore size distribution of BC, MBC, and AS |
BC、MBC和AS的比表面积SBET、总孔容Vtotal、微孔容VH-K、中孔容VBJH等结构参数如表 3所示.其中BC的比表面积为7.20 m2·g-1, 微孔占8.52%, 中孔85.20%; MBC的比表面积为23.38 m2·g-1, 微孔占0.71%, 中孔高达98.55%; AS的比表面积为7.05 m2·g-1, 微孔占5.09%, 中孔高于90%;说明了3种材料均以中孔结构为主, 并且复合材料的比表面积和总孔容约为单独煅烧的小麦秸秆和菱铁矿的3倍, 说明混合煅烧的方式对生物质活性炭产品的孔结构参数有较大的影响.
|
|
表 3 小麦秸秆炭和复合材料的比表面积、孔容参数及质量磁化率 Table 3 Main characteristics of wheat straw carbon and the magnetic compound material |
2.1.2 红外光谱
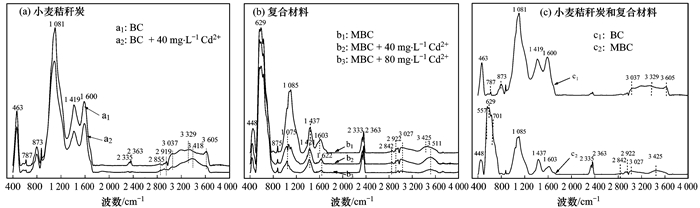
小麦秸秆炭(BC)和复合材料(MBC)实验前后的FTIR谱图如图 2(a)、2(b)所示, 小麦秸秆炭和复合材料的对比FTIR谱图如图 2(c)所示.从图 2(a)中可以看出BC在波数463、787、873、1 081、1 419、1 600、2 335、2 363、2 855、2 919、3 329、3 418 cm-1处出现吸收谱带.其中主要的吸收谱带归属如下:463、787和1 081 cm-1处为Si—O—Si振动吸收峰[30], 873 cm-1处为芳香族的C—H振动峰; 1 419 cm-1为—COOH, —CHO振动峰[31], 1 600 cm-1处主要是芳环的CC、CO伸缩振动峰[32]; 2 855 cm-1和2 919 cm-1处分别为脂肪性—CH2和—CH3的对称和非对称的C—H伸缩振动峰, 3 329 cm-1和3 418 cm-1处为酚羟基或醇羟基的伸缩振动宽峰, 由此可知BC表面存在大量的羧基和羟基, 这些表面官能团能够提供H+, H+可以与Cd2+发生离子交换[33].
|
图 2 小麦秸秆炭和复合材料吸附镉前后及小麦秸秆和复合材料的对比图 Fig. 2 FTIR spectra of the BC and MBC before and after adsorption of Cd2+ and comparison of wheat straw carbon and composite materials |
如图 2(c)所示, MBC对比BC在557、629、701 cm-1处新出现的峰为Fe—O振动峰与报道的Fe3O4的红外光谱相一致[34]; 1 085 cm-1处的宽峰带可能存在Si—O—C键[35], 与BC相比峰的强度明显减弱.如图 2(b)所示, MBC实验后1 437 cm-1的—COOH峰向低波数迁移, 1 603 cm-1处芳环的CO和CC键向高波数移动, 2 855 cm-1和2 919 cm-1振动峰强度减弱, 3 425 cm-1处的羟基的伸缩振动宽峰向高波数位移, 可能是因为Cd2+和—OH中的H+以及—CH2中的H+发生了离子交换, 羧基等含氧官能团可以和Cd2+发生络合反应[36]; 463 cm-1和1 081 cm-1处的Si—O振动峰在吸附镉后发生了明显偏移和减弱, 说明了SiO2通过羟基化作用对Cd2+有一定的吸附作用, 与Yang等[37]的研究一致.
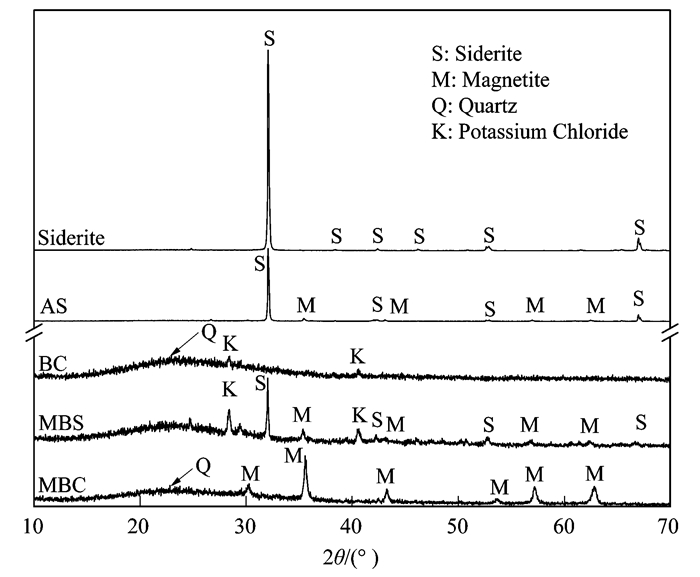
2.1.3 XRD图 3依次是乳山菱铁矿、AS、BC、MBS和MBC的XRD图谱.菱铁矿原样只在2θ为24.8°、32.0°、38.4°、42.4°、46.2°、52.8°、61.5°、68.2°出现了菱铁矿的特征衍射峰, 说明了乳山菱铁矿主要矿物是菱铁矿(FeCO3); AS中菱铁矿的衍射峰的仍然存在但强度明显减弱, 在2θ为30.1°、35.4°、43.0°、56.8°、62.3°处出现磁铁矿的峰, 说明了有部分菱铁矿发生了分解反应生成了磁铁矿; BC在2θ为23°处出现SiO2的宽衍射峰带, 28.4°和40.5°为KCl的衍射峰; 煅烧后单纯混合的MBS, 生物质和菱铁矿没有发生化学反应, MBS中含有AS的菱铁矿以及磁铁矿的特征衍射峰, 以及BC中的SiO2的宽衍射峰带及KCl的衍射峰, MBS相比AS铁矿含量降低, 所以菱铁矿的衍射峰强度低于AS; 在MBC的XRD谱图中, 菱铁矿的衍射峰消失, 只有SiO2的宽衍射峰带以及磁铁矿的峰, 说明了复合材料中的菱铁矿全部分解成了磁铁矿.可能是由于小麦秸秆和菱铁矿混合煅烧的过程中, 生物质炭高温热解过程生成的H2和CO以及单质炭等还原剂, 可以促使菱铁矿分解成磁铁矿, 也有可能生物质和铁矿混合煅烧的方式, 可以使MBC的孔隙率、界面化学反应接触面积增加, 提高小粒空隙的还原气体密度, 降低表观活化能, 从而促进菱铁矿还原成磁铁矿[38].
|
图 3 小麦秸秆炭、复合材料等的XRD图 Fig. 3 XRD patterns of the siderite, AS, BC, MBS, and MBC |
对BC和MBC进行磁化测试, 从磁化率数据(表 3)和磁分离实验(图 4)也能看出复合材料中的菱铁矿煅烧后形成了利于固液分离的Fe3O4.

|
图 4 小麦秸秆炭和复合材料在水中的磁化表现 Fig. 4 Magnetic performance of the BC and MBC in water |
如图 5(a1)所示, BC表面一部分被灼烧, 结构出现不完整性, 能谱图 5(a3)显示BC表面富集了较多的SiO2、K、Mg、Ca等无机矿物质[39].由图 5(b1)可看出MBC表面比较粗糙, 镶嵌着铁矿类物质, 对比图 5(a3)和图 5(b3), 也可证明MBC表面负载了Fe.由图 5(a3)可以看出BC的表面富集大量的SiO2, 并且吸附了一定的Cd2+, 与红外图谱结果相对应.

|
图 5 小麦秸秆炭和复合材料吸附镉前后的SEM-EDX谱图 Fig. 5 SEM images of BC and MBC before and after adsorption |
由图 6(a)和图 6(b)可知, 复合材料在284.80 eV附近有一个主峰, 是C—H、C—C或CC集团中的C原子, 是碳存在的主要形式[36], 吸附前后结合能没有变化, 说明此种形式存在的C没有参与吸附反应; MBC吸附镉前288.9 eV附近的峰是生物炭材料中的CO双键, 主要来自苯环上的—COOH[39], 吸附镉后电子结合能降低, 有明显的失电子倾向; 由图 6(c)可知, 405.74 eV和412.49 eV处的峰分别对应Cd3d5/2, 和Cd3d3/2, 对比标准XPS能谱可知, 吸附后Cd3d5/2, 和Cd3d3/2的结合能增加, 说明反应中Cd2+有明显的得电子倾向[36], 由此证明羧基炭和Cd2+发生了络合反应.

|
图 6 复合材料吸附Cd2+前后XPS谱图 Fig. 6 XPS spectra of the MBC before and after adsorption |
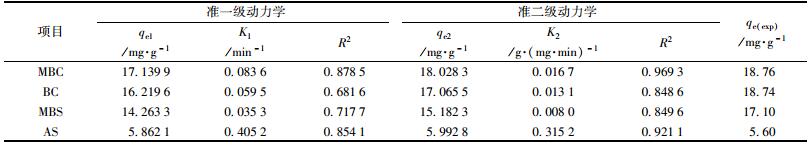
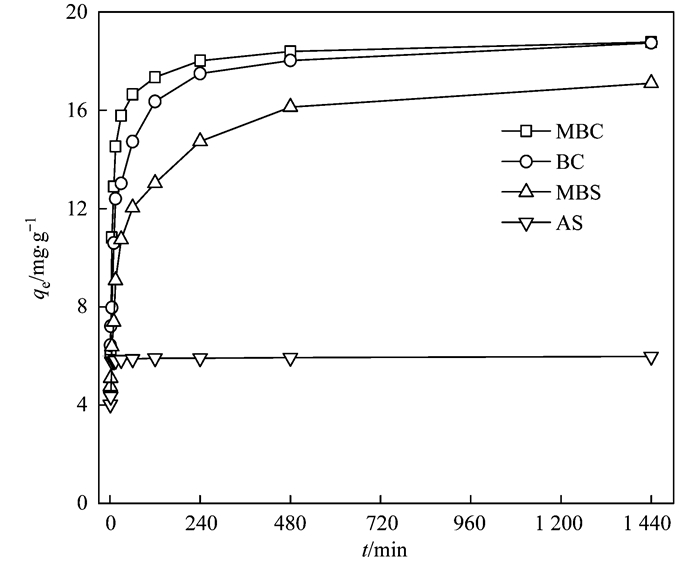
MBC、BC、AS、MBS对Cd2+吸附容量随时间的变化如图 7所示. 4种材料在前1 h对Cd2+的吸附速率很快, 8 h后基本达到平衡, 24 h后MBC对Cd2+的吸附容量为18.77 mg·g-1、BC为18.74 mg·g-1、MBS为17.10 mg·g-1而AS仅为5.6mg·g-1, 证明了MBC对Cd2+的吸附性能较好.对4种材料的动力学数据进行准一级和准二级模型拟合, 拟合参数见表 4. 4种材料的准一级动力学模型qe1和实验测得平衡吸附容量qe(exp)差别较大, 相关系数R2均小于0.9.对比准一级动力学, 准二级动力学拟合的qe2和qe(exp)较接近, 相关系数R2更接近1, 说明4种材料对Cd2+的吸附过程更符合准二级动力学行为, 反应过程以化学吸附为主[40].
|
图 7 4种材料对Cd2+的吸附动力学 Fig. 7 Effect of contact time on the removal of Cd2+ with different materials |
|
|
表 4 由准一级和准二级动力学模型拟合得到的速率常数和平衡吸附容量qe Table 4 Parameters of pseudo-first-order and pseudo-second-order kinetic models for Cd2+ adsorption |
2.2.2 等温吸附曲线
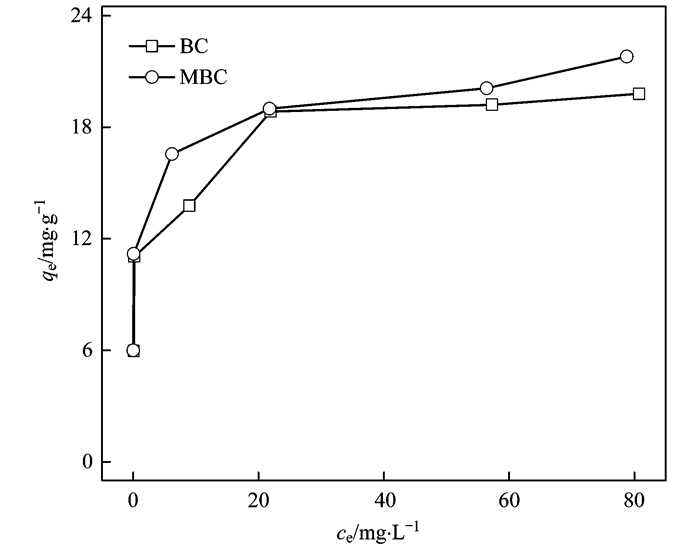
BC和MBC对Cd2+的吸附容量随溶液中Cd2+平衡浓度的变化如图 8所示.低浓度时随着溶液中Cd2+平衡浓度的增加, BC和MBC对Cd2+的吸附容量是逐渐增加的, 当浓度继续增加时BC和MBC对Cd2+的吸附容量逐渐趋于稳定, 并且MBC对Cd2+的吸附量要大于BC, 说明了复合材料的吸附性能优于小麦秸秆炭.
|
图 8 小麦秸秆炭和复合材料对Cd2+的吸附等温线 Fig. 8 Adsorption isotherms for cadmium on the BC and MBC |
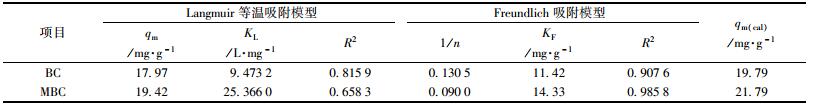
将BC和MBC对Cd2+的等温式数据用Langmuir等温吸附模型、Freundlich等温吸附模型进行拟合, 拟合的模型参数见表 5. Langmuir模型拟合的相关系数R2分别为0.815 9和0.658 3; Freundlich模型拟合的相关系数R2分别为0.907 6和0.985 8, 说明了Freundlich模型可以很好地描述BC对Cd2+等温吸附过程, BC和MBC对Cd2+的吸附过程更符合Freundlich模型, 属于多层分子吸附[41~42].
|
|
表 5 BC和MBC对Cd2+的等温吸附模型参数 Table 5 Fitting parameters of the Langmuir and Freundlich models for the adsorption isotherms of Cd2+ on the BC and MBC |
2.2.3 pH值及离子强度对吸附容量及解析量的影响
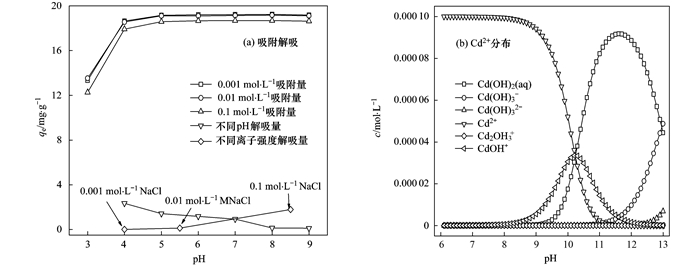
离子强度分别为0.001、0.01、0.1mol·L-1, MBC对Cd2+吸附容量在不同初始pH的变化情况; 0.01mol·L-1的离子强度下不同pH时Cd2+的解析量; 相同pH(pH=8.5, 反应后的pH)不同离子强度的Cd2+的解析量变化如图 9(a)所示. Vminteq09软件模拟的0.000 1 mol·L-1的Cd2+在0.01 mol·L-1的离子强度下, 在水溶液中的存在状态随pH的变化见图 9(b), pH≥8时Cd2+开始水解转化成Cd(OH)2(aq)、CdOH+、Cd(OH)2等形式.所以在等温式、动力学等实验中, 初始pH统一在5.0左右, 避免Cd2+水解造成的误差.
|
图 9 pH及离子强度对复合材料吸附及解吸的影响及Cd2+的分布 Fig. 9 Adsorption isotherms and desorption curves of Cd2+ with solution pH/ionic strength |
由图 9(a)可以看出, pH小于5时Cd2+的吸附容量随pH增加而增大; 解析量随pH增加而减少.离子强度增加, Cd2+的吸附容量略有减少, 解析量由0.51%提升至8.5%, 说明pH和离子强度对Cd2+的吸附都有影响. pH过高超过吸附剂的电荷零点时, 吸附剂和吸附质都带负电荷而产生静电排斥作用; pH值过低时往往造成吸附剂和吸附质都带正电荷, 也产生静电排斥作用, 另外H+和Cd2+之间会存在竞争吸附, 或者造成络合等作用被削弱而不利于吸附[43~45].离子强度抑制Cd2+的吸附容量的原因可能是电解质离子与吸附质之间的离子交换竞争使得吸附剂对吸附质的吸附总点位数的减小[46].
结合吸附等温线拟合结果以及pH对吸附解吸量的影响, 可说明本实验的MBC对Cd2+的吸附主要是化学反应过程[2]; 离子交换和阳离子-π作用是生物炭对Cd2+吸附的两种最主要的可能机制[47].增加离子强度是依据离子交换作用解吸重金属离子, 但是对络合作用吸附的重金属阳离子解吸效果较差, 本实验增加离子强度后解析量增加但只有吸附容量的8.5%, 说明有离子交换作用但以络合作用为主[48]; 吸附容量随离子强度的增加变化不大, 说明吸附剂和吸附质离子间有外层表面络合但以内层表面络合为主[46].
3 结论以小麦秸秆和山东乳山菱铁矿为原料, 在质量比为2:1, 温度为500℃煅烧60 min, 可制得比表面积为23.38 m2·g-1、质量磁化率为42 900×10-8 m3·kg-1的C-Fe3O4复合材料, 且生物质可驱动菱铁矿分解形成Fe3O4.制得C-Fe3O4复合材料对镉的吸附动力学符合准二级动力学模型, 说明了材料对Cd2+的吸附过程以化学作用为主; 吸附等温式符合Freundlich模型; 磁化率数据及磁分离实验结果显示复合材料可通过磁分离技术实现固液分离.结合离子强度影响及红外光谱、XPS表征结果分析得出, 复合材料表面羧基、硅羟基等含氧官能团通过内核络合作用吸附溶液中Cd2+, 对降低溶液中Cd2+浓度具有重要贡献.
| [1] | Tong K S, Kassim M J, Azraa A. Adsorption of copper ion from its aqueous solution by a novel biosorbent Uncaria gambir: equilibrium, kinetics, and thermodynamic studies[J]. Chemical Engineering Journal, 2011, 170(1): 145-153. DOI:10.1016/j.cej.2011.03.044 |
| [2] |
谭光群, 袁红雁, 刘勇, 等. 小麦秸秆对水中Pb2+和Cd2+的吸附特性[J]. 环境科学, 2011, 32(8): 2298-2304. Tan G Q, Yuan H Y, Liu Y, et al. Characteristics of Pb2+ and Cd2+ sorption in aqueous solution by wheat straw[J]. Environmental Science, 2011, 32(8): 2298-2304. |
| [3] |
李力, 陆宇超, 刘娅, 等. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2012, 31(11): 2277-2283. Li L, Lu Y C, Liu Y, et al. Adsorption mechanisms of cadmium(Ⅱ) on biochars derived from corn straw[J]. Journal of Agro-Environment Science, 2012, 31(11): 2277-2283. |
| [4] |
李瑞月, 陈德, 李恋卿, 等. 不同作物秸秆生物炭对溶液中Pb2+、Cd2+的吸附[J]. 农业环境科学学报, 2015, 34(5): 1001-1008. Li R Y, Chen D, Li L Q, et al. Adsorption of Pb2+ and Cd2+ in aqueous solution by biochars derived from different crop residues[J]. Journal of Agro-Environment Science, 2015, 34(5): 1001-1008. DOI:10.11654/jaes.2015.05.025 |
| [5] |
曹美珠, 潘丽萍, 张超兰, 等. 四种生物质炭的表面特性及其对水溶液中镉-阿特拉津的吸附性能研究[J]. 农业环境科学学报, 2014, 33(12): 2350-2358. Cao M Z, Pan L P, Zhang C L, et al. Surface characteristics of four biochars and their adsorption of Cd and atrazine in aqueous solution[J]. Journal of Agro-Environment Science, 2014, 33(12): 2350-2358. DOI:10.11654/jaes.2014.12.011 |
| [6] | Trakal L, Veselská V, Šafa Dřík I, et al. Lead and cadmium sorption mechanisms on magnetically modified biochars[J]. Bioresource Technology, 2016, 203: 318-324. DOI:10.1016/j.biortech.2015.12.056 |
| [7] | Mohan D, Kumar H, Sarswat A, et al. Cadmium and lead remediation using magnetic oak wood and oak bark fast pyrolysis bio-chars[J]. Chemical Engineering Journal, 2014, 236: 513-528. DOI:10.1016/j.cej.2013.09.057 |
| [8] |
李文文, 李梦蕊, 赵广超. 磁性竹基炭对Pb2+、Cd2+与Cu2+的吸附机理研究[J]. 环境科学学报, 2014, 34(4): 938-943. Li W W, Li M R, Zhao G C. Adsorption mechanism of Pb2+, Cd2+ and Cu2+ onto bamboo-based magnetic carbon[J]. Acta Scientiae Circumstantiae, 2014, 34(4): 938-943. |
| [9] |
雷娜. 磁性生物载体的制备及处理Cd2+/苯酚复合污染废水特性研究[D]. 湘潭: 湘潭大学, 2012. Lei N. Preparation of magnetic bio-carriers and their characteristics on the Cd2+/phenol complex wastewater treatment[D]. Xiangtan: Xiangtan University, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10530-1013301458.htm |
| [10] |
吴明山, 马建锋, 杨淑敏, 等. 磁性生物炭复合材料研究进展[J]. 功能材料, 2016, 47(7): 7028-7033. Wu M S, Ma J F, Yang S M, et al. Progress of the magnetic biochar composite materials[J]. Journal of Functional Materials, 2016, 47(7): 7028-7033. |
| [11] | Zhang M, Gao B, Varnoosfaderani S, et al. Preparation and characterization of a novel magnetic biochar for arsenic removal[J]. Bioresource Technology, 2013, 130: 457-462. DOI:10.1016/j.biortech.2012.11.132 |
| [12] | Mubarak N M, Alicia R F, Abdullah E C, et al. Statistical optimization and kinetic studies on removal of Zn2+ using functionalized carbon nanotubes and magnetic biochar[J]. Journal of Environmental Chemical Engineering, 2013, 1(3): 486-495. DOI:10.1016/j.jece.2013.06.011 |
| [13] | Liu Z G, Zhang F S. Nano-zerovalent iron contained porous carbons developed from waste biomass for the adsorption and dechlorination of PCBs[J]. Bioresource Technology, 2010, 101(7): 2562-2564. DOI:10.1016/j.biortech.2009.11.074 |
| [14] | Ngarmkam W, Sirisathitkul C, Phalakornkule C. Magnetic composite prepared from palm shell-based carbon and application for recovery of residual oil from POME[J]. Journal of Environmental Management, 2011, 92(3): 472-479. DOI:10.1016/j.jenvman.2010.08.031 |
| [15] | Quan G X, Sun W J, Yan J L, et al. Nanoscale zero-valent iron supported on biochar: characterization and reactivity for degradation of acid orange 7 from aqueous solution[J]. Water, Air, & Soil Pollution, 2014, 225(11): 2195. |
| [16] | Devi P, Saroha A K. Synthesis of the magnetic biochar composites for use as an adsorbent for the removal of pentachlorophenol from the effluent[J]. Bioresource Technology, 2014, 169: 525-531. DOI:10.1016/j.biortech.2014.07.062 |
| [17] | Gaklagher P K, West K W, Warne S S J. ChemInform abstract: use of the mössbauer effect to study the thermal decomposition of siderite[J]. ChemInform, 1982, 13(11). DOI:10.1002/chin.198211040 |
| [18] | Gallagher P K, Warne S S J. Thermomagnetometry and thermal decomposition of siderite[J]. Thermochimica Acta, 1981, 43(3): 253-267. DOI:10.1016/0040-6031(81)85183-0 |
| [19] |
张迎春, 杨秀红, 施倪承, 等. 菱铁矿热分解产物及其变化规律的研究[J]. 湘潭矿业学院学报, 2002, 17(1): 55-57, 82. Zhang Y C, Yang X H, Shi N C, et al. Study on the decomposition products of heat-treated siderite and it's change regularation[J]. Journal of Xiangtan Mining Institute, 2002, 17(1): 55-57, 82. |
| [20] |
庞永莉, 肖国先, 酒少武. 菱铁矿热分解动力学研究[J]. 西安建筑科技大学学报(自然科学版), 2007, 39(1): 136-139, 144. Pang Y L, Xiao G X, Jiu S W. Study on thermal decomposition kinetics of siderite[J]. Journal of Xi'an University of Architecture & Technology (Natural Science Edition), 2007, 39(1): 136-139, 144. |
| [21] |
张汉泉, 余永富, 陈雯. 大冶铁矿强磁选精矿磁化焙烧热力学研究[J]. 钢铁, 2007, 42(4): 8-11. Zhang H Q, Yu Y F, Chen W. Study on thermodymatics of magnetic roasting of magnetic separated concentrates at daye mine[J]. Iron and Steel, 2007, 42(4): 8-11. |
| [22] |
余贵芬, 青长乐, 牟树森, 等. 汞在腐殖酸上的吸附与解吸特征[J]. 环境科学学报, 2001, 21(5): 601-606. Yu G F, Qing C L, Mou S S, et al. Characteristics of mercury adsorption and desorption on humic acids[J]. Acta Scientiae Circumstantiae, 2001, 21(5): 601-606. |
| [23] |
孙璇, 李恋卿, 潘根兴, 等. 不同作物原料生物质炭对溶液芘的吸附特性[J]. 农业环境科学学报, 2014, 33(8): 1637-1643. Sun X, Li L Q, Pan G X, et al. Adsorption of pyrene from aqueous solution by biochars produced from different crop residues[J]. Journal of Agro-Environment Science, 2014, 33(8): 1637-1643. DOI:10.11654/jaes.2014.08.024 |
| [24] | Durano Dğlu D, Trochimczuk A W, Beker U. Kinetics and thermodynamics of hexavalent chromium adsorption onto activated carbon derived from acrylonitrile-divinylbenzene copolymer[J]. Chemical Engineering Journal, 2012, 187: 193-202. DOI:10.1016/j.cej.2012.01.120 |
| [25] | Jung C, Heo J, Han J, et al. Hexavalent chromium removal by various adsorbents: powdered activated carbon, chitosan, and single/multi-walled carbon nanotubes[J]. Separation and Purification Technology, 2013, 106: 63-71. DOI:10.1016/j.seppur.2012.12.028 |
| [26] |
李坤权, 李烨, 郑正, 等. 高比表面生物质炭的制备、表征及吸附性能[J]. 环境科学, 2013, 34(1): 328-335. Li K Q, Li Y, Zheng Z, et al. Preparation, characterization and adsorption performance of high surface area biomass-based activated carbons[J]. Environmental Science, 2013, 34(1): 328-335. |
| [27] |
李坤权, 李烨, 郑正, 等. 富含中孔与酸性基团的生物质炭的制备与吸附性能[J]. 环境科学, 2013, 34(6): 2479-2485. Li K Q, Li Y, Zheng Z, et al. Preparation, Characterization and adsorption performance of mesoporous activated carbon with acidic groups[J]. Environmental Science, 2013, 34(6): 2479-2485. |
| [28] | Arami-Niya A, Daud W M A W, Mjalli F S. comparative study of the textural characteristics of oil palm shell activated carbon produced by chemical and physical activation for methane adsorption[J]. Chemical Engineering Research and Design, 2011, 89(6): 657-664. DOI:10.1016/j.cherd.2010.10.003 |
| [29] | Yang H P, Yan R, Chen H P, et al. Characteristics of hemicellulose, cellulose and lignin pyrolysis[J]. Fuel, 2007, 86(12-13): 1781-1788. DOI:10.1016/j.fuel.2006.12.013 |
| [30] |
陈再明, 方远, 徐义亮, 等. 水稻秸秆生物碳对重金属Pb2+的吸附作用及影响因素[J]. 环境科学学报, 2012, 32(4): 769-776. Chen Z M, Fang Y, Xu Y L, et al. Adsorption of Pb2+ by rice straw derived-biochar and its influential factors[J]. Acta Scientiae Circumstantiae, 2012, 32(4): 769-776. |
| [31] | Chun Y, Sheng G Y, Chiou C T, et al. compositions and sorptive properties of crop residue-derived chars[J]. Environmental Science & Technology, 2004, 38(17): 4649-4655. |
| [32] | Chen B L, Zhou D D, Zhu L Z. Transitional adsorption and partition of nonpolar and polar aromatic contaminants by biochars of pine needles with different pyrolytic temperatures[J]. Environmental Science & Technology, 2008, 42(14): 5137-5143. |
| [33] | Chen B L, Johnson E J, Chefetz B, et al. Sorption of polar and nonpolar aromatic organic contaminants by plant cuticular materials: role of polarity and accessibility[J]. Environmental Science & Technology, 2005, 39(16): 6138-6146. |
| [34] | Hoseini S J, Nasrabadi H, Azizi M, et al. ChemInform abstract: Fe3O4 nanoparticles as an efficient and magnetically recoverable catalyst for friedel—crafts acylation reaction in solvent-free conditions[J]. ChemInform, 2013, 44(31). DOI:10.1002/chin.201331073 |
| [35] | Becerril H A, Mao J, Liu Z F, et al. Evaluation of solution-processed reduced graphene oxide films as transparent conductors[J]. ACS Nano, 2008, 2(3): 463-470. DOI:10.1021/nn700375n |
| [36] |
徐楠楠. 生物炭对Cd污染土壤钝化修复效应研究[D]. 长春: 吉林大学, 2014. Xu N N. Iochar on soil cd pollution remediation effect of passivation[D]. Changchun: Jilin University, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10183-1014281553.htm |
| [37] | Yang H, Xu R, Xue X M, et al. Hybrid surfactant-templated mesoporous silica formed in ethanol and its application for heavy metal removal[J]. Journal of Hazardous Materials, 2008, 152(2): 690-698. DOI:10.1016/j.jhazmat.2007.07.060 |
| [38] |
罗思义, 马晨, 孙鹏鹏. 铁矿-生物质复合球团还原行为及还原动力学[J]. 工程科学学报, 2015, 37(2): 150-156. Luo S Y, Ma C, Sun P P. Reduction behavior and reaction kinetics of iron ore-biomass composite pellets[J]. Chinese Journal of Engineering, 2015, 37(2): 150-156. |
| [39] | 刘田田. 生物质炭基固体酸碱催化剂的制备、表征及应用[D]. 武汉: 华中农业大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10504-1016021681.htm |
| [40] | Nethaji S, Sivasamy A, Mandal A B. Preparation and characterization of corn cob activated carbon coated with nano-sized magnetite particles for the removal of Cr(Ⅵ)[J]. Bioresource Technology, 2013, 134: 94-100. DOI:10.1016/j.biortech.2013.02.012 |
| [41] |
苏峰, 罗胜联, 曾光明, 等. 海带对镉的吸附动力学与热力学研究[J]. 环境工程学报, 2009, 3(5): 857-860. Su F, Luo S L, Zeng G M, et al. Kinetics and thermodynamics of Cd(Ⅱ) biosorption onto Laminaria japonica[J]. Chinese Journal of Environmental Engineering, 2009, 3(5): 857-860. |
| [42] | Langmuir I. The adsorption of gases on plane surfaces of glass, mica and platinum[J]. Journal of the American Chemical Society, 1918, 40(9): 1361-1403. DOI:10.1021/ja02242a004 |
| [43] | Liu H N, Ye X S, Li Q, et al. Boron adsorption using a new boron-selective hybrid gel and the commercial resin D564[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2009, 341(1-3): 118-126. |
| [44] | Wu Z J, Wu J H, Xiang H, et al. Organosilane-functionalized Fe3O4 composite particles as effective magnetic assisted adsorbents[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006, 279(1-3): 167-174. DOI:10.1016/j.colsurfa.2005.12.054 |
| [45] |
游来江, 蒋严, 向虹, 等. 改性介孔无机凝胶的制备及其在溶液中的吸附机理[J]. 材料导报, 2006, 20(专辑Ⅵ): 20-23. You L J, Jiang Y, Xiang H, et al. Synthesis of modified mesoporous inorganic gels and their adsorption mechanism in solution[J]. Materials Review, 2006, 20(SⅥ): 20-23. |
| [46] |
吴志坚, 刘海宁, 张慧芳. 离子强度对吸附影响机理的研究进展[J]. 环境化学, 2010, 29(6): 997-1003. Wu Z J, Liu H N, Zhang H F. Research progress on mechanisms about the effect of ionic strength on adsorption[J]. Environmental Chemistry, 2010, 29(6): 997-1003. |
| [47] | Cho H H, Wepasnick K, Smith B A, et al. Sorption of aqueous Zn[Ⅱ] and Cd[Ⅱ] by multiwall carbon nanotubes: the relative roles of oxygen-containing functional groups and graphenic carbon[J]. Langmuir, 2010, 26(2): 967-981. DOI:10.1021/la902440u |
| [48] |
郑刘春. 玉米秸秆及其纤维素的改性和吸附水体镉离子的机理研究[D]. 广州: 华南理工大学, 2011. Zheng L C. Studies on the modification of corn stalk (cellulose) and the mechanism of Cd(Ⅱ) adsorption[D]. Guangzhou: South China University of Technology, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10561-1011188586.htm |
 2017, Vol. 38
2017, Vol. 38