2. 重庆市农业资源与环境研究重点实验室, 重庆 400716;
3. 三峡库区生态环境教育部重点实验室, 重庆 400715
2. Chongqing Key Laboratory of Agricultural Resources and Environment, Chongqing 400716, China;
3. Key Laboratory of Eco-environments in Three Gorges Reservoir Region, Ministry of Education, Chongqing 400715, China
铅对人群健康危害极大,不同暴露途径的铅进入人体后可不断蓄积,对血红细胞和脑、神经系统等功能产生不可修复的损伤,尤其会对婴幼儿的生长和智力发育造成重大危害[1].土壤铅 (Pb) 污染可通过直接接触或食物链传递危害人群健康,由于工业化、城镇化和农业集约化的快速发展,我国土壤铅污染呈加重态势,目前已经成为仅次于镉的第二大土壤重金属污染元素[2, 3].土壤中铅对人群健康的危害不仅与其总量水平有关,更与其在土壤中的赋存形态及由此决定的移动性和生物可利用性 (有效性) 紧密联系[4].
广泛存在于自然环境的腐殖质类物质,因其复杂的结构和所含的羧基、醇羟基等多种活性官能团,对土壤中重金属的形态转化,迁移能力和生物可利用性具有重要影响[5, 6],施用有机肥等各类含腐殖酸的物料常作为土壤重金属污染修复措施之一[7].蒋煜峰等[8]研究表明添加腐殖酸可使土壤中具有直接生物毒性的可溶态重金属含量急剧减少60%~80%.高卫国等[9]发现单独添加腐殖酸和堆肥均可促使土壤中Zn、Pb从容易被植物吸收利用的交换态和碳酸盐结合态向难利用的有机结合态和残渣态转化.但也有不少学者发现施用有机肥作为Cd、Pb活性钝化剂并非总能抑制植物吸收,有时甚至表现出相反的效果[10, 11].一般认为有机物料中的低分子量组分如简单有机酸、富里酸 (FA) 等可提高重金属的移动性和植物有效性,而高分子量组分如胡敏酸 (HA) 可能主要起吸持固定作用,从而降低重金属的移动性和生物活性[12~15].但实际有机物料一般为复杂非均质混合物,其活性组分组成因有机物料来源、堆肥条件及腐熟化程度的不同而异,其对土壤重金属活性的表观效应是各种组分共同作用的结果.探究阐明腐殖质的关键活性组分及其赋存比例对铅生物活性的效应与机制,是利用该类材料进行土壤铅污染修复的重要科学基础.笔者的初步研究表明[16],胡敏酸与富里酸配比不同对土壤中汞形态转化和生物活性的影响方向和程度有很大差异.本研究以对人群健康危害大、污染现象普遍的重金属铅为对象,采用室内模拟实验,探讨腐殖质的两个主要活性组分胡敏酸 (HA) 和富里酸 (FA) 的含量及其不同比例 (HA/FA) 对土壤铅赋存形态的影响,阐明腐殖酸影响下土壤铅形态转化与有效性的关系,明确腐殖酸钝化或活化土壤铅的临界用量或比例,以期为土壤铅污染的修复治理及利用含腐殖酸各类物料,降低土壤铅的生物有效性、迁移性、生物毒性提供科学依据.
1 材料与方法 1.1 供试材料 1.1.1 供试腐殖酸实验所用腐殖酸为商品腐殖酸.其中,胡敏酸 (HA) 购于天津光复精细化工研究所,样品含碳量为41.21%,其主要成分为胡敏酸 (HA),灰分质量分数占10%,水分质量分数 < 8%;富里酸购于上海笛柏化学品技术有限公司,含碳量为29.29%,灰分质量分数占4%,水分质量分数≤2%.
1.1.2 供试土壤供试土壤为三峡库区消落带广泛分布的紫色潮土,于2015年3月采自重庆市开县厚坝镇村 (108°27′21″E,31°11′26″ N) 表层土 (0~20 cm).所采土样去除砾石及植物残体,自然风干后磨细过2 mm标准筛备用.供试土壤的基本理化性质见表 1.
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physicochemical properties of soil samples |
1.2 实验方法 1.2.1 不同水平腐殖酸对紫色潮土中铅形态转化与有效性变化的影响
室内培养实验和铅形态分级于2015-11~2016-03进行.称取9份过2 mm筛的紫色潮土500 g,其中一份土样设为对照 (CK),不加腐殖酸,其余8份土样分为两组,其中一组按土重的0.5%C、1%C、3%C、5%C添加HA,另一组按相同碳含量梯度添加FA,充分混匀,于25℃恒温恒湿条件下 (调节土壤含水量在20%) 避光培养1个月,制成不同腐殖酸状态的模拟土样,具体的腐殖酸添加量见表 2.然后向制好的土样中加入Pb (NO3)2溶液,使得土壤外源铅添加量为600 mg ·kg-1,充分混匀后避光培养 (含水量为20%),所有土壤培养处理均设置两个平行 (下同).分别在培养0、7、15、30、60 d后,采集混合土样进行铅形态连续浸提,并测定土壤铅有效态含量,所有测定均重复3次 (下同).
1.2.2 不同胡富比 (HA/FA) 对紫色潮土中铅形态转化与有效性变化的影响称取6份过2 mm筛的紫色潮土500 g,其中一份土样设为空白对照 (CK),不加腐殖酸,剩下的5份土样按土重的1%C加入HA和FA,调节HA/FA比值分别为0/10、3/7、5/5、7/3、10/0(表 2).充分混匀后于25℃恒温恒湿条件下 (调节土壤含水量在20%) 避光培养1个月,制成不同HA/FA比的模拟土样.然后向制好的土样中加入Pb (NO3)2溶液,使得土壤外源铅添加量为600 mg ·kg-1,在前述相同条件下测定土壤铅形态与有效性变化动态.
|
|
表 2 土壤各处理腐殖酸的添加量 (以土计)/g ·(100 g)-1 Table 2 Addition amount of humic acids to soil/g ·(100 g)-1 |
1.3 分析方法 1.3.1 土壤和腐殖酸基本理化性质
土壤基本理化性质pH、CEC、有机质含量、碳酸钙含量的测定参照文献[17].土壤总铅含量采用王水 (1体积HNO3 :3体积HCl) :HClO4为2 :1的混合酸消煮,消煮后的Pb2+溶液采用火焰原子吸收分光光度法测定 (TAS-900,北京普析).土壤有效铅含量[18]采用1 mol ·L-1 CH3COO (NH4)2溶液提取.铅形态分级采用Tessier连续提取法[19],将土壤铅分为交换态、碳酸盐结合态、铁锰氧化物结合态、有机结合态和残渣态这5种形态,提取液中的铅采用火焰原子吸收分光光度法测定 (TAS-900,北京普析),所有土壤样品的总Pb加标回收率均高于85%.
1.3.2 数据处理采用Microsoft Excel 2007进行数据处理,Origin Pro 8.0进行数据分析作图,SPSS 17.0进行数据分析.
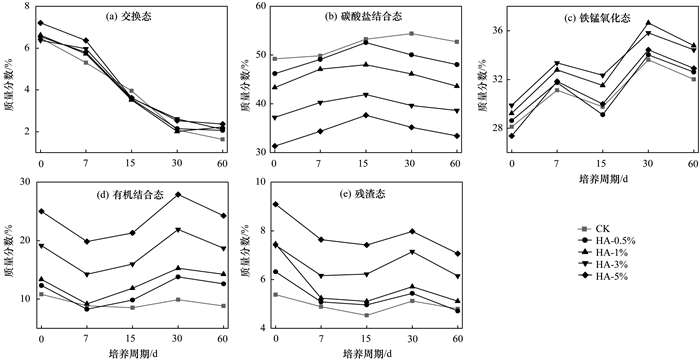
2 结果与讨论 2.1 不同水平腐殖酸对紫色潮土中铅形态转化的影响 2.1.1 胡敏酸 (HA) 的影响不同HA添加量处理的土壤中铅形态分配比例随培养时间的变化如图 1所示.从中可知,各个处理的交换态铅在整个培养过程中均不超过8%,占比最低;土壤铅主要以碳酸盐结合态的形式存在,铁锰氧化态次之,二者形态之和占总量的百分比为55%~85%,这可能与土壤pH (8.15) 及碳酸钙组分较高 (5.14g ·kg-1) 有关.
|
cPb2+=600mg ·kg-1 图 1 不同水平胡敏酸处理土壤各形态铅百分比随时间的变化情况 Fig. 1 Dynamics of Pb fraction distribution at different HA levels |
与对照相比,添加胡敏酸后并未改变外源铅在土壤中转化的动态规律,不同处理土壤中铅的形态演变相似.随培养时间的延长,土壤中交换态铅所占比例迅速降低,于30 d后趋于平衡;碳酸盐结合态铅呈先上升后下降的趋势,在培养15 d时达到峰值,此后逐步降低趋于平衡;铁锰氧化态铅随培养时间呈波动上升趋势;有机结合态铅在培养7 d时降到最低,之后逐渐上升并于培养30 d时达到峰值;残渣态铅在培养7 d时降低,之后回升达波动平衡.经过60 d的转化平衡后,与培养前比较,对照及施加0.5%C~5%C HA的土壤交换态铅和残渣态铅降低,碳酸盐结合态铅和铁锰氧化态铅增加,有机结合态铅变化不明显,其中变化显著的交换态铅降低了4.26~4.85个百分点,铁锰氧化态铅增加3.89~5.55个百分点.
经过60 d的转化平衡后,与不添加HA的对照相比,添加HA后土壤交换态铅有所增加,碳酸盐结合态铅显著降低,土壤铁锰氧化态、有机结合态和残渣态这3个难利用态在土壤中的占比显著增加.其中HA添加量为0.5%C、1%C、3%C、5%C的土壤碳酸盐结合态铅百分含量较对照分别降低了2.4%、7.2%、13.4%、18.7%,呈显著负相关关系,而有机结合态和残渣态铅则与HA添加量呈显著正相关关系,二者较对照增加的百分点分别为3.76~15.41,0.01~2.26.表明HA促进了土壤中碳酸盐结合态铅向其他难利用的形态转化,且促进作用随添加量的增加而愈加明显.出现以上结果的原因可能在于,HA增加了重金属在土壤中的吸附络合点位[20~23],促使反应初期吸附速率增大,交换态铅显著降低,转化平衡后土壤交换态铅略微高于对照可能与提取液中土壤可溶性有机碳 (DOC) 溶出有关[24].残渣态铅随时间的延长逐渐降低可能是由于腐殖酸等有机质具有强络合能力,且土壤铁、锰含量 (28.49g ·kg-1、0.48g ·kg-1) 较高,因此土壤铅由残渣态向有机结合态及铁锰氧化态转化[25, 26].
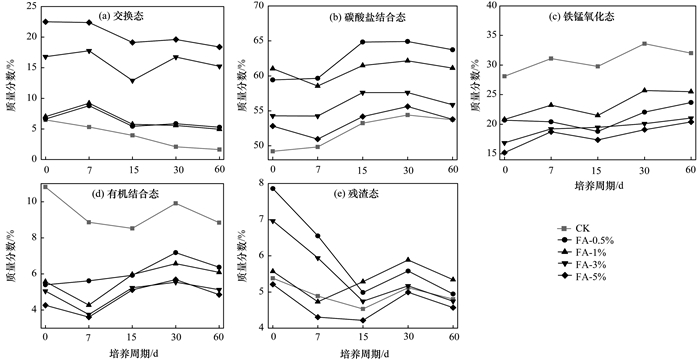
2.1.2 富里酸 (FA) 的影响不同FA添加量处理的紫色潮土中铅形态分配比例随培养时间的变化如图 2所示.从中可知,与添加HA处理相似,FA并未改变铅在土壤中转化的整体趋势,不同FA处理形态分配演变动态差异不明显.随培养时间的延长,交换态铅先小幅上升后缓慢下降;碳酸盐结合态和有机结合态铅先降低后逐渐增加最终趋于稳定;铁锰氧化态铅小幅波动上升后趋于平衡;残渣态铅在培养前15 d内急剧下降,之后出现回升最终趋于平衡.与培养前比较,经过60 d的转化平衡后,各处理土壤交换态、残渣态铅降低,碳酸盐结合态、铁锰氧化态和有机结合态铅增加.
|
cPb2+=600mg ·kg-1 图 2 不同水平富里酸处理土壤各形态铅百分比随时间的变化情况 Fig. 2 Dynamics of percentages of different species of Pb at different FA levels |
FA对土壤铅形态分异的影响与HA具有显著差异.对比图 1、图 2发现,外源铅进入土壤后,FA处理能使得交换态和碳酸盐结合态铅在整个培养期内维持在较高的水平,土壤交换态和碳酸盐结合态铅分配比例 (5.28%~18.40%和51.78%~59.74%) 明显高于HA处理的土壤 (2.06%~2.36%和33.43%~48.03%),而铁锰氧化态、有机结合态和残渣态铅分配比例整体低于施加HA的土壤. 60 d转化平衡后,与对照相比,添加HA能促进铁锰氧化态、有机结合态和残渣态铅增加,碳酸盐结合态铅减少;而添加FA的作用方向与HA相反,使得交换态和碳酸盐结合态铅均高于对照,而铁锰氧化态和有机结合态铅则均低于对照.同时,FA对铅在土壤中的形态分配与其用量有关.当FA≥3%C时残渣态铅低于对照,FA≤1%C时高于对照.当FA≤1%C时FA对铅的活化能力较弱,铁锰氧化态铅和有机结合态铅向交换态铅少量转化,另一部分向残渣态铅转化.与对照相比,FA添加量为0.5%C、1%C、3%C、5%C的土壤交换态铅分别增加3.64、3.31、13.59、16.77个百分点,呈显著正相关关系;碳酸盐结合态铅分别增加10.03、7.41、2.15、0.07个百分点;有机结合态铅与FA添加量呈负相关关系,铁锰氧化态铅与FA添加量无相关性. HAs (HA、FA) 对土壤铅形态转化的不同影响,势必会反映在铅的有效性与生物活性上,对此,将在下一节中进一步讨论.
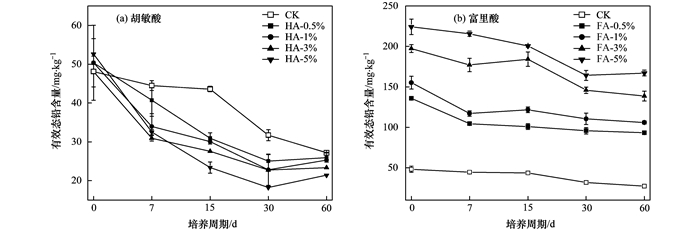
2.1.3 腐殖酸对土壤铅有效性变化动态的影响及其与铅赋存形态的相关性土壤中铅的生物有效性目前尚无公认的标准方法予以评价,一般常用特定浸提剂提取量与植物吸收的相关性作为有效性提取剂选择的依据.本文以1 mol ·L-1 CH3COO (NH4)2溶液作为有效铅提取剂[18]. 图 3为不同添加量胡敏酸、富里酸的处理外源铅进入土壤后有效态铅含量随培养时间的动态变化.从中可知,外源铅进入土壤后,有效铅随培养时间的延长而降低.添加HA的处理土壤有效铅远低于FA处理,且在培养后30 d内下降幅度最大,FA处理培养期间土壤有效铅保持在较高的水平,随培养时间的延长缓慢降低.经过60 d的转化平衡后,添加HA (0.5%C、1%C、3%C、5%C) 的土壤有效态铅含量较对照分别降低4.72%、7.04%、14.19%、21.34%,而FA较对照则分别增加2.43、2.89、4.09、5.14倍.结果表明HA对土壤铅活性具有钝化作用,而FA则表现为活化作用,且活化或钝化作用随HAs用量的增加而增加.
|
图 3 不同水平腐殖酸处理土壤有效态铅随时间的变化规律 Fig. 3 Changes of bioavailable fraction of Pb under different levels of humic acid |
HAs对土壤铅有效性的影响与其活性组分对土壤铅形态转化的不同影响密切相关.采用多元逐步回归方法,对土壤有效铅与Tessier法连续提取的5种形态铅含量进行回归分析 (表 3),结果表明,供试土壤中交换态和碳酸盐结合态铅对土壤有效铅具有显著正向贡献.这与何峰等[18]的研究结果一致.
|
|
表 3 土壤有效铅与形态的多元回归分析1) Table 3 Analysis of the relationship between bioavailable fraction of Pb and chemical extractive fraction of Pb by multiple regression analysis |
前述分析结果表明,HA能促进铁锰氧化态、有机结合态、残渣态铅分配比例增加,碳酸盐结合态铅减少;而添加FA的作用方向与HA相反.采用Duncan's新复极差法对转化平衡后各形态绝对含量的差异进行统计分析 (表 4),结果进一步证实,HA和FA及其不同添加量处理土壤各形态铅含量存在显著差异.说明HA通过降低铅向碳酸盐结合态的分配对土壤铅活性起钝化作用,而FA则通过提高交换态和碳酸盐结合态的赋存比例而发挥活化作用.吴新民等[27]的研究表明,交换态和碳酸盐结合态重金属与土壤结合能力较弱,易被释放,导致土壤重金属活性增加,因此将可交换态与碳酸盐结合态之和Q作为易被动植物吸收利用的形态来判定腐殖酸对土壤铅的活化百分率[28].
|
|
表 4 腐殖酸对铅离子各形态含量的影响1) Table 4 Influence of humic acid on contents of Pb fractions |
|
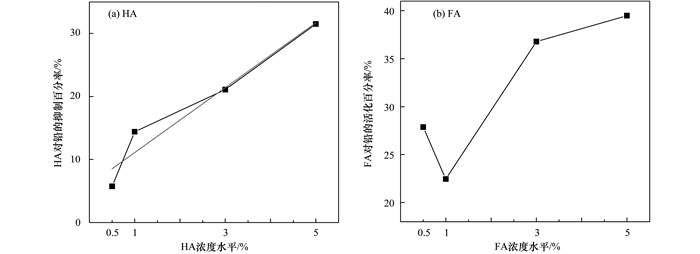
图 4 不同浓度水平的HAs对土壤铅的活化程度 Fig. 4 Influence of different concentrations of HAs on the activation of lead in soil |
土壤铅抑制百分率计算公式如下:
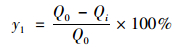
|
(1) |
土壤铅活化百分率计算公式如下:
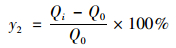
|
(2) |
式中,y1表示土壤铅的抑制百分率;y2表示土壤铅的活化百分率;Qi表示不同添加量腐殖酸土壤交换态铅与碳酸盐结合态铅含量之和,mg ·kg-1;Q0表示未添加腐殖酸的土壤交换态铅与碳酸盐结合态铅含量之和,mg ·kg-1.
转化平衡后 (培养60 d) 土壤铅抑制百分率和活化百分率与HA、FA添加量的关系如图 4所示,HA对土壤铅的钝化作用与其用量 (x) 呈显著正相关关系:
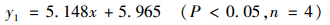
|
HA添加量为0.5%C、1%C、3%C、5%C的土壤铅抑制百分率分别为5.74%、14.41%、21.10%、31.51%;FA对土壤铅的活化作用存在临界点,当FA用量≥1%C时,土壤铅活化百分率急剧增加,1%、3%和5%(C) FA处理分别为22.44%、36.78%、39.48%.吴烈善等[29]的研究结果也表明HA能明显抑制土壤铅的活性,且用量越高抑制作用越明显;FA对铅存在临界活化点,可能是因为当FA < 1%C时,易被土壤固相强烈吸持或微生物分解所致.
HA和FA对土壤铅形态转化和有效性的不同影响,可能与两者分子量大小和结构复杂程度有关.事实上,HA与FA的基本组成与结构单元并无本质区别,但HA的分子量大,结构复杂,且不溶于水,在土壤中易与黏粒、铁锰氧化物等无机组分结合形成有机-无机复合胶体,同时,HA对重金属离子的络合稳定常数lgK和配位数均大于FA[30, 31],所吸持的铅难以从复合胶体上解离,因此,铅主要以铁锰氧化物、有机结合态等低活性形态存在,有效性较低[32, 33]. FA为分子量较低的可溶性有机质,与金属离子发生络合反应或螯合作用形成的复合物的溶解性与FA与重金属离子的分子比率有关,当腐殖酸中的FA组分与重金属之比大于2时,有利于形成水溶性的络合物[34],因此随FA用量的增加,对土壤铅的活化作用显著增强.
2.2 不同胡富比 (HA/FA) 对紫色潮土中铅形态转化和有效性的影响前述结果表明HA可钝化土壤铅,而FA则起活化作用.但实际有机物料中的活性组分既包括HA,也含有FA及其他低分子组分,其对土壤重金属活性的影响是各种组分共同作用的结果,对有机物料钝化或活化土壤铅的活性组分的临界阈值尚不明确.本研究在固定HAs添加量为1%C条件下,比较了不同HA/FA比对紫色潮土中铅形态分配和有效性的影响.
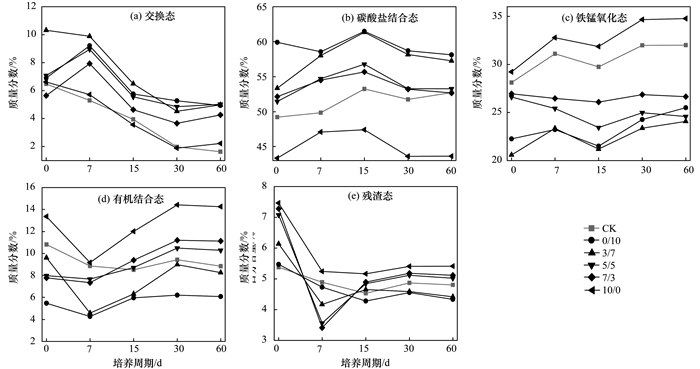
2.2.1 不同胡富比 (HA/FA) 对紫色潮土中铅形态分配的影响由图 5可知,随培养时间的延长,交换态铅在培养7 d时增加,之后逐渐降低;碳酸盐结合态铅在前15 d增加后逐渐降低趋于稳定;铁锰氧化态铅呈小幅波动上升趋势;有机结合态铅在培养7 d时降低后逐渐增加;残渣态铅随时间的变化为先大幅降低后缓慢上升最终趋于平衡.与培养前比较,经过60 d的转化平衡后,各处理交换态铅降低1.90~5.28个百分点,碳酸盐结合态铅变化不显著,铁锰氧化态和有机结合态铅整体呈增加趋势,残渣态铅降低0.43~2.41个百分点.
|
cPb2+=600 mg ·kg-1; HA-1% 图 5 不同胡富比 (HA/FA) 处理土壤各形态铅百分比随时间的变化情况 Fig. 5 Dynamics of fraction distribution of Pb at different levels of HA/FA |
经过60 d的转化平衡后,与未添加HAs的土壤相较,不同HA/FA比处理的土壤交换态铅均增加,且随HA/FA比的增加逐渐降低;当HA/FA≥7/3时碳酸盐结合态铅高于对照,HA/FA≤5/5时低于对照,但与HA/FA比呈显著负相关关系;除HA/FA比为10/0处理外,土壤铁锰氧化态铅均低于对照,且随HA/FA的增加而增加;土壤有机结合态和残渣态铅与HA/FA比值呈正相关关系,其中HA/FA为5/5、7/3、10/0的土壤有机结合态铅百分含量较对照分别增加1.46%、2.29%、5.43%;当HA/FA≤3/7时土壤有机结合态、残渣态铅均低于对照.
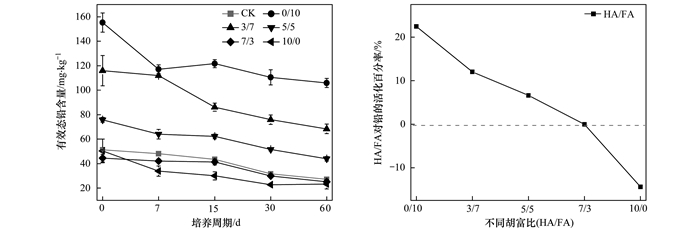
2.2.2 不同胡富比 (HA/FA比) 对紫色潮土中铅有效性变化动态的影响图 6为不同胡富比 (HA/FA比) 处理土壤添加外源铅后有效铅含量随培养时间的动态变化规律以及各个处理活化百分率的变化情况.从中可知,外源铅进入土壤后,有效铅随培养时间的延长而逐渐降低.经过60d的转化平衡后,随HA/FA比的增加有效态铅含量逐渐降低,呈负相关关系,且HA/FA比≤5/5的土壤有效态铅均高于对照,而当HA/FA比≥7/3时则恰好相反. HA/FA比处理为0/10、3/7、5/5的土壤铅活化百分率分别是22.44%、11.99%、6.60%;HA/FA比处理为7/3和10/0的土壤抑制百分率为0.06%、14.41%.以上结果说明在相同HAs (1%C) 用量水平下,HAs对于土壤铅的钝化或活化作用受胡敏酸/富里酸比 (HA/FA比) 制约,当HA/FA比≥7/3时主要表现为胡敏酸性质,对土壤铅产生钝化作用;当HA/FA≤5/5时更趋向于富里酸的性质,促使有机结合态和残渣态铅减少,并向交换态、碳酸盐结合态铅转化,导致土壤铅活性保持在较高水平,对环境和生物等产生危害.
|
图 6 不同胡富比 (HA/FA) 处理土壤的有效态铅动态变化规律及活化百分率 Fig. 6 Change of bioavailable fraction of Pb influenced by different HA/FA ratio |
(1) 外源铅进入土壤后,土壤铅主要以碳酸盐结合态存在,随培养时间的延长,交换态、残渣态铅逐渐向铁锰氧化态、有机结合态铅转化,添加HA的土壤交换态铅降低速率高于FA.
(2) HA对土壤中铅具有钝化作用,FA能活化土壤中的铅,且随着HAs用量的增加,钝化或活化作用越强.转化达平衡后,紫色潮土以交换态铅和碳酸盐结合态铅对有效铅贡献最大,添加HA的土壤交换态较对照略微增加,铁锰氧化态、有机结合态、残渣态铅均高于对照,碳酸盐结合态铅远低于对照;添加FA的土壤交换态、碳酸盐结合态铅均高于对照,铁锰氧化态、有机结合态铅均低于对照,添加HA (0.5%C、1%C、3%C、5%C) 的土壤有效态铅含量较对照分别降低4.72%、7.04%、14.19%、21.34%,而FA较对照则分别增加2.43、2.89、4.09、5.14倍. FA (1%C) 是土壤铅活化的突变点,当FA > 1%C时土壤铅活化百分率出现明显上升拐点,生物有效性和毒性显著增加.
(3) 在相同HAs (1%C) 用量水平下,HAs对于土壤铅的钝化或活化作用受HA/FA比制约.当HA/FA≥7/3时,表观作用与HA相似,通过降低碳酸盐结合态铅,增加有机结合态和残渣态铅对土壤中的铅产生钝化作用;而当HA/FA≤5/5时会促进土壤中难利用态铅向交换态和碳酸盐结合态铅转化,从而活化土壤中的铅.
| [1] | 邓芠, 罗付香, 吴彦瑜, 等. 铅在环境中的形态迁移转化研究进展[A]. 见: 中国环境科学学会. 中国环境科学学会2013年学术年会论文集[C]. 北京: 中国环境科学出版社, 2014. 5101-5106. |
| [2] | 蔡美芳, 李开明, 谢丹平, 等. 我国耕地土壤重金属污染现状与防治对策研究[J]. 环境科学与技术, 2014, 37(12O): 223–230. Cai M F, Li K M, Xie D P, et al. The status and protection strategy of farmland soils polluted by heavy metals[J]. Environmental Science & Technology, 2014, 37(12O): 223–230. |
| [3] | 成杰民, 张英, 王岩. 中国污染农地整理工程的环境问题及解决途径[J]. 农业工程学报, 2016, 32(16): 1–6. Cheng J M, Zhang Y, Wang Y. Potential environmental problems resulted from contaminated farmland and solution for land consolidation in China[J]. Transactions of the Chinese Society of Agricultural Engineering, 2016, 32(16): 1–6. DOI: 10.11975/j.issn.1002-6819.2016.16.001 |
| [4] | Abollino O, Aceto M, Malandrino M, et al. Distribution and mobility of metals in contaminated sites. Chemometric investigation of pollutant profiles[J]. Environmental Pollution, 2002, 119(2): 177–193. DOI: 10.1016/S0269-7491(01)00333-5 |
| [5] | Brown S, Christensen B, Lombi E, et al. An inter-laboratory study to test the ability of amendments to reduce the availability of Cd, Pb, and Zn in situ[J]. Environmental Pollution, 2005, 138(1): 34–35. DOI: 10.1016/j.envpol.2005.02.020 |
| [6] | 马明广, 周敏, 蒋煜峰, 等. 不溶性腐殖酸对重金属离子的吸附研究[J]. 安全与环境学报, 2006, 6(3): 68–71. Ma M G, Zhou M, Jiang Y F, et al. Study on adsorption of heavy metal ions onto insolublized humic acid[J]. Journal of Safety and Environment, 2006, 6(3): 68–71. |
| [7] | Ruttens A, Colpaert J V, Mench M, et al. Phytostabilization of a metal contaminated sandy soil. Ⅱ:influence of compost and/or inorganic metal immobilizing soil amendments on metal leaching[J]. Environmental Pollution, 2006, 144(2): 533–539. DOI: 10.1016/j.envpol.2006.01.021 |
| [8] | 蒋煜峰, 袁建梅, 卢子扬, 等. 腐殖酸对污灌土壤中Cu、Cd、Pb、Zn形态影响的研究[J]. 西北师范大学学报 (自然科学版), 2005, 41(6): 42–46. Jiang Y F, Yuan J M, Lu Z Y, et al. The effect of humic acid on species of Cu, Cd, Pb, Zn in sewage farm[J]. Journal of Northwest Normal University (Natural Science), 2005, 41(6): 42–46. |
| [9] | 高卫国, 黄宗益. 堆肥和腐殖酸对土壤锌铅赋存形态的影响[J]. 环境工程学报, 2009, 3(3): 549–554. Gao W G, Huang Z Y. Effects of humic acid and compost on speciation transformation of zinc and lead in soil[J]. Chinese Journal of Environmental Engineering, 2009, 3(3): 549–554. |
| [10] | 王美, 李书田, 马义兵, 等. 长期不同施肥措施对土壤和作物重金属累积的影响[J]. 农业环境科学学报, 2014, 33(1): 63–74. Wang M, Li S T, Ma Y B, et al. Effect of long-term fertilization on heavy metal accumulation in soils and crops[J]. Journal of Agro-Environment Science, 2014, 33(1): 63–74. DOI: 10.11654/jaes.2014.01.008 |
| [11] | Ushijima K, Fukushima M, Kanno S, et al. Risks and benefits of compost-like materials prepared by the thermal treatment of raw scallop hepatopancreas for supplying cadmium and the growth of alfalfa (Medicago sativa L.)[J]. Journal of Environmental Science and Health, Part B:Pesticides, Food Contaminants, and Agricultural Wastes, 2016, 51(3): 170–175. DOI: 10.1080/03601234.2015.1108810 |
| [12] | 魏世强, 李光林, SterbergR, 等. 腐殖酸-金属离子反应动力学特征与稳态指标的探讨[J]. 土壤学报, 2003, 40(4): 554–561. Wei S Q, Li G L, Sterberg R, et al. Kinetics of metal ion reactions with humic acids and index for steady-state[J]. Acta Pedologica Sinica, 2003, 40(4): 554–561. DOI: 10.11766/trxb200112110411 |
| [13] | 何雨帆, 刘宝庆, 吴明文, 等. 腐植酸对小白菜吸收Cd的影响[J]. 农业环境科学学报, 2006, 25(S): 84–86. He Y F, Liu B Q, Wu M W, et al. Effect of humus on uptake of cadmium in pakchoi[J]. Journal of Agro-Environment Science, 2006, 25(S): 84–86. |
| [14] | 陕红, 李书田, 刘荣乐. 秸秆和猪粪的施用对土壤镉有效性的影响和机理研究[J]. 核农学报, 2009, 23(1): 139–144. Shan H, Li S T, Liu R L. Availability and the related mechanisms of cadmium in soils as influenced by the application of straw or pig manure[J]. Journal of Nuclear Agricultural Sciences, 2009, 23(1): 139–144. |
| [15] | An J, Jho E H, Nam K. Effect of dissolved humic acid on the Pb bioavailability in soil solution and its consequence on ecological risk[J]. Journal of Hazardous Materials, 2015, 286: 236–241. DOI: 10.1016/j.jhazmat.2014.12.016 |
| [16] | 高洁, 李雪梅, 闫金龙, 等. 腐殖酸对灰棕紫泥中汞赋存形态的影响[J]. 水土保持学报, 2014, 28(5): 199–203. Gao J, Li X M, Yan J L, et al. Effect of humic acids on species of mercury in gray brown purple mud[J]. Journal of Soil and Water Conservation, 2014, 28(5): 199–203. |
| [17] | 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. |
| [18] | 何峰, 苗金燕, 魏世强. 外源砷、铅在三类紫色土中形态分配与其化学、生物有效性研究[J]. 农业工程学报, 2005, 21(S): 44–47. He F, Miao J Y, Wei S Q. Speciation distribution and its chemical, biological availability of arsenic, lead added in acid, neutral and alkali purple soil[J]. Transactions of the CSAE, 2005, 21(S): 44–47. |
| [19] | Tessier A, Campbell P G C, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 1979, 51(7): 844–851. DOI: 10.1021/ac50043a017 |
| [20] | 熊雄, 李艳霞, 韩杰, 等. 堆肥腐殖质的形成和变化及其对重金属有效性的影响[J]. 农业环境科学学报, 2008, 27(6): 2137–2142. Xiong X, Li Y X, Han J, et al. Formation and transformation of humus in composting and its impacts on bioavailability of toxic metals[J]. Journal of Agro-Environment Science, 2008, 27(6): 2137–2142. |
| [21] | Brown S, Chaney R, Hallfrisch J, et al. In situ soil treatments to reduce the phyto-and bioavailability of lead, zinc, and cadmium[J]. Journal of Environmental Quality, 2004, 33(2): 522–531. DOI: 10.2134/jeq2004.5220 |
| [22] | 陈苏, 孙丽娜, 晁雷, 等. 不同浓度组合的镉、铅在不同污染负荷土壤中的吸附-解吸动力学行为[J]. 应用基础与工程科学学报, 2007, 15(1): 32–44. Chen S, Sun L N, Chao L, et al. Sorption-desorption dynamic behavior of cadmium, lead with different concentrations combination in different metal burden soils[J]. Journal of Basic Science and Engineering, 2007, 15(1): 32–44. |
| [23] | 吴蝶, 黄莺, 杨倩, 等. 腐殖酸对石灰 (岩) 土中铅形态和分布的影响[J]. 广东农业科学, 2014, 41(4): 74–78. Wu D, Huang Y, Yang Q, et al. Effect of humic acid on the form and distribution of lead in calcareous soil[J]. Guangdong Agricultural Sciences, 2014, 41(4): 74–78. |
| [24] | 孙波, 孙华, 张桃林. 红壤重金属复合污染修复的生态环境效应与评价指标[J]. 环境科学, 2004, 25(2): 104–110. Sun B, Sun H, Zhang T L. Bio-environmental effects and index of remediation of multi-heavy metals polluted red soils[J]. Environmental Science, 2004, 25(2): 104–110. |
| [25] | 余贵芬, 蒋新, 和文祥, 等. 腐殖酸对红壤中铅镉赋存形态及活性的影响[J]. 环境科学学报, 2002, 22(4): 508–513. Yu G F, Jiang X, He W X, et al. Effect of humic acids on species and activity of cadmium and lead in red soil[J]. Acta Scientiae Circumstantiae, 2002, 22(4): 508–513. |
| [26] | 余贵芬, 蒋新, 孙磊, 等. 有机物质对土壤镉有效性的影响研究综述[J]. 生态学报, 2002, 20(5): 770–776. Yu G F, Jiang X, Sun L, et al. A review for effect of organic substances on the availability of cadmium in soils[J]. Acta Ecological Sinica, 2002, 20(5): 770–776. |
| [27] | 吴新民, 潘根兴. 影响城市土壤重金属污染因子的关联度分析[J]. 土壤学报, 2003, 40(6): 921–928. Wu X M, Pan G X. The correlation analysis between the content of heavy metals and the factors influencing the pollution of heavy metals in urban soils in Nanjing City[J]. Acta Pedologica Sinica, 2003, 40(6): 921–928. DOI: 10.11766/trxb20030618 |
| [28] | 汪斌, 谭建新, 代静玉. 腐殖酸对池塘底泥中铅、镉的离子形态分布及其活性的影响[J]. 土壤通报, 2007, 38(1): 106–110. Wang B, Tan J X, Dai J Y. Effect of humic acid on ionic form distribution and activity of lead and cadmium in pond sediment[J]. Chinese Journal of Soil Science, 2007, 38(1): 106–110. |
| [29] | 吴烈善, 曾东梅, 莫小荣, 等. 不同钝化剂对重金属污染土壤稳定化效应的研究[J]. 环境科学, 2015, 36(1): 309–313. Wu L S, Zeng D M, Mo X R, et al. Immobilization impact of different fixatives on heavy metals contaminated soil[J]. Environmental Science, 2015, 36(1): 309–313. |
| [30] | Xian X F. Response of kidney bean to concentration and chemical form of cadmium, zinc, and lead in polluted soils[J]. Environmental Pollution, 1989, 57(2): 127–137. DOI: 10.1016/0269-7491(89)90005-5 |
| [31] | Stevenson F J. Nature of divalent transition metal complexes of humic acids as revealed by a modified potentiometric titration method[J]. Soil Science, 1977, 123(1): 10–17. DOI: 10.1097/00010694-197701000-00002 |
| [32] | Grasso D, Chin Y P, Weber W J. Structural and behavioral characteristics of a commercial humic acid and natural dissolved aquatic organic matter[J]. Chemosphere, 1990, 21(10-11): 1181–1197. DOI: 10.1016/0045-6535(90)90139-K |
| [33] | 吴曼, 徐明岗, 徐绍辉, 等. 有机质对红壤和黑土中外源铅镉稳定化过程的影响[J]. 农业环境科学学报, 2011, 30(3): 461–467. Wu M, Xu M G, Xu S H, et al. Effects of organic matter on the stabilization process of added cadmium and lead in red soil and black soil[J]. Journal of Agro-Environment Science, 2011, 30(3): 461–467. |
| [34] | Schnitzer M, Skinner S I M. Organo-metallic interactions in soils:1. Reactions between a number of metal ions and the organic matter of a podzol Bh horizon[J]. Soil Science, 1963, 96(2): 86–93. DOI: 10.1097/00010694-196308000-00003 |
 2017, Vol. 38
2017, Vol. 38


