大气颗粒物现已成为影响人类身体健康的主要因素之一.流行病学研究表明,当人体暴露在颗粒物浓度较高的环境下并且吸入颗粒物时,颗粒物在人体中的沉积是造成多种疾病发生或加重的原因之一,尤其是心血管疾病[1, 2]和呼吸系统疾病[3, 4],颗粒物浓度增加与患者的入院率和死亡率上升有关[5, 6];不同粒径颗粒物在不同沉积部位诱发的疾病类型也有所不同[7].国际癌症研究总局已将大气颗粒物归为致癌物之一[8, 9].
近年来,我国霾现象日渐频发,颗粒物对人体健康的影响引起了政府和公众的广泛关注.目前国内对于颗粒物对健康影响的研究主要集中在细粒子与心血管疾病和呼吸系统疾病的关系[10, 11],以及对人体内颗粒物传输与沉积的数值模拟[12, 13].许多研究表明,颗粒物的毒性效应与其粒径关系密切,而且细粒子较粗粒子毒性更强[14, 15];在北京,局部缺血性心脏病的死亡率与30~100 nm粒径段粒子的数量关系最为密切[16].然而在国内对于人体内颗粒物沉积量的定量分析还较为欠缺.
长江三角洲一直是霾污染高发区域,南京近年来的空气质量更是不容乐观.吉贵祥等[17]发现2013~2014年南京市PM2.5与非肿瘤类呼吸疾病住院人数显著相关,可见南京地区空气污染与人体健康关系密切.方叠[18]发现南京较周边城市对PM2.5致死的耐受性更强,自然环境、人为环境以及污染成分不同都可能导致南京地区人体内颗粒物沉积特性有别于其他地区.所以,本研究时段选择了呼吸系统疾病高发的冬季 (2015年1月1日至2015年1月31日) 和春季 (2015年4月1日至2015年4月30日),应用多路径粒子剂量测量模型 (multiple-path particle dosimetry model,MPPD,v.3.04) 对南京北郊地区细粒子在人体内不同部位的沉积特性进行定量分析,以期为评价细粒子的暴露风险、剂量和健康效应提供参考.
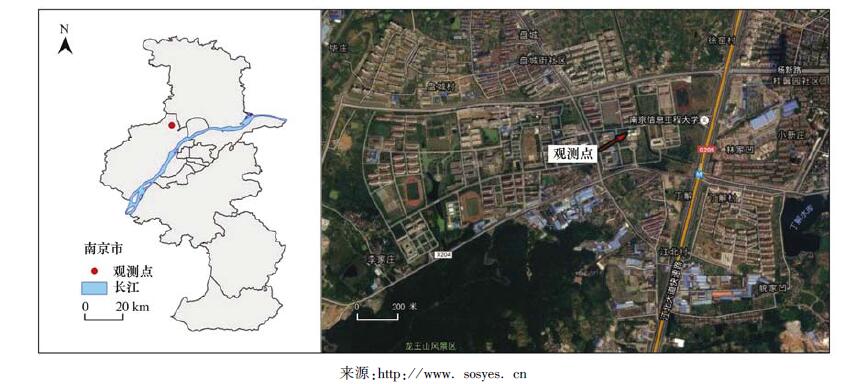
1 材料与方法 1.1 观测站点观测点位于南京北郊的南京信息工程大学气象楼大气物理学院及中国气象局气溶胶与云降水重点实验室 (32°12′N,118°42′E,海拔62 m),其东面约500 m为主干道路宁六路,双向六车道,上空有高架快速路和轻轨;其西南方向约900 m为南京龙王山风景区,海拔约100 m;其西侧和北侧为南京信息工程大学校园主体、城镇住宅区和农田,无明显的污染排放源.观测点周边情况如图 1所示.冬季观测时间为2015年1月1日至2015年1月31日,春季观测时间为2015年4月1日至2015年4月30日.
|
图 1 观测点地理位置及周边环境示意 Fig. 1 Location of observation station and the surrounding environment |
气溶胶粒子数浓度 (number concentration,NC) 的观测采用美国MSP公司生产的宽范围颗粒粒径谱仪 (WPS),测量直径范围为10 nm~10 μm,仪器原理介绍见文献[19].由于WPS适应的环境湿度为0%~90%、非冷凝,根据观测的实施情况,剔除了部分无效数据.
PM2.5浓度的观测使用美国热电公司生产的FH62C14型β射线测尘仪,仪器采用C-14密封发射源来感知堆积在移动滤带上的尘粒,时间分辨率为30 min.该仪器使用前已标定,符合美国EPA的技术规格[20].
SO2、NO2、CO及O3的观测均采用美国赛默飞世尔环境设备公司生产的大气污染物环境监测分析仪.仪器参数及标定方法见文献[21].为保证观测数据的有效性和可靠性,观测期间对分析仪每月进行一次校准,并剔除部分无效数据.
1.3 空气质量指数级别的划分空气质量指数 (AQI) 级别按中华人民共和国环境保护部发布的《环境空气质量指数 (AQI) 技术规定 (试行)》[22]划分.污染物项目P的空气质量分指数按式 (1) 计算.
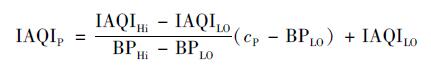
|
(1) |
式中,IAQI为污染物项目P的空气质量分指数;cP为污染物项目P的质量浓度值 (μg·m-3或mg·m-3);BPHi为与cP相近的污染物浓度限值的高位值 (μg·m-3或mg·m-3);BPLO为与cP相近的污染物浓度限值的低位值 (μg·m-3或mg·m-3);IAQIHi为与BPHi对应的空气质量分指数;IAQILO为与BPLO对应的空气质量分指数.空气质量指数按式 (2) 计算:
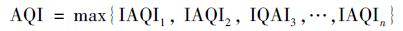
|
(2) |
式中,IAQI为空气质量分指数;n为污染物项目.
1.4 MPPD模式MPPD v.3.04是由美国哈姆纳健康科学研究院与荷兰国家公共卫生和环境研究所共同开发的计算模型,其功能介绍见官方网站[23].模式中包含的多路径模式可以基本反映人类呼吸系统的真实结构,原理见文献[24].
本研究选用模式中的随机肺模型,参考Li等[25]研究中所选用的代表北京地区人体生理特征的参数,肺部尺寸选取第60百分位点;参考Roy等[26]研究结果,选取适合中国人生理特征的参数为,功能性余气量2 950.0 mL (其数值变化与是否运动无直接关系,故视为常数[27]),上呼吸道体积44.7 mL,休息状态下呼吸频率为16次·min-1,潮气量为537.5 mL;参考运动生理学教材[28]内容,选取运动状态下呼吸频率为50次·min-1,潮气量为2 000.0 mL.由于气溶胶粒子密度与粒径大小相关,本文参考了Hu等[29]的研究结果,即北京地区1 μm以下粒子的实际密度和有效密度均在1.5 g·cm-3附近浮动,并且Li等[25]也将其设定为1.5 g·cm-3,故本次研究中将1 μm以下粒子的平均密度估计为1.5 g·cm-3.其他参数,如重力加速度、呼吸过程中吸气和暂停的时间比例等,均使用模式中的默认值.
本研究主要使用模式计算所得的沉积分数 (deposition fraction,DF),呼吸系统的总沉积分数 (total deposition fraction,TDF) 定义如式 (3) 所示.
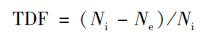
|
(3) |
式中,Ni为人体吸入的粒子总数 (个);Ne为随后呼出的粒子总数 (个)[30].
在可吸入颗粒物经呼吸道进入人体内的过程中,一方面,其粒径大小会决定其在呼吸系统中的沉降部位,粒子形状也会造成一定影响[31];另一方面,粒径会影响粒子的悬浮时间和沉降速度,是决定其DF的最主要原因[32].同时DF也受呼吸型显著影响,主要包括上呼吸道体积、潮气量、功能性余气量、呼吸频率、吸入停顿时间等[26];同时也受颗粒物密度、形状、电荷、吸湿效应、温度[33]以及呼吸者年龄[34]、性别[34]、健康状况 (影响气道通畅程度) 等因素影响[35, 36].如Yamada等[34]的研究中,不同分组人体的总肺容量、功能性余气量和肺活量的大小关系为:成年男性>成年女性>10岁儿童,该差异致使肺部的沉积效率峰值大小关系为:成年男性>成年女性>10岁儿童,同时,儿童胸外区域中1 μm粒子沉积效率比成年男性和女性高出5%~7%,且微米级粒子沉积较高,但其肺部沉积效率是三组中最低的,且纳米级粒子沉积较高.再如,Chalupa等[36]的研究结果表明,哮喘病人体内沉积分数普遍高于健康人;休息时较为明显,高出约0.15,运动时差异不大,高出约0.02;其主要原因是哮喘病人潮气量整体水平高于健康人.
本研究假设大气气溶胶粒子形状为球体,未考虑其他形状的情况;呼吸型参数的选取仅符合中国成人呼吸特征的平均水平,未考虑年龄、性别、健康状况等因素,以及长时间运动过程中的生理变化.
2 结果与讨论 2.1 数浓度谱分布图 2为南京北郊冬春两季各AQI级别下的细粒子数浓度谱分布平均值.其中1月有效数据30 d,含AQI二级10 d、三级12 d、四级5 d、五级3 d,样本量7 213个;4月有效数据27 d,含AQI一级3 d、二级20 d、三级2 d、四级2 d,样本量7 311个.
|
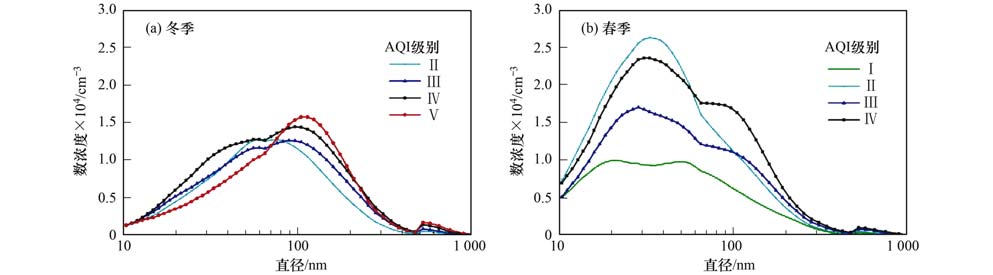
图 2 南京北郊冬季和春季在不同AQI级别下的数浓度谱分布 Fig. 2 Particle size distributions of NC at different AQI levels in winter and spring in northern suburb of Nanjing |
冬季数浓度谱分布[图 2(a)]在不同AQI级别间差异不大,平均总数浓度为35.16×104 cm-3.各级别的最大值分别为二级1.27×104 cm-3、三级1.26×104cm-3、四级1.44×104 cm-3、五级1.57×104 cm-3;总体最大值出现在AQI五级的105 nm粒径附近.五级数浓度谱为单峰分布;三级和四级为结构相似的明显双峰分布,二级也有较小的双峰结构,第一个峰值均出现在55~65 nm粒径段,第二个峰值略大于第一个峰值,出现在70~105 nm粒径段,且位置随空气质量降低而向大粒径移动.各级别的最高峰值均在70~115 nm随空气质量降低而向大粒径移动,可以说明空气质量越差,较大粒径段数浓度越高.其中积聚模态 (100~1 000 nm) 数浓度与空气质量的相关性更加明显,空气质量越差,积聚模态数浓度越高.
春季数浓度谱分布[图 2(b)]在不同AQI级别之间差异较大,这点与冬季明显不同.平均总数浓度为52.62×104 cm-3,明显高于冬季.各级别的最大值分别为一级1.00×104 cm-3、二级2.63×104 cm-3、三级1.70×104 cm-3、四级2.36×104 cm-3;总体最大值出现在二级的30~35 nm粒径段.一级数浓度谱有微弱的双峰特征且两峰值差异不大,分别出现在20 nm和50 nm粒径附近;二级为单峰分布;三级和四级与冬季分布类似,但实际上65~100 nm范围内仅是斜率明显减小,并没有第二个峰值出现.各模态数浓度与空气质量之间未表现出明显的相关性.
2.2 不同生理状态下的沉积分数在休息和运动两种状态下,人体内颗粒物TDF及呼吸系统中各部位的DF均表现出明显差异[图 3(a)和图 3(b)].
|
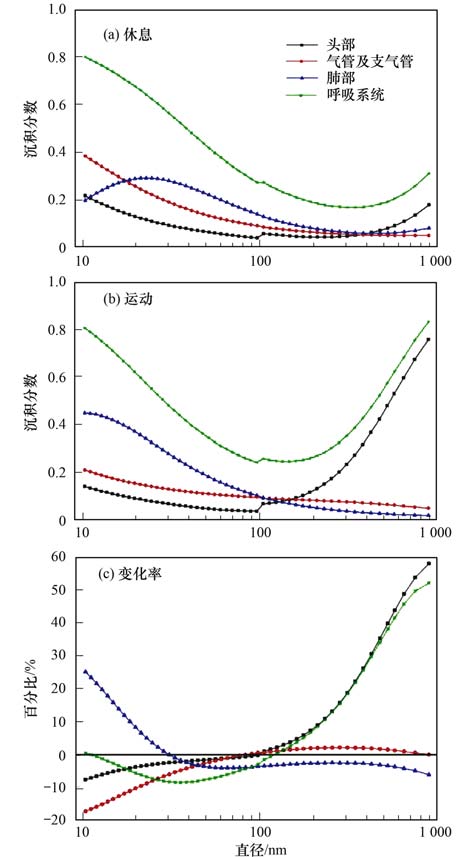
图 3 人体在休息与运动状态下的颗粒物DF及变化率 Fig. 3 DF and change rate in human airway at rest and exercise |
休息时TDF最大值出现在10 nm附近可达0.80,在 < 350 nm粒径段TDF随粒径增长而降低,最小值出现在310~380 nm约为0.17,之后有所回升,在1 000 nm附近增长至0.31.头部 (主要包括鼻腔、口腔、咽部和喉部) DF也呈现随粒径增长先降低再回升的分布,在10 nm和1 000 nm附近分别达到0.22和0.18,最低值出现在90~105 nm约为0.04.气管及支气管DF呈递减趋势,10 nm附近约为0.38,100 nm附近约为0.05.肺部DF呈一峰一谷分布,峰值出现在20~25 nm约为0.29,谷值出现在380~475 nm约为0.06.
运动时TDF呈“U”形分布,10 nm附近约为0.81与休息时差异不大,最低值出现在120~145 nm粒径段约为0.25,而在1 000 nm附近回升至0.83,甚至超过了10 nm处的TDF,远大于休息状态.头部DF在10 nm附近约为0.14,略低于休息时;在100~1 000 nm范围内DF急剧增长,在1 000 nm附近约为0.76.气管支气管中DF分布型与休息时类似,但斜率相对减小,最大值出现在10nm附近约为0.21,较休息时减少17.00%;1 000 nm处约为0.05,与休息时差异不大.肺部DF随粒径增大而降低,分布型与休息时不同,最大值约为0.45出现在10 nm附近,最小值约为0.02出现在1 000 nm附近.
两种状态下核模态 (10~25 nm) 和爱根核模态 (25~100 nm) TDF非常近似,而运动时积聚模态TDF是休息时的2.49倍;肺部对核模态和爱根核模态TDF贡献最大,休息时约占48.17%,运动时约占54.23%,头部对积聚模态TDF贡献最大,休息时约占41.23%,运动时约占80.47%.
从运动状态较休息状态的DF变化率[图 3(c)]来看,TDF在 < 115 nm粒径段为运动小于休息,在115 nm~1 000 nm为运动大于休息.各部位中,肺部DF变化率始终随粒径增长而减小,在30nm附近由正转负;头部和气管支气管中DF变化率分别在100 nm和80 nm附近由负转正.10~40 nm范围内,各部位运动较休息DF变化率的大小关系为:肺部>头部>气管支气管,110~1 000 nm范围内为:头部>气管支气管>肺部.可见,核模态粒子在休息时易沉积在头部和气管中,运动时更易沉积在肺部;爱根核在各部位均是休息状态沉积更多;积聚模态在休息时易沉积在肺部,运动时多数沉积在头部.
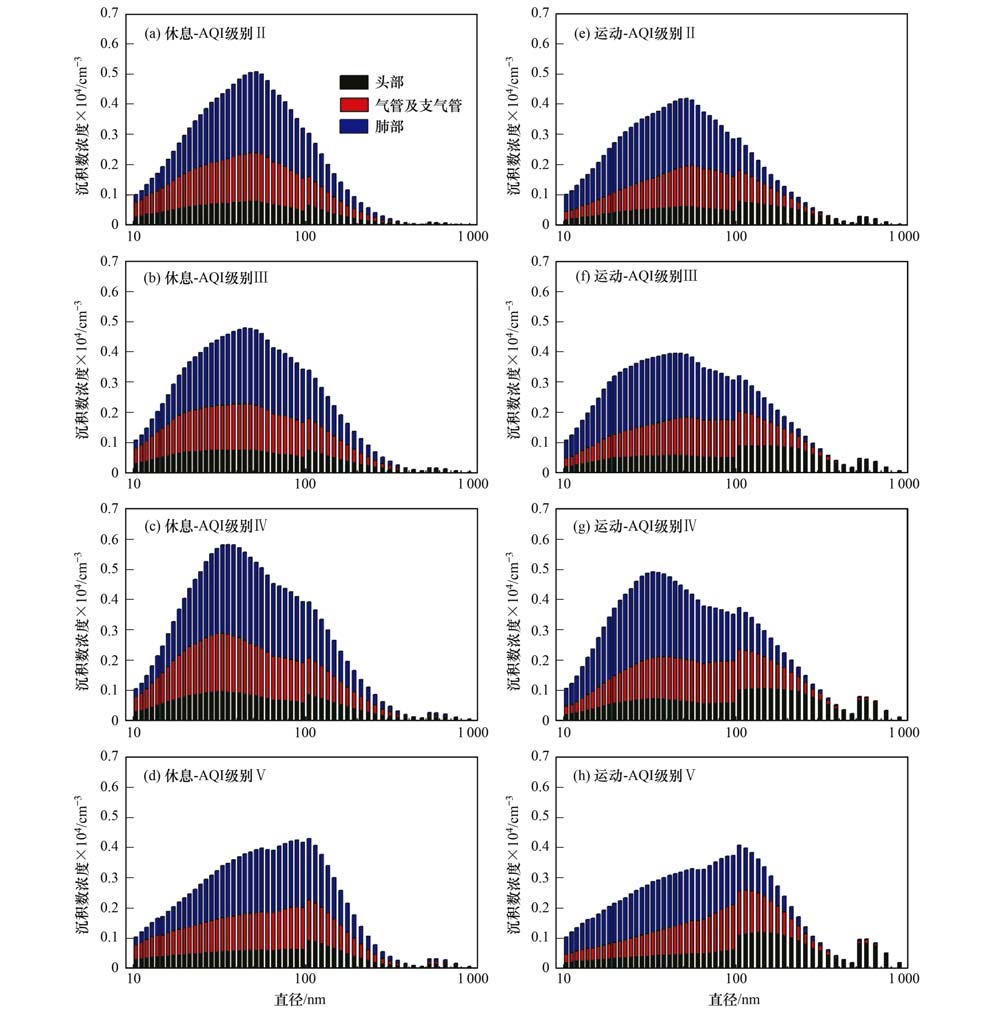
2.3 不同空气质量下的沉积数浓度图 4和图 5为南京北郊冬春两季在各AQI级别下的人体内细粒子沉积数浓度谱分布.冬季 (图 4) 总沉积数浓度均呈单峰分布.从空气质量来看,二、三、四级的总沉积数浓度峰值和各部位沉积数浓度峰值均出现在爱根核模态,且峰位置随空气质量下降而轻微向小粒径移动;五级的总沉积数浓度峰值出现在积聚模态,其主要原因是头部积聚模态粒子沉积增多,肺部和气管中的沉积数浓度较二至四级略有增长.沉积数浓度大小与空气质量无明显关系,可见总空气质量较高时也可能影响人体健康.从两种生理状态来看,休息状态下平均总沉积数浓度为13.53×104 cm-3,各级别峰值分别为二级0.51×104 cm-3、三级0.48×104 cm-3、四级0.58×104 cm-3、五级0.43×104 cm-3;运动状态下平均总沉积数浓度为12.79×104 cm-3,各级别峰值分别为二级0.42×104 cm-3、三级0.40×104 cm-3、四级0.49×104 cm-3、五级0.41×104 cm-3.可以发现运动状态的总沉积数浓度及其峰值均略低于休息状态,核模态和爱根核模态在休息时沉积较高,积聚模态在运动时沉积较高,这一点在头部体现得更加显著.
|
图 4 冬季人体内颗粒物沉积数浓度 Fig. 4 Particle NC deposition in human airway in winter |
|
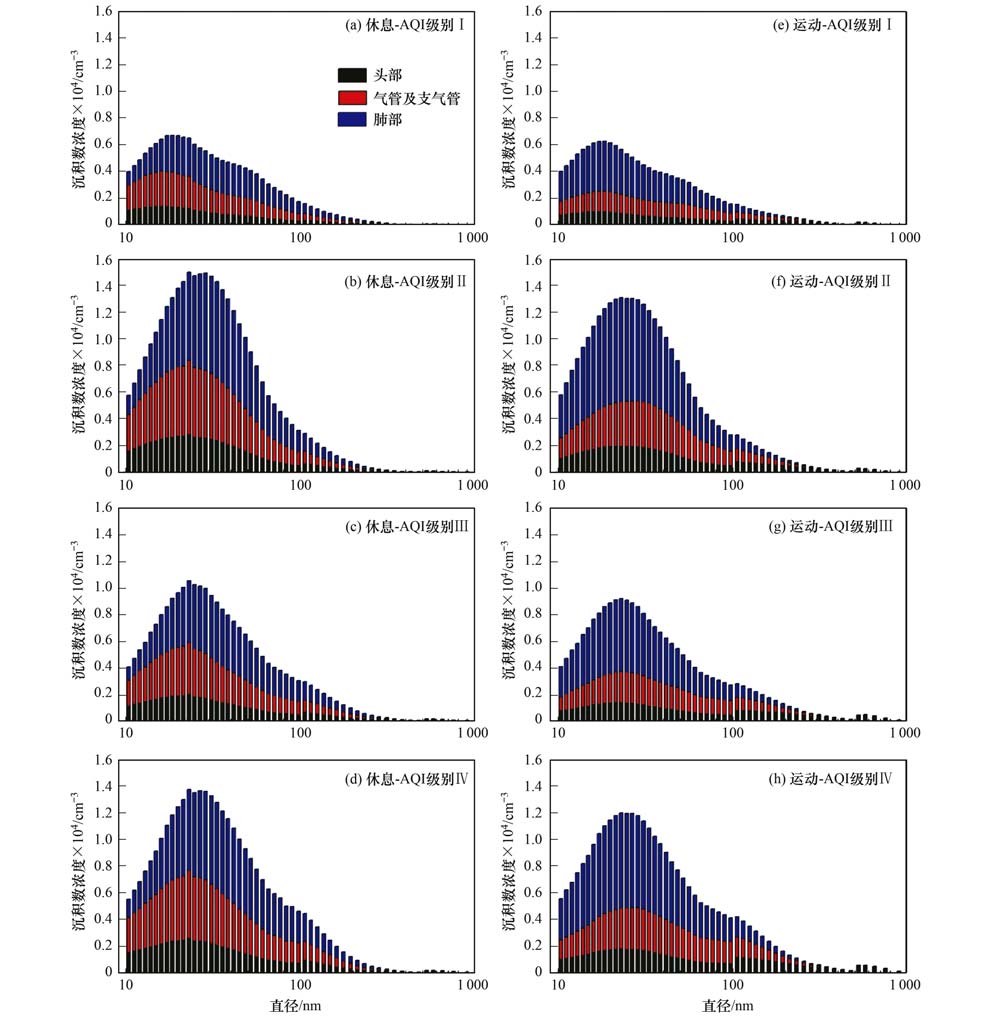
图 5 春季人体内颗粒物沉积数浓度 Fig. 5 Particle NC deposition in human airway in spring |
春季 (图 5) 总沉积数浓度均呈单峰分布,且明显高于冬季.从空气质量来看,一级总沉积数浓度峰值和各部位沉积数浓度峰值均出现在核模态,且总量远小于其他几级;二至四级的峰值均在20~35 nm粒径段浮动.休息状态下平均总沉积数浓度为25.89×104 cm-3,约为冬季的1.92倍,各级别峰值分别为一级0.67×104 cm-3、二级1.50×104 cm-3、三级1.05×104 cm-3、四级1.37×104 cm-3;运动状态下平均总沉积数浓度为0.24×104 cm-3,约为冬季的1.84倍,各级别峰值分别为一级0.63×104 cm-3、二级1.31×104 cm-3、三级0.92×104 cm-3、四级1.20×104 cm-3.可见不同季节中,人体内沉积数浓度分布的差异很大程度取决于环境中粒子数浓度分布的差异,而两种生理状态下的差异基本不受季节影响.
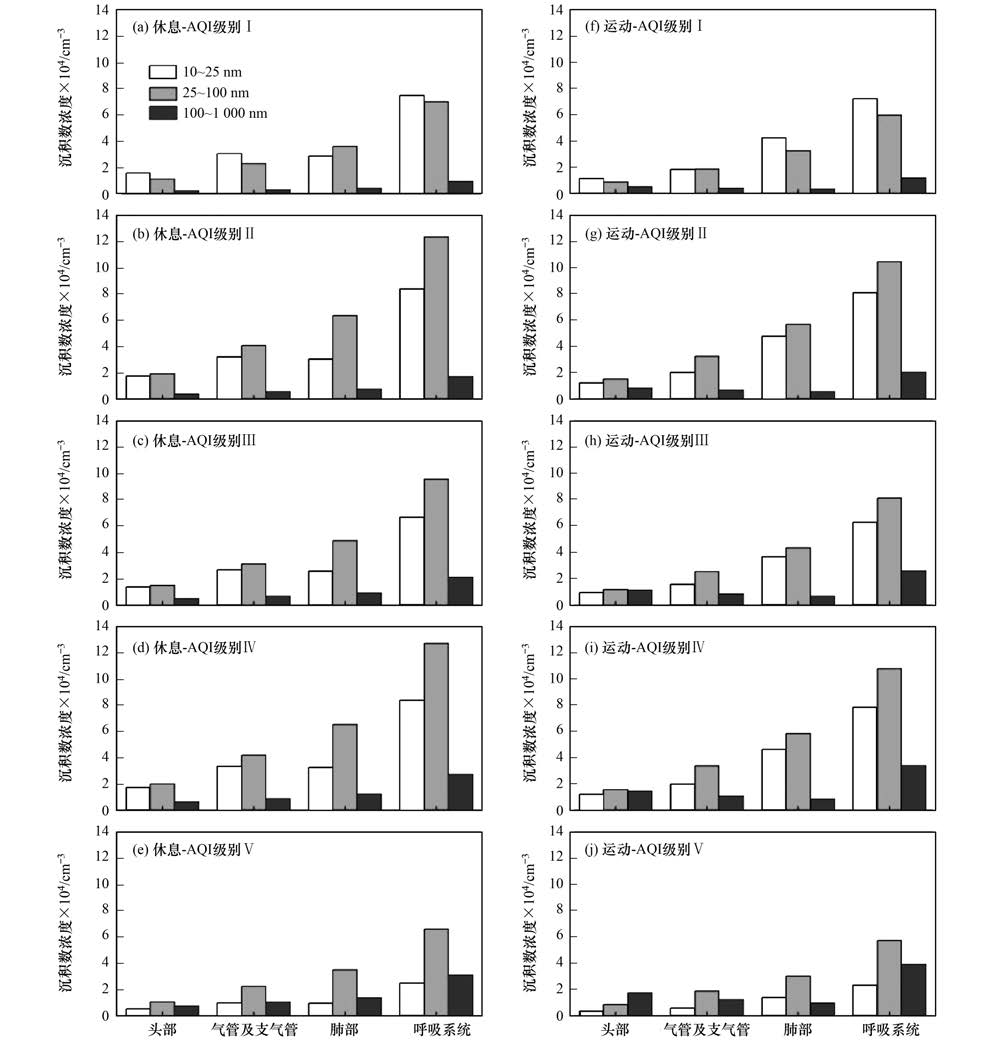
2.4 各模态在不同部位的沉积数浓度图 6为各AQI级别下,休息和运动状态中,各模态粒子在人体不同部位的沉积数浓度.从不同空气质量来看,一级核模态沉积数浓度高于爱根核模态;二至四级爱根核模态高于核模态,且各模态总沉积数浓度均相对较高;五级总沉积数浓度明显较低.积聚模态沉积数浓度随空气质量下降而增长,这一点在运动状态下体现得更为显著,原因在于污染空气中粗粒子数浓度高于洁净大气.休息时各模态平均沉积数浓度分别为核模态6.76×104 cm-3、爱根核模态9.66×104 cm-3、积聚模态2.12×104 cm-3;运动时为核模态6.35×104 cm-3、爱根核模态8.21×104 cm-3、积聚模态2.63×104 cm-3.
|
图 6 各模态在人体不同部位沉积数浓度 Fig. 6 Total NC of deposited particles in different modes in human airway |
各部位的总沉积数浓度大小关系为:肺部>气管支气管>头部,休息和运动状态下的沉积分布差异明显.运动时核模态和爱根核模态在头部、气管支气管和呼吸系统中的总沉积数浓度均低于休息状态,积聚模态反之;肺部在运动时的核模态沉积为休息状态的1.44倍,而爱根核模态和积聚模态均低于休息状态.对于两种运动状态下的相对变化,各模态中总沉积数浓度变化程度最大的是积聚模态,其增长的主要贡献来源为头部,运动时为休息时的2.26倍,且大体趋势表现出空气质量越差,运动较休息增长越多的特点,因此污染较为严重时进行室外运动更易患上呼吸道疾病.核模态和爱根核模态的沉积情况,以及积聚模态在气管和肺部的沉积情况,均保持在较稳定水平.
2.5 不同地区的人体沉降特性对比目前常用的计算人体内颗粒物沉积情况的模式,除MPPD外还有国际辐射防护委员会开发的人体呼吸道模式ICRP Model (1994),以及美国国家辐射防护委员会开发的NCRP (1997) 模式.3种模式均被广泛应用,计算结果也有较高的一致性[36].本研究选取了国内外研究中使用这3种计算模式的5个地区进行对比讨论,具体内容见表 1.
|
|
表 1 选取地区及研究内容介绍 Table 1 Introduction of selected regions and research contents |
在普适沉积规律方面,DF与环境颗粒物浓度无关[37];细粒子在肺泡区域沉积量较高,粗粒子更易沉积在呼吸道外端,如胸外区域 (包括鼻腔、口腔、咽部、喉部)[38];运动时的细粒子DF略高于休息时[36].
在人体内DF方面,日本[34]成年男性在轻运动状态下的DF与本实验结果非常相近,但肺部沉积效率峰值远大于南京地区休息和运动时的最大值,其位置也略有差异,可能是由于不同地区人群体质的不同或运动状态参数不同;总沉积效率最低值与本实验休息时接近但位置出现在较小粒径段.研究发现,日本成年男性与白种人沉积型很相似,两者总沉积效率在1 500 nm粒径处出现最大差值仅为2.80%;白种人肺部沉积效率峰值为53.40%,与日本仅差0.40%;虽然两者肺体积相差超过20.00%且呼吸频率不同,但沉积效率差异非常小.可以看出DF基本不受人种影响,但是仍然受不同地域所造成的不同人群体质的影响.
在定量分析方面,北京的研究结果表明[25, 39],粒径<300 nm的大气细粒子的沉积数浓度随粒径增长而减小,并主要沉积至肺泡内,而粒径>300 nm时粒子在人体头部的沉积量逐渐增加至超过肺部;肺部沉积数浓度最高,约占总吸入颗粒物的一半,且绝大部分为超细颗粒 (冬季90.00%,春季86.00%),这些都与南京相似.但两地沉积数浓度分布型不同,季节变化特征相反,南京的人体各部位沉积数浓度均明显低于北京.此外,北京与洛杉矶同为受交通源影响显著的国际大都市,北京交通干线附近人群体内沉积的粒子总数为洛杉矶的1.50倍,北京人群体内不同部位的沉积量均明显高于洛杉矶.沉积数浓度取决于该地区环境中的颗粒物数浓度,其分布型也与环境中颗粒物的分布情况密切相关.3个地区数值上的差异主要来源于气溶胶数谱分布的差异以及空气质量的不同.
3 结论(1) 核模态和爱根核模态在休息和运动状态下DF近似,积聚模态在运动时DF是休息时的2.49倍.肺部对核模态和爱根核模态的DF贡献最大 (休息时48.17%,运动时54.23%),头部对积聚模态DF贡献最大 (休息41.23%,运动80.47%).
(2) 冬春两季的人体内细粒子沉积数浓度均呈单峰分布,且冬季明显低于春季;沉积数浓度峰值出现的位置与空气质量有关,无污染时出现在核模态,轻度至中度污染时出现在爱根核模态,污染较严重时出现在积聚模态.运动状态的总沉积数浓度和峰值均略低于休息状态,核模态和爱根核模态在休息时沉积较高,积聚模态在运动时沉积较高.
(3) 人体各部位的总沉积数浓度大小关系为:肺部>气管支气管>头部.与休息时相比,运动时肺部核模态沉积增多,气管及支气管和头部积聚模态沉积增多,且头部表现出空气质量越差,运动较休息增长越多的特点.
(4) 南京北郊人体内沉积数浓度的分布型与北京不同,季节变化特征与北京相反,各部位中沉积量均明显低于北京.
| [1] | Brook R, Brook J R, Urch B, et al. Inhalation of fine particulate air pollution and ozone causes acute arterial vasoconstriction in healthy adults[J]. Circulation, 2002, 105(13): 1534–1536. DOI: 10.1161/01.CIR.0000013838.94747.64 |
| [2] | Simkhovich B Z, Kleinman M T, Kloner R A. Air pollution and cardiovascular injury:epidemiology, toxicology, and mechanisms[J]. Journal of the American College of Cardiology, 2008, 52(9): 719–726. DOI: 10.1016/j.jacc.2008.05.029 |
| [3] | Pope Ⅲ C A, Burnett R T, Thun M J, et al. Lung cancer, cardiopulmonary mortality, and long-term exposure to fine particulate air pollution[J]. JAMA, 2002, 287(9): 1132–1141. DOI: 10.1001/jama.287.9.1132 |
| [4] | Delfino R J, Sioutas C, Malik S. Potential role of ultrafine particles in associations between airborne particle mass and cardiovascular health[J]. Environmental Health Perspectives, 2005, 113(8): 934–946. DOI: 10.1289/ehp.7938 |
| [5] | Pope Ⅲ C A, Burnett R T, Thurston G D, et al. Cardiovascular mortality and long-term exposure to particulate air pollution:epidemiological evidence of general pathophysiological pathways of disease[J]. Circulation, 2004, 109(1): 71–77. |
| [6] | Dominici F, Peng R D, Bell M L, et al. Fine particulate air pollution and hospital admission for cardiovascular and respiratory diseases[J]. JAMA, 2006, 295(10): 1127–1134. DOI: 10.1001/jama.295.10.1127 |
| [7] | Brown D M, Wilson M R, MacNee W, et al. Size-dependent proinflammatory effects of ultrafine polystyrene particles:a role for surface area and oxidative stress in the enhanced activity of ultrafines[J]. Toxicology and Applied Pharmacology, 2001, 175(3): 191–199. DOI: 10.1006/taap.2001.9240 |
| [8] | International Agency for Research on Cancer. IARC:outdoor air pollution a leading environmental cause of cancer deaths[J]. Air Quality & Climate Change, 2013, 47(4): 16. |
| [9] | Hamra G B, Guha N, Cohen A, et al. Outdoor particulate matter exposure and lung cancer:a systematic review and meta-analysis[J]. Environmental Health Perspectives, 2014, 122(9): 906–911. |
| [10] | Chen R J, Kan H D, Chen B H, et al. Association of particulate air pollution with daily mortality:the china air pollution and health effects study[J]. American Journal of Epidemiology, 2012, 175(11): 1173–1181. DOI: 10.1093/aje/kwr425 |
| [11] | Meng X, Ma Y J, Chen R J, et al. Size-fractionated particle number concentrations and daily mortality in a Chinese city[J]. Environmental Health Perspectives, 2013, 121(10): 1174–1178. |
| [12] | 周鑫. 颗粒物在人体呼吸系统中传输与沉积的数值模拟研究[D]. 长沙: 中南大学, 2010. Zhou X. Numerical investigation on the transport and deposition of particulate matter in human pulmonary airways[D]. Changsha:Central South University, 2010. |
| [13] | 欧翠云. 颗粒物在人体气管支气管模型中传输与沉积的数值模拟研究[D]. 长沙: 中南大学, 2011. Ou C Y. Numerical simulation of the particle transport and deposition in human tracheobronchial airways[D]. Changsha:Central South University, 2010. |
| [14] | Kan H D, London S J, Chen G H, et al. Differentiating the effects of fine and coarse particles on daily mortality in Shanghai, China[J]. Environment International, 2007, 33(3): 376–384. DOI: 10.1016/j.envint.2006.12.001 |
| [15] | Valavanidis A, Fiotakis K, Vlachogianni T. Airborne particulate matter and human health:toxicological assessment and importance of size and composition of particles for oxidative damage and carcinogenic mechanisms[J]. Journal of Environmental Science and Health, Part C:Environmental Carcinogenesis and Ecotoxicology Reviews, 2008, 26(4): 339–362. DOI: 10.1080/10590500802494538 |
| [16] | Breitner S, Liu L Q, Cyrys J, et al. Sub-micrometer particulate air pollution and cardiovascular mortality in Beijing, China[J]. Science of the Total Environment, 2011, 409(24): 5196–5204. DOI: 10.1016/j.scitotenv.2011.08.023 |
| [17] | 吉贵祥, 徐诚, 顾爱华, 等. 南京市PM2. 5污染特征及人群健康效应研究[A]. 见: 中国毒理学会. 中国毒理学会第七次全国毒理学大会暨第八届湖北科技论坛论文集[C]. 武汉: 中国毒理学会, 2015. 47-47. |
| [18] | 方叠. 中国主要城市空气污染对人群健康的影响研究[D]. 南京: 南京大学, 2014. Fang D. Impact assessment of air pollution on the population health in major cities of China[D]. Nanjing:Nanjing University, 2014. |
| [19] | Gao J, Wang T, Zhou X H, et al. Measurement of aerosol number size distributions in the Yangtze River Delta in China:formation and growth of particles under polluted conditions[J]. Atmospheric Environment, 2009, 43(4): 829–836. DOI: 10.1016/j.atmosenv.2008.10.046 |
| [20] | United States Environmental Protection Agency. Air monitoring methods-criteria pollutants[EB/OL]. http://www.epa.gov/ttn/amtic/criteria.html, 2016-09-30. |
| [21] | 邵平, 安俊琳, 杨辉, 等. 南京北郊夏季近地层臭氧及其前体物体积分数变化特征[J]. 环境科学, 2014, 35(11): 4031–4043. Shao P, An J L, Yang H, et al. Variation characteristics of surface ozone and its precursors during summertime in Nanjing Northern Suburb[J]. Environmental Science, 2014, 35(11): 4031–4043. |
| [22] | HJ 633-2012, 环境空气质量指数 (AQI) 技术规定 (试行)[S]. HJ 633-2012, Technical regulation on ambient Air Quality Index (on trial)[S]. |
| [23] | ARA. Multiple-path particle dosimetry model (MPPD v 3.04)[EB/OL]. https://www.ara.com/products/multiple-path-particle-dosimetry-model-mppd-v-304.html, 2016. |
| [24] | Anjilvel S, Asgharian B. A multiple-path model of particle deposition in the rat lung[J]. Fundamental and Applied Toxicology, 1995, 28(1): 41–50. DOI: 10.1006/faat.1995.1144 |
| [25] | Li X Y, Yan C Q, Patterson R F, et al. Modeled deposition of fine particles in human airway in Beijing, China[J]. Atmospheric Environment, 2016, 124: 387–395. DOI: 10.1016/j.atmosenv.2015.06.045 |
| [26] | Roy M, Becquemin M H, Bouchikhi A. Ventilation rates and lung volumes for lung modelling purposes in ethnic groups[J]. Radiation Protection Dosimetry, 1991, 38(1-3): 49–55. DOI: 10.1093/oxfordjournals.rpd.a081071 |
| [27] | 杨海平. 关于《运动生理学》教材中氧债功能余气量的探讨[J]. 沈阳体育学院学报, 1991(3): 73–76. Yang H P. Discussion on the functional residual capacity in Exercise Physiology[J]. Journal of Shenyang Sport University, 1991(3): 73–76. |
| [28] | 曹志发, 孟昭琴, 姚为俊. 新编运动生理学[M]. 北京: 人民体育出版社, 2004: 130. |
| [29] | Hu M, Peng J F, Sun K, et al. Estimation of size-resolved ambient particle density based on the measurement of aerosol number, mass, and chemical size distributions in the winter in Beijing[J]. Environmental Science & Technology, 2012, 46(18): 9941–9947. |
| [30] | Kim C S, Jaques P A. Analysis of total respiratory deposition of inhaled ultrafine particles in adult subjects at various breathing patterns[J]. Aerosol Science and Technology, 2004, 38(6): 525–540. DOI: 10.1080/02786820490465513 |
| [31] | Bunchatheeravate P, Curtis J S. Deposition of non-spherical particles in bifurcating airways[J]. Pharmaceutical Development and Technology, 2014, 19(8): 942–951. DOI: 10.3109/10837450.2013.840848 |
| [32] | Hussain M, Madl P, Khan A. Lung deposition predictions of airborne particles and the emergence of contemporary diseases Part I[J]. TheHealth, 2011, 2(2): 51–59. |
| [33] | 尹景娟. 颗粒物在人体上呼吸道内运动沉降规律的研究[D]. 北京: 北京交通大学, 2007. Yin J J. Study on the characteristics of transporation and deposition of inhalational particles in respiratory tract[D]. Beijing:Beijing Jiaotong University, 2007. |
| [34] | Yamada Y, Fukutsu K, Kurihara O, et al. Influences of biometrical parameters on aerosol deposition in the ICRP 66 Human Respiratory Tract Model:Japanese and Caucasians[J]. Earozoru Kenkyu, 2007, 22(3): 236–243. |
| [35] | Horemans B, Van Holsbeke C, Vos W, et al. Particle deposition in airways of chronic respiratory patients exposed to an urban aerosol[J]. Environmental Science & Technology, 2012, 46(21): 12162–12169. |
| [36] | Chalupa D C, Morrow P E, Oberd rster G, et al. Ultrafine particle deposition in subjects with asthma[J]. Environmental Health Perspectives, 2004, 112(8): 879–882. DOI: 10.1289/ehp.6851 |
| [37] | Sánchez-Soberón F, Mari M, Kumar V, et al. An approach to assess the Particulate Matter exposure for the population living around a cement plant:modelling indoor air and particle deposition in the respiratory tract[J]. Environmental Research, 2015, 143(Part A): 10–18. |
| [38] | Megido L, Suárez-Peña B, Negral L, et al. Relationship between physico-chemical characteristics and potential toxicity of PM10[J]. Chemosphere, 2016, 162: 73–79. DOI: 10.1016/j.chemosphere.2016.07.067 |
| [39] | 郑玫, 李小滢, 闫才青, 等. 大气细颗粒物在人体不同部位沉降特性研究[A]. 见: 中国环境科学学会. 第19届中国大气环境科学与技术大会暨中国环境科学学会大气环境分会2012年学术年会论文集[C]. 青岛: 中国环境科学学会, 2012. 103. |
 2017, Vol. 38
2017, Vol. 38


