2. 中国科学院生态环境研究中心环境水质学国家重点实验室, 北京 100085;
3. 中国地质大学(武汉)环境学院, 武汉 430074
2. State Key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China;
3. School of Environmental Studies, China University of Geosciences, Wuhan 430074, China
随着我国城市污水处理设施的普及,处理率的提高和处理程度的深化,污泥的产生量有了较大的增长[1].如果没有对这些大量的污泥进行有效妥善的处理,这将对我国的生态环境造成巨大的威胁[2].然而,传统的污泥处理工艺费用昂贵,占到了整个污水处理厂运行成本的60%以上[3].此外,污泥处理还面临着许多的技术难题与挑战,从二沉池产生的剩余活性污泥含水率达到了99%以上,由于高的污泥含水率总是伴随着污泥体积庞大、 运输费用昂贵、 污泥运输难度大以及占用处理场地大等问题.因此,改善污泥脱水效率成为了污水处理乃至环境科学技术领域的重要研究方向.
通常,污泥中的水分包括游离水(约占70%)、 间隙水(约占20%)、 吸附水(约占7%)和结合水(约占3%)等[4].如果不考虑污泥本身的性质,污泥的脱水效率主要取决于脱水设备的选型和化学调理方式[5].一般而言,为了改善污泥的过滤脱水性能,之前会对污泥进行适当的化学预处理.例如,通过电中和以及吸附架桥作用,无机或者有机絮凝剂可以使得污泥胶体形成较大的絮体,便于大幅去除污泥中的水含量[6, 7].胞外聚合物(extracellular polymeric substances,EPS)占到了污泥总固体的60%~80%[8].污泥EPS中含有大量的结合水,而传统的污泥调理方法并不能有效地破坏EPS,使之将结合水转化成自由水去除[9].而高级污泥调理技术(AST)可以通过溶解EPS到达改善污泥过滤脱水性能以及降低泥饼含水率的目的,例如,光Fenton/Fenton氧化技术[10~12]、 酸碱处理[13]、 热处理[9]、 酶处理[14]以及集成化处理等.
过氧化钙(CaO2)是一种通用并且安全的经典氧化剂,被称为“固态”过氧化氢(H2O2)[15].一般情况下,CaO2在水中会缓慢生成H2O2和氧气(O2),是一种强氧化剂; 同时,生成的Ca2+还有助于混凝作用[16].此外,CaO2同时还具有漂白、 脱臭以及消毒杀菌的作用,因此,它被广泛应于农业、 水产养殖业以及制药领域[17].以前的研究表明,CaO2可以修复有机微污染的土壤[18].同时,CaO2可以在不同pH条件下有效地氧化四氯乙烯[19].Zhang等[20]的研究表明,CaO2可以有效去除污泥中的内分泌干扰物(endocrine disrupting chemicals,EDCs)并且提高污泥的溶解效率.此外,CaO2在氧化过程中产生的强碱——Ca(OH)2不仅可以提高污泥的水解效率[13, 21],而且可以有效改善污泥的厌氧消化特性[22].
然而,采用过氧化钙预调理对污泥脱水性能影响的研究较少,尤其是调理过程中污泥的絮体形态特性.本研究的目的在于: 第一,研究过氧化钙调理对污泥过滤脱水性能的影响; 第二,深入了解调理过程中污泥絮体形态特性的变化以及反应动力学机制; 第三,优化CaO2调理的工艺方法和控制参数,以期为过氧化钙在污泥处理过程中的应用提供理论支持.
1 材料与方法 1.1 污泥与试剂来源本研究所采用的污泥取自北京市北小河再生水厂,该厂处理规模为10万t·d-1,采用膜生物反应器(membrane bio-reactor,MBR)与臭氧连用工艺.剩余活性污泥的含水率为98.3%,初始pH为6.81,平均粒径为58.677 μm,污泥比阻(specific resistance to filtration,SRF)为1.53×1013 m·kg-1; 此外,污泥上清液化学需氧量(chemical oxygen demand,COD)为132mg·L-1,Zeta电位值为-14.3.
本研究所采用的试剂均由国药集团化学试剂有限公司提供.另外,除过氧化钙(CaO2)试剂的纯度为70%以外,其余试剂均为分析纯.
1.2 实验方法 1.2.1 CaO2污泥溶解实验分别取不同剂量的CaO2于150 mL污泥中,并将盛放污泥的250 mL锥形瓶置于水平恒温振荡器中(25℃±1℃),在200r·min-1条件下充分反应1h.污泥溶解动力学实验: 取800 mL污泥置于1 L烧杯中,并投加CaO2,同时采用悬臂式机械搅拌仪进行充分搅拌反应.实验在60 min内分别取不同的时间间隔进行取样,并将污泥样品及时进行分离提取,以免产生实验误差.
1.2.2 污泥溶解性组分的分离提取将污泥置于50 mL离心管中,在3 000r·min-1下离心10 min,得到污泥上清液组分[6].
1.2.3 亚铁离子协同CaO2溶解污泥实验分别(以TSS计)取50 mg·g-1的CaO2于100 mL污泥中,并在此基础之上,分别同时投加不同剂量的FeSO4粉末,使得Fe2+/CaO2(摩尔比)位于0.05~1之间,在水平恒温振荡器中(25℃±1℃,200r·min-1)充分反应1h后进行样品提取分析.
1.3 分析方法 1.3.1 污泥脱水性测定污泥比阻(SRF)是表征污泥过滤特性的综合性指标,它表示单位质量的污泥在一定压力下过滤时单位过滤面积上的阻力.SRF测定时,抽滤所采用的真空压力为0.06MPa,并且计算机通过电子天平每隔2 s记录一次50 mL污泥的过滤体积,直至10 min后停止测定.同时,取出滤纸上形成的泥饼,利用差量法计算含水率.此外,比阻计算公式:
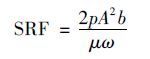
|
(1) |
式中,p为过滤压力(kg·m-2); A为过滤面积(m2);μ为滤液的动力黏度(kg·s·m-2); ω为滤过单位体积的滤液在过滤介质上截留的干固体重量(kg·m-3); b为过滤方程t/V=bV+a所代表的直线的斜率,t为过滤时间(s); V为滤液体积(m3).
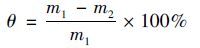
|
(2) |
式中, θ表示污泥含水率,m1为抽滤脱水后泥饼质量,m2为烘干后泥饼质量.
1.3.2 三维荧光光谱分析实验采用Hitachi F-7000荧光光谱仪对污泥上清液组分的三维荧光光谱(Three-dimentional excitation emission matrix,3DEEM)进行测定.激发光源为氙弧灯,激发波长Ex为200~400 nm,发射波长Em为220~550 nm,激发和发射狭缝宽度为5 nm,扫描速度为12 000nm·min-1.
1.3.3 高效体积排阻色谱高效体积排阻色谱(HPSEC)采用Waters液相色谱系统,由Waters 2487双波长吸收检测器、 Waters 1525泵组成.分离所用色谱柱为Shodex KW 802.5柱(Shoko Co.,Japan).流动相为5mmol·L-1的磷酸盐缓冲液和0.01 mol·L-1 NaCl溶液,配制后用0.22 μm的膜过滤,然后超声波脱气15 min.流动相流速为0.8 mL·min-1,进样量为200 μL.聚苯乙烯磺酸钠(PSS)作为分子量的标准物质,标线中所用的PSS相对分子质量分别为1 800、 4 200、 6 500和32 000(Sigma,Aldrich)[23, 24].
1.3.4 其他指标溶解性有机碳(dissolved organic carbon,DOC)采用TOC分析仪(TOC-L,SHIMADZU Inc.,Japan)测定.粒径分析采用马尔文激光粒度仪(Malvern Mastersizer 2000,Malvern,UK)测定.另外,电镜观测采用HITACHI SU8020型场发射扫描电镜,污泥样品需经过冷冻干燥处理.
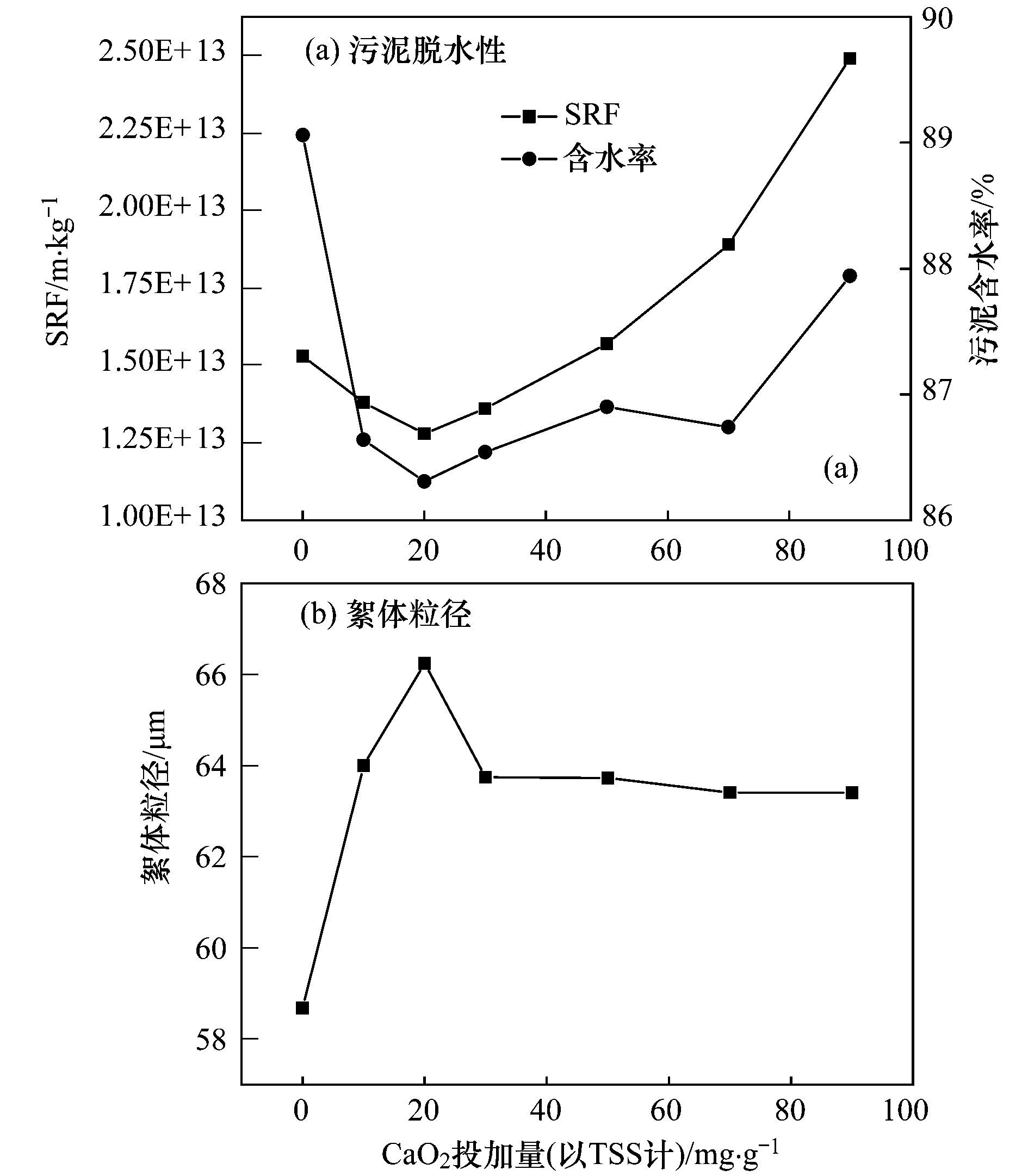
2 结果与讨论 2.1 CaO2对污泥特性的影响 2.1.1 CaO2投加量对污泥脱水性能的影响通过图 1(a)可以看出,随着过氧化钙投加量的增加,SRF呈现先下降后上升的趋势,同样,抽滤后泥饼的含水率与SRF的变化相同.当过氧化钙的投加量(以TSS计,下同)为20 mg·g-1时,污泥SRF达到最低,为1.28×1013 m·kg-1; 此时,泥饼的含水率也达到最低的86.31%.此外,结合图 1(b),污泥絮体的平均粒径分布随着投加量的上升,起初出现了较为明显的增长,在投加量为20 mg·g-1时,絮体粒径出现明显的峰值,随后在投加量为30 mg·g-1处趋于平缓.有研究表明,投加无机混凝剂导致污泥颗粒迅速聚集形成较大的絮体是由于吸附架桥和电中和的共同作用[16].
|
图 1 CaO2投加量对污泥脱水性和絮体粒径的影响 Fig. 1 Effect of CaO2 dosage on sludge dewaterability and floc size |
然而CaO2在氧化裂解污泥的同时,生成的Ca2+又加速了污泥絮体的团聚,导致絮体的粒径出现了明显的增长.随后污泥粒径出现的明显下降并趋于平稳,可能是由于随着CaO2投加量的增多,其氧化裂解作用逐渐增强使得絮体裂解程度加剧而导致的,并在氧化混凝作用达到平衡的时候,污泥粒径逐渐趋于稳定.因此,当CaO2的投加量为20 mg·g-1时,污泥的过滤脱水效果最佳.
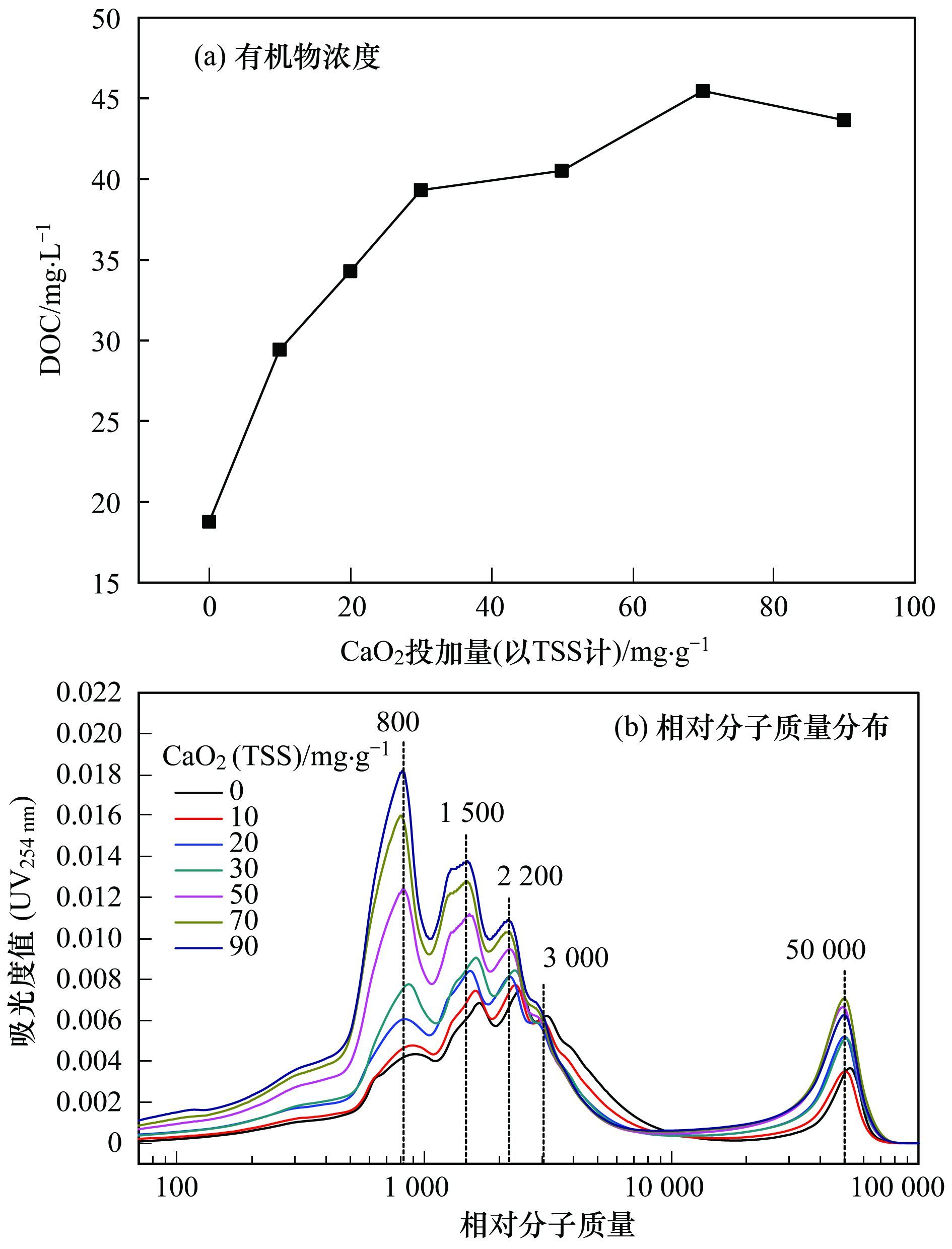
2.1.2 CaO2投加量对污泥上清液组分的影响如图 2(a)所示,污泥上清液的有机物浓度随着CaO2的投加量出现了明显的上升,从18.77mg·L-1增至43.65mg·L-1.同时,由图 2(b)可知,污泥上清液组分的相对分子质量分布出现了5个峰值,分别为800、 1 500、 2 200、 3 000和50 000.在这些分子量中,除3 000所对应的峰值无明显变化以外,其余4个峰值均出现了较为明显的上升.根据Lyko等[25]的分类方法,污泥胞外聚合物的分子量可以大致分为3个部分: 蛋白质和多糖类等大分子有机物大分子组分(>5 000)、 中分子量组分(1 000~5 000)和分子骨架物质等低分子量组分(<1 000).因此,CaO2投加量的增加使得污泥中大分子有机物裂解并释放至污泥上清夜中,从而导致了其DOC浓度的上升.此外,Kiss等[26]的研究表明,腐殖酸类有机物的平均分子量在100~800之间.因此,污泥在过氧化钙预调理之后,其上清液组分中并未出现腐殖酸类物质.
|
图 2 CaO2投加量对污泥上清液有机物浓度和相对分子质量分布的影响 Fig. 2 Effect of CaO2 dosage on organic concentration and relative molecular weight distribution in sludge supernatant |
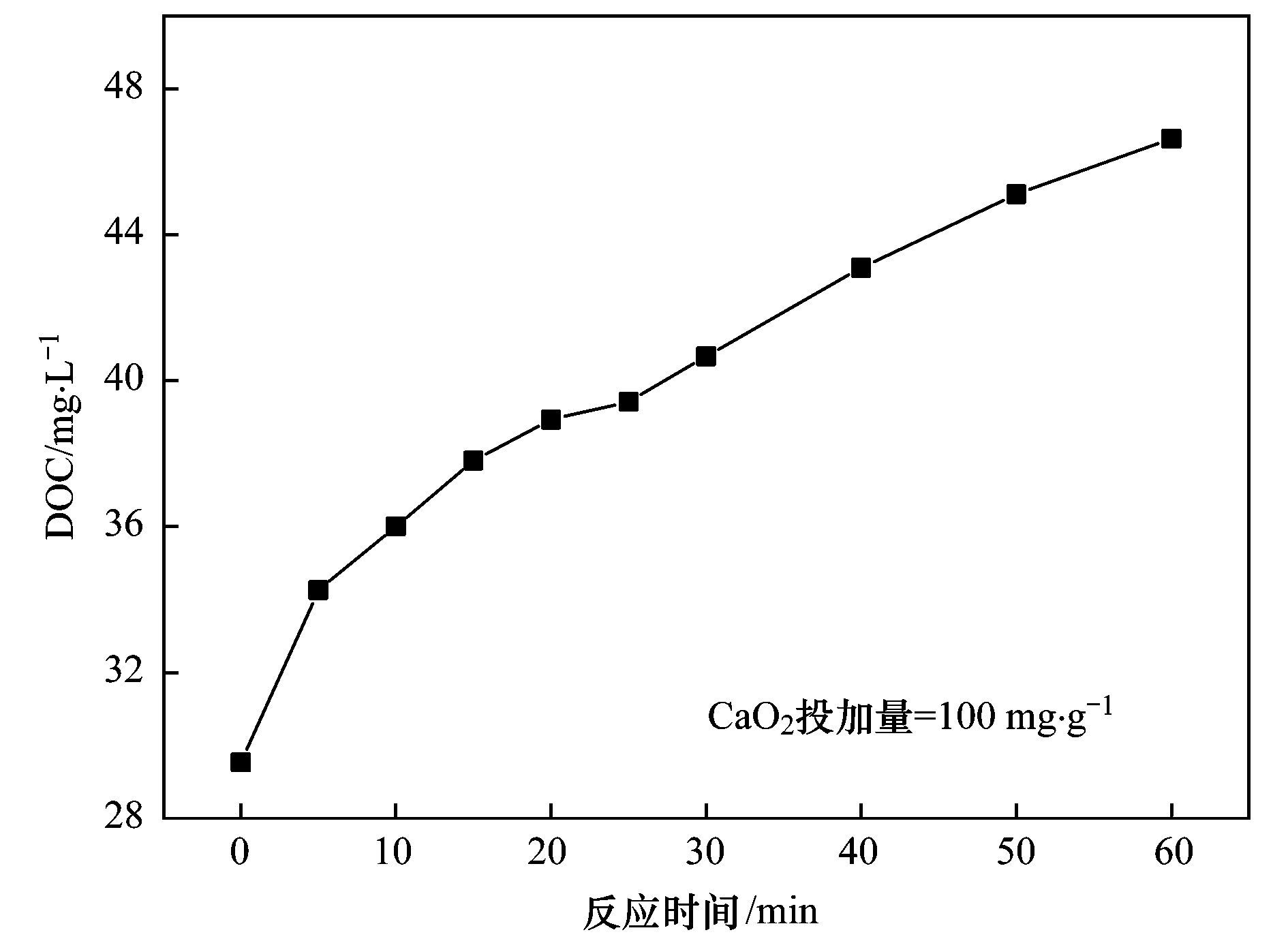
由图 3可知,随着反应时间的变化,污泥上清液DOC含量出现了明显的上升,最终从29.54mg·L-1上升至46.62mg·L-1.这可能是由于经过氧化钙调理后,污泥大分子得到了有效的裂解所导致[20].反应动力学方程如下:
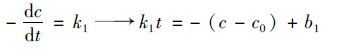
|
(3) |
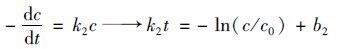
|
(4) |
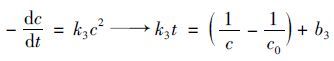
|
(5) |
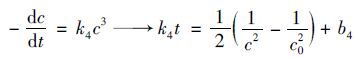
|
(6) |
式(3)~(6)分别表示0、 1、 2和3级反应动力学方程.式中,c表示污泥上清液有机物浓度,kn(n=1,2,3,4)分别代表污泥裂解速率常数,并且均拥有各自不同的量纲; bn(n=1,2,3,4)分别表示每个方程的积分常数.通过分别构建c-t、 ln(c/c0)-t、 1c-t以及1c2-t,利用拟合出的斜率和截距即可求得k和b值(见表 1).由此可见,CaO2溶解污泥遵循准零级反应动力学,拟合相关系数达0.925,反应速率常数为15.2 mg·L-1·h-1.
|
图 3 污泥上清液有机物含量随反应时间的变化 Fig. 3 Variation of organic concentration in sludge supernatant with reaction time |
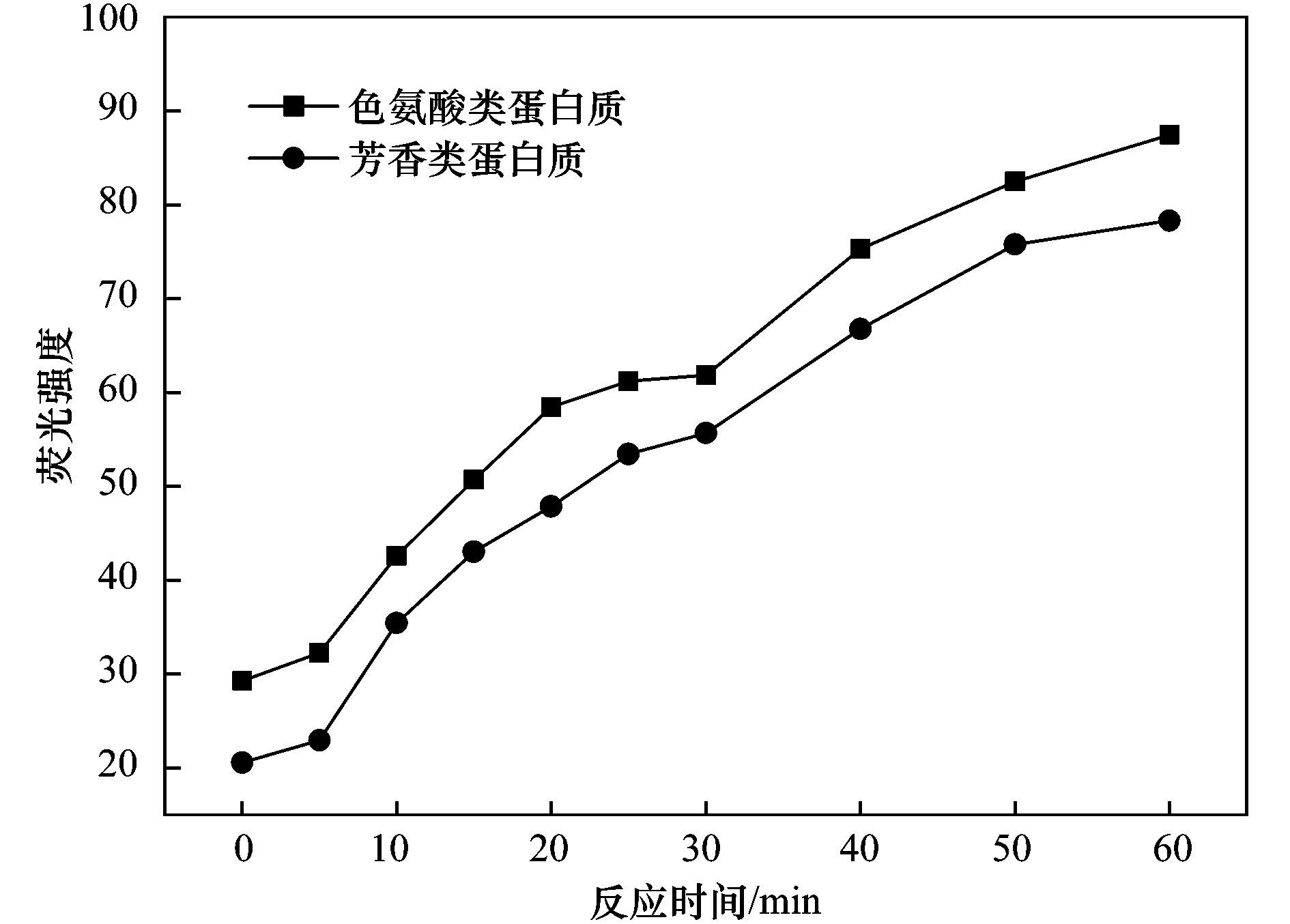
三维荧光光谱分析由于其具有较高的灵敏度和选择性被广泛应用于各种水质中有机物质的检测[27].有研究表明,三维荧光光谱被分为5大区域,分别为: 色氨酸类蛋白、 芳香类蛋白Ⅰ、 芳香类蛋白Ⅱ、 腐殖酸和富里酸[28].图 4为污泥上清夜的荧光光谱,图谱中分别在色氨酸类蛋白(Ex/Em=280/335 nm)和芳香类蛋白(Ex/Em=230/335 nm)的位置出现两个峰值,而峰值随时间出现了明显的上升,并表现出来与DOC相同的趋势,分别从29.25和20.56增至87.47和78.33(见图 5).不难推断,CaO2的加入导致了污泥絮体的裂解及有机物的释放.然而,光谱中并未检测到腐殖酸以及富里酸类物质的荧光峰,说明CaO2预裂解并不能使得污泥絮体裂解释放此类小分子物质,而这也证实了之前文中HPSEC的分析结果.
|
|
表 1 CaO2溶解污泥不同级数反应动力学拟合 Table 1 Different kinetic curve fitting of CaO2 dissolution in sludge |

|
图 4 CaO2处理污泥上清液荧光光谱随反应时间的变化 Fig. 4 Variation in fluorescence spectrum of sludge supernatant after CaO2 addition with reaction time |
|
图 5 CaO2处理后上清液荧光强度随反应时间的变化 Fig. 5 Variation of fluorescent intensities in EEM under CaO2 oxidation with reaction time |
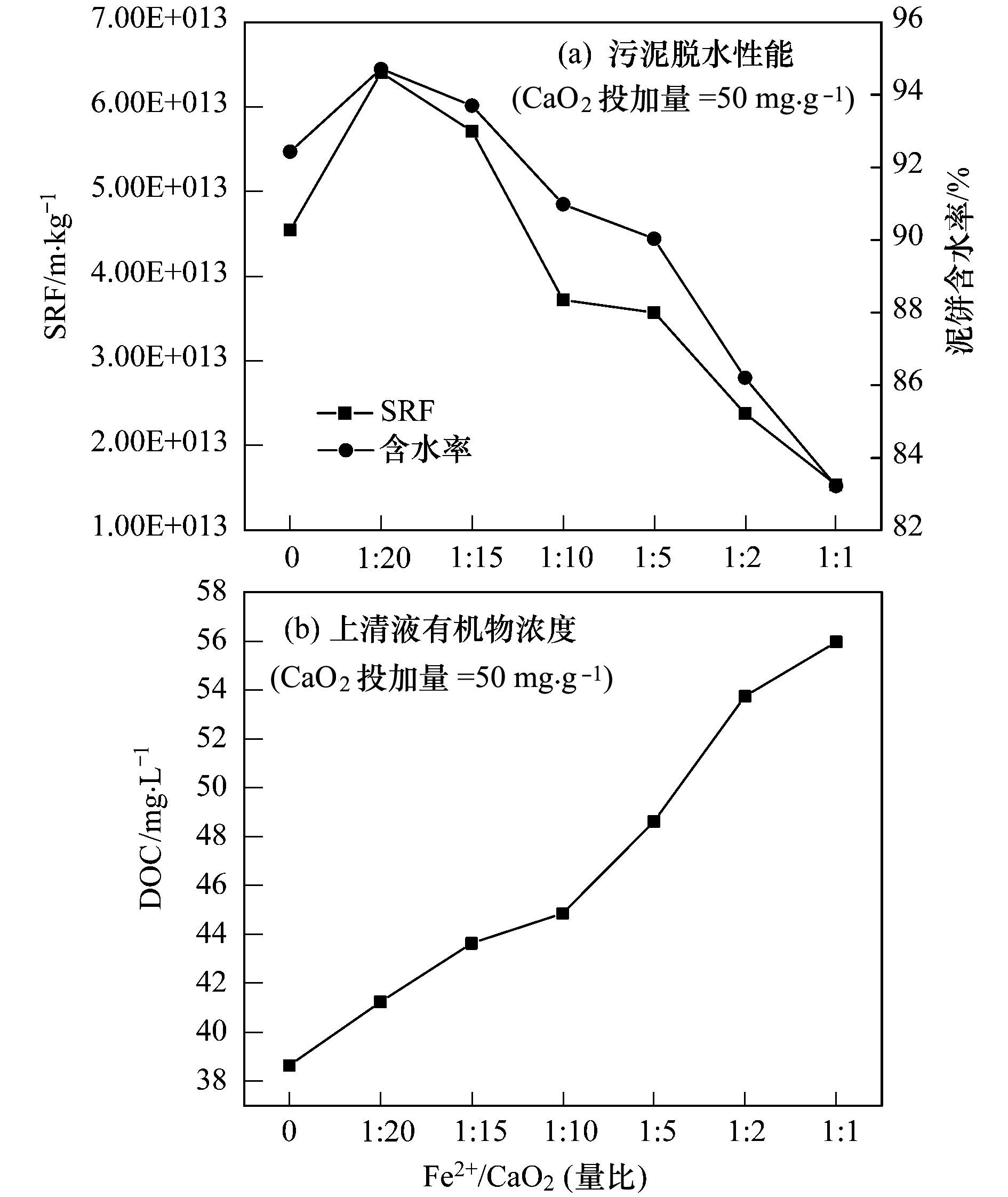
如图 6所示,污泥的过滤脱水性能随着Fe2+和CaO2比例的升高出现了明显的改善,SRF从4.55×1013 m·kg-1降至1.54×1013 m·kg-1,而滤后泥饼的含水率也从92.44%降至83.23%; 与此同时,污泥上清液有机物浓度却出现了较为明显的上升,由38.64mg·L-1增至55.96mg·L-1.根据公式(7)~(9):
|
图 6 Fe2+与CaO2不同摩尔比对对污泥脱水性能和上清液有机物浓度的影响 Fig. 6 Effects of different molar ratios of Fe2+ and CaO2 on sludge dewaterability and organic concentration in supernatant |
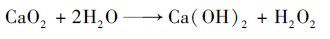
|
(7) |
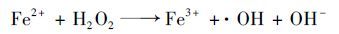
|
(8) |
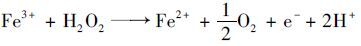
|
(9) |
这可能是由于Fe2+的加入使得反应构成了芬顿(Fenton)体系[20],其过程中产生的羟基自由基(·OH)具有较强的氧化特性,从而强化了污泥的裂解过程.同时,反应过程中产生的Fe3+会在压缩双电层的作用下,将絮体变得更为密实,有助于自由水的去除[6].因此,随着Fe2+/CaO2(摩尔比)增大,污泥过滤脱水性能得到了进一步的改善.
2.2.2 Fe2+协同CaO2调理对污泥絮体形态的影响通过图 7可以看出污泥絮体在FE-SEM下的具体形态,未经处理的污泥絮体[见图 7(a)]表面相对比较平滑,而经过氧化钙处理后的污泥絮体[见图 7(b)和7(c)]结构则表现出疏松、 孔隙分布复杂等的特点,并且高CaO2投加量的污泥絮体结构越破碎分散.这也就不难推断,污泥絮体在CaO2的调理下裂解作用明显; 此外,通过图 7(d)可以看出,污泥絮体经过Fe2+协同CaO2调理之后,明显出现了破碎絮体紧密团聚的现象,其多表现为体积较小而致密并且类似于结晶的碎片,而这与文中先前所提到的污泥絮体重建过程相吻合.

|
(a)原泥; (b)CaO2=20 mg·g-1; (c)CaO2=90 mg·g-1; (d)Fe2+/CaO2(摩尔比)=1:1(10 000倍) 图 7 电镜下的污泥絮体 Fig. 7 Sludge floc morphology observed by FE-SEM (magnified by 10 000 times) |
(1) 经过CaO2处理之后,污泥的过滤脱水性能先改善后恶化,当投加量(以TSS计)为20 mg·g-1时,污泥的过滤脱水效果达到最佳,这可能是由于CaO2兼具氧化和混凝的双重作用.
(2) 经过CaO2调理过后,污泥絮体结构变得疏松破碎,其上清液有机物浓度出现了明显的上升,证明污泥得到了有效裂解.
(3) 污泥溶解反应过程遵循零级反应动力学模型,反应速率常数为15.2 mg·L-1·h-1.
(4) 相比CaO2单一处理,Fe2+可以使得污泥中的大分子有机物进一步裂解释放,并且可以有效强化CaO2处理污泥的过滤脱水性能,这可能是由于反应体系中产生的羟基自由基和Fe3+的共同作用所致.
| [1] | Kim Y K, Bae J H, Oh B K, et al. Enhancement of proteolytic enzyme activity excreted from Bacillus stearothermophilus for a thermophilic aerobic digestion process[J]. Bioresource Technology, 2002, 82(2) : 157–164. DOI: 10.1016/S0960-8524(01)00177-8 |
| [2] | Wei Y S, van Houten R T, Borger A R, et al. Comparison performances of membrane bioreactor and conventional activated sludge processes on sludge reduction induced by Oligochaete[J]. Environmental Science & Technology, 2003, 37(14) : 3171–3180. |
| [3] | Low E W, Chase H A, Milner M G, et al. Uncoupling of metabolism to reduce biomass production in the activated sludge process[J]. Water Research, 2000, 34(12) : 3204–3212. DOI: 10.1016/S0043-1354(99)00364-4 |
| [4] | Vaxelaire J, Cézac P. Moisture distribution in activated sludges:a review[J]. Water Research, 2004, 38(9) : 2215–2230. DOI: 10.1016/j.watres.2004.02.021 |
| [5] | Beauchesne I, Ben Cheikh R, Mercier G, et al. Chemical treatment of sludge:in-depth study on toxic metal removal efficiency, dewatering ability and fertilizing property preservation[J]. Water Research, 2007, 41(9) : 2028–2038. DOI: 10.1016/j.watres.2007.01.051 |
| [6] | Niu M Q, Zhang W J, Wang D S, et al. Correlation of physicochemical properties and sludge dewaterability under chemical conditioning using inorganic coagulants[J]. Bioresource Technology, 2013, 144 : 337–343. DOI: 10.1016/j.biortech.2013.06.126 |
| [7] | Zhang W J, Xiao P, Liu Y Y, et al. Understanding the impact of chemical conditioning with inorganic polymer flocculants on soluble extracellular polymeric substances in relation to the sludge dewaterability[J]. Separation And Purification Technology, 2014, 132 : 430–437. DOI: 10.1016/j.seppur.2014.05.034 |
| [8] | Liu H, Fang H H P. Extraction of extracellular polymeric substances (EPS) of sludges[J]. Journal of Biotechnology, 2002, 95(3) : 249–256. DOI: 10.1016/S0168-1656(02)00025-1 |
| [9] | Neyens E, Baeyens J, Dewil R, et al. Advanced sludge treatment affects extracellular polymeric substances to improve activated sludge dewatering[J]. Journal of Hazardous Materials, 2004, 106(2-3) : 83–92. DOI: 10.1016/j.jhazmat.2003.11.014 |
| [10] | Tokumura M, Sekine M, Yoshinari M, et al. Photo-Fenton process for excess sludge disintegration[J]. Process Biochemistry, 2007, 42(4) : 627–633. DOI: 10.1016/j.procbio.2006.11.010 |
| [11] | Liu H, Yang J K, Zhu N R, et al. A comprehensive insight into the combined effects of Fenton's reagent and skeleton builders on sludge deep dewatering performance[J]. Journal of Hazardous Materials, 2013, 258-259 : 144–150. DOI: 10.1016/j.jhazmat.2013.04.036 |
| [12] | Neyens E, Baeyens J. A review of classic Fenton's peroxidation as an advanced oxidation technique[J]. Journal of Hazardous Materials, 2003, 98(1-3) : 33–50. DOI: 10.1016/S0304-3894(02)00282-0 |
| [13] | 朱建平, 彭永臻, 李晓玲, 等. 碱性发酵污泥脱水性能的变化及其原因分析[J]. 化工学报, 2013, 64(11) : 4210–4215. Zhu J P, Peng Y Z, Li X L, et al. Change and mechanism of sludge dewaterability during alkaline fermentation[J]. CIESC Journal, 2013, 64(11) : 4210–4215. |
| [14] | Chen Z, Zhang W J, Wang D S, et al. Enhancement of activated sludge dewatering performance by combined composite enzymatic lysis and chemical re-flocculation with inorganic coagulants:kinetics of enzymatic reaction and re-flocculation morphology[J]. Water Research, 2015, 83 : 367–376. DOI: 10.1016/j.watres.2015.06.026 |
| [15] | Qian Y J, Zhou X F, Zhang Y L, et al. Performance and properties of nanoscale calcium peroxide for toluene removal[J]. Chemosphere, 2013, 91(5) : 717–723. DOI: 10.1016/j.chemosphere.2013.01.049 |
| [16] | Higgins M J, Novak J T. Dewatering and settling of activated sludges:the case for using cation analysis[J]. Water Environment Research, 1997, 69(2) : 225–232. DOI: 10.2175/106143097X125380 |
| [17] | Ma Y, Zhang B T, Zhao L X, et al. Study on the generation mechanism of reactive oxygen species on calcium peroxide by chemiluminescence and UV-visible spectra[J]. Luminescence, 2007, 22(6) : 575–580. DOI: 10.1002/(ISSN)1522-7243 |
| [18] | Ndjou'ou A C, Cassidy D. Surfactant production accompanying the modified Fenton oxidation of hydrocarbons in soil[J]. Chemosphere, 2006, 65(9) : 1610–1615. DOI: 10.1016/j.chemosphere.2006.03.036 |
| [19] | Northup A, Cassidy D. Calcium peroxide (CaO2) for use in modified Fenton chemistry[J]. Journal of Hazardous Materials, 2008, 152(3) : 1164–1170. DOI: 10.1016/j.jhazmat.2007.07.096 |
| [20] | Zhang A, Wang J, Li Y M. Performance of calcium peroxide for removal of endocrine-disrupting compounds in waste activated sludge and promotion of sludge solubilization[J]. Water Research, 2015, 71 : 125–139. DOI: 10.1016/j.watres.2015.01.005 |
| [21] | Wu H Y, Gao J Y, Yang D H, et al. Alkaline fermentation of primary sludge for short-chain fatty acids accumulation and mechanism[J]. Chemical Engineering Journal, 2010, 160(1) : 1–7. DOI: 10.1016/j.cej.2010.02.012 |
| [22] | Chen Y G, Jiang S, Yuan H Y, et al. Hydrolysis and acidification of waste activated sludge at different pHs[J]. Water Research, 2007, 41(3) : 683–689. DOI: 10.1016/j.watres.2006.07.030 |
| [23] | Wang D S, Xing L N, Xie J K, et al. Application of advanced characterization techniques to assess DOM treatability of micro-polluted and un-polluted drinking source waters in China[J]. Chemosphere, 2010, 81(1) : 39–45. DOI: 10.1016/j.chemosphere.2010.07.013 |
| [24] | Chow C W K, Fabris R, van Leeuwen J, et al. Assessing natural organic matter treatability using high performance size exclusion chromatography[J]. Environmental Science & Technology, 2008, 42(17) : 6683–6689. |
| [25] | Lyko S, Al-Halbouni D, Wintgens T, et al. Polymeric compounds in activated sludge supernatant-characterisation and retention mechanisms at a full-scale municipal membrane bioreactor[J]. Water Research, 2007, 41(17) : 3894–3902. DOI: 10.1016/j.watres.2007.06.012 |
| [26] | Kiss G, Tombácz E, Varga B, et al. Estimation of the average molecular weight of humic-like substances isolated from fine atmospheric aerosol[J]. Atmospheric Environment, 2003, 37(27) : 3783–3794. DOI: 10.1016/S1352-2310(03)00468-0 |
| [27] | Henderson R K, Baker A, Murphy K R, et al. Fluorescence as a potential monitoring tool for recycled water systems:a review[J]. Water Research, 2009, 43(4) : 863–881. DOI: 10.1016/j.watres.2008.11.027 |
| [28] | Chen W, Westerhoff P, Leenheer J A, et al. Fluorescence excitation-Emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24) : 5701–5710. |
 2017, Vol. 38
2017, Vol. 38


