2. 中国科学院高能物理研究所, 核技术应用研究中心, 北京 100049;
3. 中国地质科学院地球物理与地球化学勘查研究所, 廊坊 065000
2. Division of Nuclear Technology and Application, Institute of High Energy Physics, Chinese Academy of Sciences, Beijing 100049, China;
3. Institute of Geophysical and Geochemical Exploration, Chinese Academy of Geological Sciences, Langfang 065000, China
多环芳烃(PAHs)是一类由2个或2个以上的苯环连接而成的有机化合物,广泛存在于自然环境中[1]. PAHs主要来源于化石燃料的加工使用和燃烧(如炼焦、燃煤)、生物质和有机物的燃烧[2~4],因具有明显的“三致”作用和内分泌干扰作用而备受关注[5, 6]. 多环芳烃可能包含数百种化合物,其中16种于1976年被美国环保署(EPA)列入优先控制污染物名单. 土壤是多环芳烃主要的汇[7],环境中产生的多环芳烃可直接进入土壤或者通过降水、降尘进入土壤,土壤承担了90%以上多环芳烃的环境负荷[8]. 土壤中的PAHs可通过土壤扬尘的呼吸摄入、皮肤接触、以及食物链传递等方式对人类健康产生更大的威胁[9],由土壤进入人体的多环芳烃量要高于大气和水体[10].
钢铁企业是我国国民经济的重要支柱,在企业生产活动中涉及了炼焦、烧结、炼铁、炼钢、轧钢等生产行为,消耗大量的煤炭等化石燃料,加之大型运输车辆的燃油排放,导致大量多环芳烃的产生和排放. 已有研究表明,储煤厂、焦化厂、发电厂、钢铁厂等周边地区的土壤PAHs污染水平较高[11~13]. 张强等[14]对无锡某钢铁厂土壤中15种多环芳烃分布做了研究,但该钢铁厂没有焦化、烧结、球团等工艺,不能代表工艺完整的大型钢铁企业土壤中PAHs的污染特征.
本文以我国北方某大型钢铁企业表层土壤为研究对象,探讨了16种优控PAHs的含量特征、污染水平、来源与健康风险,对预防钢铁企业土壤污染,指导钢铁企业搬迁后土壤的修复及安全处置具有重要意义.
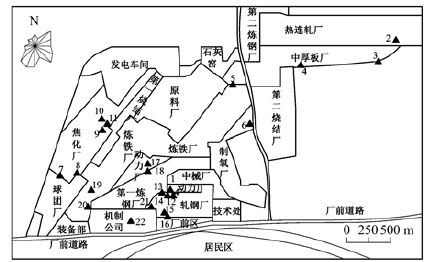
1 材料与方法 1.1 研究区概况与点位布设该大型钢铁企业建于20世纪50年代,年生产钢1 000余万t,拥有从原料、焦化、烧结、球团、炼铁、炼钢到轧钢完整的生产工艺系统. 点位布设以烧结机头、球团竖炉、焦炉装煤出焦、高炉出铁场等废气排放点源为中心采取放射状布点,每个方向至少布设5个监测点,主导风向下风向增加2个点监测点,共布设22个监测点位,点位布设如图 1所示.
|
图 1 钢铁厂表层土壤采样点位布设示意 Fig. 1 Map of the surface soil sampling sites in the steel enterprise |
在每个采样点上,用采样铲向下切取1片长10 cm、宽5 cm、深20 cm的土壤样品至1 000 mL棕色玻璃广口瓶,并装实装满,于实验室-18℃冷冻保存. 分析前将样品放入冻干机中冻干,去除砾石和植物根系,研磨过1 mm筛,备用.
1.3 分析测试采用气相色谱-质谱联用仪(GCMS-QP2010plus)分析EPA优控的16种PAHs,2环:萘(Nap); 3环:苊烯(Acy)、苊(Ace)、芴(Fl)、菲(Phe)、蒽(Ant); 4环:荧蒽(Flu)、芘(Pyr)、苯并(a)蒽(BaA)、(Chr); 5环:苯并(b)荧蒽(BbF)、苯并(k)荧蒽(BkF)、苯并(a)芘(BaP)、二苯并(a, h)蒽(DBA); 6环:苯并(g, h, i)苝(BgP)、茚并(1, 2, 3-cd)芘(InP).
气相色谱条件:色谱柱为亚芳基聚合物色谱柱(DB-5MS:60 m×0.25 mm×0.32 μm),升温程序为:初始温度45℃,保持1 min,以40℃ ·min-1升温至130℃,以12℃ ·min-1升温至180℃,以7℃ ·min-1升温至240℃,以12℃ ·min-1升温至320℃,保持8 min; 载气为He; 流速控制模式:线流速控制模式,柱流速1.66mL ·min-1、线流速2.33 mL ·min-1; 进样方式:高压注射模式,进样口压力100 kPa、进样量为1.0 μL、分流比7 ∶1.
质谱条件为,离子源:EI源; 扫描方式:SIM模式; 溶剂延迟时间:5 min; 调谐方式:DFTPP.
萃取条件:丙酮与正己烷混合溶剂萃取(体积比50 ∶50) ; 静态萃取时间5 min; 萃取温度120℃; 萃取3次.
GPC净化条件:凝胶柱500 mm×25 mm,柱填料为200~400目Bio Bead S-X3; 流动相为二氯甲烷,柱流速5mL ·min-1,样品定量环5 mL,收集800~1 800 s流出液.
浓缩装置(旋转蒸发装置); 氮吹仪(可控制流速和可控制加热).
1.4 质量控制实验室内部质量控制采用仪器空白检查(进样瓶装入空白溶剂,按照样品分析步骤运行仪器空白,空白色谱图中应无目标物影响定性定量分析); 仪器连续校准(仪器每运行12 h采用校准曲线中间点进行检查,校准化合物响应因子相对偏差大于20%应需要重新校准)、溶剂空白(所用有机试剂按分析过程最大浓缩倍数浓缩后进行空白检查)、全程序空白(每批样品以石英砂替代土壤样品,按照与试样相同预处理和测定步骤进行全程序空白试验)、替代物加标回收试验(替代物在样品制备前加入土壤中,分析时测定回收率,替代物回收率控制在60%~120%).
1.5 数据处理采用Excel 2003、Origin 8.6对数据统计分析.
2 结果与讨论 2.1 土壤中PAHs含量与组成特征将土壤中16种优控PAHs单体的统计数据列于表 1. 16种多环芳烃单体在钢铁厂各功能区表层土壤中均有检出,检出率为22.7%~95.5%. 不同单体含量的变异系数均大于110%,显示出较强的空间分布差异性. 各单体均值高于对应的中位值,呈现正偏态分布,以4环Flu、Pyr的平均含量最高,检出率低的Acy、DBA其含量亦较低. 16种PAHs(∑16PAHs)含量范围为22.0~20 062.0 μg ·kg-1,均值为2 564.7 μg ·kg-1. 7种致癌性PAHs(∑7CarPAHs)含量范围为n.d.~7 010.3 μg ·kg-1,均值为1 051.8 μg ·kg-1,占∑16PAHs的41.0%.
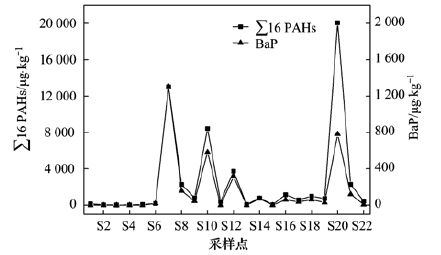
由表 1可知,16种PAHs单体中致癌性最强的BaP浓度范围为n.d.~1 305μg ·kg-1,均值为164 μg ·kg-1. 由图 2可以看出,表层土壤中PAHs总量与BaP具有相似的变化趋势(R=0.89,P<0.01) . PAHs总量以在炼铁厂S20中最大,BaP则以在焦化厂、球团厂附近S7中最大,二者的相对高值均位于焦化厂、球团厂、炼铁厂等区域,可能与炼钢、炼铁过程中煤炭、焦炭的燃烧有关,而原料厂、烧结厂等采样点PAHs总量及BaP含量相对较低. 焦化厂以煤为主要原料,其车间内化石燃料的不完全燃烧及焦油、煤气等产品的加工过程都可能导致PAHs类物质的排放[13, 15]. 有研究表明,焦化厂是多环芳烃的重要污染源,所排放出的污染物能够影响2~3 km或更大范围的地区[16].
|
|
表 1 钢铁厂表层土壤中16种PAHs含量统计 /μg ·kg-1 Table 1 Statistics of the contents of 16 PAHs in surface soils of the steel enterprise/μg ·kg-1 |
|
图 2 不同采样点表层土壤中PAHs和BaP含量 Fig. 2 PAHs and BaP concentrations in the surface soil samples at different sampling points |
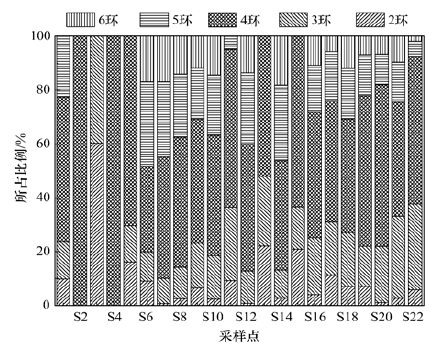
不同采样点PAHs组分差异如图 3所示,钢铁厂表层土壤中S2、S4 PAHs组成仅为4环,S3 PAHs组成仅为2环和3环,S5、S13、S15高环(5环、6环)组分缺失. 研究区表层土壤PAHs的组成主要以4环组分为主,占PAHs总量的31.9%~100%. 在PAHs总量较高的土壤采样点中,5环组分仅次于4环(炼铁厂S20 4环、3环占较大比例),占比范围为4.88%~31.25%. 由此可知,钢铁厂表层土壤PAHs污染主要源于毒性较高的中、高环组分,与已有研究结果一致[12, 17, 18].
|
图 3 不同采样点表层土壤中PAHs组成比例 Fig. 3 Proportion of PAHs components in the surface soil samples at different sampling points |
与国内其他钢铁企业厂区或周边土壤中PAHs含量相比(表 2),该钢铁厂表层土壤PAHs含量基本处于中等水平,低于北京市某焦化厂[13]、东北某钢铁厂[17]及苏南地区某钢铁厂周边农田表层土壤[18]中PAHs含量,高于无锡某钢铁厂[14]、杭州某钢铁厂[19]及邯郸某钢铁厂[12]周边农田表层土壤中 PAHs含量,与本市典型工业区[20]土壤PAHs含量 (包括BaP)基本持平.
土壤中典型的内源性PAHs为1~10 μg ·kg-1,主要来自植物的分解和自然火灾[21]. Trapido[22]对未受人类活动干扰的土壤PAHs本底值的界定为小于100 μg ·kg-1. 该钢铁厂表层土壤中PAHs总量明显高于上述限值,表明土壤已经受到了一定程度PAHs的人为污染. 由于我国尚无统一的PAHs土壤环境质量标准,参照Maliszewska-Kordybach[23]建议的对土壤中16种优控PAHs污染程度的分级方法,在钢铁厂各功能区生产活动影响下,清洁土壤采样点(<200 μg ·kg-1)仅占36.4%,而中度(600~1 000 μg ·kg-1)、重度(>1 000 μg ·kg-1)污染采样点分别为18.2%、31.8%,主要位于焦化厂、球团厂、炼铁厂、轧钢厂这4个典型区域,应当引起关注.
对表层土壤中16种PAHs单体采用荷兰土壤质量标准[24]中10种PAHs的目标值、北京市工业场地土壤14种PAHs筛选值进行评价(表 1). 根据荷兰土壤质量目标值,S3、S4中10种PAHs含量低于目标值,其他采样点都存在部分PAHs单体超标,超标率为27.3%(Ant)~90.9%(Flu),且10种PAHs均值都超过对应目标值,超标倍数为1.69(Ant)~14.45(BaA). 由于标准制定的差异性,北京工业场地土壤中14种PAHs筛选值均高于相应的荷兰土壤质量目标值,除S7、S10、S12、S20采样点BaA、BaP超标外,其余PAHs单体均低于筛选值,BaA、BaP超标率分别为18.2%、13.6%.
|
|
表 2 相关研究区域土壤中∑PAHs含量水平 Table 2 Concentrations of ∑PAHs in soil of other researches |
2.3 土壤中PAHs的迁移沉降
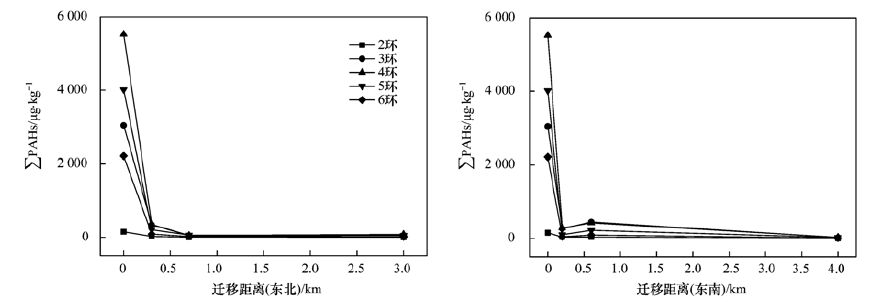
结合厂区布置和常年主导方向,以BaP含量最高的S7为起点,对PAHs不同组分在主导风向的下风向(即东北和东南方向)含量变化进行研究(图 4). 表层土壤PAHs含量受常年主导风向的影响十分明显,大气沉降可能是导致研究区PAHs污染的重要途径之一. 不同环数PAHs含量随距离增加均表现出较好的衰减规律,但衰减幅度不同,低环组分的空间变异程度小于高环组分. 原因可能在于各PAH单体的含量及理化性质不同,低环芳烃挥发性强,饱和蒸气压高,通常趋向以气态形式存在于空气中并易于长距离迁移,反映大气输送的影响; 而高环芳烃不易挥发,多趋向于结合在固相颗粒物上,并伴随干、湿沉降返回地表,反映本地污染源的影响[25~27]. 在东北方向0.3 km处,除2环PAHs组分外,均有近90%的衰减,在0.7 km处不同环数PAHs含量相似,并与3 km处PAHs含量基本持平. 东南方向在长距离的迁移过程中,除2环PAHs组分外,其余组分PAHs含量变化呈阶梯状,在距离0.6 km处比0.2 km处略有升高,可能的原因包括:一是采样点周围PAHs排放源较多,颗粒物性质复杂,二是新污染源(轧钢厂、交通源)的叠加效应.
|
图 4 不同方向多环芳烃迁移沉降趋势 Fig. 4 PAHs migration and deposition trends in different directions |
不同分子量PAHs的相对丰度可以用来解析其来源于不完全燃烧过程还是石油泄漏. 通常低分子量(2环和3环)PAHs主要来源于石油类泄漏,而高分子量(4环及其以上)PAHs来源于煤等化石燃料的不完全燃烧[28, 29]. 由于研究区表层土壤PAHs组成以中高环组分为主,说明PAHs主要来源于煤等化石燃料的燃烧,但在炼铁厂、轧钢厂的部分重度污染点位,3环组分亦占有较大比例,厂区内繁忙的运输工作可能会引起部分石油类产品的泄漏,从而污染该采样点的土壤.
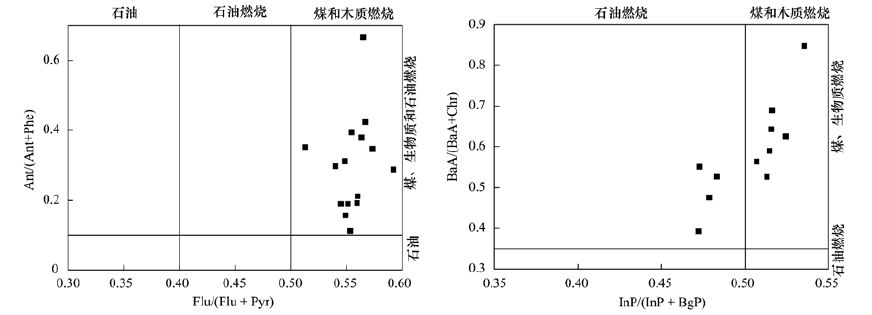
母体PAHs同分异构体具有相似的理化性质,进入环境后具有相同的迁移分配与稀释行为,因此一些特定的PAHs异构体,如Ant/(Ant+Phe)、Flu/(Flu+Pyr)、BaA/(BaA+Chr)和InP/(InP+BgP),被用来解析环境中PAHs的来源[30]. 如图 5所示,Ant/(Ant+Phe)在0.11~0.67,Flu/(Flu+Pyr)在0.51~0.57,BaA/(BaA+Chr)在0.39~0.85,说明钢铁厂表层土壤主要来源于煤和生物质燃烧,在S3、S10、S12、S13采样点InP/(InP+BgP)在0.2~0.5之间,其中S10、S12为重度污染采样点,说明焦化厂、轧钢厂土壤中PAHs可能来自石油、煤和生物质的混合燃烧. 表层土壤中Flu、Pyr的检出含量最高,而Phe、Flu、Pyr和Ane的排放是煤燃烧源的重要特征[31]. 总体而言,钢铁厂不同功能区表层土壤中的PAHs主要来源于以煤为主的化石燃料的燃烧,石油类燃烧和泄漏的贡献较少.
|
图 5 土壤中PAHs多特征比值判源 Fig. 5 Source identification with compositional analysis of PAHs in soil samples |
有研究认为用于特征比值的同分异构体的环境行为不完全一致,从排放源进入多介质环境后,受其自身稳定性(挥发、迁移、降解等)及环境介质性质(土壤性质如有机质等)的影响,其比例并非一成不变,且对于实际环境中各PAHs组分降解的速率,观点也不尽相同[12, 32]. 因此,在进行PAHs的来源识别时,采用多元统计方法(主成分分析法、正定矩阵因子分析法等),并深入研究PAHs组分及单体的环境行为是十分必要的.
2.5 PAHs健康风险评价参照《污染场地风险评估技术导则》(HJ 25.3-2014) ,以钢铁厂表层土壤中16种PAHs的含量进行健康风险评价,考虑经口摄入、呼吸吸入、皮肤接触这3种暴露途径. 该土地现为工业用地,将来或规划为居住用地. 工业用地条件下以成人为敏感受体,居住用地条件下综合考虑儿童和成人的健康风险. 表 3结果显示,在两种用地方式下,9种PAHs的危害商均在可接受风险水平以内(<1) ,不会对目标人群产生非致癌危害. 在居住用地条件下BaP、BaA、DBA、BbF、InP最大值的致癌风险超过了可接受风险水平(1×10-6),且BaP的平均致癌风险水平亦超过了此限值. 在工业用地条件下BaP、BaA、DBA最大值的致癌风险超过此限值,表明钢铁厂表层土壤中PAHs已对人群健康产生危害. BaP在16种PAHs中致癌性最强,不同用地方式下BaP的致癌风险水平均高于其他6种致癌性PAHs. 超风险PAHs单体主要位于焦化厂、球团厂北部、炼铁厂南部及轧钢厂部分地区,并以BaP的修复范围最大. 因此,厂区有必要进行能源结构改造与污染监控,并对上述功能区实施土壤修复工程.
|
|
表 3 不同用地方式下土壤中多环芳烃的健康风险 Table 3 Health risk of polycyclic aromatic hydrocarbons in the soils with different land utilization manners |
3 结论
(1) 钢铁厂表层土壤PAHs的组成以毒性较高的中高环(4、5环)为主,∑16PAHs含量范围为22.0~20 062.0 μg ·kg-1,与BaP含量具有相似的变化趋势,单体以Flu、Pyr的含量最高. ∑7CarPAHs含量范围为n.d.~7 010.3 μg ·kg-1,均值为1 051.8 μg ·kg-1. 与同类相关研究比较,土壤PAHs污染处于中等水平,中、重度污染采样点占50.0%,主要位于焦化厂、球团厂等典型区域. 20个采样点PAHs单体均超过荷兰土壤质量标准中10种PAHs的目标值,而与北京工业场地土壤筛选值相比,则仅部分采样点BaA、BaP超标.
(2) 以BaP含量最高的S7为起点,不同环数PAHs含量随距离增加呈衰减规律,但低环组分的空间变异程度小于高环组分. 源解析结果表明:表层土壤中PAHs主要来源于以煤为主的化石燃料的燃烧,石油类燃烧和泄漏的贡献较少.
(3) 健康风险评价结果表明:BaP、BaA、DBA、BbF、InP在居住用地条件下的致癌风险超过了1×10-6,BaP、BaA、DBA在工业用地条件下的致癌风险超过了1×10-6,BaP的致癌风险最大,该钢铁厂表层土壤中PAHs已对人群健康产生危害,需实施土壤修复工程.
| [1] | Zhuang P, McBride M B, Xia H P, et al. Health risk from heavy metals via consumption of food crops in the vicinity of Dabaoshan mine,South China[J]. Science of the Total Environment , 2009, 407 (5) : 1551–1561. DOI:10.1016/j.scitotenv.2008.10.061 |
| [2] | Cao H B, Chen J J, Zhang J, et al. Heavy metals in rice and garden vegetables and their potential health risks to inhabitants in the vicinity of an industrial zone in Jiangsu,China[J]. Journal of Environmental Sciences , 2010, 22 (11) : 1792–1799. DOI:10.1016/S1001-0742(09)60321-1 |
| [3] | Huang S S, Liao Q L, Hua M, et al. Survey of heavy metal pollution and assessment of agricultural soil in Yangzhong district,Jiangsu Province,China[J]. Chemosphere , 2007, 67 (11) : 2148–2155. DOI:10.1016/j.chemosphere.2006.12.043 |
| [4] | Qiao X, Schmidt A H, Tang Y, et al. Demonstrating urban pollution using toxic metals of road dust and roadside soil in Chengdu,southwestern China[J]. Stochastic Environmental Research and Risk Assessment , 2014, 28 (4) : 911–919. DOI:10.1007/s00477-013-0790-2 |
| [5] | 刘硕, 吴泉源, 曹学江, 等. 龙口煤矿区土壤重金属污染评价与空间分布特征[J]. 环境科学 , 2016, 37 (1) : 270–279. |
| [6] | Liu H Y, Probst A, Liao B H, et al. Metal contamination of soils and crops affected by the Chenzhou lead/zinc mine spill (Hunan,China)[J]. Science of the Total Environment , 2005, 339 (1-3) : 153–166. DOI:10.1016/j.scitotenv.2004.07.030 |
| [7] | 姬艳芳, 李永华, 杨林生, 等. 湘西凤凰铅锌矿区典型土壤剖面中重金属分布特征及其环境意义[J]. 环境科学学报 , 2009, 29 (5) : 1094–1102. |
| [8] | 张敏, 王美娥, 陈卫平, 等. 湖南攸县典型煤矿和工厂区水稻田土壤镉污染特征及污染途径分析[J]. 环境科学 , 2015, 36 (4) : 1425–1430. |
| [9] | Gong C, Ma L, Cheng H, et al. Characterization of the particle size fraction associated heavy metals in tropical arable soils from Hainan Island,China[J]. Journal of Geochemical Exploration , 2014, 139 : 109–114. DOI:10.1016/j.gexplo.2013.01.002 |
| [10] | Yao Q Z, Wang X J, Jian H M, et al. Characterization of the Particle Size Fraction associated with heavy metals in suspended sediments of the Yellow River[J]. International Journal of Environmental Research and Public Health , 2015, 12 (6) : 6725–6744. DOI:10.3390/ijerph120606725 |
| [11] | 刘冠男, 刘新会. 土壤胶体对重金属运移行为的影响[J]. 环境化学 , 2013, 32 (7) : 1308–1317. |
| [12] | Tang Z Y, Wu L H, Luo Y M, et al. Size fractionation and characterization of nanocolloidal particles in soils[J]. Environmental Geochemistry and Health , 2009, 31 (1) : 1–10. DOI:10.1007/s10653-008-9131-7 |
| [13] | Zhang H B, Luo Y M, Makino T, et al. The heavy metal partition in size-fractions of the fine particles in agricultural soils contaminated by waste water and smelter dust[J]. Journal of Hazardous Materials , 2013, 248-249 : 303–312. DOI:10.1016/j.jhazmat.2013.01.019 |
| [14] | 龚仓, 马玲玲, 成杭新, 等. 典型农耕区黑土和沼泽土团聚体颗粒中重金属的分布特征解析[J]. 生态环境学报 , 2012, 21 (9) : 1635–1639. |
| [15] | Artz R R E, Chapman S J, Robertson A H J, et al. FTIR spectroscopy can be used as a screening tool for organic matter quality in regenerating cutover peatlands[J]. Soil Biology and Biochemistry , 2008, 40 (2) : 515–527. DOI:10.1016/j.soilbio.2007.09.019 |
| [16] | Solomon D, Lehmann J, Kinyangi J, et al. Carbon K-Edge NEXAFS and FTIR-ATR spectroscopic investigation of organic carbon speciation in soils[J]. Soil Science Society of America , 2005, 69 : 107–119. DOI:10.2136/sssaj2005.0107dup |
| [17] | 张耀方, 赵世伟, 李晓晓, 等. 利用方式对灌淤土团聚体稳定性及有机碳官能团特征的影响[J]. 水土保持学报 , 2015, 29 (1) : 169–174. |
| [18] | Chaudhuri S, McDonald L M, Skousen J, et al. Soil organic carbon molecular properties:effects of time since reclamation in a minesoil chronosequence[J]. Land Degradation&Development , 2015, 26 (3) : 237–248. |
| [19] | 路雨楠.土壤团聚体中元素种态分布的研究[D].北京:北京化工大学,2015.19-25. |
| [20] | 熊毅. 土壤胶体-第二册:土壤胶体研究法[M]. 北京: 科学出版社, 1985 . |
| [21] | 国家环境保护局.GB 15618-1995,土壤环境质量标准[S].北京:中国标准出版社,1995. |
| [22] | 潘佑民, 杨国治. 湖南土壤背景值及研究[M]. 北京: 中国环境科学出版社, 1988 . |
| [23] | 魏复盛, 陈静生, 吴燕玉, 等. 中国土壤环境背景值研究[J]. 环境科学 , 1991, 12 (4) : 12–19. |
| [24] | 龙永珍, 戴塔根, 邹海洋, 等. 长沙、株洲、湘潭地区土壤重金属污染现状及评价[J]. 地球与环境 , 2008, 36 (3) : 231–236. |
| [25] | 龚仓, 徐殿斗, 成杭新, 等. 典型热带林地土壤团聚体颗粒中重金属的分布特征及其环境意义[J]. 环境科学 , 2013, 34 (3) : 1094–1100. |
| [26] | Acosta J A, Cano A F, Arocena J M, et al. Distribution of metals in soil particle size fractions and its implication to risk assessment of playgrounds in Murcia City (Spain)[J]. Geoderma , 2009, 149 (1-2) : 101–109. DOI:10.1016/j.geoderma.2008.11.034 |
| [27] | Chen G, Flury M, Harsh J B, et al. Colloid-facilitated transport of cesium in variably saturated Hanford sediments[J]. Environmental Science&Technology , 2005, 39 (10) : 3435–3442. |
| [28] | Citeau L, Lamy I, van Oort F, et al. Colloidal facilitated transfer of metals in soils under different land use[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects , 2003, 217 (1-3) : 11–19. |
| [29] | Yin X Q, Gao B, Ma L Q, et al. Colloid-facilitated Pb transport in two shooting-range soils in Florida[J]. Journal of Hazardous Materials , 2010, 177 (1-3) : 620–625. DOI:10.1016/j.jhazmat.2009.12.077 |
| [30] | 李士杏, 骆永明, 章海波, 等. 红壤不同粒级组分中砷的形态——基于连续分级提取和XANES研究[J]. 环境科学学报 , 2011, 31 (12) : 2733–2739. |
| [31] | Khanlari Z V, Jalali M. Concentrations and chemical speciationof five heavy metals (Zn,Cd,Ni,Cu,and Pb) in selectedagricultural calcareous soils of Hamadan Province,western Iran[J]. Archives of Agronomy and Soil Science , 2008, 54 (1) : 19–32. DOI:10.1080/03650340701697317 |
| [32] | Jalali M, Hemati N. Chemical fractionation of seven heavy metals (Cd,Cu,Fe,Mn,Ni,Pb,and Zn) in selected paddy soils of Iran[J]. Paddy and Water Environment , 2013, 11 (1-4) : 299–309. DOI:10.1007/s10333-012-0320-8 |
| [33] | 任雅阁, 马玲玲, 成杭新, 等. 典型农耕区褐土水稳性团聚体有机碳的分布及组成[J]. 水土保持通报 , 2014, 34 (2) : 15–19. |
| [34] | Dumat C, Quenea K, Bermond A, et al. Study of the trace metal ion influence on the turnover of soil organic matter in cultivated contaminated soils[J]. Environmental Pollution , 2006, 142 (3) : 521–529. DOI:10.1016/j.envpol.2005.10.027 |
| [35] | Quenea K, Lamy I, Winterton P, et al. Interactions between metals and soil organic matter in various particle size fractions of soil contaminated with waste water[J]. Geoderma , 2009, 149 (3-4) : 217–223. DOI:10.1016/j.geoderma.2008.11.037 |
 2016, Vol. 37
2016, Vol. 37


