2. 中国环境科学研究院水污染控制技术研究中心, 北京 100012;
3. 中国环境科学研究院环境基准与风险评估国家重点实验室, 北京 100012;
4. 湖南省排污权储备交易中心, 长沙 410014
2. Research Center of Water Pollution Control Technology, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;
3. State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;
4. Hunan Province Reserve Trading Center for Pollution Discharge Rights, Changsha 410014, China
畜禽养殖废水主要由尿液、 残余的粪便、 饲料残渣和冲洗水等组成,具有COD、 SS、 NH4+-N含量高、 可生化性好、 水质水量变化大、 含有致病菌并有恶臭等特点[1]. 由于畜禽粪尿的淋溶性很强,粪尿中的N、 P及水溶性有机物等淋溶量很大,这些污染物如不进行适当处理就排放于环境或直接农用,将会造成当地生态环境和农田的严重污染. 限于经济技术条件,分散养猪废水仅仅只是进入沼气池,厌氧发酵之后直接排出,仍是面源污染的重要来源.
生物-生态组合工艺为分散养殖废水的治理提供了一条经济可行的路线[2~4]. 人工湿地是一种常用的生态工艺,但是其存在脱氮能力较弱的缺点. 微生物的硝化、 反硝化作用是人工湿地最主要的脱氮途径[5]. 但是,常规的人工湿地主要靠植物根系复氧来强化氧扩散,复氧量不能满足大量有机物降解和NH4+-N硝化的需求[6]. 强化湿地复氧性能、 改进湿地填料等措施可以显著强化人工湿地的脱氮性能. 潮汐流[7]、 间歇流[8]等运行方式可以强化人工湿地复氧性能. 生物沸石可实现NH4+-N吸附和原位再生,可持续性去除NH4+-N,而且石灰石与沸石混合填充可促进沸石的生物再生[9].
分散养猪冲洗水经厌氧折流板反应器(ABR)处理后仍含有高浓度有机物、 N和P[10]. 为强化人工湿地对其的处理性能,在前期研究的基础上[3, 4, 9],根据生物沸石的硝化速率,基于生物沸石快速吸附-再生动态平衡技术,构建了三级生物沸石人工湿地,考察其启动阶段性能、 出水时污染物随时间变化、 启动后性能以及生物沸石层ORP分布,以期为其实际推广应用提供技术支持.
1 材料与方法 1.1 试验材料试验选用的天然斜发沸石产自浙江省缙云县,其元素组成为:SiO2,69.58%; Al2O3,12.2%; Na2O,2.59%; CaO,2.59%; K2O,1.13%; Fe2O3,0.87%; MgO,0.13%; 其他,10.91%. 沸石粒径为3~5 mm. 试验所用砾石和砖渣经筛选后,用自来水清洗干净并晒干后备用. 接种污泥取自湖南省长沙县黄花镇污水处理厂. 试验的进水为经ABR处理后的分散养猪冲洗水(经过源分离工艺将猪粪和猪尿与冲洗水分开). 分散养猪冲洗水COD、 NH4+-N、 TN和TP的质量浓度分别约为1 432~2 068、 152.8~214.5、 206.3~263.6和14.6~23.4 mg ·L-1 [11]. 试验所用的氯化铵、 磷酸氢二钾、 过硫酸钾、 碘化钾、 氢氧化钠等试剂均为分析纯.
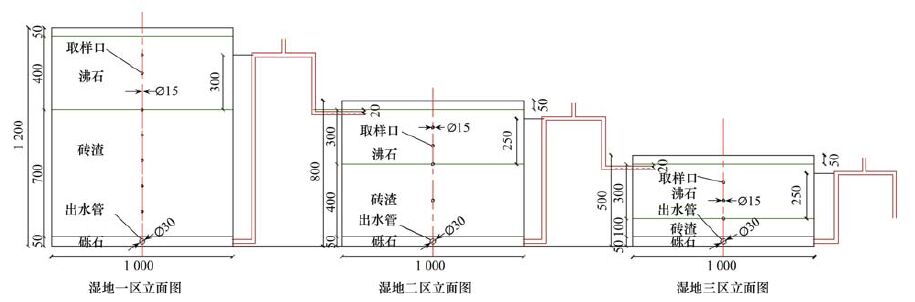
1.2 试验装置试验装置为3个由PVC板材制成的湿地反应器,如图 1所示. 湿地一区长1.5 m、 宽1 m、 高1.2 m(主要实现有机物、 N和P的去除),湿地二区长1.5 m、 宽1 m、 高0.8 m(主要实现P的去除和NH4+-N硝化),湿地三区长1.5 m、 宽1 m、 高0.5 m(主要实现NH4+-N硝化),每个湿地分区设有进水口、 取样口及出水口. 每个湿地分区从底部往上依次填充粒径为3~5 cm的砾石、 粒径为5~40 mm的砖渣、 沸石(3~5 mm)与石灰石(5~10 mm)混合物. 根据前期研究结果,沸石与石灰石的质量比为5 ∶1[9]. 每个湿地分区各填料的填充高度如表 1所示.
|
单位:mm 图 1 三级生物沸石人工湿地结构示意 Fig. 1 Structure diagram of three-stage enhanced nitrification constructed wetland reactor |
|
|
表 1 湿地填料填充高度 /mm Table 1 Filling height of wetland packing/mm |
在湿地底部沿长度方向设有1根直径为5 cm的集水管,集水管一端密封,另一端与出水口相连,集水管周边均匀开有集水槽,槽长为5 cm,槽宽为5 mm. 湿地一区在装填料前,插入2根(均距湿地一区壁0.5 m)直径5 cm的PVC管(强化复氧管,长为120 cm),PVC管的下端深入至湿地底部,与集水管相通. PVC管位于湿地一区高度的75~115 cm部分交错开有直径为3 mm向上倾斜45度的圆形小孔. 布水系统位于沸石表层下3 cm处,3个湿地分区均种植空心菜(Ipomoea aquatic Forsk),每个分区种植4排,每排6窝,每窝1~2颗空心菜幼苗.
1.3 试验方法三级湿地串联运行. 为了提高湿地挂膜的速度,取湖南省长沙县黄花镇污水处理厂的生化剩余污泥进行接种. 在进水中加入污泥,使污泥质量浓度为2 000 mg ·L-1. 用潜水泵将加有污泥的进水从湿地顶部抽入至沸石被完全淹没,每天进水1次,此时湿地一区、 二区和三区的进水量分别为750、 500和300 L. 进水在湿地停留4 h后由底部出水口排出,出水收集后继续作为进水进行接种. 接种3 d后,不再加入污泥,并在随后的3 d均将湿地由底部排空,以避免接种污泥残留在湿地. 随后,湿地以潮汐流方式运行(作为运行的第1d),进水期为1 h(09:00开始),每天进水1次,进水量为210 L,其余时间为落干期,湿地静置. 3级湿地的水力负荷为0.047 m3 ·(m2 ·d)-1,单级湿地的水力负荷为0.141 m3 ·(m2 ·d)-1. 出水由湿地底部的出水口排出,分别通过虹吸管控制湿地的饱和液位,3个区的饱和液位高度分别为750、 450和150 mm. 前期的研究表明,沸石前期对NH4+-N的吸附能力较强,为尽快实现三级人工湿地的顺利启动,在湿地一区和二区的出水中加入葡萄糖和氯化铵,使其COD和NH4+-N质量浓度分别为150 mg ·L-1和110 mg ·L-1. 启动后不再调整湿地二区和三区的进水浓度. 以发生明显硝化作用作为湿地启动的标志.
考察污染物随时间变化时,湿地运行参数与启动后的一致. 0 min为出水前取样,出水后每隔15 min取一次样(虹吸出水时间60 min左右). 启动后,在湿地3个分区的不同位置和沸石层的不同厚度(一区为10、 20、 30和40 cm,二、 三区为10、 20和30 cm)分别插有ORP电极. 稳定1周后,在进水前测定ORP,连续测定3 d,取其平均值,考察湿地氧化还原电位空间分布情况.
1.4 分析方法COD使用快速消解法测定(华通,CTL-12型). NH4+-N采用纳氏试剂分光光度法测定,NO3--N采用紫外分光光度法测定,NO2--N采用N-(1-萘基)-乙二胺分光光度法测定(UNICUV-2100分光光度计),TN采用过硫酸钾氧化-紫外分光光度法,TP采用钼锑抗分光光度法测定[12]. pH采用pH仪进行测定(METTLER TOLEDO FE20 pH计). ORP采用ORP仪测定(FJA-6 ORP仪).
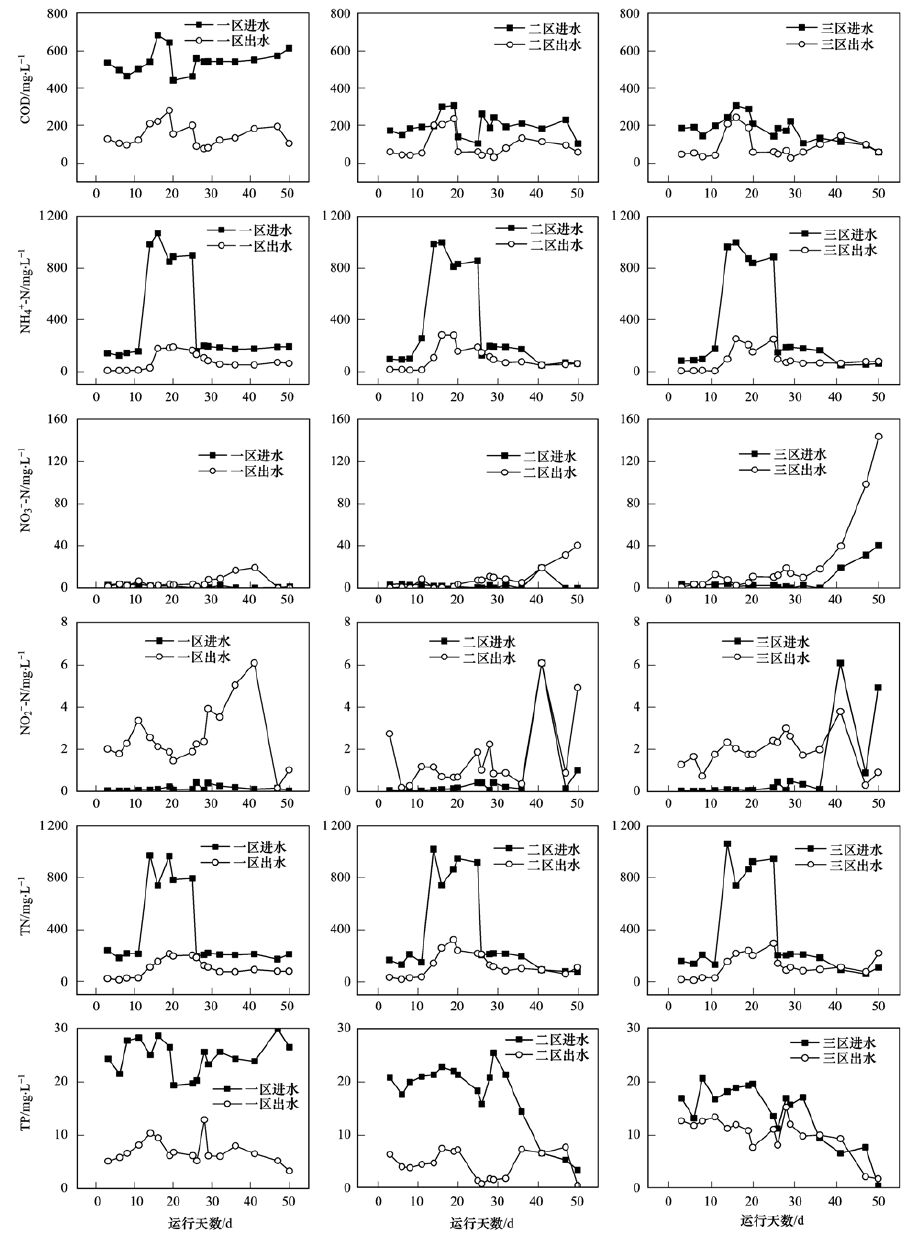
2 结果与讨论 2.1 人工湿地启动阶段运行性能三级生物沸石人工湿地串联运行,污水先经ABR厌氧降解后进入湿地系统,湿地3个分区均采用虹吸管控制饱和液位,使沸石层在进水期处于浸没状态,并在达到虹吸液位后通过虹吸使沸石层落干. 进水期,水中的有机物随水流的下渗被湿地中的微生物快速吸附截留,NH4+-N被上层填充的沸石快速吸附,落干期沸石表面生物膜中的微生物利用氧气降解有机物并将沸石吸附的NH4+-N氧化成NO2--N和NO3--N,随后扩散至水中,实现生物沸石的原位再生,最终达到吸附-再生的动态平衡. 沸石层产生的NO3--N和NO2--N随水流进入湿地下部砖渣层,砖渣层表面的厌氧微生物利用水中残存的有机物还原NO3--N和NO2--N,最终实现了TN的去除. 三级人工湿地启动阶段的运行性能如图 2所示. 由于三级人工湿地沸石填充量大(一区、 二区和三区填充沸石的量分别为586.96、 382.02和377.80 kg),而湿地进水量仅为210 L ·d-1,且进水中NH4+-N质量浓度仅为150 mg ·L-1,使得湿地要达到吸附-再生的动态平衡的时间较久. 为此,进水第14 d时,在各自进水中加入NH4Cl,使NH4+-N质量浓度升高至1 000 mg ·L-1左右,12 d后不再加入NH4Cl.
|
图 2 三级生物沸石人工湿地启动阶段运行性能 Fig. 2 Operating performance of the three-stage bio-zeolite constructed wetland in the startup phase |
由图 2可以看出,湿地一区去除COD明显,由进水的543.16 mg ·L-1降至148.01 mg ·L-1. 湿地一区、 二区和三区的COD平均去除率分别为72.7%、 52.8%和48.4%. 启动初期,沸石中的吸附位点多,湿地一区、 二区和三区的出水NH4+-N质量浓度都很低,为10 mg ·L-1左右; 当NH4+-N质量浓度升高至1 000 mg ·L-1左右时,出水NH4+-N质量浓度有明显升高; 不再加入NH4Cl后,3个区的出水NH4+-N保持稳定,分别为60.66、 65.47和74.01 mg ·L-1. 启动初期,生物膜尚未成熟,湿地3个分区出水的NO3--N浓度都很低,随着湿地的运行,沸石表面的生物膜逐渐成熟,沸石层硝化作用逐渐增强,出水NO3--N浓度缓慢升高,运行36 d后,二、 三区出水NO3--N浓度急剧升高,湿地一区NO3--N质量浓度也明显升高并在41 d时达到最高(19.35 mg ·L-1),表明湿地的启动期为40 d左右. 沸石的生物再生是沸石所吸附的NH4+-N通过界面发生生物硝化而解吸的过程,是沸石吸附的NH4+-N解吸及生物硝化共同作用的结果[9]. 随着启动过程,沸石表面的生物膜逐渐成熟,硝化作用增强,使得产生的NO3--N浓度逐渐与吸附的NH4+-N浓度基本一致,即生物沸石在进水期吸附的NH4+-N可在落干期被硝化,空出等量的吸附位点在下一个进水周期继续吸附NH4+-N,此时生物沸石基本达到快速吸附-再生动态平衡. 运行36 d后,进水NH4+-N基本稳定,此时湿地一区出水的NH4+-N也基本稳定,表明湿地一区中的生物沸石可能达到了快速吸附-再生动态平衡.
湿地一区NO3--N浓度在41 d后有明显降低,这可能是由于湿地一区砖渣层较厚,有良好的淹水厌氧环境,且水中的有机物浓度高,使得NO3--N通过反硝化途径被去除. 苗莹[3]以生物沸石人工湿地处理养殖废水时,也发现湿地具有明显的功能分区,湿地上层(沸石层)和下层(砖渣层)分别发生了明显的硝化和反硝化反应,并且以高通量测序技术分别检测出了硝化菌和反硝化菌. 湿地3个区出水NO2--N的质量浓度较低,其均值分别为2.57、 1.58和1.91 mg ·L-1,无明显的NO2--N的累积. 启动初期进出水TN的变化趋势与NH4+-N的变化趋势基本相同,表明对TN的去除,主要依赖于沸石对NH4+-N离子的吸附,微生物的硝化反硝化作用相对较小. 启动末期,湿地二区和三区的出水TN有逐渐上升的趋势,这主要是由于此时的硝化作用较强,产生的NO3--N浓度超过了吸附去除的NH4+-N浓度. 湿地二区和三区的砖渣厚度分别只有40 cm和10 cm,明显比一区(70 cm)的低. 而且,湿地二区和三区的有机物浓度也明显比一区的低. 因此,理论上,湿地三区的反硝化作用要比湿地二区和一区的低.
由图 2所示,在进水P质量浓度分别为30、 25和20 mg ·L-1时,湿地一区、 二区和三区对总P的去除率差别较大,分别为71.9%、 79.1%和30.3%. 天然沸石为多孔性构造,含有一定孔径的空腔和孔道,使其对P具有良好的吸附性能[13, 14]. 胡细全等[15]在天然沸石吸附NH4+-N和P的静态试验中测得低浓度下P的吸附去除率为4%左右. 3个湿地分区的填料种类相同,湿地植物的品种和种植密度相同,沸石层的填充高度差距较小,只有砖渣层的填充高度差别较大. 前期的研究也表明,砖渣吸附的P占人工湿地P去除总量的84.33%,沸石吸附的P占人工湿地P去除总量的12.86%,而植物吸收与微生物同化作用对TP去除的贡献不大,分别为 1.03%和 1.78%[4]. 表明砖渣填充高度差异是导致湿地3个分区P去除率差异显著的主要原因. 一区和二区对P的去除率相当,可能是因为在当前运行条件下,40 cm厚的砖渣已能很好的实现对P的去除.
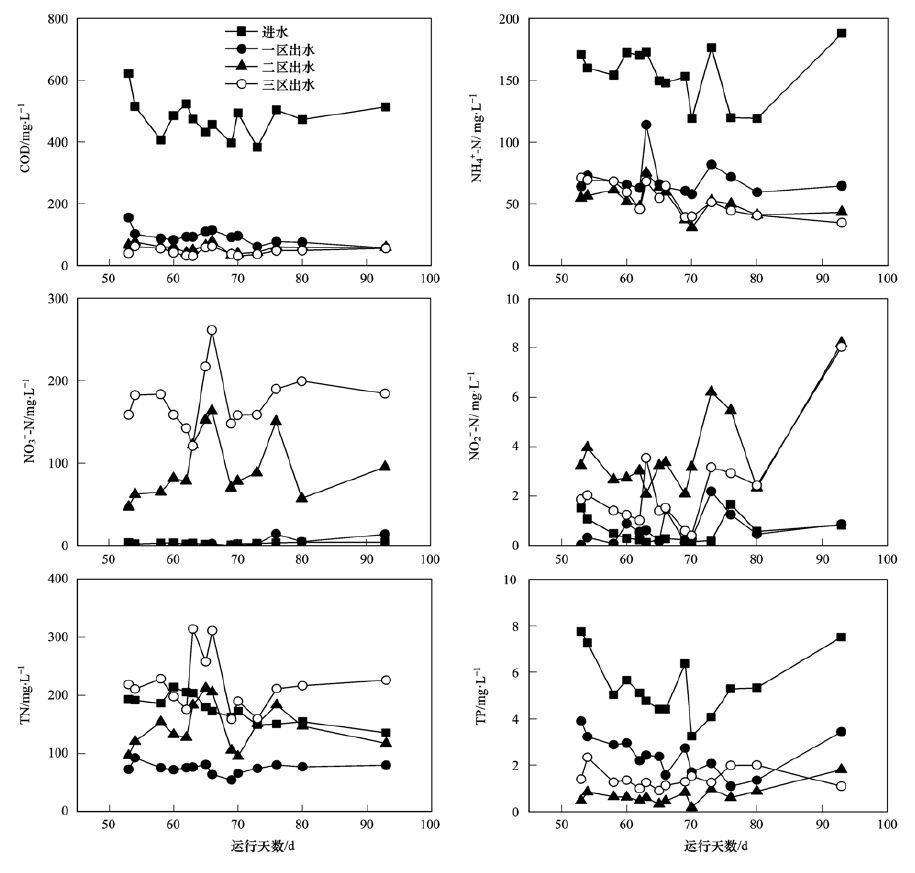
2.2 启动后运行性能三级生物沸石人工湿地启动后的运行性能如图 3和表 2所示. 从中可以看出,三级人工湿地可将分散养猪冲洗水厌氧出水的平均COD由477.69 mg ·L-1降至45.81 mg ·L-1. COD主要在湿地一区被去除,平均去除率为80.6%,其在湿地二区和三区的平均去除率只有7.6%和2.3%. 分散养猪废水经ABR厌氧处理后,其所含的易于降解的有机物首先在湿地一区的沸石层在进水期被快速吸附,随后在砖渣层被反硝化微生物作为碳源利用. 湿地一区出水中仍含有少量微生物能降解的有机物,因此在湿地二区COD仍有一定的去除,平均去除的COD质量浓度为36.32 mg ·L-1. 经过湿地一区和二区的处理,废水中剩余的有机物很难被微生物利用,因此湿地三区对COD的去除不明显. NH4+-N的沿程去除规律与COD的类似,主要在湿地一区被去除,由155.29 mg ·L-1降至69.44 mg ·L-1,在二区被进一步降低至51.84 mg ·L-1,在三区去除不明显. 这是由于环境温度较高(18.5~29.0℃),湿地一区沸石表面硝化菌的活性较高,硝化性能较强使得沸石在落干期可再生出较多的吸附位点,保障在进水期对NH4+-N的吸附. 湿地二区进水的NH4+-N浓度比沸石吸附-解吸的平衡浓度高,因此沸石仍可继续吸附NH4+-N. 湿地三区进水NH4+-N浓度与沸石吸附-解吸的平衡浓度基本相当,因此NH4+-N在此区域去除不明显.
|
图 3 三级生物沸石人工湿地启动后运行性能 Fig. 3 Operating performance of the three-stage bio-zeolite constructed wetland after the startup phase |
从图 3可知,湿地一区出水NO2--N和NO3--N质量浓度很低,平均为0.66 mg ·L-1和2.64 mg ·L-1. TN平均质量浓度由进水的176.43 mg ·L-1降至74.00 mg ·L-1,去除率为58.1%. 湿地一区对TN的去除主要包括以下两个方面:首先是沸石对NH4+-N的吸附,其次是沸石生物再生产生的NO3--N通过反硝化作用被去除. 由于湿地经过较长时间的稳定运行,可认为湿地一区的生物沸石基本达到快速吸附-再生动态平衡,即沸石对NH4+-N的吸附浓度与硝化产生的NO3--N和NO2--N浓度之和基本相同. 因此,湿地一区反硝化去除氮的平均质量浓度是NH4+-N平均去除质量浓度(85.85 mg ·L-1)与一区出水中NO3--N和NO2--N质量浓度之和的差值,为82.55 mg ·L-1,其占TN平均去除质量浓度的80.6%. 启动后,沸石表面生物膜硝化作用明显,湿地二区和三区的平均NO3--N质量浓度分别为93.69 mg ·L-1和176.1 mg ·L-1,是TN的主要组成部分. 由于硝化和反硝化作用,湿地的NO2--N略有升高,湿地二区和三区的平均质量浓度分别为3.70 mg ·L-1和2.26 mg ·L-1. 湿地二区和三区硝化作用产生的NO3--N和NO2--N的质量浓度之和分别为94.09 mg ·L-1和80.97 mg ·L-1,超过各自吸附去除的NH4+-N浓度,即沸石生物再生量大于吸附量,导致湿地三区出水TN大于系统进水的TN. 这主要是由于湿地二区和三区的生物沸石在启动阶段吸附了较多的NH4+-N,导致启动后微生物有足够的硝化底物. 这也表明,湿地在进水NH4+-N浓度突然升高或不利微生物硝化的条件下(如冬季低温),可以通过沸石吸附作用,保证对NH4+-N的去除; 运行条件改善后,沸石可通过生物再生,释放吸附位点,即三级生物沸石人工湿地对冲击负荷等不利条件的适应能力较强.
|
|
表 2 启动后污染物平均去除率 /% Table 2 Average removal rate of pollutants after the startup phase/% |
三级生物沸石人工湿地出水平均NO3--N质量浓度较高,为176.1 mg ·L-1. 廉价的稻秆可以作为反硝化固体碳源及生物膜载体用于分散养猪冲洗水的脱氮,NO3--N的去除率为95%以上[16].
人工湿地对污水中P的去除主要通过植物吸收、 基质吸附、 微生物固定等作用实现[17],最终通过植物收割及更换吸附饱和的基质达到除P的目的,其中基质对P的去除是人工湿地除P的主要途径[18]. 沸石和砖渣对P都有很好的吸附效果. 湿地对P的吸附量与进水中P的浓度及吸附剂的量均相关. 张翠玲等[19]研究表明沸石对P的吸附量随P初始浓度的增加而增大并最终趋于平衡. 郭强等[20]在矿化垃圾除P的静态吸附试验中,也发现初始浓度越高,固液比越小,矿化垃圾吸附P量越多. 王帅等[21]研究发现,在20 mL质量浓度为5 mg ·L-1磷酸盐溶液中,沸石对P的去除率随投加量的增加而升高,当投加量接近7 g 时,P的去除率基本稳定. 养殖废水中P的浓度经过湿地填料的吸附,将沿程降低. 湿地中,沸石和砖渣的填充量为湿地一区>二区>三区. 因此,湿地一区对TP的去除量最大,平均去除率为55.4%; 其次为二区,对TP的平均去除率为31.8%. 湿地三区出水TP浓度比二区的高,这主要是由于启动阶段湿地三区进水中TP浓度较高,导致沸石层吸附较高浓度的TP,当进水中TP浓度明显降低后,沸石所吸附的TP由于吸附-解吸平衡作用被释放至水中.
2.3 污染物随时间变化研究人工湿地中的硝化反硝化作用在时间和空间上的分布规律,对于全面深入的了解人工湿地内部的污染物净化机制、阐明湿地脱氮的关键性步骤、 丰富微生物的理化性质、 提高湿地的效率等具有重要意义[22]. 三级生物沸石人工湿地以潮汐流方式运行,污染物在湿地系统随时间的变化具有不均匀性. 为此,考察出水期间水质随时间的变化,试验结果如表 3所示.
由表 3可以看出,COD和NH4+-N主要在湿地一区被去除. 出水中污染物随时间变化不均匀,这种变化体现了潮汐流人工湿地的特点. 湿地在进水前,沸石表面生物膜将进水期吸附的有机物降解,将沸石吸附的NH4+-N转化为NO2--N或NO3--N; 砖渣表面生物膜利用水中的有机物将NO2--N或NO3--N还原为N2. 因此,0 min时COD的浓度较低. 湿地一区进水稳定,因此其出水的变化最能代表潮汐流人工湿地随时间的变化特征. 进水期,水中的有机物和NH4+-N被快速吸附,导致其浓度在15 min时迅速降低. 湿地一区COD随时间逐渐降低,可能是由于系统对有机物的吸附容量大,同时也可能是因为较高浓度的有机物和NO3--N在砖渣层发生了反硝化反应. NH4+-N浓度先快速降低,再缓慢升高. 这是由于NH4+-N的去除主要靠沸石的吸附,落干期沸石生物再生释放了部分吸附位点,因此开始阶段对NH4+-N的吸附容量大,随后由于吸附位点减少,导致出水NH4+-N浓度升高. NO3--N水溶性好,因此在进水的初期被大量地从沸石层冲刷下来,随着进水的进行其浓度快速降低. 湿地一区NO2--N质量浓度在15 min时最高,但仅为8.86 mg ·L-1,表明其在落干期略有累积,但NO3--N仍是硝化反应的主要产物.
|
|
表 3 底部分时间点出水情况 /mg ·L-1 Table 3 Situation of effluent over time at the bottom/mg ·L-1 |
湿地二区和三区NH4+-N的变化规律与湿地一区的类似. 有机物主要在湿地一区被去除,湿地二区和三区的COD浓度较低,因此湿地二区和三区降解有机物的异养菌对硝化菌的竞争性抑制作用要比湿地一区的弱,使得湿地二区和三区产生的NO3--N浓度明显高于湿地一区. 另外,由于湿地二区和三区有机物浓度明显比湿地一区的低,在落干期其反硝化作用较弱,导致0 min时湿地二区和三区的NO3--N浓度明显比湿地一区的高. 与进水相比,湿地一区的pH有明显的降低. 硝化反应将消耗碱度,而反硝化反应产生碱度. 湿地一区pH的降低是硝化和反硝化反应综合作用的结果,且硝化反应强度超过了反硝化反应. pH在湿地二区和三区依次降低,这主要是由于在这两个湿地分区发生了明显的硝化反应,而且由于有机物浓度低,反硝化作用弱.
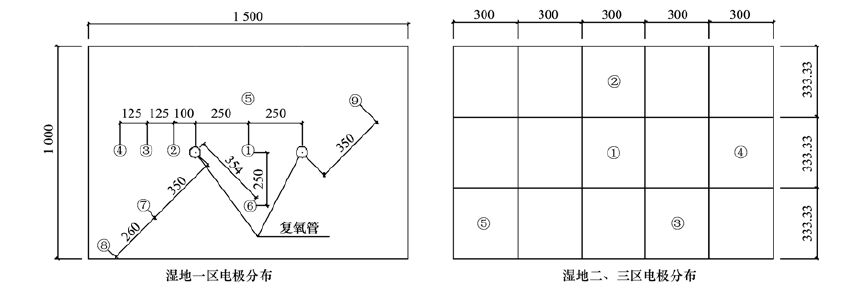
2.4 氧化还原电位空间分布ORP是反映人工湿地氧化还原状态的重要指标,是微生物活动以及有机物质降解和营养盐转化的重要影响因素[23]. 三级人工湿地的沸石层均发生了明显的好氧硝化反应. 通常,人工湿地的硝化性能与ORP正相关. 解析湿地沸石层硝化性能空间分布情况,可为优化湿地结构提供依据. 为此,在湿地3个分区的不同位置和沸石层的不同厚度(一区为10、 20、 30和40 cm,二、 三区为10、 20和30 cm)分别插有ORP电极(电极位置分布如图 4所示),通过ORP空间分布情况间接反映湿地沸石层硝化性能空间分布情况,试验结果如图 5所示.
|
单位: mm 图 4 人工湿地ORP电极位置分布平面示意 Fig. 4 Distribution diagram of ORP electrode in the constructed wetland |
|
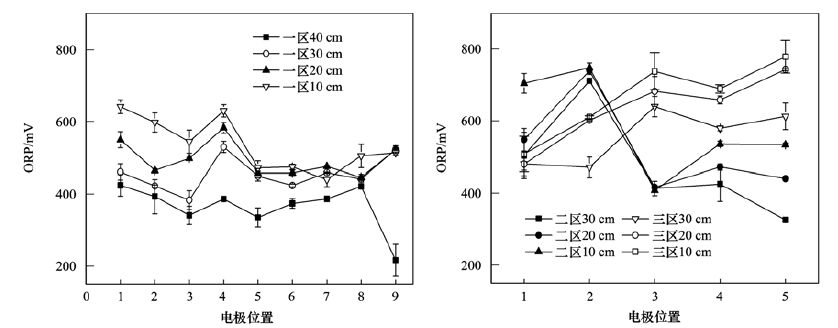
图 5 沸石层ORP空间分布 Fig. 5 ORP spatial distribution in the zeolite layer |
由图 5可以看出,在不同水平位置和不同沸石层高度处,湿地3个分区ORP值大部分都保持在400 mV以上,表明三级湿地沸石层复氧效果均较好. 潮汐流人工湿地利用潮汐运行过程中床体浸润面的变化产生的空隙吸力将大气氧吸入湿地基质或者土壤空隙,从而提高人工湿地的溶解氧含量[24]. 另外,三级湿地上方均种植空心菜,植物对湿地有一定的供氧作用. 植物根系除了泌氧外[25],根系发育导致的湿地填料疏松空隙也能促进湿地表面复氧[26]. 湿地3个分区ORP沿沸石层厚度从上往下依次降低. 湿地一区1号位置距复氧管距离比2号位置远,与3号位置的相同,但其ORP却比2号和3号位置的高,这是因为1号位置位于两根复氧管中间,两根复氧管共同复氧的效果强于单根; 4、 5、 6、 7、 9号位置距复氧管距离相同,但其ORP值有明显差异,表明湿地沸石层的氧化还原环境不均一; 9号位置ORP在沸石层底部40 cm处明显偏低,可能是此处沸石间的间隙水较多,电极部分浸泡在水中所致. 尽管湿地二区和三区没有复氧管,但是其ORP值仍较高,复氧效果良好. 与湿地一区相似,湿地二区和三区不同位置的ORP也有一定的波动. 平安等[27]研究的水平潜流人工湿地系统运行期间ORP范围在-236~40 mV 之间,多数位点ORP均为负值,整个湿地内部大部分区域处于厌氧状态,不同位点间变化范围较大,ORP沿水深方向逐渐降低. 湿地一区、 二区和三区沸石层30 cm处的平均ORP分别为454.4、 475.5和556.3 mV,可能是由于进水中有机物沿程逐渐减少,好氧异养菌降解有机物所需的氧沿程降低,导致湿地氧化还原电位沿程升高. 这与付融冰等[23]研究的连续流水平潜流湿地沿程变化一致.
3 结论(1) 基于生物沸石的三级人工湿地可实现分散养猪废水厌氧出水(ABR处理)的高效处理. 水力负荷为0.047 m3 ·(m2 ·d)-1时,可将分散养猪废水厌氧出水的平均COD由477.69 mg ·L-1降至45.81 mg ·L-1. COD和NH4+-N主要在湿地一区去除,COD去除机制包括在沸石层的好氧降解及在砖渣层的反硝化,NH4+-N由155.29 mg ·L-1降至69.44 mg ·L-1,其首先在沸石层被吸附及转化为NO3--N,随后NO3--N在砖渣层被还原为N2.
(2) 三级人工湿地采用潮汐流的方式运行,复氧效果良好,ORP基本在400 mV以上. 启动后,湿地二区和三区可将沸石在启动阶段过量吸附的NH4+-N转化为NO3--N,出水质量浓度分别为94.1 mg ·L-1和176.1 mg ·L-1. 三级生物沸石人工湿地在进水NH4+-N负荷较高或环境条件不利情况下,可先将NH4+-N吸附,随后再缓慢再生,释放对NH4+-N的吸附位点,即对冲击负荷等不利条件的适应能力较强.
| [1] | Sánchez E, Borja R, Travieso L, et al. Effect of influent substrate concentration and hydraulic retention time on the performance of down-flow anaerobic fixed bed reactors treating piggery wastewater in a tropical climate[J]. Process Biochemistry , 2005, 40 (2) : 817–829. DOI:10.1016/j.procbio.2004.02.005 |
| [2] | 杨利伟.分散式养猪废水处理技术工艺研究[D].西安:西安建筑科技大学,2011. http://cdmd.cnki.com.cn/article/cdmd-10703-1011297081.htm |
| [3] | 苗莹.ABR-功能分区型人工湿地强化TN去除区处理分散养猪废水试验研究[D].西安:长安大学,2015. http://cdmd.cnki.com.cn/article/cdmd-10710-1015802390.htm |
| [4] | 宋爱红.强化脱氮人工湿地处理分散养猪冲洗水特性研究[D].西安:长安大学,2015. http://cdmd.cnki.com.cn/article/cdmd-10710-1015802455.htm |
| [5] | 张政, 付融冰, 顾国维, 等. 人工湿地脱氮途径及其影响因素分析[J]. 生态环境学报 , 2006, 15 (6) : 1385–1390. |
| [6] | 吴树彪, 张东晓, 柳清青, 等. 潮汐流人工湿地床处理生活污水的优化研究[J]. 中国农业大学学报 , 2010, 15 (2) : 106–113. |
| [7] | Li C Y, Wu S B, Dong R J. Dynamics of organic matter,nitrogen and phosphorus removal and their interactions in a tidal operated constructed wetland[J]. Journal of Environmental Management , 2015, 151 : 310–316. DOI:10.1016/j.jenvman.2015.01.011 |
| [8] | Wu H M, Fan J L, Zhang J, et al. Decentralized domestic wastewater treatment using intermittently aerated vertical flow constructed wetlands:impact of influent strengths[J]. Bioresource Technology , 2015, 176 : 163–168. DOI:10.1016/j.biortech.2014.11.041 |
| [9] | 沈志强, 牟锐, 李元志, 等. 人工湿地生物沸石快速吸附-再生性能与再生机理研究[J]. 环境科学学报 , 2016, 36 (4) : 1242–1247. DOI:10.13671/j.hjkxxb.2015.0587 |
| [10] | 肖宇, 沈志强, 周岳溪, 等. 厌氧折流板反应器对分散养猪冲洗水有机物去除特性研究[J]. 农业环境科学学报 , 2015, 34 (10) : 2004–2011. |
| [11] | 万风.农村分散养猪废水处理工艺研究[D].邯郸:河北工程大学,2012. |
| [12] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版).北京: 中国环境科学出版社, 2002 . |
| [13] | 张翔凌, 陈俊杰, 郭露, 等. 垂直流人工湿地LDHs覆膜改性沸石基质强化除磷效果及其机制[J]. 环境科学 , 2014, 35 (12) : 4553–4559. |
| [14] | 叶志平, 于凤娥, 何国伟. 天然沸石处理富营养化水的生物基作用研究[J]. 环境工程学报 , 2009, 3 (1) : 85–88. |
| [15] | 胡细全, 胡志操, 王春秀, 等. 天然沸石吸附氨氮和磷的研究[J]. 环境科学与管理 , 2009, 34 (4) : 72–74. |
| [16] | 宋爱红, 沈志强, 周岳溪, 等. 以稻秆为固体碳源处理分散养猪冲洗水的试验研究[J]. 中国环境科学 , 2015, 35 (7) : 2052–2058. |
| [17] | Dong C S, Cho J S, Lee H J, et al. Phosphorus retention capacity of filter media for estimating the longevity of constructed wetland[J]. Water Research , 2005, 39 (11) : 2445–2457. DOI:10.1016/j.watres.2005.04.032 |
| [18] | Westholm L J. Substrates for phosphorus removal-Potential benefits for on-site wastewater treatment?[J]. Water Research , 2006, 40 (1) : 23–36. DOI:10.1016/j.watres.2005.11.006 |
| [19] | 张翠玲, 党瑞, 贺建栋, 等. 白银天然沸石对磷的吸附机理及性能研究[J]. 环境科学与管理 , 2014, 39 (12) : 104–108. |
| [20] | 郭强, 柴晓利, 赵由才. 矿化垃圾除磷特性及其影响因素的研究[J]. 环境污染与防治 , 2006, 28 (2) : 93–95. |
| [21] | 王帅, 周震峰, 刁玲玲. 沸石对水中磷吸附性能的初步研究[J]. 环境科学导刊 , 2014, 33 (5) : 52–56. |
| [22] | Song K, Hernandez M E, Batson J A, et al. Long-term denitrification rates in created riverine wetlands and their relationship with environmental factors[J]. Ecological Engineering , 2014, 72 : 40–46. DOI:10.1016/j.ecoleng.2013.06.041 |
| [23] | 付融冰, 朱宜平, 杨海真, 等. 连续流湿地中DO、ORP状况及与植物根系分布的关系[J]. 环境科学学报 , 2008, 28 (10) : 2036–2041. |
| [24] | Zhao Y Q, Sun G, Allen S J. Anti-sized reed bed system for animal wastewater treatment:a comparative study[J]. Water Research , 2004, 38 (12) : 2907–2917. DOI:10.1016/j.watres.2004.03.038 |
| [25] | Stottmeister U, Wiener A, Kuschk P, et al. Effects of plants and microorganisms in constructed wetlands for wastewater treatment[J]. Biotechnology Advances , 2003, 22 (1-2) : 93–117. DOI:10.1016/j.biotechadv.2003.08.010 |
| [26] | 谢飞, 黄磊, 高旭, 等. 潜流人工湿地对微污染河水的净化效果[J]. 环境工程学报 , 2013, 7 (1) : 65–71. |
| [27] | 平安, 种云霄, 余光伟, 等. 使用含铁基质的水平潜流人工湿地间隙水亚铁离子及理化环境的动态变化[J]. 环境科学学报 , 2014, 34 (12) : 3043–3049. |
 2016, Vol. 37
2016, Vol. 37


