2.上海城市水资源开发利用国家工程中心有限公司, 上海 200082;
3.华东理工大学药学院, 制药工程与过程化学教育部工程研究中心, 上海 200237
2.National Engineering Research Center of Urban Water Resources, Shanghai 200082, China;
3.Research Center of Pharmaceutical Process Chemistry, Ministry of Education, School of Pharmacy, East China University of Science and Technology, Shanghai 200237, China
1982年首次报道地表水中检出大环内酯类、 磺胺类和四环素类抗生素[1]. 近年来,抗生素在环境中的残留、 生态风险,尤其对人体健康的潜在威胁日益引起广泛关注. 环境中残留的微量抗生素会诱导细菌产生抗性基因,从而导致细菌具有耐药性[2, 3]. 2013年我国的抗生素总使用量为162000 t,人均用量是欧美国家的6~10倍[4]. 抗生素在生物体内并不能完全地被代谢分解,约60%~90%以原药的形式排出体外[5, 6],而目前污水处理工艺不能有效地去除微量的抗生素[7, 8]. 残留的抗生素最终进入自然水体,潜在影响饮用水源地水质安全[9].
磺胺类(sulfonamides,SAs)抗生素具有稳定的化学结构、 低廉的价格和广谱的抗菌效果,广泛用于治疗人类、 动物的疾病[10]. 同时磺胺类抗生素的酸碱两性特征使其在环境中具有很好的迁移能力[11, 12]. 我国的黄浦江[13]、 渤海湾[14]、 部分饮用水源地[15],均检测出甲氧苄啶、 磺胺甲唑和磺胺二甲嘧啶等磺胺类抗生素. 美国和葡萄牙的自来水中检测出磺胺甲唑等常见磺胺类抗生素[9, 16]. 甚至在学龄儿童尿液中检出了5~142 μg·L-1的磺胺类抗生素[17]. 抗生素可能通过饮用水的途径进入人体对健康产生威胁.
水源水质与饮用水安全密切相关. 本研究通过分析13种磺胺类抗生素在华东地区某水源水中的浓度,并基于风险熵的方法评价水源水中残留抗生素的潜在人体健康风险,有助于揭示水源水中磺胺类抗生素的分布特征和季节变化规律,并对正确理解水源水中微量磺胺类抗生素的健康风险具有指导意义.
1 材料与方法 1.1 仪器与试剂Agilent 1260高效液相色谱仪(Agilent,USA); Agilent 6430三重四极杆串联质谱仪(Agilent,USA); 固相萃取装置(Supelco,USA); HLB 固相萃取柱 (6 mL,500 mg,Waters,USA); DC-12氮气吹干仪(上海安谱科学仪器有限公司); 玻璃纤维滤膜(GF/F,0.7 μm,Whatman,UK); 0.22 μm的针头式过滤器(天津津腾实验设备有限公司).
13种磺胺类抗生素标品: 甲氧苄啶(Trimethoprim,TMP)、 磺胺(Sulfanilamide,SAM)、 磺胺脒(Sulfaguanidine,SG)、 磺胺嘧啶(Sulfadiazine,SDZ)、 磺胺甲基嘧啶 (Sulfamerazine,SMR)、 磺胺二甲嘧啶(Sulfamethazine,SMZ)、 磺胺噻唑 (Sulfathiazole,STZ)、 磺胺甲噻二唑(Sulfamethizole,SMT)、 磺胺甲唑 (Sulfamethoxazole,SMX)、 磺胺二甲异噻唑(Sulfisoxazole,SFX)、 磺胺氯哒嗪 (Sulfachloropyridazine,SCP)、 磺胺对甲氧嘧啶(Sulfameter,SMD)、 磺胺二甲氧嘧啶(Sulfadimethoxine,SAT)和磺胺甲唑同位素标记物(SMX-13C6)均购自Sigma公司(Sigma,USA); 盐酸、 乙二胺四乙酸二钠均为分析纯,购自国药集团化学试剂有限公司; 甲酸、 甲醇、 乙腈均为色谱纯,购自Thermo Fisher公司(Fisher Scientific,USA); 实验用纯水取自Milli-Q纯水仪(Millipore,USA).
1.2 样品采集采样水源地位于我国华东地区长江下游. 采样时间按12月~次年2月、 3~5月、 6~8月、 9~11月依次分为冬、 春、 夏和秋季. 于2014年12月至2015年11月期间,每月采集水源地入水口、 库中和出水口水样(相邻采样点相距约7 km),共采集样品数72个. 每次取表层水面以下0.5 m处水样,置于棕色玻璃瓶内,用冰块保持低温环境,运回实验室并尽快进行固相萃取富集浓缩.
1.3 抗生素分析 1.3.1 样品预处理固相萃取在文献[18]的方法上进行优化,1 L的水样经0.7 μm孔径的玻璃纤维滤膜过滤,加入0.2 g 乙二胺四乙酸二钠,用0.1 mol·L-1 的盐酸调节水样pH为3.0,加入100 ng磺胺甲唑-13C6 (1 mL,100 μg·L-1的SMX-13C6)内标物. HLB固相萃取柱依次用10 mL甲醇、 10 mL超纯水和10 mL pH为3.0的盐酸水溶液活化. 水样以3~5 mL·min-1的流速通过HLB固相萃取柱,水样萃取完后,萃取柱在真空下抽干30 min,用5%(体积比)的甲醇水溶液淋洗去杂质,最后用10 mL纯甲醇洗脱. 收集的洗脱液在35℃水浴条件下,用氮气缓慢地吹至近干,用50%(体积比)的甲醇水溶液定容至1 mL,经0.22 μm滤膜过滤,-20℃保存,待进样分析.
1.3.2 HPLC/MS/MS分析方法液相条件: CNW Athena C18-WP色谱柱(2.1 mm×150 mm,3 μm); 进样量: 5 μL; 流动相流速: 0.4 mL·min-1; 柱温:30℃; 流动相A(0.1%甲酸的乙腈),流动相B(0.1%甲酸的水溶液). 梯度洗脱程序: 0~13 min,85%的流动相B线性降低至55%,14 min时降低至15%并保持4 min,在19 min时回到85%并保持4 min. 质谱参数详见表 1.
1.3.3 方法回收率及精密度采用内标法定量,以目标物质响应值与内标物SMX-13C6响应值之比对浓度作图,得定量曲线,定量曲线在1.0~1000 μg·L-1范围内线性关系良好,相关系数范围0.9968~0.9995. 通过信噪比来计算方法的检出限,以3倍信噪比为抗生素质量浓度的检出限.
|
|
表 1 目标抗生素的质谱参数、 回收率和检测限 Table 1 Mass spectrometric parameters,recoveries and limits of quantitation of target antibiotics |
在1 L的水源水中加入10、 50和200 ng的13种磺胺类抗生素混标,同时测空白组分中磺胺类抗生素含量,计算回收率(见表 1),每组3个平行样. 磺胺(SAM)和磺胺脒(SG)的回收率分别为55.2%和63.3%,其他11种磺胺类抗生素回收率在87.1%~106.8%,方法相对标准偏差小于5%,检测实际水样中磺胺类抗生素时,数据结果不再进行回收率的校正.
1.4 人体健康风险评价方法水源水中的抗生素对人体健康风险评价是基于风险熵的方法,并同时考虑对不同年龄段人群的风险,若风险熵大于1,则认为是有风险[16]. 具体的计算方法见公式(1) 、 (2) .
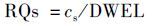
|
(1) |
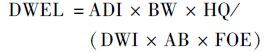
|
(2) |
式中,cs是抗生素的检出浓度(μg·L-1),DWEL是抗生素的饮用水当量值(μg·L-1). ADI是日均可接受摄入量[μg·(kg·d)-1],BW是人均体重(kg),HQ是最高风险,按1计算. DWI是每日饮水量(L·d-1),AB是胃肠吸收率,按1计算,FOE是暴露频率(350 d·a-1),按0.96计算. BW和DWI的相关数据采用美国环保署(EPA)推荐值[19],磺胺类抗生素的ADI值参考自澳大利亚卫生署的药物ADI清单[20],具体参数详见表 2. 评价饮用水源水中抗生素对人体的健康风险,为考虑最大的风险,均以每种磺胺类抗生素的最大检出浓度用于计算饮用水当量水平(DWEL)和风险熵(RQs).
|
|
表 2 各年龄段人群的平均体重、 日饮用水量[19]及磺胺类药品的每日可接受摄入量[20] Table 2 Selected age groups and average body weights and drinking water intakes(DWI) and acceptable daily intakes(ADI) of selected sulfonamides |
2 结果与讨论 2.1 磺胺类抗生素在水源水中的总体检出水平
13种磺胺类抗生素在该水源水中均不同程度检出(见表 3). SMX和SAM 100%检出,TMP、 SDZ、 SMZ和SCP检出频率也较高,为73%~86%,其余7种磺胺类抗生素检出频率在7%~50%. 值得注意的是,以往较少报道SAM在水体中的污染水平,本研究发现SAM在水源水中100%地检出非常值得关注. 水源水中磺胺类抗生素总检出浓度最高达238.5 ng·L-1,其中 SMX的检出浓度最高为 107.0 ng·L-1,平均值为21.0 ng·L-1. SAM和TMP检出的最高浓度分别为43.1 ng·L-1和22.0 ng·L-1. SDZ、 SMR、 SMZ和SCP检出的浓度范围为n.d.~14.5 ng·L-1.
|
|
表 3 磺胺类抗生素在饮用水源水中的总体检出水平1) /ng·L-1 Table 3 Summary of sulfonamides concentrations in drinking water source/ng·L-1 |
SMX的高频率、 高浓度检出,与SMX在我国其它水域的检出结果一致,例如珠江[21]、 渤海湾[14]、 黄浦江[13]等地表水中SMX的检出率为97%~100%,浓度为2~765 ng·L-1. 这与SMX具有良好的环境迁移能力及化学稳定性、 不易发生降解和吸附有关[22]. SAM和TMP相对较高的检出频率和浓度,可能因为SAM是磺胺类抗生素的对氨基苯磺酰胺的母体结构,是用于合成磺胺类药物的主要原料. TMP是磺胺类抗生素的增效剂,常与SMX等磺胺类抗生素混合使用以增加药效,同时约87.5%的TMP通过动物排泄物以原药形式排出[23]. SDZ、 SMZ和SCP的虽然检出浓度较低(n.d.~14.5 ng·L-1),但检出频率较高(72%~86%),因其是常用的兽用类抗生素,广泛用于畜禽养殖行业[4]. 其余7种磺胺类抗生素的检出浓度和检出频率都比较低. 这可能因为其使用量低,以SG和STZ为例,使用量在磺胺类抗生素中分别只占0.8%和1.9%[4].
与国内外其它地区相比,该水源水中磺胺类抗生素的浓度水平(10.5~238.5 ng·L-1)与崇明地区(n.d.~305.5 ng·L-1)[24]地表水中磺胺类抗生素浓度相当,低于我国的黄浦江(27.0~1555.2 ng·L-1)[13]、 珠江(9~852 ng·L-1)[21, 25]、 渤海湾(n.d.~431 ng·L-1)[14]等地表水,但高于同为饮用水源地的深圳铁岗水库(6.1~47 ng·L-1)[15]以及美国东南部(2.0~19.9 ng·L-1)[9]和葡萄牙里斯本市水源水(8~25 ng·L-1)[16]. 可能与该地区处于长江下游,其上游存在密集的养殖业、 抗生素使用量大有关. 长江三角洲地区的典型废水中,生猪养殖废水所含磺胺类抗生素SMX、 SDZ、 SMZ、 SCP和SMD浓度0.21~8.88 μg·L-1,是水体抗生素污染的主要源头[26, 27]. 华东地区磺胺类抗生素使用量占全国磺胺类抗生素总使用量的28.6%,是华南地区的4倍[4]. 这可能是该水源水中磺胺类抗生素含量高于地处华南的深圳铁岗水库原因之一.
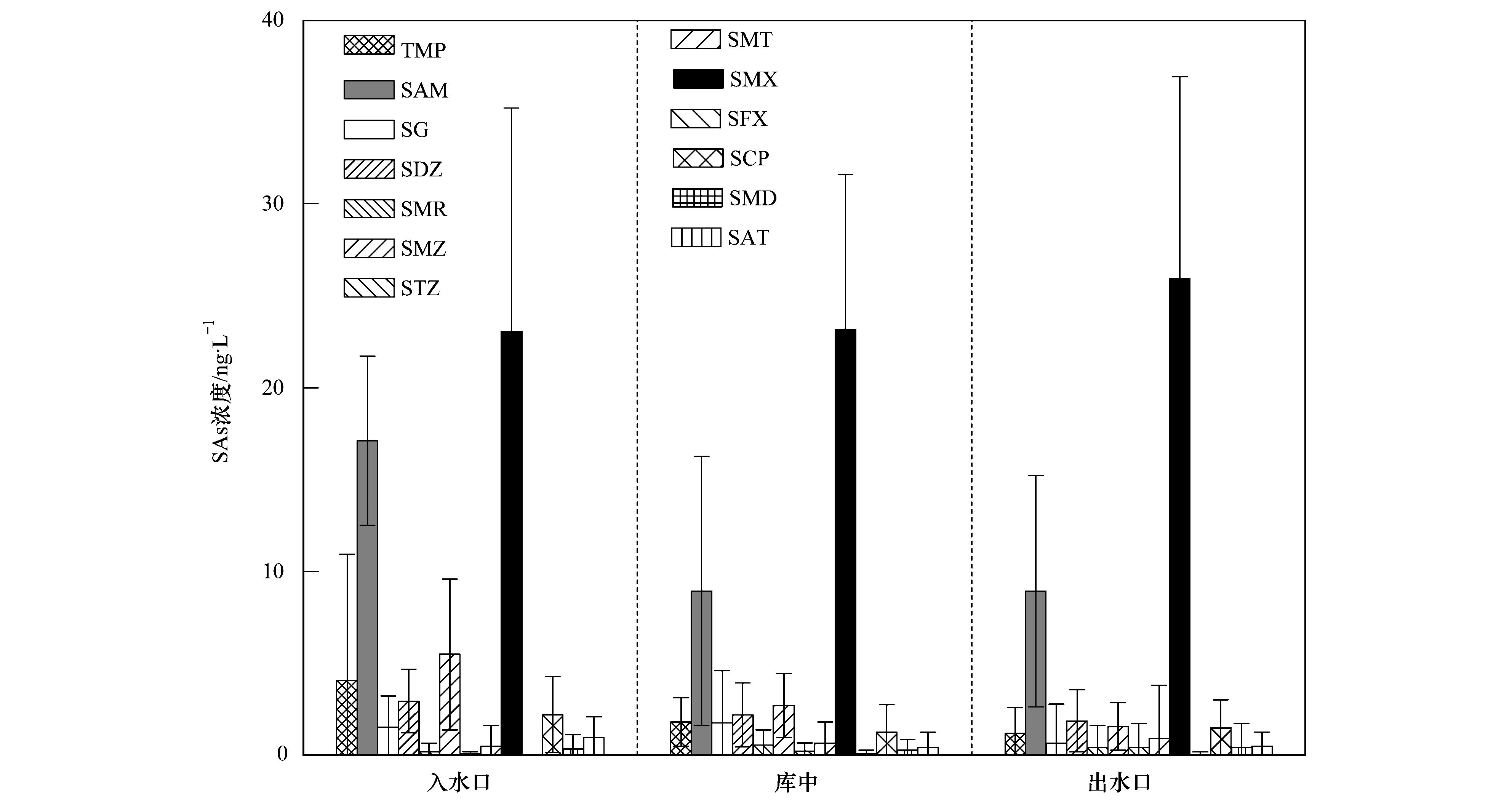
2.2 磺胺类抗生素在水源水中的空间分布特征磺胺类抗生素在水源地的空间分布特征如图 1所示. 入水口,库中和出水口磺胺类抗生素总的平均浓度分别为: 58.6、 44.2和44.4 ng·L-1. 比较水库上下游不同采样点,检出磺胺类中浓度相对最高的是SMX,占总浓度的39%~58%,其次是SAM,占20%~29%,其余的磺胺类抗生素则只占21%~31%. SMX在不同区域浓度变化不大,而其它的12种磺胺类抗生素,如TMP,SAM和SMZ等抗生素浓度在水源地不同位置表现出入水口检出浓度相对较高,库中和出水口浓度相近,且低于入水口的趋势.
|
图 1 磺胺类抗生素在水源水中的空间分布特征 Fig. 1 Spatial distribution characteristics of sulfonamides in drinking water source |
Kurwadkar等[28]研究磺胺类抗生素的环境迁移能力时,发现SMX的环境迁移能力强于SMR、 STZ、 SCP等其它磺胺类抗生素. 中性条件下,SMX的lgKow值为-0.33,其它磺胺类如SMR、 SMZ、 STZ、 SCP和SAT的lgKow依次为0.03、 0.67、 0.13、 0.13和0.61[29]. 较低的lgKow值使得SMX的亲水性强于其它磺胺类抗生素,这可能也是SMX在水源地不同位置,浓度变化不明显的一个原因. 水库水流自上而下逐渐变缓,有利于抗生素的微生物分解和光降解、 热分解等自然降解过程[30]. 与此同时一部分磺胺类抗生素被吸附于悬浮物,在流动过程中随之沉降[31],因此入水口磺胺类抗生素总浓度高于库中和出水口. 抗生素在水相与沉积物之间的吸附与解吸是一个动态的过程,受水环境等条件变化影响,致使沉积物吸附对抗生素浓度变化的影响是有限的[32]. 光解等非生物降解是环境中磺胺类抗生素降解的主要途径,其次是微生物降解、 沉积物吸附[33].
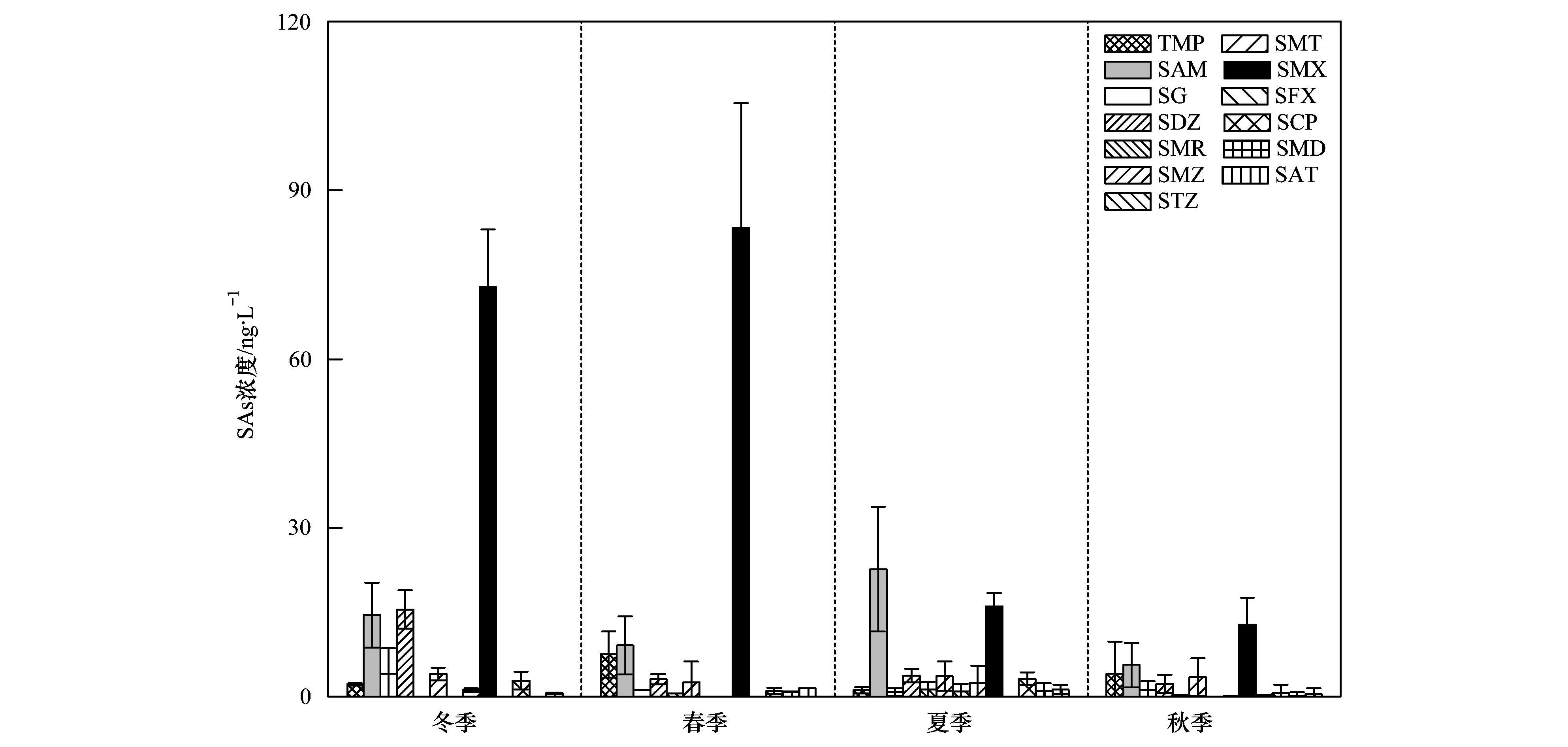
2.3 磺胺类抗生素在水源水中的季节变化特征水源水中磺胺类抗生素呈现出较为明显的季节分布特征(图 2). 春季、 夏季、 秋季、 冬季水源水中13种磺胺类抗生素平均浓度的总和分别为110.8、58.3、30.9和117.9 ng·L-1. 春季和冬季的磺胺类抗生素总浓度高,是夏季和秋季的3.6~3.8倍,呈现出春冬季节明显高于夏秋季节的趋势. 不同磺胺类抗生素中,浓度最高的SMX呈现出明显的季节特征,冬、 春季浓度为51.4~107.0 ng·L-1,夏、 秋季浓度为10.8~16.1 ng·L-1. 其它磺胺类中,TMP、 SDZ 也有类似的特征,冬、 春季节浓度为2.20~15.5 ng·L-1,夏、 秋季节的浓度为1.14~4.12 ng·L-1. 不同的是,SAM呈现出夏季浓度高于其它季节,其余的磺胺类抗生素因检出浓度较低,季节变化特征不明显.
|
图 2 磺胺类抗生素在水源水中的季节变化特征 Fig. 2 Seasonal changes of sulfonamides in drinking water source |
水源水中抗生素的季节变化特征主要受降雨量的稀释作用、 季节温度变化、 光解作用和微生物代谢活性等因素影响[9, 34]. 冬季、 春季属于流感等常见疾病多发季节,抗生素使用量是夏季的两倍[35]. 该地区冬季气温2.1~11.3℃、 平均降雨量57 mm,夏季气温 20.9~35.2℃、 平均降雨量 188 mm[36]. 冬春季节降雨量少,水库属于枯水期,同时冬季气温低、 光解及微生物代谢作用弱. 夏季降雨量大,降雨的稀释作用明显,气温高、 光解及微生物代谢分解抗生素的能力强[30, 37]. 夏季SAM的检出浓度相对较高,可能是自然光解作用增强,部分磺胺类抗生素分解生成SAM. Boreen 等[38]研究发现SMX、 SMT和STZ等包含五元杂环结构的磺胺类抗生素在光解过程会有SAM生成.
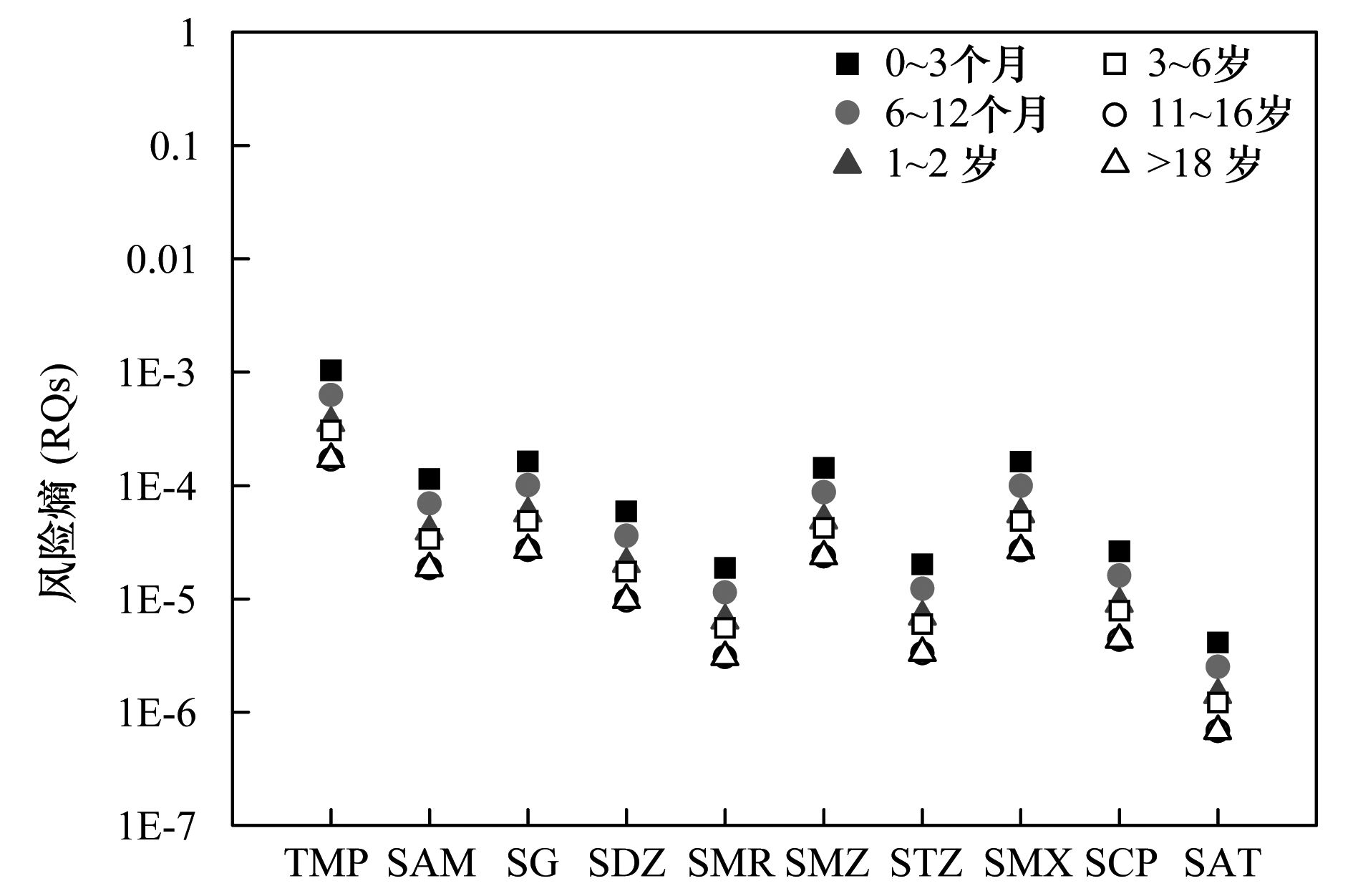
2.4 人体健康风险评价水源水检出的磺胺类抗生素对从婴幼儿到成人不同年龄段人群的健康风险如图 3所示. 磺胺类抗生素的风险熵均小于1,并表现出随年龄增长而降低. 各种磺胺类抗生素均对0~3个月的婴儿表现出最高的风险,3~6岁以下儿童,风险值随年龄增长降低较为明显,11~16岁及以上人群,风险值较为接近. 风险值最大的是TMP(RQs=0.001) ,这是由于该物质ADI值是所研究的磺胺类中最低的,仅为4.2 μg·(kg·d)-1. 风险熵超过0.0001的有SAM、 SG、 SMZ和SMX,其余的风险熵均小于0.0001.
|
图 3 水源水中磺胺类抗生素的人体健康风险 Fig. 3 Human health risk assessment of sulfonamides in drinking water source |
该结果表明华东某市水源中磺胺类抗生素对人体健康无直接风险,这与世界卫生组织以及其它研究的结果是一致的[16, 39, 40]. 但水源水中通常残留多种抗生素,其潜在的综合风险和长期风险值得关注. 水源水中痕量的抗生素诱导产生的抗性基因和抗性微生物的潜在风险不容忽视. 虽然原水中痕量的抗生素经过饮用水处理工艺处理会有部分的去除,但目前的饮用水处理工艺并不能完全去除这些痕量的抗生素[9, 16, 39]. 通过饮用水途径进入人体的抗生素,尤其是对学龄儿童,长期接触低剂量抗生素是导致儿童肥胖的风险因素[17]. 因此,抗生素在目前自来水厂工艺中的迁移转化规律也亟需研究和关注.
3 结论(1) 华东地区某水源水中13种磺胺类抗生素均有不同程度检出,其中SMX和SAM检出频率为100%,SMX的检出浓度最高.
(2) 磺胺类抗生素在水源水中呈现明显的区域和季节分布特征,水源地入水口检出浓度高,库中和出水口浓度相近,且低于入水口; 冬季和春季水源水中磺胺类抗生素浓度是夏季和秋季的3.6~3.8倍.
(3) 水源水中残留微量的磺胺类抗生素的风险值均远小于1,对人体健康尚不构成直接威胁.
| [1] | Homem V, Santos L. Degradation and removal methods of antibiotics from aqueous matrices-A review[J]. Journal of Environmental Management, 2011, 92(10) :2304-2347. |
| [2] | Jiang L, Hu X L, Xu T, et al. Prevalence of antibiotic resistance genes and their relationship with antibiotics in the Huangpu River and the drinking water sources, Shanghai, China[J]. Science of the Total Environment, 2013, 458-460:267-272. |
| [3] | Luo Y, Mao D Q, Rysz M, et al. Trends in antibiotic resistance genes occurrence in the Haihe River, China[J]. Environmental Science & Technology, 2010, 44(19) :7220-7225. |
| [4] | Zhang Q Q, Ying G G, Pan C G, et al. Comprehensive evaluation of antibiotics emission and fate in the river basins of china:source analysis, multimedia modeling, and linkage to bacterial resistance[J]. Environmental Science & Technology, 2015, 49(11) :6772-6782. |
| [5] | Hirsch R, Ternes T, Haberer K, et al. Occurrence of antibiotics in the aquatic environment[J]. Science of the Total Environment, 1999, 255(1-2) :109-118. |
| [6] | Halling-Sørensen B, Nielsen N S, Lanzky P F, et al. Occurrence, fate and effects of pharmaceutical substances in the environment-A review[J]. Chemosphere, 1998, 36(2) :357-393. |
| [7] | Zhou L J, Ying G G, Liu S, et al. Occurrence and fate of eleven classes of antibiotics in two typical wastewater treatment plants in South China[J]. Science of the Total Environment, 2013, 452-453:365-376. |
| [8] | Watkinson A J, Murby E J, Costanzo S D. Removal of antibiotics in conventional and advanced wastewater treatment:implications for environmental discharge and wastewater recycling[J]. Water Research, 2007, 41(18) :4164-4176. |
| [9] | Padhye L P, Yao H, Kung'u F T, et al. Year-long evaluation on the occurrence and fate of pharmaceuticals, personal care products, and endocrine disrupting chemicals in an urban drinking water treatment plant[J]. Water Research, 2014, 51:266-276. |
| [10] | Garoma T, Umamaheshwar S K, Mumper A. Removal of sulfadiazine, sulfamethizole, sulfamethoxazole, and sulfathiazole from aqueous solution by ozonation[J]. Chemosphere, 2010, 79(8) :814-820. |
| [11] | Dirany A, Sirés I, Oturan N, et al. Electrochemical treatment of the antibiotic sulfachloropyridazine:kinetics, reaction pathways, and toxicity evolution[J]. Environmental Science & Technology, 2012, 46(7) :4074-4082. |
| [12] | Tolls J. Sorption of veterinary pharmaceuticals in soils:A review[J]. Environmental Science & Technology, 2001, 35(17) :3397-3406. |
| [13] | Chen K, Zhou J L. Occurrence and behavior of antibiotics in water and sediments from the Huangpu River, Shanghai, China[J]. Chemosphere, 2014, 95:604-612. |
| [14] | Zou S C, Xu W H, Zhang R J, et al. Occurrence and distribution of antibiotics in coastal water of the Bohai Bay, China:impacts of river discharge and aquaculture activities[J]. Environmental Pollution, 2011, 159(10) :2913-2920. |
| [15] | 朱婷婷, 段标标, 宋战锋, 等. 深圳铁岗水库水体中抗生素污染特征分析及生态风险评价[J]. 生态环境学报,2014,23 (7) : 1175–1180. |
| [16] | Gaffney V D J, Almeida C M M, Rodrigues A, et al. Occurrence of pharmaceuticals in a water supply system and related human health risk assessment[J]. Water Research, 2015, 72:199-208. |
| [17] | Wang H X, Wang N, Wang B, et al. Antibiotics detected in urines and adipogenesis in school children[J]. Environment International, 2016, 89-90:204-211. |
| [18] | Cheng W H, Jiang L, Lu N, et al. Development of a method for trace level determination of antibiotics in drinking water sources by high performance liquid chromatography-tandem mass spectrometry[J]. Analytical Methods, 2015, 7(5) :1777-1787. |
| [19] | US EPA (U. S. Environmental Protection Agency). Guidance on selecting age groups for monitoring and assessing childhood exposures to environmental contaminants[EB/OL]. http://www.epa.gov/risk/guidance-selecting-age-groups-monitoring-and-assessing-childhood-exposures-environmental,2015-11. |
| [20] | Australian Government Department of Health. Acceptable Daily Intakes for Agricultural and Veterinary Chemicals[EB/OL]. http://www.health.gov.au/internet/main/publishing.nsf/Content/ocs-adi-list.htm,2016-03-31. |
| [21] | 徐维海, 张干, 邹世春, 等. 香港维多利亚港和珠江广州河段水体中抗生素的含量特征及其季节变化[J]. 环境科学,2006,27 (12) : 2458–2462. |
| [22] | Huang C H, Renem J E, Smeby L K, et al. Assessment of potential antibiotic contaminants in water and preliminary occurrence analysis[J]. Journal of Contemporary Water Research & Education, 2001, 120(1) :30-40. |
| [23] | Ji Y F, Xie W P, Fan Y, et al. Degradation of trimethoprim by thermo-activated persulfate oxidation:reaction kinetics and transformation mechanisms[J]. Chemical Engineering Journal, 2016, 286:16-24. |
| [24] | 洪蕾洁, 石璐, 张亚雷, 等. 固相萃取-高效液相色谱法同时测定水体中的10种磺胺类抗生素[J]. 环境科学,2012,33 (2) : 652–657. |
| [25] | Yang J F, Ying G G, Zhao J L, et al. Spatial and seasonal distribution of selected antibiotics in surface waters of the Pearl Rivers, China[J]. Journal of Environmental Science and Health, Part B:Pesticides, Food Contaminants, and Agricultural Wastes, 2011, 46(3) :272-280. |
| [26] | 姜蕾, 陈书怡, 杨蓉, 等. 长江三角洲地区典型废水中抗生素的初步分析[J]. 环境化学,2008,27 (3) : 371–374. |
| [27] | 丁佳丽, 刘锐, 郑炜, 等. 养猪废水和污泥中11种兽用抗生素的同时分析技术及其在生物降解过程的应用[J]. 环境科学,2015,36 (10) : 3918–3925. |
| [28] | Kurwadkar S T, Adams C D, Meyer M T, et al. Comparative mobility of sulfonamides and bromide tracer in three soils[J]. Journal of Environmental Management, 2011, 92(7) :1874-1881. |
| [29] | Martínez F, Gómez A. Thermodynamic study of the solubility of some sulfonamides in octanol, water, and the mutually saturated solvents[J]. Journal of Solution Chemistry, 2001, 30(10) :909-923. |
| [30] | Yi L, Lin X, Michal R, et al. Occurrence and transport of tetracycline, sulfonamide, quinolone, and macrolide antibiotics in the Haihe River Basin, China[J]. Environmental Science & Technology, 2011, 45(5) :1827-1833. |
| [31] | Christian T, Schneider R J, Färber H A, et al. Determination of antibiotic residues in manure, soil, and surface waters[J]. Acta Hydrochimica et Hydrobiologica, 2003, 31(1) :36-44. |
| [32] | Zhou J, Broodbank N. Sediment-water interactions of pharmaceutical residues in the river environment[J]. Water Research, 2014, 48:61-70. |
| [33] | 钟振兴. 磺胺抗生素在湖泊沉积物中的吸附和降解行为研究[D]. 重庆:西南大学, 2012. 23-32. |
| [34] | Yao L L, Wang Y X, Lei T, et al. Seasonal variation of antibiotics concentration in the aquatic environment:a case study at Jianghan Plain, central China[J]. Science of the Total Environment, 2015, 527-528:56-64. |
| [35] | 齐新玉, 王鸣. 不同季节抗生素的利用分析[J]. 农垦医学,2003,25 (3) : 183–184. |
| [36] | 国家统计局. 中国统计年鉴2015[EB/OL]. http://www.stats.gov.cn/tjsj/ndsj/,2015-10. |
| [37] | Zheng S L, Qiu X Y, Chen B, et al. Antibiotics pollution in Jiulong River estuary:Source, distribution and bacterial resistance[J]. Chemosphere, 2011, 84(11) :1677-1685. |
| [38] | Boreen A L, Arnold W A, Kristopher M N. Photochemical fate of sulfa drugs in the aquatic environment:sulfa drugs containing five-membered heterocyclic groups[J]. Environmental Science & Technology, 2004, 38(14) :3933-3940. |
| [39] | Leung H W, Jin L, Wei S, et al. Pharmaceuticals in tap water:human health risk assessment and proposed monitoring framework in China[J]. Environmental Health Perspectives, 2013, 121(7) :839-846. |
| [40] | Maycock D S, Watts C D. Pharmaceuticals in drinking water[A]. In:Nriagu J O (Ed.). Encyclopedia of Environmental Health. Amsterdam:Elsevier, 2011. 472-484. |
 2016, Vol. 37
2016, Vol. 37


