近年来,由于农业病虫害现象的加重,我国农药消耗量随之大幅度上升,导致大量的农药进入地表水体,对水体造成了严重的污染[1]. 其中,对水体危害最严重、 污染最广的是有机合成农药[2]. 该类产品见效快、 种类多、 价格低廉,占据了国内农药市场的主要份额,成为造成农药污染危害事件的主要剂型[1]. 近几年,我国2,4-二氯苯氧乙酸每年平均需求量达5 000 t以上,属于除草剂用量较大的种类之一[3]. 施于渠道和水中的除草剂可以引起水体污染,在环境中具有持久性,如果施用剂量较大,则被污染的水体可以引起严重公害[4~8].
目前国内外去除水中2,4-二氯苯氧乙酸(2,4-D)的主要方法有臭氧氧化技术、 Fenton氧化技术、 光化学技术、 吸附技术等[9~12]. 臭氧氧化技术运行费用较高且操作难度较大; Fenton氧化技术不适用于碱性废水的处理. 金属有机框架是继活性炭、 矿物吸附剂、 金属(氢)氧化物、 生物吸附剂、 离子交换树脂、 工业废弃物等传统吸附剂之后又一新兴的吸附剂[13, 14]. 目前,对于MOFs材料吸附特性的研究主要集中于气体污染物的去除,对于水中污染物的吸附研究主要涉及到染色剂、 酚类以及甲苯等物质[15~18]. UiO-66是在标准溶解热条件下,使用无水ZrCl4作为金属前驱体,对苯二甲酸作为有机配体,在N,N-二甲基甲酰胺(DMF)溶剂中进行反应合成的金属有机框架材料. 本实验采用UiO-66 吸附处理被2,4-D污染的水体,探索最佳吸附条件,研究吸附等温模型、 吸附动力学、 热力学、 内扩散模型、 吸附活化能和吸附机制.
1 材料与方法 1.1 实验仪器恒温水浴振荡器(SHA-B),分析天平(FA1004),高速冷冻离心机(TDL-5,TGL-16M),纯水机(Aquelix5),三频数控超声波清洗器(KQ-500VDE),高温烘箱(D1-101-2),循环水式多用真空泵(SHB-ⅢS),pH计(A211),X-射线衍射仪(D8 Advance),扫描电镜(Supra55),高效液相色谱仪(泵型号为waters1525,检测器型号为waters2487).
1.2 实验试剂四氯化锆(分析纯),对苯二甲酸(分析纯),N,N-二甲基甲酰胺(分析纯),冰乙酸(色谱纯),2,4-D(分析纯),氢氧化钠(优级纯),盐酸(优级纯),甲醇(色谱纯).
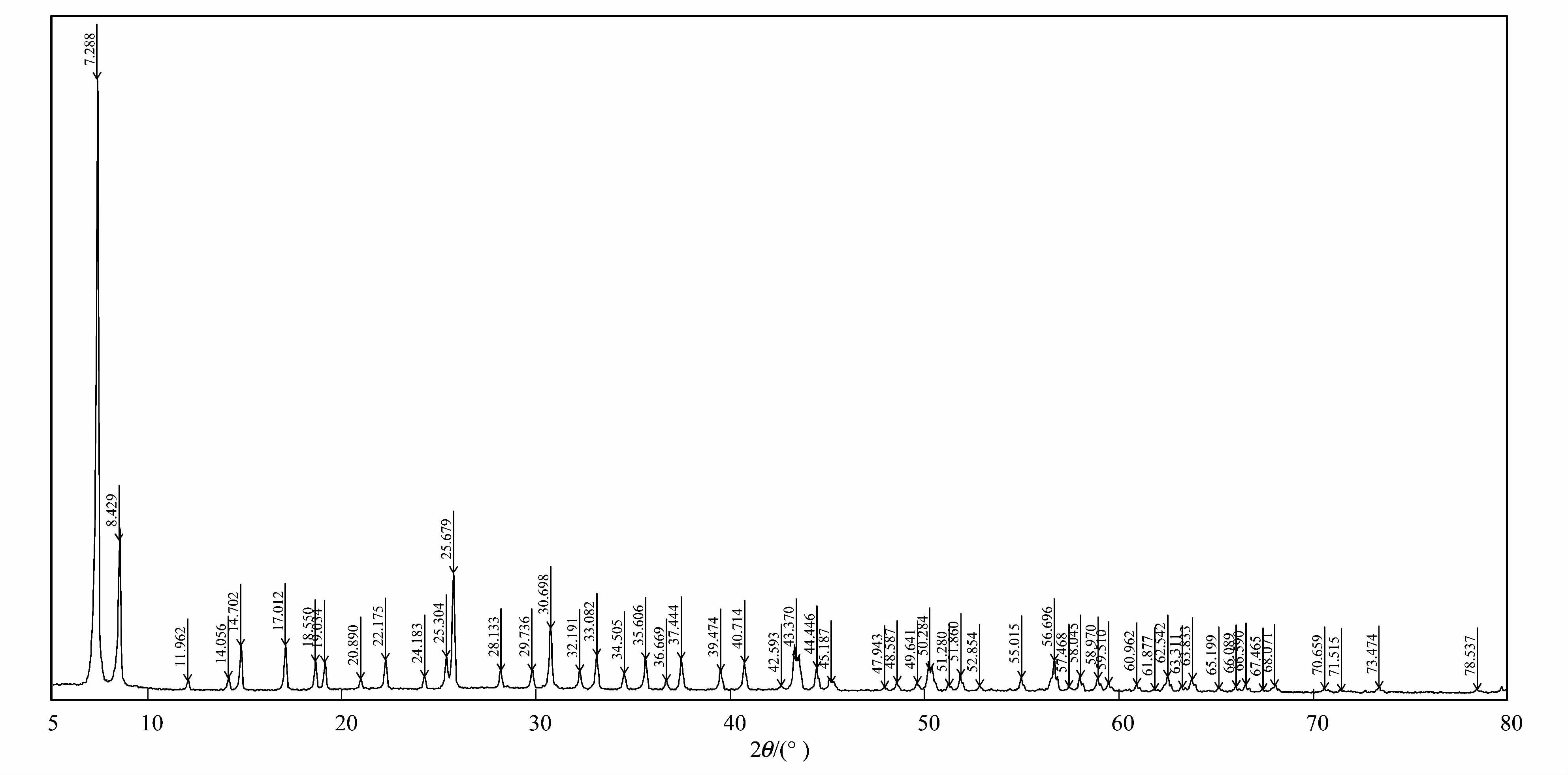
1.3 材料合成及溶液配制 1.3.1 UiO-66的合成与表征UiO-66的合成采用溶剂热法,在100 mL水热反应釜中进行反应. 首先将ZrCl4、 对苯二甲酸、 乙酸以一定物质的量比例(ZrCl4 ∶对苯二甲酸 ∶乙酸=1 ∶1 ∶30)溶解在二甲基甲酰胺(DMF)中,超声助溶. 然后,将水热反应釜盖子拧紧,放入120℃的烘箱中反应24 h. 再以6℃ ·h-1速率降温至室温后取出反应釜,将反应液离心,取上清液,室温干燥,得白色粉末. 之后对合成样品进行溶剂置换: 将干燥后的样品浸泡在甲醇中,每12 h更换一次溶剂,共更换3次. 室温下抽真空24 h后,80℃过夜烘干. 对所制得的样品进行XRD表征,表征结果如图 1.
|
图 1 UiO-66的X射线衍射 Fig. 1 X-ray pattern of UiO-66 |
将图 1与文献[19, 20]中UiO-66的XRD谱图对比可知,所合成的样品在峰位置及强度上均与已有报道基本一致,说明所合成的样品是UiO-66.
1.3.2 2,4-D溶液的配制称取1.0 g 2,4-D粉末,以甲醇溶解,移至50 mL棕色容量瓶定容,配制成浓度为20.0 g ·L-1的2,4-D储备溶液.
1.4 实验方法准确称取一定质量的吸附剂置于反应瓶中,并加入一定浓度的2,4-D溶液后密封,将反应瓶置于水浴振荡器中,按照预设的不同实验参数进行吸附实验; 每隔一定时间,取样2 mL过0.22 μm聚四氟乙烯滤膜,使用高效液相色谱仪测定溶液中2,4-D剩余浓度,计算样品的吸附容量等数据.
1.5 检测方法通过高效液相色谱仪定量测定2,4-D浓度,色谱柱为C-18反相色谱柱,紫外检测波长284 nm. 流动相体积比甲醇 ∶水=90 ∶10,以1.0 mL ·min-1的流速等速淋洗.
以D8 Advance型 X-射线衍射仪对样品进行表征,设定KV=40,MA=40的工作条件,以Cu靶为辐射线源.
以Supra55型扫描电镜对样品进行表征,显微镜的加速电压为0.1-30 kV,放大倍数为5 000和15 000倍,分辨率为1.0 nm.
1.6 吸附等温线Langmuir吸附等温式:
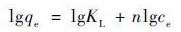
|
(1) |
Freundlich吸附等温式:
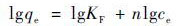
|
(2) |
Temkin吸附等温式:
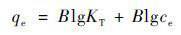
|
(3) |
Dubinin-Radushkevich吸附等温式:
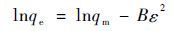
|
(4) |
式中,ce为平衡时溶液浓度(mg ·L-1),qe为平衡时的吸附容量(mg ·g-1),qm为理论饱和吸附容量(mg ·g-1),KF为Freundlich常数,与吸附容量相关,n与吸附强度相关; KL为吸附的平衡常数(L ·mg-1),R是理想气体常数[8.314 J ·(mol ·K)-1]; T是绝对温度(K),qm为理论饱和吸附容量(mol ·g-1),B是表征吸附自由能的吸附常数; ε是Polanyi电位[21].
1.7 吸附动力学拟一级动力学:
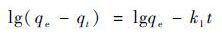
|
(5) |
拟二级动力学:
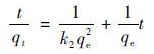
|
(6) |
式中,t为吸附时间,qe为平衡时的吸附容量(mg ·g-1),qt为在反应t时刻吸附剂对吸附质的吸附量(mg ·g-1),k2为拟一级吸附动力学常数[22].
1.8 吸附热力学
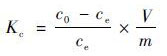
|
(7) |
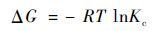
|
(8) |
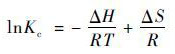
|
(9) |
式中,Kc为固液分配系数; c0为初始溶液浓度(mg ·L-1); ce为平衡时溶液浓度(mg ·L-1); V为溶液体积(mL); m为吸附剂质量(g); T为吸附溶液温度(K); R为理想气体常数[8.314 J ·(mol ·K)-1][23].
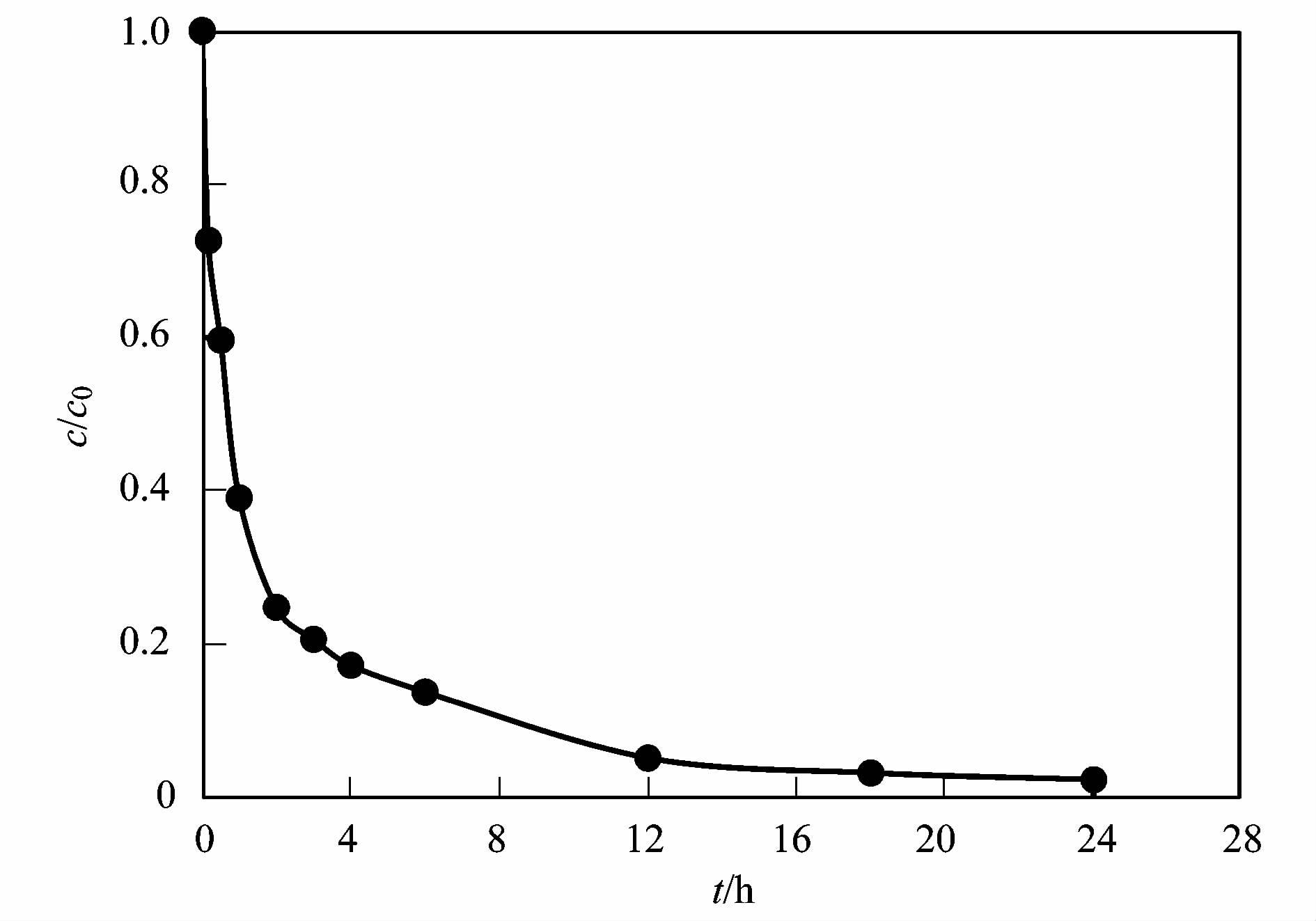
2 结果与分析 2.1 吸附时间对UiO-66吸附性能影响本实验研究了30℃下,0.015 g UiO-66对100 mL 初始浓度为20 mg ·L-1的2,4-D溶液的吸附行为. 图 2是UiO-66在不同时间对2,4-D溶液的吸附结果. 可见,在最初的4 h内吸附速度很快,2,4-D的去除率达到83%,18 h后吸附曲线几乎不发生变化,吸附达到平衡,2,4-D的去除率可达98%.
|
图 2 吸附时间对UiO-66吸附性能影响 Fig. 2 Effect of adsorption time on the adsorption performance of UiO-66 |
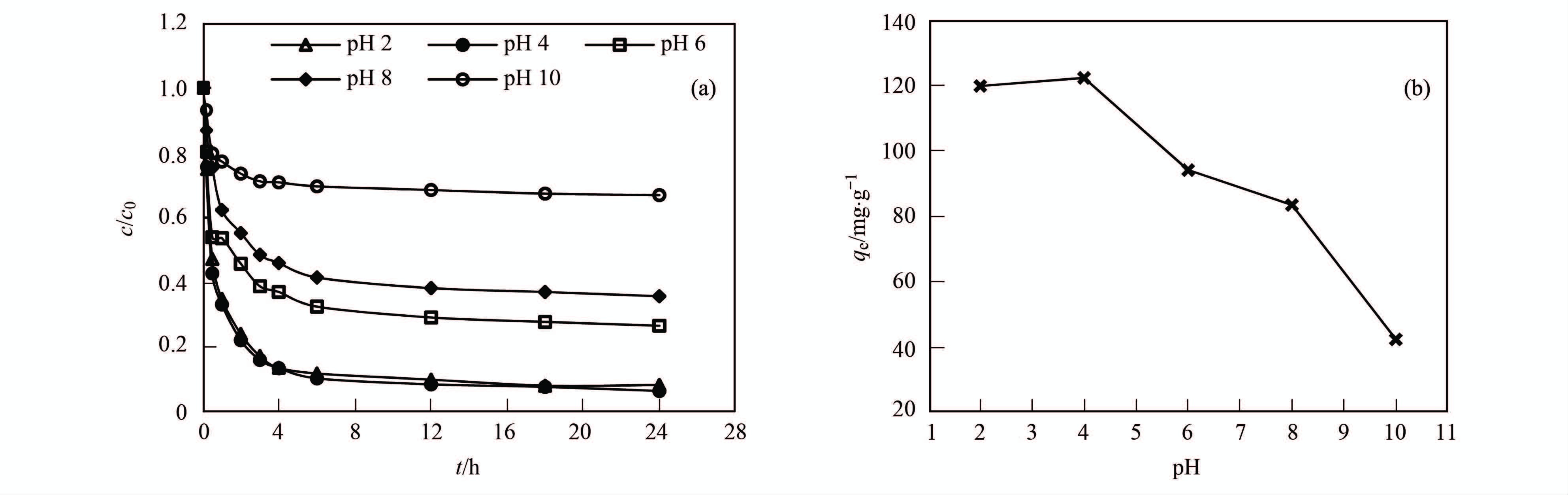
反应液pH值是吸附反应的重要影响因素,本实验研究了在0.15 g ·L-1 UiO-66、 20 mg ·L-1 2,4-D,初始pH值分别为2、 4、 6、 8和10,反应时间24 h,温度30℃条件下,pH值对UiO-66吸附2,4-D的影响,如图 3所示. 从中可以看出,pH值对UiO-66的吸附性能影响很大,当pH值为4.0时吸附效果最好,随着pH的增加,2,4-D的去除效率逐渐下降,反应平衡时UiO-66上的吸附容量也呈明显下降趋势. 当pH值为4,吸附平衡时2,4-D的去除率可达95%,UiO-66上的吸附容量为122.13 mg ·g-1. pH对UiO-66吸附2,4-D性能影响很大. 首先,pH会影响UiO-66的表面性质,一般来说,当pH低于吸附剂的零点电荷时,吸附剂表面会带正电荷,当pH高于吸附剂的零点电荷时,吸附剂表面会带负电荷[25]. 其次,pH会改变2,4-D分子形态的比例,从而影响UiO-66对2,4-D的吸附效果. 有研究表明,2,4-D的pKa值为2.64[23]. 当pH较低时,2,4-D主要以分子态存在; 而随着pH的升高,离子态的2,4-D所占比例逐渐升高,UiO-66对于2,4-D的吸附量降低,同时UiO-66表面聚集的负电荷也阻碍了其对于2,4-D的吸附[26].
|
图 3 pH值对UiO-66吸附性能影响 Fig. 3 Effect of pH on the adsorption performance of UiO-66 |
吸附剂UiO-66浓度为0.15 g ·L-1固定不变,2,4-D溶液初始浓度分别为10、 20、 40、 60和 80 mg ·L-1,初始pH值为4,反应时间为24 h,反应温度分别为10、 20、 30和40℃.
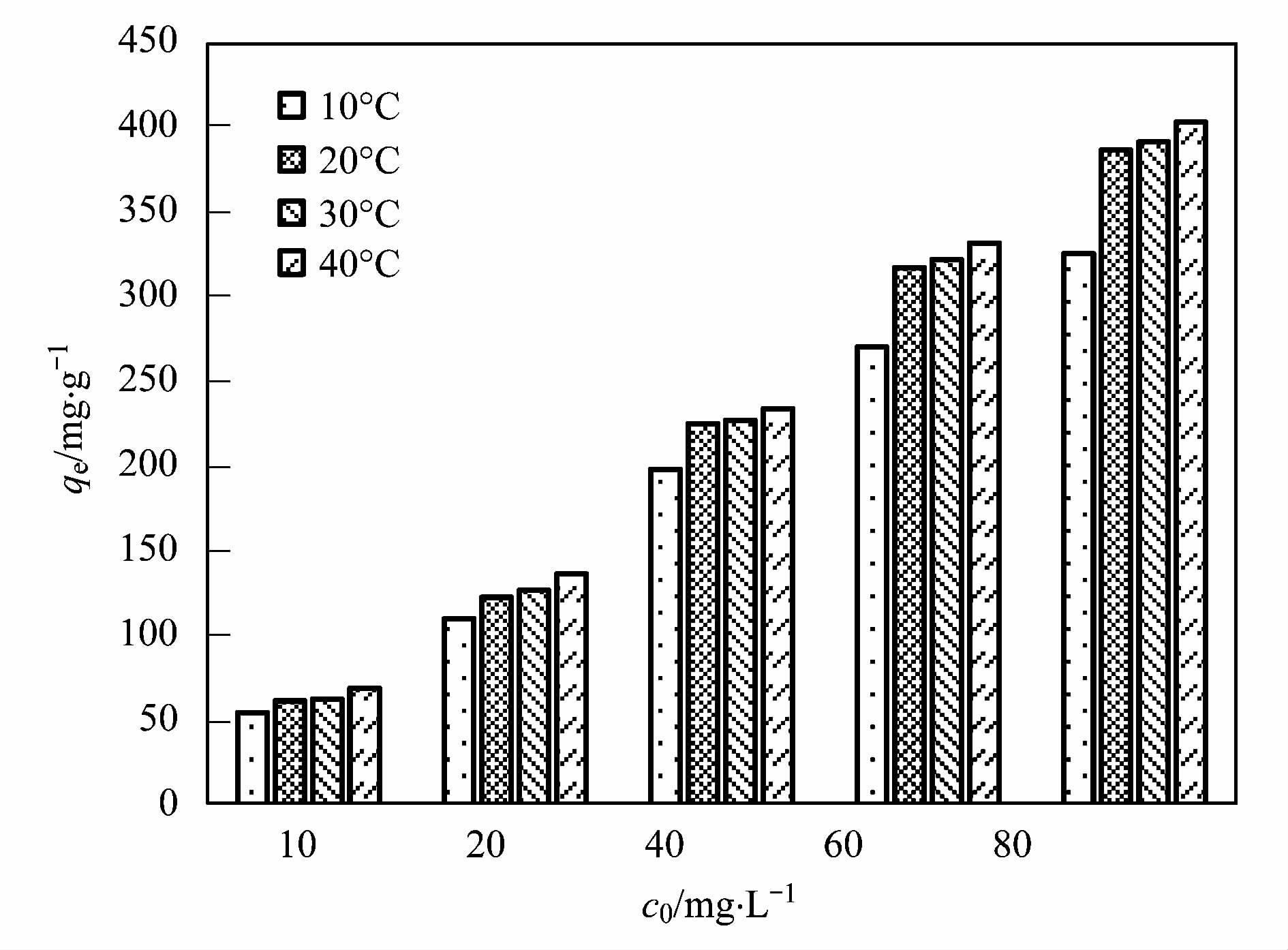
温度对UiO-66吸附不同溶液浓度2,4-D的影响见图 4. 可知,在10-40℃内,对于不同初始浓度的2,4-D,UiO-66上的平衡吸附量均随温度的升高而增加,说明吸附反应为吸热反应,升高温度有利于吸附的进行. 但温度从20℃上升到40℃,吸附量增加不明显,实验最佳温度应控制在30℃. 温度升高加速了分子热运动,从而提高了UiO-66对2,4-D的物理吸附速率,此外,温度升高为反应过程提供了更多的能量,促进了UiO-66表面与有机物之间稳定化学键的形成,从而提高了吸附效果.
|
图 4 温度对UiO-66吸附性能影响 Fig. 4 Effect of temperature on the adsorption performance of UiO-66 |
2,4-D溶液的初始浓度为20 mg ·L-1,初始pH为4.0,反应温度为10、 20、 30、 40℃,吸附剂UiO-66浓度为0.15 g ·L-1,取样时间点设置为10、 30、 60、 120、 180、 240、 360、 720、 1 080、 1 440 min.
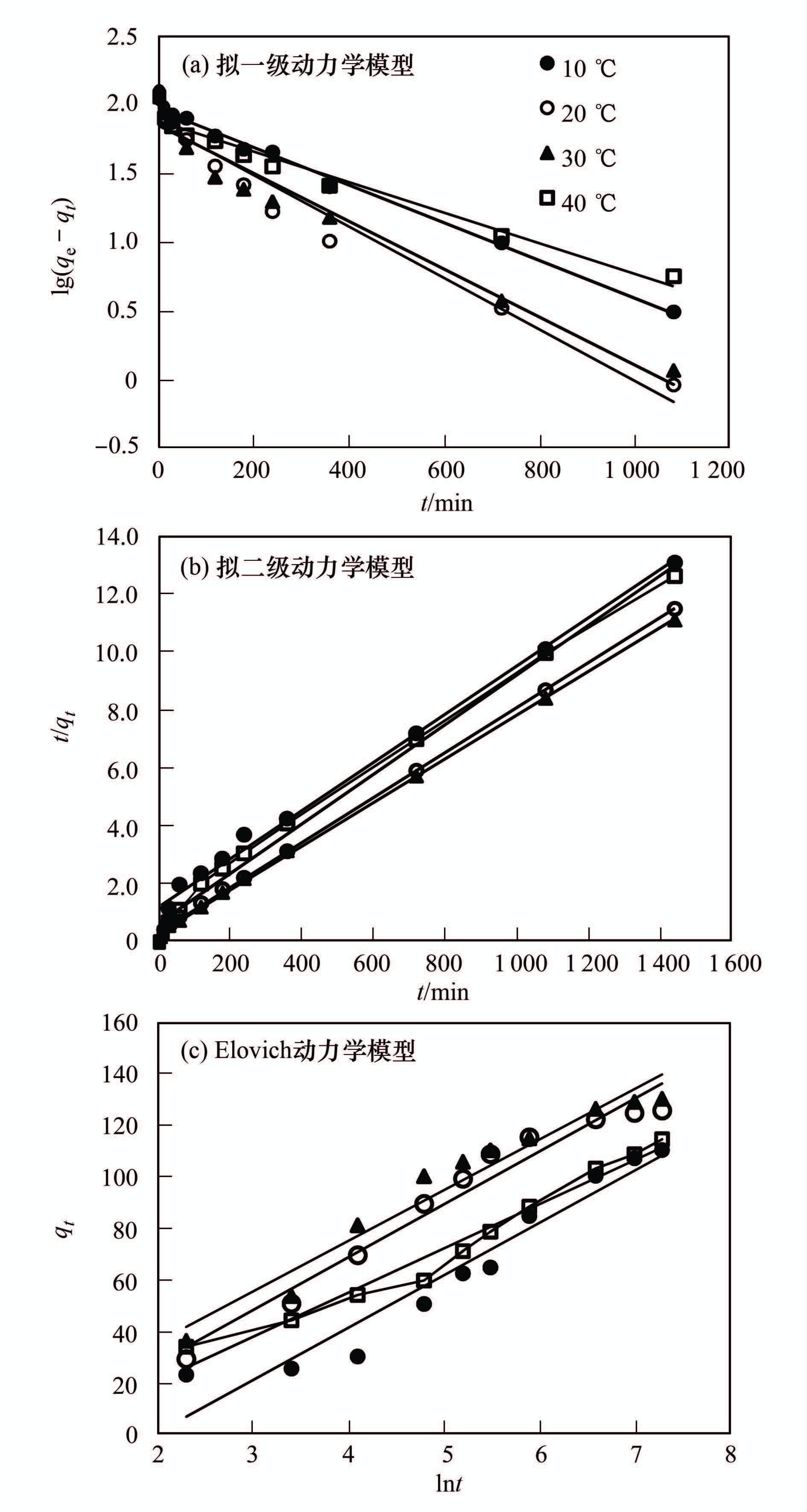
对不同温度下UiO-66吸附2,4-D的实验数据分别以拟一级动力学模型、 拟二级动力学模型和Elovich模型进行拟合,拟合结果如图 5所示.
|
图 5 UiO-66吸附2,4-D动力学拟合曲线 Fig. 5 Kinetics curves of the adsorption of 2,4-D on UiO-66 |
3种动力学模型拟合相关性系数R2均在 0.90以上,其中,拟二级动力学模型的拟合效果最好,相关性系数R2均高于0.99,并且实验测定的吸附量与计算所得最大吸附量非常接近,表明UiO-66吸附2,4-D的过程最符合拟二级动力学.
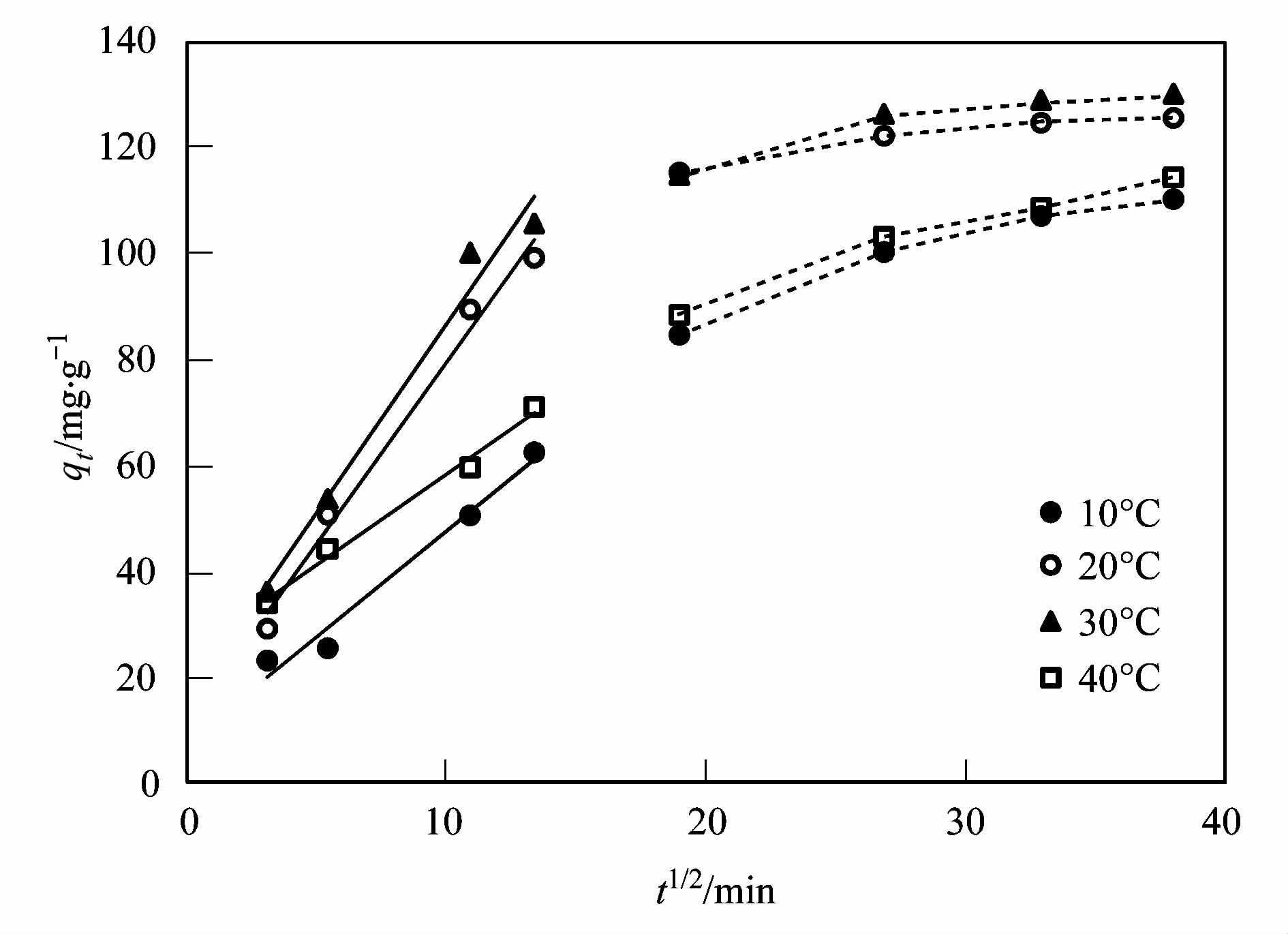
2.5 UiO-66内扩散模型采用Weber-Morris内扩散模型来描述10、 20、 30和40℃下,UiO-66吸附2,4-D的内扩散行为. 内扩散拟合曲线如图 6所示. 从中可以看出,曲线不通过原点,大致可分为两个阶段,第一阶段可认为是膜扩散过程,第二阶段可认为是颗粒内扩散过程,说明在UiO-66吸附2,4-D的过程中,颗粒内扩散过程是吸附速率的控制步骤,但不是唯一的控制步骤,同时还受颗粒外扩散过程(如表面吸附和液膜扩散)的影响. 根据拟合直线的斜率可以求得内扩散速率常数Kip1和 Kip2(分别为第一阶段和第二阶段的速率常数),见表 1,Kip1值比 Kip2值大,说明第一阶段吸附速率比第二阶段快[28~31]. 这是由于吸附初始阶段吸附剂表面有大量的吸附空位,可以使吸附质在较短时间内快速被吸附,随着时间的延长,吸附剂表面 所吸附的吸附质会增大扩散阻力,使得吸附速率变慢. 截距值c代表了吸附剂周围边界层对吸附过程的影响,由拟合参数结果可见,随着温度的升高c值增加,说明温度升高,边界层对吸附的影响变大,并且c2大于c1,表明吸附第二阶段边界层的影响要大于第一阶段.
|
图 6 UiO-66吸附2,4-D内扩散拟合结果 Fig. 6 Internal diffusion fitting results of adsorption of 2,4-D on UiO-66 |
|
|
表 1 UiO-66吸附2,4-D内扩散拟合结果 Table 1 Internal diffusion fitting results of adsorption of 2,4-D on UiO-66 |
2.6 UiO-66等温吸附性能
当吸附剂UiO-66浓度为0.15 g ·L-1,2,4-D反应液初始浓度分别为5、 10、 20、 40、 60、 80和100 mg ·L-1,初始pH 为4.0时,对不同温度(10、 20、 30和40℃)下UiO-66对2,4-D的等温吸附过程进行研究,为更好地说明吸附剂和吸附反应的特性,吸附实验数据以线性Langmuir、 Freundlich、 Tempkin和Dubinin-Radushkevich等温吸附模型进行拟合.
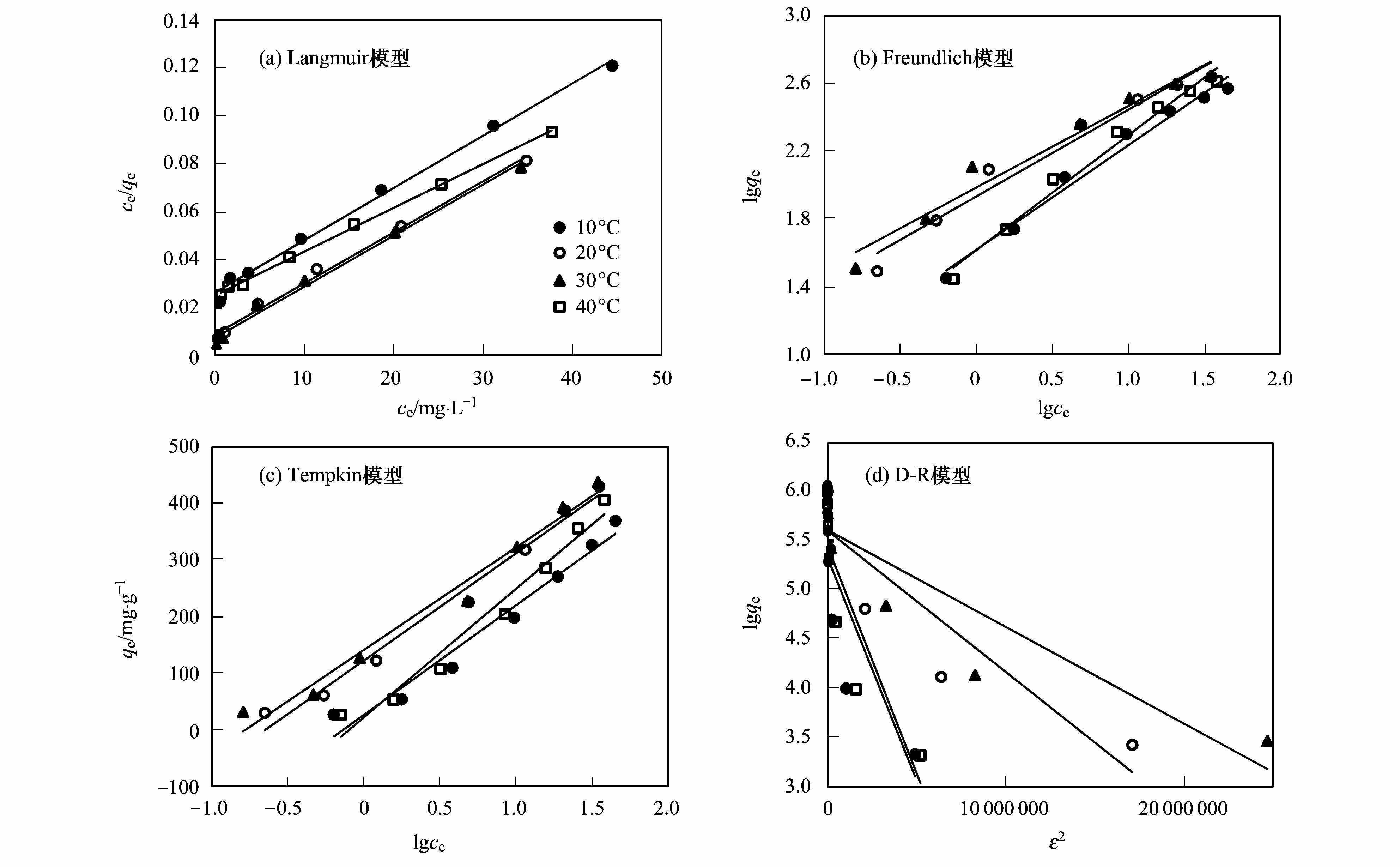
对4个温度下UiO-66对2,4-D等温数据进行模型拟合,如图 7所示,模型拟合参数见表 2. 从中可以看出,Langmuir等温吸附模型在不同温度下拟合的相关性系数R2值均大于0.99,高于其他3种模型. 对Langmuir模型进行显著性检验,所得P值远小于0.05,故以Langmuir等温吸附模型对吸附效果进行模拟是具有统计学意义的. 一般认为n小于1有利于吸附,从表 2中可以看出UiO-66对于2,4-D的吸附过程容易发生[32]. 吸附过程符合Langmuir等温吸附模型,对于样品吸附前后的形貌差异,本研究通过扫描电镜在不同的放大倍数下进行观测. 从图 8中可以看出,UiO-66样品在吸附2,4-D前后形貌较为规则,大部分呈球状,粒径分布较大; 吸附后,样品颗粒有少许聚集变大,且吸附剂表面粗超程度变大,其他形貌特征并无差异. 表明吸附发生在吸附剂表面,吸附质在吸附剂表面形成单分子层吸附,同时吸附质彼此间也不发生相互作用.
|
|
表 2 UiO-66 吸附2,4-D的4种等温吸附模型拟合参数 Table 2 Fitting parameters for four kinds of isothermal adsorption models of adsorption of 2,4-D on UiO-66 |
|
图 7 UiO-66吸附2,4-D等温吸附模型拟合曲线 Fig. 7 Fitting curves of isothermal adsorption models for adsorption of 2,4-D on UiO-66 |

|
图 8 UiO-66吸附2,4-D前后的SEM图 Fig. 8 SEM patterns of UiO-66 before and after the adsorption of 2,4-D |
不同温度下,计算的RL值均在0-1.0 之间,表明UiO-66对2,4-D的吸附是容易进行的[33]. 当温度为10、 20、 30和40℃时,实验所得平衡吸附容量值为368.134、 428.855、 435.769和 404.565 mg ·g-1,以Langmuir等温吸附模型拟合出的最大吸附容量qm为 454.545、 476.190、 476.190和555.560 mg ·g-1,与实验值所得平衡吸附容量接近.
2.7 UiO-66吸附热力学2,4-D溶液的初始浓度为20 mg ·L-1,初始pH为4.0,反应温度为10、 20、 30℃,称取0.015 0 g UiO-66,反应时间24 h,待吸附平衡取样测2,4-D溶液平衡浓度.
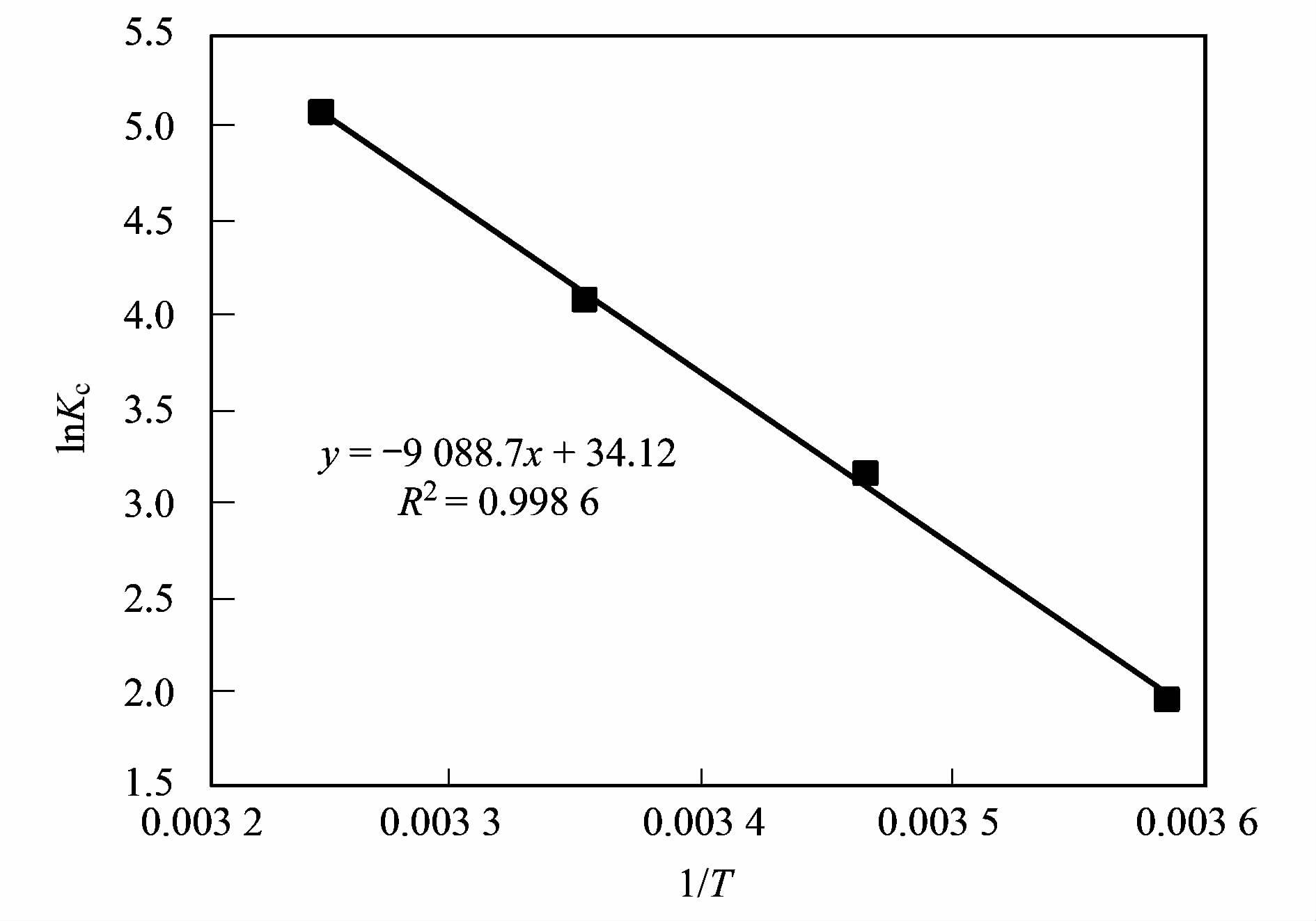
考察了10、 20和30℃下UiO-66对2,4-D的吸附热力学行为. 以lnKc对1/T作图,热力学计算曲线如图 9所示,热力学参数计算结果如表 3所示. 可见,ΔG<0,说明吸附反应是自发的,且随着温度的升高,ΔG绝对值增大,表明升高温度易于吸附进行. ΔH>0,说明UiO-66对2,4-D的吸附是吸热反应,其绝对值大于20.9 kJ ·mol-1,可以推断吸附以化学吸附为主. ΔS>0,说明UiO-66吸附2,4-D的过程中,无序度增大. 在本研究中2,4-D溶液是一个以水为溶剂的溶液,2,4-D分子体积远大于水,这样在2,4-D分子吸附的同时会有大量的水分子脱附,结果水分子解吸引起的熵增加远大于2,4-D分子吸附引起的熵减小,因此导致ΔS>0[34, 35].
|
图 9 UiO-66吸附2,4-D热力学拟合曲线 Fig. 9 Thermodynamic curve for adsorption of 2,4-D on UiO-66 |
|
|
表 3 UiO-66吸附2,4-D热力学参数 Table 3 Thermodynamic parameters of adsorption of 2,4-D on UiO-66 |
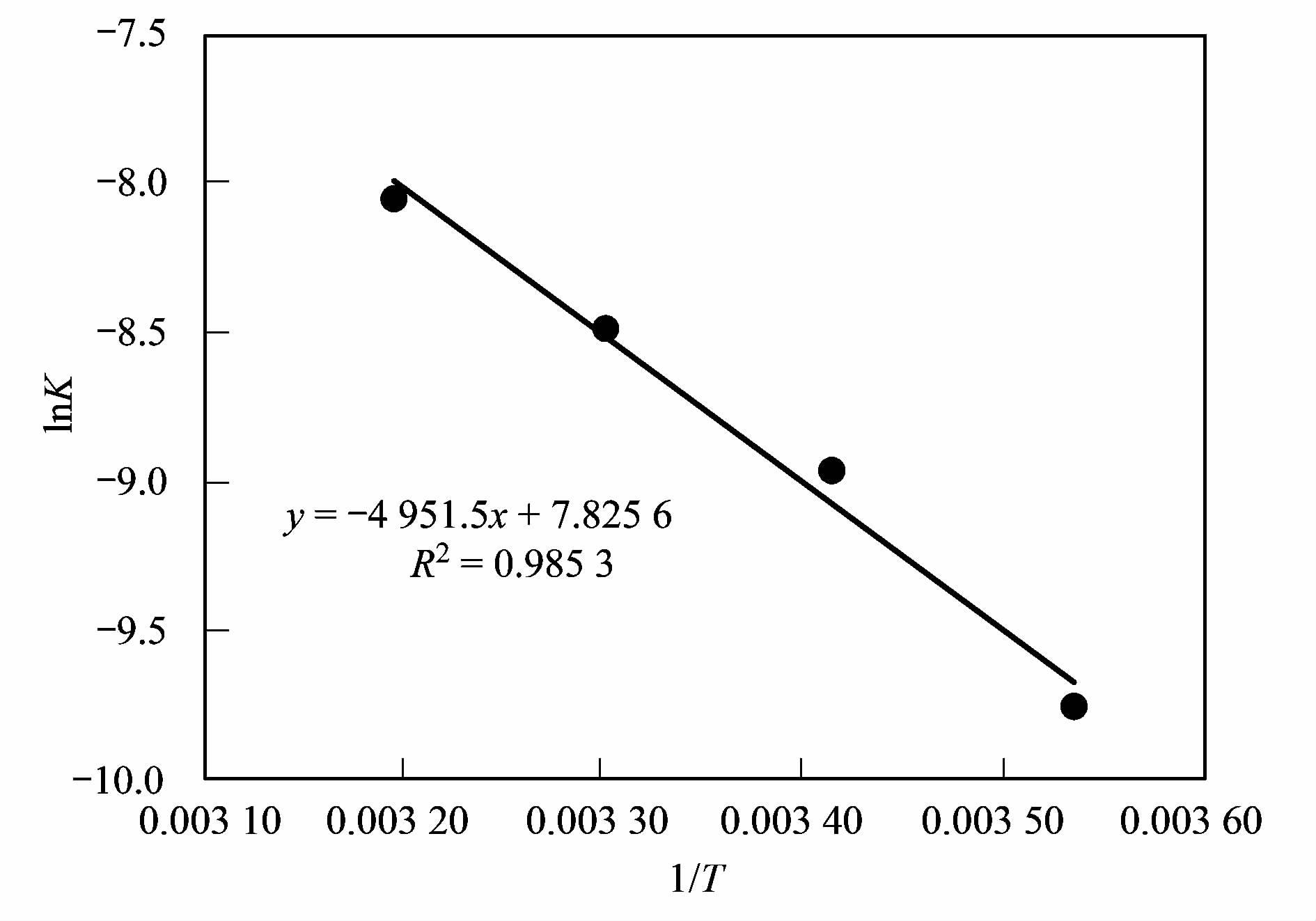
根据阿伦尼乌斯公式,对10、 20和30℃下吸附数据进行处理,以lnK对1/T作图,结果如图 10,通过直线公式的斜率求得UiO-66对2,4-D的吸附活化能为41.17 kJ ·mol-1. 故UiO-66对2,4-D的吸附以化学吸附为主.
|
图 10 UiO-66吸附2,4-D阿伦尼乌斯方程拟合结果 Fig. 10 Fitting result of Arrhenius equation for adsorption of 2,4-D on UiO-66 |
一般来说,吸附质与吸附剂间的作用可以用以下4种机制来解释: 范德华力、 化学键力、 氢键力、 疏水键力、 配位基交换和偶极间力等作用,可根据不同吸附热判断作用力类型,各种作用力的吸附热数据如表 4所示; 吸附剂表面含氧基团与吸附质之间发生的电子供体-受体作用; 吸附质和吸附剂的静电引力和斥力作用; 石墨结构的离域π电子与吸附质之间发生的π-π色散作用[36].
|
|
表 4 各种作用力引起的吸附热 /kJ ·mol-1 Table 4 Adsorption heat caused by different interactions/kJ ·mol-1 |
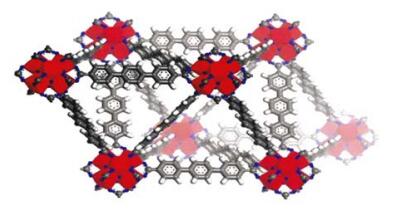
图 11中这种结合一共包含了8个无机Zr4+金属单元. UiO-66是晶态的,由一个六元锆金属簇Zr6O4(OH)4与12个配体配位而成,在三维空间网状结构当中,一个中心八面体笼与8个四面体笼通过面面相接,并形成三角形的窗口[24].
|
图 11 一个八面体笼与两个相邻的四面体笼相结合 [24] Fig. 11 Combination of one octahedral cage and two adjacent tetrahedral cages form a cubic unit consisting of eight inorganic bricks |
由于UiO-66中金属离子具有不饱和配位点,故可发生吸附作用; 此外,其规则的网状结构也为吸附提供了依据[37, 38]. 根据UiO-66的性质、 吸附过程中影响因素的分析可推断UiO-66对2,4-D的吸附机制如下.
(1)化学键力作用 吸附热力学计算得出吸附焓为75.57 kJ ·mol-1,可推断在本吸附体系中化学键力为吸附过程主要作用力. 吸附活化能研究也表明,UiO-66对2,4-D的吸附以化学吸附为主,则吸附过程中必存在化学键力作用.
(2)静电力作用 根据吸附过程中pH值的影响分析,可以判定在UiO-66吸附2,4-D的过程中存在静电力作用.
3 结论(1)自制UiO-66对水中2,4-D吸附有很好的吸附性能. 平衡时(24h)2,4-D的去除率可达98%; 吸附溶液最佳pH值为4,UiO-66上的吸附容量为122.13 mg ·g-1; UiO-66上的平衡吸附量均随温度的升高而增加,说明吸附过程为吸热反应,升高温度有利于吸附进行,但温度从20℃上升到40℃,吸附量增加不明显,实验最佳温度应控制在30℃.
(2)采用Langmuir、 Freundlich、 Tempkin 及Dubinin-Radushkevich 吸附等温模型对不同温度条件下的等温吸附数据进行拟合. 可知,Langmuir吸附等温模型可以较好地描述UiO-66对2,4-D的吸附行为; 不同温度下UiO-66对2,4-D的吸附行为均遵循拟二级动力学规律; 颗粒内扩散过程是吸附速率的控制步骤,吸附过程同时还受颗粒外扩散过程的影响; 热力学研究表明,UiO-66对2,4-D的吸附是自发的、 吸热的、 熵增加的化学吸附过程. UiO-66对2,4-D的吸附机制为: 化学键力作用和静电力作用.
 2016, Vol. 37
2016, Vol. 37


