2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environmental Science and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
剩余污泥作为污水处理厂生物处理的主要副产物,其进一步处理费用已占整个污水处理厂运行成本的25%~65%[1].因此,剩余污泥的处理与处置成为污水处理厂面临的非常棘手的难题[2].然而,剩余污泥中含有丰富的有机质[3],不但可以作为生物产甲烷、产氢等能源与底物[2],还可以用于微生物培养、堆肥的原料[4],人们已经逐渐意识到剩余污泥的重要经济价值,相关研究和应用也开展起来[5].
微生物燃料电池(MFC)是一种新型的生物电化学系统,能够利用微生物作为催化剂将存储在有机物中的化学能以电能形式回收[6].MFC不仅可利用单一碳水化合物(如葡萄糖、醋酸盐、丁酸盐等)作为燃料发电,而且能利用废水(如养殖废水、生活污水、啤酒废水、淀粉加工废水、造纸废水等)、废物中的复杂有机物回收电能.以剩余污泥作为MFC的燃料,是剩余污泥资源化利用的又一种新形式,既处理了污泥,又能将污泥中丰富的有机质转化为电能,从而实现污泥的稳定化、减量化与资源化利用,对于解决污泥处理过程中高能耗等问题具有重要意义.目前,基于MFC的剩余污泥资源化利用研究,包括直接方式与间接方式,其中直接利用剩余污泥的方式即直接以剩余污泥为底物,不进行预处理;而间接方式则需要进行必要的预处理,以提高污泥的可生化性.由于污泥中的蛋白质、还原性糖和可溶性化学需氧量(SCOD)浓度较低,生化性能较差,直接以污泥为底物时,MFC输出功率密度较低,为了改善MFC产电性能,一般需对剩余污泥进行必要的预处理,如热处理、酶处理以及酸碱处理等[7].
对于MFC产电性能的研究,多局限于对其功率密度的提升.而在实际应用中,对一些小型用电器,如LED照明导航、无线传感器[8]、充电电池[9]及电容器[10]等进行供电时,由于环境条件复杂多变,即使有电能存贮设备,也需要MFC具有不连续供电的能力[11],在电压变化或供电开闭时,需要MFC能够快速恢复供电.可见,探讨MFC不连续供电性能具有重要的现实意义.
在此背景下,本研究分析MFC以预处理剩余污泥为燃料产电的可行性;同时通过开闭电路和变换不同电子受体改变电势,探讨MFC产电性能对输出电压变化的响应,以期为MFC实现不连续供电提供依据.
1 材料与方法 1.1 反应器装置采用双室MFC,两极室有效容积均为165 mL,装置如图 1.两极室间以质子交换膜(Nafion 117,Dupont,美国)隔开,质子交换膜的有效面积为40 cm2.阳极材料为碳布(6.5 cm×10 cm),阴极材料为石墨碳板(5.0 cm×7.5 cm),浸入1×PBS溶液(50mmol·L-1,pH 7.0)或铁氰化钾溶液中.电极以钛丝作为连接导线,外接1 000 Ω电阻,电阻两端接电势数据采集卡(PISO-813型,台湾宏格),对电压进行在线记录.
 | 图 1 MFC实验装置示意 Fig. 1 MFC bioreactors used in this study |
MFC底物为经过预处理的污水处理厂剩余污泥上清液.本研究采用加热处理方式对污泥进行预处理,以增强污泥的生物可利用性,提高污泥降解效果[12].预处理方法如下:取适量污泥置于100℃水浴中处理1 h,然后离心获取上清液备用,未经处理的剩余污泥以及预处理过的剩余污泥理化特性如表 1.
| 表 1 阳极室所用原污泥及污泥经热处理后上清液理化性质1) Table 1 Characteristics of excess sludge used in the anode chamber and supernatant of thermal pretreated excess sludge |
MFC接种污泥取自青岛市李村河污水处理厂好氧曝气池,污泥TSS为10.43g·L-1,将其在室温厌氧驯化一周以富集产电微生物.MFC启动和运行均采用批式方式进行.取污泥10 mL接入阳极室,加满终浓度为1 000 mg·L-1(COD)的预处理剩余污泥,同时加入2 mL·L-1微量元素、200 μL·L-1氨基酸、200 μL·L-1维生素[13].在MFC启动初期,每隔2 d更换一次阳极液,待启动成功后,反应器电压降到0.1 V时,即更换新鲜阳极液.在MFC启动过程中,阴极室为1×PBS磷酸盐缓冲溶液,并持续曝气.整个实验在25℃条件下进行.
1.3 改变MFC的输出电势当MFC启动成功且输出电压稳定后,将阴极液由1×PBS缓冲溶液换为30mmol·L-1铁氰化钾.为探讨MFC能否不连续供电,将反应器分为两组,每组设置两个平行.第一组反应器阴极室溶液依次为30mmol·L-1铁氰化钾、1×PBS缓冲溶液(曝氧气)、30mmol·L-1铁氰化钾,3个阶段分别标记为Pb1、Pb2、Pb3.第二组反应器阴极室溶液均为30mmol·L-1铁氰化钾,在反应器运行过程中,电路分别转换为闭路、开路及闭路状态,3个阶段分别标记为Op1、Op2、Op3.
1.4 化学及电化学参数分析进出水COD采用重铬酸钾(K2Cr2O7)氧化法测定;进出水氨氮采用纳氏试剂比色法测定[14].功率密度曲线、极化曲线等电化学参数均按文献[15]中的方法,以在线获得的电压为基础进行分析.伏安特性曲线采用LK2005B 电化学工作站(兰力科化学电子,天津)进行测试,循环变化的电压施加于工作电极和参比电极之间,采用三电极体系:阳极为工作电极,甘汞电极为参比电极,阴极为对电极.
2 结果与分析 2.1 MFC的启动以热处理的剩余污泥上清液为基质,两组MFC启动阶段输出电压随时间变化如图 2.启动过程中,电池输出电压稳定上升,启动第148 h,两组MFC电压均达到0.18 V;在第290 h时,两组MFC最大电压均达到0.24 V左右,重现性较好,电压稳定输出3个周期,表明系统已成功启动.
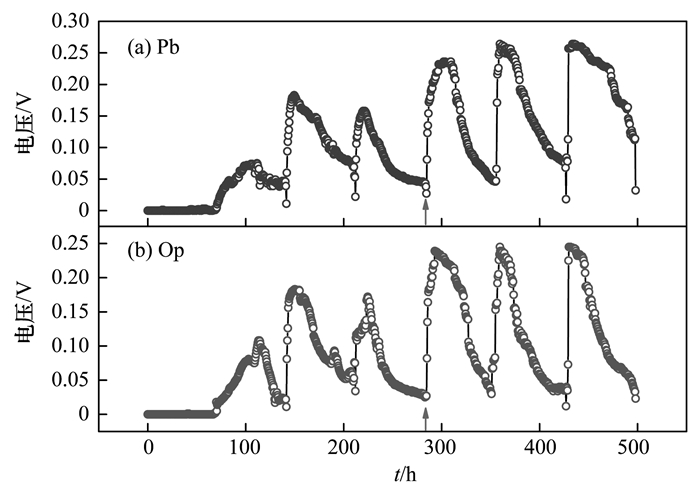 | 图 2 两组MFC以热处理污泥上清液为底物启动 Fig. 2 Startup of two groups of MFCs feeding with supernatant of thermal pretreated excess sludge |
MFC启动成功后,在扫描速度1 mV·s-1,-0.60~0 V范围内5次循环条件下绘制伏安曲线(图 3). MFC启动成功后的循环伏安曲线没有明显的氧化还原峰,表明MFC在整个循环伏安测试过程中均以恒定速度进行充放电,电池性能较为稳定.
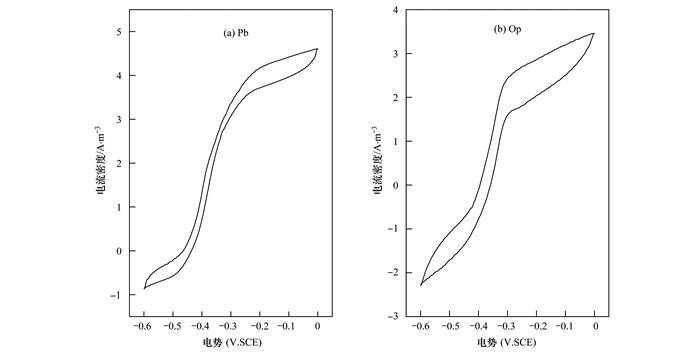 | 图 3 MFC启动成功后的循环伏安特性曲线 Fig. 3 Cyclic voltammogram scanning after MFC startup |
MFC阴极室电子受体经铁氰化钾/氧气/铁氰化钾这3个阶段的变换,MFC输出电压随时间变化如图 4中的Pb所示. Pb1输出电压在0.60~0.70 V之间,阴极电子受体换为O2时,Pb2输出电压降到0.30~0.40 V之间,最后再次将阴极电子受体换回铁氰化钾时,Pb3最大输出电压亦快速恢复到同Pb1阶段. Op1~Op3阴极液均为铁氰化钾,电池电路经闭路、开路、
 | 图 4 阴极电子受体短暂变化对MFC输出电压的影响 Fig. 4 Effect of transient changes of cathode electron acceptor on the output voltage of MFC |
闭路模式转换,MFC的输出电压及开路电势如图 4中的Op. Op1闭路状态输出电压在0.60~0.70 V之间,电路断开时,Op2的开路电势最大在0.8 V,当电路再次变为闭路时,Op3最大输出电压亦快速恢复到同Op1阶段.
2.2.2 MFC功率密度、极化曲线电子受体变化前后的功率密度曲线如图 5.Pb1、Pb2和Pb3阶段时,MFC的功率密度达到最大值分别为1.86、1.94和4.21W·m-3. 可见,Pb实验组功率密度随电子受体变化前、中、后呈逐渐上升趋势,可能阴极室由铁氰化钾换为缓冲溶液时对质子交换膜有冲洗作用,增大了质子交换膜传质效率,再次变为铁氰化钾后功率密度继续增大,这与Oh等[16]发现使用铁氰化物代替氧气作为电子受体,将MFC功率提高1.5~1.8倍的结果一致.
 | 图 5 电子受体短暂变化各阶段的功率密度与极化曲线 Fig. 5 Power density and polarization curves during electron acceptor transient changes |
Op1、Op2和Op3阶段MFC的功率密度最大值分别为1.91、5.37以及3.90W·m-3,该实验组MFC功率密度随电子受体变化呈现先升后降的趋势. 在Op2阶段,阴极电子受体从无到有的瞬间,其最大功率密度最大,但该值为开路电压下的获得,并非MFC实际运行能够产生的功率密度.
2.2.3 MFC对COD和氨氮的去除选择Pb、Op实验组每个阶段一个周期,测定MFC阳极室中COD和氨氮剩余浓度,结果如图 6.阳极液的COD初始浓度为(1 000±200)mg·L-1;氨氮浓度为(200±50)mg·L-1.COD和氨氮的剩余浓度在电子受体变化时呈逐渐下降趋势,但每阶段浓度变化波动较小,COD最大可获得70%的去除率,氨氮最大去除率为80%.可见,MFC对有机物去除效果不受阴极电子受体短暂变化的影响.
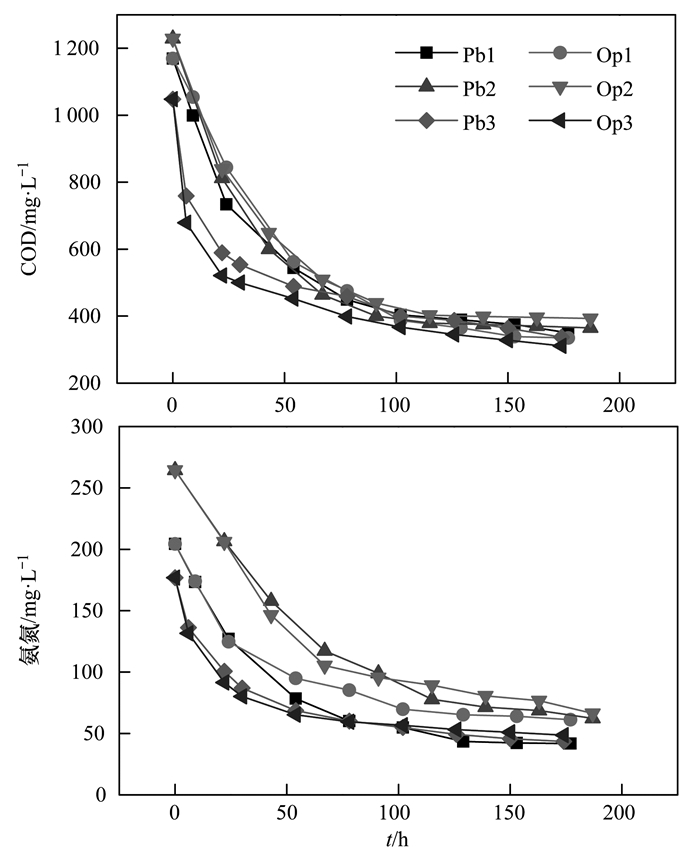 | 图 6 MFC电子受体变化各阶段COD和氨氮的剩余浓度变化 Fig. 6 Variation of residual COD and ammonia nitrogen in MFC during electron acceptor transient changes |
本研究结果表明,以剩余污泥热处理上清液为基质,MFC可以获得稳定的输出电压,当以铁氰化钾为阴极电子受体时可获得0.66 V的最高输出电压、4.21 W·m-3的最大功率密度(图 4),均优于目前以单一简单有机物为底物的MFC报道.在他们的研究中,当以葡萄糖[17]、乙酸钠或淀粉[18]为底物时,获得的MFC最大功率密度分别为400、36.03和6.32 mW·m-3.同以复杂有机物为底物的MFC相比,本研究的结果也有一定的优势,例如Huang等[19]应用MFC处理造纸废水时,其最大输出电压和最大功率密度分别达0.42 V和0.675W·m-3.在Feng等[20]研究中,以啤酒废水为底物时能获得5.1W·m-3的最大功率密度,可能与其底物的生物可利用性好、反应器运行温度高有关.可见,无论是简单的有机物,还是复杂有机物,底物种类不同,MFC产电性能差异较大,但本研究以剩余污泥热处理上清液为基质,输出电压和功率密度均不低于已有报道.究其原因,可能是剩余污泥经过热预处理,破坏了污泥中微生物的细胞壁,促使胞内有机质溶出,从而使基质中蛋白质、还原性糖和SCOD浓度增大.碳源越丰富,可生化性则越强,越有利于MFC阳极微生物的厌氧发酵[21].
3.2 MFC可以实现不连续供电如果将MFC用于小型仪器设备的实际供电,其必须具有不连续供电的能力,不仅需要切换高低电压,还需要适应开关电路.一般情况下,阳极最大电势取决于底物的氧化还原电位,本研究由于底物不变,阳极最大电势保持一定值[22],所以如从阳极底物入手,研究MFC不连续供电的可行性,其输出电压不易控制.另一方面,由于阴极电子受体能够克服阴极电位损失,阴极最终电子受体的还原电位在很大程度上影响电池输出电压[23, 24],因此从阴极电子受体角度入手研究MFC是否能实现不连续供电更为合适.
由于铁氰化钾在水中较好的溶解性,增加了其传质效率,铁氰化钾作为阴极电子受体的最大优势在于其具有超低过电势,使得MFC阴极工作电压接近开路电压;而O2在水中的低溶解度,限制了其阴极电位,因此以铁氰化钾为阴极电子受体的电池要比以O2为阴极电子受体的电池的输出电压高[16, 25].本研究通过反复切换铁氰化钾和O2两种阴极电子受体,发现MFC的输出电压在阴极电子受体为O2时较低,一旦阴极电子受体转换为铁氰化钾后,电压亦快速恢复.由此说明MFC产电微生物群落稳定,不会随着阴极受体的变化而发生较大波动,MFC可以输出不同电压,能够适应用电器功率的波动.
在线监测开闭路电压发现,由闭路转为开路时,开路电压呈规律性周期变化;当再次换为闭路时,MFC输出电压能够快速恢复到切换电路前的电压和功率. Sevda等[11]分别以醋酸盐、葡萄糖人工废水以及高浓度的工业废水为基质,利用单室空气阴极MFC,监测电路从闭路变为开路,再变回闭路的阴阳极电位的变化,结果发现电压在10~20 min内就能恢复到初始状态,其研究也支持本实验中电压随电路变化迅速恢复的结果.当MFC电路断开时,电子不能由阳极传递到阴极,导致阳极微生物不能利用阳极作为外部电子受体,但阳极表面已经形成了极其稳定的电活性生物膜[26];因此,当电路恢复到闭路时,生物膜的产电活性亦能快速恢复.
4 结论(1)利用双室MFC,以热处理的剩余污泥上清液为基质,MFC可快速启动,获得0.66 V的最大电压及4.21W·m-3的最大功率密度,反应器产电性能良好,MFC以预处理剩余污泥为燃料产电具有可行性.
(2)短时间内改变阴极电子受体或开闭电路,MFC对有机物的去除效果基本不受影响,输出电压响应比较迅速,MFC可应用于实际电路的不连续供电.
| [1] | Liu Y. Chemically reduced excess sludge production in the activated sludge process[J]. Chemosphere, 2003, 50 (1): 1-7. |
| [2] | Xiao B Y, Yang F, Liu J X. Evaluation of electricity production from alkaline pretreated sludge using two-chamber microbial fuel cell[J]. Journal of Hazardous Materials, 2013, 254-255 : 57-63. |
| [3] | Wilson C A, Novak J T. Hydrolysis of macromolecular components of primary and secondary wastewater sludge by thermal hydrolytic pretreatment[J]. Water Research, 2009, 43 (18): 4489-4498. |
| [4] | Xiao B Y, Yang F, Liu J X. Enhancing simultaneous electricity production and reduction of sewage sludge in two-chamber MFC by aerobic sludge digestion and sludge pretreatments[J]. Journal of Hazardous Materials, 2011, 189 (1-2): 444-449. |
| [5] | Tyagi V K, Lo S L. Sludge: A waste or renewable source for energy and resources recovery?[J]. Renewable and Sustainable Energy Reviews, 2013, 25 : 708-728. |
| [6] | Logan B E, Hamelers H, Rozendal R, et al. Microbial fuel cells methodology and technology[J]. Environmental Science & Technology, 2006, 40 (17): 5181-5192. |
| [7] | 沈春花, 曾庆玲, 郭义海. 以微生物燃料电池技术资源化利用剩余污泥的研究进展[J]. 化工进展, 2011, 30 (9): 2075-2079. |
| [8] | Donovan C, Dewan A, Heo D, et al. Batteryless, wireless sensor powered by a sediment microbial fuel cell[J]. Environmental Science & Technology, 2008, 42 (22): 8591-8596. |
| [9] | Tender L M, Gray S A, Groveman E, et al. The first demonstration of a microbial fuel cell as a viable power supply: Powering a meteorological buoy[J]. Journal of Power Sources, 2008, 179 (2): 571-575. |
| [10] | Hatzell M C, Kim Y, Logan B E. Powering microbial electrolysis cells by capacitor circuits charged using microbial fuel cell[J]. Journal of Power Sources, 2013, 229 : 198-202. |
| [11] | Sevda S, Dominguez-Benetton X, De Wever H, et al. Evaluation and enhanced operational performance of microbial fuel cells under alternating anodic open circuit and closed circuit modes with different substrates[J]. Biochemical Engineering Journal, 2014, 90 : 294-300. |
| [12] | Climent M, Ferrer I, Baeza M D M, et al. Effects of thermal and mechanical pretreatments of secondary sludge on biogas production under thermophilic conditions[J]. Chemical Engineering Journal, 2007, 133 (1-3): 335-342. |
| [13] | 尹亚琳, 高崇洋, 赵阳国, 等. 好氧-厌氧混合污泥启动微生物燃料电池产电性能及微生物群落动态特征[J]. 微生物学报, 2014, 54 (12): 1471-1480. |
| [14] | 国家环境保护总局. 水和废水监测分析方法[M].(第四版). 北京: 中国环境科学出版社, 2002. 354-359. |
| [15] | Zhu X P, Yates M D, Hatzell M C, et al. Microbial community composition is unaffected by anode potential[J]. Environmental Science & Technology, 2014, 48 (2): 1352-1358. |
| [16] | Oh S E, Logan B E. Proton exchange membrane and electrode surface areas as factors that affect power generation in microbial fuel cells[J]. Applied Microbiology and Biotechnology, 2006, 70 (2): 162-169. |
| [17] | 孔晓英, 李连华, 李颖, 等. 葡萄糖浓度对微生物燃料电池产电性能的影响[J]. 太阳能学报, 2013, 34 (2): 349-352. |
| [18] | 易丹, 陶虎春, 李兆飞, 等. 双室微生物燃料电池利用乙酸钠和淀粉产电研究[J]. 环境科学研究, 2008, 21 (3): 141-145. |
| [19] | Huang L P, Logan B E. Electricity generation and treatment of paper recycling wastewater using a microbial fuel cell[J]. Applied Microbiology and Biotechnology, 2008, 80 (2): 349-355. |
| [20] | Feng Y J, Wang X, Logan B E, et al. Brewery wastewater treatment using air-cathode microbial fuel cells[J]. Applied Microbiology and Biotechnology, 2008, 78 (5): 873-880. |
| [21] | Kim D, Lee K, Park K Y. Enhancement of biogas production from anaerobic digestion of waste activated sludge by hydrothermal pre-treatment[J]. International Biodeterioration & Biodegradation, 2015, 101 : 42-46. |
| [22] | 卜文辰, 蔡昌凤. 微生物燃料电池阴极电子受体研究进展[J]. 应用化工, 2013, 42 (6): 1124-1127. |
| [23] | He C S, Mu Z X, Yang H Y, et al. Electron acceptors for energy generation in microbial fuel cells fed with wastewaters: A mini-review[J]. Chemosphere, 2015, 140 : 12-17. |
| [24] | 孔晓英, 袁振宏, 孙永明, 等. 微生物燃料电池阴极电子受体与结构的研究进展[J]. 可再生能源, 2010, 28 (1): 122-126. |
| [25] | 陈庆云, 王云海. 微生物燃料电池阴极功能的研究进展[J]. 化工进展, 2013, 32 (10): 2352-2360. |
| [26] | Lovley D R. Bug juice: harvesting electricity with microorganisms[J]. Nature Reviews Microbiology, 2006, 4 (7): 497-508. |
 2016, Vol. 37
2016, Vol. 37


