氯代烃多数具有“三致”效应而被美国环保署(EPA)列为优先控制污染物,而其作为重要的化工原料、 有机溶剂和中间体在化工、 制药、 制革等行业中广泛使用,导致很多工业废水和废气中有机物严重超标. 所以寻求一种安全、 高效地去除氯代烃的方法是十分必要的.
氯代烃作为常见的挥发性有机化合物的一种,其传统处理方法有吸附法、 吸收法、 燃烧法、 冷凝法等[1, 2, 3, 4, 5],但吸收法不适合于处理难溶于水或化学性质稳定的有机废气; 吸附法因为吸附剂价格昂贵、 容易形成二次污染而受限制; 催化燃烧法的运行成本较高,不适用于低浓度废气; 冷凝法也只适于高浓度有机废气的处理[6]. 近年出现的电晕法、 等离子体法、 光氧化分解法等新技术,在处理VOCs中也都取得了很好的成果,但在操作上存在一定的安全风险[7, 8, 9, 10, 11, 12]. 相比于以上的物理化学方法,生物法能利用微生物的代谢活动将VOCs完全转化成CO2和水,可用于不同性质废气的处理,尤其适用于大气量、 低浓度的有机废气的净化,是一种经济、 安全、 高效的处理技术,得到了国内外越来越多的学者的重视[13, 14, 15]. 然而氯代烃又因其极低的水溶性及可生物降解性使得传统的生物处理技术对氯代烃的降解速率和去除率均不高. 因此,探索氯代烃混合废气的生物净化工艺具有重大的理论和实践意义.
生物滴滤法以填料塔由结合生物膜净化技术,不仅操作简便、 运行费用低,而且处理效果好、 不产生二次污染[13, 16, 17]. 本实验以二氯甲烷(DCM)和1,2-二氯乙烷(1,2-DCA)这两种使用较多的氯代烃作为研究对象,利用生物滴滤塔对其进行净化,考察了稳定期总负荷和两者之间的相互作用对去除效果的影响,同时考察了反应器运行阶段生物量的变化情况.
1 材料与方法 1.1 实验装置及流程
本实验装置主要由生物滴滤塔装置、 空气压缩机、 玻璃转子流量计、 磁力搅拌器、 pH自动控制系统、 质量流量计、 计量泵、 蠕动泵、 不锈钢吹脱瓶、 混气瓶等组成. 实验采用逆流式操作,含氯烷烃混合废气采用动态鼓泡法配制,空气经泵、 质量流量计进入装有液态DCM(或1,2-DCA)的鼓泡瓶中产生气泡,利用平衡分压产生的DCM(或1,2-DCA)废气经胶管到达混气瓶与空气充分混合,混合空气流量由玻璃转子控制. 经流量计调节流量后,模拟废气从塔底进入生物滴滤塔,经滴滤塔中附着在填料上的生物膜降解、 净化. 实验装置如图 1所示.
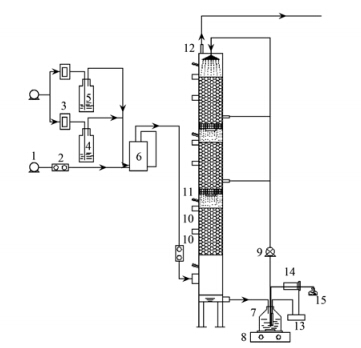 | 1.空气泵; 2.转子流量计; 3.质量流量计; 4、 5吹脱瓶; 6.混合瓶; 7.营养液储液瓶; 8.磁力搅拌器; 9.计量泵; 10.填料取样口; 11.采气口; 12.尾气排放口; 13.pH自动控制系统; 14.蠕动泵; 15.氢氧化钠储液瓶图 1 生物滴滤塔工艺流程图示意 Fig. 1 Schematic of biotrickling filter |
生物滴滤塔由总高1080 mm、 内径100 mm的有机玻璃制成,填料层每层高度为191 mm (3×191 mm),共由3层组成,沿塔高方向设置4个气体采样口(1个进气口,3个出气口)和6个填料取样口. 每层的隔板上都装有填料,填料层高191 mm,每层填料之间由隔板隔开,隔板开孔率在70%以上. 实验采用气液逆流操作,气体由塔底进入,由下而上,营养液经计量泵从储液瓶提升至塔顶向下喷淋,储液瓶容积为2 L. 为了提高底层和中层的滴淋效果,避免上层营养液向下滴时出现分布不均匀的情况,本喷淋装置设置3条管线分层喷淋,控制管路流量上 层>中层>下层,这样营养液在塔内横截面上就能更均匀地分布. 营养液最后回流至储液瓶,回流速度为12 L ·h-1,每4天更换一次营养液. 装置设有pH自动控制系统,pH维持在7.0~7.2.
实验装置具体结构参数见表 1
| 表 1 生物滴滤塔的基本参数 Table 1 Characteristics of biotrickling filter |
生物滴滤塔中的填料为聚氨酯小球,该填料的特征为较大的比表面积,一定的机械强度、 空隙率较大、 压降小、 抗老化力强. 具体参数见表 2.
| 表 2 填料特性参数 Table 2 Characteristics of packing carriers |
滴滤塔营养液采用连续喷淋,营养液组成如下(g ·L-1):Na2HPO4 ·12H2O 4.5、 KH2PO4 1.0、 NH4Cl 2.5、 MgSO4 ·7H2O 0.2、 CaCl2 ·2H2O 0.023、 微量元素1 mL,调节pH为7.2.
微量元素配方(g ·L-1):CuSO4·5H2O 0.02、 FeSO4·7H2O 1.0、 H3BO3 0.014、 ZnSO4·7H2O 0.10、 MnSO4 ·4H2O 0.10、 Na2MoO4 ·2H2O 0.02、 CoCl2·6H2O 0.02,pH为7.2,110℃高压灭菌40 min.
1.3 分析方法(1)生物量的测定
采用Folin-酚法测定蛋白质的含量.
(2)气相色谱法(GC)
DCM和1,2-DCA检测分析方法:采用Agilent 6890分析模拟废气浓度,色谱柱为HP-Innowax毛细管柱(30 m×0.32 mm×0.5 μm). 柱温采用升温程序:初始温度为90℃,保持4 min; 30℃ ·min-1的速度至150℃,保持0.5 min. 检测器:FID,温度:200℃,柱流量:1 mL ·min-1,进样量:800 μL. 载气:氮气,总流量:16.5 mL ·min-1,分流比为15 ∶1. 氢气流:40 mL ·min-1,空气流量:450 mL ·min-1.
CO2定量检测: 采用Agilent6890检测,色谱柱为HP-Plot-Q毛细管柱(30 m×0.32 mm×20 μm). 进样口温度:90℃,检测器(TCD) 温度:100℃,柱温:40℃,柱流量:5 mL ·min-1,进样量:800 μL,尾吹气:氦气.
2 结果与讨论 2.1 反应器启动阶段
活性污泥取自浙江某制药厂的曝气池,经测试污泥体积指数SVI值为1.624 mL ·g-1,污泥沉降比SV为75%,混合液悬浮固体浓度MLSS为4468 mg ·L-1,混合液挥发性悬浮固体浓度MLVSS为3575 mg ·L-1.
为了避免填料对混合废气的吸附作用,消除吸附作用对实验影响,启动反应器初期不添加活性污泥,通入100 mg ·m-3的DCM和1,2-DCA混合模拟废气,按实验条件正常喷淋营养液,运行一周. 通过气相检测DCM和1,2-DCA进出口浓度,直到进出口浓度一致时即可认为吸附饱和. 按照活性污泥 ∶营养液=1 ∶2通过喷淋塔喷淋循环挂膜,通过测定运行参数分析反应器的运行性能.
对目标污染物的去除率是反映生物滴滤塔挂膜启动情况的重要参数. 在启动挂膜阶段停留时间(EBRT)设为60 s,废气浓度均为100 mg ·m-3. 在启动阶段,反应器对废气的去除率如图 2所示. 其中DCM在挂膜30 d后去除率达80%以上. 在相同的运行条件下,1,2-DCA启动35 d后,去除率达到75%以上,并能持续保持此去除性能.
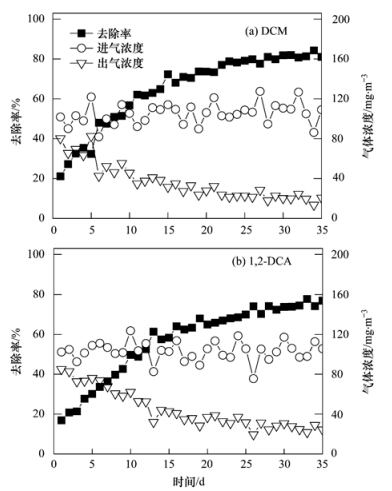 | 图 2 反应器挂膜阶段混合废气进出口浓度和去除率 Fig. 2 Concentration and removal efficiency of mixed waste gas during the startup phase of BTF |
实验结果表明,用活性污泥进行挂膜的生物滴滤塔启动时间为35 d. 张定丰等[18]利用高效降解菌加活性污泥对生物滴滤塔挂膜净化多组分废气,启动完成需要30 d左右. 本实验只用活性污泥挂膜,挂膜完成所需的时间与之相比较需要长一些,挂膜完成后对DCM和1,2-DCA的去除率分别达到80%和75%以上.
2.2 进气浓度对去除率和去除负荷影响混合废气去除率和去除负荷随进气浓度的变化如图 3所示,考察了EBRT=60 s时进气浓度对去除效果的影响. 随着进气总浓度从100 mg ·m-3提高到400 mg ·m-3,DCM的去除率从80%降至30%; 1,2-DCA的去除率从75%降至34%; 随着进气负荷的增加,DCM的去除负荷从5 g ·(m3 ·h)-1逐步上升至13 g ·(m3 ·h)-1, 当进气负荷进一步加大时,去除负荷下降至7 g ·(m3 ·h)-1, 1,2-DCA的去除负荷从5 g ·(m3 ·h)-1逐步上升至10 g ·(m3 ·h)-1,但随后下降至8 g ·(m3 ·h)-1. 这与进气浓度的升高抑制了活性污泥的降解活性有关. 王家德[19]等利用生物滴滤池处理DCM的研究中也显示了高浓度的DCM会降低生物滴滤池的去除效率. 这表明在较高进气负荷下, 由于受系统内有效生物量和气液传质的限制影响,单位生物量的底物转化能力接近最大值. 若进一步增加进气负荷,可能使系统内生物活性受到抑制,从而使底物转化能力降低.
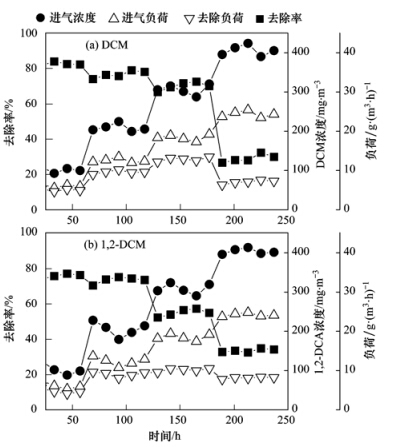 | 图 3 进气浓度对混合废气去除率影响 Fig. 3 Effects of inlet concentration on removal rate |
利用滴滤塔处理多组分废气时,气体之间往往会存在相互竞争或抑制作用,所以研究混合废气的相互作用是很有必要的[15, 20, 21]. 为了考察1,2-DCA和DCM在反应器中的相互作用,在反应器运行至稳定运行阶段,考察混合废气各组分浓度变化对于生物滴滤塔工艺去除效果的影响. 实验过程中,混合废气中某一组分浓度由低到高变化,另一组分的浓度则保持稳定,即在保持DCM进气浓度为100 mg ·m-3时,1,2-DCA的浓度从0~450 mg ·m-3逐步提高; 保持1,2-DCA进气浓度为100 mg ·m-3时,DCM的浓度从0~450mg ·m-3逐步提高,检测不同进气浓度条件下各组分的去除率. 结果如图 4和图 5所示
 | 图 4 1,2-DCA浓度变化对DCM的去除性能的影响 Fig. 4 Effects of concentration changes of 1,2-DCA on removal of DCM |
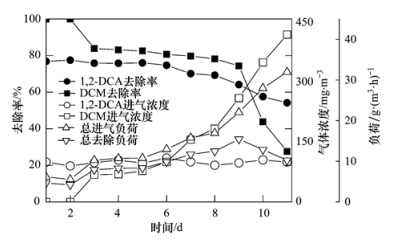 | 图 5 DCM浓度变化对1,2-DCA的去除性能的影响 Fig. 5 Effects of concentration changes of DCM on removal of 1,2-DCA |
如图 4所示,当DCM的进气浓度维持在100 mg ·m-3左右,逐步提高1,2-DCA的进气浓度,总进气负荷由6.0 g ·(m3 ·h)-1提高到33.8 g ·(m3 ·h)-1. 在只有单一组分DCM时,生物滴滤塔对DCM 的去除率为83%以上. 当1,2-DCA的浓度为55 mg ·m-3时,DCM的去除率为82%,总去除负荷为7.1 g ·(m3 ·h)-1,提高1,2-DCA的进气浓度到100 mg ·m-3时,DCM的去除率为81%,总去除负荷为9.5 g ·(m3 ·h)-1,当1,2-DCA的进气浓度为200 mg ·m-3和300 mg ·m-3时,DCM的去除率为76%和68%,且可取的最高去除负荷14 g ·(m3 ·h)-1,当1,2-DCA的进气浓度上升到400 mg ·m-3时,DCM的去除率为60%,总去除负荷为12 g ·(m3 ·h)-1,当1,2-DCA的进气浓度为450 mg ·m-3时,DCM的去除率为55%,总去除负荷下降至11 g ·(m3 ·h)-1. 由此可知,在反应体系中,低浓度1,2-DCA(低于100 mg ·m-3)的存在不会对DCM的降解产生抑制效应,但高浓度1,2-DCA的存在(高于200 mg ·m-3)会对DCM的降解产生一定的抑制效应.
如图 5所示,1,2-DCA的进气浓度维持在100 mg ·m-3左右,逐步提高DCM的进气浓度,总进气负荷由6.2 g ·(m3 ·h)-1上升到32 g ·(m3 ·h)-1. 当组分中只存在1,2-DCA时,反应体系对1,2-DCA的去除率为77%. 当DCM的浓度为68 mg ·m-3时,DCA的去除率为76%,总去除负荷为7.9 g ·(m3 ·h)-1,提高DCM的进气浓度到100 mg ·m-3时,1,2-DCA的去除率为75%,总去除负荷为9.8 g ·(m3 ·h)-1,当DCM的进气浓度为184 mg ·m-3时,1,2-DCA的去除率为69%,总去除负荷为12 g ·(m3 ·h)-1,当DCM的进气浓度为261 mg ·m-3时,1,2-DCA的去除率为64%,具有最高总去除负荷15 g ·(m3 ·h)-1,当DCM的进气浓度上升至420 mg ·m-3时,1,2-DCA的去除率为55%,总去除负荷下降至10 g ·(m3 ·h)-1. 由此可知,在反应体系中,低浓度DCM(低于100 mg ·m-3)的存在不会对1,2-DCA的降解产生抑制效应,但高浓度DCM的存在(高于200mg ·m-3)会对1,2-DCA的降解产生一定的抑制效应.
结合图 4和图 5可知,用生物滴滤塔去除含DCM和1,2-DCA的混合废气时,当各组分的浓度低于100 mg ·m-3时,不会对另一组分产生抑制效应,当进气浓度高于100 mg ·m-3低于200 mg ·m-3时,对另一组分有轻微的抑制效应,当进气浓度高于400 mg ·m-3时,DCM和1,2-DCA的去除率分别由80%和75%降低到60%和55%左右. 保持一组分的浓度不变提高另一组分的浓度时,在一定范围内能提高反应器的总去除负荷,但当另一组分的浓度过高时,由于对两组分去除率的降低会导致总去除负荷的下降.
2.4 二氧化碳生成量分析生物滴滤塔运行过程中,目标污染物VOCs在有氧条件下主要会被微生物降解成CO2和水,也可被微生物利用合成自身物质. 因此,常用CO2生成量来反映生物滴滤塔的去除性能. 有报道指出生物滴滤床降解苯的矿化率达77%左右[22],而CO2生成量与BTEX的去除负荷的比例为2.50~2.93之间[23, 24, 25, 26],有研究比较下流式和上流式生物过滤塔处理高负荷甲苯废气,CO2生成量随着甲苯进气浓度的增大而增大,在EBRT为3.1 min时,甲苯转化CO2的百分率分别为81%和70%[27].
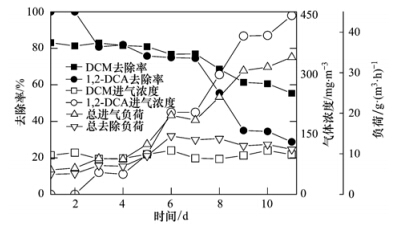
CO2的理论生成量表示有机物降解过程中所含的碳能完全转化成CO2时的CO2生成量. 然而在混合废气组分中,因为各组分的含碳量是存在差异的,所以如果各组分的去除是不成比例的话,是难以计算出理论矿化率的,因此根据本反应器对DCM和1,2-DCA的去除情况,本实验尽可能地将DCM和1,2-DCA按1 ∶1的浓度调整进气负荷,CO2随混合去除负荷的变化情况如图 6所示. 实验过程中DCM和1,2-DCA的进气浓度分别由20 mg ·m-3逐渐提高到420 mg ·m-3,二者的去除负荷分别从1.28 g ·(m3 ·h)-1和1.04 g ·(m3 ·h)-1上升到10.38 g ·(m3 ·h)-1和9.90 g ·(m3 ·h)-1,而后又分别下降到4.41g ·(m3 ·h)-1和6.61 g ·(m3 ·h)-1. 根据CO2的实际产生量,结合DCM和1,2-DCA完全矿时CO2的理论生成量,求出总CO2理论生成量,从而求出反应器对混合废气的矿化率.
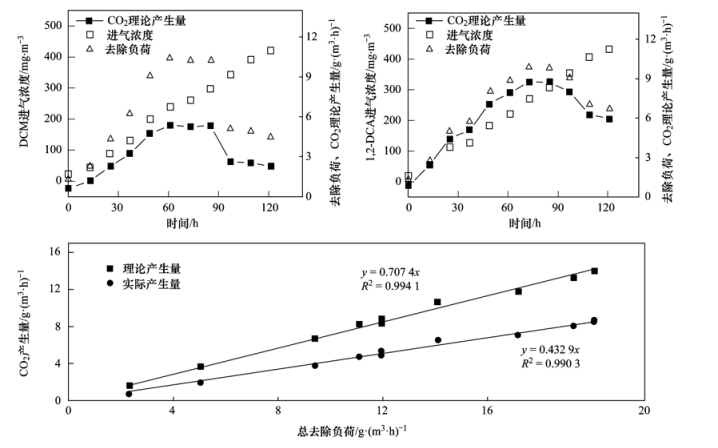 | 图 6 生成量随去除负荷的变化关系 Fig. 6 Relationship between the CO2 production rate and elimination capacity |
结果显示,该实验下CO2生成量与总去除负荷呈线性关系,y=0.4329x,R2=0.9903,而理论上CO2生成量与混合废气总去除负荷拟合的结果可表示为y=0.7074x,R2=0.9941. 表明生物滴滤塔对混合废气的矿化率为61.2%. 与实际值有一定的差距,表明反应器中微生物菌群对混合降解除了转化为CO2以外,还有一部分转化为生物碳供微生物自身生长,还有一些以HCO3-、 H2CO3或者CO2-3无机碳的形式存在于液相中,没有被检测到,另外的其他部分则可能是生成了难降解的中间产物.
2.5 反应器运行过程中生物量的变化生物滴滤塔中填料中所含有的生物量是评价反应器性能的重要参数之一[28]. 由于反应器内生物量变化难以准确测定,有研究采用蛋白质含量来表征生物滴滤塔内的生物量变化,即将填料上的生物膜清洗下来,提取蛋白质,进而测定蛋白含量[29,30]. 在生物滴滤塔工艺运行过程中,对启动器和稳定期的各层填料进行取样并测定其中生物量,在DCM和1,2-DCA浓度分别为100 mg ·m-3下测定各层的去除负荷,结果如表 3所示.
| 表 3 不同时期蛋白量含量及去除负荷的变化 Table 3 Protein amount and elimination capacity during different phases of BTF |
由表 3可见生物滴滤塔上、 中、 下各层的生物量(以填料计,下同)在启动完成后较挂膜初期都有明显的增加,其中上层由0.191 mg ·g-1增加到0.968 mg ·g-1,中层由0.257mg ·g-1增加到1.105 mg ·g-1,生物塔的下层由0.499 mg ·g-1增加到1.290 mg ·g-1. 稳定运行期,填料上微生物的生长与脱落维持动态平衡,生物量基本维持不变,老化的生物膜随营养液的更换排出系统. 不同运行时期,反应器各层的去除负荷规律为:下层>中层>上层,这与生物量的分布规律一致,表明生物量的多少会直接影响污染物的去除效果.
3 结论
(1)采用制药厂活性污泥循环挂膜,可用于去除低浓度的DCM和1,2-DCA混合废气. 挂膜所需的时间为35 d,挂膜完成后二者可分别保持80%和75%的稳定去除率.
(2)反应器运行过程中随进气负荷的增加去除负荷遵循先上升后下降的规律,对DCM和1,2-DCA的最大去除负荷分别为13 g ·(m3 ·h)-1和10 g ·(m3 ·h)-1. 当两组分的浓度低于100 mg ·m-3时,无相互作用,当一组分的浓度高于200mg ·m-3时,开始对另一组分出现抑制,影响另一组分的去除.
(3)稳定运行期,当DCM和1,2-DCA的进气负荷为1 ∶1时,生物滴滤塔对混合废气的矿化率为61.2%. 反应器各层的去除负荷规律为:下层>中层>上层.
| [1] | 马超, 薛志钢, 李树文, 等. VOCs排放、污染以及控制对策[J]. 环境工程技术学报, 2012, 2 (2): 104-105. |
| [2] | 席劲瑛, 武俊良, 胡洪营, 等. 工业VOCs气体处理技术应用状况调查分析[J]. 中国环境科学, 2012, 32 (11): 1955-1960. |
| [3] | Chiang C Y, Liu Y Y, Chen Y S, et al. Absorption of hydrophobic volatile organic compounds by a rotating packed bed [J]. Industrial & Engineering Chemistry Research, 2012, 51 (27): 9441-9445. |
| [4] | Guihéneuf S, Castillo A S R, Paquin L, et al. Absorption of hydrophobic volatile organic compounds in ionic liquids and their biodegradation in multiphase systems[A]. In: Fang Z, Smith R L Jr, Qi X H (Eds.). Production of Biofuels and Chemicals with Ionic Liquids[M]. Netherlands: Springer, 2014. |
| [5] | Morozov G, Breus V, Nekludov S, et al. Sorption of volatile organic compounds and their mixtures on montmorillonite at different humidity [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2014, 454: 159-171. |
| [6] | 王小军, 徐校良, 李兵, 等. 生物法净化处理工业废气的研究进展[J]. 化工进展, 2014, 33 (1): 213-218. |
| [7] | 任爱玲, 赫环环, 郭斌, 等. 生物滴滤塔净化含低浓度苯乙烯废气的研究[J]. 环境科学学报, 2013, 33 (7): 1840-1848. |
| [8] | Van Durme J, Dewulf J, Sysmans W, et al. Abatement and degradation pathways of toluene in indoor air by positive corona discharge[J]. Chemosphere, 2007, 68 (10): 1821-1829. |
| [9] | Demidiouk V, Moon S I, Chae J O. Toluene and butyl acetate removal from air by plasma-catalytic system [J]. Catalysis Communications, 2003, 4 (2): 51-56. |
| [10] | Ko Y, Yang G, Chang D P Y, et al. Microwave plasma conversion of volatile organic compounds [J]. Journal of the Air & Waste Management Association, 2012, 53 (5): 580-585. |
| [11] | Urashima K, Chang J S. Removal of volatile organic compounds from air streams and industrial flue gases by non-thermal plasma technology[J]. IEEE Transactions on Dielectrics and Electrical Insulation, 2000, 7 (5): 602-614. |
| [12] | 吴亚西, 陈烈贤. 光催化氧化分解空气挥发性有机污染物的研究[J]. 卫生研究, 2002, 31 (5): 384-385. |
| [13] | 何觉聪, 黄倩茹, 陈洲洋, 等. 生物滴滤塔处理苯酚气体研究 [J]. 环境科学, 2014, 35 (2): 521-525. |
| [14] | 李超, 赵东风, 张庆冬, 等. 生物过滤法处理低浓度有机废气的研究进展[J]. 化工环保, 2013, 33 (6): 503-508. |
| [15] | Wang X Q, Lu B H, Zhou X X, et al. Evaluation of o-xylene and other volatile organic compounds removal using a xylene-acclimated biotrickling filter. [J]. Environmental Technology, 2013, 34 (19): 2691-2699. |
| [16] | Liu D Z, Andreasen R R, Poulsen T G, et al. A comparative study of mass transfer coefficients of reduced volatile sulfur compounds for biotrickling filter packing materials [J]. Chemical Engineering Journal, 2015, 260: 209-221. |
| [17] | Sun D F, Li J J, Xu M Y, et al. Toluene removal efficiency, process robustness, and bacterial diversity of a biotrickling filter inoculated with Burkholderia sp. Strain T3[J]. Biotechnology & Bioprocess Engineering, 2013, 18 (1): 125-134. |
| [18] | 张定丰, 房俊逸, 叶杰旭, 等. 生物滴滤塔净化多组分废气的研究[J]. 环境科学, 2013, 34 (6): 2116-2120. |
| [19] | 王家德, 陈建孟, 庄利. 生物滴滤池处理二氯甲烷废气研究[J]. 中国环境科学, 2002, 22 (3): 214-217. |
| [20] | Jiang X, Yan R, Tay J H. Simultaneous autotrophic biodegradation of H2S and NH3 in a biotrickling filter[J]. Chemosphere, 2009, 75 (10): 1350-1355. |
| [21] | 谢志荣, 魏在山, 曾贵华, 等. 生物法处理含氮硫无机有机恶臭气体研究[J]. 环境科学与技术, 2011, 34 (1): 136-139. |
| [22] | Jang J H, Hirai M, Shoda M. Enhancement of styrene removal efficiency in biofilter by mixed cultures of Pseudomonas sp. SR-5 [J]. Journal of Bioscience and Bioengineering, 2006, 102 (1): 53-59. |
| [23] | Jiang X, Yan R, Tay J H. Transient-state biodegradation behavior of a horizontal biotrickling filter in co-treating gaseous H2S and NH3[J]. Applied and Environmental Microbiology, 2009, 81 (1): 969-975. |
| [24] | Jorio H, Bibeau L, Heitz M. Biofiltration of air contaminated by styrene: effect of nitrogen supply, gas flow rate, and inlet concentration [J]. Environmental Science & Technology, 2000, 34 (9): 1764-1771. |
| [25] | Hassan A A, Sorial G. Biological treatment of benzene in a controlled trickle bed air biofilter[J]. Chemosphere, 2009, 75 (10): 1315-1321. |
| [26] | Mathur A K, Majumder C B, Chatterjee S. Combined removal of BTEX in air stream by using mixture of sugar cane bagasse, compost and GAC as biofilter media [J]. Journal of Hazardous Materials, 2007, 148 (1-2): 64-74. |
| [27] | Znad H T, Katoh K, Kawase Y. High loading toluene treatment in a compost based biofilter using up-flow and down-flow swing operation [J]. Journal of Hazardous Materials, 2007, 141 (3): 745-752. |
| [28] | 胡俊, 郑江玲, 吴越新, 等. 生物滴滤塔降解甲苯废气长期运行生物膜相特性研究[J]. 环境科学, 2012, 33 (9): 2979-2986. |
| [29] | American Public Health Association. Standard Methods for the Examination of Water and Wastewater [S]. Washington: APHA, 1998. |
| [30] | Steinle P, Stucki G, Stettler R, et al. Aerobic mineralization of 2,6-dichlorophenol by Ralstonia sp. strain RK1 [J]. Applied and Environmental Microbiology, 1998, 64 (7): 2566-2571. |
 2015, Vol. 36
2015, Vol. 36


