2. 中国地质科学院岩溶地质研究所,联合国教科文组织国际岩溶研究中心,国土资源部/广西岩溶动力学重点实验室,桂林 541004;
3. 中国地质大学环境学院,武汉 430074;
4. 山东省地矿工程勘察院,济南 250014
2. Key Laboratory of Karst Dynamics, Ministry of Land and Resources/ Guangxi, International Research Center on Karst Under the Auspices of UNESCO, Institute of Karst Geology, Chinese Academy of Geological Sciences, Guilin 541004, China;
3. School of Environmental Studies, China University of Geosciences, Wuhan 430074, China;
4. Shandong Geological Engineering Investigation Institute, Ji'nan 250014, China
人类活动向地下河中排放的污染物质往往具有多样性和多源性,运用单一的指标判别地下水中所有污染源往往缺乏针对性和科学性,因此,需要结合多种同位素分别示踪污染物质来源. 地下水中硝酸盐污染的来源较多,早期主要利用氮同位素技术识别氮源[1, 2, 3, 4, 5, 6],但由于不同污染源NO3-的初始δ15 N值存在交迭现象,以及诸如反硝化作用等地球化学作用引起同位素分馏,利用单一的δ15 N值难以区分[7,8]. 为此,将δ15 N-NO3-和δ18 O-NO3-相结合能有效地确定污染来源,识别反硝化作用[9, 10, 11, 12, 13, 14, 15, 16]. 而针对地下河中硫酸盐来源问题,根据代表不同来源污染物特征化学指纹的δ34 S值,在没有硫同位素分馏效应以及已知潜在硫源的δ34 S的情况下,可以通过所测样品的δ34 S推测其硫源,较好地进行示踪[17, 18, 19, 20, 21]. 基于此,本研究在监测里湖地下河各常规离子时间变化特征的基础上,联系城市发展情况和流域的水文地质条件,利用硫同位素示踪硫酸盐来源,氮氧同位素示踪硝酸盐来源,以期为厘清城市污染物质来源,从源头上减少硫酸盐、硝酸盐输入,协调城市经济发展与水质保护提供科学依据. 1 研究区概况
里湖地下河位于广西河池市南丹县中北部,是区内最大的地下河水系,其流域面积为517.4 km2,其中碳酸盐岩出露面积占总面积的85%左右(图 1). 里湖地下河发源于拉易、关西的峰林、峰丛溶盆-溶洼地区,水系呈树枝状展布,径流于峰林溶洼山地,于贵州省荔波县拉娘村西北打狗河西岸陡崖脚出露排泄. 流域内出露地层主要为石炭系、二叠系、三叠系,仅在南丹河河谷地带存在第四系堆积物,广泛分布含燧石石灰岩,偶夹煤层及白云岩,灰岩,砂岩,页岩等. 研究区为中亚热带季风性湿润气候,年平均气温为17~20℃,月平均最高气温为27℃,最低气温7℃. 本区降水充沛,据南丹县1965~2009年以来45年的降水数据显示,降水主要集中在5~8月,达965.2 mm,占全年降水量的65.7%[22],是地下水的主要补给来源之一[23]. 受降水季节变化的影响,地下河平水期流量4 593.75L ·s-1,枯季流量3 339.66 L ·s-1,其中地表水补给流量1 259.05 L ·s-1.
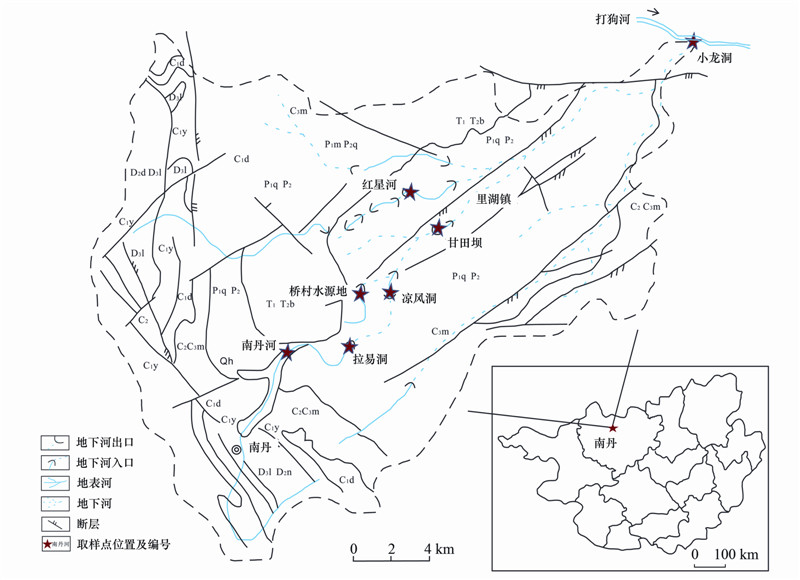 | 根据文献[25]修改图 1 研究区水文地质图及采样点位置 Fig. 1 Hydrogeological map of the studied area and the locations of sampling sites |
里湖地下河是南丹县兼有城市供水、农业灌溉,工业用水等多重社会和经济功能的重要水源(图 1). 由于90年代以来城市化进程的加快,城市工业废水,生活污水和人畜废水大量排放,里湖地下河污染载荷增加,水质变差. 已有研究表明氨氮是里湖地下河主要污染指标,亚硝态氮、锰、总铁、化学需氧量(chemical oxygen demand,COD)、生化需氧量(biochemical oxygen demand,BOD)部分浓度超过国家Ⅲ类水标准,砷、铬、硝态氮的部分浓度值超过国家Ⅱ类水质量标准,部分采样点水污染严重,已基本不能利用[23]. 郭芳等[24]选取水中主要离子和微量元素,分析了里湖地下河的自净能力,为地下河水资源管理和保护提供了依据. 上述研究从不同角度对里湖地下河的水质进行了分析,指出人类活动是里湖地下河水质变化的因素,但得出的污染源的结果较为粗略,要从源头上减少污染物质的输入,还需要利用同位素示踪方法直接、明确地追踪出污染来源. 2 材料与方法
在里湖地下河共布设7个采样点(图 1),采样工作分3个时间段,即2010年1~12月(马振杰[23]的采样)、2014年5月16日、2014年10月18日. 其中,在小场采集里湖地下河上游的南丹河水样,该地表水流经南丹县城,途经居民区,菜市场等,生活和生产废水被直接或间接地排放到南丹河,对南丹河的水质产生直接影响. 拉易洞为其上游地表河转化为地下河的结点,是里湖地下河的主要入口之一. 凉风洞、甘田坝、红星河等是里湖地下水的出露点,其间明暗流交替. 桥村是南丹县的备用水源地,根据柳州水文队调查,认为该股水与拉易洞水为上下层关系,最终将汇入里湖地下河. 小龙洞是里湖地下河汇入打狗河的出口.
现场用WTW 3430多参数水质测定仪(德国WTW公司)测定水温、溶解氧(dissolved oxygen,DO)、pH值,电导率,精度分别为0.1℃、0.01 mg ·L-1、0.01个pH单位、1 μS ·cm-1; HCO3-和Ca2+采用德国Merck公司便携式试剂盒,精度分别为0.1 mmol ·L-1和2mg ·L-1.
每次采样前,用水样清洗采样瓶3~4次,现场用直径50 mm、0.45 μm的醋酸纤维滤膜过滤水样后,存储于100 mL聚乙烯采样瓶中,带回实验室用离子色谱分析仪测定其SO2-4、NO3-、Cl-,此测试工作在广西/国土资源部岩溶动力学重点实验室完成; 取过滤水样,装于事先用水样清洗过的50 mL聚乙烯样瓶中,并立即加1 ∶1优级纯硝酸溶液5~8滴,调节pH<2,用美国Perkin Elmer公司产的Optima 2100DV全谱直读型ICP-OES测定水样中的K+、Na+、Mg2+,阳离子测试在西南大学地理科学学院地球化学同位素实验室完成.
水中SO2-4的δ34 S在2014年5月16日采集,现场用0.45 μm醋酸纤维滤膜过滤1.5 L水样装入事先清洗3遍的采样瓶. 带回实验室后,加HCl酸化,使pH≤2,视水样中SO2-4浓度加入过量的饱和BaCl2溶液,使SO2-4完全生成BaSO4,静置过夜. 用去离子水反复冲洗沉淀保证完全去除Cl-,并用0.45 μm醋酸纤维滤膜过滤生成的BaSO4沉淀,置于850℃烘干2 h. δ34 S-SO2-4采用元素分析仪(Carlo Erba 1108)结合同位素质谱仪(IRMS,Delta C Finningan Mat)测定,测定结果相对于国际标准V-CDT,测试精度优于±0.2‰,测试工作在中国地质大学(武汉)环境学院教学实验中心完成.
用事先清洗3遍的50 mL聚乙烯瓶取水样,密封,冷藏送实验室进行水中δ15 N-NO3-和δ18 O-NO3-同位素分析,样品用反硝化细菌法结合痕量气体分析仪(TraceGas)/同位素比质谱仪进行测试. 利用天然存在无N2O还原性酶活性的反硝化细菌将NO3-转化为N2O气体,再采用痕量气体分析仪TraceGas在线提取和纯化N2O气体,利用含高氯酸镁及碱石棉的水阱除去水分和CO2,再用液氮捕集浓缩N2O气体,然后加热释放,经Porapak Q色谱柱分离后由He气带入同位素比质谱仪进行测定,测试工作在中国农业科学院农业环境与可持续发展研究所稳定同位素实验室完成. 3 结果与分析 3.1 水化学类型
表 1为里湖地下河部分测试数据,图 2为研究区7个采样点的水化学Piper三线图,在阳离子三角图上,里湖地下河阳离子以Ca2+为主,平均占阳离子组成的74%,阴离子三角图上以HCO3-为主要离子,平均占阴离子组成的71%,其次为SO2-4,平均占阴离子组成的24%,水化学类型为HCO3-Ca型. 从阳离浓度均值来看,Ca2+>Na+>Mg2+>K+; 从阴离子浓度均值来看,HCO3->SO2-4>NO3->Cl-.
| 表 1 里湖地下河部分测试数据1)Table 1 Part of the testing data of Lihu Lake underground water |
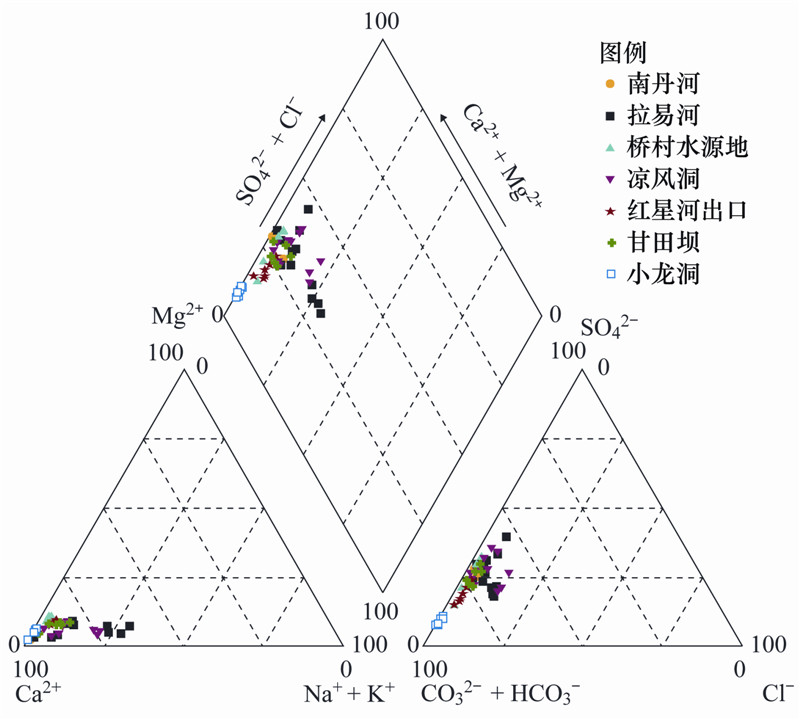 | 图 2 里湖水化学Piper三线图 Fig. 2 Piper chart of Lihu Lake underground water |
里湖地下河电导率变化在231~803μS ·cm-1,pH在7.10~8.87之间,水温变化在13.5~24.7℃之间,受气温影响,夏季大于冬季. 分别选取代表里湖地下河上、中、下游的拉易洞、凉风洞、小龙洞来分析里湖地下河水化学时间变化(图 3). 上游拉易洞和中游凉风洞各离子浓度时间变化上基本相同,即K+、Na+、Ca2+、Mg2+在5月急剧降低,之后一直呈降低趋势,8月后浓度又逐渐上升,主要是受到雨季降水稀释及至2010年4月30日起位于拉易洞上游约200 m处的污水处理厂开始运营,集中处理由城镇排放出的生活和生产污水,使地下河中各离子浓度在2010年4月后开始出现显著降低; 基于同样的原因,HCO3-、Cl-、NO3-、SO2-4也出现类似的时间变化规律,但NO3-、SO2-4等阴离子相对于其他离子波动较大. 从下游地下河出口小龙洞处 2010年7~12月的数据来看,除HCO3-离子外,各离子浓度均较上游和中游的拉易洞和凉风洞低,且基本保持在较低水平,随时间变化小.
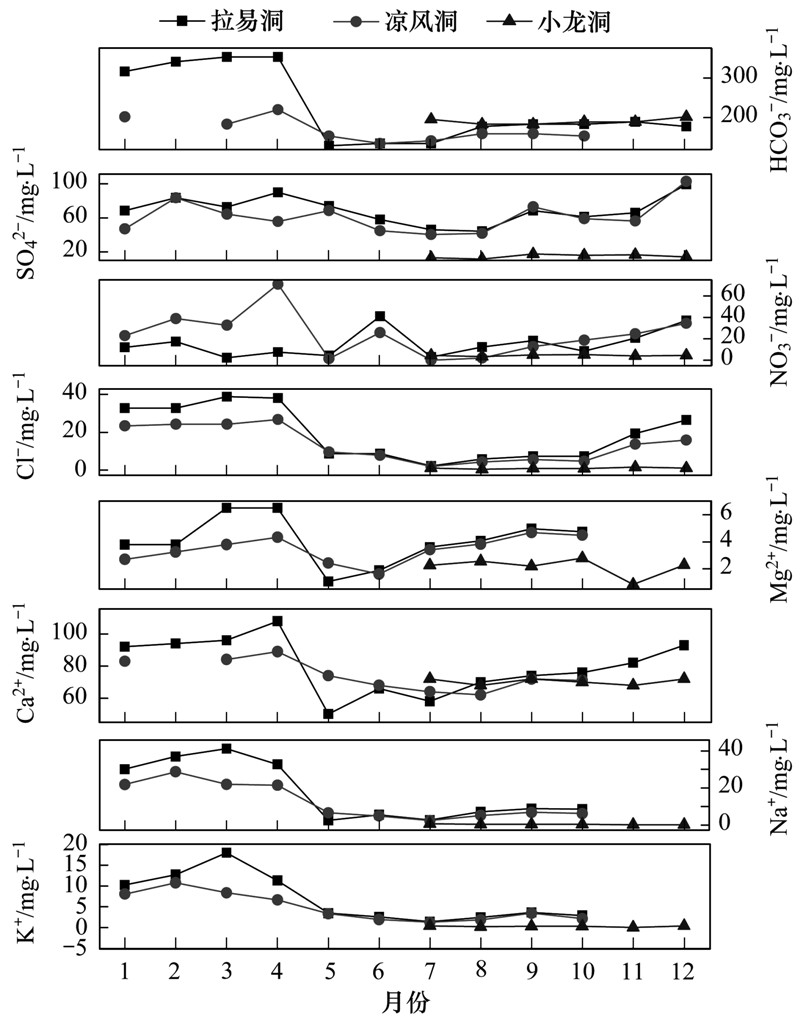 | 图 3 里湖地下河2010年各月水化学指标时间变化 Fig. 3 Temporal variation of the hydrochemistry in Lihu Lake underground water in each month of the year 2010 |
测得里湖地下河2014年5月水体中δ34 S-SO2-4值在-4.12‰~-0.93‰之间波动,平均为-2.46‰(表 2); δ15 N-NO3-值在4.79‰~10.22‰之间,平均为7.71‰,δ18 O-NO3-值在5.62‰~21.76‰之间,平均为12.53‰. 同年10月的硝酸盐中的氮氧同位素组成与5月相比,δ15 N-NO3-值变化幅度更大,在0.26‰~11.58‰之间,平均为7.50‰,δ18 O-NO3-值与5月相比普遍偏低,在-2.33‰~12.56‰之间,平均为6.22‰.
| 表 2 2014年里湖地下河硫同位素、氮氧同位素特征 Table 2 Values of δ34 S in sulfur and the values of δ15 N and δ18 O in nitrate in Lihu Lake underground water in the year 2014 |
里湖地下河中SO2-4较高,2010年5月平均浓度为71.17mg ·L-1,10月平均浓度为48.27mg ·L-1,2014年5月平均为47.11mg ·L-1,10月平均为48.02mg ·L-1,远远高于世界河水SO2-4的平均值11.2 mg ·L-1[26].图 4对比了里湖地下河2010年5月、10月与2014年5月、10月的SO2-4浓度时空变化,其中2010年大于2014年,表明从2010年污水处理厂开始运营后,虽其浓度仍偏高,但比2010年有所降低. NO3-浓度在1.15~71.21mg ·L-1之间,其时间变化表现出不同于SO2-4的特征. 从图 4可以看出2014年5、10月的NO3-浓度都分别大于2010年5、10月,这说明硝酸盐的污染在加剧,指示了工、农业活动的加剧和城市污水的排放增加了地下河的氮负荷. 从空间分布上看,上游南丹河,拉易洞、中游凉风洞、甘田坝等硫酸盐、硝酸盐浓度较高,下游小龙洞处则较低. 结合实地考察,在城关镇小场采集的南丹河水样流经南丹县城,途经居民区,菜市场,沿途生活、生产废水直接或间接地排放到南丹河,污染物质在向下运移的途中不断积累; 拉易洞为地表河转为地下河的入口,汇集了来自上游的大量地表污水,加上周围分布有采石场、水泥厂、砖厂等,堆积在地表的岩石风化物和工业废水被输送到河水中; 凉风洞周围正在进行旅游开发,地下河污染负荷随人类活动的加剧而增大; 甘田坝周围为大片农田,农业活动也是地下水污染来源之一. 据此粗略地认为地下水中硫酸盐、硝酸盐主要是来源于人类活动,但具体的污染来源需要结合硫同位素、氮氧同位素进行示踪.
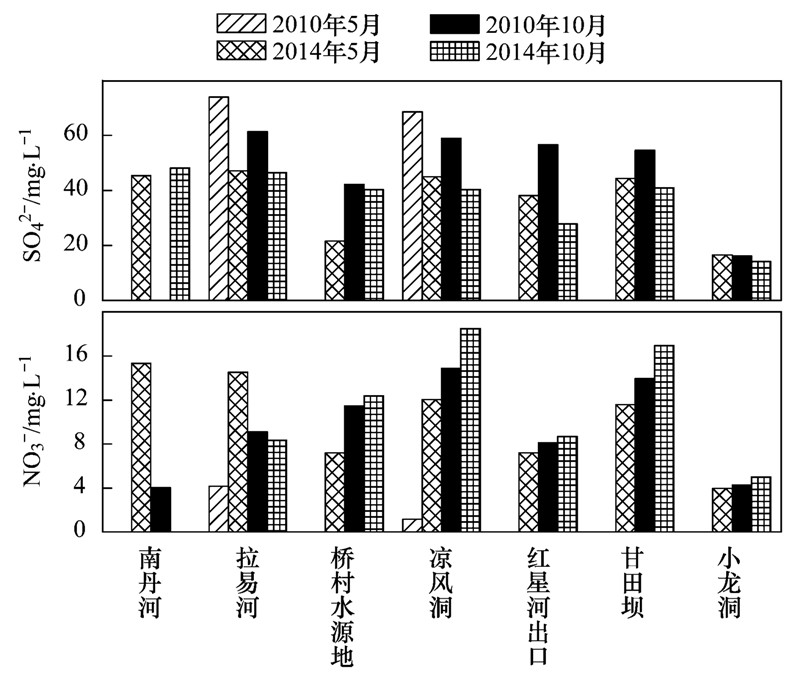 | 图 4 里湖地下河硫酸盐、硝酸盐时空分布变化 Fig. 4 Spatial and temporal variation of sulfur and nitrate in Lihu Lake underground water |
地下水中硫酸盐主要有以下几种来源:大气降水、蒸发岩的溶解、硫化物的氧化及土壤带中有机硫的矿化,海岸地区还受到海水入侵的影响或传输的海盐通过降水补给而导致地下水中硫酸盐浓度增大[27]. 此外,随着工农业的发展和城市化进程的加快,人类活动(如开采矿床、施用化肥等)的输入也成为硫酸盐的主要来源之一[28, 29, 30, 31]. 稳定同位素的组成(δ34 S)代表各污染源的特征化学指纹,不同来源的δ34 S存在较大差异,这使利用硫稳定同位素示踪污染来源成为可能[32],而被广泛运用于自然生态系统中各种硫源的示踪和地球化学循环的研究[33].
里湖地下河中δ34 S-SO2-4值在-4.12‰~-0.93‰之间,平均值为-2.47‰(表 2),其相对较窄的分布范围反映了当地硫源较为单一. 里湖地下河流经地区出露的二叠纪、三叠纪地层中偶夹薄层石膏,地下水在流经石膏层时,水岩作用的结果是水体会有较高的SO2-4浓度和高的δ34 S值. 临近地区贵州的海相蒸发岩(石膏)的δ34 S值的变化区间为23.7‰~29.56‰[34],四川盆地三叠系硬石膏δ34 S值为14.7‰~35.4‰[35]. Querol等[36]研究西班牙地区地下水、地表水及矿物中SO2-4的硫同位素组成时,发现三叠纪和中新世石膏的δ34 S值多数分布在12‰~14‰之间. 通常地层中石膏的δ34 S值均偏正,与研究区地下水中δ34 S值-4.12‰~-0.93‰之间差异较大,可以得出里湖地下河中没有或较少存在石膏溶解的情况.
据Moncaster等[37]报道,英国化肥的δ34 S值在5.4‰~8.5‰之间; Mizota等[38]报道了日本的化肥硫铵(俗称肥田粉)和普通过磷酸钙δ34 S值为10.2‰,在澳大利亚和新西兰的更高,在15.7‰~20.7‰之间; 在四川盆地西南部的峨眉山,人造化肥为7.1‰~8.9‰[22]. 由凉风洞以下的里湖中下游地区虽分布有大片农田,但农业化肥的δ34 S值皆分布在正值范围内,与里湖地下水的δ34 S-SO2-4值主要是在负值范围不一致,由此认为农业活动中施用的化肥不是里湖地下河SO2-4的主要来源.
里湖地下河的补给来源主要是大气降水,所属的河池市是广西地区酸雨较严重的城市之一,约82%的大气降水的pH值<5.6[39],酸雨可向地下河中输入大量SO2-4. 据广西地区的柳州气象局地面站、桂林市环境保护监测站、合山电厂化学分场等的监测数据,湘桂走廊地区大气降水的δ34 S-SO2-4值的变化范围为-4.8‰~-0.1‰,集中分布在负值范围内[40],涵盖了里湖地下水的硫同位素组成范围(-4.12‰~-0.93‰),据此推断地下水中SO2-4大部分来自于大气降水. 又将里湖地下河的δ34 S-SO2-4值与1/SO2-4做图(图 5),水体δ34 S-SO2-4值主要落在大气降水的δ34 S值范围内,部分落在大气降水和煤重合的值域内,但里湖流经地层主要为石炭系下统岩关阶、石炭系上统马平群、二叠系下统栖霞阶、二叠系上统、三叠系下统,三叠系中统百逢组,并没有煤系地层的存在,出现这种情况可能是由于煤炭是里湖地区工业生产和居民生活的主要能源,洪业汤等[41]研究中国大气降水的南北分异时发现,中国在长江以南地区,由拉萨,经贵阳往深圳地区,大气降水的δ34 S值均为负值,这与中国煤炭δ34 S值的南北分异相似,认为煤炭燃烧过程中的同位素分馏效应造成了这种分异.
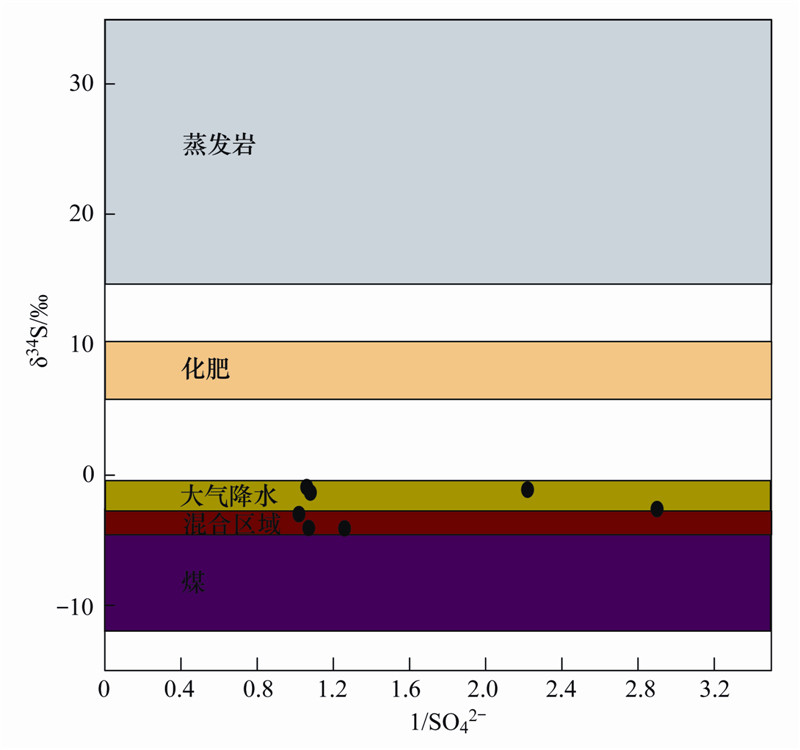 | 图 5 里湖地下水δ34 S与1/SO2-4的变化关系 Fig. 5 Variation relationship of δ34 S and 1/SO2-4 in the Lihu Lake underground water |
地下水中的硝酸盐来源很多,而且一经污染则难以治理,因此查明硝酸盐来源,对从根源上减少硝酸盐的输入具有重要意义[42]. 岩溶地区的土壤、岩石和包气带的渗透性较好,由源进入地下水过程中氮同位素分馏作用通常较小[43, 44, 45],应用δ15 N-NO3-,并结合δ18 O-NO3-能够有效地进行地下水污染溯源. 但发生反硝化作用导致氮同位素分馏,致使不同氮源的硝酸盐同位素组成值域发生重合的可能仍然存在,因此,有必要辨识反硝化过程,排除同位素分馏导致的氮源识别干扰[46]. 在识别反硝化作用之前还应先判定该区的地下水环境是否适宜反硝化作用的发生. 由于反硝化作用发生在厌氧环境下,因此水中溶解氧的多少可以作为判别指标之一,研究发现在DO浓度<0.2mg ·L-1条件下,反硝化速率最理想[47]. 而Gillham等[48]经野外调查研究认为,地下水环境中反硝化作用的DO上限为2.0mg ·L-1; Desimone等[47]对地下水NO3--N污染晕监测分析时发现,在DO浓度为2~6mg ·L-1条件下仍有反硝化作用的存在,但速率很小[49]. 反硝化作用是受NO3-污染地下水的一种重要的自净过程,可以降低水中NO3-的污染水平,一般反硝化过程中,NO3-浓度降低伴随着δ15 N/δ18 O成比例增加,增加比率接近2 ∶1[50],应用这种线性关系,可以识别地下水是否发生反硝化作用.
据2014年5月和10月现场测定的DO数据(表 1),仅10月在桥村水源地测得的DO值为5.16mg ·L-1,小于6mg ·L-1,其余样点的DO值在6.88~13.55mg ·L-1之间,平均为7.92mg ·L-1,指示当地地下水环境并不适宜反硝化作用的进行. 从研究区的水文地质条件来看,南丹河到甘田坝的里湖中上游段,地下水埋藏较浅,小于30 m,而且地下河管道为很大的洞穴,明暗流交替,空气充足,属于好氧环境,硝化作用占主导地位,再次印证了以上推断. 地下河大多数样点δ15 N在4.79‰~11.58‰这一较小的变化范围,相反,δ18 O却有较广的分布范围,在-2.33‰~21.76‰间. 通过计算δ15 N/δ18 O得到的比值多数在-0.11~1.68之间,比值小于2,仅采于2014年10月的桥村水源地与凉风洞比值较大,分别为3.16和2.00(表 2). 从图 6也可以看出,δ15 N与NO3-的浓度间并不存在显著的相关关系,并未出现NO3-浓度降低伴随着δ15 N增加这一反硝化作用的线性关系. 综上分析,判断反硝化作用
并不是影响同位素变化的因素.
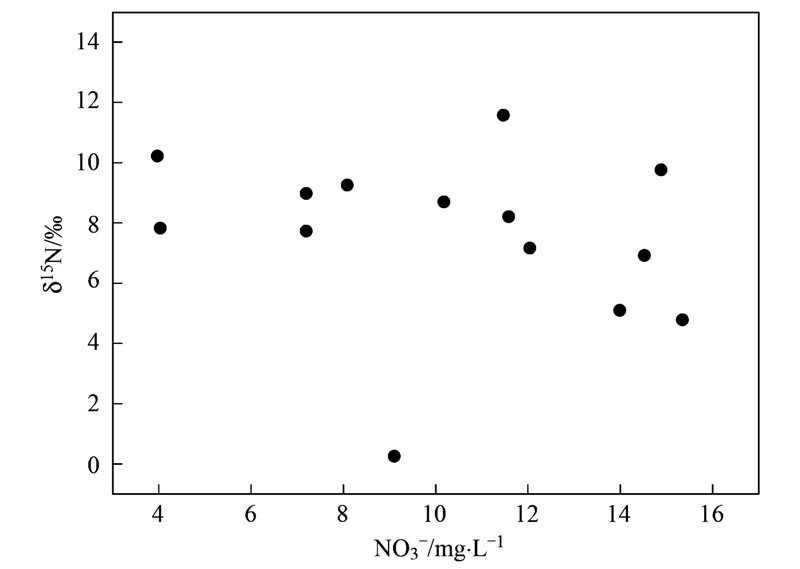 | 图 6 里湖地下水NO3-浓度与δ15 N的关系 Fig. 6 Relationship between the NO3- concentration and the δ15 N values |
氯在自然界中是相对稳定的元素,其可能来源包括农用钾肥,动物粪便,生活污水等,因此氯可以作为指示污染源的元素[51]. NO3-/Cl-可以用来识别NO3-浓度变化过程中的稀释效应和生物作用[52,53]. 2014年5月,里湖地下河中Cl-的平均浓度为2.97mg ·L-1,10月平均为5.39mg ·L-1,受雨水稀释作用明显,从图 7可以看出,大多数采样点的NO3-与Cl-呈一定的正相关趋势,指示它们具有相似的来源,5月的样品中NO3-与Cl-之间呈正相关(R2=0.461 0),这揭示样品NO3-受到大气降水和其他来源的混合作用.
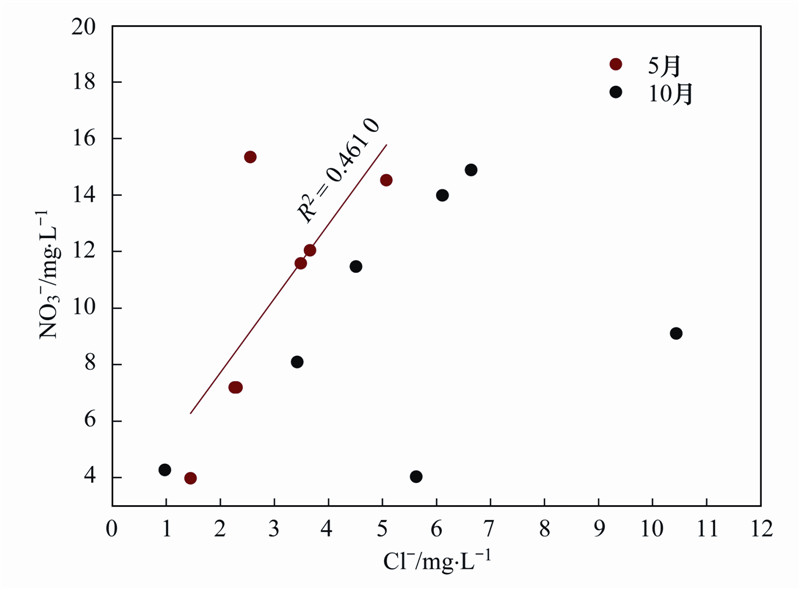 | 图 7 地下水Cl-和NO3-的关系 Fig. 7 Relationship between Cl- and NO3- concentrations in Lihu Lake underground water |
地下水δ15 N-NO3-值在0.26‰~11.58‰之间,平均为7.61‰,δ18 O-NO3-值在-2.33‰~21.76‰之间,平均为9.38‰. 图 8为较常用的不同来源的硝酸盐的N、O同位素的典型特征值,将里湖各采样点的N、O同位素在图 8中表示,主要是落在土壤氮、人畜粪便和污水的交叉区间,说明人类生活排放的污水、饲养家畜排出的粪便以及有机氮浓度较高的土壤是当地硝酸盐主要来源. 一般来说,土壤N的浓度较为稳定,人畜粪便和生产生活污水排放是引起里湖流域硝酸盐浓度在空间上波动变化的主要原因. 需要特别注意的是,在2014年5月采集的桥村水源地和小龙洞这两个点的N、O同位素主要落在大气沉降NO3-这一范围内,桥村水源地为当地的备用水源,居民注重对饮水水质的保护,小龙洞周围为大片的未开垦的山地,植被覆盖良好,远离人类活动,且这两个采样点的NO3-浓度显著低于其他采样点(图 4),这都说明在化肥,人畜粪便和污水等输入较少,森林覆盖条件较好的地区,雨季大气降水的混入也是当地地下水重要的氮源[54, 55, 56],且对样品N同位素影响较大; 在旱季的10月份,大气降水较少,土壤氮、人畜粪便和污水便成为了主要的污染来源.
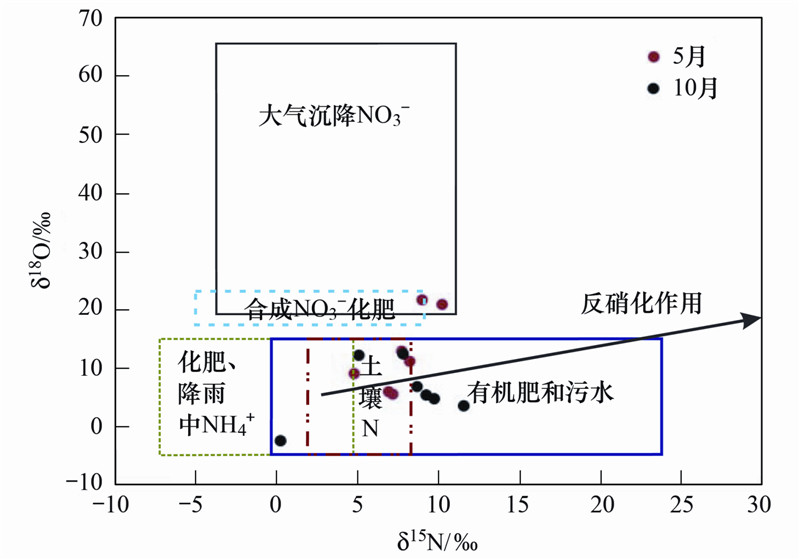 | 图 8 不同来源硝酸盐的δ15 N和δ18 O典型值 [57] Fig. 8 Typical ranges of δ15 N and δ18 O values of nitrate of different sources |
(1)里湖地下河水中主要阴离子为HCO3-,主要阳离子为Ca2+、Mg2+,基本水化学类型为HCO3-Ca型. 水体中离子的主要来源为碳酸盐岩的风化,其次各离子变化还受到人类活动的影响,除HCO3-外,其他离子浓度在里湖地下河上游、中游偏高,下游偏低. 受中亚热带季风气候的影响,地下水中各离子浓度呈现出雨季降低,旱季增大的特点.
(2)自2010年污水处理厂开始运营后,地下河中硫酸盐浓度有所降低,但仍然偏高,硝酸盐浓度略有增加,指示当地硝酸盐污染在加剧. 从空间变化上看,上游南丹河,拉易洞、中游凉风洞、甘田坝等人类活动强度较大,地下河硫酸盐、硝酸盐浓度较高,下游小龙洞处植被良好且远离人类活动干扰,其硫酸盐、硝酸盐浓度较低.
(3)里湖地下河δ34 S-SO2-4值分布在-4.12‰~-0.93‰这一相对较窄的范围,反映了当地硫源较为单一,并且该值域与大气降水的δ34 S值一致,因此认为大气降水输入是当地SO2-4的主要来源.
(4)将2014年与2010年相对比,里湖地下河中硝酸盐浓度呈增加趋势,表明硝酸盐污染在加剧. 根据地下水DO值,并结合NO3-与δ15 N、NO3-与Cl-、δ15 N-NO3-与δ18 O-NO3-的关系排除了反硝化作用对氮氧同位素的影响. 地下水硝酸盐的δ15 N值在0.26‰~11.58‰之间,δ18 O值在-2.33‰~21.76‰之间,指示土壤氮、人畜粪便和污水是研究区硝酸盐的主要贡献者,为有针对地开展硝酸盐污染防治提供了依据.
| [1] | 张翠云, 张胜, 马琳娜, 等. 污灌区地下水硝酸盐污染来源的氮同位素示踪[J]. 地球科学——中国地质大学学报, 2012, 37 (2): 350-356. |
| [2] | 刑萌, 刘卫国, 胡婧. 浐河、涝河河水硝酸盐氮污染来源的氮同位素示踪[J]. 环境科学, 2010, 31 (10): 2305-2310. |
| [3] | 汪智军, 杨平恒, 旷颖仑, 等. 基于15N同位素示踪技术的地下河硝态氮来源时空变化特征分析[J]. 环境科学, 2009, 30 (12): 3548-3554. |
| [4] | Choi W J, Han G H, Lee S M, et al. Impact of land-use types on nitrate concentration and δ15N in unconfined groundwater in rural areas of Korea[J]. Agriculture, Ecosystems & Environment, 2007, 120 (2-4): 259-268. |
| [5] | Wilson G B, Andrews J N, Bath A H. Dissolved gas evidence for denitrification in the Lincolnshire Limestone groundwaters, eastern England[J]. Journal of Hydrology, 1990, 113 (1-4): 51-60. |
| [6] | Vogel J C, Talma A S, Heaton T H E. Gaseous nitrogen as evidence for denitrification in groundwater[J]. Journal of Hydrology, 1981, 50 : 191-200. |
| [7] | 贾小妨, 李玉中, 徐春英, 等. 氮、氧同位素与地下水中硝酸盐溯源研究进展[J]. 中国农学通报, 2009, 25 (14): 233-239. |
| [8] | Kohl D H, Shearer G B, Commoner B. Fertilizer nitrogen: contribution to nitrate in surface water in a corn belt watershed[J]. Science, 1971, 174 (4016): 1331-1334. |
| [9] | Chen Z X, Yu L, Liu W G, et al. Nitrogen and oxygen isotopic compositions of water-soluble nitrate in Taihu Lake water system, China: implication for nitrate sources and biogeochemical process[J]. Environmental Earth Sciences, 2014, 71 (1): 217-223. |
| [10] | 徐志伟, 张心昱, 于贵瑞, 等. 中国水体硝酸盐氮氧双稳定同位素溯源研究进展[J]. 环境科学, 2014, 35 (8): 3230-3238. |
| [11] | Liu T, Wang F, Michalski G, et al. Using 15N, 17O, and 18O to determine nitrate sources in the Yellow River, China[J]. Environmental Science & Technology, 2013, 47 (23): 13412-13421. |
| [12] | 任玉芬, 张心昱, 王效科, 等. 北京城市地表河流硝酸盐氮来源的氮氧同位素示踪研究[J]. 环境工程学报, 2013, 7 (5): 1636-1640. |
| [13] | Jia G D, Chen F J. Monthly variations in nitrogen isotopes of ammonium and nitrate in wet deposition at Guangzhou, south China [J]. Atmospheric Environment, 2010, 44 (19): 2309-2315. |
| [14] | Savard M M, Somers G H, Smirnoff A, et al. Nitrate isotopes unveil distinct seasonal N-sources and the critical role of crop residues in groundwater contamination [J]. Journal of Hydrology, 2010, 381 (1-2): 134-141. |
| [15] | 刘君, 陈宗宇. 利用稳定同位素追踪石家庄市地下水中的硝酸盐来源[J]. 环境科学, 2009, 30 (6): 1602-1607. |
| [16] | Heaton T H E. Isotopic studies of nitrogen pollution in the hydrosphere and atmosphere: a review[J]. Chemical Geology: Isotope Geoscience Section, 1986, 59 : 87-102. |
| [17] | 赵敏, 曾成, 杨睿, 等. 贵州普定灯盏河岩溶泉的硫同位素季节变化特征[J]. 地球科学与环境学报, 2012, 34 (3): 83-88. |
| [18] | Li X D, Liu C Q, Liu X L, et al. Identification of dissolved sulfate sources and the role of sulfuric acid in carbonate weathering using dual-isotopic data from the Jialing River, Southwest China[J]. Journal of Asian Earth Sciences, 2011, 42 (3): 370-380. |
| [19] | 肖红伟, 肖化云, 龙爱民, 等. 贵阳大气降水硫同位素地球化学特征[J]. 地球化学, 2011, 40 (6): 559-565. |
| [20] | Li X D, Masuda H, Ono M, et al. Contribution of atmospheric pollutants into groundwater in the northern Sichuan Basin, China[J]. Geochemical Journal, 2006, 40 (1): 103-119. |
| [21] | 储雪蕾. 北京地区地表水的硫同位素组成与环境地球化学[J]. 第四纪研究, 2000, 20 (1): 87-96. |
| [22] | 黄丽秋, 黎玉梅, 周慧僚. 南丹县45年气温、降水变化特征分析[J]. 农家之友(理论版), 2010, (12): 36-38. |
| [23] | 马振杰. 城市生活废弃物对岩溶地下河的污染研究——以南丹县里湖地下河为例[D]. 重庆: 西南大学, 2011. 33-43. |
| [24] | 郭芳, 王文科, 姜光辉, 等. 岩溶地下河污染物运移特征及自净能力——以广西里湖地下河为例[J]. 水科学进展, 2014, 25 (3): 414-419. |
| [25] | 张连凯, 杨慧. 岩溶地下河中砷迁移过程及其影响因素分析——以广西南丹县里湖地下河为例[J]. 中国岩溶, 2013, 32 (4): 377-383. |
| [26] | 沈照理, 朱宛华, 钟佐燊. 水文地球化学基础[M]. 北京: 地质出版社, 1993. 68-69. |
| [27] | 刘丛强. 生物地球化学过程与地表物质循环——西南喀斯特流域侵蚀与生源要素循环[M]. 北京: 科学出版社, 2007. 311-314. |
| [28] | Han G L, Liu C Q. Water geochemistry controlled by carbonate dissolution: a study of the river waters draining karst-dominated terrain, Guizhou Province, China[J]. Chemical Geology, 2004, 204 (1-2): 1-21. |
| [29] | Montoroi J P, Grünberger O, Nasri S. Groundwater geochemistry of a small reservoir catchment in Central Tunisia[J]. Applied Geochemistry, 2002, 17 (8): 1047-1060. |
| [30] | Macpherson G L. Hydrogeology of thin limestones: the Konza Prairie long-term ecological research site, Northeastern Kansas[J]. Journal of Hydrology, 1996, 186 (1-4): 191-228. |
| [31] | Hanshaw B B, Back W. Major geochemical processes in the evolution of carbonate—aquifer systems[J]. Journal of Hydrology, 1979, 43 (1-4): 287-312. |
| [32] | 郭照冰, 董琼元, 陈天, 等. 硫稳定同位素对环境污染物的示踪[J]. 南京工程信息大学学报(自然科学版), 2010, 2 (5): 426-430. |
| [33] | 宋柳霆, 刘丛强, 王中良, 等. 贵州红枫湖硫酸盐来源及循环过程的硫同位素地球化学研究[J]. 地球化学, 2008, 37 (6): 556-564. |
| [34] | 韩志钧, 金占省. 贵州省水文地质志[M]. 北京: 地震出版社, 1996. 1-508. |
| [35] | 林耀庭, 曹善行, 熊淑君, 等. 四川盆地海相三叠系硬石膏和盐卤水的硫同位素组成及意义[J]. 化工矿产地质, 1997, 19 (3): 171-176. |
| [36] | Querol X, Alastuey A, Chaves A, et al. Sources of natural and anthropogenic sulphur around the Teruel power station, NE Spain. Inferences from sulphur isotope geochemistry[J]. Atmospheric Environment, 2000, 34 (2): 333-345. |
| [37] | Moncaster S J, Bottrell S H, Tellam J H, et al. Migration and attenuation of agrochemical pollutants: insights from isotopic analysis of groundwater sulphate[J]. Journal of Contaminant Hydrology, 2000, 43 (2): 147-163. |
| [38] | Mizota C, Sasaki A. Sulfur isotope composition of soils and fertilizers: differences between Northern and Southern Hemispheres[J]. Geoderma, 1996, 71 (1-2): 77-93. |
| [39] | Chen A Z, Wei H H, Tan F. Analysis of the temporal-spatial distribution and seasonal variation of the acid rain in Guangxi province[J]. Meteorological and Environmental Research, 2010, 1 (1): 62-65. |
| [40] | 张洪斌, 胡霭琴, 卢承祖, 等. 华南地区酸沉降的硫同位素组成及其环境意义[J]. 中国环境科学, 2002, 22 (2): 165-169. |
| [41] | 洪业汤, 张鸿斌, 朱咏煊, 等. 中国大气降水的硫同位素组成特征[J]. 自然科学进展: 国家重点实验室通讯, 1994, 4 (6): 741-745. |
| [42] | 邓林, 曹玉清, 王文科. 地下水NO3-氮与氧同位素研究进展[J]. 地球科学进展, 2007, 22 (7): 716-724. |
| [43] | Buzek F, Kadlecova R, Knezek M. Model reconstruction of nitrate pollution of riverbank filtration using 15N and 18O data, Karany, Czech Republic[J]. Applied Geochemistry, 2006, 21 (4): 656-674. |
| [44] | Kellman L M, Hillaire-Marcel C. Evaluation of nitrogen isotopes as indicators of nitrate contamination sources in an agricultural watershed[J]. Agriculture, Ecosystems & Environment, 2003, 95 (1): 87-102. |
| [45] | Wassenaar L I. Evaluation of the origin and fate of nitrate in the Abbotsford aquifer using the isotopes of 15N and 18O in NO3-[J]. Applied Geochemistry, 1995, 10 (4): 391-405. |
| [46] | 周迅, 姜月华. 氮、氧同位素在地下水硝酸盐污染研究中的应用[J]. 地球学报, 2007, 28 (4): 389-395. |
| [47] | Desimone L A, Howes B L. Nitrogen transport and transformations in a shallow aquifer receiving wastewater discharge: a mass balance approach[J]. Water Resources Research, 1998, 34 (2): 271-285. |
| [48] | Gillham R W, Cherry J A. Field evidence of denitrification in shallow ground water flow systems[J]. Water Pollution Research. Canada, 1978, 13 (1): 53-71. |
| [49] | 吴耀国. 地下水环境中反硝化作用[J]. 环境污染治理技术与设备, 2002, 3 (3): 27-31. |
| [50] | Amberger A, Schmidt H L. Natürliche Isotopengehalte von Nitrat als Indikatoren für dessen Herkunft[J]. Geochimica et Cosmochimica Acta, 1987, 51 (10): 2699-2705. |
| [51] | Mengis M, Schiff S L, Harris M, et al. Multiple geochemical and isotopic approaches for assessing ground water NO3-elimination in a riparian zone[J]. Ground Water, 1999, 37 (3): 448-459. |
| [52] | Widory D, Petelet-Giraud E, Négrel P, et al. Tracking the sources of nitrate in groundwater using coupled nitrogen and boron isotopes: a synthesis[J]. Environmental Science & Technology, 2005, 39 (2): 539-548. |
| [53] | Koba K, Tokuchi N, Wada E, et al. Intermittent denitrification: the application of a 15N natural abundance method to a forested ecosystem[J]. Geochimica et Cosmochimica Acta, 1997, 61 (23): 5043-5050. |
| [54] | Schiff S L, Devito K J, Elgood R J, et al. Two adjacent forested catchments: Dramatically different NO3- export[J]. Water Resources Research, 2002, 38 (12): 28-1-28-13. |
| [55] | Kendall C, Aravena R. Nitrate isotopes in groundwater systems[A]. In: Cook P, Hercze A L (eds). Environmental Tracers in SubSurface Hydrology[M]. Dordrecht: Kluwer Academic Publishers, 2000. 261-297. |
| [56] | Durka W, Schulze E D, Gebauer G, et al. Effects of forest decline on uptake and leaching of deposited nitrate determined from 15N and 18O measurements[J]. Nature, 1994, 372 (6508): 765-767. |
| [57] | Kendall C. Tracing nitrogen sources and cycling in catchments[A]. In: Kendall C, McDonnell J J (eds). Isotope Tracers in Catchment Hydrology[M]. Amsterdam: Elsevier Science B V, 1998. 519-576. |
 2015, Vol. 36
2015, Vol. 36


