2. 湖北省环境监测中心站, 武汉 430072
2. Hubei Environmental Monitoring Central Station, Wuhan 430072, China
四环素类抗生素是由放线菌产生的一类抗生素,包括金霉素、 土霉素、 四环素及一些半合成衍生物等. 其中,由于四环素(TC)对革兰氏阳性菌、 革兰氏阴性菌、 立克次氏体和衣原体等微生物均可发挥作用,具有广谱抗菌性和良好的治疗效果[1],因此被广泛应用于预防和治疗人类、 动物和植物的疾病,同时在畜牧业中做为饲料添加剂促进生长[2]. 在生物代谢过程中,绝大部分四环素都通过粪便和尿液直接排出体外[3],最终进入到水环境中,对水生生态系统造成危害,同时诱导环境中抗性基因的产生,造成持续性的污染[4]. 目前,四环素在自来水、 饮用水、 地表水等环境介质中均有检出,浓度集中在 ng ·L-1~μg ·L-1[5, 6, 7].
吸附法由于具有高效、 无副产物等特点,在水中四环素的去除方面得到了广泛的应用. 目前研究的材料包括石墨烯[8]、 氧化铝[9]、 单壁和多壁碳纳米管[10]、 沸石[11]、 活性炭[12]等. 纳米级碳基材料具有大的比表面积和丰富的孔隙结构,已经被证实能够快速、 高效地去除水中的四环素[13]. 碳纳米材料中的石墨烯和碳纳米管由于其独特的结构和良好的吸附性能是近年来研究的热点. 它们的制备方法主要包括石墨电弧法、 热解法、 氧化还原法[14]等,这些生产方法成本高、 能耗大,难以大量生产应用于实际,限制了碳纳米材料的发展. Yin等[15]使用电化学方法,在Li-Na-K碳酸盐的共熔体系中捕集CO2,生成一种纳米级的不定形碳粉. 该方法具有生产成本低、 能耗小、 生产过程简单等优点,同时在生成过程中没有有毒有害物质产生,是一种环境友好型的材料合成方法. 通过前期的研究可知,碳粉呈雾状,具有很大的比表面积(616 m2 ·g-1),同时通过Zeta电位分析,当溶液pH值大于2时,表面带有负电荷,是十分理想的吸附材料.
本研究测试了该碳粉对水中四环素的吸附性能,并结合吸附剂和吸附质的特性讨论吸附机制.
1 材料与方法
1.1 实验材料与仪器
1.1.1 材料
供试碳粉由Yin等提供,吸附剂的具体表征及参数见文献[15].
四环素: 购自Solarbio公司,其分子式为C22H24N2 O8 ·HCl,纯度≥98%; 乙腈(色谱纯)、 乙酸铵(色谱纯,≥99.0%): 购自Sigma-Aldrich公司; 其他化学试剂均为分析纯; 实验用水均为去离子水.
1.1.2 仪器
1290超高效液相色谱与6460 QQQ质谱联用仪(Angilent,美国),SHA-B水浴恒温振荡器(上海比朗仪器有限公司),FE20 pH计(METTLER TOLEDO,瑞士).
1.2 实验方法
通过预实验可知碳粉对四环素的吸附在17 h内可达到平衡,溶液初始pH值为4时,吸附量最大. 每组实验均设置碳粉和四环素溶液空白,及两个平行样. 由于在制作过程中碳粉的产量较少,同时预实验结果显示同样条件下碳粉的用量在2 mg时吸附量最大. 因此,每组实验都使用分析天平准确称量2 mg碳粉于100 mL锥形瓶中,加入一定浓度的四环素溶液50 mL,聚四氟乙烯膜封口,于水浴恒温振荡器中160r ·min-1振荡平衡17 h.
1.2.1 吸附动力学
四环素溶液浓度为6 mg ·L-1,温度为(25±0.5)℃. 分别在0、 1、 2、 4、 8、 16、 32、 64、 128、 256、 512和1 024 min取样 2 mL,经0.22 μm混合纤维素酯滤膜过滤后,测定滤液中四环素的浓度.
1.2.2 吸附等温线
四环素溶液起始浓度范围1~80 mg ·L-1,振荡平衡17 h后,取样测定,其它实验操作同1.2.1节.
1.2.3 pH和离子强度对吸附的影响
测定pH对吸附的影响时,体系的pH范围2~11,此时体系中无外加阳离子. 测定离子强度对吸附影响时,Ca(Na)离子浓度范围0~0.5mol ·L-1,此时体系pH为4,振荡平衡17 h后,取样测定,其它实验操作同1.2.1节.
1.2.4 解吸实验
当体系中吸附达到平衡后,溶液立即过0.45 μm的滤膜. 使用等量的去离子水多次冲洗滤膜,将膜上的碳粉转入100 mL锥形瓶中,分别加入50 mL 0.25mol ·L-1的CaCl2和NaCl溶液. 25℃下,振荡平衡20 h后,取样测定.
1.2.5 吸附量的计算
碳粉吸附四环素达到吸附平衡时的吸附量(qe,mg ·g-1)使用以下公式进行计算:
液相色谱条件: Eclipse Plus-C18色谱柱(100 mm×2.1 mm,1.8 μm,Agilent),柱温40℃,进样体积10 μL,采用0.2%甲酸2 mmol ·L-1乙酸铵水溶液和乙腈做为流动相,流动相配比为75 ∶25,流速0.3mL ·min-1.
质谱条件: 电喷雾电离源(ESI)正离子方式,选择MRM模式,干燥气温度325℃,流量5L ·min-1,鞘气温度350℃,流量11L ·min-1. 四环素的母离子和子离子的质荷比分别为445和410.1,碰撞电压130 V,碰撞能15 eV.
2 结果与讨论
2.1 碳粉对四环素的吸附动力学
为了阐述吸附的过程,分别将实验结果拟合了拟一级动力学模型、 拟二级动力学模型和颗粒内扩散模型(图 1~3). 计算公式如下:
拟一级动力学模型和拟二级动力学模型分别描述了与吸附容量有关的单因子和多因子控制下的吸附. 颗粒内扩散模型用来确定吸附的限速过程[16].
由表 1可知,拟二级动力学方程能够更好地拟合吸附的过程,R2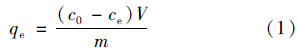
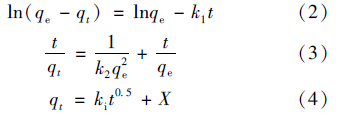
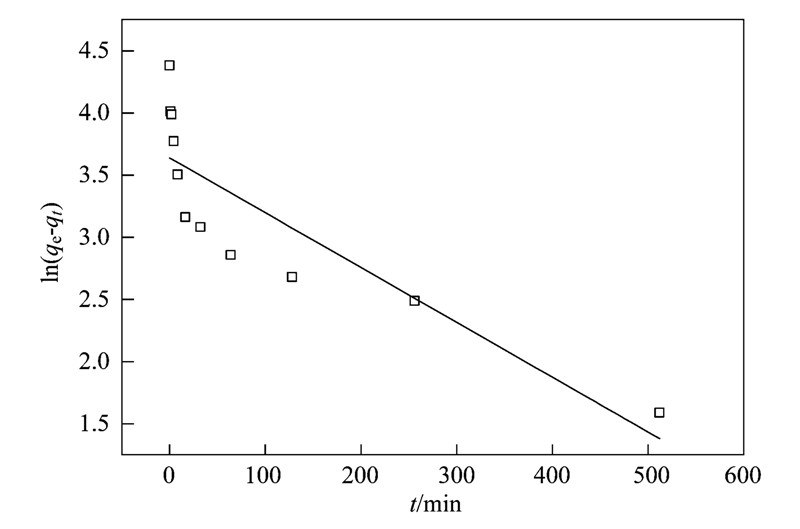
图 1 碳粉吸附四环素的拟一级动力学模型
Fig. 1 Pseudo-first-order model of tetracycline adsorption to carbon powder
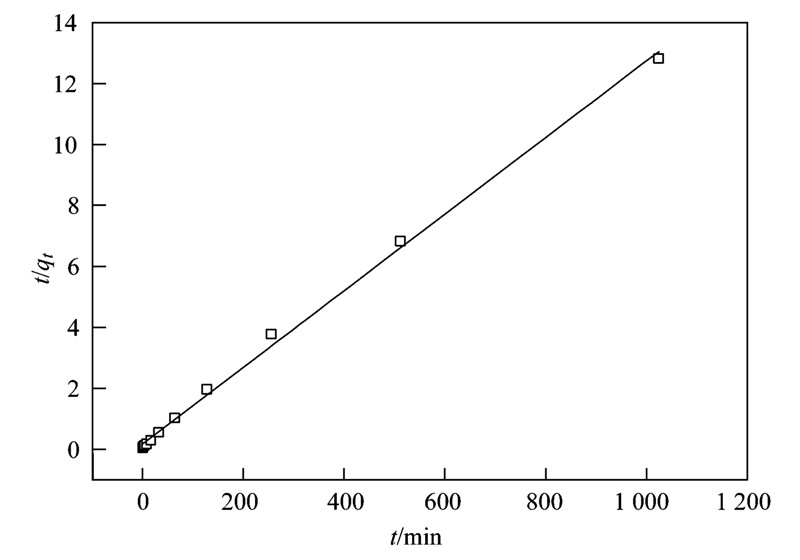
图 2 碳粉吸附四环素的拟二级动力学模型
Fig. 2 Pseudo-second-order model of tetracycline adsorption to carbon powder
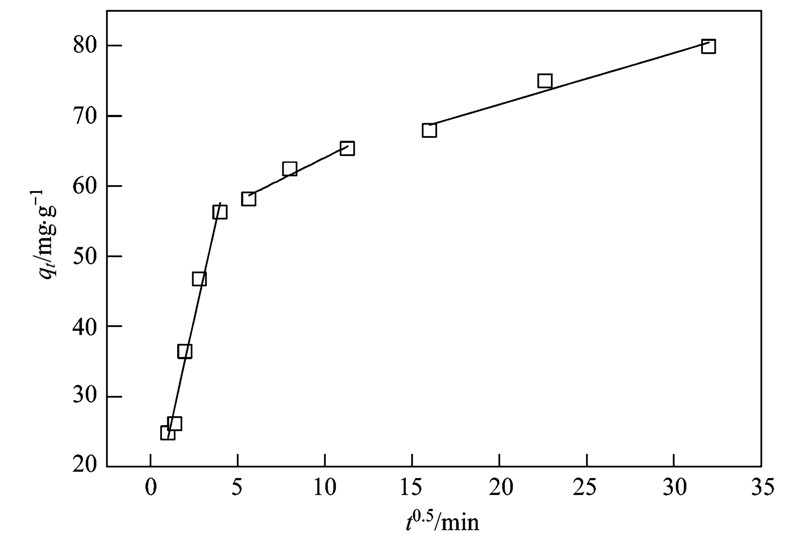
图 3 碳粉对四环素吸附的颗粒内扩散模型
Fig. 3 Intra particle diffusion model of tetracycline adsorption to carbon powder
| 表 1 碳粉对四环素吸附的吸附动力学模型常数及相关系数 Table 1 Parameters of kinetic models for tetracycline adsorption to carbon powder |
碳粉对四环素吸附过程可分3个阶段. 第一阶段为碳粉表面的吸附,第二阶段为颗粒内快速扩散过程,第三阶段边界层效应增大,颗粒内扩散缓慢. 图 3也明显呈现了吸附的3个阶段. 同时,图形没有过原点,说明颗粒内扩散不是限制吸附速率的步骤,因此,在吸附开始的时候膜扩散或化学反应可能控制吸附的速率. 2.2 碳粉对四环素的吸附等温线
在298K下进行了吸附等温线的测定. 为了阐明碳粉对四环素的吸附特性,分别拟合了Freundlich和Langmuir方程(图 4):

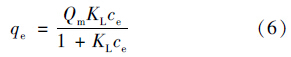
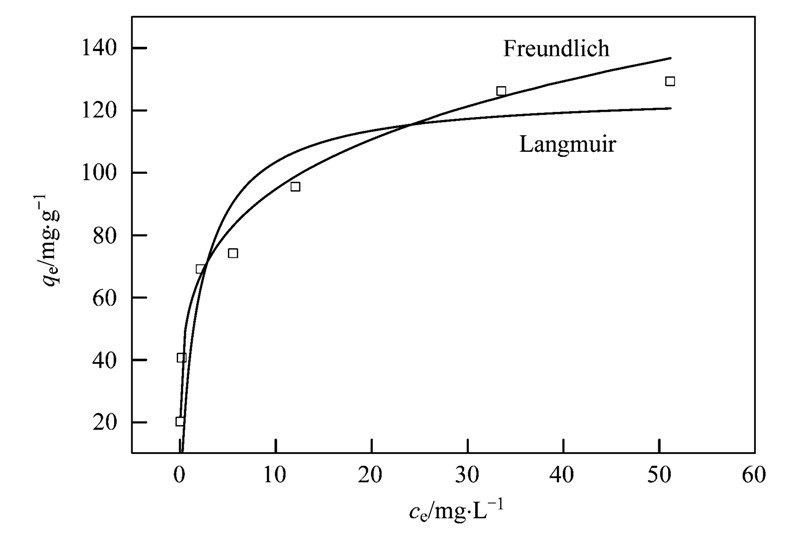 | 图 4 碳粉对四环素吸附的吸附等温线模型 Fig. 4 Adsorption isotherms of tetracycline to carbon powder |
由表 2可知,与Langmuir吸附等温模型相比,Freundlich吸附等温模型可以更好地描述碳粉对四环素的等温吸附行为. Freundlich模型参数1/n介于0~1之间,表明碳粉对四环素的吸附过程属于优惠吸附[18]. Langmuir模型还计算出了碳粉对四环素的最大吸附量Qm,反映吸附能力的大小,值越大,吸附能力也越大[19]. 如表 3所示,与其他吸附剂相比,碳粉在较低的温度下就具有更高的吸附量,对四环素表现出了良好的吸附性能.
| 表 2 碳粉对四环素吸附的吸附等温线模型常数及相关系数 Table 2 Parameters of the Freundlich and Langmuir equations for tetracycline adsorption to carbon powder |
| 表 3 不同吸附剂对四环素的吸附性能比较 1) Table 3 Comparison of different adsorption performances for tetracycline |
Langmuir 等温模型参数RL可以表述为:
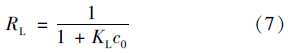
经计算,Langmuir模型参数RL值(四环素初始浓度1~80mg ·L-1范围内,碳粉对四环素的RL值介于0.19~0.93之间)均在0~1之间,进一步说明了该吸附是优惠吸附. 2.3 吸附热力学
为了测定温度对吸附的影响,分别在293~308 K下进行吸附实验. 吸附过程中热力学参数的变化通过以下方程进行计算:

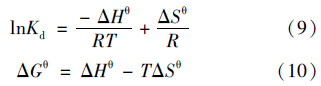
ΔHθ是正值,表明吸附是一个吸热过程,实验结果也显示随着温度的升高碳粉对四环素的吸附容量逐渐增加. 如表 4所示,随着温度的升高,ΔGθ逐渐降低,说明较高的温度对吸附有利. ΔGθ是吸附驱动力的体现,为负值,说明碳粉吸附四环素是自发的. ΔHθ值在 50~65 kJ ·mol-1之间,属于化学吸附热范围,说明吸附的作用以化学作用为主[24].
| 表 4 碳粉对四环素吸附的热力学相关参数 Table 4 Thermodynamic parameters for tetracycline to carbon powder |
在反应液初始pH值为2~11条件下考察了碳粉吸附四环素的行为,结果如图 5所示. 当pH值介于2~4之间时,碳粉对四环素的吸附量随着pH值的升高而升高,而当pH值大于4,碳粉对四环素的吸附量则随着pH值的升高而降低. 溶液在酸性较强时吸附能力最强. 这与四环素的性质有关. 由于四环素带有氨基、 羧基、 苯酚、 醇、 酮等有极性、 可电离的官能团,四环素在不同pH值下形态不同. 四环素有3个酸离解常数,分别是3.3、 7.7、 9.7[8]. 因此,当溶液pH值小于3.3时,四环素溶液以H4TC+离子占主导; 当pH值在3.4和7.7之间时,四环素溶液以H3TC形态占主导; 当pH值在7.7和9.7之间时,四环素溶液以H2TC-形态占主导; 当溶液pH值大于9.7时,四环素溶液以HTC2-占主导. 当溶液中酸性较强时,四环素分子上的阳离子基团可以通过阳离子交换或静电引力的方式与碳粉表面的负电荷结合而产生吸附作用. 但当pH值过低(<4)时,过多的H+的竞争作用,反而降低了四环素的吸附作用[25]. 当溶液中pH值为中性到弱碱性时,吸附量呈上升趋势,说明碳粉对中性离子也有一定的吸附作用. 由于中性离子相对于质子化的离子有更大的疏水性,可通过疏水作用与碳粉上的疏水位点相结合. 同时,四环素分子中含有许多含氧官能团,还可能通过氢键与碳粉结合.
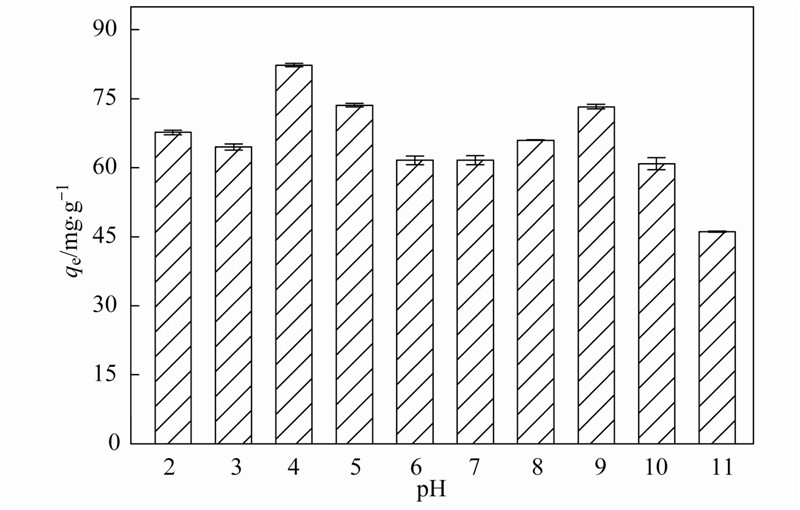 | 图 5 pH值对碳粉吸附四环素的影响 Fig. 5 Effect of pH value on the adsorption of tetracycline to carbon powder |
实验观察了溶液中不同浓度的Ca2+和Na+对吸附的影响. 如图 6所示,对于Ca2+来说,随着离子强度的增加,碳粉对四环素的吸附量有一定程度上的减少,而对于Na+来说,现象不明显. 可能由于Ca2+更容易与四环素螯合,从而阻碍了碳粉对四环素的吸附. 同时测定了溶液中Ca2+和Na+在吸附前后浓度的差别,发现溶液中Ca2+的浓度在吸附后有一定程度上的下降,因此推测,Ca2+对吸附的影响主要作用是对四环素吸附位点的竞争,这也从侧面证实了碳粉对四环素吸附的原理主要是阳离子交换作用. Chang[26]等也发现了同样的现象. Parolo等[27]研究了在有阳离子存在的情况下四环素离子的形态变化,发现四环素能与溶液中的金属阳离子发生螯合反应,也可能对吸附产生一定的影响,这一作用会受溶液pH值的影响. Gao等[8]推测阳离子会产生静电屏蔽作用,从而影响吸附作用.
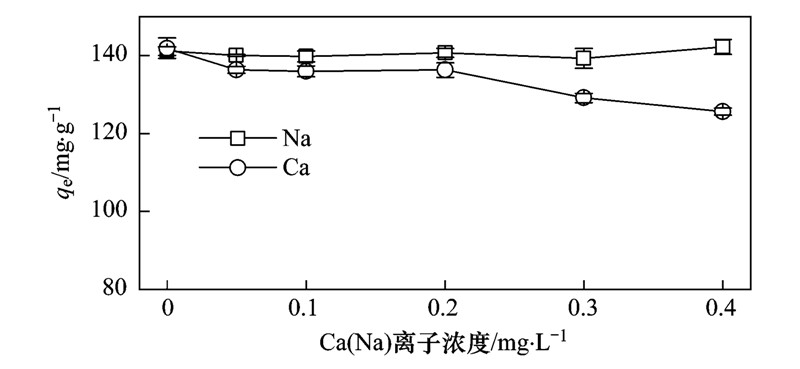 | 图 6 不同阳离子浓度对碳粉吸附四环素的影响 Fig. 6 Effects of cation concentrations on the tetracycline adsorption to carbon powder |
在吸附达到平衡后,立即使用0.25mol ·L-1的CaCl2或NaCl溶液对四环素初始浓度为6mg ·L-1和15mg ·L-1的样品进行了解吸实验. CaCl2的解吸效率分别为14.3%和25%,NaCl的解吸效率分别为7.42%和18.28%. CaCl2比NaCl的解吸效率高. 这一研究结果与Oleszczuk等[28]的研究结果类似. 作者研究了碳纳米管对氧四环素的吸附和解吸作用,通过解吸动力学的研究,发现解吸过程分为两个阶段. 在碳纳米管表面的四环素分子首先占据了高能的吸附位点,因此低浓度的四环素很难从吸附剂中解吸出来. 而较高浓度的四环素的解吸率更高,说明在解吸的第二阶段四环素可以更快、 更容易地从吸附剂中解吸出来. 解吸效率较低也从侧面反映了碳粉对四环素吸附化学作用力很强,可以高效地将四环素从水中去除. 但解吸效率低也说明该碳粉不能很好的循环使用,后期会对碳粉的解吸及其循环利用作进一步的研究. 3 结论
(1)在Li-Na-K碳酸盐共熔体系中生成的纳米级不定形碳粉对水中的四环素表现出较好的吸附性能,最大吸附容量为127.76mg ·g-1.
(2)实验通过动力学方程及吸附等温线的拟合发现,碳粉对四环素的吸附更符合拟二级动力学方程及Freundlich吸附等温线,表现为优惠吸附.
(3)通过热力学的计算可知,碳粉对四环素的吸附是吸热的、 自发的,以化学吸附为主.
(4)吸附易受溶液初始pH值的影响,阳离子浓度对吸附有一定的影响.
(5)使用CaCl2和NaCl溶液对吸附剂进行解吸,解吸效率低.
(6)碳粉对水中的四环素有较大的吸附容量,在水处理领域有较好的应用前景. 后续还可对碳粉的结构进行修饰和优化,以便得到更大的吸附容量.
| [1] | Chopra I, Roberts M. Tetracycline antibiotics: mode of action, applications, molecular biology, and epidemiology of bacterial resistance [J]. Microbiology and Molecular Biology Reviews, 2001, 65 (2): 232-260. |
| [2] | Zhang X X, Zhang T, Fang H H P. Antibiotic resistance genes in water environment [J]. Applied Microbiology and Biotechnology, 2009, 82 (3): 397-414. |
| [3] | Sarmah A K, Meyer M T, Boxall A B A. A global perspective on the use, sales, exposure pathways, occurrence, fate and effects of veterinary antibiotics(VAs) in the environment [J]. Chemosphere, 2006, 65 (5): 725-759. |
| [4] | Kim S R, Nonaka L, Suzuki S. Occurrence of tetracycline resistance genes tet(M) and tet(S) in bacteria from marine aquaculture sites [J]. FEMS Microbiology Letters, 2004, 237 (1): 147-156. |
| [5] | Kim S, Jensen J N, Aga D S, et al. Tetracycline as a selector for resistant bacteria in activated sludge [J]. Chemosphere, 2007, 66 (9): 1643-1651. |
| [6] | Kolpin D W, Furlong E T, Meyer M T, et al. Pharmaceuticals, hormones, and other organic wastewater contaminants in U. S. streams, 1999-2000: A national reconnaissance [J]. Environmental Science & Technology, 2002, 36 (6): 1202-1211. |
| [7] | Choi K J, Kim S G, Kim C W, et al. Determination of antibiotic compounds in water by on-line SPE-LC/MSD [J]. Chemosphere, 2007, 66 (6): 977-984. |
| [8] | Gao Y, Li Y, Zhang L, et al. Adsorption and removal of tetracycline antibiotics from aqueous solution by graphene oxide [J]. Journal of Colloid and Interface Science, 2012, 368 (1): 540-546. |
| [9] | Chen W R, Huang C H. Adsorption and transformation of tetracycline antibiotics with aluminum oxide [J]. Chemosphere, 2010, 79 (8): 779-785. |
| [10] | Ji L L, Shao Y, Xu Z Y, et al. Adsorption of monoaromatic compounds and pharmaceutical antibiotics on carbon nanotubes activated by KOH etching [J]. Environmental Science & Technology, 2010, 44 (16): 6429-6436. |
| [11] | An W H, Xiao H, Yu M, et al. Adsorptive removal of trace oxytetracycline from water by acid-modified zeolite: influencing factors [J]. Water Science & Technology, 2013, 68 (11): 2473-2478. |
| [12] | Huang L H, Sun Y Y, Wang W L, et al. Comparative study on characterization of activated carbons prepared by microwave and conventional heating methods and application in removal of oxytetracycline(OTC) [J]. Chemical Engineering Journal, 2011, 171 (3): 1446-1453. |
| [13] | Lin Y X, Xu S, Li J. Fast and highly efficient tetracyclines removal from environmental waters by graphene oxide functionalized magnetic particles [J]. Chemical Engineering Journal, 2013, 225 (1): 679-685. |
| [14] | Tung V C, Allen M J, Yang Y, et al. High-throughput solution processing of large-scale graphene [J]. Nature Nanotechnology, 2009, 4 (1): 25-29. |
| [15] | Yin H Y, Mao X H, Tang D Y, et al. Capture and electrochemical conversion of CO2 to value-added carbon and oxygen by molten salt electrolysis [J]. Energy & Environmental Science, 2013, 6 (5): 1538-1545. |
| [16] | Zhu X D, Liu Y C, Qian F, et al. Preparation of magnetic porous carbon from waste hydrochar by simultaneous activation and magnetization for tetracycline removal [J]. Bioresource Technology, 2014, 154: 209-214. |
| [17] | 黎园, 赵纯, 邓慧萍. 2种孔径沸石分子筛对水中土霉素的去除研究[J]. 环境科学, 2010, 31 (4): 990-995. |
| [18] | Hameed B H. Equilibrium and kinetic studies of methyl violet sorption by agricultural waste[J]. Journal of Hazardous Materials, 2008, 154 (1-3): 204-212. |
| [19] | 童锡臻, 石宝友, 解岳, 等. 改性活性炭对水中 PFOS 的吸附去除研究[J]. 环境科学, 2012, 33 (9): 3132-3138. |
| [20] | Liao P, Zhan Z, Dai J, et al. Adsorption of tetracycline and chloramphenicol in aqueous solutions by bamboo charcoal: A batch and fixed-bed column study[J]. Chemical Engineering Journal, 2013, 228: 496-505. |
| [21] | Guan W S, Wang X, Pan J M, et al. Synthesis of magnetic halloysite composites for the effective removal of tetracycline hydrochloride from aqueous solutions[J]. Adsorption Science & Technology, 2012, 30 (7): 579-592. |
| [22] | 陈瑞萍, 张丽, 于洁, 等. 活性污泥对四环素的吸附性能研究[J]. 环境科学, 2012, 33 (1): 156-162. |
| [23] | 叶林静, 关卫省, 卢勋, 等. 改性纳米Fe3O4去除水溶液中四环素的研究[J]. 安全与环境学报, 2014, 14 (1): 202-207. |
| [24] | 张爱丽, 刘玥, 周集体, 等. 壳聚糖复合树脂对亚硝酸盐氮的吸附性能[J]. 环境科学, 2009, 30 (2): 463-468. |
| [25] | 高鹏, 莫测辉, 李彦文, 等. 高岭土对喹诺酮类抗生素吸附特性的初步研究[J]. 环境科学, 2011, 32 (6): 1740-1744. |
| [26] | Chang P H, Li Z H, Jean J S, et al. Adsorption of tetracycline on 2: 1 layered non-swelling clay mineral illite [J]. Applied Clay Science, 2012, 67-68: 158-163. |
| [27] | Parolo M E, Avena M J, Savini M C, et al. Adsorption and circular dichroism of tetracycline on sodium and calcium-montmorillonites [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2013, 417: 57-64. |
| [28] | Oleszczuk P, Pan B, Xing B S. Adsorption and desorption of oxytetracycline and carbamazepine by multiwalled carbon nanotubes [J]. Environmental Science & Technology, 2009, 43 (24): 9167-9173. |
 2015, Vol. 36
2015, Vol. 36


