吸附技术在水处理领域中占有重要的地位,对水中的色度、 浊度、 重金属和有机物等有较好的净化行为[1],原水与吸附剂发生接触和传质作用而使水中污染物被吸附去除. 从流态角度上讲,吸附床中吸附填料(吸附剂)一般处于固定态,水相的流动不会导致吸附剂的流态发生变化. 这种固定床吸附反应器在工程上已经有了广泛的应用[2,3, 4]. 近年来,基于固-液流化床的吸附反应工艺引起研究者的关注[5,6,7,8]. 在流化床吸附反应器中,水相流动向固相吸附剂施加剪切力,使吸附剂处于流态化并做无规则运动,反应器中温度和污染物质的浓度在各处趋于同化. 与固定吸附床相比,流化床吸附反应器因吸附剂的流动而较好避免了死角或堵塞的现象[9, 10]. 研究者认为流态化吸附床具有一定的优势:当吸附剂处于流态化时,由固相吸附剂的无规则运动而引起水流在其周围发生微涡流动,强化了水中吸附质与吸附剂的接触面积和接触效率,使吸附剂的各位置均发挥着等同的吸附作用,各位置的污染物浓度均保持一致,对吸附反应的发生具有较强的促进作用[1]. 目前,关于流化床吸附反应器高效的吸附效率已得到广泛的证实[11]. 实际上,基于流态化作用的吸附剂与吸附质的吸附反应动力学模型能够描述并解释流化床吸附反应器对于水中污染物质的去除行为,且该吸附反应器的吸附穿透特性和吸附剂的饱和吸附量将对这一新型反应器在实际工程应用时的经济性具有重要影响. 然而,关于流化床吸附反应器上述特征的研究还鲜见报道.
在上述研究背景下,本研究以苯酚废水为处理对象、 活性炭为吸附剂,探讨了流化床吸附反应器在不同流态紊流强度时的吸附效率、 吸附动力学特性、 吸附反应穿透曲线和饱和吸附量. 研究结果与固定床吸附反应器的吸附行为进行了对比,以期为流态化作用下的吸附工艺的发展和应用奠定理论基础.
实验装置如图1所示,设置底部进水,通过改变进水流量调整流体作用于活性炭颗粒表面的曳力,引起床层膨胀高度的变化使得活性炭处于流态化状态[见图1(a)]. 设置顶部进水,使活性炭压实,处于固定态状态[见图1(b)]. 吸附装置由有机玻璃加工,柱总高840 mm,管内径30 mm. 吸附柱底部设有分布板和配水室,起混合和改善流体分布的作用. 分布板与床体之间设有细孔筛网,防止颗粒流失进入分布室. 吸附柱进水表观流速以恒流泵配备的数显转速调节设备和流量计调节控制.
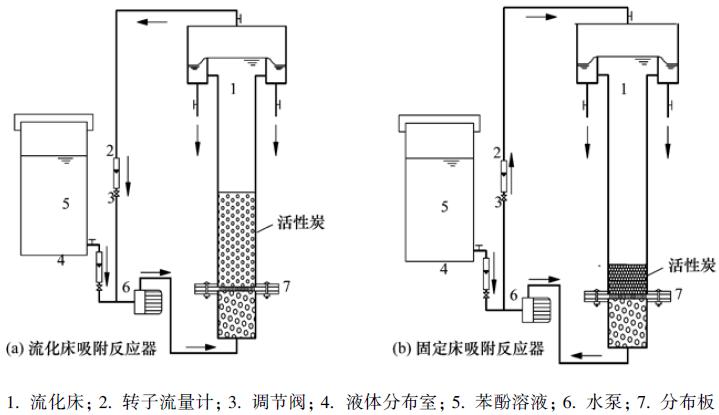 |
图 1吸附反应器Fig.1 Modelling of the adsorption reactor |
吸附剂采用日本Kurea活性炭,粒径分布区间为500~700 μm,其中粒径600 μm的活性炭占总活性炭质量的90%以上; 质量密度ρs为1317 kg ·m3; 孔隙度ε0为0.388; 形状为规则球形,球形度s=1; 易吸附挥发性有机物质:如对苯酚具有非常高的吸附性. 苯酚废水为人工配水,由一定质量的苯酚晶体与自来水混合配制成目标质量浓度的苯酚溶液.
苯酚的检测方法为紫外分光光度法.
当吸附反应充分后,取反应出水,利用分光光度法测其质量浓度,作为出水质量浓度. 计算苯酚在不同时间的吸附效率. 则苯酚的吸附效率为:
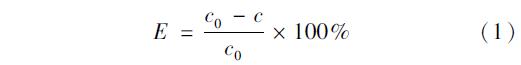
计算各时间的吸附量q:
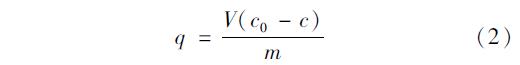
一级经典动力学方程认为吸附质吸附到吸附剂表面上的速率与其保留在溶液中的吸附质数量呈正比. 按Lagergren一级经典速率方程线性模式:
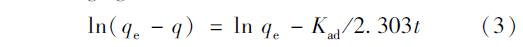
二级经典动力学方程是以吸附平衡能力为基础获得的,被认为吸附质吸附到吸附剂表面上的速率与其保留在溶液中的吸附质数量的二次方呈正比. 该方程常用来描述包括外部液膜扩散、 表面吸附和颗粒内部扩散等整个吸附过程. 按Lagergren二级经典动力学方程线性模式如下:
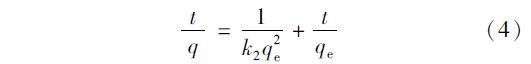
吸附剂饱和吸附量为单位质量的吸附剂在吸附器反应穿透时,对吸附质的吸附量. 首先,确定吸附反应过程中单位时间的吸附量qi,qi为吸附穿透过程中一段时间间隔的吸附量,时间间隔见图4,假设该时间段内吸附量为恒定值.
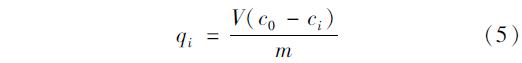
则饱和吸附量Q:
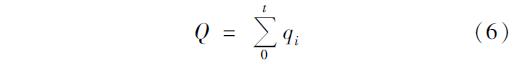
苯酚挥发量的测定是在与本研究中反应器的空气-溶液接触界面的面积相当的敞口容器中进行的. 经实验测得,当苯酚质量浓度为100 mg ·L-1时,敞口容器中苯酚溶液4 h挥发量仅为1.23%,故苯酚在吸附反应器的挥发可忽略不计.
在图 1所示的反应装置内,采用序批式循环进水,探讨了基于流态化作用下活性炭对苯酚吸附效率的影响. 反应器内填充高度为30 mm,质量为12.1 g活性炭. 当吸附剂为固定态(fixed bed reactor, FBR)时,床层膨胀高度不发生变化. 当吸附剂为流态化(fluidized bed reactor, FLBR)时,床层膨胀高度H较初始高度H0增加. 分别控制表观流速为8 mm ·s-1和13 mm ·s-1,H分别达到56 mm和87 mm,吸附剂流态对苯酚废水处理效率的影响如图2所示.
从图 2可以看出Kurea活性炭对苯酚的吸附效率非常高,各流态下不同紊流强度在5 min内基本完成吸附作用,吸附效率均达到93%以上. 吸附剂在不同流态、 紊流强度下,吸附效率曲线具有一定的相似性:初始反应阶段,吸附剂吸附量迅速增加,吸附量在短时间(5 min)内就基本到达到饱和吸附量. 在5 min以后,吸附剂吸附量增加量逐渐缓慢. 整个吸附反应可以分为两个阶段:前5 min吸附快反应阶段,5 min以后吸附慢反应阶段. 吸附快反应阶段的吸附量决定了吸附反应效率[14,15]. 其中,表观流速为8 mm ·s-1基于流态化吸附反应效率较基于固定态吸附效率几乎相等,而表观流速为13 mm ·s-1基于流态化吸附反应效率较基于固定态吸附效率低5%. 这可能与床体中流体流态的差异有关. 基于流态化作用下,颗粒处于无规则运动和边壁效应的影响,表观流速为13 mm ·s-1较8 mm ·s-1颗粒间水流紊流强度更为剧烈,导致苯酚废水在流化床中发生短流的可能性更高,表现为相同吸附时间时出水苯酚浓度略高.
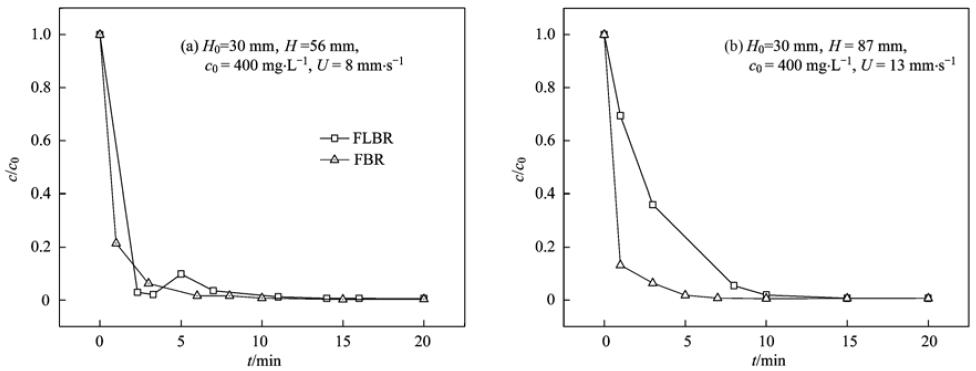 |
图 2序批式实验中流态对吸附效率的影响Fig.2Efficiency of adsorption based on the fluidization condition and fixed condition in batch mode |
当吸附剂处于流态化与固定态时,将吸附量与经典一级动力学方程和二级动力学方程拟合[公式(3)和(4)],得出经典动力学拟合图和拟合方程,如图 3、 表1所示.
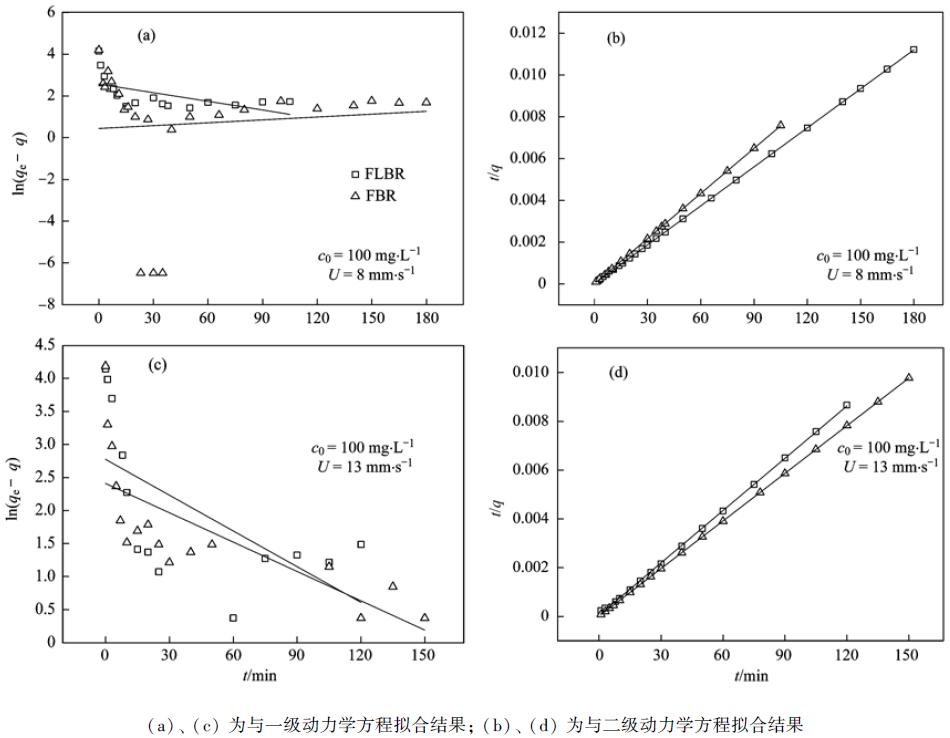 |
图 3基于流态化与固定态活性炭吸附苯酚与经典一、 二级动力学拟合图 Fig.3Plots of phenol adsorption reaction based on the fluidization condition and fixed condition fitted to Pseudo-first-order and Pseudo-second-order |
| 表1 经典二级动力学方程对不同颗粒流态、 紊流强度拟合结果Table 1 Pseudo-second-order parameters of phenol adsorption on activated carbon |
无论是基于流态化还是基于固定态的吸附反应,均与一级动力学方程拟合相关度不高,而与二级动力学方程拟合时的相关系数均大于0.999. 可见,吸附反应发生过程中,吸附剂的流态对反应的动力学行为影响较小. 当表观流速为8 mm ·s-1时,基于流态化吸附速率常数和平衡时吸附总量均大于基于固定态. 这是因为当颗粒处于流态化并做无规则运动时,显著增加了固液接触的几率,从而其吸附速率常数和吸附总量也随之增大. 而表观流速为13 mm ·s-1时基于流态化吸附速率与平衡吸附总量却低于基于固定态,这也进一步验证了基于流态化吸附行为与流态的紊流强度有关,表观流速为13 mm ·s-1流态化水流紊流程度较8 mm ·s-1时更剧烈,发生短流的概率增加,表现为相同时间吸附速率与饱和吸附量较低. 可见,基于流化态作用下水流的紊流强度不能过于剧烈,否则处理效果将会降低. 因此余下的研究内容中表观流速的选取为6 mm ·s-1和8 mm ·s-1.
在图 1反应装置内,采用连续进水,研究不同流态下的吸附穿透特性. 根据公式(5)和(6)计算得出总吸附量Q(每g活性炭吸附的苯酚的总量mg ·g-1),拟合基于流态化和基于固定态的吸附穿透曲线如图 4所示. 总体上,表观流速为6 mm ·s-1和8 mm ·s-1时,基于流态化和基于固定态的吸附反应穿透特性相似,其中,前50 min基于流态化的吸附反应出水苯酚浓度略高,其c/c0较基于固定态吸附反应高9.14%~5.67%. 在50 min后流态化出水苯酚浓度低. 其c/c0较基于固定态吸附反应低0.94%~2.16%. 值得注意的是,由表2可以看出,流化床总吸附量均高于固定床吸附总量,且随着紊流强度越大,流态化与固定态吸附量的差值也越大. 这是因为在流态化的固相颗粒作用下,其周围苯酚废水形成微涡,使颗粒周围的浓度相同,颗粒表面各位置发挥着同等的吸附效率,整个床层内的活性炭均发挥着吸附作用,各位置的污染物浓度均保持一致,对吸附作用的发生具有较强的促进作用. 而在固定态颗粒周围,最初的吸附发生在表层,表层的活性炭吸附了大量的苯酚,使得吸附孔隙率减小,实际流速逐渐降低,处理水量逐渐减小,失效的活性炭也随之增加,具体如图 5所示. 在上述作用下,吸附剂在基于流态化作用下的饱和吸附量较固定态显著增加,6 mm ·s-1和8 mm ·s-1增加的饱和吸附量为8.77 mg ·g-1和24.70 mg ·g-1. 这说明流化床吸附反应器中的吸附剂利用率较固定床吸附反应器高,再生周期长,在工程经济上更具有优势.
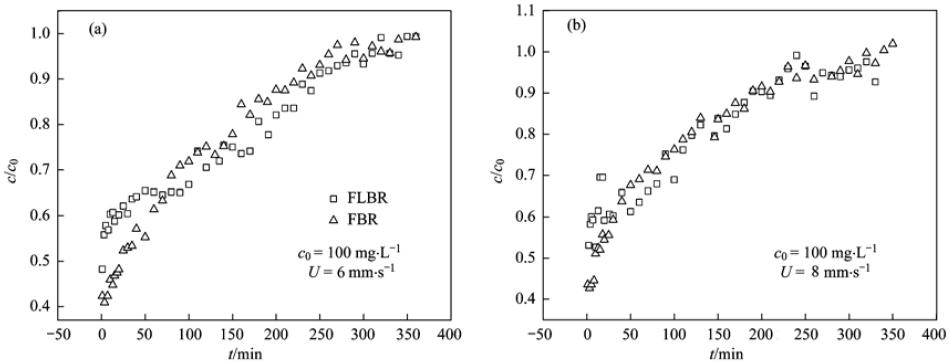 |
图 4基于流态化与固定态吸附剂吸附苯酚穿透反应拟合图Fig.4Adsorption capacity based on the fluidization condition and fixed condition |
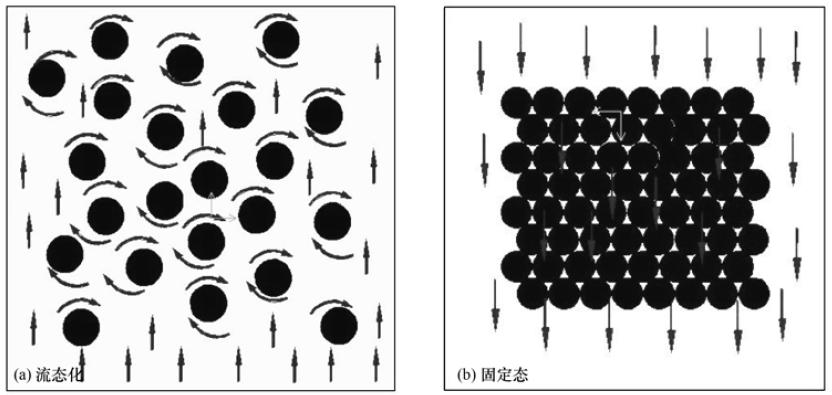 |
图 5吸附剂流化态与固定态示意Fig.5Adsorbent based on the fluidization condition and fixed condition |
| 表2 基于不同流态、 流速吸附剂的吸附总量Table 2 Adsorption capacity of a fluidized bed reactor and a fixed bed reactor |
在吸附效率上,基于流态化的活性炭对苯酚的吸附效率与固定态相比没有显著差异,5 min内均达到93%以上,且基于流态化和基于固定态的吸附反应均符合经典二级动力学方程. 在穿透特性上,基于流态化的活性炭对苯酚的吸附总量较固定态相比显著增大,且随着流态化的紊流程度的加剧而更为优化. 这表明流态化的吸附反应对吸附剂的利用更为充分. 总之,基于流态化作用吸附反应具有高效性、 吸附剂利用充分的特点,流化床吸附反应器是一种具有发展潜力的新型吸附反应器.
| [1] | Zhang X, Li A M, Jiang Z M, et al. Adsorption of dyes and phenol from water on resin adsorbents: Effect of adsorbate size and pore size distribution[J]. Journal of Hazardous Materials, 2006, 137 (2): 1115-1122. |
| [2] | Sabio E, Zamora F, Ganan J, et al. Adsorption of p-nitrophenol on activated carbon fixed-bed[J]. Water Research, 2006, 40 (16): 3053-3060. |
| [3] | Li P, Xiu G H, Jiang L. Competitive adsorption of phenolic compounds onto activated carbon fibers in fixed bed[J]. Journal of Environmental Engineering, 2001, 127 (8): 730-734. |
| [4] | Lua A C, Jia Q P. Adsorption of phenol by oil-palm-shell activated carbons in a fixed bed[J]. Chemical Engineering Journal, 2009, 150 (2): 455-461. |
| [5] | Wright P R, Liu X, Glasser B J. Laboratory-A fluidized bed adsorption laboratory experiment[J]. Chemical Engineering Education, 2004, 38 (1): 14-21. |
| [6] | Tsibranska I, Chemical H E. Modelling of heavy metal adsorption into activated carbon from apricot stones in fluidized bed[J]. Chemical Engineering and Processing, 2010, 49 (10): 1122-1127. |
| [7] | Ng Y L, Yan R, Tsen L T S, et al. Volatile organic compound adsorption in a gas-solid fluidized bed[J]. Water Science and Technology, 2004, 50 (4): 233-240. |
| [8] | Cui H P, Li L Y, Grace J R. Exploration of remediation of acid rock drainage with clinoptilolite as sorbent in a slurry bubble column for both heavy metal capture and regeneration[J]. Water Research, 2006, 40 (18): 3359-3366. |
| [9] | Yazbek W, Pre P, Delebarre A. Adsorption and desorption of volatile organic compounds in fluidized bed[J]. Journal of Environmental Engineering, 2006, 132 (5): 442-452. |
| [10] | Avarro A E, Cuizano N A, Lazo J C, et al. Comparative study of the removal of phenolic compounds by biological and non-biological adsorbents[J]. Journal of Hazardous Materials, 2009, 164 (2-3): 1439-1446. |
| [11] | Masao T, Noriaki S, Fumio Y. Application of radiation-graft material for metal adsorbent and crosslinked natural polymer for healthcare product[J]. Radiation Physics and Chemistry, 2004, 71 (1): 223-228. |
| [12] | Wang R C, Chang S C. Adsorption/desorption of phenols onto granular activated carbon in a liquid-solid fluidized bed[J]. Journal of Chemical Technology & Biotechnology, 1999, 74 (7): 647-657. |
| [13] | Rakhshaee R, Khosravi M, Ganji M T. Kinetic modeling and thermodynamic study to remove Pb(Ⅱ), Cd(Ⅱ), Ni (Ⅱ) and Zn(Ⅱ) from aqueous solution using dead and living Azolla filiculoides[J]. Journal of Hazardous Materials, 2006, 134 (1-3): 120-129. |
| [14] | 李朝丽, 周立祥. 黄棕壤不同粒级组分对镉的吸附动力学与热力学研究[J]. 环境科学, 2008, 29 (5): 1406-1411. |
| [15] | 李颖, 岳钦艳, 高宝玉, 等. 活性炭纤维对活性染料的吸附动力学研究[J]. 环境科学, 2007, 28 (17): 2637-261. |
| [16] | Li B Z, Sun K Q, Guo Y B, et al. Adsorption kinetics of phenol from water on Fe/AC[J]. Fuel, 2013, 110: 99-106. |
| [17] | Skodras G, Diamantopoulou I, Pantoleontos G, et al. Kinetic studies of elemental mercury adsorption in activated carbon fixed bed reactor[J]. Journal of Hazardous Materials, 2008, 158 (1): 1-13. |
| [18] | Zhu J, Huang Z, Kang F, et al. Adsorption kinetics of activated bamboo charcoal for phenol[J]. Carbon, 2009, 47 (6): 1614-1614. |
| [19] | Veeraraghavan S, Fan L T, Mathews A P. Modeling adsorption in liquid-solid fluidized beds[J]. Chemical Engineering Science, 1989, 44 (10): 2333-2344. |
| [20] | Sugimoto H, Miki T, Kanayama K, et al. Dielectric relaxation of water adsorbed on cellulose[J]. Journal of Non-Crystalline Solids, 2008, 354 (27): 3220-3224. |
| [21] | Al-Degs Y S, Khraisheh M A M, Allen S J, et al. Adsorption characteristics of reactive dyes in columns of activated carbon[J]. Journal of Hazardous Materials, 2009, 165 (1-3): 944-949. |
| [22] | Cheng T B, Jiang Y, Zhang Y P, et al. Prediction of breakthrough curves for adsorption on activated carbon fibers in a fixed bed[J]. Carbon, 2004, 42 (15): 3081-3085. |
| [23] | Chern J M, Chien Y W. Adsorption of nitrophenol onto activated carbon: isotherms and breakthrough curves[J]. Water Research, 2002, 36 (3): 647-655. |
| [24] | Murillo R, Garcia T, Aylon E, et al. Adsorption of phenanthrene on activated carbons: Breakthrough curve modeling[J]. Carbon, 2004, 42 (10): 2009-2017. |
| [25] | Namane A, Hellal A. The dynamic adsorption characteristics of phenol by granular activated carbon[J]. Journal of Hazardous Materials, 2006, 137 (1): 618-625." |
 2014, Vol.35
2014, Vol.35 


