2. 哈尔滨工业大学市政环境工程学院, 哈尔滨 150090
2. School of Municipal and Environmental Engineering, Harbin Institute of Technology, Harbin 150090, China
随着我国工业化进程的加快,采矿、 冶炼、 金属加工、 电镀、 电子等工业废水大量产生,影响生态环境危害人体健康. 铜离子是工业废水中普遍存在的重金属污染源,以单质或各种矿物形式存在. 除了采矿,热交换以及其他工业用途都可以把铜排入水体中. 铜是人体必需微量元素之一,对于造血、 细胞生长、 某些酶的活性及内分泌腺功能均有重要作用. 但体内过多的铜会引起贫血、 肝脏病理性改变及神经系统损伤,导致肾衰、 肝硬化、 老年痴呆和帕金森病等[1,2]. 在我国,含铜废水必需经过处理至少达到污水排放三级标准[3]时才能排放. 目前,处理含Cu2+废水的传统方法主要有化学沉淀、 离子交换、 反渗透、 氧化还原、 活性炭吸附等,这些方法在处理低浓度重金属废水时具有费用高、 能耗大、 操作繁琐、 易造成二次污染,不适于低浓度含铜废水的处理[4,5].
生物吸附法就是利用某些生物体本身的化学结构及成分特性来吸附溶于水中的金属离子,再通过固液两相分离来去除水溶液中金属离子的方法[6]. 生物吸附法具有低成本、 高效率、 无污染、 可回收再利用等优势,尤其适用于1~100 mg ·L-1重金属废水的处理[7]. 近年来,利用农业和食品工业废弃物,如橘皮、 木屑、 稻壳、 废弃菌体等作为生物吸附剂,去除废水重金属的研究备受关注[8, 9, 10].
中国是食用菌生产大国,2012年全国食用菌生产总量约为3100万t,菌糠总量约为800万t,其中黑龙江省在2010年就已成为国内食用菌产量最高的地区,每年会产生大量的菌糠废弃物. 菌糠除少数用于还田和栽培基质外,绝大多数被废弃或就地燃烧,既浪费了资源又污染了环境[11]. 食用菌菌糠主要成分为纤维素、 半纤维素、 木质素、 菌丝体及经菌丝体生物转化过程中产生的糖类、 有机酸和生物活性物质,其表面丰富的羟基、 羰基、 羧基、 酰胺基、 磷酸基等可以螯合废水中的金属阳离子. 国内外已有大量关于农业废弃物或菌丝体吸附重金属离子的报道,且吸附效果明显[12, 13, 14]. 但大多数报道中的铜离子浓度在每升几十毫克到几百毫克之间,10 mg ·L-1以下的情况鲜有报道. 本研究以平菇菌糠废料制成吸附剂,探讨菌糠对低浓度废水中铜离子的吸附特性,利用扫描电镜-能谱、 傅里叶红外光谱和X射线衍射对其吸附机制进行初步分析.
平菇菌糠废料来自哈尔滨香坊木材食用菌厂,将平菇菌糠在80℃烘干至恒重,粉碎,过40目筛,经高压蒸汽灭菌,置于干燥环境下备用.
铜标准曲线的配制: 将铜标准溶液分别配制成浓度为1、 2、 3、 4和5 mg ·L-1的铜溶液,用原子吸收分光光度计(日本岛津)测定后绘制标准曲线,利用该标准曲线校正仪器误差(其中该仪器的检测线为≤0.005 μg ·mL-1,精密度为≤1%).
铜离子储备液:准确称取0.3775 g Cu(NO3)2 ·3H2O,用去离子水定容于100 mL容量瓶中,配制成1 g ·L-1铜溶液母液,使用时用去离子水稀释到所需浓度.
取一定量菌糠吸附剂,加入装有稀释到一定浓度、 体积为100 mL铜溶液的锥形瓶中,于150 r ·min-1、 30℃恒温摇床中振荡吸附. 吸附完成后过滤取滤液,用原子吸收分光光度计测定滤液中剩余铜离子浓度(铜离子平衡浓度),每组实验重复3次,数据取3次结果的平均值,另设对照.
吸附率(R)和吸附容量(Q)的计算公式:
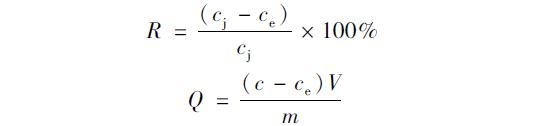
在菌糠投加量为10 g ·L-1,溶液pH为6,吸附时间为120 min,温度为30℃,摇床转速为 150 r ·min-1条件下,调节铜离子初始浓度分别为2、 4、 6、 8、 10、 12 mg ·L-1,测定吸附平衡时滤液中的Cu2+浓度ce.
SEM-EDX:取适量吸附前后的平菇菌糠60℃下烘干,粘到碳导电介质板上镀金,置于扫描电镜(美国FEI,QUANTA200型)下室温扫描,观察样品形貌、 照相,并用能谱仪观察分析样品表面元素.
FTIR:取吸附前后的菌糠在60℃下烘干并研磨成粉末状,分别与KBr混匀(比例约为1 ∶100),在玛瑙研钵中仔细研磨,放入压片机内压片,采用傅里叶变换红外光谱仪(德国Bruker,ALPHA-T)分析.
XRD:取吸附Cu2+前后的菌糠在60℃下烘干,采用XRD仪(日本理学,D/max2200型)分析. 操作条件为:Cu Kα辐射源,2θ扫描区间5°~80°,扫描速率4° ·min-1,步距0.02°,波长0.154 nm,电压40 kV,电流30 mA.
铜离子属于硬金属离子,其特征是离子半径小、 极化性低且所带正电荷量高,易与硬配体(如H2O、 OH-、 Cl-、 PO3-4、 NH3和ROH)配位优先形成离子键. 由图1(a)可知,在溶液初始pH为2时,菌糠吸附率很低,只有50.53%,可能由于低pH时,溶液中大量H+与Cu2+竞争吸附剂表面的吸附位点,降低了吸附率. 在初始pH 3~6之间,吸附率逐渐缓慢上升,初始pH为6时,吸附率达到最大,为74.42%,而10 mg ·L-1铜溶液的原始pH值为6,故实验中无需再进行pH值的调节. 但当初始pH值过大时,部分Cu2+会以Cu(OH)+、 Cu(OH)2的沉淀形式存在,从而影响了菌糠对Cu2+的吸附效果. 张芝利等[15]以菌糠为吸附剂对铜离子进行吸附,在初始pH为5时吸附率可达75%左右,但其对pH要求较严格,pH 3~7间吸附率波动较大,而本实验中pH为3时的吸附率就已达到最大吸附率的93.3%,说明平菇菌糠对铜离子的吸附pH值的适合范围较广.
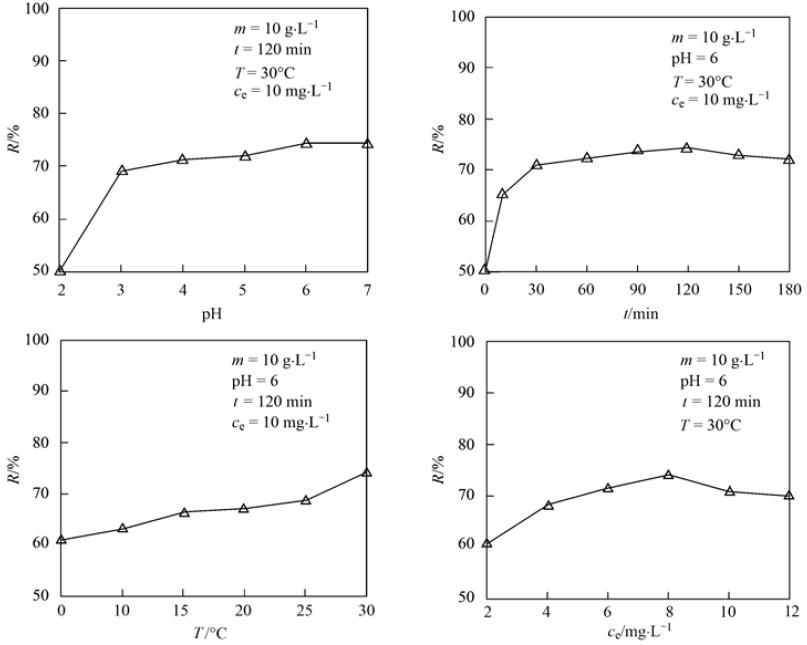 |
图 1单因素对Cu2+吸附效果的影响Fig.1Single factor experiment of Cu2+ biosorption |
由图1(b)可见,菌糠对Cu2+的吸附率随着吸附时间的增加而增大,0~30 min内吸附率增加较快,30~120 min内吸附率缓慢增加,120 min后吸附率略有下降. 可能是由于开始时溶液中Cu2+浓度高于菌糠表面铜离子的浓度,菌糠表面空白吸附位点较多,故铜离子可与其表面的吸附位点快速结合; 随着吸附的进行,Cu2+逐渐进入菌糠孔隙中,Cu2+在孔隙中的传质速度逐渐减慢,固液两相中铜离子浓度梯度也逐渐减小,故吸附率随时间缓慢增加直至平衡; 随着吸附时间的增加和持续的振荡,可能会出现轻微的解吸现象,但吸附率基本不变. 如图1(b)在120 min时吸附率达到最大为74.46%,故120 min为吸附平衡时间.
温度是影响吸附反应过程的重要环境因素之一. 如图1(c),菌糠对Cu2+的吸附率随温度的升高而增大,在温度30℃达到最大为74.22%. 这是因为在较高的温度下,菌糠上一些吸附位点被活化,且温度的提高有利于粒内传质或化学吸附的发生[16]. 温度的升高有利于吸附表明该生物吸附是一个吸热反应过程[17],温度升高平衡向吸热的方向移动. 但是在实际生产中,温度越高,能耗越大,且就黑龙江地区温度情况,选30℃为最佳吸附温度.
在溶液体积和投加量不变的情况下,溶液初始浓度也是影响吸附率的重要因素之一. 如图1(d)所示,随着Cu2+浓度的增加,菌糠吸附率逐渐增大,当浓度为8 mg ·L-1时达到最大值为74.16%,之后吸附率开始下降. 一般认为,重金属离子的吸附过程与重金属离子浓度和吸附剂投加量的比值有关. 在一定范围内,重金属离子浓度与吸附剂投加量的比值越大,吸附率就越大,直到达到饱和,如继续增加重金属离子浓度,表面位点被充分占满的吸附剂已不能再吸附过多重金属离子,故吸附率逐渐下降[18]. 因此,根据实验结果选择Cu2+的浓度为8 mg ·L-1. 郭学益等[19]报道利用改性柿子为吸附剂吸附铜离子,当铜离子初始浓度为50 mg ·L-1时,吸附率可达90%,而本实验中铜离子初始浓度仅为8 mg ·L-1,且未经改性,故吸附容量也相应降低,但已基本达到国家污水排放三级标准的要求.
将吸附平衡所得数据分别用Langmuir方程和Freundlich进行拟合,吸附模型线性表达式如下.
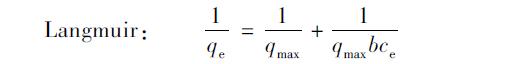
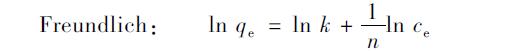
由图 2和图 3的吸附等温线可见,平菇菌糠对铜离子吸附容量qe与平衡浓度ce的双倒数和平菇菌糠对铜离子吸附容量qe与平衡浓度ce的双对数均具有线性关系,且拟合结果都很好. Langmuir方程是假设吸附剂表面均匀,各处的吸附能相同; 吸附是单分子层的,当吸附剂表面的吸附质饱和时,其吸附量达到最大值; 在吸附剂表面上吸附的吸附质之间没有相互作用; 达到动态平衡时,吸附和脱附的速度一样. 而 Freundlich吸附模型适用于对中等浓度范围内的吸附现象的描述,对于过低或过高浓度吸附质则不符合实际吸附现象[20]. Chia等[21]也报道,血红栓菌、 鲁氏毛霉等吸附水溶液中镉离子的吸附等温线更符合 Langmuir方程,其吸附过程主要为吸附剂表面单层的化学吸附. 从图 2和图 3中也可以看出用 Langmuir方程拟合的效果更好,其线性相关系数R2为0.9949. 根据图 2可以算出 Langmuir方程的参数值: qmax=0.8114 mg ·g-1,b=3.953 L ·mg-1.
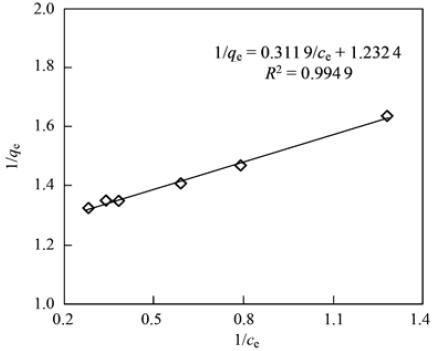 |
图 2Langmuir吸附等温模型Fig.2Langmuir adsorption isotherm |
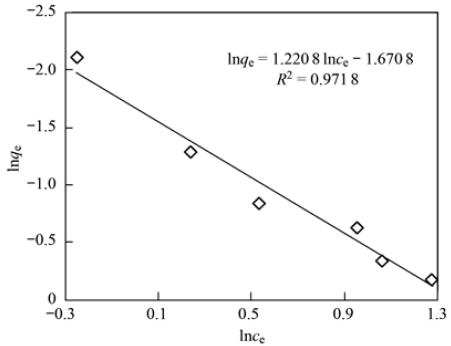 |
图 3Freundlich吸附等温模型Fig.3Freundlich adsorption isotherm |
由Langmuir吸附等温方程还可以定义一个无量纲的分离因子RL,其表达式为:
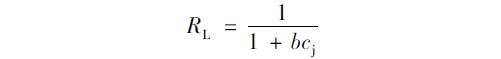
分离因子RL可用于表示吸附过程的性质,当 0<RL<1,表示优惠吸附; 当RL>1,为非优惠吸附; 当RL=1,为可逆吸附; 当RL=0,为非可逆吸附[22].
而本研究中 b和cj均大于零,可以得到该吸附过程的特征分离因子一定在 0<RL<1之内,这表明平菇菌糠对水体铜离子的吸附是优惠吸附. 这表示在溶质浓度较低时,菌糠仍能对铜离子进行有效地吸附(吸附率达70%以上); 而非优惠吸附表示吸附较难进行,不利于有效成分的吸附. 以上可表明:铜离子浓度较低时,平菇菌糠对铜离子的吸附是发生在吸附剂表面的单层吸附,铜离子之间的相互干扰可忽略不计.
对吸附前后菌糠进行SEM扫描观察发现,菌糠主要由木屑和菌丝体构成,而木屑主要由纤维素、 半纤维素和木质素交联聚合而成,此外还含有少量灰分和木材抽提物[23],其中纤维素和半纤维素是由大量长短不一的纤维微纤丝连接而成,而微纤丝又是由许多毫微纤丝组成,这些纤维丝之间存在诸多微小空隙,通过水溶液中的振荡,更多的木质片层碎片、 内部填充物溶出,这些都进一步增加了菌糠的吸附表面积. 从图4(a)可以看出吸附前,菌糠表面比较粗糙、 质地相对紧密,且具有许多微观孔洞、 沟壑和褶皱,表面还附着一定量的菌丝,这些都表明菌糠具有很大的吸附表面积. 图4(b)为菌糠吸附铜离子后的微观表面结构,吸附作用的发生及外部环境的突然改变大大地影响了吸附剂的外观形态,经水浸泡、 摇床振动后的菌糠内部层次更加鲜明,结构更加松散,暴露出更多吸附位点[24],且0.072 nm的铜离子半径使得它们更易于进入吸附剂微孔内[25],更加有利于菌糠表面活性基团与溶液中金属离子接触.
 |
图 4平菇菌糠吸附前后的扫描电镜图Fig.4SEM of native and adsorbed spent substrate of pleurotus oyster |
一般来说,吸附剂对金属离子的吸附应同时存在物理吸附和化学吸附,物理吸附包括范德华力和静电作用等,化学吸附包括离子交换、 表面络合等[5]. 比较图5可以看出,在菌糠吸附铜离子后,多种元素质量比都发生一定的改变,图5(b)中出现了微小的铜峰. 由单因素也可知,在吸附开始时,吸附率上升很快,这可能主要发生物理吸附; 而后吸附率上升缓慢趋于平衡,这可能是铜离子与木屑及菌丝体表面基团通过化学键结合,发生化学吸附.
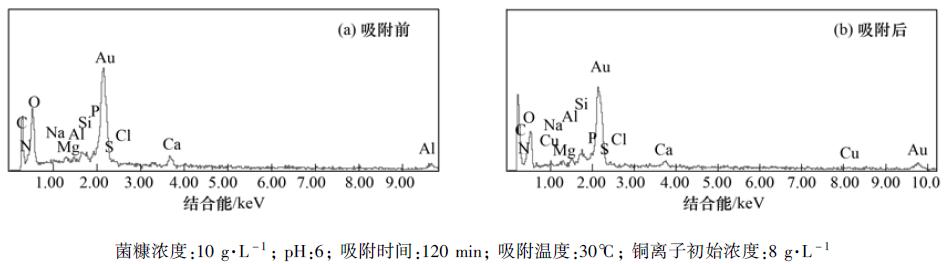 |
图 5平菇菌糠吸附前后的X射线能谱图Fig.5EDX of native and adsorbed spent substrate of pleurotus oyster |
由表1可以看出,菌糠吸附剂主要由 C、 O、 N和少量的Ca、 P以及微量的Na、 Mg、 Al、 Si组成. 其中 C、 O、 N为生物生长的大量元素,故比重较大; 平菇在栽培过程中加入过磷酸钙既可以消毒杀菌还可促进生长,所以菌糠成分中含有一定量的 Ca、 P; Cu和 Cl为食用菌生长所需微量元素,比重极小,故未检出; Na、 Mg、 Al、 Si也属于食用菌菌生长必要的矿质元素(EDX检测前吸附剂表面喷金,检测时没有计算金含量).
| 表1 菌糠吸附前和吸附后的X射线能谱分析 1)/% Table 1 EDX analysis of native and adsorbed spent substrate of pleurotus oyster/% |
菌糠吸附铜离子之后,菌糠元素成分中出现了少量的铜,初步说明有铜元素附着在吸附剂上. Na、 Mg、 Ca元素都有不同程度的减少,可能在吸附过程中发生离子交换反应,Ngah等[26]也报道过,离子交换是铜离子吸附的机制之一,且 Ca元素减少比例较大,而铜离子又是二价金属阳离子,故更易与钙离子发生离子交换[21]; 其中 N、 P也有不同程度减少,初步认为菌糠中的酰胺基、 氨基等基团可能与 铜离子发生了表面络合配位反应.
对吸附Cu2+前后平菇菌糠进行FTIR测定,利用OMNIC 8.0红外光谱处理软件进行分析,结果如图6.
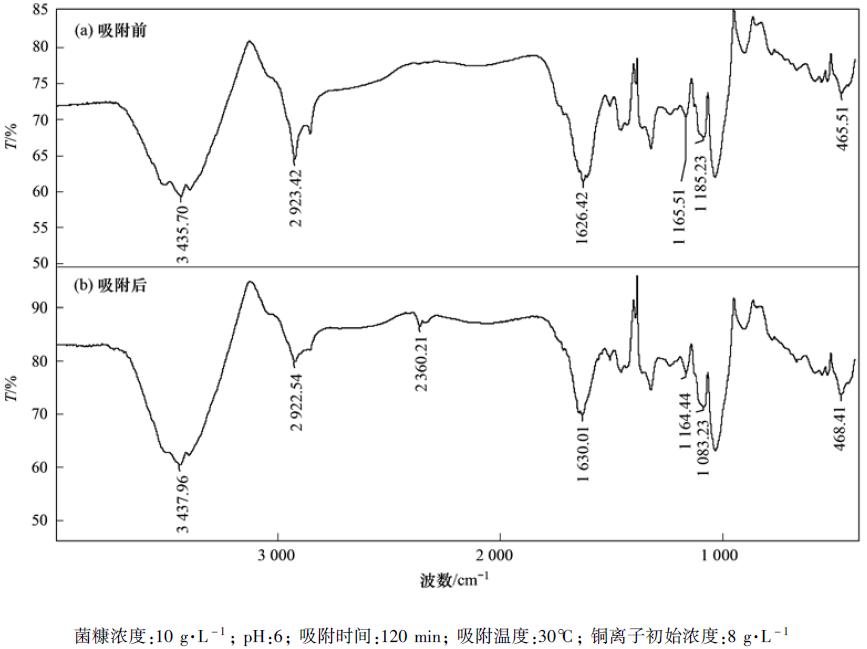 |
图 6平菇菌糠吸附前后的红外光谱图Fig.6FTIR Spectra of native and adsorbed spent substrate of pleurotus oyste |
图6分别为吸附Cu2+前后的平菇菌糠的红外光谱图. 由于每一个官能团都有其特有的吸收峰[30],由该红外光谱图中含有较多吸收峰可知,菌糠吸附剂表面有大量且复杂的官能团. 通过吸附前后平菇菌糠红外光谱图的比较,可以判断其表面官能团的变化.
红外吸收峰所对应官能团的一般波数范围已列于表2中,其中3200~3750 cm-1范围内为—OH和—NH键的交叉伸缩振动峰[30,31]. 本实验中吸附后平菇菌糠红外吸收峰由3435.70 cm-1移动到3437.96 cm-1,可能是基于—NH或者—OH键的伸缩振动作用,由于平菇菌糠主要由平菇菌丝体和木屑组成,故其中含有多种不同的生物聚合物,如真菌细胞壁中的壳聚糖、 多磷酸盐、 脂质和蛋白质等[32],以及木屑中的纤维素、 半纤维素和木质素等[33],Alka等[34]报道过木屑中的这些物质都是易于发生离子交换反应的复合物. 由于该吸附剂成分的复杂性,不能够准确判断该处起作用的官能团,Chen等[35]也报道过,吸附剂表面络合物的形成可能对—OH的吸收峰产生影响; 吸附后2923.42 cm-1处的吸收峰移动到2922.54 cm-1,Zhang等[36]曾报道,随着吸附剂制备时温度的提高,此处—CH2基团中C—H键的吸收峰会发生一定位移,但本研究中菌糠吸附剂制备时温度仅为60℃,故该位移很小,可忽略不计; 在2360.21 cm-1处出现了新的吸收峰,可能为多酚上的氨基或有机直链的累积[37],表明在吸附铜离子后的吸附剂表面新增加的这个基团极有可能参与了铜离子的成键; 1626.42 cm-1和1165.51 cm-1处吸收峰经吸附后分别移动到1630.01 cm-1和1164.44 cm cm-1,表明铜离子可能与酰胺中氨基、 羧基以及木质素上的酚羟基发生了化学反应,它们参与了铜离子的成键过程[33,38]; 而吸附后的平菇菌糠吸收峰由1085.23 cm-1移动到1083.23 cm-1处的强吸收峰,可能是木质素上或纤维素中β(1~4)糖苷键上C—O的伸缩振动,也可能是酰胺基团中—CN的伸缩振动[18,39]; 此外,吸附后465.51 cm-1处吸收峰移动到了468.41 cm-1处,范春辉等[40]推测该处为O—Si—O键的弯曲振动,可能存在SiO2,Zhang等[36]也得出了类似结论.
| 表2 平菇菌糠红外吸收带的一般官能团 [27, 28, 29] Table 2 General peak assignments of FTIR spectra adsorption bands of pleurotus oyste |
以上分析可得,吸附剂表面含有大量的羧基和羟基,它们都可以作为质子供体,因此去质子化的羧基和羟基可能与铜离子发生了配位反应[41]. 此外,Ma等[42]报道过水溶液中的Cu2+非常易于与有机质上的多种官能团形成络合物,上述红外光谱的分析中指出,平菇菌糠上的氨基和硅酸盐的吸收峰也发生一定变化,可能是与铜离子反应形成了复杂的表面络合物. 以上这些反应改变了菌糠表面官能团的化学环境,使得菌糠的红外吸收峰发生位移. 由此可知,羧基、 羟基、 氨基以及二氧化硅在铜离子吸附的过程中起着关键作用[43].
图 7为吸附Cu2+前后的平菇菌糠的XRD图谱,从中可以看出,在2θ约15.9°和21.96°处分别有一个次峰和主峰,是典型的纤维素衍射图谱,其中次峰表示具有较低有序度的多糖结构,而主峰表示有序度高的纤维素晶体结构. 平菇菌糠吸附铜离子后的XRD峰形整体变化不大,分别又在26°、 32°、 43° 等多处出现衍射峰,其中2θ在26°左右是SiO2的主要衍射峰,暴露明显的SiO2活性位点和骨架使得菌糠成为一种理想的吸附剂,吸附后菌糠的EDX也可以看到Si较吸附前有所增加. 吸附后,不仅主峰和次峰高度都明显增加,而且30°~50°较大的衍射峰范围说明有玻璃体存在,菌糠与铜离子形成了具有晶体结构的金属化合物. 吸附前的能谱图7(a)上没有出现含铜离子化合物的吸收峰,对照JCPDS PDF卡片上也没有铜元素; 而吸附后能谱图7(b)中2θ在25°~70°测试范围内有许多尖锐的衍射峰,由MDI Jade5.0软件检索分析,对照JCPDS PDF Card No.420663,也发现吸附前后均出现了SiO2. 在较大量物质区间中查到,吸附后的菌糠上主要在2θ为14°左右增加了Cu(NH3)2(N3)2、 2θ在23°左右增加了Cu(NH3)3NO3; 在较小量物质区间中查到,2θ在43°左右增加了CuO,由于其衍射峰相对较少,可忽略不计. 说明Cu2+主要与平菇菌糠中氨基发生了络合反应.
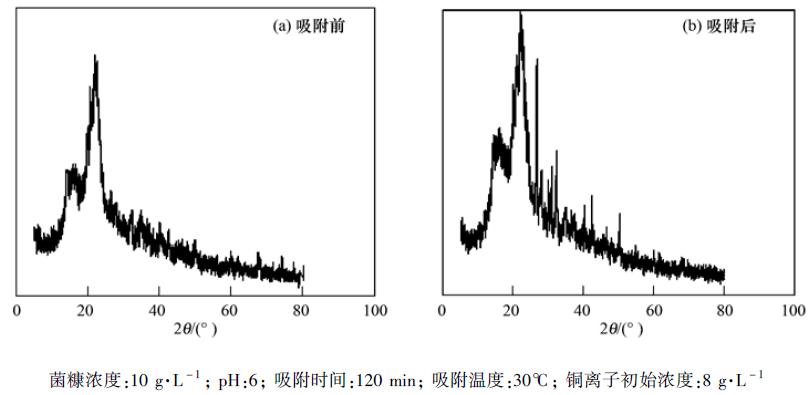 |
图 7菌糠吸附Cu2+前后的X射线衍射图Fig.7X-ray spectra of spent mushroom substrate before and after Cu2+ biosorption |
(1)平菇菌糠吸附Cu2+的单因素最佳吸附条件为:菌糠浓度10 g ·L-1,溶液 pH 6,吸附时间 120 min,吸附温度30℃,溶液初始浓度 8 mg ·L-1,吸附率 74.46%,吸附后水中 Cu2+基本达到国家污水排放三级标准.
(2)Langmuir等温线很好地描述了平菇菌糠吸附Cu2+的过程. 通过SEM观察到菌糠表面有许多不规则突起、 空隙,具有较大的吸附表面积,木屑中的纤维素、 半纤维素和木质素以及菌丝体同时对Cu2+有吸附作用; 由EDX中各元素含量的改变可推测,菌糠吸附铜离子的过程中可能发生了离子交换等化学反应; 由FTIR可知羟基、 羧基和氨基在吸附过程中起主要作用,且吸附过程主要发生了配位和络合反应; 通过XRD可知铜离子主要以Cu(NH3)2(N3)2、 Cu(NH3)3NO3等形式结合到菌糠上.
(3)平菇菌糠不需要经过任何化学处理,对Cu2+即有较强吸附性. 该农业废弃物,可以作为一种去除水体重金属的新型生物吸附剂,从而达到“以废治废”的目的,具有较大的开发潜力和较高的应用价值.
| [1] | Wu W Q, Yang Y, Zhou H, et al. Highly efficient removal of Cu(Ⅱ) from aqueous solution by using Graphene Oxide[J]. Water, Air, & Soil Pollution, 2013, 224 (1): 1372-1379. |
| [2] | Harvey A. The composition and environmental hazard of copper slags in the context of the Basel Convention[J]. Resource, Conservation and Recycling, 2005, 43 (4): 353-360. |
| [3] | GB 8978-1996, 污水综合排放标准[S]. |
| [4] | Nadeem F, Mohsin K, Naveed R. Dead immobilized Rhizopus arrhizus as a potential biosorbent for copper removal[J]. Korean Journal of Chemical Engineering, 2013, 30 (1): 95-100. |
| [5] | Asha A J, Sanjeev K S, Ackmez M. A comprehensive overview of elements in bioremediation[J]. Reviews in Environmental Science and Bio/Technology, 2010, 9 (3): 215-288. |
| [6] | 王建龙, 陈灿. 生物吸附法去除重金属离子的研究进展[J]. 环境科学学报, 2010, 30 (4): 673-701. |
| [7] | Wang J L, Chen C. Biosorbents for heavy metals removal and their future[J]. Biotechnology Advances, 2009, 27 (2): 195-226. |
| [8] | Khani M H, Pahlavanzadeh H, Alizadeh K. Biosorption of strontium from aqueous solution by fungus Aspergillus terreus[J]. Environmental Science and Pollution Research, 2012, 19 (6): 2408-2418. |
| [9] | Hossain M A, Ngo H H, Guo W S, et al. Adsorption and desorption of copper(Ⅱ) ions onto garden grass[J]. Bioresource Technology, 2012, 121: 386-395. |
| [10] | Lim L B L, Priyantha N, Tennakoon D T B, et al. Biosorption of cadmium (Ⅱ) and copper (Ⅱ) ions from aqueous solution by core of Artocarpus odoratissimus[J]. Environmental Science and Pollution Research, 2012, 19 (8): 3250-3256. |
| [11] | Phan C W, Sabaratham V. Potential uses of spent mushroom substrate and its associated lignocellulosic enzymes[J]. Applied Microbiology and Biotechnology, 2012, 96 (4): 863-873. |
| [12] | Meriem M, Kamel N, Hakim L, et al. Characterization and properties of Pleurotus mutilus fungal biomass as adsorbent of the removal of uranium (Ⅵ) from uranium leachate[J]. Journal of Radioanalytical and Nuclear Chemistry, 2013, 295 (1): 393-403. |
| [13] | Marina S, Mile K, Biljana S. Modified hardwood sawdust as adsorbent of heavy metal ions from water[J]. Wood Science and Technology, 2006, 40 (3): 217-227. |
| [14] | Altun T, Pehlivan E. Removal of Cr(Ⅵ) from aqueous solutions by modified walnut shells[J]. Food Chemistry, 2012, 132 (2): 697-700. |
| [15] | 张芝利, 周飞. 改性菌糠对水中铜离子的吸附能力[J]. 西安工程大学学报, 2012, 26 (1): 62-66. |
| [16] | Tokuyama H, Yanagawa K, Sakohara S. Temperature swing adsorption of heavy metals on novel phosphate-type adsorbents using thermosensitive gels and/or polymers[J]. Separation and Purification Technology, 2006, 50 (1): 8-14. |
| [17] | Vimal C S, Indra D M, Indra M M. Adsorption thermodynamics and isosteric heat of adsorption of toxic metal ions onto bagasse fly ash(BFA) and rice husk ash(RHA)[J]. Chemical Engineering Journal, 2007, 132 (1-3): 267-278. |
| [18] | 曹玉娟, 张扬, 夏军, 等. ε-聚赖氨酸生产菌体对六价铬吸附影响的研究[J]. 环境科学, 2012, 33 (2): 499-504. |
| [19] | 郭学益, 公琪琪, 梁莎, 等. 改性柿子生物吸附剂对铜和铅的吸附性能[J]. 中国有色金属学报, 2012, 22 (2): 599-603. |
| [20] | 李国新, 张丹丹, 颜昌宙, 等. 轮叶黑藻对铅的吸附特征及生物吸附机理研究[J]. 中国环境科学, 2011, 31 (8): 1327-1333. |
| [21] | Chia C T, Hong H L, Chun Y Y, et al. Biosorption of cadmium ions using Pleurotus ostreatus: Growth kinetics, isotherm study and biosorption mechanism[J]. Korean Journal of Chemical Engineering, 2011, 28 (3): 825-830. |
| [22] | 王毅, 张婷, 冯辉霞, 等. 阴离子改性膨润土对水中亚甲基蓝吸附性能研究[J]. 非金属矿, 2008, 31 (2): 57-61. |
| [23] | Kwon T N, Jeon C. Selective adsorption for indium(Ⅲ) from industrial wastewater using chemically modified sawdust[J]. Korean Journal of Chemical Engineering, 2012, 29 (12): 1730-1734. |
| [24] | 袁红江, 全学军, 冉秀芝, 等. 油茶饼粕生物吸附剂对Ni2+的吸附性能[J]. 化工学报, 2011, 62 (4): 986-993. |
| [25] | Febriana N, Lesmana S O, Soetaredjo F E, et al. Neem leaf utilization for copper ions removal from aqueous solution[J]. Journal of the Taiwan Institute of Chemical Engineers, 2010, 41 (1): 111-114. |
| [26] | Ngah W S W, Hanafiah M A K M. Biosorption of copper ions from dilute aqueous solutions on base treatedrubber (Hevea brasiliensis) leaves powder: kinetics, isotherm, and biosorption mechanisms[J]. Journal of Environmental Sciences, 2008, 20 (10): 1168-1186. |
| [27] | Majumdar S S, Das S K, Saha T, et al. Adsorption behavior of copper ions on Mucor rouxii biomass through microscopic and FTIR analysis[J]. Colloids and Surfaces B: Biointerfaces, 2008, 63 (1): 138-145. |
| [28] | Arief V O, Trilestar K, Sunarso J, et al. Recent progress on biosorption of heavy metals from liquids using low cost biosorbents: characterization, biosorption parameters and mechanism Studies[J]. CLEAN-Soil, Air, Water, 2008, 36 (12): 937-962. |
| [29] | 卢涌泉, 邓振华. 实用红外光谱解析[M]. 北京: 电子工业出版社, 1989. 21-150. |
| [30] | Panda G C, Das S K, Guha A K. Biosorption of cadmium and nickel by functionalized husk of Lathyrus sativus[J]. Colloid and Surfaces B: Biointerfaces, 2008, 62 (2): 173-179. |
| [31] | Ngah W S W, Hanafiah M A K M. Adsorption of copper on rubber(Hevea brasiliensis) leaf powder: Kinetic, equilibrium and thermodynamic studies[J]. Biochemical Engineering Journal, 2008, 39 (3): 521-530. |
| [32] | Javaid A, Bajwa R, Shafique U, et al. Removal of heavy metals by adsorption on Pleurotus ostreatus[J]. Biomass and Bioenergy, 2011, 35 (5): 1675-1682. |
| [33] | Rahman M S, Islam M R. Effects of pH on isotherms modeling for Cu(Ⅱ) ions adsorption using maple wood sawdust[J]. Chemical Engineering Journal, 2009, 149 (1-3): 273-280. |
| [34] | Alka S, Zang Y H, Dubey P, et al. The role of sawdust in the removal of unwanted materials from water[J]. Journal of Hazardous Materials, 2002, 95(1-2): 137-152. |
| [35] | Chen H, Dai G L, Zhao J, et al. Removal of copper(Ⅱ) ions by a biosorbent-Cinnamomum camphora leaves powder[J]. Journal of Hazardous Materials, 2010, 177 (1-3): 228-236. |
| [36] | Zhang J H, Fu H, Lv X S, et al. Removal of Cu(Ⅱ) from aqueous solution using the rice husk carbons prepared by the physical activation precess[J]. Biomass and Bioenergy, 2011, 35 (1): 464-472. |
| [37] | Sarin V, Singh T S, Pant K K. Thermodynamic and breakthrough column studies for the selective sorption of chromium from industrial effluent on activated eucalyptus bark[J]. Bioresource Technology, 2006, 97 (16): 1986-1993. |
| [38] | 李克斌, 王勤勤, 党艳, 等. 荞麦皮生物吸附去除水中Cr(Ⅵ)的吸附特性和机理[J]. 化学学报, 2012, 70 (7): 929-937. |
| [39] | Pitsari S, Tsoufakis E, Loizidou M. Enhanced lead adsorption by unbleached newspaper pulp modified with citric acid[J]. Chemical Engineering Journal, 2013, 233 (1): 18-30. |
| [40] | 范春辉, 张颖, 张颖超等. 红外光谱法研究低温焚烧稻壳灰对Cr(Ⅴ)的吸附机理[J]. 光谱学与光谱分析, 2010, 30 (9): 2345-2349. |
| [41] | Han R P, Zhang L J, Song C, et al. Characterization of modified wheat straw, kinetic and equilibrium study about copper ion and methylene blue adsorption in batch mode[J]. Carbohydrate Ploymers, 2010, 79 (4): 1140-1149. |
| [42] | Ma L, Xu R K, Jiang J. Adsorption and desorption of Cu(Ⅱ) and Pb(Ⅱ) in paddy soils cultivated for different years in subtropical China[J]. Journal of Environmental Sciences, 2010, 22 (5): 689-695. |
| [43] | Veneu D M, Pino G A H, Torem M L. Fundamental aspects of copper and zinc removal from aqueous solutions using a Streptomyces lunalinharesii strain[J]. Minerals Engineering, 2012, 29: 112-120." |
 2014, Vol.35
2014, Vol.35 


