2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environment and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
河口地区是河流生态系统和海洋生态系统之间的生态交错带,具有独特的环境特征和重要的生态服务功能. 在生源要素向海洋的输送中,河流一直扮演着至关重要的角色[1, 2]. 辽河是渤海海域较大的入海河流之一,沿岸工农业发达,大量的营养物质排泄入海,导致辽河口已普遍受到氮、 磷等营养物质的点源污染和面源污染,富营养化程度严重. 引起大辽河口及邻近海域浮游植物和其他水生植物异常繁殖,初级生产力急剧增加,水体溶解氧下降,水质恶化.
关于河口地区及其海域营养盐的分布变化规律,已有不少研究报道[3, 4, 5, 6, 7, 8, 9]. 蒋岳文等[10]对辽河口营养盐分布及变化规律进行分析得出,溶解无机氮和硅酸盐主要受海水稀释扩散作用控制,其行为是保守的,磷酸盐行为变化与季节有关; 王继龙等[11]的研究也表明辽河口溶解无机氮具有良好的保守行为,而磷酸盐存在吸附-解吸作用; 雷坤等[12]也发现N营养盐(硝酸盐、 亚硝酸盐、 氨氮)保守性较好,磷酸盐由于其缓冲特征,保守性较差.
尽管对大辽河口营养盐的行为已有一些研究,但这些研究大多集中于河口之外的海域,对淡咸水混合区营养盐的形态及行为缺乏系统的分析. 本研究拟通过对大辽河口春(4月)、 夏(7月)、 秋(11月)不同季节营养盐浓度的分析,探讨营养盐浓度的季节变化及其影响因素.
分别于2010年4、 7和11月,对大辽河口水域进行现场调查,用聚乙烯瓶采集表层水样,调查水域及具体采样站位位置见图 1所示.
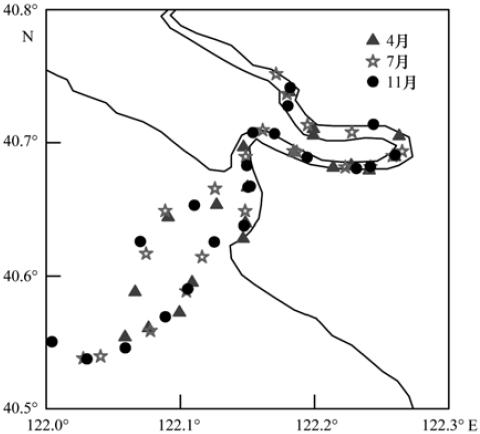 |
图 1 2010年4、 7、 11月大辽河口采样站位示意Fig.1Schematic map of sampling stations in April,July,November,2010 at Daliaohe Estuary |
预先准备好醋酸纤维滤膜(将其浸泡在1 ∶1000 HC1中24 h,之后再用Milli-Q水将其洗至中性)和聚乙烯瓶(将其浸泡在1 ∶5 HCl中24 h,之后再用去离子水将其洗至中性). 之后将水样用准备好的0.45 μm醋酸纤维滤膜进行过滤,过滤完毕后将滤液分别装在2个准备好的100 mL聚乙烯瓶中. 其中一个需保存在-20℃的冷冻环境中,以便于之后对磷酸盐(PO3-4-P)、 硝酸盐(NO-3-N)、 亚硝酸盐(NO-2-N)、 氨氮(NH+4-N)、 溶解态总磷(DTP)和溶解态总氮(DTN)的测定; 另准备聚醚砜膜(将其进行和醋酸纤维膜相同的处理,处理完后要将其烘干,并称重以用于对水体中悬浮颗粒物的测定),取另一份水样用聚醚砜膜进行过滤,过滤完后将滤膜在-20℃下的环境下进行冷冻保存以用于测定颗粒态磷(PP)、 颗粒态(PN).
德国BRAN+LUEBBE公司生产的QUAATRO型营养盐自动分析仪可以在实验室用来对无机态营养盐进行测定,测定的检出限分别为:PO3-4-P为0.01 μmol ·L-1,NO-3-N为0.02 μmol ·L-1,NO-2-N为0.02 μmol ·L-1,NH+4-N为0.03 μmol ·L-1,SiO2-3-Si为0.04 μmol ·L-1. 利用碱性过硫酸钾氧化法对颗粒态磷、 颗粒态氮、 溶解态总磷和溶解态总氮进行消化[13, 14],同时利用德国BRAN+LUEBBE公司生产的AAⅢ型营养盐自动分析仪进行测定. 溶解有机磷DOP=DTP-(PO3-4-P),溶解有机氮DON=DTN-DIN,总磷TP=DTP+PP,总氮TN=DTN+PN.
水中悬浮物含量是衡量水污染程度的指标之一,悬浮物是造成水浑浊的主要原因. 大辽河口表层水体中悬浮颗粒物含量很大,2010年4、 7、 11月表层水体中悬浮颗粒物的含量变化范围比较大,分别是0.12~0.81、 0.33~0.50、 0.044~0.44 g ·L-1,平均值分别是0.41、 0.16、 0.22 g ·L-1. 4月水体中悬浮颗粒物含量最大,7月最小. 2010年4、 11月表层水体中悬浮颗粒物的含量远大于四类海水水质标准[15]. 4月盐度<13时,SPM浓度在0.40 g ·L-1上下波动,盐度为13时出现SPM最低值,可能是由于河口区悬浮细颗粒物质发生絮凝作用,加速了悬浮物的沉降[3, 16]; 在盐度>13后,随盐度增加SPM浓度有逐渐增大的趋势,海水端达到最大值,这主要由于大辽河口水浅且当天口门风力很强,水体扰动加剧了底层颗粒物的再悬浮和表层颗粒物的不易沉降. 7月盐度<12.7时,随盐度增加SPM浓度有逐渐增大的趋势,盐度为12.7时达到最大值,随后SPM浓度逐渐降低; 11月盐度<10时SPM浓度随盐度增加逐渐增大,后随盐度增加有减小趋势. 这主要由于盐度15左右是咸淡水强烈混合区,水体扰动造成高的SPM浓度,往海水端由于混合减弱SPM浓度逐渐降低.
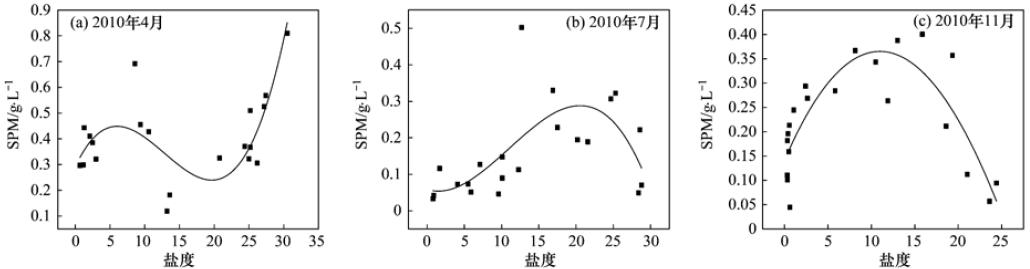 |
图 22010年4、 7、 11月大辽河口SPM与盐度的关系Fig.2Relationships between salinity and SPM in April,July and November of 2010 at Daliaohe Estuary |
4、 7、 11月叶绿素含量范围分别为2.07~11.5、 1.54~54.4、 1.48~95.8 μg ·L-1; 平均含量分别为6.80、 28.0、 48.7 μg ·L-1. 11月叶绿素含量最高,7月次之,4月最低,原因可能是经过一个夏天浮游植物的迅速增长时期,使得11月大辽河口水体的叶绿素浓度达到一个较大的水平. 4月、 11月叶绿素的最大值出现在淡水端,含量随盐度增加而降低; 7月最大值出现在海水端,含量随盐度增加而升高.
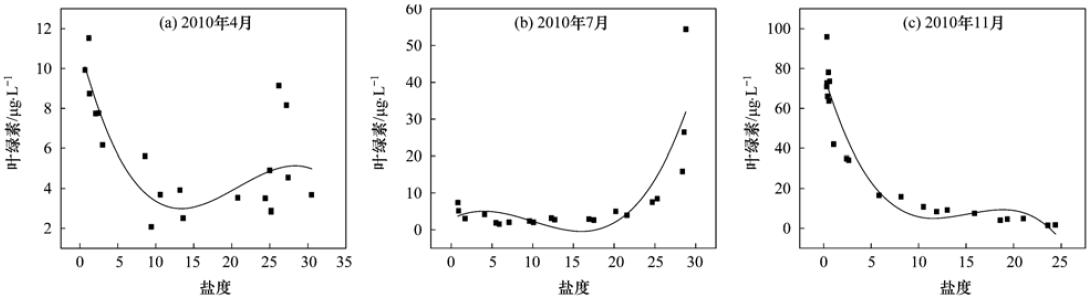 |
图 32010年4、 7、 11月大辽河口叶绿素与盐度的关系Fig.3Relationships between salinity and chlorophyll in April,July and November of 2010 at Daliaohe Estuary |
4月,PP占TP的比例为28%~50%,平均值为40%; DTP占TP的比例为50%~72%,平均值为60%,即DTP为TP的主要存在形态. 在DTP中,PO3-4-P占DTP的比例为14%~74%,平均值为43%; DOP占DTP的比例为26%~86%,平均值为57%,即大多数站位DOP为DTP的主要存在形态. 在所调查水域,磷酸盐、 DOP、 PP三者的含量相差并不太大. 7月,大辽河口水域大多数站位DOP为DTP的主要存在形态,DTP为TP的主要存在形态.
11月,DOP仍为DTP的主要存在形态.
大辽河口水域PO3-4-P、 DOP、 DTP、 TP平均含量的季节分布相似,均为4月最高,11月次之,7月最低(表1). 4月由于农业灌溉及化肥施用等导致PO3-4-P含量最高; 7月温跃层的出现导致水体垂直混合较差,底层的PO3-4-P无法到达表层水体及大量浮游植物对磷酸盐的吸收[17, 18, 19]导致其含量最低. 11月由于夏季大量繁殖的浮游生物死亡分解后,DOP转换为PO3-4-P,在海水中不断积累,此外沉积物再悬浮释放出PO3-4-P,所以PO3-4-P的浓度也比较高.
| 表1 2010年4、 7、 11月大辽河口各形态磷的含量 /μmol ·L-1Table 1 Concentrations of different P species in April,July and November of 2010 at Daliaohe Estuary/μmol ·L-1 |
不同季节、 不同形态磷的河口行为相差很大. DOP、 DTP浓度在4、 11月皆表现为淡水端浓度较高,随着盐度的增加浓度逐渐降低,其行为是保守的; 而7月,DOP、 DTP在淡水端浓度较低,随着盐度增加而逐渐升高,至盐度15左右达到最高值,后随着盐度增加浓度逐渐降低; 4、 7月PO3-4-P分布趋势为:海水端低,淡水端高,其行为是保守的,主要受海水对淡水的稀释作用控制; 11月活性磷酸盐的含量随水体中盐度增大变化的规律比较复杂,其原因是受到某种缓冲机制的控制(图 4). 在河口地区,磷酸盐会与悬浮颗粒物发生固-液界面的吸附-解吸作用,从而产生缓冲现象[18, 19, 20]; 此外这种分布特征还可能受沿岸人类生活及含磷废水排放的影响,活性磷酸盐[21, 22]、 石油类等是近岸水质的主要污染因子. 但是前者可能是主要原因,所以,辽河口水域活性磷酸盐的分布变化,除了物理混合过程外,也存在化学和生物过程的影响以及其他转移的可能[23, 24, 25].
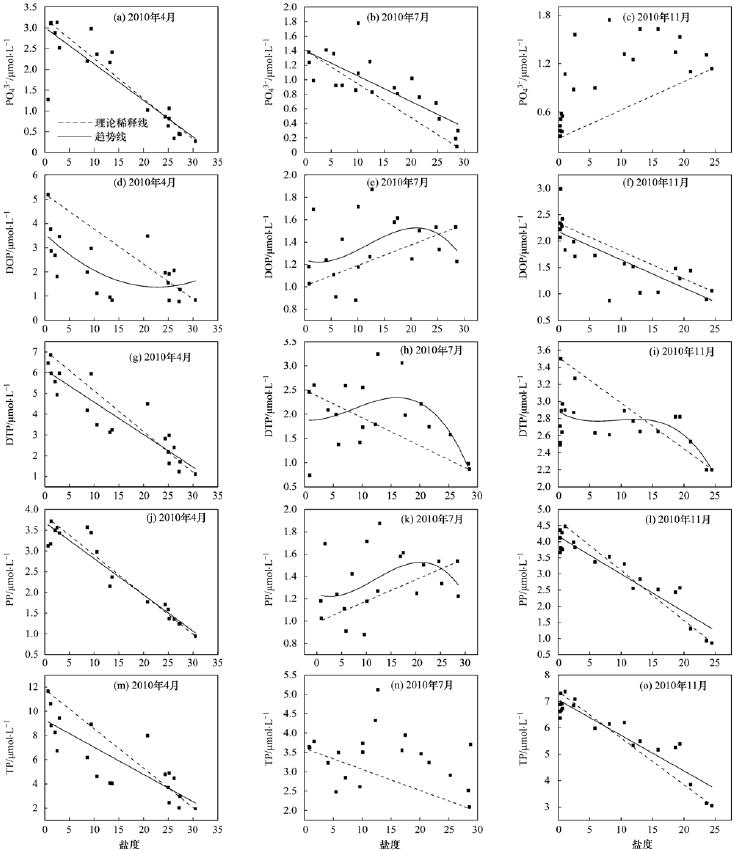 |
图 42010年4、 7、 11月大辽河口各形态磷与盐度的关系Fig.4Relationships between salinity and different forms of phosphorus in April,July and November of 2010 at Daliaohe Estuary |
与《海水水质标准》(GB 3097-1997)比较,4月有10个站位活性磷酸盐超过四类水质(1.45μmol ·L-1); 7月仅有1个站位超过四类水质; 11月有5个站位超过四类水质.
大辽河口水域4月,氨氮占DIN的比例为5%~82%,平均值为66%,大部分站位在50%以上,氨氮为DIN的主要存在形态(A20站除外,该站位氨氮只占5%,硝酸盐是DIN的主要存在形态); 硝酸盐占DIN的比例为17%~91%,平均值为33%; 亚硝酸盐占DIN的比例为1%~4%,平均值为2%,即亚硝酸盐在DIN中所占的比例最小. DIN占DTN的比例为34%~94%,平均值为70%; 即大多数站位DIN为DTN的主要存在形态(表2).
| 表2 2010年4、 7、 11月大辽河口各形态氮的含量 /μmol ·L-1Table 2 Concentrations of different N species in April,July and November of 2010 at Daliaohe Estuary/μmol ·L-1 |
PN占TN的比例为15%~67%,平均值为33%; DTN占TN的比例为33%~85%,平均值为67%,大多数站位DTN为TN的主要存在形态. 在调查的大部分水域,氨氮为TN的主要存在形态,其余依次是PN、 DON、 硝酸盐、 亚硝酸盐.
7月硝酸盐占DIN的比例为86%~98%,平均值为93%,为DIN的主要存在形态; 亚硝酸盐和氨氮占DIN的比例相近,亚硝酸盐稍大; DIN为DTN
的主要存在形态,DTN为TN的主要存在形态,各形态氮平均含量由大到小依次为硝酸盐、 DON、 PN、 亚硝酸盐、 氨氮.
11月硝酸盐占DIN的比例为73%~84%,平均值为77%,为DIN的主要存在形态; 亚硝酸盐和氨氮占DIN的比例相近,亚硝酸盐稍大,DIN为DTN的主要存在形态. DTN为TN的主要存在形态,各形态氮平均含量由大到小依次为硝酸盐、 DON、 PN、 氨氮、 亚硝酸盐.
大辽河口各形态氮浓度存在明显的季节变化,NO-3-N、 NO-2-N浓度7月最高,4月最低; NH+4-N、 DON、 PN的含量分布与NO-3-N、 NO-2-N相反,4月最高,7月最低. 2010年4月大辽河口水体中氨氮含量的异常高值,仅氨氮的平均含量就达到201 μmol ·L-1,是11月氨氮平均含量的4倍,7月氨氮平均含量的50倍之多,可能主要是由于春季沿岸农业生产基地化肥施用和灌溉用水退水所致. 大辽河口DIN含量相当高,远远高于长江口[26, 27]、 珠江口[28]、 黄河口[29]等河口.
不同季节、 不同形态氮的河口行为相差很大(图 5). NO-3-N、 DIN、 DTN皆表现为淡水端浓度最高,随着盐度的增加浓度逐渐降低,其行为是保守的,浓度主要受淡咸水混合过程控制. NO-2-N、 NH+4-N、 DON浓度在4、 11月皆表现为淡水端浓度较高,随着盐度的增加浓度逐渐降低,其行为是保守的; 而7月,NO-2-N、 NH+4-N和DON的分布则不同,表现为盐度<20时随盐度增加含量增大,说明河段及河口陆源输入对大辽河水域表层NO-2-N、 NH+4-N和DON有影响; 盐度>20后随盐度增大含量减小,而叶绿素此时迅速增加,说明主要是由于这段水体浮游植物量迅速增多,加速了对NO-2-N、 NH+4-N和DON的吸收以及海水的稀释作用. 由图 5所示,NO-2-N (7月)、 NH+4-N(7月)有添加行为,而同期NO-3-N未发现有移出现象,NO-3-N浓度平均含量225.6 μmol ·L-1,而NO-2-N、 NH+4-N的平均含量还不足10 μmol ·L-1,即使有移出行为也不会在数据上表现出来.
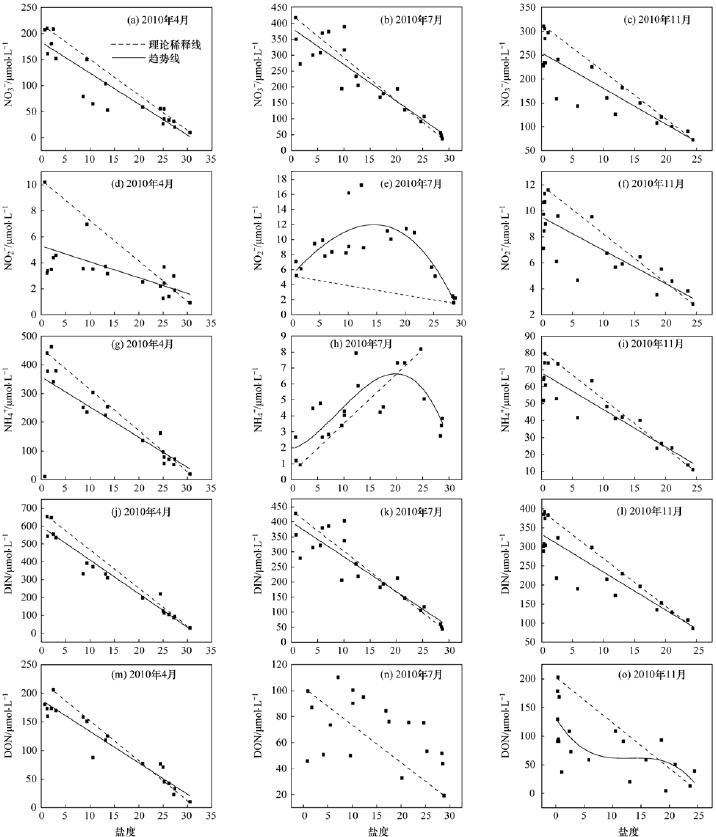 |
图 52010年4、 7、 11月大辽河口各形态氮与盐度的关系Fig.5Relationships between salinity and different forms of nitrogen in April,July and November of 2010 at Daliaohe Estuary |
与《海水水质标准》比较,水域所测站位溶解无机氮含量较高,虽然这3个月硝酸盐、 亚硝酸盐、 氨氮这3种形态所占比例相差很大,但溶解无机氮含量相差不大; 除4月一个站位外,其余站位溶解无机氮均超过四类《海水水质标准》(35.7 μmol ·L-1),由此可见大辽河口水域溶解无机氮的含量严重超标.
大辽河口水域4、 7、 11月硅酸盐的浓度变化范围是10.4~206.4、 7.14~121.5、 43.9~189.4μmol ·L-1,平均值为106.4、 70.7、 125.0μmol ·L-1, 11月的硅酸盐平均含量最高,4月最低(图 6).
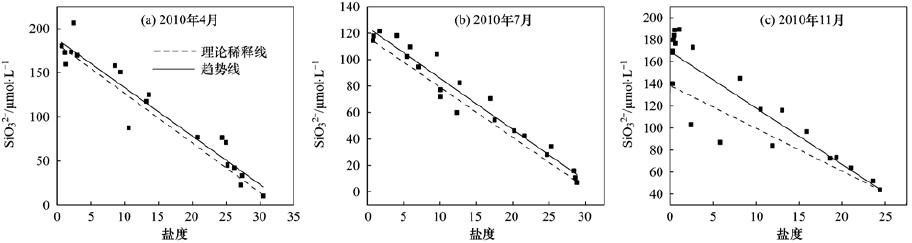 |
图 62010年4、 7、 11月大辽河口硅酸盐与盐度的关系Fig.6Relationships between salinity and silicate in April,July and November of 2010 at Daliaohe Estuary |
这3个月大辽河口水域的硅酸盐浓度呈现出了随水体盐度值增大而递减的趋势,均呈现保守行为. 于立霞[30]的研究与本研究结果基本一致,认为生物和化学作用对大辽河口水域硅酸盐分布变化的影响甚微,而起着主要影响作用的是辽河水和海水的物理混合过程.
在对水体中的营养盐结构进行考察时,往往需要用到N/P值这一重要指标. 在海水中,N/P值的正常比一般为16 ∶1[31],而浮游植物元素组分的CN/CP往往也处于同一水平,N/P值的波动会对浮游生物的生长产生一定的影响. 所以,CN/CP比值16被称为Redfield比值,可以用来判断生态环境中氮或磷是否处在缺乏状态.
有研究者提出一个系统评估每一种营养盐化学计量限制的标准[32]:①若Si/P>22和N/P>22,则PO3-4-P为限制因素; ②若N/P<10和Si/N>1,则无机氮为限制因素; ③若Si/P<10和Si/N<1,则SiO2-3-Si为限制因素.
随着盐度值的增大,DIN/P和Si/P随之逐渐下降,直到在海水端到达最低值. 通过表3可以看出,在4、 7和11月,辽河口的N/P的比例严重的失调,N/P值远远大于Redfield比值,初步推断对该水域中浮游植物的生长起重要作用的是PO3-4-P. 通过以上分析,可以得出这样的结论:大辽河口水域是受磷限制的.
| 表3 2010年4、 7、 11月大辽河口营养盐的比值Table 3 Ratio of nutrients in April,July and November of 2010 at Daliaohe Estuary |
(1)大辽河口水域各形态磷含量的季节变化明
显,PO3-4-P、DOP、DTP、TP含量春季最高,夏季最低; 不同季节不同形态磷的河口行为相差很大,PO3-4-P在4、 7月为保守的,在11月行为是非保守的; DOP、 DTP在4、 11月是保守的,在7月是非保守的.
(2)硝酸盐、 亚硝酸盐、 氨氮这3种形态在3个季节所占比例相差很大,但溶解无机氮含量相差不大,大辽河口水域溶解无机氮的含量严重超标. 不同季节不同形态氮的河口行为相差很大,NO-3-N、 DIN、 TN的行为在3个季节的行为都是保守的; NO-2-N、 NH+4-N、 DON的行为在4、 11月皆是保守的,而在7月其行为是非保守的,在河口内部存在添加源,同时也受生物活动的影响.
(3)硅酸盐含量为11月最高,4月最低; 3个季节其行为皆是保守的.
(4)大辽河口的营养盐结构严重失调,N/P值远远大于Redfield比值,PO3-4-P可能成为该水域浮游植物生长的限制因子之一.
| [1] | Benitez-Nelson C R. The biogeochemical cycling of phosphorus in marine systems[J]. Earth-Science Reviews, 2000, 51 (1-4): 109-135. |
| [2] | Shen Z L, Liu Q, Zhang S M, et al. A nitrogen budget of the Changjiang River catchment[J]. AMBIO, 2003, 32 (1): 65-69. |
| [3] | 李军, 高抒. 长江口悬浮颗粒体粒度特征及其季节性差异[J]. 海洋与湖沼, 2003, 34 (5): 499-509. |
| [4] | 王毅, 张天相. 辽河湾北部至辽西沿岸海域营养盐的分布特征及水质状况评价[J]. 海洋环境科学, 2001, 20 (2): 63-70. |
| [5] | 刘际弟. 海水中磷氮不同形态的同时测定[J]. 东海海洋, 2003, 21 (3): 47-53. |
| [6] | 王玉衡. 夏冬季东海营养盐的分布及水系化学特征的初步研究. 黑潮调查研究论文选(四)[M]. 北京: 海洋出版社, 1992. 280-288. |
| [7] | 王保栋, 王桂云, 郑昌洙, 等. 南黄海营养盐的平面分布及横向运输[J]. 海洋学报, 1999, 21 (6): 124-129. |
| [8] | Struyf E, Van Damme S, Meire P, et al. Possible effects of climate changes on estuarine nutrient fluxes: a case study in the highly nitrified Schelde estuary (Belgium, The Netherlands)[J]. Estuarine, Coastal and Shelf Science, 2004, 60 (4): 649-661. |
| [9] | Gao L, Li D J. Nutrient budgets averged over tidal cycles off the Changjiang Estuary[J]. Estuarine, Coastal and Shelf Science, 2008, 77 (3): 331-336. |
| [10] | 蒋岳文, 陈淑梅, 关道明, 等. 辽河口营养盐要素的化学特性及其入海通量估算[J]. 海洋环境科学, 1995, 14 (4): 39-45. |
| [11] | 王继龙, 郑丙辉, 秦延文, 等. 辽河口水域溶解氧与营养盐调查与分类[J]. 海洋技术, 2004, 23 (3): 92-96. |
| [12] | 雷坤, 郑丙辉, 孟伟, 等. 大辽河口N、P营养盐的分布特征及其影响因素[J]. 海洋环境科学, 2007, 26 (1): 19-22. |
| [13] | 王江涛, 赵卫红, 谭丽菊, 等. 海水中胶体有机碳的测定——高温燃烧法和紫外-过硫酸钾法的比较[J]. 海洋学报, 2000, 22 (2): 67-70. |
| [14] | 谭加强, 于志刚, 林桂炽, 等. 过硫酸盐氧化法测定海水中溶解总磷[J]. 青岛海洋大学学报(自然科学版), 2001, 31 (2): 256-262. |
| [15] | GB 3097-1997, 海水水质标准[S]. |
| [16] | Yang S L, Eisma D, Ding P X. Sedimentary processes on an estuarine island within the turbidity maximum zone of the Yangtze River mouth[J]. Geo-marine Letters, 2000, 20 (2): 87-92. |
| [17] | 宋树林. 车由岛附近海域营养盐分布特征[J]. 黄渤海海洋学报, 1994, 12 (3): 50-55. |
| [18] | 张正斌, 陈镇东, 刘莲生, 等. 海洋化学原理和应用——中国近海的海洋化学[M]. 北京: 海洋出版社, 1999. |
| [19] | 姚庆祯, 于志刚. 调水调沙对黄河下游营养盐变化规律的影响[J]. 环境科学, 2009, 30 (12): 3534-3540. |
| [20] | 石晓勇, 史致丽, 于恒, 等. 黄河口磷酸盐缓冲机制的探讨[J]. 海洋与湖沼, 1999, 30 (2): 193-198. |
| [21] | 张晟, 郑坚. 三峡水库入库支流水体中营养盐季节变化及输出[J]. 环境科学, 2009, 30 (1): 58-63. |
| [22] | 叶红, 潘蔚. 辽河口沿岸水质污染的光谱检测研究[J]. 水土保持研究, 2006, 13 (6): 188-194. |
| [23] | 李峥, 沈志良. 长江口及其附近海域磷的分布变化特征[J]. 海洋科学, 2007, 31 (1): 28-36. |
| [24] | 周菊珍, 谷国传. 长江口夏季营养盐的分布、变化及锋面对营养盐的影响[J]. 广州环境科学, 2002, 17 (1): 1-5. |
| [25] | 蒋岳文, 关道明, 陈淑梅, 等. 辽河口水域夏季营养盐分布与变化特征[J]. 海洋通报, 1996, 15 (3): 92-96. |
| [26] | 石晓勇, 王修林. 长江口邻近海域营养盐分布特征及其控制过程的初步研究[J]. 应用生态学报, 2003, 14 (7): 1086-1092. |
| [27] | 周俊丽, 刘征涛. 长江口营养盐浓度分布及变化特征[J]. 环境科学研究, 2006, 19 (6): 139-144. |
| [28] | 林以安, 苏纪兰. 珠江口夏季水体中的氮和磷[J]. 海洋学报, 2004, 26 (5): 63-73. |
| [29] | 张继民, 刘霜. 黄河口附近海域营养盐特征及富营养化程度评价[J]. 海洋通报, 2008, 27 (5): 65-71. |
| [30] | 于立霞. 夏季辽河口各形态营养盐的河口混合行为[J]. 海洋科学, 2011, 35 (12): 68-74. |
| [31] | Pilson M E Q. Annual cycles of nutrients and chlorophyll in Narragansett Bay, Rhode Island[J]. Journal of Marine Research, 1985, 43 (4): 849-873. |
| [32] | 张均顺, 沈志良. 胶州湾营养盐结构变化的研究[J]. 海洋与湖沼, 1997, 28 (5): 529-535. |
 2014, Vol.35
2014, Vol.35 


