2. 江苏大洋环保工程有限公司, 扬州 225000;
3. 同济大学环境科学与工程学院, 上海 200092;
4. 同济大学污染控制与资源化国家重点实验室, 上海 200092
2. Jiangsu Dayang Environmental Protection Engineering Co., Ltd., Yangzhou 225000, China;
3. School of Environmental Science and Engineering, Tongji University, Shanghai 200092, China;
4. State Key Laboratory of Pollution Control and Resource Recovery, Tongji University, Shanghai 200092, China
氨氮(ammonia nitrogen, NH4+-N)是引发水体富营养化的主要污染因子之一.据统计, 2020年全国废水总氮排放量为322.3万t, 其中氨氮排放量为98.4万t, 占总氮排放量的30.5%[1].大量氨氮废水排放到自然水体会加速水质的恶化, 引发水体富营养化和水体黑臭等环境问题[2].因此, 污水中氨氮的去除对于防治水体富营养化和改善水生态环境具有重大意义.
相对生物法、离子交换法和膜分离法等常见氨氮废水处理方法, 吸附法具有操作简单、效果稳定和处理成本低等优点.常用的NH4+-N吸附剂包括沸石、蒙脱石矿物[3]和生物炭[4]等.生物炭(biochar, BC)可由农业秸秆、生活垃圾和动物粪便等废弃生物质制备而来, 用于处理NH4+-N废水, 能够实现资源的回收利用.但将BC直接用于NH4+-N废水的处理存在去除性能较低的问题, 限制了BC在废水脱氮领域的推广和应用.因此, 对BC进行改性以提高其NH4+-N吸附性能有重要的研究和应用价值.
纳米金属粒子具有较大的比表面积和较多的吸附位点, 被广泛用于材料改性并可显著提升材料的吸附性能[5].其中, 纳米零价铁(nano zero-valent iron, nZVI)制备简单且来源广泛, 在水污染物治理领域表现出较好的应用前景[6].有研究表明, 纳米零价铁在沸石孔道内的负载可显著提升沸石的NH4+-N吸附性能[7].纳米零价铁在BC孔道内的负载也可以提升BC对水中重金属[8]、难降解有机物[9]和营养物质等[10]的去除能力.然而生物炭负载纳米零价铁对水中NH4+-N的去除效果和作用机制尚不明确, 有待进一步研究.
本文采用“Fe(Ⅱ)浸润-液相还原法”制备生物炭基纳米零价铁(nano-zero-valent iron modified biochar, nZVI@BC)复合材料, 考察其对水中NH4+-N的吸附性能.主要研究目标包括:①优化nZVI@BC的nZVI负载量, 提升复合材料对NH4+-N的吸附性能; ②通过动力学和等温吸附实验考察nZVI@BC对NH4+-N的吸附特性; ③探究污水中常见的共存阳离子对nZVI@BC吸附NH4+-N性能的影响; ④通过扫描电镜- X射线能谱(SEM-EDS)、比表面积分析(BET)、X射线衍射(XRD)和傅里叶变换红外光谱(FTIR)等表征手段揭示nZVI@BC的物化特性和NH4+-N吸附机制.
1 材料与方法 1.1 实验材料本实验中所用NH4Cl、NaOH、FeSO4·7H2O和NaBH4等试剂均为分析纯, 购自国药集团.碱改性生物炭的制备方法为:将新鲜竹子洗净后于80℃下烘至含水率在30%以内, 破碎至2 cm大小, 继续在80℃下干燥12 h, 将干燥后的竹子颗粒置于管式炉(YTGKD406-12, 叶拓, 上海)中, 在600℃的氮气氛围中热解30 min后取出, 过25目筛后于1 mol·L-1的NaOH溶液浸泡4 h, 滤出后使用去离子水洗涤至中性, 再在干燥箱(DZF-6050-220V, 科晶, 中国)中于110℃条件下烘干12 h, 制得本实验所用碱改性BC.
1.2 nZVI@BC的制备以上述制得的BC为基体, 通过“FeSO4浸润-NaBH4液相还原”的技术路线, 将nZVI负载于BC孔道内制备nZVI@BC.为考察nZVI负载量对nZVI@BC吸附NH4+-N性能的影响, 控制Fe和BC质量比为1 ∶5、1 ∶10、1 ∶20、1 ∶30、1 ∶40、1 ∶50和1 ∶60制备得到不同nZVI负载量的nZVI@BC, 分别命名为nZVI@BC1/5、nZVI@BC1/10、nZVI@BC1/20、nZVI@BC1/30、nZVI@BC1/40、nZVI@BC1/50和nZVI@BC1/60.具体方法为:称取一定量的FeSO4·7H2O溶于50 mL去离子水中, 加入0.56 g碱改性BC, 将氮气通入上述溶液中吹脱溶解氧, 在恒温振荡器(THZ-82, 精达, 常州)中于25℃条件下反应24 h; 使用蠕动泵(BT100-2J, LongerPump, 中国)缓慢向上述溶液中滴加20 mL浓度为1 mol·L-1的NaBH4溶液, 持续搅拌30 min.将所得样品使用去离去水和无水乙醇清洗3次, 冷冻干燥12 h制得复合吸附剂nZVI@BC.
1.3 吸附实验通过批次吸附实验研究nZVI负载量对nZVI@BC吸附NH4+-N的影响, 在装有100 mL含30 mg·L-1 NH4+-N溶液的锥形瓶中, 分别投加100 mg的BC、nZVI@BC1/5、nZVI@BC1/10、nZVI@BC1/20、nZVI@BC1/30、nZVI@BC1/40、nZVI@BC1/50和nZVI@BC1/60, 在25℃和转速180 r·min-1的条件下恒温振荡反应24 h.NH4+-N浓度采用纳氏试剂分光光度计法(752, 菁华, 上海)在420 nm下测定.分别投加100、150、200、250、300和350 mg优化负载量的nZVI@BC于固定体积和浓度的NH4+-N溶液中开展批次吸附实验, 考察nZVI@BC投加量对NH4+-N吸附的影响.在上述研究基础上, 开展nZVI@BC对NH4+-N的吸附动力学实验、等温吸附实验和竞争离子影响实验, 其中竞争离子实验中, 选择污水中常见的4种阳离子(Na+、K+、Mg2+和Ca2+)作为共存离子, 考察不同离子浓度对nZVI@BC吸附NH4+-N的影响.实验中以nZVI@BC对NH4+-N的吸附量为参考指标, 吸附量计算方法见式(1).
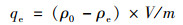
|
(1) |
式中, qe为NH4+-N吸附量, mg·g-1; ρ0为实验初始溶液中NH4+-N的质量浓度, mg·L-1; ρe为吸附结束后滤液中NH4+-N的质量浓度, mg·L-1; m为nZVI@BC的质量, g; V为实验中溶液的体积, mL.
NH4+-N去除率(w)的计算见式(2).

|
(2) |
分别采用扫描电子显微镜-X射线能谱(SEM-EDS, Vega-3XMU, Tescan, 捷克)、比表面积分析仪(BET, TRI-STAR3020, Micromeritics, 美国)、X射线衍射仪(XRD, 7000LX, Shimadzu, 日本)和傅里叶变换红外光谱仪(FTIR, iS5, Thermo Nicolet, 美国)测定BC和nZVI@BC的物理化学特性, 并探究nZVI@BC吸附NH4+-N的主要机制.
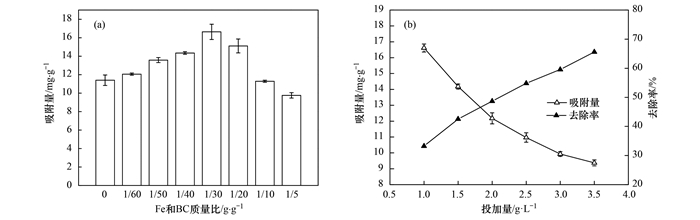
2 结果与讨论 2.1 nZVI@BC的优化nZVI负载量是制备nZVI@BC的重要条件, 对nZVI@BC的理化特性和吸附性能有重要影响.本文考察了7种不同的nZVI负载量对nZVI@BC吸附NH4+-N的影响.由图 1(a)可知, nZVI负载量对nZVI@BC吸附NH4+-N的性能有较明显的影响, 负载nZVI前生物炭对NH4+-N的吸附量为11.40 mg·g-1, 而负载nZVI后nZVI@BC1/60、nZVI@BC1/50、nZVI@BC1/40、nZVI@BC1/30和nZVI@BC1/20对NH4+-N的吸附量均高于BC, 其中Fe和BC质量比为1 ∶30时制备的nZVI@BC1/30对NH4+-N的吸附量最大, 达到16.64 mg·g-1. 已有研究表明, 有氧条件下nZVI会被氧化生成Fe(OH)3[7], 而Fe(OH)3具有吸附NH4+-N的性能[11].本研究中并未对实验用水进行脱氧处理, 具备将ZVI氧化为Fe(OH)3的反应条件, 从而促进nZVI@BC对NH4+-N的吸附.随着nZVI负载量的增加nZVI@BC对NH4+-N的吸附量逐渐增加, 当nZVI负载量超过1 ∶30时, nZVI@BC对NH4+-N的吸附量开始逐渐降低, 其中nZVI@BC1/10和nZVI@BC1/5对NH4+-N的吸附量均低于BC.已有研究表明, nZVI负载量较高时易发生团聚[12], 堵塞BC孔道, 导致nZVI@BC比表面积和活性位点减少, 从而降低材料的NH4+-N吸附性能, Xu等[13]的研究也得到了类似的结果.后续实验中如无特殊说明, 均采用nZVI@BC1/30开展研究.
|
(a)ZVI负载量对NH4+-N吸附性能的影响; (b)投加量对NH4+-N吸附性能的影响 图 1 nZVI@BC的优化 Fig. 1 Optimization of nZVI@BC |
由图 1(b)nZVI@BC投加量对NH4+-N吸附的影响可知, NH4+-N去除率与nZVI@BC投加量呈正相关, 而NH4+-N吸附量与投加量呈负相关.nZVI@BC的投加量越多, 吸附体系内的活性位点数也越多, NH4+-N被吸附的概率越大.但吸附体系内NH4+-N的初始浓度有限, 投加nZVI@BC超过一定量后, 体系内没有足够的NH4+-N与吸附位点结合, 导致nZVI@BC的吸附量降低[14].应用中应结合处理工艺和处理要求, 选择合适的nZVI@BC投加量, 达到节省物料和去除NH4+-N的目的.本研究综合考虑nZVI@BC的吸附量、去除率和处理成本等因素, 将nZVI@BC的最佳投加量设定为2.0 g·L-1.
2.2 吸附动力学在上述研究基础上, 为探究nZVI@BC对NH4+-N的潜在吸附机制, 本研究开展了nZVI@BC对NH4+-N的吸附动力学实验[15], 并采用伪一级动力学模型、伪二级动力学模型和颗粒内扩散模型对nZVI@BC吸附NH4+-N的吸附动力学实验数据进行拟合[16].
伪一级动力学模型:
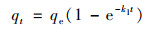
|
(3) |
伪二级动力学模型:

|
(4) |
颗粒内扩散模型:
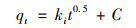
|
(5) |
式中, qt为t时刻nZVI@BC对NH4+-N的吸附量, mg·g-1; qe为nZVI@BC吸附NH4+-N平衡时的吸附量, mg·g-1; t为nZVI@BC吸附NH4+-N时间, min; k1、k2和ki分别为伪一级动力学、伪二级动力学和颗粒内扩散速率常数; C为涉及到厚度和边界层的常数.
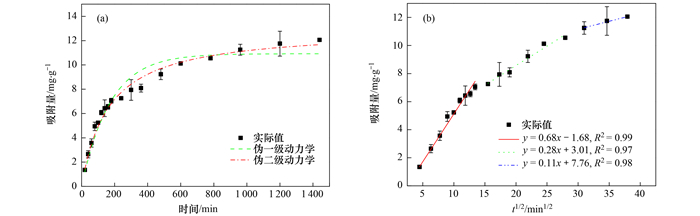
由伪一级动力学模型和伪二级动力学模型的拟合结果可以看出[图 2(a)], 在nZVI@BC吸附NH4+-N的初始阶段(前200 min内), nZVI@BC对NH4+-N的吸附速率较快, 约占材料对NH4+-N吸附总量的58.46%, 随后吸附速度逐渐变缓; 在960 min时nZVI@BC对NH4+-N的吸附达到饱和, 进入吸附平衡阶段.从伪一级动力学和伪二级动力学模型常数可知(表 1), 伪二级动力学相关系数(R2=0.99)大于伪一级动力学的相关系数(R2=0.98), 说明nZVI@BC吸附NH4+-N的过程中存在化学反应[17].
|
(a)nZVI@BC1/30对NH4+-N吸附随时间变化曲线; (b)颗粒内扩散模型 图 2 nZVI@BC1/30 NH4+-N吸附动力学 Fig. 2 Adsorption kinetics of NH4+-N on nZVI@BC1/30 |
|
|
表 1 nZVI@BC1/30吸附NH4+-N的吸附动力学模型参数 Table 1 Kinetic parameters of NH4+-N removal by nZVI@BC1/30 |
为考察NH4+-N向nZVI@BC内的扩散机制, 使用颗粒内扩散模型对其吸附过程进行拟合, 拟合结果如图 2(b)所示, 呈三段式直线特征.第一阶段、第二阶段和第三阶段的相关系数R2分别为0.99、0.97和0.98.起始阶段(200 min以内)为NH4+-N扩散到nZVI@BC外表面的过程, 由液膜扩散控制, k值较大(0.68), 说明NH4+-N的液膜扩散过程很快, 吸附量迅速上升.第二阶段(200~780 min)为NH4+-N在nZVI@BC颗粒内的渐进吸附阶段, 当nZVI@BC颗粒外表面吸附达到饱和时, NH4+-N进入内孔区, 并被nZVI@BC的内表面吸附, 由于吸附位点的减少、扩散阻力的增加以及溶液中NH4+-N浓度的逐渐降低, 导致扩散速率下降, k值较小(0.28), 此阶段为重要的吸附速率控制阶段.第三阶段(780~1 440 min)是最终的吸附平衡阶段, 其中NH4+-N吸附和解吸的速率保持相等, k值最小(0.11).颗粒内扩散模型拟合得到的线性方程截距均不为零, 且第一阶段和第二阶段的吸附量分别约为饱和吸附量的58.46%和28.86%, 说明nZVI@BC对NH4+-N的吸附过程除了受表面吸附控制之外, 还受nZVI@BC内扩散的控制, 且内扩散阶段为限速阶段[18].
2.3 等温吸附曲线为进一步研究nZVI@BC对NH4+-N的吸附作用, 本研究开展了nZVI@BC对NH4+-N的等温吸附实验.等温吸附实验数据使用Langmuir模型和Freundlich模型进行拟合[19].
Langmuir方程:

|
(6) |
Freundlich方程:
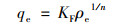
|
(7) |
式中, qe为nZVI@BC吸附NH4+-N平衡时的吸附量, mg·g-1; qm为nZVI@BC对NH4+-N的最大吸附量, mg·g-1; ρe为nZVI@BC吸附平衡时溶液中剩余的NH4+-N质量浓度, mg·L-1; KL为Langmuir模型参数, L·mg-1; KF为Freundlich模型参数, (mg·g-1)·(L·mg-1)1/n; n为Freundlich模型参数.
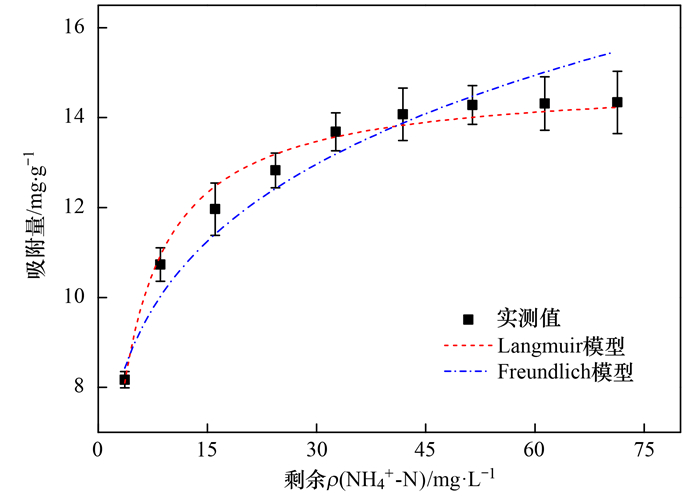
由图 3可知, nZVI@BC1/30对NH4+-N的吸附量随着NH4+-N初始浓度的升高而增加, 但当剩余NH4+-N质量浓度超过41.85 mg·L-1时, 吸附量便趋于平衡.Langmuir模型一般用于描述等温条件下均一表面的单层吸附过程, 认为吸附点均匀分布在吸附剂的表面, 这种吸附一般情况下主要为化学吸附[20].由表 2 nZVI@BC1/30对NH4+-N的等温吸附拟合参数可知, Langmuir模型的相关系数R2为0.99, Freundlich模型的相关系数R2为0.96, Langmuir模型更适合用来描述nZVI@BC1/30对NH4+-N的等温吸附过程, 表明nZVI@BC表面吸附位点分布较为均匀.
|
图 3 nZVI@BC1/30对NH4+-N的等温吸附曲线 Fig. 3 Isotherm adsorption curves of NH4+-N by nZVI@BC1/30 |
|
|
表 2 nZVI@BC1/30吸附NH4+-N的等温吸附模型的吸附参数 Table 2 Isothermal parameters for NH4+-N adsorption by nZVI@BC1/30 |
通过下式可以求得一个无量纲的平衡常数RL:
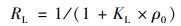
|
(8) |
当RL=0时这个过程是不可逆的; RL在0~1之间时, 通常认为该过程是有利且自发进行的; 当RL=1时, 该过程是线性吸附过程; 当RL大于1时, 该过程不能自发进行[21].由表 2可知, RL的值为0.03~0.13, 说明nZVI@BC对NH4+-N的吸附为有利吸附.且随着初始浓度的增加, RL值不断减小, 说明污染物浓度越高越有利于吸附.此外, Freundlich常数n值大于1, 同样说明nZVI@BC对NH4+-N的吸附是有利吸附[22], 与Langmuir中平衡常数RL所推导的结论一致.
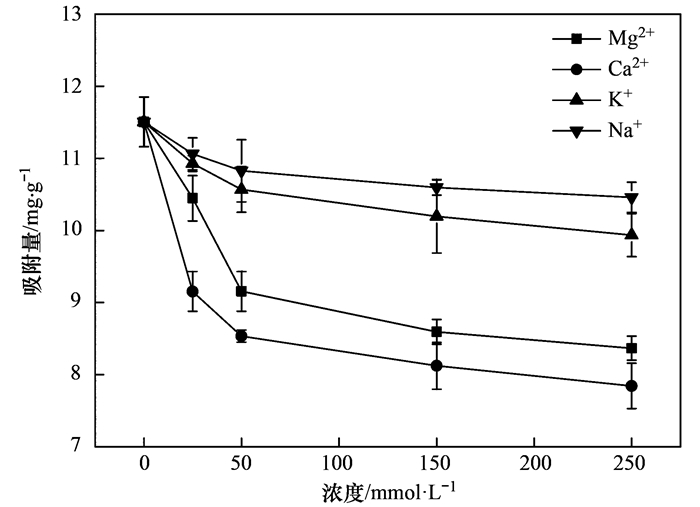
2.4 共存离子对吸附的影响废水中通常存在大量的矿物质和盐类, 这些共存离子可能会对nZVI@BC吸附NH4+-N产生影响.本研究考察了4种污水中常见的阳离子K+、Na+、Mg2+和Ca2+对nZVI@BC吸附NH4+-N的影响.由图 4可知, 随着共存阳离子浓度的升高nZVI@BC对NH4+-N的吸附性能逐渐降低, 其中K+和Na+对NH4+-N吸附的影响要小于Mg2+和Ca2+, 说明低价态阳离子的吸附竞争能力更弱, 吸附竞争能力由强到弱依次为:Ca2+>Mg2+>K+>Na+.有研究表明Mg2+和Ca2+相较于K+和Na+具有更大的电荷密度, 且对某些官能团有一定的络合能力, 因此会占据更多的吸附位点, 导致Mg2+和Ca2+对NH4+-N具有更强的竞争吸附能力[23].此外, 也有研究认为共存阳离子对NH4+-N吸附产生影响说明吸附机制存在离子交换[19].
|
图 4 共存离子对NH4+-N吸附的影响 Fig. 4 Influence of coexisting ions on NH4+-N adsorption |
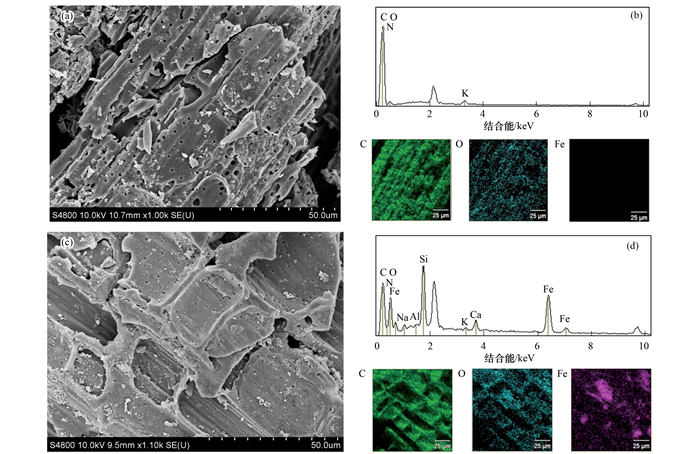
采用扫描电镜对零价铁改性前后BC的组成和微观结构进行表征, 由图 5(a)可以看出, BC表面粗糙, 具有孔状结构, 孔隙丰富, 可提供NH4+-N吸附和零价铁负载的位点[24].由图 5(c)可以看出, 负载零价铁后nZVI@BC表面呈现出“糖霜”样结构.对比分析图 5(b)和图 5(d)中BC和nZVI@BC的元素分布, 在nZVI@BC和BC中均含有C和O元素, BC中未检测到Fe元素, 而nZVI@BC中存在Fe元素, 且Fe元素能较为均匀地分布于nZVI@BC表面, 说明材料合成是成功的. EDS可以定性分析出材料的组成和元素占比, 从图 5(b)和图 5(d)可以看出, BC无铁峰, 而负载ZVI后nZVI@BC出现了明显的Fe峰.由表 3可知, Fe元素在nZVI@BC中占比为3.22%, O元素在零价铁负载后, 在材料中的占比也提高了约3.20个百分点, 说明nZVI@BC表面部分零价铁被氧化.BC和nZVI@BC中均含有一定量的K+离子, 而K+可与水中的NH4+-N发生离子交换[23].
|
(a)生物炭SEM图; (b)生物炭EDS图以及元素分布; (c)nZVI@BC SEM图; (d)nZVI@BC EDS图以及元素分布 图 5 扫描电镜图 Fig. 5 Scanning electron microscope |
|
|
表 3 BC和nZVI@BC主要元素组成/% Table 3 Composition of major elements in BC and nZVI@BC/% |
BC和nZVI@BC的BET分析结果如表 4所示.与BC相比, nZVI@BC的比表面积、孔容、微孔比表面积和微孔孔容都有着不同程度的降低; 生物炭的平均孔径在微孔范围(<2 nm), 而nZVI@BC的平均孔径在介孔范围(2~50 nm), 说明nZVI的负载对BC的孔结构产生了明显的影响.结合SEM分析, 比表面积减少和平均孔径增大的原因可能是nZVI颗粒进入到BC的多孔结构中, 微孔和部分介孔被填充, 导致整体比表面积降低, 平均孔径增加[25].本研究中nZVI@BC对NH4+-N的吸附性能并未因比表面积和微孔孔容的减少而降低, 反而有显著提升, 说明范德华力和微孔填充并不是nZVI@BC吸附NH4+-N的主要作用机制.
|
|
表 4 BC和nZVI@BC的BET分析 Table 4 BET analysis of BC and nZVI@BC |
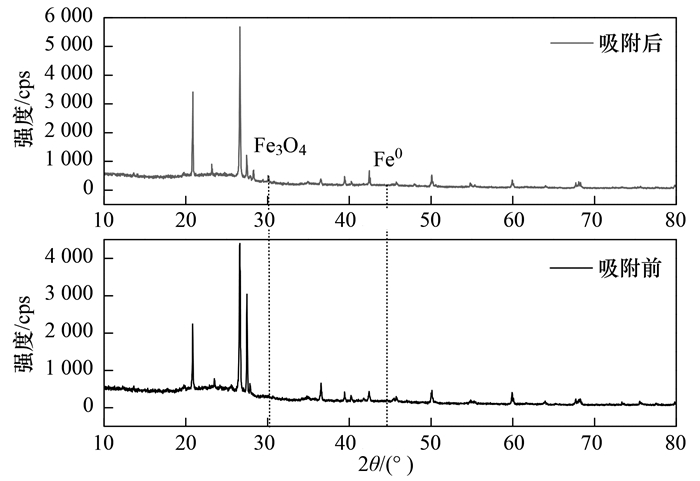
材料中的XRD图谱如图 6所示, 吸附NH4+-N前的nZVI@BC材料中存在零价铁的特征峰(44.8°)[7], 吸附NH4+-N后的nZVI@BC材料出现了Fe3O4的特征峰(30.1°)[26], 而零价铁的特征峰消失.nZVI可通过Fe0→Fe(OH)2→Fe3O4→(γ-Fe2O3)的途径被氧化[27], 并且好氧条件有利于Fe(OH)3的形成[28].本文氨氮吸附实验中, 并未进行脱氧处理, 水中溶解氧浓度约为8 mg·L-1, nZVI@BC中的nZVI可被氧化形成Fe(OH)3[见式(9)~式(11)][7].Fe(OH)3可通过氢键与NH4+-N结合[11], 提升nZVI@BC对NH4+-N的吸附性能.

|
(9) |

|
(10) |
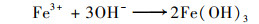
|
(11) |
|
图 6 nZVI@BC XRD图谱 Fig. 6 XRD patterns of nZVI@BC nZVI@BC |
对吸附NH4+-N前后的nZVI@BC进行FTIR检测.由图 7可知, nZVI@BC吸附NH4+-N后, 在1 536 cm-1处产生了1个新峰, 它是N—H的伸缩振动[29], 说明NH4+-N成功地吸附到了nZVI@BC表面.而630~750 cm-1处有一个宽峰带同时也发生了变化, 这处的峰主要是Fe—O等金属含氧官能团的吸收峰[30], 它们在吸附NH4+-N后, 峰强有一定减弱, 说明NH4+-N和这些含氧官能团产生了反应, 这可能是N与O元素之间的氢键结合.另外1处宽峰带位于3 300~3 450 cm-1处, 它是羟基(—OH)的吸收峰[19], 它的减弱也是由于N与O元素之间的氢键结合.

|
图 7 傅里叶变换红外光谱图 Fig. 7 Fourier transform infrared spectra |
综合前述内容可知, nZVI@BC吸附NH4+-N的机制主要为离子交换和氢键结合(图 8), 其中离子交换与BC原材料的特性有关, 而氢键结合主要源于负载nZVI的氧化.
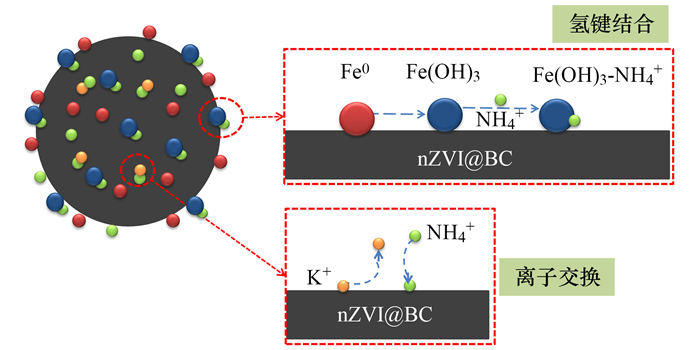
|
图 8 nZVI@BC NH4+-N吸附机制 Fig. 8 Removal pathways of NH4+-N by nZVI/BC |
(1) nZVI@BC1/30对NH4+-N的吸附效果最佳, 在298 K下其对NH4+-N的最大吸附量可达16.60 mg·g-1, NH4+-N吸附性能提高了45.96%.
(2) 污水中4种常见的共存阳离子对nZVI@BC吸附NH4+-N的竞争性抑制效果由大到小依次为:Ca2+>Mg2+>K+>Na+.
(3) nZVI@BC对NH4+-N的吸附过程更符合伪二级动力学和Langmuir模型, 且NH4+-N吸附的内扩散阶段是限速阶段.
(4) nZVI@BC吸附NH4+-N的主要机制为BC与NH4+-N之间的离子交换和负载nZVI后与NH4+-N之间的氢键结合.
| [1] | 中华人民共和国生态环境部. 2020年中国生态环境统计年报[M]. 北京: 中国环境出版社, 2022. |
| [2] |
高寒, 周其胤, 贺振洲, 等. 城市黑臭水体识别监测与治理技术研究现状及进展[J]. 环境工程, 2018, 36(10): 1-4. Gao H, Zhou Q Y, He Z Z, et al. Research status and progress of the identification, monitoring and treatment technology of black and odorous water body in the city[J]. Environmental Engineering, 2018, 36(10): 1-4. DOI:10.13205/j.hjgc.201810001 |
| [3] |
焦巨龙, 杨苏文, 谢宇, 等. 多种材料对水中氨氮的吸附特性[J]. 环境科学, 2019, 40(8): 3633-3641. Jiao J L, Yang S W, Xie Y, et al. Adsorption properties of ammonia nitrogen in aqueous solution by various materials[J]. Environmental Science, 2019, 40(8): 3633-3641. DOI:10.13227/j.hjkx.201811199 |
| [4] | Zhang M, Song G, Gelardi D L, et al. Evaluating biochar and its modifications for the removal of ammonium, nitrate, and phosphate in water[J]. Water Research, 2020, 186. DOI:10.1016/j.watres.2020.116303 |
| [5] | Liu J W, Jiang J G, Meng Y, et al. Preparation, environmental application and prospect of biochar-supported metal nanoparticles: a review[J]. Journal of Hazardous Materials, 2020, 388. DOI:10.1016/j.jhazmat.2020.122026 |
| [6] |
徐妍, 苑春刚. 纳米零价铁复合材料制备、稳定方法及其水处理应用[J]. 化学进展, 2022, 34(3): 717-742. Xu Y, Yuan C G. Preparation, stabilization and applications of Nano-zero-valent iron composites in water treatment[J]. Progress in Chemistry, 2022, 34(3): 717-742. |
| [7] | Eljamal O, Eljamal R, Maamoun I, et al. Efficient treatment of ammonia-nitrogen contaminated waters by nano zero-valent iron/zeolite composite[J]. Chemosphere, 2022, 287. DOI:10.1016/j.chemosphere.2021.131990 |
| [8] | Newsome L, Morris K, Cleary A, et al. The impact of iron nanoparticles on technetium-contaminated groundwater and sediment microbial communities[J]. Journal of Hazardous Materials, 2019, 364: 134-142. DOI:10.1016/j.jhazmat.2018.10.008 |
| [9] | Song Y, Fang G D, Zhu C Y, et al. Zero-valent iron activated persulfate remediation of polycyclic aromatic hydrocarbon-contaminated soils: an in situ pilot-scale study[J]. Chemical Engineering Journal, 2019, 355: 65-75. DOI:10.1016/j.cej.2018.08.126 |
| [10] | Ruhl A S, Vnal N, Jekel M. Evaluation of two-component Fe(0) fixed bed filters with porous materials for reductive dechlorination[J]. Chemical Engineering Journal, 2012, 209: 401-406. DOI:10.1016/j.cej.2012.08.006 |
| [11] | Liu H B, Chen Z H, Guan Y N, et al. Role and application of iron in water treatment for nitrogen removal: a review[J]. Chemosphere, 2018, 204: 51-62. DOI:10.1016/j.chemosphere.2018.04.019 |
| [12] | Wang X Y, Du Y, Ma J. Novel synthesis of carbon spheres supported nanoscale zero-valent iron for removal of metronidazole[J]. Applied Surface Science, 2016, 390: 50-59. DOI:10.1016/j.apsusc.2016.08.027 |
| [13] | Xu C H, Zhu L J, Wang X H, et al. Fast and highly efficient removal of chromate from aqueous solution using nanoscale zero-valent iron/activated carbon (NZVI/AC)[J]. Water, Air, & Soil Pollution, 2014, 225(2). DOI:10.1007/s11270-013-1845-1 |
| [14] | Chen T, Zhang Y X, Wang H T, et al. Influence of pyrolysis temperature on characteristics and heavy metal adsorptive performance of biochar derived from municipal sewage sludge[J]. Bioresource Technology, 2014, 164: 47-54. DOI:10.1016/j.biortech.2014.04.048 |
| [15] |
魏存, 吕豪豪, 汪玉瑛, 等. 铁改性稻壳生物炭对铵态氮的吸附效果研究[J]. 植物营养与肥料学报, 2021, 27(4): 595-609. Wei C, Lü H H, Wang Y Y, et al. Adsorption effectiveness of ammonium nitrogen by iron-modified rice husk biochars[J]. Journal of Plant Nutrition and Fertilizers, 2021, 27(4): 595-609. |
| [16] |
赵文金, 张顺, 安晓强, 等. 聚硫代酰胺修饰活性炭对Au(Ⅲ)的选择性吸附效果与机制[J]. 环境科学, 2022, 43(3): 1521-1528. Zhao W J, Zhang S, An X Q, et al. S Selective adsorption of Au(Ⅲ) by activated carbon supported polythioamides and adsorption mechanism[J]. Environmental Science, 2022, 43(3): 1521-1528. |
| [17] | Ho Y S, McKay G. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 1999, 34(5): 451-465. DOI:10.1016/S0032-9592(98)00112-5 |
| [18] | Arami M, Limaee N Y, Mahmoodi N M. Evaluation of the adsorption kinetics and equilibrium for the potential removal of acid dyes using a biosorbent[J]. Chemical Engineering Journal, 2008, 139(1): 2-10. DOI:10.1016/j.cej.2007.07.060 |
| [19] |
王芳君, 桑倩倩, 邓颖, 等. 磁性铁基改性生物炭去除水中氨氮[J]. 环境科学, 2021, 42(4): 1913-1922. Wang F J, Sang Q Q, Deng Y, et al. Synthesis of magnetic iron modifying biochar for ammonia nitrogen removal from water[J]. Environmental Science, 2021, 42(4): 1913-1922. |
| [20] | Yao Y, Gao B, Inyang M, et al. Removal of phosphate from aqueous solution by biochar derived from anaerobically digested sugar beet tailings[J]. Journal of Hazardous Materials, 2011, 190(1-3): 501-507. DOI:10.1016/j.jhazmat.2011.03.083 |
| [21] | Jack J, Huggins T M, Huang Y P, et al. Production of magnetic biochar from waste-derived fungal biomass for phosphorus removal and recovery[J]. Journal of Cleaner Production, 2019, 224: 100-106. DOI:10.1016/j.jclepro.2019.03.120 |
| [22] |
陈梅, 王芳, 张德俐, 等. 生物炭结构性质对氨氮的吸附特性影响[J]. 环境科学, 2019, 40(12): 5421-5429. Chen M, Wang F, Zhang D L, et al. Effect of biochar structure on adsorption characteristics of ammonia nitrogen[J]. Environmental Science, 2019, 40(12): 5421-5429. |
| [23] | Yang H I, Lou K Y, Rajapaksha A U, et al. Adsorption of ammonium in aqueous solutions by pine sawdust and wheat straw biochars[J]. Environmental Science and Pollution Research, 2018, 25(26): 25638-25647. DOI:10.1007/s11356-017-8551-2 |
| [24] | Clough T J, Bertram J E, Ray J L, et al. Unweathered wood biochar impact on nitrous oxide emissions from a bovine-urine-amended pasture soil[J]. Soil Science Society of America Journal, 2010, 74(3): 852-860. DOI:10.2136/sssaj2009.0185 |
| [25] | Neeli S T, Ramsurn H. Synthesis and formation mechanism of iron nanoparticles in graphitized carbon matrices using biochar from biomass model compounds as a support[J]. Carbon, 2018, 134: 480-490. DOI:10.1016/j.carbon.2018.03.079 |
| [26] | Zhao H X, Lang Y H. Adsorption behaviors and mechanisms of florfenicol by magnetic functionalized biochar and reed biochar[J]. Journal of the Taiwan Institute of Chemical Engineers, 2018, 88: 152-160. DOI:10.1016/j.jtice.2018.03.049 |
| [27] | Kumar N, Auffan M, Gattacceca J, et al. Molecular insights of oxidation process of iron nanoparticles: spectroscopic, magnetic, and microscopic evidence[J]. Environmental Science & Technology, 2014, 48(23): 13888-13894. |
| [28] | Peng X, Xi B D, Zhao Y, et al. Effect of arsenic on the formation and adsorption property of ferric hydroxide precipitates in ZVI treatment[J]. Environmental Science & Technology, 2017, 51(17): 10100-10108. |
| [29] | Zhu K R, Fu H, Zhang J H, et al. Studies on removal of NH4+-N from aqueous solution by using the activated carbons derived from rice husk[J]. Biomass and Bioenergy, 2012, 43: 18-25. |
| [30] | Zhu Z Q, Huang C P, Zhu Y N, et al. A hierarchical porous adsorbent of Nano-α-Fe2O3/Fe3O4 on bamboo biochar (HPA-Fe/C-B) for the removal of phosphate from water[J]. Journal of Water Process Engineering, 2018, 25: 96-104. |
 2023, Vol. 44
2023, Vol. 44

