Primary Factors Affecting Soil Bioavailable Cadmium and Asenic by Different Properties of Silicon Fertilizer
镉(Cd)和砷(As) 是广泛存在于自然界中的两种重(类重)金属元素, 具有极强的生物毒性, 若其大量集聚在土壤中不仅会危害农作物生长, 更会通过食物链聚集到人体中给人类健康造成不可逆的伤害[1, 2].近年来, 随着现代工业及农业的发展, 人类不合理的生产活动导致Cd和As被大量排放进入环境中, 造成严重的土壤Cd和As污染, 土壤Cd和As污染点位超标率分别高居我国无机污染物类型的第一和第三位[3], 污染形势严峻, 矿区及冶炼区附近大量耕作区土壤被污染更严重威胁到粮食安全以及人类社会的可持续发展[4].而值得注意的是, 重金属的生物活性与毒性不仅与其在土壤中的总量有关, 更多的是由其在土壤中的有效态所决定的[5, 6].从重金属进入到植物体内的迁移过程来看, 土壤中活性态Cd和As从土壤矿物质表面迁移至植物根系表层并被吸收利用的过程是决定植物体内Cd和As积累量的关键[7, 8], 因此减少农作物中Cd和As积累量最重要措施之一就是从源头降低农田土壤中Cd和As的迁移性和生物有效性.在所有土壤重金属污染修复技术中, 原位钝化技术是目前应用于降低土壤中重金属有效性的主要措施之一, 但是一方面由于原位钝化技术一般会引入其他物质进入土壤, 因此可能会造成二次污染; 另一方面, 对原位钝化技术是否会长期有效, 后期是否会造成重金属的再次活化而造成污染加剧缺乏长期大范围定位试验验证[9, 10].
Cd和As在耕作土壤中的迁移性、赋存形态和生物活性的大小不仅受成土母质等自然原因的影响, 还会受到农艺调控措施的影响如肥料的施用、耕作和栽培措施以及田间水分管理等措施[11].适当的农艺调控措施通过对土壤pH、Eh和有机质含量等土壤物理化学性质产生影响, 从而影响吸附在土壤固相上的Cd和As的赋存形态、迁移性和生物有效性.相比其他修复措施, 农艺调控措施治理Cd和As污染稻田土壤具有经济成本低、操作简单且绿色高效二次污染小等优点[12].其中, 目前国内外学者对如何利用田间施肥措施调控土壤重金属污染研究较为广泛[13, 14].而硅肥由于其可同时缓解土壤Cd和As复合污染对植物造成的危害, 而被科研工作者广泛报道研究[14~16].如Ji等[17]通过往Cd污染稻田土壤中施用硅肥, 发现硅肥的施用能显著抑制水稻籽粒中Cd积累, 达到安全生产的目的.高子翔等[18]研究了基施硅肥对土壤中Cd生物有效性及对水稻籽粒中Cd积累量的影响, 发现使用15~60 mg·kg-1能显著降低低Cd和高Cd污染土壤中Cd的生物有效性和水稻中籽粒Cd的积累量.Wang等[16]在田间试验中同时施用硅钙肥和硅钾肥可同时降低水稻籽粒中Cd和As的含量.据报道, 硅肥主要通过改变土壤pH和提高土壤中有效硅含量与土壤中活性态Cd形成稳定的Si-Cd络合物来降低土壤中Cd的活性和植物对Cd的吸收[3].但是一般硅肥的施用导致的土壤pH上升对于土壤中As来说却有活化作用[4], 硅肥主要通过阻控水稻对As的吸收和转运来降低籽粒中As的积累[3].
但是, 就土壤层面来说, 施用硅肥可以改变土壤pH和土壤有效硅等土壤理化性质从而对土壤中Cd和As生物有效性产生影响.但是多数研究在试验中应用的硅肥都是碱性硅肥[16~18], 都具有提高土壤pH和土壤有效态硅的作用, 从而影响土壤中活性态Cd和As含量, 这就造成很难区分究竟是pH还是土壤有效硅在影响土壤中Cd和As的生物有效性; 另外土壤中有效态磷的含量也对土壤Cd和As的生物有效性存在影响[19~22], 如磷可与Cd形成稳定的磷酸盐沉淀Cd3(PO4)2[23], 但是不同添加量硅肥对土壤中有效态磷的释放是否存在影响, 进而影响到土壤中生物有效态Cd和As的含量却少有研究, 因此, 本研究采用不同种类和酸碱性的硅肥, 通过添加不同剂量的硅肥, 对土壤pH、有效态硅、有效态磷、生物有效态Cd和As以及其他土壤理化性质进行考察, 进而明确不同种类和酸碱性硅肥在减轻土壤Cd和As复合污染的主要机制, 以期为粮食安全生产提供指导, 并为促进人类社会可持续发展做出贡献.
1 材料与方法
1.1 试验材料
供试土壤:供试Cd和As复合污染稻田土壤采自湖南省浏阳市永和镇(N28.290°, E113.556°) 耕作层(0~20 cm), 由于该地上游七宝山矿山不合理的采矿和冶炼活动, 导致了下游农田土壤严重的Cd-As复合污染.将采回的土样在阴凉透风处自然晾晒后, 剔除混在土壤中的动植物残体, 并将所有土壤均匀混合, 研磨过筛(≤2 mm).对供试土壤的基本理化性质进行检测, 结果如表 1所示.
表 1
(Table 1)
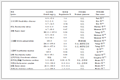
表 1 供试土壤基本理化性状1)
Table 1 Basic physicochemical properties of the tested soil
| 项目 |
pH |
ω |
| 总Cd |
有效态Cd
(0.01 mol·L-1 CaCl2) |
总As |
有效态As
(0.5 mol·L-1 KH2PO4) |
有效磷 |
有效态硅 |
总铁 |
| 参数 |
5.16 |
1.33 |
0.28 |
50.89 |
6.33 |
29.04 |
119.52 |
40.55 |
| 1)pH无量纲, 总铁单位为g·kg-1, 其余单位为mg·kg-1 |
|
表 1 供试土壤基本理化性状1)
Table 1 Basic physicochemical properties of the tested soil
|
供试硅肥:在本试验中应用了3种不同性质碱性硅肥和一种弱酸偏中性水溶硅肥(neutral soluble silicon fertilizer, NSSF, pH 5~6, Si含量为13.8%), 其中3种碱性硅肥分别为:硅酸钠(Na2SiO3)、硅酸钙(CaSiO3)和碱性水溶硅肥(alkaline soluble silicon fertilizer, ASSF, pH为10~11, Si:24.6%).其中ASSF和NSSF采购自河北衡水市格美微量元素有限公司.
1.2 试验设计
本试验采取室内土盆试验, 等量称取研磨过筛后的土样每盆450 g.各处理以硅(Si)计(下同), ω(Si)梯度分别为25、50、100、200、400和800 mg·kg-1, 换算成各硅肥含量后并分别与土壤均匀混合放入土盆中; 并设置1个未施硅肥处理[CK, ω(Si) 为0 mg·kg-1], 共设置4 (4种硅肥)×6 (6个Si梯度)+1 [CK, ω(Si)为0 mg·kg-1]=25个处理, 每个处理3个平行样, 共25×3=75个土盆.根据田间施肥经验和文献[4, 24]可知, 施肥后约3周土壤理化性质基本趋于稳定, 因此本试验设置淹水时间为21 d, 每盆淹水约350 mL, 整个淹水时期维持淹水深度为2~3 cm.
相比其他土壤有效态重金属的化学提取方法, 薄膜扩散梯度(diffusive gradients in thin films, DGT) 提取的土壤有效态Cd和As被证明是与生物有效态Cd和As相关性最显著的一种短期原位提取方法[25, 26].ZrO-Chelex DGT可同时提取土壤中多种阴阳离子, 因此本试验采用新型双模式(new dual-mode) ZrO-Chelex DGT提取土壤中有效态Cd和As (DGT-Cd和DGT-As) 来评价不同种类硅肥对土壤生物有效态Cd和As的防控效果.
1.3 样品采集与检测方法
土水共育试验第21 d时利用pH计-氧化还原电位(Eh) 仪[f2standrad, 梅特勒-托利多仪器(上海)有限公司]和电导率仪(CD-12, 南京传滴仪器设备有限公司) 原位测定每盆淹水土壤的pH、Eh和电导率(electrical conductivity, EC).之后小心均匀收集每个土盆中的土壤, 并将其分别填充在new dual-mode ZrO-Chelex DGT装置中, 注意在填充过程中可在桌面小心晃动该装置, 以便土壤可均匀填充于装置内腔中直至填满, 同时使得土壤与DGT表面滤膜充分接触.土壤填充完成后将DGT装置转移到自封袋中, 每个处理一组, 同时每个自封袋中需装有少量的超纯水并保持袋口呈半封闭状态以保持DGT装置在整个提取过程中处于湿润状态.然后将所有DGT装置置于恒温状态下[(25±1)℃]静置24 h. 24 h提取完成后, 分别小心将每个DGT装置中土壤去除, 并取出用超纯水冲洗干净后的ZrO-Chelex DGT固定膜.将冲洗干净后的固定膜, 首先用1.8 mL的1 mol·L-1HNO3提取DGT-Cd, 静置24 h后, 取出固定膜并用超纯水清洗2 h, 之后转入1.8 mL的1 mol·L-1 NaOH中静置24 h提取DGT-As.土壤DGT有效态Cd和As计算浓度过程参考文献[24].
将所有淹水后的土壤回收并分别移至阴凉通风处自然晾干, 然后研磨过10目筛, 并按照文献[27], 使用柠檬酸提取-钼蓝比色法和盐酸-氟化铵法分别检测土壤有效态硅和有效态磷.
1.4 数据处理与分析
数据采用Microsoft Excel 2010进行处理, 并利用Origin 2021进行绘图与线性-非线性拟合, 各因素之间相关性分析(Pesrsen相关系数法) 采用Origin 2021中Correlation Plot插件进行数据分析与制图.
2 结果与分析
2.1 不同性质硅肥及其用量对土壤pH、Eh和EC的影响
由图 1(a)可知, 随着硅肥添加量的增加, Na2SiO3、CaSiO3和ASSF这3种碱性硅肥处理的土壤pH也随之持续上升, 当硅肥添加量(以Si计) 达到800 mg·kg-1时, 土壤pH增长了0.36~0.80个单位, 其中Na2SiO3的添加在提升土壤pH方面效果最佳, 其次为ASSF和CaSiO3; 而与之相反的是, 随着Si添加量的增加, NSSF处理土壤pH随之持续下降, 下降了0.34~1.52个单位[图 1(a)].随着CaSiO3和ASSF添加量增加, 土壤Eh先上升后波动下降, 即在Si添加量为25~400 mg·kg-1土壤Eh均高于未施用硅肥(CK), 当Si添加量达到800 mg·kg-1时, 土壤Eh才低于CK, 下降了12~21 mV; 而Na2SiO3硅肥处理随着添加量的增加土壤Eh值则持续下降, 相较于CK下降了14~89 mV; 与3种碱性硅肥不同的是, 随着NSSF添加量的增加, 土壤Eh则大幅度持续上升, 增长了164~301 mV [图 1(b)].随着Si添加量从25 mg·kg-1增长至800 mg·kg-1, 4种硅肥处理土壤EC值均随之上升, 上升0.130~1.854 mS·cm-1, 其中Na2SiO3施用后土壤EC值上升最为显著[图 1(c)].
土壤pH对Cd和As生物有效性有较大影响, 因此为明确不同种类硅肥和不同添加量对土壤pH影响情况, 对不同硅肥添加量与土壤pH之间的关系作线性拟合, 线性拟合结果表明, 4种硅肥的不同添加量与土壤pH均有显著的线性关系.而3种碱性硅肥与土壤pH呈显著正相关关系(P < 0.01), 其中, Na2SiO3与土壤pH线性相关性最强, 相关系数r达到了0.990 (P < 0.001), 且Na2SiO3提升土壤pH的能力也最强, 即每增加1 mg的Si添加可提高0.001个单位的土壤pH.而NSSF与土壤pH呈显著负相关关系(P < 0.01), NSSF每增加1 mg的Si添加可使土壤pH下降0.001 7个单位(图 2).
2.2 不同性质硅肥及其用量对土壤有效硅和磷的影响
随着Si添加量由25 mg·kg-1增长至800 mg·kg-1, 4种硅肥处理的土壤中有效硅含量均持续增加, 其中当Si添加量达到800 mg·kg-1时, 4种硅肥处理的土壤中ω(有效硅)达到577.20~1 048.44 mg·kg-1[图 3(a)], 相较于CK [ω(Si)为0 mg·kg-1], 增长率达到242.92%~522.88%, 表明硅肥的施用可显著增加土壤有效硅的含量, 且不同性质硅肥添加量与土壤有效硅呈显著正相关关系(P < 0.001), 其中单位质量(mg) Si添加量可提升土壤有效硅含量能力为:NSSF>Na2SiO3>ASSF>CaSiO3 (图 4).
而随着3种碱性硅肥添加量的增加, 土壤中有效磷的含量呈波动下降的趋势, 当Si添加量达到800 mg·kg-1时, 相较于CK, 各处理中土壤ω(有效磷)下降了4.56~8.38 mg·kg-1; 与之相反的是, 随着NSSF添加量的增加, 土壤ω(有效磷)呈波动上升的趋势, 增加了4.02~12.26 mg·kg-1[图 3(b)].线性拟合结果表明, 土壤中有效磷与土壤中有效硅含量线性关系较差, 没有显著相关性[P>0.05, 图 5(a)]; 但是土壤pH与土壤中有效磷含量存在显著的负相关关系[P < 0.001, 图 5(b)], 表明硅肥的添加主要通过影响土壤pH来影响到土壤中有效磷含量, 而不是通过土壤中有效硅含量影响.
2.3 不同性质硅肥及其用量对土壤DGT-Cd和DGT-As影响
DGT可以在短期内原位提取土壤中活性态的重金属, 且操作较为简便省时, DGT提取态重金属已被众多研究者证明是与生物有效态重金属相关性最显著的金属形态, 因此已被广泛用于模拟土壤中生物有效态Cd和生物有效态As的土壤试验中.本试验引入DGT来检测不同处理下土壤中Cd和As的生物有效性.由图 6(a)可知, 随着Si添加量的增加, 3种碱性硅肥处理DGT-Cd浓度先快速下降, 然后基本保持稳定或波动上升的趋势; 其中Na2SiO3和CaSiO3在Si添加量达到100 mg·kg-1时, ASSF在Si添加量达到200 mg·kg-1时, ρ(DGT-Cd)基本达到最低值, 为0.30~0.33 μg·L-1, 相较于CK处理, 下降率达到50.89%~56.15%; 之后随着Si添加量的增加, 土壤中DGT-Cd浓度下降趋势不大.而随着Si添加量的增加, NSSF处理土壤中DGT-Cd浓度持续上升, 当Si添加量达到400 mg·kg-1时, DGT-Cd浓度基本达到平衡状态, 之后随着Si添加量的增加, DGT-Cd浓度也基本保持稳定.3种碱性硅肥和NSSF对土壤DGT-Cd浓度完全相反的影响可能主要是土壤pH引起的, 拟合图发现土壤pH与土壤DGT-Cd浓度可能存在一个转换区间, 当土壤pH为6.5~7.0时, 土壤DGT-Cd浓度基本达到最低值, 而当土壤pH < 6时, 淹水土壤中DGT-Cd浓度则显著上升[图 7(a)].
随着Si添加量的增加, 3种碱性硅肥处理中土壤DGT-As浓度呈波动上升的趋势, 当Si添加量达到800 mg·kg-1时, ρ(DGT-As) 达到了162.22~205.68 μg·L-1, 相较于CK, 增长率达到了39.25%~76.55%.而NSSF处理土壤中DGT-As浓度随着Si添加量的增加而减少, 其中, 当Si添加量达到400 mg·kg-1时, 土壤中ρ(DGT-As) 达到最低值16.46 μg·L-1, 相较CK下降了约100.05 μg·L-1, 之后随着Si添加量增加到800 mg·kg-1, 土壤中DGT-As浓度基本保持不变[图 6(b)].随着Si添加量的增加, 淹水土壤中DGT-As和DGT-Cd浓度变化趋势完全相反, 造成这一变化的主要影响因素是土壤pH.线性拟合发现, 淹水土壤中DGT-As浓度与土壤pH呈显著正相关性[P < 0.001, 图 7(b)], 且当土壤pH在5~5.5之间时, DGT-As浓度基本达到最低值.
2.4 土壤中DGT-Cd和DGT-As浓度与土壤基本理化性质相关性
淹水稻田土壤中活性态DGT-Cd和DGT-As浓度受土壤理化性质影响较为巨大, 图 8相关性分析表明, 土壤DGT-Cd和土壤pH与DGT-As呈显著负相关性(P < 0.05), 相关系数分别为-0.80和-0.73, 因此, 在本试验中随着3种碱性硅肥施用的增加使得土壤pH持续上升, Cd生物有效性大大降低; 而NSSF的施用导致土壤pH持续下降继而使得土壤DGT-Cd浓度大幅度上升; 另外由于Cd和As在土壤中截然不同的化学性质且呈显著负相关性, 使得利用某种硅肥同时减控土壤层面中有效态Cd和有效态As较为困难.另一方面, 土壤DGT-Cd与土壤Eh、土壤有效硅和土壤有效磷呈显著正相关性(P < 0.05), 相关系数分别为0.73、0.59和0.71.值得注意的是, 土壤pH与土壤DGT-Cd之间的相关系数r=0.80远大于土壤有效态硅与DGT-Cd之间的相关系数|r|=0.59, 这一结果说明就土壤层面来说, 不同酸碱性硅肥施用对土壤pH的改变作用对土壤中Cd生物有效性的影响远大于提高土壤中有效硅含量对土壤中Cd生物有效性的影响; 土壤EC与土壤DGT-Cd基本无相关性.
由图 8可知, 土壤中DGT-As与土壤pH和土壤EC呈显著正相关性(P < 0.05), 其中土壤pH与土壤DGT-As的相关系数高达0.92; 土壤中DGT-As与土壤Eh和土壤有效磷呈显著负相关性(P < 0.05), 相关系数分别为-0.87和-0.74, NSSF的加入使得土壤pH降低Eh升高, 所以随着NSSF添加量的增加, 土壤DGT-As浓度快速下降, 3种碱性硅肥的加入则起到相反的作用.
土壤中有效磷和土壤pH具有显著负相关性(P < 0.05, r=-0.75), 与土壤Eh呈显著正相关性(P < 0.05, r=0.60, 图 8), 这一结果表明土壤中pH的降低有利于提高土壤中有效磷的有效性, 而高pH条件下, 土壤中磷的移动性和生物有效性则大幅度下降.因此, 在本试验中, NSSF的施用使得土壤pH降低, 继而使得土壤中有效态磷含量升高, 3种碱性硅肥的施用使得土壤有效态磷降低.另外, 土壤有效态磷含量与土壤有效态硅含量之间无显著相关性, 表明, 硅肥的施用主要通过改变土壤pH值来影响土壤中有效磷的含量, 而土壤中有效硅的含量基本对土壤中有效磷含量没有影响.
3 讨论
3.1 不同性质硅肥对土壤主要理化性质的影响
土壤Cd和As的生物有效性主要受到土壤的理化性质影响.本试验为了避免仅使用碱性硅肥影响试验结果, 引入了非碱性硅肥——偏中性可溶硅肥(NSSF, pH 5~6).相较于CK, 随着3种碱性硅肥添加量的增加, 土壤pH值持续增加[图 1(a)], 其中, Na2SiO3提升土壤pH值效果最佳, 每mg的Si添加量可提升土壤pH 0.001个单位[图 2(a)], 这与Lu等[28]研究结果一致, 主要原因可能是在这3种碱性硅肥中Na2SiO3水溶液pH值最高, 达到11~13, 含有更多碱性氧化物, 水解后使土壤溶液中OH-比例较高[29, 30], 从而使得土壤pH值上升较快.而随着NSSF的添加量增加, 土壤pH则在持续下降, 这可能是由于NSSF的pH为5~6, 呈弱酸性所导致的, 即随着土壤中NSSF含量的增加, 其电离出的H+离子越多, 导致土壤pH持续下降.土壤Eh值代表着土壤的氧化还原状态, 一般范围在-300~900 mV, 而淹水土壤Eh一般小于350 mV, 已证实土壤pH与Eh一般呈显著负相关关系[31, 32].在本试验中, 随着CaSiO3和ASSF添加量的增加, 土壤Eh值首先上升然后保持波动下降的趋势, 但除了Si添加量为800 mg·kg-1时, 其他Si添加量土壤Eh值均高于未施用硅肥时的土壤Eh值, 这可能是由于在一定情况下施Si增加了土壤溶液中的硅酸胶体, 这些硅酸胶体可以和土壤中的还原态物质如Fe2+和Mn4+等形成一些难溶性沉淀的物质, 从而减少土壤中还原性物质的含量使得土壤Eh值存在一定程度的上升[33].但和其他两种碱性硅肥不同的是, Na2SiO3处理使得土壤Eh值持续下降, 这可能是由于土壤Eh和pH呈负相关关系, Na2SiO3作为强碱盐比其他两种碱性硅肥碱性更强, 提升土壤pH能力更强, 这与以往研究一致[34, 35].而NSSF处理随着添加量的增加, Eh值持续上升[图 1(b)].值得注意的是, 在Si添加量达到400 mg·kg-1后再增加用量, 无论是3种碱性硅肥还是NSSF, 土壤pH和Eh变化都趋于平缓.另外不同性质硅肥施用的增加, 均导致土壤EC值显著增加, 这提醒在实际应用过程中施用硅肥时要注重添加量, 避免土壤盐碱化.
施用硅肥可提高土壤中有效硅含量, 在本试验中, 4种硅肥处理中土壤有效硅含量均随着Si添加量的增加而增加, 且均呈极显著线性正相关关系[P < 0.001, 图 3 (a)和图 4], 提高土壤中有效硅含量能力为:NSSF(1.073 9)>Na2SiO3(0.733 9)>ASSF(0.614 3)>CaSiO3(0.508 2).这可能与硅肥的种类有关, 由于CaSiO3是缓效性硅肥且不溶于水, 所以有效硅释放较其他种类水溶性硅肥少.值得注意的是, 在Si添加量为0~400 mg·kg-1时, NSSF和Na2SiO3对土壤有效硅提升水平相当, 但是到800 mg·kg-1时, NSSF处理土壤有效硅含量远高于Na2SiO3处理, 这可能是由于土壤pH对土壤中硅释放量影响巨大.刘俐等[36]研究表明, 在pH < 5.6时土壤硅会大量释放出来, 而NSSF的施用使得土壤pH较CK大幅度下降, 因而可能使得土壤中有效硅提取量大大增加.
磷是作物生长发育所必需的营养元素之一, 同时, 土壤中活性态磷的含量对土壤Cd和As生物有效性影响较大[37, 38], 硅肥的施用导致土壤理化性质的改变是否会对土壤中磷的释放产生影响值得关注.土壤中磷素释放受到多种因素影响, 如土壤pH和氧化还原电位等[39~41].本试验结果显示土壤中有效硅的含量与土壤有效磷含量并无显著相关性, 影响土壤中磷释放的主要因素是土壤pH, 二者呈显著负相关性(P < 0.001, 图 5), 这主要是由于土壤pH值升高时, 磷酸就会和钙、铝或铁形成沉淀, 进而造成土壤中有效磷含量的降低[42~44]; 相反, 随着土壤pH值降低磷有效性增强, 在本试验中土壤pH每降低1个单位土壤磷释放量约增加6.895 7 mg·kg-1, 这与马凯强等[40]的研究结果低pH加剧Cd污染土壤淋出液中总磷和正磷酸盐含量一致.说明不同酸碱性质硅肥的施用可以通过改变土壤pH来调节土壤磷的释放, 而土壤中有效硅含量对土壤中磷基本无影响.
3.2 不同性质硅肥影响土壤DGT-Cd和DGT-As浓度的主要因素
薄膜扩散梯度(DGT) 提取态Cd和As已被众多研究证明是短期原位模拟生物有效态Cd和As最有效的方法之一[45], 因而在本试验中采用DGT来提取土壤生物有效态Cd和As.Cd和As在土壤中呈现完全相反的化学性质和价态, 施用不同酸碱性质硅肥对土壤DGT-Cd和DGT-As浓度有着截然不同的影响.本试验结果显示, 3种碱性硅肥在降低土壤DGT-Cd方面有良好的应用性, 但是却使得土壤DGT-As浓度持续波动上升, 综合来看, 3种碱性硅肥中, 在CaSiO3添加量(以Si计)为100 mg·kg-1时, 可以在显著降土壤DGT-Cd的同时(降低约50.89%) 又不引起DGT-As大幅度上升[图 6(a)].值得注意的是, 当Na2SiO3添加量(以Si计)由400 mg·kg-1增加到800 mg·kg-1时, 土壤DGT-Cd浓度却有所增加, 这可能是由于Na2SiO3添加量的大幅度增加, 同时使得土壤中Na+显著增加, EC值大幅度增加[图 1(c)], 而研究表明土壤中Na+增加会提高土壤中Cd的有效态[46], 这提醒在实际应用中要注重肥料添加量和对土壤EC值的监测, 防止土壤中过多盐基离子影响植物生长及加重重金属在植株体内的积累量.NSSF的施用则表现出完全相反的现象, 即NSSF在降低DGT-As方面展现出了良好的特性, 但是却显著提高了DGT-Cd; 在NSSF添加量(以Si计)为400 mg·kg-1时, DGT-As浓度基本达到稳定状态, 显著降低了DGT-As浓度约100.04 μg·L-1, 降As率达85.87% [图 6(b)].有研究表明施Si可以降低土壤中Cd生物活性[47], 但是却会增加土壤中As的生物有效性[4], 与之不同的是, 本文研究结果表明可以利用不同酸碱性质的硅肥来分别降低土壤中生物有效态Cd和As; 碱性硅肥在降低土壤生物有效态Cd方面效果显著, 而NSSF则可应用于降低土壤生物有效态As, 不同酸碱性质的硅肥并不适用于同时修复Cd和As复合污染土壤.
近年来, 利用硅肥来调控土壤Cd和As复合污染对水稻的毒害已受到广大科研工作者的青睐, 研究表明影响土壤生物有效态Cd和As的因素主要有土壤pH、Eh、有效磷、有效硅和盐基饱和度等因素[4, 46, 48].但是, 由于以往施用硅肥多为碱性硅肥, 一般添加进入土壤后都会使得pH升高, 因此很难分辨究竟是土壤pH还是土壤有效硅或其他因素影响土壤中Cd和As生物活性, 因此本试验中采取了不同酸碱性质的硅肥, 以更好分辨影响土壤Cd和As生物活性的最佳因素.由图 8可知, 硅肥施用对土壤DGT-Cd浓度影响最为显著的是土壤pH, 相关系数r达到-0.80 (P < 0.001), 主要是由于土壤pH提高显著增加了土壤中OH-浓度, 与土壤中Cd2+形成的稳定络合物增加, 极大程度降低其移动性和生物活性[34], 图 7(a)拟合结果显示, 施用硅肥后当土壤pH为6.5~7.0时, 土壤DGT-Cd浓度基本达到最低值, 而当土壤pH < 6时, 淹水土壤中DGT-Cd浓度则显著上升, 这与陈楠等[49]的研究结果一致; 其次是土壤Eh (r=0.73), 这可能主要是由于pH与Eh呈显著性负相关关系(P < 0.05), 继而导致Eh与土壤DGT-Cd呈负相关关系; 在本试验中土壤有效态硅与DGT-Cd呈显著正相关性(r=0.59, P < 0.05), 这与以往研究土壤有效态Si可以显著降低土壤中有效态Cd完全相反[13, 47], 这可能是由于, 在本试验中引入了pH为5~6的弱酸偏中性水溶硅肥NSSF, NSSF的施用虽然使得土壤有效硅大幅度增加, 但同时也降低了土壤pH从而使得土壤DGT-Cd浓度大幅度增长, 因此也使得最终相关性分析显示土壤有效硅与土壤DGT-Cd呈显著正相关关系.这也进一步证明与其他研究结果不同的是, 就土壤层面来说, 硅肥的施用主要是通过改变土壤pH来影响土壤中Cd的生物有效性, 而受土壤中活性硅影响不大.
图 8相关性分析结果显示, 土壤DGT-Cd和DGT-As呈显著负相关关系(r=-0.73, P < 0.05), 这主要是由于在土壤中Cd和As呈现完全相反的化学特性、价态和形态[50], 因此, 这也造成协同修复土壤Cd和As复合污染难度较大.对土壤DGT-As浓度影响排序为土壤pH (r=0.92)>Eh(r=0.87)>土壤有效磷(r=0.74)>EC (r=0.51, P < 0.05).As在淹水稻田土壤中主要以+3价、+5价以及各种含As氧阴离子(如HASO42-、H2AsO4-和HAsO32-等)存在, 其中还原态As3+毒性约为氧化态As5+的60倍[51]; 而土壤中As形态主要受到pH和Eh的影响, 研究结果表明, 当土壤中pH降低时土壤胶体所带正电荷随之增加, 因而使得含As阴离子更容易被土壤胶体吸附从而降低As的移动性与活性[52].本试验中拟合结果显示, 当硅肥调控土壤pH至5~5.5之间时, DGT-As浓度基本达到最低值.土壤中Eh受到pH影响, 二者呈显著负相关关系; 当土壤中pH上升而Eh降低并长期呈还原性时土壤溶液中大量As5+被还原为As3+, 土壤胶体对As3+的吸附效率远大于As3+, 土壤中As生物活性与毒性大大增加[3, 53], 因而使得土壤pH与土壤DGT-As呈显著正相关关系, 与Eh呈显著负相关关系(P < 0.05, 图 8).而DGT-As与土壤有效硅无显著相关性(r=0.007, P>0.05), 这进一步说明, 就土壤层面来说, 土壤中有效态硅含量对土壤中As的生物有效性并无影响, 而是主要通过影响植物对As的吸收来减控As对作物的毒害, 这与之前研究一致[54].值得注意的是, 在本研究中土壤有效磷与DGT-Cd呈显著正相关关系, 与DGT-As呈显著负相关关系, 这与其他研究结果不同[21], 这可能由于在本试验中土壤有效磷的变化并不是由于外源添加磷所引起的, 而是由于硅肥添加引起土壤pH的变化造成的土壤磷释放导致, 因而可能导致土壤磷本身对土壤中Cd和As的影响较为微弱, 而主要反映出来为pH对土壤Cd和As生物有效性的影响.综上所述, 不同酸碱性质硅肥施用主要是靠影响土壤pH对土壤DGT-Cd和DGT-As浓度产生影响, 土壤有效硅和土壤有效磷对土壤中Cd和As的生物有效性的影响可忽略不计.
4 结论
(1) 不同酸碱性质硅肥对土壤pH和Eh影响差异较大, 3种碱性硅肥与土壤pH呈显著正相关关系(P < 0.01), 其中Na2SiO3提升土壤pH的能力最强; 而NSSF与土壤pH呈显著负相关关系(P < 0.01), 这可能主要是由于NSSF为弱酸偏中性可溶硅肥(pH为5~6) 所导致; 土壤Eh和pH呈显著负相关关系(P < 0.05).在Si添加量达到400 mg·kg-1后, 3种碱性硅肥和NSSF土壤pH和Eh变化都趋于平缓, 即Si添加量为400 mg·kg-1时可使土壤达到平衡状态.
(2) 施用不同性质硅肥均可大幅度提高土壤有效硅含量, 提升土壤有效硅含量能力为:NSSF>Na2SiO3>ASSF>CaSiO3, 硅肥施用引起的土壤pH变化会影响土壤有效磷释放, pH每降低1个单位, 土壤磷释放量约增加6.895 7 mg·kg-1.
(3) 3种碱性硅肥可以显著降低土壤DGT-Cd浓度, 其中, 在CaSiO3添加量为100 mg·kg-1 (以Si计) 时, 可以在显著降低土壤DGT-Cd浓度的同时(降低约50.89%) 又不引起DGT-As浓度大幅度上升; 而NSSF在降低土壤DGT-As浓度方面展现出了良好的特性, 添加量为400 mg·kg-1时, 土壤DGT-As浓度基本达到稳定状态, 降As率达85.87%.
(4) 土壤有效硅和土壤有效磷对土壤Cd和As生物有效性影响可忽略不计, 不同性质硅肥影响土壤DGT-Cd和DGT-As主要是由于硅肥施用影响土壤pH, 施用硅肥后当土壤pH为6.5~7.0时, 土壤DGT-Cd浓度基本达到最低值; 当pH为5~5.5时, DGT-As浓度基本达到最低值.
 2023, Vol. 44
2023, Vol. 44











