2. 上海海洋大学水产与生命学院环境DNA技术与水生态健康评估工程中心, 上海 201306
2. Engineering Research Center of Environmental DNA and Ecological Water Health Assessment, College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306, China
附着藻类/附着藻膜(periphytic algae)是指生长在淹没于水体中的各种基质表面的层状藻类群落[1~5].附着藻类群落结构复杂, 对生态环境变化具有独特的敏感性, 可以快速地进行群落重建, 并对水环境的变化做出响应[6, 7].因此, 附着藻类常被认为是水质监测、生态系统健康指示和生态毒性评价的优良指示生物.此外, 附着藻类还可以通过影响水体初级生产力、食物链和养分循环, 在自然水生生态系统的物质转化和能量流动中发挥重要作用[8, 9]; 这也使得附着藻类在水质净化、污染物降解和生态恢复等方面发挥巨大的应用潜能[3, 7].谷雪维[10]利用成熟期附着藻膜对抗生素的去除研究发现, 在20 d内其对恩诺沙星的去除率高达90%, 对磺胺的去除率也可达50%.孙沉沉等[11]研究发现, 当污水中加入吲哚乙酸时, 7 d内附着藻膜对氮磷去除率超过80%.
附着藻类的生物量和群落组成和其生态功能密切相关, 而影响附着藻类群落组成因素通常包括:附着基质的类型、淹没时间、水体的理化性质、光照和营养物质等[2, 12~14].其中, 附着基质是附着藻类生长的首要条件, 它影响着后续的生物定殖、群落演替、生产力动态变化和对水体污染物的净化能力等.Tsavatopoulou等[15]以6种不同材料(软木、海绵毛巾、牛仔布、有机塑料板、不锈钢和硅橡胶)作为基质研究了对栅藻(Scenedesmus spp.)生物膜形成的影响, 结果表明有机塑料板可获得最大的附着藻类生物量.Oberbeckmann等[16]和Ogonowski等[17]的研究表明, 不同塑料聚合物类型(PET、HDEP和LDEP)上的附着藻类群落组成之间存在显著差异.除了附着基质的材质之外, 其本身的粗糙度、表面积等性质也是影响附着藻膜形成和发育的重要因素[18].伍良雨等[18]研究发现, 具有粗糙表面、可以提供营养物质的载体可能会更有利于附着藻膜的形成和生长.Guo等[19]研究发现, 附着基质的表面积越大, 附着生物更易附着.塑料基质除了材质和表面特征不同外, 颜色也非常丰富.近期调查发现, 水体中的塑料制品或残片的颜色就多达十余种[20, 21].尽管Xu等[22]研究发现, 不同颜色的塑料膜遮光, 会对水体浮游植物群落产生显著影响, 然而, 目前有关于塑料颜色对附着藻类生物膜生长发育和群落结构影响的研究还鲜见报道.
本研究选取了5种颜色的PC塑料(透明、绿色、蓝色、茶色和白色)作为附着基质, 通过测定其上生长的附着藻类的叶绿素a、干重、光合作用活力和群落结构组成, 来探究不同颜色的PC塑料作为附着基质对附着藻类的生长和群落结构的影响, 以期为利用周丛生物技术开展水污染治理时, 挑选合适颜色的附着基质提供参考资料.
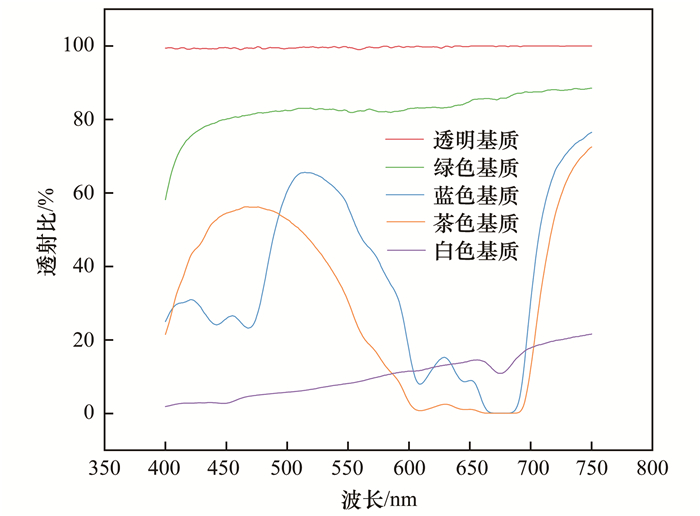
1 材料与方法 1.1 实验设计以55 L透明塑料筐(60 cm×30 cm×40 cm)作为实验水槽.2021年8月, 在上海海洋大学校园内明湖(30°53′14″N, 121°53′23″E)采集实验用水.实验用水使用前用浮游动物网(孔径112 μm)过滤以去除水体中的浮游动物.实验用水总体积为48 L, 实验期间, 每天定时补水维持实验用水总体积不变.箱底分别铺满透明、绿色、蓝色、茶色和白色PC塑料板(10 cm×3 cm×0.3 cm)作为附着藻类生长的附着基质, 每组设3个平行, 不同颜色对光的透射比见图 1.静置培养7 d待附着藻类定植.第7 d作开始实验的第一次采样, 此后, 每隔2 d(即在第7、10、13、16、19、22、25、31、34和40 d取样)进行采样.
|
图 1 不同颜色PC塑料的透光性 Fig. 1 Light transmittance of PC plastics with different colors |
每次取2片PC板(总面积为60 cm2), 使用硬毛牙刷将其表面上的附着生物全部刷下, 并用去离子水冲洗附着基和牙刷, 将获得的藻水混合液定容至100 mL.用超声波振荡, 使其分散, 获得均匀藻液, 用于后续分析.丙酮法对附着藻类的叶绿素a含量进行测定[23].干重法测定附着藻类干重含量[10].使用浮游植物荧光分析仪(Phyto-PAM, Walz, Germany)测定光合系统Ⅱ(PS Ⅱ)的最大光合效率(Fv/Fm)和实际光合效率(Yield)[24, 25].
选取第7、25和40 d的附着藻类样品分析鉴定物种组成.样品分析鉴定前, 先用10%的甲醛和4%的鲁格试剂进行固定[26].然后, 取0.1 mL固定好的样品于浮游植物计数框内, 用普通光学显微镜(Olympus CX21)对藻类进行分类鉴定和计数.藻类鉴定方法依据文献[27~29].
1.3 数据分析 1.3.1 优势种依据McNaughton优势度指数(Y), 确定优势种, 计算公式如下[30, 31]:
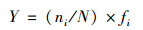
|
式中, fi为物种i出现的频率, N为同一样点中的个体总数, ni为物种i的个体数; Y>0.02则为优势种.
1.3.2 数据统计分析利用Microsoft Excel 2013 (Microsoft, America)对实验数据进行预处理, 实验数据由平均值±标准偏差(SD)表示, 采用单因素方差分析(one-way ANOVA)比较不同实验组间各指标差异的显著性, 采用方差齐性检验检测正态分布, P < 0.05认为具有显著差异性, P < 0.01认为具有极显著的差异性.根据附着藻类群落结构之间的Bray-Curtis距离矩阵, 进行主坐标分析(principal coordinates analysis, PCoA)不同组别之间的群落β多样性.所有统计分析均在SPSS 26.0和R中完成, 运用Origin 2019进行图表的绘制.
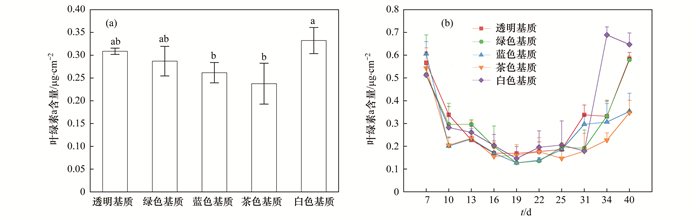
2 结果和分析 2.1 附着藻类生长量的变化茶色组的叶绿素a含量显著低于透明组(P < 0.05), 极显著低于白色组(P < 0.01)[图 2(a)].白色组的叶绿素a含量显著高于蓝色组[P < 0.05, 图 2(a)].所有实验组附着藻类的叶绿素a含量均呈现先降低后升高的趋势[图 2(b)].白色组的叶绿素a含量在第34 d出现最大值(0.69±0.04)μg ·cm-2, 且显著高于其他实验组[P < 0.05, 图 2(b)].
|
(a)整个实验周期内叶绿素a含量平均值, (b)叶绿素a含量随时间的变化情况; 不同小写字母表示不同处理组之间存在显著差异(P < 0.05), 下同 图 2 不同颜色PC塑料板上附着藻类叶绿素a含量 Fig. 2 Chlorophyll a content of periphytic algae on PC substrates with different colors |
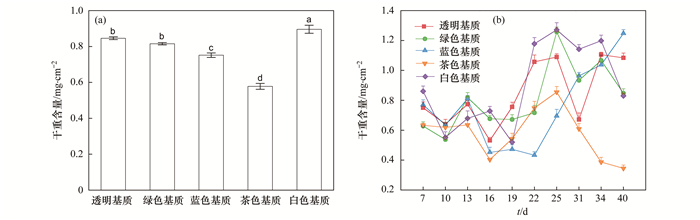
茶色组的干重含量极显著低于其他4个实验组[P < 0.01, 图 3(a)].蓝色组的干重含量极显著低于透明组、绿色组和白色组[P < 0.01, 图 3(a)].绿色组和透明组的干重含量极显著低于白色组(P < 0.01), 绿色组和透明组的干重含量之间没有显著差异[P>0.05, 图 3(a)].茶色组的干重含量从第25 d[(0.86±0.04)mg ·cm-2]开始持续降低, 蓝色组的干重含量从第22 d[(0.43±0.02)mg ·cm-2]开始持续上升[图 3(b)].
|
(a)整个实验周期内干重含量平均值, (b)干重含量随时间的变化情况 图 3 不同颜色PC塑料板上附着藻类干重含量 Fig. 3 Dry weight content of periphytic algae on PC substrates with different colors |
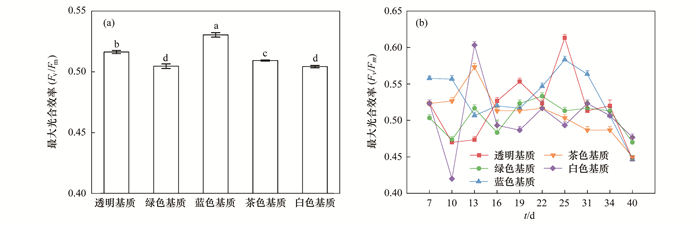
蓝色组的Fv/Fm显著高于其他4个实验组[P < 0.05, 图 4(a)].从第25 d开始, 所有实验组的Fv/Fm呈持续下降趋势, 并在第40 d降到最低[图 4(b)].透明组第25 d的Fv/Fm达到整个实验周期的最大值(0.61±0.00)[图 4(b)].茶色组的Fv/Fm在第13 d达到最大值(0.57±0.00), 之后持续下降[图 4(b)].
|
(a)整个实验周期内最大光合效率(Fv/Fm)平均值, (b)最大光合效率(Fv/Fm)随时间的变化情况 图 4 不同颜色PC塑料板上附着藻类最大光合效率(Fv/Fm) Fig. 4 Maximum photosynthetic efficiency (Fv/Fm) of periphytic algae on PC substrates with different colors |
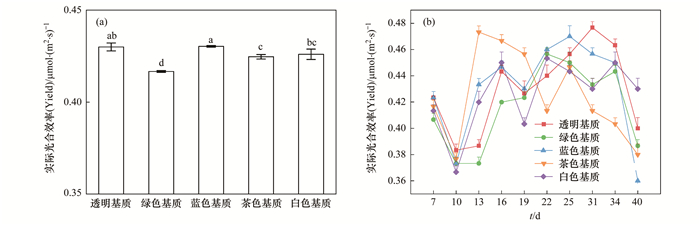
随时间的变化情况绿色组的Yield显著低于其他4个颜色组[P < 0.05, 图 5(a)].所有实验组的Yield从第10 d之后均呈现先上升后下降的趋势[图 5(a)].透明组、绿色组、茶色组和白色组均在第10 d出现最小值, 而蓝色组在第40 d出现最小值(0.45±0.00)[图 5(b)].各实验组的Yield最大值出现时间不同, 大小依次为:透明组、茶色组、蓝色组、绿色组和白色组[图 5(b)].
|
(a)整个实验周期内实际光合效率平均值, (b)实际光合效率随时间的变化情况 图 5 不同颜色PC塑料板上附着藻类实际光合效率(Yield) Fig. 5 Actual photosynthetic efficiency (Yield) of periphytic algae on PC substrates with different colors |
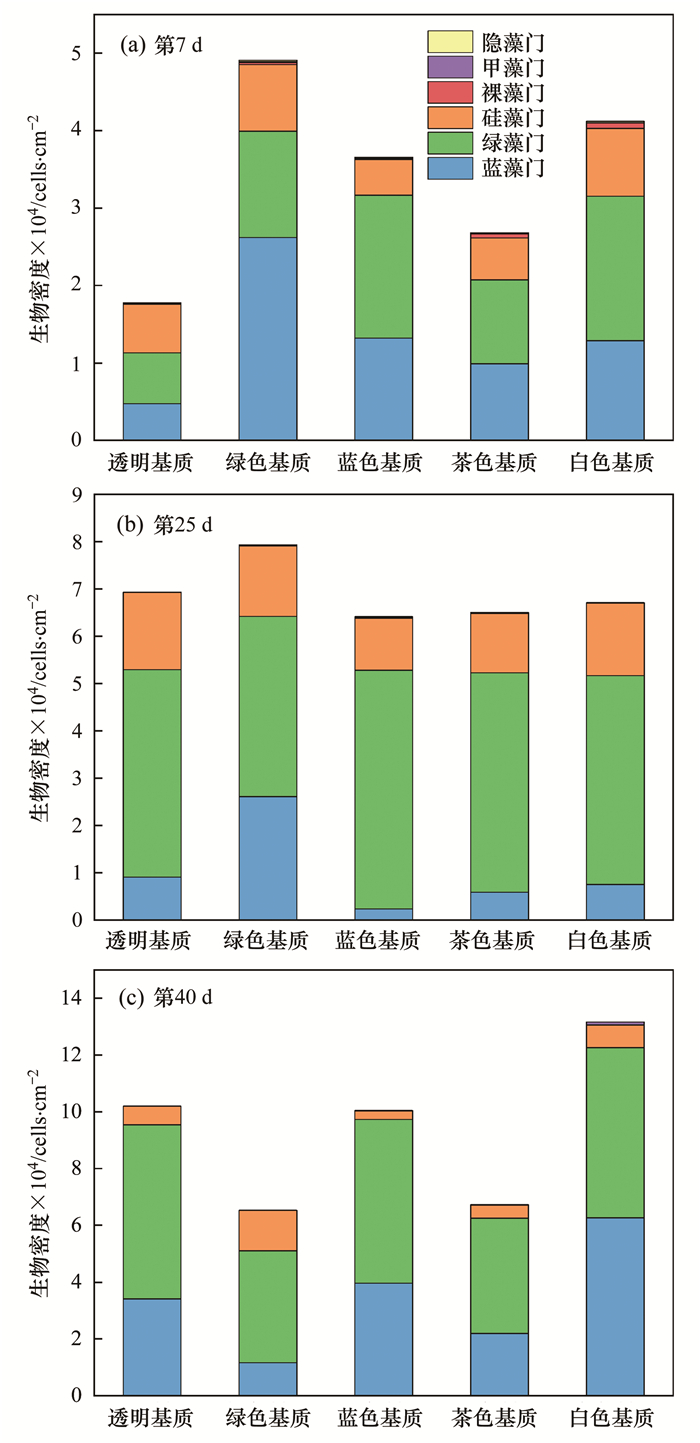
各实验组中附着藻类群落主要由蓝藻门、绿藻门和硅藻门组成.绿色组在第7 d的生物密度为4.91×104 cells ·cm-2, 显著高于透明组的1.78×104 cells ·cm-2(P < 0.05, 图 6).除绿色组外, 其他4个实验组的蓝藻门的相对丰度从第7 d(实验初期)到第25 d再到第40 d(实验结束)均呈现先减少再增加的趋势, 绿藻门则表现为先升高再减少的趋势(图 6).
|
图 6 附着藻类群落不同生长时间的生物密度 Fig. 6 Abundance of periphytic algae at different growth time |
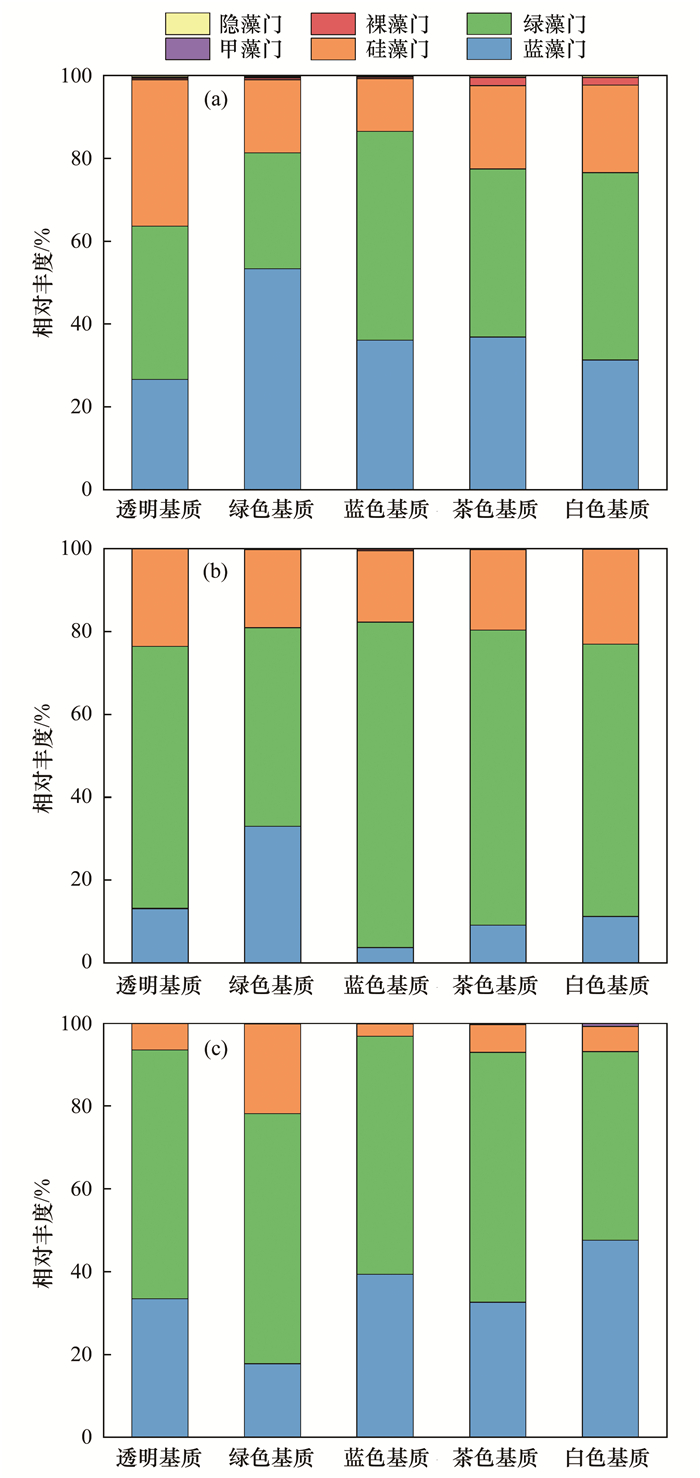
本实验初期(第7 d), 透明、蓝色、茶色和白色这4个实验组中附着藻类相对丰度大小为:绿藻门>蓝藻门>硅藻门, 而绿色组则是蓝藻门的相对丰度最高(图 7).绿色组在实验中期和后期, 绿藻门的相对丰度远大于其他门类(图 7).
|
(a)第7 d, (b)第25 d, (c)第40 d 图 7 附着藻类不同生长时间的相对丰度 Fig. 7 Relative abundance of periphytic algae at different growth time |
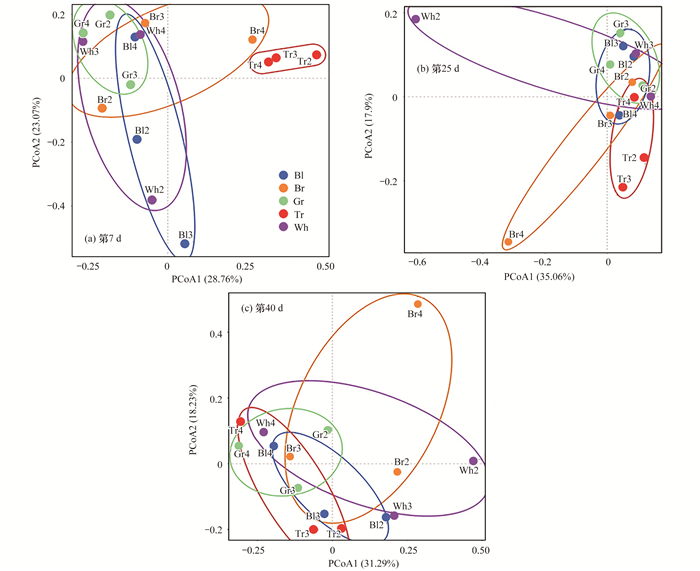
主坐标分析(PCoA分析)的结果显示, 实验第7 d透明组和绿色组的群落组成在PCoA 1上相距较远, 有显著性差异[P < 0.05, 图 8(a)].实验第25 d和实验第40 d, 各实验组的群落组成有大量重叠, 表明在第25 d和第40 d各实验组的群落组成没有显著差异[P>0.05, 图 8(b)和8(c)].
|
Bl表示蓝色(blue); Br表示茶色(brown); Gr表示绿色(green); Tr表示透明(transparent); Wh表示白色(white) 图 8 附着藻类群落不同生长时间PCoA分析 Fig. 8 PCoA analysis of periphytic algae community at different growth time |
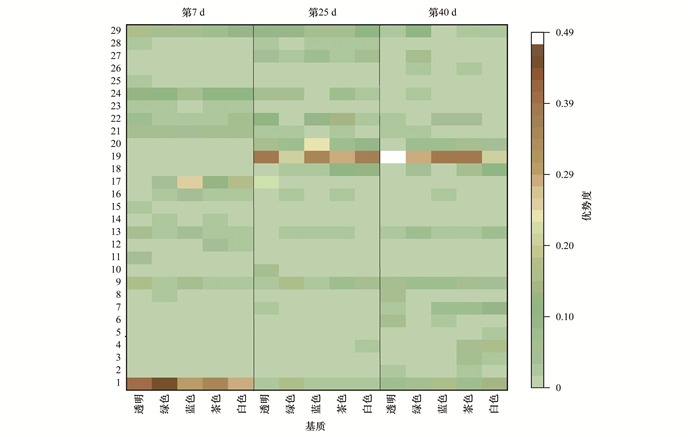
实验初期(第7 d)蓝藻门的伪鱼腥藻属(Pseudoanabaena)为所有实验组的优势属, 在实验中后期(第25 d和第40 d)绿藻门的转板藻属(Mougeotia)为优势属(图 9).
|
1.伪鱼腥藻属(Pseudoanabaena); 2.隐杆藻属(Aphanothece); 3.微囊藻属(Microcystis); 4.隐球藻属(Aphanocapsa); 5.柱胞藻属(Cylindrospermum); 6.拟柱孢藻属(Cylindrospermopsis); 7.长孢藻属(Dolichospermum); 8.拟浮丝藻属(Planktothricoides); 9.鞘丝藻属(Lyngbya); 10.浮鞘丝藻属(Planktolyngbya); 11.颤藻属(Oscillatoria); 12.衣藻属(Chlamydomonas); 13.小球藻属(Chlorella); 14.十字藻属(Crucigenia); 15.卵囊藻属(Oocystis); 16.盘星藻属(Pediastrum); 17.集星藻属(Actinastrum); 18.鼓藻属(Cosmarium); 19.转板藻属(Mougeotia); 20.毛枝藻属(Stigeoclonium); 21.栅藻属(Scenedesmus); 22.空星藻属(Coelastrum); 23.空球藻属(Eudorina); 24.小环藻属(Cyclotella); 25.直链藻属(Melosira); 26.舟形藻属(Navicula); 27.针杆藻属(Synedra); 28.脆杆藻属(Fragilaria); 29.菱形藻属(Nitzschia) 图 9 不同颜色PC塑料板上第7、25和40 d附着藻类优势属 Fig. 9 Dominant genera of periphytic algae on day 7, 25, and 40 on PC substrates with different colors |
本研究中, 所有实验组附着藻类的物种主要是由蓝藻门、绿藻门和硅藻门这三大门类组成.实验中期, 蓝藻门的占比下降而绿藻门上升; 随着附着藻膜的成熟, 实验中后期硅藻门的占比持续降低(图 6和图 7).定植初期(第7 d)透明组和绿色组的附着藻类生物密度差别较大, PCoA分析表明, 两处理组藻类群落有显著差异(P < 0.05).这可能是因为实验初期(第7 d)定植者直接和附着基质表面接触, 附着藻类更易受到附着基质颜色添加剂的影响, 即不同藻类物种对不同的颜色添加剂的敏感度和耐受力不同, 这可能会导致各实验组的附着藻类群落组成不同[32].塑料制品在生产过程中, 人为添加的添加剂, 如增塑剂、阻燃剂、颜料、抗菌剂和热稳定剂等, 可以确定和改变特定的塑料特性[33].如Oehlmann等[34]研究发现, 塑化剂会干扰不同海洋生物群体的激素功能, 影响其发育和繁殖.De Tender等[35]研究发现, 塑料颗粒中的某些色素可以解释附着细菌定植的差异, 如Mycobacterium frederiksbergense, 在蓝色和黄色的塑料上具有较高的丰度, 而在其他塑料颗粒上几乎没有; 这种差异的产生是因为这两种塑料上存在蒽衍生物, 从而影响了细菌的定植.本研究中后期(第25 d和40 d)附着藻类总生物密度无显著差异(P>0.05); PCoA分析也发现, 各实验组附着藻类的群落结构趋同, 虽有差异, 但不显著(P>0.05).这可能是由于随着附着藻膜的逐步发育成熟, 生物膜厚度不断增加[36, 37], 后期定植的附着藻类不再直接和附着基质接触, 基质本身化学特性对附着藻类群落组成的影响逐渐减小[38, 39].Oberbeckmann等[40]研究发现, 在PS、PE和木板上培养2周后, 新的附着藻膜可能会直接定植到已形成的附着藻膜上形成次级附着藻层, 主要和现有附着藻膜有关, 而非附着基质本身.附着藻膜在自然水体中发育成熟一般需要3~4周时间, 分为两个阶段, 第一个阶段是不同环境条件下附着生物在附着基质表面的定植, 第二个阶段是后续的附着生物和基质表面已存在的附着藻之间的相互作用[32].所以, 只有早期的主要定植者, 才有可能直接和附着基质相互作用, 受到附着基质的影响较大.
本研究中, 叶绿素a含量在初期(第7 d)较高, 叶绿素a和干重含量呈现先降低后上升的“U”现象(图 2和图 3), 这可能因为:本实验将附着基平铺于水槽底部, 附着藻类的种源主要由水柱中的藻类沉降而来; 水柱中浮游藻和真性附着藻类并存, 在无水流运动的情况下, 无鞭毛藻类会开始下沉[41], 在首次测定时, 叶绿素a含量来源主要为水柱沉降的藻类, 之后, 一些不能适应附着/底栖生活的藻类会逐渐死亡, 可营附着/底栖生活的藻类逐渐增加, 演替为附着藻类群落.本研究中, 茶色PC塑料组会抑制附着藻类的生长, 该组叶绿素a和干重含量显著低于其他实验组(图 2).不同颜色的PC塑料上附着藻类的生长的差异可能是由不同颜色对光的选择性吸收造成的. 唐青青等[42]和魏群等[43]研究都表明, 红蓝光有利于蛋白核小球藻叶绿素a和β-胡萝卜素的合成, 而蓝光可促进叶绿素b的合成.如韩军军等[44]研究发现, 藻类对可见光的吸收波长主要集中在400~510 nm的蓝紫光区和610~720 nm的红橙光区.本实验中, 透明组和绿色组在400~750 nm的透射比远高于其他实验组.蓝色组、茶色组和白色组分别在512、465和748 nm出现峰值.在600~700 nm范围内, 白色组的透射比高于绿色组和茶色组(图 1). Fv/Fm表示植物的最大光合效率, 它反映的是植物的光合能力的强弱.Yield表示植物叶片中光系统Ⅱ的实际光合效率, 反映了光系统Ⅱ在部分反应中心关闭的情况下, 植物叶片实际的光能捕获效率[4].茶色组的Fv/Fm和Yield从第13 d起持续降低(图 4和图 5), 这反映了茶色组附着藻类PSⅡ反应中心内光能转换效率的下降.茶色组Yield值在实验中后期低于其他组, 表明茶色组的最大光合效率(Fv/Fm)和实际光合效率(Yield)在中后期持续减弱, 从而使附着藻类的生长受到限制.
4 结论PC塑料颜色差异导致对附着藻类群落结构影响主要在发育/定植阶段, 对后期发育成熟阶段的影响不大.群落发育初期(实验第7 d), 绿色组附着藻类的生物密度高于其他实验组, 而中后期(第25 d和40 d)各实验组群落结构趋同, 密度无显著差异.总体上, 茶色PC塑料会抑制附着藻类的生长, 而绿色PC塑料会抑制附着藻类的光合作用活力, 白色PC可获得最高生物量.
| [1] | Dickman M. Changes in periphyton community structure following diatom inhibition[J]. Oikos, 1974, 25(2): 187-193. DOI:10.2307/3543640 |
| [2] | Azim M E, Wahab M A, Verdegem M C J, et al. The effects of artificial substrates on freshwater pond productivity and water quality and the implications for periphyton-based aquaculture[J]. Aquatic Living Resources, 2002, 15(4): 231-241. DOI:10.1016/S0990-7440(02)01179-8 |
| [3] | Wu Y H. Periphyton: functions and application in environmental remediation[M]. Amsterdam: Elsevier, 2017. |
| [4] | Larned S T. A prospectus for periphyton: recent and future ecological research[J]. Journal of the North American Benthological Society, 2010, 29(1): 182-206. DOI:10.1899/08-063.1 |
| [5] |
陈重军, 韩志英, 朱荫湄, 等. 周丛藻类及其在水质净化中的应用[J]. 应用生态学报, 2009, 20(11): 2820-2826. Chen C J, Han Z Y, Zhu Y M, et al. Periphyton and its application in water purification[J]. Chinese Journal of Applied Ecology, 2009, 20(11): 2820-2826. DOI:10.13287/j.1001-9332.2009.0387 |
| [6] | Stevenson R J. Epilithic and epipelic diatoms in the Sandusky River, with emphasis on species diversity and water pollution[J]. Hydrobiologia, 1984, 114(3): 161-175. DOI:10.1007/BF00031868 |
| [7] |
梁霞. 周丛藻类环境响应与水质处理应用研究[D]. 上海: 华东师范大学, 2007. Liang X. Effect of periphyton on water environment and its application in water quality treatment[D]. Shanghai: East China Normal University, 2007. |
| [8] | Battin T J, Kaplan L A, Newbold J D, et al. Contributions of microbial biofilms to ecosystem processes in stream mesocosms[J]. Nature, 2003, 426(6965): 439-442. DOI:10.1038/nature02152 |
| [9] | Cantonati M, Lowe R L. Lake benthic algae: toward an understanding of their ecology[J]. Freshwater Science, 2014, 33(2): 475-486. DOI:10.1086/676140 |
| [10] |
谷雪维. 周丛生物对恩诺沙星和磺胺的生物降解研究[D]. 上海: 上海海洋大学, 2021. Gu X W. Study on biodegradation of enrofloxacin and sulfanilamide by periphyton[D]. Shanghai: Shanghai Ocean University, 2021. |
| [11] |
孙沉沉, 马兰, 吴永红, 等. 吲哚乙酸对周丛生物去除水体中氮磷的影响及机理[J]. 中国农业科技导报, 2022, 24(3): 204-209. Sun C C, Ma L, Wu Y H, et al. Effects and mechanism of indoleacetic acid on the removal of nitrogen and phosphorus from water by peripheral organisms[J]. Journal of Agricultural Science and Technology, 2022, 24(3): 204-209. |
| [12] | Murdock J N, Dodds W K. Linking benthic algal biomass to stream substratum topography[J]. Journal of Phycology, 2007, 43(3): 449-460. DOI:10.1111/j.1529-8817.2007.00357.x |
| [13] | Azim M E, Asaeda T. Periphyton structure, diversity and colonization[A]. In: Azim M E, Verdegem M C J, van Dam A A, et al (Eds. ). Periphyton: Ecology, Exploitation and Management[M]. Oxford: CABI, 2005. |
| [14] | Chessman B, Growns I R, Currey J, et al. Predicting diatom communities at the genus level for the rapid biological assessment of rivers[J]. Freshwater Biology, 1999, 41(2): 317-331. DOI:10.1046/j.1365-2427.1999.00433.x |
| [15] | Tsavatopoulou V D, Manariotis I D. The effect of surface properties on the formation of Scenedesmus rubescens biofilm[J]. Algal Research, 2020, 52. DOI:10.1016/j.algal.2020.102095 |
| [16] | Oberbeckmann S, Loeder M G J, Gerdts G, et al. Spatial and seasonal variation in diversity and structure of microbial biofilms on marine plastics in Northern European waters[J]. FEMS Microbiology Ecology, 2014, 90(2): 478-492. DOI:10.1111/1574-6941.12409 |
| [17] | Ogonowski M, Motiei A, Ininbergs K, et al. Evidence for selective bacterial community structuring on microplastics[J]. Environmental Microbiology, 2018, 20(8): 2796-2808. DOI:10.1111/1462-2920.14120 |
| [18] |
伍良雨, 吴辰熙, 康杜. 载体对周丛生物生物量和群落的影响研究[J]. 环境科学与技术, 2019, 42(1): 50-57. Wu L Y, Wu C X, Kang D. Study on the effect of substrate on biomass and community of periphyton[J]. Environmental Science & Technology, 2019, 42(1): 50-57. |
| [19] | Guo K, Freguia S, Dennis P G, et al. Effects of surface charge and hydrophobicity on anodic biofilm formation, community composition, and current generation in bioelectrochemical systems[J]. Environmental Science & Technology, 2013, 47(13): 7563-7570. |
| [20] | Zhao S Y, Zhu L X, Wang T, et al. Suspended microplastics in the surface water of the Yangtze Estuary System, China: first observations on occurrence, distribution[J]. Marine Pollution Bulletin, 2014, 86(1-2): 562-568. DOI:10.1016/j.marpolbul.2014.06.032 |
| [21] | Nor N H M, Obbard J P. Microplastics in Singapore's coastal mangrove ecosystems[J]. Marine Pollution Bulletin, 2014, 79(1-2): 278-283. DOI:10.1016/j.marpolbul.2013.11.025 |
| [22] | Xu L, Pan W W, Yang G J, et al. Impact of light quality on freshwater phytoplankton community in outdoor mesocosms[J]. Environmental Science and Pollution Research, 2021, 28(41): 58536-58548. DOI:10.1007/s11356-021-14812-7 |
| [23] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002. |
| [24] | Roháček K, Barták M. Technique of the modulated chlorophyll fluorescence: basic concepts, useful parameters, and some applications[J]. Photosynthetica, 1999, 37(3): 339-363. |
| [25] | Zhang W, Jeppesen E, Wang M M, et al. Allelopathic effect boosts Chrysosporum ovalisporum dominance in summer at the expense of Microcystis panniformis in a shallow coastal water body[J]. Environmental Science and Pollution Research, 2017, 24(5): 4666-4675. DOI:10.1007/s11356-016-8149-0 |
| [26] |
SL 733-2016, 内陆水域浮游植物监测技术规程[S]. SL 733-2016, Technical code of phytoplankton monitoring in inland waters[S]. |
| [27] |
胡鸿钧, 魏印心. 中国淡水藻类-系统、分类及生态[M]. 北京: 科学出版社, 2006. Hu H J, Wei Y X. The freshwater algae of China-systematics, taxonomy and ecology[M]. Beijing: Science Press, 2006. |
| [28] | 魏印心. 中国淡水藻志-第七卷, 第1册-绿藻门, 双星藻目中带鼓藻科鼓藻目鼓藻科[M]. 北京: 科学出版社, 2004. |
| [29] |
王全喜, 曹建国, 刘妍, 等. 上海九段沙湿地自然保护区及其附近水域藻类图集[M]. 北京: 科学出版社, 2008. Wang Q X, Cao J G, Liu Y, et al. Altas of algae in Shanghai Jiuduansha Wetland nature reserve and its adjacent waters[M]. Beijing: Science Press, 2008. |
| [30] |
潘成梅, 刘洋, 安瑞志, 等. 西藏麦地卡湿地的浮游植物——1. 优势种的时空生态位[J]. 湖泊科学, 2021, 33(6): 1805-1819. Pan C M, Liu Y, An R Z, et al. Phytoplankton in the Mitika Wetland, Tibet, China: 1. Spatio-temporal niche of dominant species[J]. Journal of Lake Sciences, 2021, 33(6): 1805-1819. |
| [31] |
高梦蝶, 李艳粉, 李艳利, 等. 晋城市沁河流域秋季浮游植物群落结构特征及其与环境因子的关系[J]. 环境科学, 2022, 43(9): 4576-4586. Gao M D, Li Y F, Li Y L, et al. Characteristics of phytoplankton community structure and their relationships with environmental factors in autumn in Qinhe River Basin of Jincheng Region[J]. Environmental Science, 2022, 43(9): 4576-4586. |
| [32] | Yang Y Y, Liu W Z, Zhang Z L, et al. Microplastics provide new microbial niches in aquatic environments[J]. Applied Microbiology and Biotechnology, 2020, 104(15): 6501-6511. DOI:10.1007/s00253-020-10704-x |
| [33] | Smith M, Love D C, Rochman C M, et al. Microplastics in seafood and the implications for human health[J]. Current Environmental Health Reports, 2018, 5(3): 375-386. DOI:10.1007/s40572-018-0206-z |
| [34] | Oehlmann J, Schulte-Oehlmann U, Kloas W, et al. A critical analysis of the biological impacts of plasticizers on wildlife[J]. Philosophical Transactions of the Royal Society B: Biological Sciences, 2009, 364(1526): 2047-2062. DOI:10.1098/rstb.2008.0242 |
| [35] | De Tender C A, Devriese L I, Haegeman A, et al. Bacterial community profiling of plastic litter in the Belgian part of the North Sea[J]. Environmental Science & Technology, 2015, 49(16): 9629-9638. |
| [36] | Pinto M, Langer T M, Hüffer T, et al. The composition of bacterial communities associated with plastic biofilms differs between different polymers and stages of biofilm succession[J]. PLoS One, 2019, 14(6). DOI:10.1371/journal.pone.0217165 |
| [37] | Wright R J, Erni-Cassola G, Zadjelovic V, et al. Marine plastic debris: a new surface for microbial colonization[J]. Environmental Science & Technology, 2020, 54(19): 11657-11672. |
| [38] | Dudek K L, Cruz B N, Polidoro B, et al. Microbial colonization of microplastics in the Caribbean Sea[J]. PLoS One, 2020, 5(1): 5-17. |
| [39] | Oberbeckmann S, Osborn A M, Duhaime M B. Microbes on a bottle: substrate, season and geography influence community composition of microbes colonizing marine plastic debris[J]. PLoS One, 2016, 11(8). DOI:10.1371/journal.pone.0159289 |
| [40] | Oberbeckmann S, Bartosik D, Huang S X, et al. Genomic and proteomic profiles of biofilms on microplastics are decoupled from artificial surface properties[J]. Environmental Microbiology, 2021, 23(6): 3099-3115. |
| [41] |
张秋节. 浮游藻类和附着藻类生长特性的对比研究[D]. 成都: 西南交通大学, 2009. Zhang Q J. The comparative study of growth characteristics about phytoplankton and attached algae[D]. Chengdu: Southwest Jiaotong University, 2009. |
| [42] |
唐青青, 方治国, 嵇雯雯, 等. 光质对蛋白核小球藻(Chlorella pyrenoidosa)生长特征及生化组成的影响研究[J]. 环境科学, 2014, 35(11): 4212-4217. Tang Q Q, Fang Z G, Ji W W, et al. Effects of light quality on the growth characteristics and biochemical component of Chlorella pyrenoidosa[J]. Environmental Science, 2014, 35(11): 4212-4217. |
| [43] |
魏群, 毛瑞, 马湘蒙, 等. 光质对蛋白核小球藻膜生长及除镉效果的影响[J]. 华北水利水电大学学报(自然科学版), 2021, 42(1): 16-21. Wei Q, Mao R, Ma X M, et al. Effects of light quality on the growth of Chlorella pyrenoidosa biofilm and cadmium removal[J]. Journal of North China University of Water Resources and Electric Power (Natural Science Edition), 2021, 42(1): 16-21. |
| [44] |
韩军军, 钟晨辉, 何培民, 等. 不同光质LED光源对坛紫菜自由丝状体生长和生理特性的影响[J]. 水产学报, 2017, 41(2): 230-239. Han J J, Zhong C H, He P M, et al. Effects of different light-qualities on growth and physiological characteristics of free living conchocelis of Pyropia haitanensis[J]. Journal of Fisheries of China, 2017, 41(2): 230-239. |
 2023, Vol. 44
2023, Vol. 44


