2. 上海市农业科学院生态环境保护研究所, 上海 201403
2. ECO-Environment Protection Research Institute, Shanghai Academy of Agricultural Sciences, Shanghai 201403, China
重金属污染具有隐蔽性、难迁移和难降解等特征引起人们的关注[1, 2].镉(Cd)对生物体具有高度毒性, 不可生物降解、流动性强且在人体中易积累, 即使是极低浓度, 也会严重损害肾脏、骨骼和肺等人体器官[3, 4], 因而Cd污染控制与修复备受重视.已报道且相对成熟的环境Cd去除方法主要包括吸附、沉淀、膜分离、电动修复和生物修复等, 其中吸附法因其具有经济、高效和易处理的优点应用较广[5~7], 高效吸附材料的选择或制备一直是环境修复领域研究热点与难点之一.
生物炭(biochar, BC)是一种富含碳的多孔材料, 通过生物质的热解获得, 是一种较有前景的废水重金属吸附材料[8].有关生物炭去除水体重金属的研究报道较多, 例如Ahmed等[9]的研究通过热解西瓜籽制备生物炭, 获得的西瓜籽生物炭对Pb(Ⅱ)的最大吸附量达到44.32 mg·g-1.Nzediegwu等[10]的研究在500℃下热解油菜秸秆制得生物炭, 油菜秸秆生物炭对Pb(Ⅱ)的最大吸附量达到165 mg·g-1.生物炭吸附重金属的机制可以概括为络合、阳离子-π、化学沉淀和离子交换[11].不同原料和方法所制得的生物炭对重金属的主要吸附机制不同.掺氮生物炭对重金属的吸附机制主要是阳离子-π作用和生物炭表面羟基的络合作用[12], 而鸡粪生物炭对重金属的吸附机制主要是其PO43-或CO32-与重金属的化学沉淀作用, 通过官能团表面络合或阳离子-π吸附起到的作用相对较少[13].不同的热解条件会导致生物炭性质的巨大差异[14], 热解温度的升高提高了生物炭对Pb(Ⅱ)的吸附能力, 这是由于pH、灰分含量和比表面积的增加, 从而增加了离子交换能力、化学沉淀和络合作用[15].可见, 探究生物炭对重金属吸附机制以确定重金属高效吸附生物炭制备条件和方法具有重要意义.
农业废弃物是制备生物炭的重要原料, 我国是人口大国, 在满足国民日常生活需要的同时, 也产生了大量的农业废弃物.根据Wang等[16]的报道, 2016年我国水稻、小麦、玉米、大豆和土豆等农作物秸秆产量约为7.5亿t, 这些农业废弃物具有量大易获取和可再生的潜在资源.利用农业废弃物制备生物炭是实现农业废弃物资源化利用的有效方式之一, 也是我国当前“碳中和”趋势下减少农业排放的重要途径.
不同农业废弃物材料及不同热解温度条件下制备的生物炭对重金属的吸附能力和吸附机制不同[17~21], 而前人较少对吸附机制进行定量分析研究[22~26].本研究以典型农作物秸秆和畜禽粪便为原料, 在不同热解温度下制备生物炭, 在进行理化性质分析和吸附性能的比较的同时, 通过定量分析方法解析不同生物炭对Cd2+吸附机制, 以期为农业废弃物资源化利用和Cd污染农田土壤修复提供理论指导.
1 材料与方法 1.1 生物炭的制备常见的6种农业废弃物收集于北京郊区农田中.使用抽屉式马弗炉以10 ℃·min-1的升温速率, 分别在300℃和700℃的峰值温度下保温2 h后冷却至室温, 制得两种热解温度的牛粪(CD)、鸡粪(CM)和猪粪(PM)这3种畜禽粪便基生物炭.使用抽屉式马弗炉以10 ℃·min-1的升温速率, 分别在300℃和500℃的峰值温度下保温2 h后冷却至室温, 得到两种热解温度的小麦秸秆(WS)、水稻秸秆(RS)和玉米秸秆(CS)这3种秸秆作物秸秆.以300℃和500℃制备的作物秸秆基生物炭, 以300℃和700℃制备的畜禽粪便基生物炭分别被命名为: CDB300、CDB700、CMB300、CMB700、PMB300、PMB700、WSB300、WSB500、RSB300、RSB500、CSB300和CSB500.
1.2 理化性质的测定与表征生物炭加去离子水振荡24 h(1∶60, g·mL-1)后用pH计(InLab Expert Pro-ISM, 瑞士METTLER TOLEDO)测定pH值, CHN元素分析仪分析(Vario EL Ⅲ, 德国Elmentar公司)C、H和N元素含量, 高温灰化法(750℃, 4 h)测定灰分含量, 并通过质量平衡计算出O的含量, 火焰原子吸收分光光度计(3530AA, 中国光谱公司)测定Cd2+浓度, 利用场发射扫描电子显微镜观测生物炭形貌, 乙酸铵提取法测定阳离子交换量(CEC), HCl和NaOH去离子水pH分别调至1.5、2.0、3.0、4.0和5.0并振荡平衡24 h, Zeta电位分析仪(90plus PALS, 美国Brookhaven公司)测定Zeta电位并得到零电位点, 利用Quadrasorb Si-MP比表面积分析仪, 采用Brunauer-Emmett-Teller (BET)方法测定了生物炭在77 K时的比表面积和孔隙率, 利用离子色谱仪(DQ501100, 美国Thermo Fisher Scientific公司)测定碳酸根(CO32-)的浓度, 傅立叶变换红外光谱(FTIR)表征了生物炭的表面官能团.用X射线衍射仪(XRD)测定生物炭表面矿组成分.
1.3 吸附实验等温吸附实验用CdCl2·2.5H2O配置ρ(Cd2+)为5、10、20、50、100、200、500、800和1 000 mg·L-1的溶液, 准确称取0.100 g生物炭于100 mL离心管, 加入25 mL不同浓度Cd2+溶液, 在恒温振荡器25℃条件下振荡24 h, 取上清液用原子吸收分光光度计测定Cd2+浓度, 吸附量Qe(mg·g-1)的计算公式为:
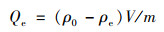
|
式中, ρe为吸附后溶液中Cd2+浓度(mg·L-1), ρ0为吸附前溶液中Cd2+浓度(mg·L-1), V为Cd2+溶液的体积(mL), m为加入生物炭的质量(mg).在该吸附实验中, 每组设置3次平行实验, 求取平均值.
采用Langmuir和Freundlich等温线方程对吸附数据进行拟合:
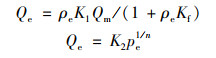
|
式中, pe为污染物的吸附量(mg·g-1), 污染物以一定浓度(ρe)存在; Qm为污染物的最大吸附量; K1为Langmuir吸附等温线常数(mg·L-1), K2为Freundlich吸附等温线常数(mg·L-1), Kf为表征吸附剂和吸附质之间亲和力的参数(L·mg-1).
1.4 不同机制对Cd2+吸附的贡献4种不同吸附机制的确定方法由文献[27]的方法改良获得, 4种吸附机制所得到的对Cd2+的吸附量确定为Qcme、Qcmp、Qco和Qcπ.
用1mol·L-1 HCl洗脱生物炭的矿质成分, 洗脱后的生物炭, 通过FTIR对比洗脱前后生物炭的官能团, 发现没有明显变化. Cd2+吸附实验平衡后的溶液中也未检测出矿质元素.矿质元素对Cd2+的吸附贡献量(Qcm)可以由下式计算得出:
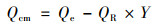
|
式中, Qcm为矿质元素对Cd2+吸附量, Qe为生物炭对Cd2+的吸附量, QR为脱矿生物炭对Cd2+的吸附量, Y为脱矿生物炭的得率.
生物炭在对Cd2+吸附前后溶液中K、Ca、Na和Mg的浓度差值为生物炭离子交换部分(Qcme)的吸附量:
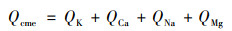
|
式中, QK、QCa、QNa和QMg为溶液前后K、Ca、Na和Mg的净释放量, 其单位均已标准化为Cd的质量分数, mg·g-1.
生物炭无机组分对Cd2+的吸附机制分为离子交换与化学沉淀, 因此生物炭对Cd2+化学沉淀机制吸附量(Qcmp)由生物炭矿质成分(Qcm)与离子交换机制吸附量(Qcme)差值获得:
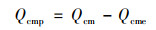
|
由于脱矿生物炭表面官能团的络合作用, 吸附后脱矿生物炭pH下降, 如下所示:
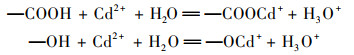
|
H+的释放量可以由pH值的减小值获得, 由上述反应式求得脱矿生物炭络合作用对Cd2+的吸附量(QH), 脱矿生物炭含氧官能团对Cd2+络合部分的吸附量Qco为:
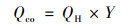
|
由于脱去了无机矿组成分, 脱矿生物炭对Cd2+的吸附作用分为络合作用(Qco)与阳离子-π作用(Qcπ), 阳离子-π作用可通过下式求得:
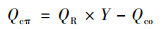
|
采用Windows SPSS 21.0软件对不同农业废弃物生物炭的主要理化特性进行单因素方差分析.所有表中的数据都表示为平均值(3个处理).采用LSD检验评价pH值、灰分和阳离子交换量的差异显著性, 不同字母表示差异显著(P < 0.05).
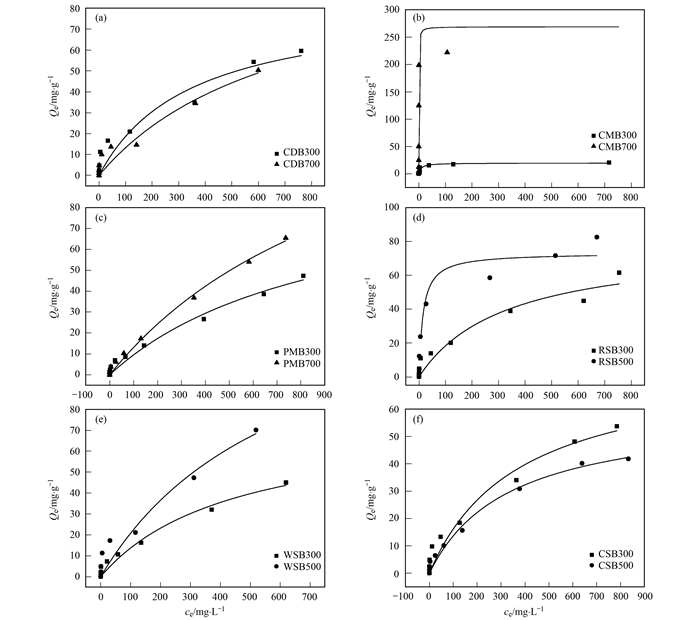
2 结果与分析Langmuir方程拟合不同农业废弃物基生物炭吸附Cd2+等温曲线见图 1, Langmuir和Freundlich拟合参数见表 1和表 2, 相关系数分别为0.848~0.992和0.881~0.996, Freundlich未能拟合所有供试生物炭.在相同热解温度下, 不同畜禽粪便基生物炭对Langmuir方程拟合的Cd2+最大吸附量(Qm)存在较大差异, PMB300对Cd2+的最大吸附量达到96.74 mg·g-1, 约为CMB300的5倍.秸秆生物炭对Cd2+的最大吸附量差异不大, 为61.03~78.97 mg·g-1.
|
图 1 不同温度制备的农业废弃物基生物炭对Cd2+在298 K的等温吸附拟合曲线 Fig. 1 Adsorption isotherm of Cd2+ on agricultural waste-based biochar prepared at different temperatures at 298 K |
|
|
表 1 不同农业废弃物基生物炭对Cd2+的Langmuir吸附方程拟合参数 Table 1 Fitting parameters of Langmuir adsorption isotherms for Cd2+ of different agricultural-waste biochars |
|
|
表 2 不同农业废弃物基生物炭对Cd2+的Freundlich吸附方程拟合参数1) Table 2 Fitting parameters of Freundlich adsorption isotherms for Cd2+ of the different agricultural-waste biochars |
随着热解温度的上升, 畜禽粪便基生物炭对Cd2+的最大吸附量显著增加, CDB、CMB和PMB对Cd2+最大吸附量分别由83.40、19.65和96.74 mg·g-1增大至106.54、268.89和164.53 mg·g-1, CMB的吸附速率常数K1值从0.117 7 mg·L-1增大至2.489 3 mg·L-1, 而作物秸秆基生物炭对Cd2+最大吸附量与吸附速率受热解温度影响不大(表 1和表 2).
所有农业废弃物基生物炭呈碱性(表 3).畜禽粪便基生物炭pH值为7.83~13.00, 作物秸秆基生物炭pH为8.73~10.25.随着热解温度的上升, 农业废弃物基生物炭的pH值显著增大(P < 0.05).除CDB外, 随着热解温度上升, 生物炭的灰分含量显著上升(P < 0.05).畜禽粪便基生物炭的灰分含量高于作物秸秆基生物炭, CMB700灰分含量为57.68%, 在所有农业废弃物基生物炭中最高.除WSB和RSB外, 农业废弃物生物炭的CEC值随温度上升而下降.农业废弃物基生物炭BET比表面积、孔容随热解温度上升而增加, CDB的BET比表面积由1.70 m2·g-1显著提升至110.52 m2·g-1; 孔径随热解温度升高而减小, RSB孔径由27.20 nm降至3.63 nm.除WSB、CMB外, 农业废弃物基生物炭的零电位点随热解温度的上升而上升. CMB、WSB、RSB和CSB的CO32-含量均随热解温度的升高而显著增大, 而CDB和CMB的CO32-含量随热解温度的升高而降低.鸡粪基生物炭中CMB700的CO32-含量高达22.96 mg·g-1, 秸秆基生物炭中RSB500的CO32-含量高达13.53 mg·g-1.作物秸秆基生物炭含碳量高于畜禽粪便基生物炭, 随热解温度上升, 畜禽粪便基生物炭CDB、CMB和PMB含碳量分别从35.18%、35.79%和45.98%减少至27.22%、29.34%和43.85%, 而作物秸秆基生物炭WSB、CSB含碳量分别从55.08%和52.26%增加至64.92%和63.02%; 不同畜禽粪便及秸秆基生物炭的H/C比值随热解温度上升均显著降低, 除CDB外O/C和(O+N)/C比值也随热解温度上升而下降(表 4).
|
|
表 3 不同农业废弃物基生物炭的理化性质1) Table 3 Main physicochemical characteristics of the different agricultural-waste biochars |
|
|
表 4 不同农业废弃物基生物炭的元素含量和原子比 Table 4 Elemental composition and atomic ratio of the different agricultural-waste biochars |
利用扫描电镜表征生物炭表面结构, 结果见图 2所示, 畜禽粪便基生物炭呈现蜂窝状孔隙结构, 而水稻和小麦秸秆基生物炭则呈现明显的长条状纤维结构, 玉米秸秆生物炭为片状结构; 随着热解温度的上升, 畜禽粪便基生物炭堆叠的块状结构分解, 颗粒变小, 生物炭表面粗糙程度逐渐增大, 孔隙结构更加明显, 而水稻和小麦秸秆生物炭出现明显的炭骨架结构, 玉米秸秆生物炭片状结构碎化为小片团簇状结构明显.

|
图 2 不同温度制备的农业废弃物基生物炭的扫描电镜图像 Fig. 2 Field emission scanning electron microscope images of the different agricultural-waste biochars |
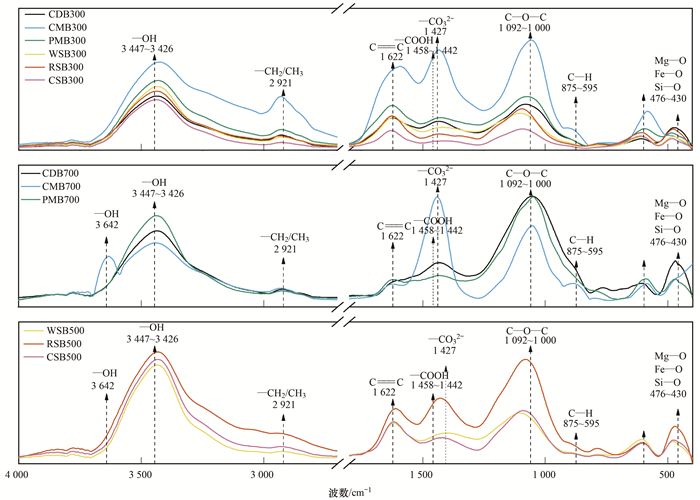
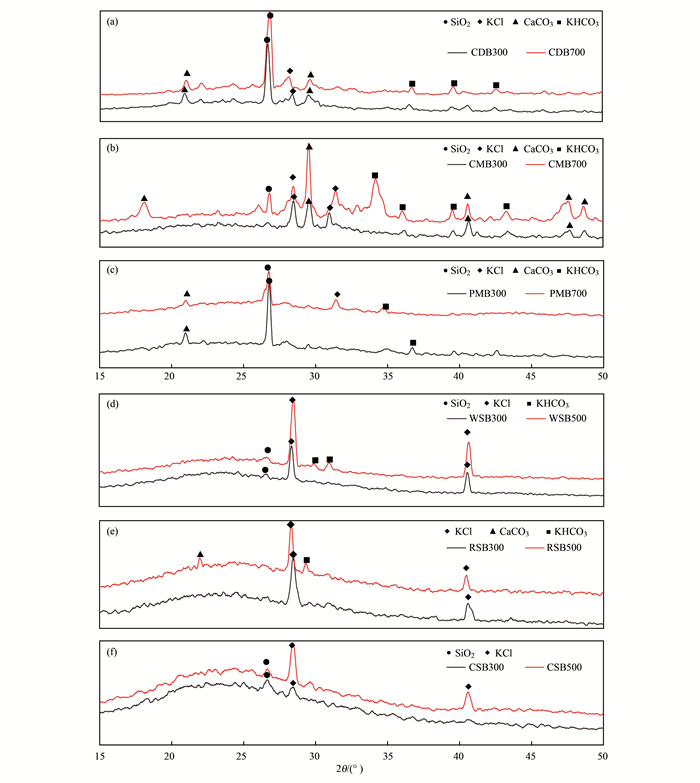
利用傅里叶红外光谱分析生物炭表面官能团结构, 结果如图 3所示, 在3 692、3 447、2 923~2 921、1 622、1 458~1 442、1 427、1 381、1 092~1 000、875~595和476~430 cm-1处出现峰值, 随着热解温度的上升, CDB在1 622 cm-1处的伸缩振动峰消失; CMB在3 642 cm-1处出现伸缩振动峰, 1 622 cm-1处出现伸缩振动峰; PMB在2 921 cm-1处伸缩振动峰消失, 1 458~1 423 cm-1和799~785 cm-1处出现伸缩振动峰; WSB在1 442 cm-1处伸缩振动峰消失; RSB在1 381 cm-1处出现伸缩振动峰, 2 921 cm-1处伸缩振动峰消失; CSB在2 923 cm-1处出现伸缩振动峰(图 3).由XRD图谱所示, 在2θ 为18°、22°、28°、29°、31°、34°、36°、39°、40°、42°和47°出现峰值(图 4).
|
图 3 不同农业废弃物基生物炭的傅里叶红外光谱图 Fig. 3 Fourier infrared spectroscopy of the different agricultural-waste biochars |
|
图 4 不同农业废弃物基生物炭的X射线衍射图像 Fig. 4 X-ray diffraction spectra for the different agricultural-waste biochars |
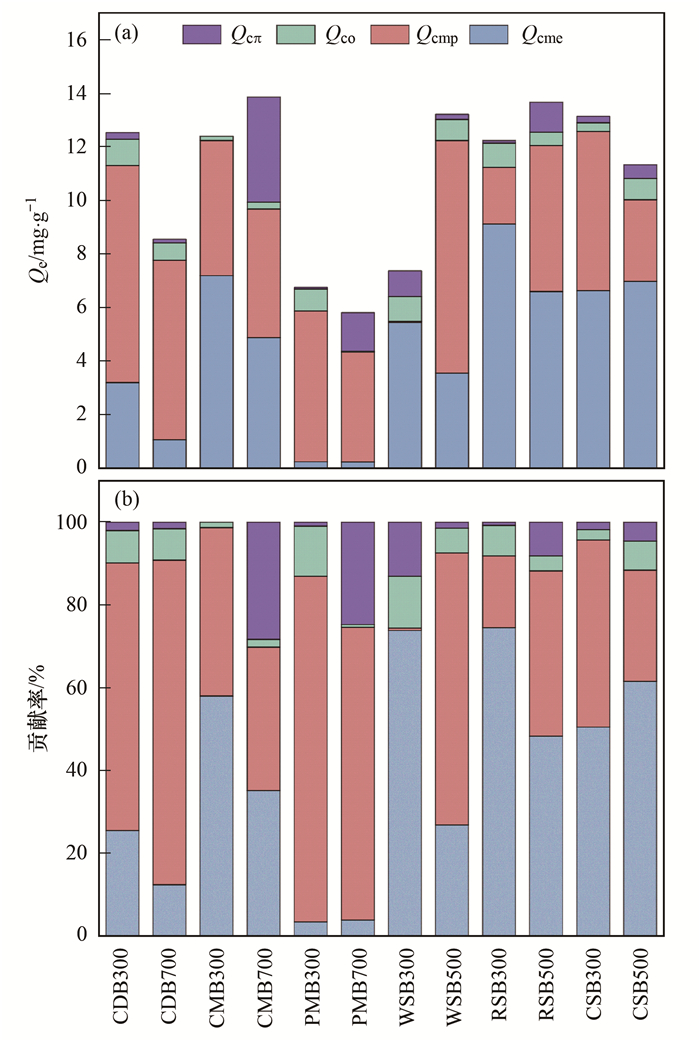
生物炭对Cd吸附的4种机制: 离子交换、化学沉淀、阳离子-π作用和络合作用对其Cd吸附贡献率由图 5所示, 随着热解温度的升高, 畜禽粪便基生物炭Cd吸附总量中, CDB、CMB离子交换的贡献率分别从25%和58%降低至12%和35%, CMB和PMB化学沉淀贡献率分别从41%和84%降低至35%和71%, PMB络合作用贡献率从12%降低至1%, CMB、PMB阳离子-π作用贡献率分别从1%和1%增加至28%和25%; 作物秸秆基生物炭Cd总吸附量中, WSB、RSB离子交换的贡献率分别从74%和75%降低至27%和48%, WSB、RSB化学沉淀贡献率分别从1%和17%增加至66%和40%, WSB和RSB络合作用贡献率分别从13%和7%降低至6%和4%, RSB和CSB阳离子-π作用贡献率分别从1%和2%增加至8%和5%.
|
图 5 农业废弃物基生物炭的不同机制对Cd2+的吸附贡献 Fig. 5 Contribution of different adsorption mechanisms of agricultural waste-based biochar to Cd2+ adsorption |
相比Freundlich方程, 供试生物炭对溶液体系Cd2+的吸附符合Langmiur方程, 表明畜禽粪便和作物秸秆生物炭对Cd2+的吸附是发生在吸附剂表面上的单层化学吸附[27].
除WSB和CMB外, 农业废弃物基生物炭Zeta零电位点随热解温度上升而增大, 这可能是由于生物炭表面在高温条件下羧基和羟基的质子化/去质子化[28].静电作用力更类似于是生物炭吸附重金属离子的基本条件, 提供重金属离子在液膜扩散中的驱动力, 并不能直接决定生物炭的吸附能力, 在吸附实验pH值恒定为5.5, 而所有生物炭的Zeta零电位点均低于5.5, 表明生物炭在吸附实验条件下带负电, 且Zeta零电位点随热解温度的上升而增大, 表明负电性随热解温度上升而减弱.随着热解温度的升高, PMB和CDB的Zeta零电位点从2.45和2.47分别升至2.98和4.02, 而PMB700和CDB700对Cd2+的最大吸附量为164.53 mg·g-1和106.54 mg·g-1, 均高于PMB300和CDB300的83.40 mg·g-1和96.74mg·g-1, 由此可知静电吸附并不是农业废弃物基生物炭对Cd2+的主要吸附机制.
供试农业废弃物基生物炭均为碱性, 随热解温度的上升, 生物炭pH值显著上升.高热解温度下, 生物炭原料大量羧基和酚羟基酯化, 减少质子的离解, 使其碱性加强[29, 30].相同热解温度下, 畜禽粪便基生物炭的灰分含量高于作物秸秆基生物炭, 这可能是由于畜禽粪便中的挥发性化合物在高温条件下才能热解; 而作物秸秆废弃物的易受热挥发的木质纤维素含量高于畜禽粪便废弃物, 这些碳有机化合物即使在低温下也易热解[31].随热解温度上升, 灰分含量增加, 而CDB灰分含量却随着热解温度上升而减少, 可能是由于饲料中的木质纤维素在高温中受热挥发, 这与SEM的结果CDB300中能看见纤维结构而在CDB700中没有发现的结果一致(图 2).RSB灰分含量高于CSB/WSB, 可能是由于水稻秸秆中硅、碳酸钙等无机成分含量较高[32].pH值与灰分含量是影响生物炭对Cd2+吸附离子交换与沉淀作用的主要因素, 进而影响其Cd2+吸附总量.灰分中的K+、Ca2+、Na+和Mg2+可与溶液中的Cd2+发生离子交换作用[33]; SO42-、PO43-和CO32-等矿物组分可与Cd2+发生沉淀作用[34].本研究所有农业废弃物基生物炭中, CMB700灰分含量最高(57.68%)且pH值最大(13.00), 其对Cd的最大吸附量也最高(268.89 mg·g-1), 表明灰分与pH值可能是影响生物炭吸附Cd2+的重要因子, 这与杜文慧等[35]的研究结论一致.XRD图谱也证实了这一点(图 4), CMB700拥有更为丰富的晶体结构, 在2θ为18°、29°、40°和47°代表的CaCO3提供的CO32-, 能与Cd2+发生沉淀作用, 2θ为28°和31°代表的KCl以及2θ=34°代表的KHCO3提供的K+, 能与Cd2+进行离子交换[30].同样, 在FTIR图谱中(图 3), CMB700在3 642 cm-1出现的特有的醇羟基(—OH)与其pH值为13.00的强碱性特征相符, —OH与Cd2+发生化学沉淀作用进而吸附Cd2+[36].定量分析结果表明, 离子交换和化学沉淀作用是农业废弃物基生物炭Cd2+吸附的主要吸附机制, 两者贡献率高达70%~96%, CMB700两者贡献率为70%.定量分析中结果也表明WSB和RSB的Cd吸附总量中化学沉淀贡献率也分别从1%和17%显著上升至66%和40%, 这一现象可能主要是因为在高温下, 生物炭中的金属转变为更稳定的结合态, 不易被交换出去[37], 同时灰分含量增加, 沉淀作用加强, 这与Wang等[16]的研究结论一致.
畜禽粪便基生物炭含碳量低于作物秸秆基生物炭, 可能是因为畜禽粪便原材料中的C和H更容易与O结合形成碳氢化合物、CO2和H2O后挥发; H和N含量随热解温度上升而下降, 这与Zhang等[38]的研究结果相似.(O+N)/C的比值随热解温度上升而下降, 说明生物炭中的极性官能团的消失, 芳香化程度提升[39], 与FTIR图谱中随着热解温度的上升, 生物炭的木质纤维素成分在脱甲基和脱水过程中被去除[37], 在2 923~2 921 cm-1处代表—CH2/CH3的峰消失结果一致; H/C比是描述生物炭芳香化程度的重要指标[40], 芳香环结构可为Cd2+的吸附提供π电子[41].FTIR图谱所示(图 3), 在3 692、3 447、2 923~2 921、1 622、1 458~1 442、1 427、1 381、1 092~1 000、875~595和476~430 cm-1处分别代表矿质—OH、—OH、—CH2/CH3、芳香环C=C、—COOH、CO32-、C—O、C—O—C、芳杂环C—H和Si—O/Fe—O/Mg—O的伸缩振动峰[34, 42~46].农业废弃物基生物炭拥有丰富的官能团结构, 这些官能团可通过络合作用吸附Cd2+.阳离子-π作用和络合作用也对农业废弃物基生物炭吸附Cd2+具有一定贡献, 两者贡献占比为4%~30%.随着热解温度的上升, 阳离子-π作用的加强比络合作用更为显著, 定量分析中畜禽粪便基生物炭PMB、CMB的阳离子-π作用贡献率分别从1%和2%显著上升至25%和28%. CMB700在1 622 cm-1处出现的芳香环C=C, PMB700在799~785 cm-1处出现芳杂环C—H, 芳香结构提高了其对Cd2+的最大吸附量.
4 结论Langmuir方程能够较好地拟合农业废弃物基生物炭对Cd2+的吸附过程.畜禽粪便基生物炭对Cd2+的吸附量随热解温度的升高而增加, 而秸秆基生物炭对Cd2+的吸附量受热解温度影响不显著.高温条件下制备的畜禽粪便基生物炭对Cd2+的吸附能力高于秸秆基生物炭.吸附效果最优的CMB700拥有最高的灰分含量与pH值, 在CMB700对Cd2+吸附过程中离子交换、化学沉淀和阳离子-π作用强于其他原料制备的生物炭.随着热解温度的升高, 芳香基团通过阳离子-π作用对生物炭Cd2+的吸附贡献显著增加, 但化学沉淀和离子交换仍是农业废弃物基生物炭吸附Cd2+的主要机制.
| [1] | Chen Y N, Li M L, Li Y P, et al. Hydroxyapatite modified sludge-based biochar for the adsorption of Cu2+ and Cd2+: adsorption behavior and mechanisms[J]. Bioresource Technology, 2021, 321. DOI:10.1016/j.biortech.2020.124413 |
| [2] | Yin G C, Tao L, Chen X L, et al. Quantitative analysis on the mechanism of Cd2+ removal by MgCl2-modified biochar in aqueous solutions[J]. Journal of Hazardous Materials, 2021, 420. DOI:10.1016/j.jhazmat.2021.126487 |
| [3] | Fu H C, Ma S L, Xu S J, et al. Hierarchically porous magnetic biochar as an efficient amendment for cadmium in water and soil: performance and mechanism[J]. Chemosphere, 2021, 281. DOI:10.1016/j.chemosphere.2021.130990 |
| [4] | Li D T, Cui H B, Cheng Y Q, et al. Chemical aging of hydrochar improves the Cd2+ adsorption capacity from aqueous solution[J]. Environmental Pollution, 2021, 287. DOI:10.1016/j.envpol.2021.117562 |
| [5] | Wu P, Cui P X, Zhang Y, et al. Unraveling the molecular mechanisms of Cd sorption onto MnOx-loaded biochar produced from the Mn-hyperaccumulator Phytolacca americana[J]. Journal of Hazardous Materials, 2022, 423. DOI:10.1016/j.jhazmat.2021.127157 |
| [6] | Liu W, Huang J, Weatherley A J, et al. Identifying adsorption sites for Cd(Ⅱ) and organic dyes on modified straw materials[J]. Journal of Environmental Management, 2022, 301. DOI:10.1016/j.jenvman.2021.113862 |
| [7] | Wang F, Jin L T, Guo C N, et al. Enhanced heavy metals sorption by modified biochars derived from pig manure[J]. Science of the Total Environment, 2021, 786. DOI:10.1016/j.scitotenv.2021.147595 |
| [8] | Chin-Pampillo J S, Perez-Villanueva M, Masis-Mora M, et al. Amendments with pyrolyzed agrowastes change bromacil and diuron's sorption and persistence in a tropical soil without modifying their environmental risk[J]. Science of the Total Environment, 2021, 772. DOI:10.1016/j.scitotenv.2021.145515 |
| [9] | Ahmed W, Mehmood S, Núñez-Delgado A, et al. Utilization of Citrullus lanatus L. seeds to synthesize a novel MnFe2O4-biochar adsorbent for the removal of U(Ⅵ) from wastewater: insights and comparison between modified and raw biochar[J]. Science of the Total Environment, 2021, 771. DOI:10.1016/j.scitotenv.2021.144955 |
| [10] | Nzediegwu C, Naeth M A, Chang S X. Lead(Ⅱ) adsorption on microwave-pyrolyzed biochars and hydrochars depends on feedstock type and production temperature[J]. Journal of Hazardous Materials, 2021, 412. DOI:10.1016/j.jhazmat.2021.125255 |
| [11] | Gao L Y, Deng J H, Huang G F, et al. Relative distribution of Cd2+ adsorption mechanisms on biochars derived from rice straw and sewage sludge[J]. Bioresource Technology, 2019, 272: 114-122. DOI:10.1016/j.biortech.2018.09.138 |
| [12] | Yu W C, Lian F, Cui G N, et al. N-doping effectively enhances the adsorption capacity of biochar for heavy metal ions from aqueous solution[J]. Chemosphere, 2018, 193: 8-16. DOI:10.1016/j.chemosphere.2017.10.134 |
| [13] | Wang H, Huang F, Zhao Z L, et al. High-efficiency removal capacities and quantitative adsorption mechanisms of Cd2+ by thermally modified biochars derived from different feedstocks[J]. Chemosphere, 2021, 272. DOI:10.1016/j.chemosphere.2021.129594 |
| [14] | Huang F, Gao L Y, Wu R R, et al. Qualitative and quantitative characterization of adsorption mechanisms for Cd2+ by silicon-rich biochar[J]. Science of the Total Environment, 2020, 731. DOI:10.1016/j.scitotenv.2020.139163 |
| [15] | Kwak J H, Islam M S, Wang S Y, et al. Biochar properties and lead(Ⅱ) adsorption capacity depend on feedstock type, pyrolysis temperature, and steam activation[J]. Chemosphere, 2019, 231: 393-404. DOI:10.1016/j.chemosphere.2019.05.128 |
| [16] | Wang R Z, Huang D L, Liu Y G, et al. Investigating the adsorption behavior and the relative distribution of Cd2+ sorption mechanisms on biochars by different feedstock[J]. Bioresource Technology, 2018, 261: 265-271. DOI:10.1016/j.biortech.2018.04.032 |
| [17] | Pan X Q, Gu Z P, Chen W M, et al. Preparation of biochar and biochar composites and their application in a Fenton-like process for wastewater decontamination: a review[J]. Science of the Total Environment, 2021, 754. DOI:10.1016/j.scitotenv.2020.142104 |
| [18] | Guo J L, Zheng L, Li Z F, et al. Effects of various pyrolysis conditions and feedstock compositions on the physicochemical characteristics of cow manure-derived biochar[J]. Journal of Cleaner Production, 2021, 311. DOI:10.1016/j.jclepro.2021.127458 |
| [19] | Zhang J, Liu J, Liu R L. Effects of pyrolysis temperature and heating time on biochar obtained from the pyrolysis of straw and lignosulfonate[J]. Bioresource Technology, 2015, 176: 288-291. DOI:10.1016/j.biortech.2014.11.011 |
| [20] | Fan X B, Wang X H, Cai Y T, et al. Functionalized cotton charcoal/chitosan biomass-based hydrogel for capturing Pb2+, Cu2+and MB[J]. Journal of Hazardous Materials, 2022, 423. DOI:10.1016/j.jhazmat.2021.127191 |
| [21] | Peng Y R, Azeem M, Li R H, et al. Zirconium hydroxide nanoparticle encapsulated magnetic biochar composite derived from rice residue: Application for As(Ⅲ) and As(Ⅴ) polluted water purification[J]. Journal of Hazardous Materials, 2022, 423. DOI:10.1016/j.jhazmat.2021.127081 |
| [22] | Chen F, Guo S H, Wang Y H, et al. Concurrent adsorption and reduction of chromium(Ⅵ) to chromium(Ⅲ) using nitrogen-doped porous carbon adsorbent derived from loofah sponge[J]. Frontiers of Environmental Science & Engineering, 2022, 16(5). DOI:10.1007/s11783-021-1491-6 |
| [23] | Murad H A, Ahmad M, Bundschuh J, et al. A remediation approach to chromium-contaminated water and soil using engineered biochar derived from peanut shell[J]. Environmental Research, 2022, 204. DOI:10.1016/j.envres.2021.112125 |
| [24] | Zeng B Y, Xu W B, Khan S B, et al. Preparation of sludge biochar rich in carboxyl/hydroxyl groups by quenching process and its excellent adsorption performance for Cr(Ⅵ)[J]. Chemosphere, 2021, 285. DOI:10.1016/j.chemosphere.2021.131439 |
| [25] | Cairns S, Chaudhuri S, Sigmund G, et al. Wood ash amended biochar for the removal of lead, copper, zinc and cadmium from aqueous solution[J]. Environmental Technology & Innovation, 2021, 24. DOI:10.1016/j.eti.2021.101961 |
| [26] | Quyen V T, Pham T H, Kim J, et al. Biosorbent derived from coffee husk for efficient removal of toxic heavy metals from wastewater[J]. Chemosphere, 2021, 284. DOI:10.1016/j.chemosphere.2021.131312 |
| [27] | 崔孝强. 水体修复植物基生物炭的环境应用及其机理研究[D]. 杭州: 浙江大学, 2018. |
| [28] | Wang H Y, Gao B, Wang S S, et al. Removal of Pb(Ⅱ), Cu(Ⅱ), and Cd(Ⅱ) from aqueous solutions by biochar derived from KMnO4 treated hickory wood[J]. Bioresource Technology, 2015, 197: 356-362. DOI:10.1016/j.biortech.2015.08.132 |
| [29] | Cao X D, Harris W. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation[J]. Bioresource Technology, 2010, 101(14): 5222-5228. DOI:10.1016/j.biortech.2010.02.052 |
| [30] | Li C X, Xie S Y, Wang Y, et al. Multi-functional biochar preparation and heavy metal immobilization by co-pyrolysis of livestock feces and biomass waste[J]. Waste Management, 2021, 134: 241-250. DOI:10.1016/j.wasman.2021.08.023 |
| [31] | 韦思业. 不同生物质原料和制备温度对生物炭物理化学特征的影响[D]. 广州: 中国科学院大学(中国科学院广州地球化学研究所), 2017. |
| [32] | Xiao X, Chen B L, Zhu L Z. Transformation, morphology, and dissolution of silicon and carbon in rice straw-derived biochars under different pyrolytic temperatures[J]. Environmental Science & Technology, 2014, 48(6): 3411-3419. |
| [33] | Yang S, Wen Q X, Chen Z Q. Effect of KH2PO4- modified biochar on immobilization of Cr, Cu, Pb, Zn and as during anaerobic digestion of swine manure[J]. Bioresource Technology, 2021, 339. DOI:10.1016/j.biortech.2021.125570 |
| [34] | Cui X Q, Fang S Y, Yao Y Q, et al. Potential mechanisms of cadmium removal from aqueous solution by Canna indica derived biochar[J]. Science of the Total Environment, 2016, 562: 517-525. DOI:10.1016/j.scitotenv.2016.03.248 |
| [35] |
杜文慧, 朱维琴, 潘晓慧, 等. 牛粪源蚓粪及其生物炭对Pb2+、Cd2+的吸附特性[J]. 环境科学, 2017, 38(5): 2172-2181. Du W H, Zhu W Q, Pan X H, et al. Adsorption of Pb2+ and Cd2+ from aqueous solution using vermicompost derived from cow manure and its biochar[J]. Environmental Science, 2017, 38(5): 2172-2181. |
| [36] |
王鑫宇, 孟海波, 沈玉君, 等. 改性生物炭特性表征及对冶炼厂周边农田土壤铜镉形态的影响[J]. 环境科学, 2021, 42(9): 4441-4451. Wang X Y, Meng H B, Shen Y J, et al. Characteristics of modified biochars and their immobilization effect on Cu and Cd in polluted farmland soil around smelter[J]. Environmental Science, 2021, 42(9): 4441-4451. |
| [37] | Ahmed W, Mehmood S, Núñez-Delgado A, et al. Enhanced adsorption of aqueous Pb(Ⅱ) by modified biochar produced through pyrolysis of watermelon seeds[J]. Science of the total environment, 2021, 784. DOI:10.1016/j.scitotenv.2021.147136 |
| [38] | Zhang P Z, Zhang X X, Yuan X R, et al. Characteristics, adsorption behaviors, Cu(Ⅱ) adsorption mechanisms by cow manure biochar derived at various pyrolysis temperatures[J]. Bioresource Technology, 2021, 331. DOI:10.1016/j.biortech.2021.125013 |
| [39] | Wang S Q, Zhang H, Huang H Y, et al. Influence of temperature and residence time on characteristics of biochars derived from agricultural residues: a comprehensive evaluation[J]. Process Safety and Environmental Protection, 2020, 139: 218-229. DOI:10.1016/j.psep.2020.03.028 |
| [40] | Luo L, Xu C, Chen Z E, et al. Properties of biomass-derived biochars: combined effects of operating conditions and biomass types[J]. Bioresource Technology, 2015, 192: 83-89. DOI:10.1016/j.biortech.2015.05.054 |
| [41] | Harvey O R, Herbert B E, Rhue R D, et al. Metal Interactions at the biochar-water interface: energetics and structure-sorption relationships elucidated by flow adsorption microcalorimetry[J]. Environmental Science & Technology, 2011, 45(13): 5550-5556. |
| [42] | Chen D, Wang X B, Wang X L, et al. The mechanism of cadmium sorption by sulphur-modified wheat straw biochar and its application cadmium-contaminated soil[J]. Science of the Total Environment, 2020, 714. DOI:10.1016/j.scitotenv.2020.136550 |
| [43] | Yan C X, Xu Y M, Wang L, et al. Effect of different pyrolysis temperatures on physico-chemical characteristics and lead(Ⅱ) removal of biochar derived from chicken manure[J]. RSC Advances, 2020, 10(7): 3667-3674. DOI:10.1039/C9RA08199B |
| [44] | Zhang H C, Wang T, Sui Z F, et al. Enhanced mercury removal by transplanting sulfur-containing functional groups to biochar through plasma[J]. Fuel, 2019, 253: 703-712. DOI:10.1016/j.fuel.2019.05.068 |
| [45] | Tao Q, Chen Y X, Zhao J W, et al. Enhanced Cd removal from aqueous solution by biologically modified biochar derived from digestion residue of corn straw silage[J]. Science of the Total Environment, 2019, 674: 213-222. DOI:10.1016/j.scitotenv.2019.03.438 |
| [46] | Li Z, Li M, Wang Z Y, et al. Coadsorption of Cu(Ⅱ) and tylosin/sulfamethoxazole on biochar stabilized by nano-hydroxyapatite in aqueous environment[J]. Chemical Engineering Journal, 2020, 381. DOI:10.1016/j.cej.2019.122785 |
 2022, Vol. 43
2022, Vol. 43


