2. 国家重金属污染防治工程技术研究中心, 长沙 410083
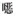 唑(SMX)和甲氧苄啶(TMP), 对比研究了其在不同碳源条件下的变化规律, 评估了吸附和生物降解等途径对抗生素去除的贡献.结果表明, 反硝化脱氮体系对NOR、OTC和TMP具有一定的去除作用, 且NOR和OTC可被用作碳源进行反硝化.反硝化污泥对NOR和OTC的去除是快速吸附和缓慢生物降解的过程, 其中, 吸附对NOR和OTC总去除量的贡献率分别达到83.5%和58.9%, 生物降解的贡献率分别为16.5%和41.1%.在吸附过程中, 胞外聚合物(EPS)吸附的贡献率达到40%以上, 而在OTC的生物降解过程中, P450酶发挥重要作用, 其贡献率达到20%.
唑(SMX)和甲氧苄啶(TMP), 对比研究了其在不同碳源条件下的变化规律, 评估了吸附和生物降解等途径对抗生素去除的贡献.结果表明, 反硝化脱氮体系对NOR、OTC和TMP具有一定的去除作用, 且NOR和OTC可被用作碳源进行反硝化.反硝化污泥对NOR和OTC的去除是快速吸附和缓慢生物降解的过程, 其中, 吸附对NOR和OTC总去除量的贡献率分别达到83.5%和58.9%, 生物降解的贡献率分别为16.5%和41.1%.在吸附过程中, 胞外聚合物(EPS)吸附的贡献率达到40%以上, 而在OTC的生物降解过程中, P450酶发挥重要作用, 其贡献率达到20%.
2. Chinese National Engineering Research Center for Control and Treatment of Heavy Metal Pollution, Central South University, Changsha 410083, China
抗生素(antibiotics)是指由细菌、霉菌或其他微生物在生活过程中所产生, 具有抗病原体或其他活性的一类次级代谢产物, 被广泛地应用于人类及动物的疾病防治、农业生产、畜牧和水产养殖等领域[1].我国是世界上最大的抗生素生产和使用国[2], 抗生素每年生产和使用量超过2.5万t[3].污水处理厂是抗生素的重要汇集场所, 人类活动使用的抗生素会通过多种途径汇集到污水处理厂生物处理系统.如我国厦门某厌氧-缺氧-好氧污水处理厂中检测到10种以上抗生素[4].在污水生物处理系统中, 未被生物降解的抗生素常被吸附到污泥上或残留在水体中.其中, 吸附到污泥上且未被去除的抗生素可能会对污泥体系中的功能微生物造成不利影响; 抗生素随剩余污泥和出水排入环境, 则会加剧水环境功能紊乱, 危害水质安全[5].因此, 研究抗生素在污水处理厂生物处理系统中的归趋及去除特性具有重要意义.
反硝化是污水处理厂生物脱氮的关键环节, 反硝化菌可在缺氧及有机物共存的条件下将硝态氮转化为氮气[6].由于抗生素是一类相对难降解的特殊有机物, 现有大多数研究集中于氧化能力更强的好氧氧化体系[7~9], 其在缺氧反硝化脱氮体系的变化规律尚不清晰.有研究表明, 反硝化对一些有毒难降解有机物的转化起着重要作用[10], 反硝化菌群甚至能够利用芳香族化合物, 如邻苯二酚[11]和苯扎氯氨[12]等作为碳源进行反硝化.因此, 阐明抗生素在反硝化脱氮体系中的去除特性对科学评估抗生素对污水生物处理系统的影响具有重要参考价值.
本研究基于抗生素的分子结构、使用量、生物毒性等特征, 筛选出诺氟沙星(norfloxacin, NOR)、土霉素(oxytetracycline, OTC)、磺胺甲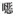
实验采用模拟废水.所需NO3--N和有机碳源分别以NaNO3和CH3COONa形式提供.4种典型抗生素, 诺氟沙星(CAS#70458-96-7, norfloxacin, NOR, C16H18FN3O3)、土霉素(CAS#79-57-2, oxytetracycline, OTC, C22H24N2O9)、磺胺甲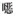
|
|
表 1 4种抗生素的理化性质1) Table 1 Physicochemical properties of four antibiotics |
1.2 实验污泥
反硝化污泥取自实验室长期运行的5 L SBR, 反应器运行温度保持为(30±1)℃, 运行周期为进水(10 min)、缺氧搅拌(300 min)、静置(20 min)、排水(20 min)和闲置(10 min).反应器氮容积负荷(以NO3--N计)为0.6 kg·(m3·d)-1, 有机容积负荷(以COD计)为2.4 kg·(m3·d)-1, 悬浮固体浓度控制在2000~3000 mg·L-1.高通量测序结果表明反应器中典型的反硝化菌属Thauera的相对丰度为26.44%.
1.3 实验方法采用批次实验考察抗生素在不同基质条件(无碳源供给和外加充足碳源)下的去除情况.配制反硝化所需的NO3--N和CH3COONa浓度, 分别加入5 mg·L-1的NOR、OTC、SMX和TMP.调节pH为6.8~7.0之间, 加入一定量洗涤干净的实验室培育好的反硝化污泥, 通入20 min 95% Ar-5% CO2气体, 密闭后置于恒温水浴振荡器中, 于30℃、170 r·min-1的条件下避光振荡.所取水样经0.22 μm滤头过滤后测定NO2--N和NO3--N等水质指标和抗生素浓度.
为了评估每种去除途径对抗生素去除的贡献, 设计了因素控制实验, 实验条件如表 2所示.在反应体系Ⅰ中, 4种去除途径同时存在; 在反应体系Ⅱ中, 加入0.1% NaN3完全抑制污泥中微生物的活性, 以排除生物降解的作用; 反应体系Ⅲ中, 不加入污泥, 考察挥发和水解对抗生素去除的贡献.采用如下算式计算生物降解、吸附、挥发和水解作用对抗生素去除量:
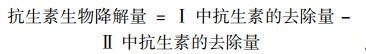
|
(1) |

|
(2) |
|
|
表 2 抗生素去除途径的实验设计1) Table 2 Experimental design of antibiotic removal pathways |
为了探究胞外聚合物(extracellular polymeric substances, EPS)和污泥在抗生素吸附中的贡献, 使用改进的方法[13]提取污泥中的EPS.取1、3、8和24 h反应后的混合液样品, 在1 793 g的条件下离心15 min, 上清液经0.22 μm滤头过滤后用于测定水中抗生素浓度.将管内剩余污泥添加5% NaCl溶液至原体积, 在60℃水浴中水浴30 min, 然后将混合污泥以13 680 g离心15 min, 上清液经0.22 μm滤头过滤后用于测定EPS吸附的抗生素浓度.污泥中抗生素浓度通过总吸附量减去EPS吸附的量确定.
为了探究P450酶在抗生素生物降解中的作用, 通过添加P450酶特征抑制剂1-氨基苯并三唑进行对照实验.
1.4 分析方法NO2--N、NO3--N和COD分别采用N-(1-萘基)-乙二胺分光光度法、紫外分光光度法、快速消解法进行测定.NOR、OTC、SMX和TMP使用超高效液相色谱(Acquity UPLC H-class)测定, 其紫外最大吸收波长(λmax)分别为278、355、268和271 nm.色谱柱为ACQUITY UPLC BEH C18(1.7 μm, 2.1 mm×50 mm)选用乙腈和磷酸盐缓冲液(PBS, 20 mmol·L-1, pH=3.0)作为流动相, 流速为0.3 mL·min-1, 进样体积为10 μL, 色谱柱温度为35℃.
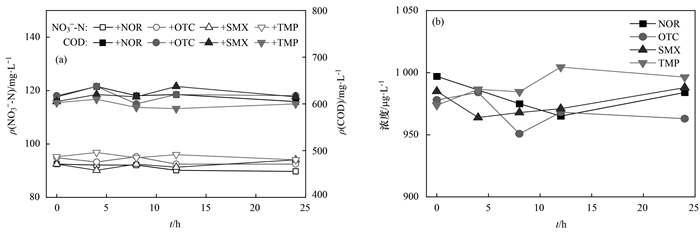
2 结果与讨论 2.1 4种抗生素在不同碳源条件下的去除特性 2.1.1 无污泥体系下的去除特性首先考察了不投加反硝化污泥时主要污染物浓度的变化情况, 结果如图 1所示.反应体系内的NO3--N和COD浓度均保持不变, 表明无微生物时基质不发生化学作用; 4种抗生素的浓度也保持不变.据报道, 抗生素在污水生物处理系统中的去除主要包括光解、挥发、水解、吸附和生物降解等作用[14].结果表明, 在所试条件下4种抗生素的挥发和水解作用均可忽略不计.其难以挥发的原因主要与其极低的亨利定律常数(1.7×10-20~6.5×10-8 Pa·m3·mol-1, 表 1)、较大的相对分子质量(>200, 表 1)和一些极性基团的存在有关[15].
|
(a)添加抗生素下的NO3--N和COD浓度的变化; (b)抗生素浓度变化 图 1 无污泥添加条件下基质和抗生素的浓度变化 Fig. 1 Concentration profile of substrates and antibiotics without addition of sludge |
由于所有实验在避光条件下进行, 也可排除光解作用对抗生素去除的影响.因此, 后续研究中将主要考察吸附和生物降解对抗生素的去除作用.
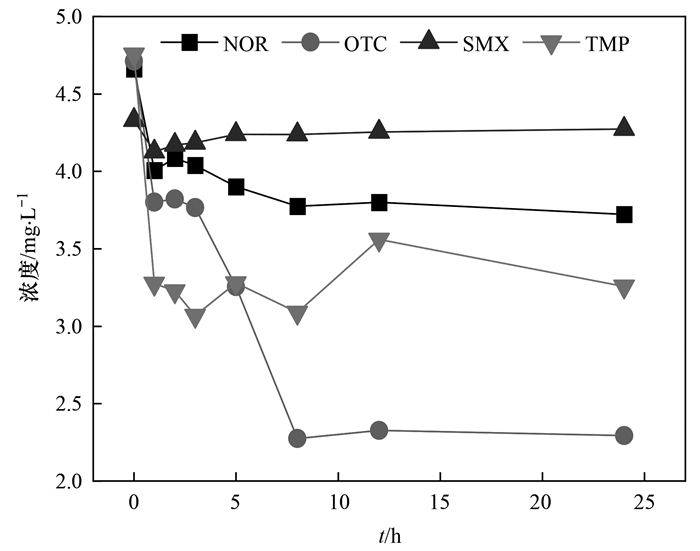
2.1.2 反硝化碳源充足时的去除特性当以乙酸钠为碳源时, 控制COD/N为5(高于理论反硝化的碳氮比2.5), 考察了碳源充足条件下4种抗生素的去除特性.前期探索实验表明, 当添加量为5 mg·L-1时, 4种抗生素均未对反硝化性能产生抑制作用.但与其他3种抗生素明显不同, 磺胺甲
|
图 2 碳源充足时抗生素的浓度变化 Fig. 2 Concentration variation of antibiotics under sufficient carbon source |
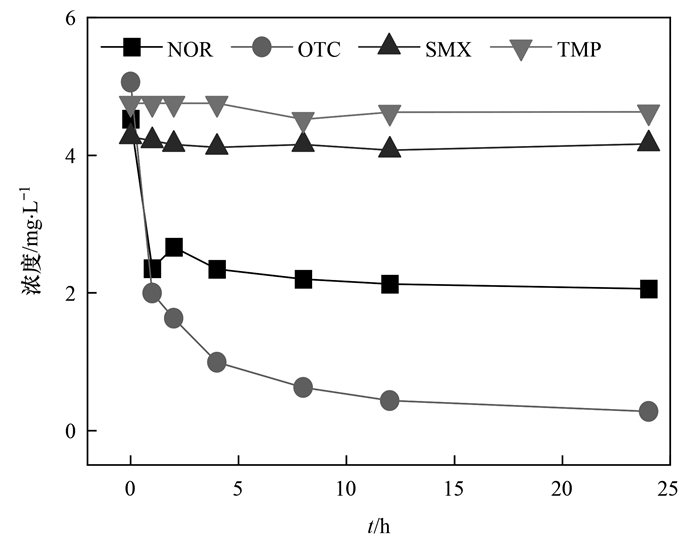
保持在反硝化体系中不外加碳源, 仅添加5 mg·L-1抗生素为反应体系中唯一有机物质, 考察了无外加碳源条件下4种抗生素的去除特性, 结果如图 3所示. SMX和TMP浓度在实验过程中几乎不发生变化, 表明SMX和TMP在实验中没有发生去除, 进一步说明两者均不能作为有机碳源被反硝化菌群利用. Suarez等[18]的研究也指出, SMX和TMP在生物处理过程中难以被降解.值得指出的是, 与碳源充足时不同(图 2), 无外加碳源时的TMP浓度保持不变, 由此可见有机碳源的存在促进了TMP的去除, 表明反硝化体系对TMP的吸附降解过程与微生物代谢作用有关.而NOR和OTC的浓度分别降至2.1 mg·L-1和0.3 mg·L-1, 去除率分别为53.3%和94.1%.由此可知, 在无外加碳源条件下, 生物降解作用在反硝化去除NOR和OTC过程中占据主导地位, 反硝化菌群能够利用NOR和OTC作为碳源进行反硝化作用, 从而导致抗生素的生物降解.
|
图 3 无外加碳源时抗生素的浓度变化 Fig. 3 Concentration variation of antibiotics without external carbon source |
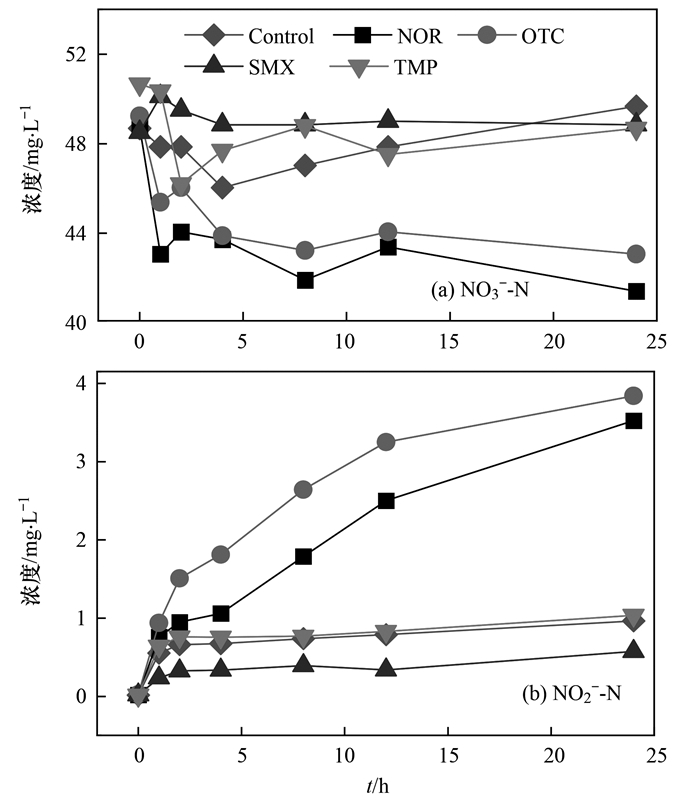
进一步测定了反应体系中NO3--N和NO2--N的浓度变化, 结果如图 4所示.加入SMX和TMP的实验结果中, NO3--N和NO2--N浓度基本没有变化.而加入NOR和OTC之后, 反应体系的硝酸盐浓度明显降低, 在反应结束时, ρ(NO3--N)从50 mg·L-1分别降低至41.4 mg·L-1和43.1 mg·L-1, 同时NO2--N随着时间的变化逐渐积累, 在24 h时累积到3.5 mg·L-1和3.8 mg·L-1, 而对照组中NO3--N和NO2--N浓度没有明显变化.这一结果证实, 加入NOR和OTC后反应体系中确实发生了反硝化反应, 反硝化菌利用NOR和OTC或其生物降解产物作为碳源进行了反硝化.
|
图 4 无外加碳源时NO3--N和NO2--N浓度变化 Fig. 4 Concentration of NO3--N and NO2--N without external carbon source |
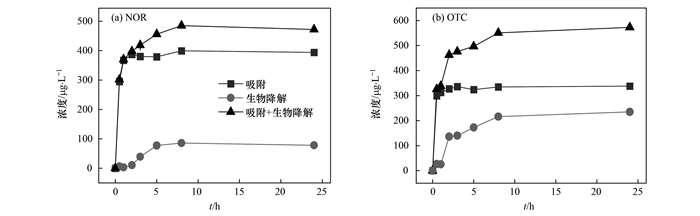
由于NOR和OTC可被反硝化菌群所利用, 而TMP和SMX难以被生物利用, 因此后续重点针对NOR和OTC的去除途径进行分析研究.在反硝化碳源充足条件下, 通过在对照组加入微生物活性抑制剂NaN3, 以完全抑制微生物活性, 对比研究了吸附和生物降解对抗生素去除的贡献率.如图 5所示, 对于NaN3抑制组, 在反应的初始1 h内, NOR和OTC都以较快速度被吸附去除, 吸附量(污泥以VSS计)分别为204 mg·g-1和173.7 mg·g-1, 之后吸附速率逐渐减慢.NOR和OTC通过吸附作用所致的去除率分别为39.4%和33.8%.这是因为吸附初期, 污泥上的吸附结合位点丰富, 吸附速度快, 随着时间的推移和吸附作用的进行, 有效结合位点减少, 吸附速率下降[19].一般认为, 抗生素会先吸附到污泥的外表面, 然后通过污泥孔隙结构进入污泥实现内部吸附, 但抗生素是有机物, 分子筛效应导致抗生素在污泥内部的吸附过程较慢[20].与吸附不同的是, 在非NaN3抑制组, NOR和OTC的生物降解过程缓慢, 且持续时间较长, 在24 h内对NOR和OTC的去除率分别为7.8%和23.5%.总体来看, 吸附和生物降解对NOR总去除量的贡献率分别为83.4%和16.5%, 对OTC去除量的贡献率分别为58.9%和44.1%.因此, 污泥对NOR和OTC的去除是先快速吸附再缓慢生物降解的过程; 吸附是反硝化体系去除抗生素的重要初始步骤, 之后再通过生物降解不断去除.
|
图 5 NOR和OTC的吸附和生物降解量随时间的变化 Fig. 5 Effect of contact time on NOR and OTC biosorption and degradation |
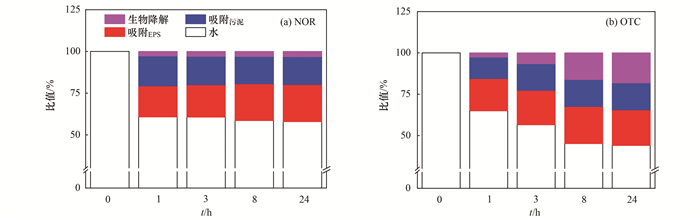
反硝化污泥对NOR和OTC都具有较强的吸附能力.胞外聚合物(EPS)作为细胞间黏合的介质, 在废水生物处理过程中对微量有机物的吸附去除具有重要作用.EPS的化学组分复杂, 包括蛋白质、多糖、核酸、腐殖质和氨基酸等, 其中蛋白质和多糖占其总量的70%以上[21], 存在多种官能团和疏水区域, 因此能够为有机物的吸附提供结合位点.有研究表明, 许多微量有机物包括抗生素都能被EPS吸附[22].为了进一步探究NOR和OTC在污泥和EPS上的吸附情况, 分别测定了水体、EPS和污泥中的抗生素含量, 结果如图 6所示.前期探索实验表明, 在所试NOR和OTC含量水平, ω(EPS)变化低于3 mg·g-1, 因此抗生素对污泥EPS产量的影响可忽略不计.NOR的分布表明, 污泥和EPS都能够吸附NOR, 初始1 h内, NOR主要被EPS吸附, EPS吸附量占总吸附量的49%.之后EPS对NOR的吸附量略有下降, 但仍然保持在43%左右; 提取EPS后的污泥对NOR的吸附比例逐渐增加, 表明被EPS吸附的NOR可能进一步进入细胞, 继而被生物降解.OTC的分布规律也显示, OTC一开始主要被吸附到EPS上, 之后逐渐释放到污泥中, EPS吸附占吸附总量的43.1%.由此可知, EPS在污泥的吸附中发挥了重要作用, 其较强的吸附能力有利于后续生物降解的进行.
|
纵坐标表示某一时刻抗生素在水体、EPS和污泥中的含量与抗生素的初始含量的比值 图 6 NOR和OTC在污泥和EPS上的吸附情况 Fig. 6 Adsorption distribution of NOR and OTC in sludge and EPS |
细胞色素P450酶普遍存在于细菌中[23], 在多种抗生素、药物的生物转化中起到重要作用[24, 25].为探究碳源充足条件下P450酶对NOR和OTC降解的贡献, 通过添加1-氨基苯并三唑(P450酶特征抑制剂), 对比研究了2种抗生素的去除情况, 结果如图 7所示.与不添加P450酶抑制剂时的去除率(NOR为54.2%, OTC为60.1%)相比, 加入P450酶抑制剂后, NOR的去除效率几乎不变; 而OTC的去除率降低了20.1%, 说明在OTC的降解中P450酶确实发挥了重要作用. P450酶是一类丰富的酶家族, 也是常见的药物降解酶, 有研究表明P450酶可以分解哌嗪基, 或者发生羟基化反应[26].但关于其对OTC的生物降解过程是否涉及反硝化或微生物共代谢机制, 尚需进一步深入研究.

|
图 7 P450酶在NOR和OTC降解中的作用 Fig. 7 Role of P450 enzyme in the biodegradation of NOR and OTC |
(1) 反硝化污泥对SMX几乎没有去除能力, 但在碳源充足时, 对NOR、OTC和TMP有一定的去除作用; 在无碳源存在的情况下, 反硝化污泥可利用NOR和OTC作为碳源进行反硝化, 去除率分别可达53.3%和94.1%.
(2) 反硝化污泥对NOR和OTC的去除是快速吸附和缓慢生物降解的过程.NOR和OTC的去除都以吸附为主, 吸附对NOR和OTC总去除量的贡献率分别为83.5%和58.9%.EPS在抗生素的吸附过程中起着重要作用, 其对NOR和OTC的吸附量均占总吸附量的40%以上.
(3) 反硝化污泥生物降解OTC的能力(23.5%)高于NOR(7.8%). P450酶在碳源充足条件下对OTC的生物降解起着重要作用, 其对生物降解的贡献率达到20%.
| [1] |
章强, 辛琦, 朱静敏, 等. 中国主要水域抗生素污染现状及其生态环境效应研究进展[J]. 环境化学, 2014, 33(7): 1075-1083. Zhang Q, Xin Q, Zhu J M, et al. The antibiotic contaminations in the main water bodies in China and the associated environmental and human health impacts[J]. Environmental Chemistry, 2014, 33(7): 1075-1083. |
| [2] | Zhu Y G, Johnson T A, Su J Q, et al. Diverse and abundant antibiotic resistance genes in Chinese swine farms[J]. Proceedings of the National Academy of Sciences of the United States of America, 2013, 110(9): 3435-3440. DOI:10.1073/pnas.1222743110 |
| [3] | Yan C X, Yang Y, Zhou J L, et al. Antibiotics in the surface water of the Yangtze Estuary: occurrence, distribution and risk assessment[J]. Environmental Pollution, 2013, 175: 22-29. DOI:10.1016/j.envpol.2012.12.008 |
| [4] | Ashfaq M, Li Y, Wang Y W, et al. Occurrence, fate, and mass balance of different classes of pharmaceuticals and personal care products in an anaerobic-anoxic-oxic wastewater treatment plant in Xiamen, China[J]. Water Research, 2017, 123: 655-667. DOI:10.1016/j.watres.2017.07.014 |
| [5] |
王大鹏, 张娴, 颜昌宙. 4种磺胺类药物及乙酰化代谢物在污水处理厂的去除及机制[J]. 环境科学, 2019, 40(3): 1347-1352. Wang D P, Zhang X, Yan C Z. Removal efficiencies and mechanism research on four sulfonamides and their acetyl metabolites in a wastewater treatment plant[J]. Environmental Science, 2019, 40(3): 1347-1352. |
| [6] |
代莎, 李彭, 彭五庆, 等. 抗生素对耐药型反硝化菌反硝化过程及微生物群落结构的影响[J]. 环境科学, 2020, 41(3): 1401-1408. Dai S, Li P, Peng W Q, et al. Influence of antibiotics on the denitrification process of antibiotic resistant denitrifying bacteria and the analysis of microbial community structure[J]. Environmental Science, 2020, 41(3): 1401-1408. |
| [7] | 赵亚奇. A/O-MBR工艺对废水中抗生素的去除效能研究[D]. 哈尔滨: 哈尔滨工业大学, 2017. |
| [8] | 邓红娜. 好氧颗粒污泥处理含磺胺甲恶唑污水效能研究[D]. 哈尔滨: 哈尔滨商业大学, 2020. |
| [9] | 赵霞. 好氧颗粒污泥系统处理含PPCPs污水的效能及微生物群落演替[D]. 哈尔滨: 哈尔滨工业大学, 2015. |
| [10] | Hutchins S R, Sewell G W, Kovacs D A, et al. Biodegradation of aromatic hydrocarbons by aquifer microorganisms under denitrifying conditions[J]. Environmental Science & Technology, 1991, 25(1): 68-76. |
| [11] | Moussavi G, Jafari S J, Yaghmaeian K. Enhanced biological denitrification in the cyclic rotating bed reactor with catechol as carbon source[J]. Bioresource Technology, 2015, 189: 266-272. DOI:10.1016/j.biortech.2015.04.019 |
| [12] | Tezel U, Pavlostathis S G. Transformation of benzalkonium chloride under nitrate reducing conditions[J]. Environmental Science & Technology, 2009, 43(5): 1342-1348. |
| [13] | Li X Y, Yang S F. Influence of loosely bound extracellular polymeric substances (EPS) on the flocculation, sedimentation and dewaterability of activated sludge[J]. Water Research, 2007, 41(5): 1022-1030. DOI:10.1016/j.watres.2006.06.037 |
| [14] | Min X B, Li W, Wei Z S, et al. Sorption and biodegradation of pharmaceuticals in aerobic activated sludge system: a combined experimental and theoretical mechanistic study[J]. Chemical Engineering Journal, 2018, 342: 211-219. DOI:10.1016/j.cej.2018.01.012 |
| [15] | Li B, Zhang T. Biodegradation and adsorption of antibiotics in the activated sludge process[J]. Environmental Science & Technology, 2010, 44(9): 3468-3473. |
| [16] | Xu J, Sheng G P, Ma Y, et al. Roles of extracellular polymeric substances (EPS) in the migration and removal of sulfamethazine in activated sludge system[J]. Water Research, 2013, 47(14): 5298-5306. DOI:10.1016/j.watres.2013.06.009 |
| [17] | Meng F G, Gao G H, Yang T T, et al. Effects of fluoroquinolone antibiotics on reactor performance and microbial community structure of a membrane bioreactor[J]. Chemical Engineering Journal, 2015, 280: 448-458. DOI:10.1016/j.cej.2015.06.025 |
| [18] | Suarez S, Lema J M, Omil F. Removal of pharmaceutical and personal care products (PPCPs) under nitrifying and denitrifying conditions[J]. Water Research, 2010, 44(10): 3214-3224. DOI:10.1016/j.watres.2010.02.040 |
| [19] | Wei D, Li M T, Wang X D, et al. Extracellular polymeric substances for Zn (Ⅱ) binding during its sorption process onto aerobic granular sludge[J]. Journal of Hazardous Materials, 2016, 301: 407-415. DOI:10.1016/j.jhazmat.2015.09.018 |
| [20] | Ji L L, Chen W, Duan L, et al. Mechanisms for strong adsorption of tetracycline to carbon nanotubes: a comparative study using activated carbon and graphite as adsorbents[J]. Environmental Science & Technology, 2009, 43(7): 2322-2327. |
| [21] |
钱飞跃, 王琰, 王建芳, 等. 好氧颗粒污泥中凝胶型聚多糖的特性研究进展[J]. 化学通报, 2015, 78(4): 320-324. Qian F Y, Wang Y, Wang J F, et al. Advances in the study on gel-forming property of exopolysaccharides isolated from aerobic granular sludge[J]. Chemistry, 2015, 78(4): 320-324. |
| [22] | Sheng G P, Yu H Q, Li X Y. Extracellular polymeric substances (EPS) of microbial aggregates in biological wastewater treatment systems: a review[J]. Biotechnology Advances, 2010, 28(6): 882-894. DOI:10.1016/j.biotechadv.2010.08.001 |
| [23] | Sheng G P, Yu H Q, Yue Z B. Production of extracellular polymeric substances from Rhodopseudomonas acidophila in the presence of toxic substances[J]. Applied Microbiology and Biotechnology, 2005, 69(2): 216-222. DOI:10.1007/s00253-005-1990-6 |
| [24] | Mir-Tutusaus J A, Masís-Mora M, Corcellas C, et al. Degradation of selected agrochemicals by the white rot fungus Trametes versicolor[J]. Science of the Total Environment, 2014, 500-501: 235-242. DOI:10.1016/j.scitotenv.2014.08.116 |
| [25] | Gao N, Liu C X, Xu Q M, et al. Simultaneous removal of ciprofloxacin, norfloxacin, sulfamethoxazole by co-producing oxidative enzymes system of Phanerochaete chrysosporium and Pycnoporus sanguineus[J]. Chemosphere, 2018, 195: 146-155. DOI:10.1016/j.chemosphere.2017.12.062 |
| [26] | Jia Y Y, Khanal S K, Shu H Y, et al. Ciprofloxacin degradation in anaerobic sulfate-reducing bacteria (SRB) sludge system: Mechanism and pathways[J]. Water Research, 2018, 136: 64-74. DOI:10.1016/j.watres.2018.02.057 |
 2022, Vol. 43
2022, Vol. 43



 唑
唑