2. 南京信息工程大学气象灾害预报预警与评估协同创新中心, 气象灾害教育部重点实验室, 南京 210044
2. Key Laboratory of Meteorological Disaster, Ministry of Education (KLME), Collaborative Innovation Center on Forecast and Evaluation of Meteorological Disasters (CIC-FEMD), Nanjing University of Information Science & Technology, Nanjing 210044, China
空气质量是影响人口健康的一个重要问题, 大量流行病学和毒理学研究表明, 环境颗粒物(PM)暴露与人类健康不良影响之间存在关系, 主要是呼吸道和心血管疾病[1~3].迄今为止, 已提出可靠度较高的病理生理机制均涉及活性氧(reactive oxygen species, ROS)的生成, 活性氧可激活许多条氧化还原信号通路, 触发一系列与炎症和潜在细胞凋亡相关的事件[1, 3~8], 氧化潜势(OP)被定义为粒子消耗生理抗氧化剂(还原剂)并具有生成活性氧的能力.OP被提议作为一种比PM浓度更具生物相关性的指标, 以代表PM中多种有毒成分的综合效应[9~11].目前常见的脱细胞OP分析包括电子自旋(或顺磁)共振(ESR)、二硫苏糖醇分析(DTT)、抗坏血酸分析(AA)和谷胱甘肽分析(GSH).相比而言, DTT方法的发展比较迅速, 一般认为DTT法是最能全面反映颗粒物化学氧化潜势大小的方法[3, 12, 13].
近年来, 国内外很多学者开始关注大气环境颗粒物氧化电位的研究, 发现腐植酸(HULIS)[14, 15]、过渡金属(Fe、Cu、Mn)[16~18]和有机碳(OC)[19~21]在颗粒物质中对氧化潜势的大小有明显的影响. 由此可见, 各区域颗粒物氧化潜势的大小与各区域大气颗粒物化学成分的不同密切相关.保定市作为京津冀地区的交界地带, 近年来经济快速发展, 大气环境仍然存在明显的污染.而针对京津冀地区氧化潜势的研究数量较少, 本研究基于DTT法模拟人体肺液环境, 测定了保定市的氧化潜势, 分析了大气中各化学组分对氧化潜势的影响, 并且利用PMF模型对影响氧化潜势特征的污染类型进行分析, 以期为精确的控制污染提供理论依据.
1 材料与方法 1.1 采样地点在保定市固城镇(115.74°E, 39.16°N), 固城的观测点位于中国气象科学研究院生态农业气象试验站.采样期为2018年11月13日至12月6日, 区分白天(07:30~18:00)和夜间(18:00~次日07:30), 总共采样50个.采样使用的石英滤膜需要用锡纸提前包被, 在马弗炉中450℃燃烧6 h, 去除杂质.正式采样时, 通过大流量PM2.5空气采样器以1.0 m3·min-1的流速采集颗粒物样品, 再将最终样品保存在-26℃的冰箱中, 防止挥发性物质损失.
1.2 PM2.5样品中的离子、糖类化合物、水溶性金属、有机碳和元素碳分析水溶性无机离子(NO3-、SO42-、NH4+、Cl-、Na+、K+和Ca2+)由离子色谱仪(ICS 5000+, Thermo Scientific, USA)测定.将一片面积为2.54 cm2的取样过滤器浸入装有15 mL超纯水的小瓶中, 密封超声处理30 min进行提取.所有离子的方法检出限(MDL)和回收率分别处于0.03~0.41 ng·m-3和90%~110%的范围内, 精密度小于2%.
糖类化合物(左旋葡聚糖、甘露聚糖和半乳聚糖), 本研究使用ICS-5000+型离子色谱仪检测大气颗粒物中糖类化合物含量.离子色谱仪的检测单元为电化学检测器.分离系统为Dionex CarboPac MA1保护柱与分析柱.为更准确地分离并检测糖类, 全部样品通过两套NaOH梯度淋洗方案淋洗, 流速均设置为0.4 mL·min-1, 样品注射回路体积为200 μL.
水溶性金属(Fe、Cu和Mn), 通过电感耦合等离子体质谱仪(ICP-OES, PerkinElmer公司, 美国)进行分析.切直径16mm的膜两张, 加入10 mL超纯水, 振荡30 min, 再用0.22 μm的滤头过滤后即可进样, 并通过电感耦合等离子体质谱法分析23种目标金属[22].电感耦合等离子体质谱法的金属输出浓度单位为ng·mL-1.水溶性金属的浓度通过以下公式从ng·mL-1转换为ng·m-3:
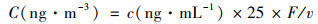
|
(1) |
式中, F为每个气溶胶样品中提取的过滤面积与总采样过滤面积的比率, v为每个气溶胶样品中的采样空气量(m3).通过对NIST SRM 1648(城市颗粒物)的分析来确保质量保证/质量控制.该方法每种元素的精密度小于2%, 回收率在93%~116%范围内.所有元素的检出限为0.01~2.09 ng·m-3.
使用半连续碳分析仪(型号4, Sunset Lab. Inc. USA)进行碳分析.在310、480、615℃、870、0和550℃的氦气环境(99.99%He)以及550、625、700、775、850和870℃的氧化性环境(1%O2+99%He)中逐步加热2.27 cm2穿孔过滤器, 以获得OC和EC浓度.检测限约为0.20 μg·m-3.在分析样品之前, 用已知量的蔗糖校准分析仪.碳的回收率为98%, 精密度为4%.
1.3 氧化潜势的评估首先, 将采集样品进行萃取处理, 切割2份直径16 mm的样品膜放入棕色玻璃瓶中, 加入5 mL超纯水振荡30 min, 利用0.22 μm PTFE注射式过滤器过滤以去除不溶物质.然后, 取1.5 mL样品溶液和5 mL 0.1 mol·L-1的磷酸钾溶液(71.8 mmol·L-1磷酸氢二钾+28.2 mmol·L-1磷酸二氢钾, 配好后将pH调至7.4)混合在一个15 mL混合瓶中.加入0.5 mL的100 μmol·L-1 DTT加入到反应混合物中, 并放在37℃、转速250 r·min-1的恒温振荡器(THZ-D, 苏州培英实验设备有限公司)中反应.在指定的时间间隔(0、10、20、30和40 min), 依次取出0.5 mL反应混合物, 转移到另一个装有0.5 mL 10%(质量浓度)三氯乙酸(TCA)的反应瓶中, 用于终止DTT和样品溶液之间的反应.接下来, 加入50 μL 0.1 mmol·L-1 DTNB[5, 5′-二硫代双(2-硝基苯甲酸)]与溶液中剩余的DTT进行反应.最后, 加入2 mL 0.4 mol·L-1 Tris缓冲液(0.4 mol·L-1 Tris+20 mmol·L-1的EDTA, 配好后将pH调至8.9).利用分光光度计检测波长为412 nm的条件下的吸光度, 分光光度计由一个紫外可见(UV-VIS)光源(海洋光学DT-mini-2)和一个多波长光检测器(USB4000微型光纤光谱仪)组成.使用数据采集软件(Spectra Suite)记录412和700 nm处的吸光度强度(选择作为TNB的基线吸光度).
测试得到的吸光度数据需要进行斜率计算处理得到DTT消耗速率(r), 经体积归一化和质量归一化计算得到DTTv[nmol·(min·m3)-1]和DTTm[pmol·(min·μg)-1], 其计算公式如下:
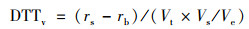
|
(2) |
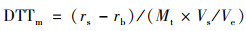
|
(3) |
式中, rs为样品的DTT消耗速率(nmol·min-1), rb为空白的DTT消耗速率(nmol·min-1), Vt为样品对应的采样体积(m3), Mt为样品对应的PM2.5浓度(μg·m-3), Vs为进样体积(mL), Ve为采样体积(mL). DTTv为每单位体积大气颗粒物对DTT的消耗速率, 一般认为该值与人体健康有关. DTTm为单位质量颗粒物的DTT消耗速率, 被认为是衡量环境颗粒物固有的氧化潜势的指标[23, 24].
1.4 质量控制在采样过程中, 为去除滤膜中有机杂质对分析的影响.在不开仪器的条件下收集1张空白膜样品作为野外空白样品, 滤膜在恒温恒湿的天平室中称重(精确到0.1 mg, 采样后滤膜两次称重误差小于0.5 mg).
水溶性离子浓度测定后均进行空白校正, 扣除采样、操作过程带入的污染, 即样品值减去空白值, 测标准样品(浓度为0.05、0.1、0.2、0.5、1、2、5和10 ng·L-1), 制作标准曲线时保证各种离子的峰面积与浓度之间的相关系数在99.9%以上, 标准曲线满足要求后进行测样.
在利用半连续碳分析仪进行有机碳和元素碳分析时, 每次样品分析结束后, 仪器都会通入定量的氦气/甲烷(He/CH4)标气, 用CH4标准峰来定量样品分析结果和校正NDIR在每次样品分析过程中可能发生的漂移.测样开始前和结束后用标准蔗糖溶液进行外标校正, 采用内外标联合校正确保仪器具有较高的精准度, 其检出限为0.5 μg·m-3.分析样品过程进行空白校正.
在进行氧化潜势评估实验时, 通过测量不同浓度下DTT(0、1、2、5、10、15、20、25、50、75和100 μg·L-1)的消耗速率进行标准曲线的绘制, 制作标准曲线相关系数在99.9%以上, 可以进行测样.每次测样之前进行空白检测, 以消除空白干扰.
1.5 其他数据来源气象数据来源于国控数据保定市地面气象站点.
1.6 污染源分析PMF模型基于受体点的化学组分浓度估算排放源的组成和对有机物浓度的贡献.本研究使用的是由美国环境保护局开发的PMF5.0对冬季DTTv进行来源解析.

|
(4) |
式中, xij为在第i个样品中测量的第j个化学成分的浓度, gki为第k个因子对第i个样品贡献率, fkj为第k个因子中第j种化学成分的含量, eij为实测值和模型估值的残差, n为因子的总数.如果输入元素的浓度大于其检测限(MDL), 则不确定度(Unc)按下式计算:

|
(5) |
式中, EF为求积相加的相对误差分数(5%).如果浓度小于检出限(MDL), 则浓度为检出限的一半, 其不确定度为检出限的5/6.
2 结果与讨论 2.1 气象数据和化学物质浓度变化在采样期间, 环境温度的平均值为(1.8±3.9)℃, 范围为-5~9℃; 相对湿度的平均值为(65.3±23.8)%, 范围为19%~98%(图 1).风速从0~4.3 m·s-1, 平均值为(1.3±1.1)m·s-1.气压相对稳定保持在102 kPa左右.能见度从0.5~22 km, 平均值为(9.4±6.5)km.在能见度较低的天气明显呈现出相对湿度较高和风速较低的现象, 表明冬季平静条件(风速 < 1 m·s-1)和潮湿空气是形成雾和霾的重要因素[25, 26].

|
图 1 2018年采样期间气象数据日变化 Fig. 1 Daily changes in meteorological data during the sampling period in 2018 |
保定市ρ(PM2.5)的平均值为(140.96±70.67)μg·m-3, 颗粒物浓度远高于同时期的北京地区[27] [(67.29±61.89) μg·m-3].白天和夜间并无明显的区别.表 1显示了本实验测定的水溶性组分(Na+、NH4+、K+、Mg2+、Ca2+、Cl-、NO3-和SO42-)、水溶性金属(Fe、Cu和Mn)、OC、EC、TC和糖类化合物(左旋葡聚糖、甘露聚糖和半乳聚糖)的昼夜平均值.保定市的ρ(OC)、ρ(EC)和ρ(TC)平均值分别为(36.09±16.64)、(3.56±1.82)和(39.65±18.14)μg·m-3, 明显高于同时期北京地区浓度[ρ(OC)和ρ(EC)分别为(17.88±12.25)、(1.77±1.32)和(30.53±11.09) μg·m-3][15].OC有两个主要来源, 一是化石燃料燃烧直接排放到大气中形成的一次有机气溶胶, 二是经过化学反应生成的二次有机气溶胶, 而EC的主要来源于化石燃料的不完全燃烧.根据表 1, 本文发现OC、EC和TC浓度夜间明显高于日间.与此同时, 还发现糖类化合物(左旋葡聚糖、甘露聚糖和半乳聚糖)的浓度同样表现出夜间明显高于日间的现象.左旋葡聚糖、甘露聚糖和半乳聚糖作为典型的生物质燃烧的示踪物, 这一点也符合保定郊区冬季利用生物质燃烧取暖的现状.另外, 保定市水溶性离子平均值大小为: NO3->NH4+>SO42->Cl->Ca2+>K+>Mg2+>草酸根>Na+, 最高的ρ(NO3-)平均值为(23.20+16.73)μg·m-3.本实验还测量了保定市大气中与气溶胶毒性相关的3种过渡金属[28], 包括Fe、Cu和Mn, 由表 1可知, 在保定市的大气金属浓度中, Fe的浓度最高, Cu的浓度其次, Mn的浓度最低, 这一点与亚特兰大地区[29]的Cu和Fe明显高于Mn的报道相同. ρ(Fe)在保定市地区并无明显昼夜差别, 全天的平均值为: (81.16±39.88)ng·m-3.在大气中ρ(Cu)仅为(4.83±3.05)ng·m-3, 但存在一定的昼夜差异, 白天明显高于晚上.Mn浓度最低, 并且存在明显的昼夜差异, 在白天ρ(Mn)为(2.06±2.42)ng·m-3, 晚上ρ(Mn)为(1.54±1.35)ng·m-3.
|
|
表 1 PM2.5化学成分的平均值 Table 1 Average concentration of PM2.5 chemical composition |
2.2 保定市氧化潜势的特征分布
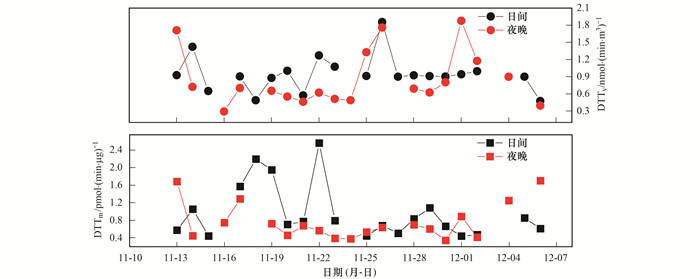
利用DTT法测量了保定市地区大气样品的氧化潜势(OP), 通过体积归一化氧化潜势DTTv和质量归一化氧化潜势DTTm作为吸入空气的暴露指标, 来表征粒子耗尽相关抗氧化剂的内在能力.观测期间, 保定市的DTTv和DTTm日变化如图 2所示, DTTv在白天和夜间分别是(2.37±0.76)nmol·(min·m3)-1和(2.14±1.17)nmol·(min·m3)-1, DTTm在白天和夜间分别是(0.96±0.60)pmol·(min·μg)-1和(0.76±0.41)pmol·(min·μg)-1.由此可见, 无论是DTTv还是DTTm, 白天的相关数值均高于夜间, 这表明白天的大气环境更有利于活性氧的生成和存活.与北京2012年春季时[30]的DTTv[城区: 0.24 nmol·(min·m3)-1, 郊区: 0.19 nmol·(min·m3)-1]和浙江大学[31]全年的DTTv平均值0.62 nmol·(min·m3)-1相比, 本实验结果偏高; 与北京大学[32] 2015年全年的DTTv平均值[(12.26±6.82) nmol·(min·m3)-1]和DTTm平均值[(130±100)pmol·(min·μg)-1], 以及广州[33]在2017年冬季[DTTv: (4.67±1.06) nmol·(min·m3)-1, DTTm: (13.47±3.86) pmol·(min·μg)-1]和2018年春季的[DTTv: (4.45±1.02)nmol·(min·m3)-1, DTTm: (14.66±4.49)pmol·(min·μg)-1]相比, 本实验值偏低, 这可能与当时的季节和排放因素有关.如图 2所示, 在严重污染期间, DTTv的值也相应显示高值, 但DTTm没有这种趋势, 表明颗粒物中的物质并非都能引发活性氧的产生, 并改变氧化潜势.
|
图 2 2018年观测期间保定市的DTTv和DTTm时间序列 Fig. 2 Time series of DTTv and DTTm in Baoding during the observation period in 2018 |
通过计算OP响应与实测环境参数之间的线性回归, 确定了气象特征(大气压、湿度、温度和能见度)和PM化学成分对氧化潜势的影响.如表 2所示, 在白天和夜晚DTTv与温度无显著相关, DTTv与相对湿度(RH)、大气压和风速有一定的关系.保定市夜晚的湿度与DTTv相关性更强(r=0.702, P<0.01).这一点与Perrone等[34]的研究结果一致, 在一定相对湿度范围中下, RH是影响了DTTv的大小.然而, 大气压与DTTv呈现明显的负相关(r=-0.458, P<0.01), 尤其是夜晚(r=-0.611, P<0.01), 可能是由于冬季夜晚大气层结稳定, 边界层高度低, 降水少, 污染物易于积聚累积.这些结果表明, 气象参数与DTTv值的高相关性可能分别与低风速、大气压和湿度有利于形成粒子有关, 而对大气的温度有利于形成的颗粒不太敏感[35~37].
|
|
表 2 DTTv与气象参数的皮尔逊相关系数1) Table 2 Correlation analysis between DTTv and meteorological parameters |
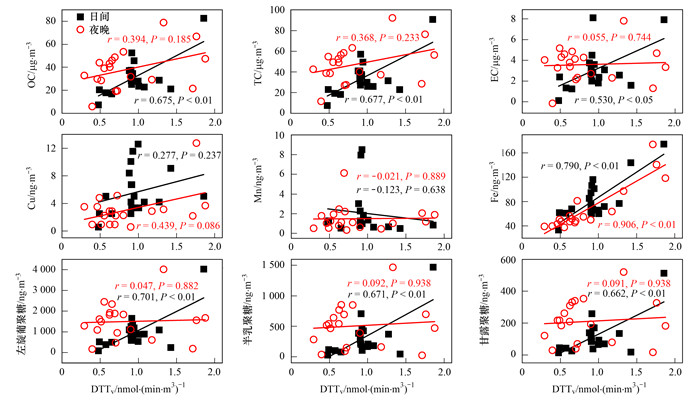
为了更好地研究昼夜氧化潜势和PM化学成分之间的联系, 应用简单线性回归(图 3中的皮尔逊相关系数r)研究特定PM2.5组分对氧化潜势的贡献.总的来说, DTTv响应在显著性水平P < 0.05上与18种物种广泛相关, 即OC、EC、TC, 金属(如Cu、Fe、Mn), 糖类化合物以及水溶性无机成分. Calas等[35]的研究指出夏蒙尼市(法国)PM2.5样品的OP响应和化学成分出现类似的结果.根据昼夜性(即白天和夜晚)对数据进行的区分, 清楚地显示了相关系数的昼夜差异性, 表明昼夜变化对DTTv的影响.
分析表明: OC、EC和TC在白天与DTTv存在明显的相关性(r=0.675, P < 0.01; r=0.530, P < 0.05; r=0.676, P < 0.01), 而夜晚OC、EC和TC并不存在相关性.这可能是昼夜气象条件的不同造成的.温度、湿度和光照对二次气溶胶的形成、半挥发性气溶胶浓度的变化和雾的形成起着重要作用.这些过程可以改变颗粒物组分的化学性质, 从而改变它们的DTT活性.除此之外, 作为生物质燃烧示踪物的左旋葡聚糖、甘露聚糖和半乳聚糖与DTTv昼夜相关性差异更加明显, 白天左旋葡聚糖、甘露聚糖和半乳聚糖与DTTv存在较强相关性(r=0.701, P < 0.01; r=0.671, P < 0.01;r=0.662, P < 0.01;)这与早期研究有机化合物催化DTT氧化的能力一致[38, 39], 这也表明生物质或化石燃料燃烧对DTTv活性的具体影响.
大气中Mn的来源主要是矿物粉尘, 而水溶性Cu和Fe具有更强的交通源(车辆制动, 车辆排放).如图 3所示, Cu和Mn在白天和夜晚与DTTv无明显相关性, 这是因为Cu与DTT反应形成络合物, 作为催化剂氧化游离DTT而不产生任何ROS[40, 41].由于Mn并不参与活性氧生成, 因此与DTTv未呈现明显的相关性.相反, 金属Fe与DTTv在白天和夜晚有着明显的相关性(白天: r=0.790, P < 0.01; 夜晚: r=0.904, P < 0.01).造成这种现象的原因, Xiong等[14]的研究认为单一的水溶性Fe并不能对DTTv做出贡献, 但是在酸性环境下与有机物发生协同反应(Fenton反应)参与活性氧的生成.然而, 通过观察SO42-的昼夜浓度也很好地验证了这一点.
|
图 3 化学成分与DTTv相关性分析 Fig. 3 Correlation analysis of chemical composition and DTTv |
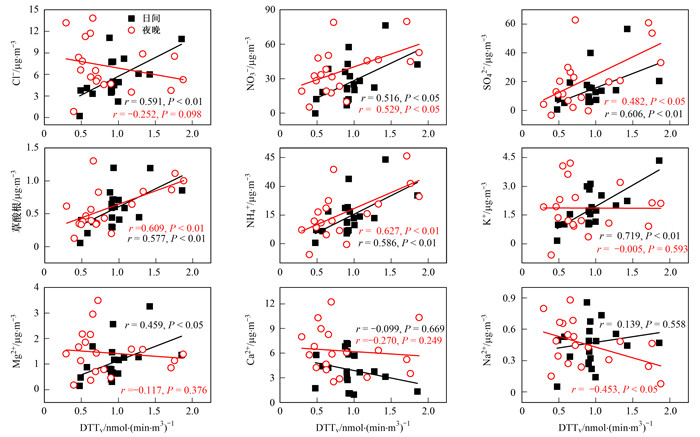
在本研究中发现, 次级无机离子(NO3-、SO42-和NH4+)也与DTTv活性之间有很强的相关性(图 4). Cho等[23]的研究指出这些物质对DTT活性并没有实际贡献.如表 3显示, NO3-、SO42-和NH4+与水溶性Fe相关(r>0.65, P < 0.01), 进一步表明它们与水溶性Fe的共线性, 而不是对DTT活性的实际贡献, 这一点与Verma等[21]的研究结果一致.草酸根作为光化学氧化有机前体物的二次排放生成物质[42], 在白天和夜晚均与DTTv有着明显的相关性, 草酸根昼夜相关性都较强(r=0.609和r=0.577, P < 0.01), 表明DTT活性可能与大气中光化学氧化途径和二次污染有关.另外, Cl-、K+和Mg2+仅仅在白天与DTTv呈现相关性(r=0.591, P < 0.01; r=0.719, P < 0.01; r=0.459, P < 0.05), 这与Liu等[43]在渤海沿岸城市的研究结果相同, 很显然, 这是因为华北地区冬季燃煤导致的.Mg2+和Ca2+是常见的地壳金属, 大气颗粒物中其来源是扬尘.为此, 本研究考察了扬尘对DTTv影响, 发现采样期间的Mg2+和Ca2+浓度并不高, 采样期间低风速也很好地验证了这一点, 并且Mg2+和Ca2+与DTTv相关性不高.说明冬季保定市活性氧的生成与扬尘关系较小.
|
图 4 化学成分与DTTv相关性分析 Fig. 4 Correlation analysis of chemical composition and DTTv |
|
|
表 3 NO3-、SO42-和NH4+与其他物质之间的皮尔逊相关系数1) Table 3 Pearson correlation coefficient between NO3-, SO42-, and NH4+ and other substances |
2.4 PMF来源解析
为了进一步了解影响氧化潜势的污染来源, 采用PMF模型直接对DTTv进行源解析[33].在本研究中, 分解了3~7个因子, 并计算每个解的Qtrue/Qexpected值, 以确定PMF模型的最佳解.当分解因子从3增加到7时, Qtrue/Qexpected比值从3.63减少到0.35.从4个因子到5个因子, Qtrue/Qexpected比值下降了1.24.相反, 从5个因子到6个因子Qtrue/Qexpected值下降0.62, 说明拟合因子过多.因此, 在这种情况下, 5个因子是最佳的解决方案.所有污染源贡献率如图 5所示.

|
图 5 各个污染源对DTTv的贡献率 Fig. 5 Contribution rate of each pollution source to PM2.5 |
图 6为PMF解析出的污染源贡献, 共确定5种可能的排放源, 即次生来源、生物质燃烧源、扬尘、矿物粉尘及工业来源和交通源.因子1被确定为次生来源, 主要以NO3-、SO42-、NH4+和草酸根为代表, 二次辐射源来源于一系列的大气反应, 而不仅仅是局部的表面辐射过程.一些已确定的来源, 如生物质燃烧、煤炭燃烧以及工业和车辆排放物, 可能通过其前体成分(如NOx、SO2和VOCs)的排放通过光氧化或降解而形成二次无机和有机气溶胶.次生来源对氧化潜势的贡献为29.9%, 是保定市最主要的氧化潜势生成源.因子2具有OC、EC、TC、K+、Cl-和左旋葡聚糖高浓度的特点, 这些物种是典型的生物质燃烧和煤燃烧的示踪物[44, 45], 该因子对氧化潜势生成的贡献率29.2%.由于采样地区位于华北地区, 时值冬季, 煤炭燃烧是大气污染物的重要排放源.因子3被确定为扬尘, Ca2+和Mg2+浓度过高, 与地壳尘埃密切相关.该因子对氧化潜势的贡献最小, 仅为11.2%.因子4被确定为矿物粉尘及工业来源, 具有高浓度Mn和Ca2+的特点.由于保定郊区监测点附近并没有大型工厂等设施, 该污染源对氧化潜势的贡献率最小, 仅为8.6%.因子5被确定为交通源, 特征为Cu和Fe浓度较高, Cu和Fe是车辆制动, 车辆排放最明显的示踪物, 该因子对氧化潜势生成的贡献为21.1%.

|
1.DTTv, 2. PM2.5, 3.OC, 4.EC, 5. Cu, 6.Fe, 7.Mn, 8.NO3-, 9. SO42-, 10.NH4+, 11.K+, 12. Ca2+, 13. Cl-, 14.Mg2+, 15.Na+, 16.草酸根, 17.TC, 18.左旋葡聚糖 图 6 保定市冬季采样期间DTTv污染来源解析因子 Fig. 6 Resolved factors of DTTv pollution sources during the winter sampling period in Baoding City |
(1) 基于DTT法测定了保定市的PM2.5昼夜氧化潜势, 无论是DTTv还是DTTm, 白天值均高于夜间, 这表明白天的大气环境更有利于活性氧的生成和存活.在严重污染期间, DTTv的值也相应显示高值, 但DTTm没有这种趋势, 表明并非颗粒物中的所有物质都能引发活性氧的产生, 并由此改变氧化潜势.
(2) DTTv与PM2.5中各化学成分和污染性气体的昼夜相关性存在明显差别, 可能是由气象条件的昼夜差异造成的.温度、湿度和光照对二次气溶胶的形成、半挥发性气溶胶浓度的变化和雾的形成起着重要作用.这些过程可以改变颗粒物组分的化学性质, 从而改变它们的DTT活性.
(3) 本研究还利用PMF模型, 分析了不同污染源对氧化潜势生成的贡献.污染类型主要包括次生来源(贡献率为29.9%)、生物质燃烧(贡献率29.2%)、扬尘(贡献率为11.2%)、矿物粉尘及工业来源(贡献率为8.6%)和交通源(贡献率为21.1%).
| [1] | Delfino R J, Sioutas C, Malik S. Potential role of ultrafine particles in associations between airborne particle mass and cardiovascular health[J]. Environmental Health Perspectives, 2005, 113(8): 934-946. DOI:10.1289/ehp.7938 |
| [2] | Pöschl U, Shiraiwa M. Multiphase chemistry at the atmosphere-biosphere interface influencing climate and public health in the anthropocene[J]. Chemical Reviews, 2015, 115(10): 4440-4475. DOI:10.1021/cr500487s |
| [3] | Ghio A J, Carraway M S, Madden M C. Composition of air pollution particles and oxidative stress in cells, tissues, and living systems[J]. Journal of Toxicology and Environmental Health Part B: Critical Reviews, 2012, 15(1): 1-21. DOI:10.1080/10937404.2012.632359 |
| [4] | Borm P J A, Kelly F, Künzli N, et al. Oxidant generation by particulate matter: from biologically effective dose to a promising, novel metric[J]. Occupational & Environmental Medicine, 2007, 64(2): 73-74. |
| [5] | Akhtar U S, Mcwhinney R D, Rastogi N, et al. Cytotoxic and proinflammatory effects of ambient and source-related particulate matter (PM) in relation to the production of reactive oxygen species (ROS) and cytokine adsorption by particles[J]. Inhalation Toxicology, 2010, 22(S2): 37-47. |
| [6] | Lodovici M, Bigagli E. Oxidative stress and air pollution exposure[J]. Journal of Toxicology, 2011, 2011. DOI:10.1155/2011/487074 |
| [7] | Delfino R J, Staimer N, Tjoa T, et al. Airway inflammation and oxidative potential of air pollutant particles in a pediatric asthma panel[J]. Journal of Exposure Science & Environmental Epidemiology, 2013, 23(5): 466-473. |
| [8] | Ahmad M, Yu Q, Chen J, et al. Chemical characteristics, oxidative potential, and sources of PM2.5 in wintertime in Lahore and Peshawar, Pakistan[J]. Journal of Environmental Sciences, 2021, 102: 148-158. DOI:10.1016/j.jes.2020.09.014 |
| [9] | Ayres J G, Borm P, Cassee F R, et al. Evaluating the toxicity of airborne particulate matter and nanoparticles by measuring oxidative stress potential--a workshop report and consensus statement[J]. Inhalation Toxicology, 2008, 20(1): 75-99. DOI:10.1080/08958370701665517 |
| [10] | Hellack B, Quass U, Nickel C, et al. Oxidative potential of particulate matter at a German motorway[J]. Environmental Science Processes & Impacts, 2015, 17(4): 868-876. |
| [11] | Janssen N A H, Strak M, Yang A L E, et al. Associations between three specific a-cellular measures of the oxidative potential of particulate matter and markers of acute airway and nasal inflammation in healthy volunteers[J]. Occupational and Environmental Medicine, 2015, 72(1): 49-56. DOI:10.1136/oemed-2014-102303 |
| [12] | Bates J T, Fang T, Verma V, et al. Review of acellular assays of ambient particulate matter oxidative potential: methods and relationships with composition, sources, and health effects[J]. Environmental Science & Technology, 2019, 53(8): 4003-4019. |
| [13] | Hedayat F, Stevanovic S, Miljevic B, et al. Review-evaluating the molecular assays for measuring the oxidative potential of particulate matter[J]. Chemical Industry and Chemical Engineering Quarterly, 2015, 21(1-2): 201-210. DOI:10.2298/CICEQ140228031H |
| [14] | Xiong Q S, Yu H R, Wang R R, et al. Rethinking dithiothreitol-based particulate matter oxidative potential: measuring dithiothreitol consumption versus reactive oxygen species generation[J]. Environmental Science & Technology, 2017, 51(11): 6507-6514. |
| [15] | Xu X Y, Lu X H, Li X, et al. ROS-generation potential of Humic-like substances (HULIS) in ambient PM2.5 in urban Shanghai: association with HULIS concentration and light absorbance[J]. Chemosphere, 2020, 256. DOI:10.1016/j.chemosphere.2020.127050 |
| [16] | Fang T, Guo H Y, Zeng L H, et al. Highly acidic ambient particles, soluble metals, and oxidative potential: a link between sulfate and aerosol toxicity[J]. Environmental Science & Technology, 2017, 51(5): 2611-2620. |
| [17] | Li Y, Zhu T, Zhao J C, et al. Interactive enhancements of ascorbic acid and iron in hydroxyl radical generation in quinone redox cycling[J]. Environmental Science & Technology, 2012, 46(18): 10302-10309. |
| [18] | Charrier J G, Anastasio C. On dithiothreitol (DTT) as a measure of oxidative potential for ambient particles: evidence for the importance of soluble transition metals[J]. Atmospheric Chemistry and Physics, 2012, 12(19): 9321-9333. DOI:10.5194/acp-12-9321-2012 |
| [19] | Dou J, Lin P, Kuang B Y, et al. Reactive oxygen species production mediated by humic-like substances in atmospheric aerosols: enhancement effects by pyridine, imidazole, and their derivatives[J]. Environmental Science & Technology, 2015, 49(11): 6457-6465. |
| [20] | Rohrer F, Berresheim H. Strong correlation between levels of tropospheric hydroxyl radicals and solar ultraviolet radiation[J]. Nature, 2006, 442(7099): 184-187. DOI:10.1038/nature04924 |
| [21] | Verma V, Fang T, Xu L, et al. Organic aerosols associated with the generation of reactive oxygen species (ROS) by water-soluble PM2.5[J]. Environmental Science & Technology, 2015, 49(7): 4646-4656. |
| [22] | Fan M Y, Zhang Y L, Lin Y C, et al. Specific sources of health risks induced by metallic elements in PM2.5 during the wintertime in Beijing, China[J]. Atmospheric Environment, 2021, 246. DOI:10.1016/j.atmosenv.2020.118112 |
| [23] | Cho A K, Sioutas C, Miguel A H, et al. Redox activity of airborne particulate matter at different sites in the Los Angeles Basin[J]. Environmental Research, 2005, 99(1): 40-47. DOI:10.1016/j.envres.2005.01.003 |
| [24] | Liu Q Y, Baumgartner J, Zhang Y X, et al. Oxidative potential and inflammatory impacts of source apportioned ambient air pollution in Beijing[J]. Environmental Science & Technology, 2014, 48(21): 12920-12929. |
| [25] | Charrier J G, McFall A S, Vu K K T, et al. A bias in the "mass-normalized" DTT response-an effect of non-linear concentration-response curves for copper and manganese[J]. Atmospheric Environment, 2016, 144: 325-334. DOI:10.1016/j.atmosenv.2016.08.071 |
| [26] | Fan M Y, Zhang Y L, Lin Y C, et al. Isotope-based source apportionment of nitrogen-containing aerosols: a case study in an industrial city in China[J]. Atmospheric Environment, 2019, 212(1): 96-105. |
| [27] | Yu S Y, Liu W J, Xu Y S, et al. Characteristics and oxidative potential of atmospheric PM2.5 in Beijing: source apportionment and seasonal variation[J]. Science of the Total Environment, 2019, 650: 277-287. DOI:10.1016/j.scitotenv.2018.09.021 |
| [28] | Velali E, Papachristou E, Pantazaki A, et al. Redox activity and in vitro bioactivity of the water-soluble fraction of urban particulate matter in relation to particle size and chemical composition[J]. Environmental Pollution, 2016, 208: 774-786. DOI:10.1016/j.envpol.2015.10.058 |
| [29] | Vreeland H, Weber R, Bergin M, et al. Oxidative potential of PM 2.5 during atlanta rush hour: measurements of in-vehicle dithiothreitol (DTT) activity[J]. Atmospheric Environment, 2017, 165: 169-178. DOI:10.1016/j.atmosenv.2017.06.044 |
| [30] | Liu Q Y, Zhang Y X, Liu Y J, et al. Characterization of springtime airborne particulate matter-bound reactive oxygen species in Beijing[J]. Environmental Science and Pollution Research, 2014, 21(15): 9325-9333. DOI:10.1007/s11356-014-2843-6 |
| [31] | Puthussery J V, Zhang C, Verma V. Development and field testing of an online instrument for measuring the real-time oxidative potential of ambient particulate matter based on dithiothreitol assay[J]. Atmospheric Measurement Techniques, 2018, 11(10): 5767-5780. DOI:10.5194/amt-11-5767-2018 |
| [32] | Sameenoi Y, Koehler K, Shapiro J, et al. Microfluidic electrochemical sensor for on-line monitoring of aerosol oxidative activity[J]. Journal of the American Chemical Society, 2012, 134(25): 10562-10568. DOI:10.1021/ja3031104 |
| [33] | Fang T, Verma V, Bates J T, et al. Oxidative potential of ambient water-soluble PM2.5 in the southeastern United States: contrasts in sources and health associations between ascorbic acid (AA) and dithiothreitol (DTT) assays[J]. Atmospheric Chemistry and Physics, 2016, 16(6): 3865-3879. DOI:10.5194/acp-16-3865-2016 |
| [34] | Perrone M G, Zhou J, Malandrino M, et al. PM chemical composition and oxidative potential of the soluble fraction of particles at two sites in the urban area of Milan, Northern Italy[J]. Atmospheric Environment, 2016, 128: 104-113. DOI:10.1016/j.atmosenv.2015.12.040 |
| [35] | Calas A, Uzu G, Kelly F J, et al. Comparison between five acellular oxidative potential measurement assays performed with detailed chemistry on PM10 samples from the city of Chamonix (France)[J]. Atmospheric Chemistry and Physics, 2018, 18(11): 7863-7875. DOI:10.5194/acp-18-7863-2018 |
| [36] | Stevanovic S, Vaughan A, Hedayat F, et al. Oxidative potential of gas phase combustion emissions - an underestimated and potentially harmful component of air pollution from combustion processes[J]. Atmospheric Environment, 2017, 158: 227-235. DOI:10.1016/j.atmosenv.2017.03.041 |
| [37] | Ehhalt D H, Rohrer F. Dependence of the OH concentration on solar UV[J]. Journal of Geophysical Research: Atmospheres, 2000, 105(D3): 3565-3571. DOI:10.1029/1999JD901070 |
| [38] | Wang J P, Lin X, Lu L P, et al. Temporal variation of oxidative potential of water soluble components of ambient PM2.5 measured by dithiothreitol (DTT) assay[J]. Science of the Total Environment, 2019, 649: 969-978. DOI:10.1016/j.scitotenv.2018.08.375 |
| [39] | Patel A, Rastogi N. Oxidative potential of ambient fine aerosol over a semi-urban site in the Indo-Gangetic Plain[J]. Atmospheric Environment, 2018, 175: 127-134. DOI:10.1016/j.atmosenv.2017.12.004 |
| [40] | Eiguren-Fernandez A, Kreisberg N, Hering S. An online monitor of the oxidative capacity of aerosols (o-MOCA)[J]. Atmospheric Measurement Techniques, 2017, 10(2): 633-644. DOI:10.5194/amt-10-633-2017 |
| [41] | Fang T, Verma V, Guo H, et al. A semi-automated system for quantifying the oxidative potential of ambient particles in aqueous extracts using the dithiothreitol (DTT) assay: results from the Southeastern Center for Air Pollution and Epidemiology (SCAPE)[J]. Atmospheric Measurement Techniques, 2015, 8(1): 471-482. DOI:10.5194/amt-8-471-2015 |
| [42] | Yang A, Jedynska A, Hellack B, et al. Measurement of the oxidative potential of PM2.5 and its constituents: the effect of extraction solvent and filter type[J]. Atmospheric Environment, 2014, 83: 35-42. DOI:10.1016/j.atmosenv.2013.10.049 |
| [43] | Liu W J, Xu Y S, Liu W X, et al. Oxidative potential of ambient PM2.5 in the coastal cities of the Bohai Sea, northern China: seasonal variation and source apportionment[J]. Environmental Pollution, 2018, 236: 514-528. DOI:10.1016/j.envpol.2018.01.116 |
| [44] | Guo Z Y, Guo Q J, Chen S L, et al. Study on pollution behavior and sulfate formation during the typical haze event in Nanjing with water soluble inorganic ions and sulfur isotopes[J]. Atmospheric Research, 2019, 217: 198-207. DOI:10.1016/j.atmosres.2018.11.009 |
| [45] | Sauvain J J, Rossi M J, Riediker M. Comparison of three acellular tests for assessing the oxidation potential of nanomaterials[J]. Aerosol Science and Technology, 2013, 47(2): 218-227. DOI:10.1080/02786826.2012.742951 |
 2022, Vol. 43
2022, Vol. 43


