2. 中国科学院生态环境研究中心水污染控制实验室, 北京 100085;
3. 中国科学院大学, 北京 100049;
4. 安平县弘嘉环保技术有限公司, 衡水 053600;
5. 江西省科学院能源研究所, 南昌 330096
2. Laboratory of Water Pollution Control Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China;
3. University of Chinese Academy of Sciences, Beijing 100049, China;
4. Anping Hongjia Environmental Protection Technology Co., Ltd., Hengshui 053600, China;
5. Institute of Energy, Jiangxi Academy of Sciences, Nanchang 330096, China
厌氧氨氧化(anaerobic ammonia oxidation, ANAMMOX)是当前最为高效低耗的生物脱氮途径之一, 相较于传统硝化-反硝化的生物脱氮工艺, 具有曝气能耗低、无需外加有机碳源、污泥产量低和脱氮负荷高等诸多优势[1, 2], 在全球污水处理行业的影响日益显著[3].ANAMMOX工艺的应用通常与短程硝化相结合, 由氨氧化菌(ammonium oxidizing bacteria, AOB)将氨氮(NH4+-N)氧化成亚硝酸盐(NO2--N), 为ANAMMOX菌提供反应底物.ANAMMOX工艺目前已成功应用于多种高氨氮废水的处理[4, 5], 但NO2--N的稳定获取仍是限制该技术推广应用的瓶颈问题[6, 7], 因此, 合理调控NO2--N是实现ANAMMOX组合工艺高效稳定运行的关键因素.
短程硝化的调控原理是根据AOB和亚硝酸盐氧化菌(nitrite oxidizing bacteria, NOB)的不同生理特性, 通过控制一种或多种运行参数以实现两目标菌种生长速率差异的最大化.实现短程硝化的调控策略主要包括控制溶解氧(DO)、曝气方式、温度、污泥龄和底物浓度等[8~10], ANAMMOX菌易受到一些抑制性化合物的影响, 即使是自身所需的反应底物NO2--N也会抑制其活性[11].不同研究所得出的ANAMMOX菌受NO2--N抑制的阈值差异较大, Strous等[7]的研究认为当NO2--N浓度超过100 mg ·L-1时, ANAMMOX菌会完全失活; 而Kimura等[12]的研究则认为当NO2--N浓度为750 mg ·L-1时, ANAMMOX菌活性受到抑制; 当NO2--N浓度降低至274 mg ·L-1时, 其活性得以恢复.因此, ANAMMOX菌对NO2--N的耐受程度受到污泥特性、生长环境、菌属种类和暴露时长的影响[13, 14].
在一体式短程硝化-厌氧氨氧化(combined partial nitritation and ANAMMOX, CPNA)工艺的启动过程, 通常需要将DO控制在非常低的浓度以实现由短程硝化向ANAMMOX反应的转化, DO降低将严重限制NO2--N的积累, 进而影响ANAMMOX菌生长; 而多数研究通过提高DO浓度以实现NO2--N的稳定供给, 但高DO环境又易导致短程硝化的失衡, 并抑制ANAMMOX菌活性, 进而限制ANAMMOX菌生长[15, 16].这就对DO和NO2--N的调控提出了新挑战, 既要避免DO对ANAMMOX菌的抑制, 又要保证ANAMMOX菌有稳定的NO2--N供给.先前的研究在不同反应器、温度条件下实现了CPNA工艺的快速原位启动[15, 17], 但其先启动短程硝化、再降低DO来启动ANAMMOX的运行策略仅局限于小试研究, 这就需要进一步考察该启动策略应用于工程规模条件下CPNA工艺处理实际废水的可行性, 探究环境因素对不同形式和规模CPNA反应器原位启动的影响.因此, 本研究以猪场废水为处理对象, 接种猪场污水处理厂的活性污泥, 分别采用序批式反应器(sequencing batch reactor, SBR)和序批式生物膜反应器(sequencing biofilm batch reactor, SBBR)同步启动CPNA工艺, 通过考察反应器的脱氮性能及相关氮转化功能菌的变化, 探究NO2--N调控对工程规模CPNA反应器原位启动的影响, 优化可实现CPNA工艺原位启动的方法, 以期促进ANAMMOX技术的应用推广.
1 材料与方法 1.1 试验装置与运行本研究将猪场污水处理厂一座水解酸化池的部分单元格分别改造为SBR(5.4 m×5.4 m×4.0 m, 116.6 m3)和SBBR(5.4 m×3.0 m×4.0 m, 64.8 m3)两个反应器(图 1), SBBR与SBR结构类似, SBBR内上部填充有22%的塑料环状纤维组合填料(Φ15 cm×200 cm), 下部填充有10%的海绵填料(4 cm×4 cm×4 cm, 10 ppi); 两反应器系统包括进水、出水和曝气装置, 基于可编程逻辑控制器(programmable logic controller, PLC)的自控装置以及加药装置, 其中曝气装置配有两组不同孔径(4 mm, 2 mm)的曝气管路, 通过微孔、穿孔协调曝气调控反应器内DO浓度.整个运行周期内, PLC(SIEMENS-S7 200 SMART, GER)通过电磁继电器控制各个反应器设备的启动和停止, 以实现反应器的自动化运行.

|
图 1 SBR和SBBR的结构示意 Fig. 1 Schematic diagram of SBR and SBBR structure |
两反应器保持同步运行, 每个反应周期为24 h, 包括进水1 h, 间歇曝气运行21 h, 沉淀1 h后排水1 h, 换水比为50%.通过调节曝气量控制DO浓度, 由PLC控制曝/停时长.整个CPNA工艺启动过程分为: 短程硝化阶段(阶段Ⅰ, 第1~17 d)、短程硝化向ANAMMOX转化阶段(阶段Ⅱ, 第18~39 d)和外加NaNO2强化ANAMMOX阶段(阶段Ⅲ, 第40~77 d), 两反应器各阶段的运行条件见表 1.
|
|
表 1 CPNA反应器各阶段的运行条件 Table 1 Operating conditions at each stage of CPNA reactor |
1.2 进水水质和接种污泥
经过中温厌氧消化处理的生猪养殖废水进入到水解酸化池, 进一步降低其C/N后的出水作为两反应器的进水.受非洲猪瘟疫情的影响, 进水中NH4+-N和TN浓度下降至136 mg ·L-1和214 mg ·L-1左右, 通过外部添加NH4HCO3、NaHCO3提高进水的氮负荷(nitrogen loading rate, NLR)和pH.进水COD为(131±40)mg ·L-1, 平均74.6%的COD为难生物降解有机污染物.由于两反应器的出水又排放至水解酸化池, 导致其进水中的NO2--N和NO3--N随着短程硝化的建立而快速增大.整个试验过程中反应器内的水温保持在(28.3±2.7)℃, pH值控制在7.7~8.1之间.
接种污泥取自河北衡水京安猪场废水处理厂的活性污泥.接种污泥的最大ANAMMOX活性(以N/MLVSS计, 下同)为0.012 kg ·(kg ·d)-1, 接种后SBR和SBBR中的混合液悬浮固体(mixed liquor suspended solids, MLSS)浓度分别为3.9 g ·L-1和3.6 g ·L-1.
1.3 取样和分析方法每个周期对反应池的进水和出水进行采样.当反应器进水完成后, 通过投加NH4HCO3和NaHCO3对池内NLR和pH进行调节, 曝气混合30 min, 取沉淀10 min后的上清液作为进水水样.分别在第1、51和77 d对两反应器进行污泥样品采集.
废水样品经过0.45 μm滤膜进行过滤后, 采用国家规定标准方法分析水样的NH4+-N、NO2--N和NO3--N[18]; TN以TN=NH4+-N+NO2--N+NO3--N计; MLSS及MLVSS采用过滤烘干称重的方法测定; DO和pH值及温度采用便携式多参数水质测试仪(HACH-HQ40d, USA) 进行测定.在30℃下测量SBR中污泥的最大ANAMMOX活性, 分别在第1、51和77 d采集SBR沉淀期间的污泥, 然后注入1 L的烧杯, 同时向烧杯中加入0.25 g的NaNO2, 将烧杯用塑料膜密封, 通过加热磁力搅拌器控制反应温度, 并搅拌污泥以进行混合.定期取样检测, 以NO2--N大于10 mg ·L-1为有效阈值, 对TN变化曲线进行线性拟合, 得出污泥中ANAMMOX菌的最大活性.由于在第1 d的ANAMMOX活性试验中出现了明显的反硝化现象, 为准确地计算接种污泥的ANAMMOX活性, 基于活性试验是处于密封厌氧条件下进行, ANAMMOX菌活性可根据式(1)计算[19]:

|
(1) |
式中, VA为ANAMMOX菌的活性[kg ·(kg ·d)-1], KN为NH4+-N拟合去除速率[mg ·(L ·min)-1], MLVSS为接种污泥的混合液挥发性悬浮固体(mixed liquid volatile suspended solids)浓度(g ·L-1).
1.4 DNA提取和实时定量qPCR取2~3 mL不同试验阶段的活性污泥样品, 经转速为13 200 r ·min-1离心10 min后, 使用Fast DNA SPIN for Soil试剂盒提取.提取的DNA分别用NanoDrop 2000(Thermo Scientific, USA)和1%琼脂糖凝胶电泳检测浓度和质量, 提取的污泥DNA样品存储在-70℃直到使用.
对包括亚硝化(amoA)、硝化(nxrB)、反硝化(narG)和厌氧氨氧化(hzsA)的氮素转化功能基因进行定量研究.将克隆质粒稀释10倍梯度, 选择5~7点预实验制备标准曲线.qPCR扩增的热循环步骤如下: ① 50℃, 2 min, ② 95℃, 5 min, ③ 95℃, 20 s, ④各功能基因退火温度分别为: 60、55、50和55℃, 30 s, ⑤ 72℃, 31 s, ⑥终点读板, 重复至步骤③~⑤, 重复次数在39次以上, ⑦熔体曲线分析: 60~95℃, 读取间隔0.2℃.反应使用ABI Real-time PCR system 7500(ABI, USA)进行, 熔解曲线和凝胶电泳验证了特异性, 用标准曲线和阴性对照一式三份定量每个基因.
1.5 功能微生物倍增时间和生长率反应器内ANAMMOX菌的倍增时间和生长率依据式(2)和式(3)进行计算[20]:

|
(2) |

|
(3) |
式中, td为倍增时间(d), t-t0为时间段(d), c为ANAMMOX菌的目标基因拷贝数浓度(copies ·mL-1), c0为ANAMMOX菌的目标基因初始拷贝数浓度(copies ·mL-1), μ为生长率(d-1).
2 结果与讨论 2.1 短程硝化阶段(Ⅰ)有研究表明, 游离氨(FA)对NOB的抑制作用强于AOB[21, 22].相较于NOB, AOB在缺氧向好氧环境转化过程中能够快速地恢复活性[23], AOB和NOB的氧饱和常数分别为0.2~0.4 mg ·L-1和1.2~1.5 mg ·L-1, 控制DO浓度在两者氧饱和常数之间时, 可有效实现AOB与NOB生长速率的差异最大化[24].因此, 在短程硝化阶段, pH控制在7.7~8.1以提高FA浓度, 采用曝停时间比(曝停比)为2 h ∶1 h的间歇曝气模式, 控制两反应器中DO浓度在(0.60±0.20)mg ·L-1, 且两反应器保持相同的运行模式.经过10 d的调试运行, 两反应器中成功实现了较高浓度的NO2--N积累, 运行期间的曝气时长、DO及NO2--N积累情况如图 2所示.相较于SBR, SBBR在第5 d率先出现NO2--N的积累, 由于两反应器的出水排至作为进水源的水解酸化池, 导致进水NO2--N浓度随之增大, SBBR中的NO2--N浓度在一周时间内迅速累积至199 mg ·L-1, NH4+-N去除率和亚硝酸盐积累率(NAR)分别为73.6%和41.2%; 而SBR运行至第8 d开始出现明显的亚氮积累, NH4+-N去除率和NAR在第10 d增长至48.0%和33.5%, NO2--N积累浓度为99 mg ·L-1.

|
图 2 两个CPNA反应器启动过程中的NO2--N和NO3--N的浓度变化 Fig. 2 Changes of NO2--N and NO3--N during the start-up of CPNA reactors |
两反应器中NO2--N积累效果表明, SBBR在启动时间和NO2--N积累速率均明显优于SBR, 这说明在相同条件下, SBBR的泥膜共生形式更适于短程硝化的快速启动.相较于活性污泥, 可能是泥膜共生的污泥形态可以更多地保留污泥中的新生菌群吸附于填料上, 再结合前期排水过程中存在明显的污泥流失, 从而实现对目标菌种的快速筛选, 促进目标菌种得以快速富集[16, 25].
2.2 短程硝化向ANAMMOX转化阶段(Ⅱ)在短程硝化向ANAMMOX转化过程中, 如何平衡DO输入和NO2--N积累是启动CPNA工艺的一个难题, 既需要供氧以实现稳定的NO2--N供给, 又需要限氧防止过量DO对ANAMMOX菌活性的抑制.本研究通过调控DO和间歇曝气方式促进ANAMMOX菌活性的显现, 运行调控策略及相应的脱氮性能变化如图 3所示.在第11~26 d, 两反应器的DO和曝停比分别由前一阶段的0.5 mg ·L-1和2 h ∶1 h逐步调整至0.35 mg ·L-1和1 h ∶2 h, 此时出水NO2--N浓度并没有随之降低, 而呈现继续增大然后逐步降低的趋势, 这是由于AOB活性逐渐增大、进水中残留有出水中的NO2--N, 使得NO2--N累积浓度的调控具有滞后性.在第27~29 d两反应器的DO进一步降低至0.15 mg ·L-1, 并采用连续曝气方式提高传质效果, 随后SBR中出现了连续稳定的TN去除, 总氮去除率(TNRE)和总氮去除负荷(TNRR, 以N计, 下同)分别稳定在13.2%和0.050 kg ·(m3 ·d)-1.随着SBR中ANAMMOX菌活性的持续增大, 反应器中的NO2--N浓度逐步降低, 较低的DO环境使得反应器中积累的NO2--N不能满足ANAMMOX菌的底物需求.第30 d仅将SBR中DO浓度提高至0.25 mg ·L-1, 以促进NO2--N的积累; 稳定运行至第39 d, SBR的脱氮效能经过快速增长后逐步保持稳定, TNRE和TNRR分别稳定在23.3%和0.069 kg ·(m3 ·d)-1;

|
图 3 两个CPNA反应器启动过程中的脱氮性能 Fig. 3 Nitrogen removal performance during start-up of CPNA reactors |
在此期间, SBBR一直未出现连续稳定的TN去除, 这可能是由于ANAMMOX菌受到长时间高浓度的NO2--N抑制所致[26].尽管SBBR的接种污泥具有一定的ANAMMOX活性, 但经过39 d的调试运行后却一直未出现连续稳定的TN去除现象, 这与先前Kimura等[12]的研究所得出的当水中NO2--N浓度低于274 mg ·L-1时, ANAMMOX活性可在3 d内完全恢复的结论不符.NO2--N对ANAMMOX菌的抑制程度不仅取决于NO2--N浓度, 暴露时间同样是非常重要的因素, 长时间、高浓度的NO2--N抑制作用会对ANAMMOX菌活性造成难以恢复的影响.鉴于SBBR中长时间未有ANAMMOX活性显现的迹象, 在第40 d尝试将池中约30%的絮状污泥进行重新接种, 经过短期适应后出现了稳定的TN去除, 反应器的TNRE和TNRR逐渐增大并稳定在22.6%和0.076 kg ·(m3 ·d)-1.而在第55~77 d期间, SBBR的TNRE和TNRR随着水温从30.9℃逐步降低至25.6℃而分别下降至11.5%和0.041 kg ·(m3 ·d)-1, 这表明较高的水温仍是保持ANAMMOX工艺稳定运行的重要控制参数.
通过对比分析, SBR和SBBR中的ANAMMOX菌分别受到了7 d介于100~129 mg ·L-1和17 d介于129~286 mg ·L-1的NO2--N抑制影响, 经过39 d的调试运行, SBR顺利完成由短程硝化向ANAMMOX工艺的转化, 而SBBR始终未能实现稳定的TN去除, 没有完成短程硝化向ANAMMOX工艺的转化.这表明长时间高浓度NO2--N抑制环境对ANAMMOX菌活性造成了难以恢复的影响, 在CPNA工艺启动过程中, 合理的NO2--N浓度控制是CPNA工艺成功启动的关键因素.
2.3 外加NaNO2强化ANAMMOX阶段(Ⅲ)在第33~39 d运行期间, SBR的TNRR并未随着运行时间而继续增大, 而是稳定在0.072 kg ·(m3 ·d)-1.而第38、39 d连续低于0.23 mg ·L-1的出水NO2--N浓度则表明(图 2), 此时SBR内有限的NO2--N供给限制了ANAMMOX菌的脱氮速率.为了进一步提高SBR中的NO2--N供给, 保证ANAMMOX菌在充足底物条件下快速增殖, 本研究尝试通过外投NaNO2和提高DO这两种方法强化反应器中NO2--N的供给. 第40 d开始向SBR中投加28.7 kg的NaNO2, 将进水NO2--N浓度增至49 mg ·L-1, SBR的TNRR和TNRE分别跃升至0.117 kg ·(m3 ·d)-1和35.4%; 然后在第42~46 d将DO升至0.35 mg ·L-1, 调整先前的连续曝气为间歇曝气(ton ∶toff=6 h ∶1 h), 通过提高供氧强化反应器内NO2--N的积累, 该期间SBR平均出水NO2--N浓度为14 mg ·L-1, 然而其TNRR和TNRE却迅速回落至0.052 kg ·(m3 ·d)-1和14.3%左右.这可能是由于反应器中ANAMMOX菌活性受到了DO的抑制[27, 28], 并且DO升高导致短程硝化的失稳, NO3--N积累增大.因此, 在第47~51 d将DO恢复至0.25 mg ·L-1, 曝停比为1 h ∶1 h, 以缓解SBR中NO3--N的过量积累.通过对比上述两种提高亚硝酸盐供给的调控策略, 阶段性外加NaNO2更加简单、有效.
在第52~77 d向SBR中分批添加NaNO2, 期间反应器脱氮效能变化如图 4所示, 随着NaNO2添加量从17.2 kg(NO2--N=30 mg ·L-1)逐渐增加到63.2 kg(NO2--N=110 mg ·L-1), SBR的TNRR和TNRE分别从第51 d的0.070 kg ·(m3 ·d)-1和16.0%迅速提高至第77 d的0.336 kg ·(m3 ·d)-1和52.2%.尽管反应温度已降至25.6℃, 但反应器脱氮负荷得到了快速增强, 同时ΔNO3--N/ΔTN稳定在0.14左右, 接近于理论值, 这表明反应器内已实现稳定的短程硝化, 且ANAMMOX反应是最为主要的脱氮途径, CPNA工艺在77 d内得到了快速启动.在反应器由短程硝化向ANAMMOX工艺转化过程中, 需要将DO降至非常低的浓度(<0.2 mg ·L-1), 这将严重限制NO2--N累积, 而NO2--N短缺又会进一步限制ANAMMOX菌生长, 从而导致启动时间延长, 甚至是系统崩溃.通过阶段性外加亚硝酸盐维持稳定的NO2--N供给, 优先保证ANAMMOX菌活性得到最大限度的增长, 可有效促进CPNA工艺的快速启动.

|
图 4 SBR在外加NaNO2强化阶段的脱氮效能 Fig. 4 Nitrogen removal performance of SBR at the biofortification stage by NaNO2 addition |
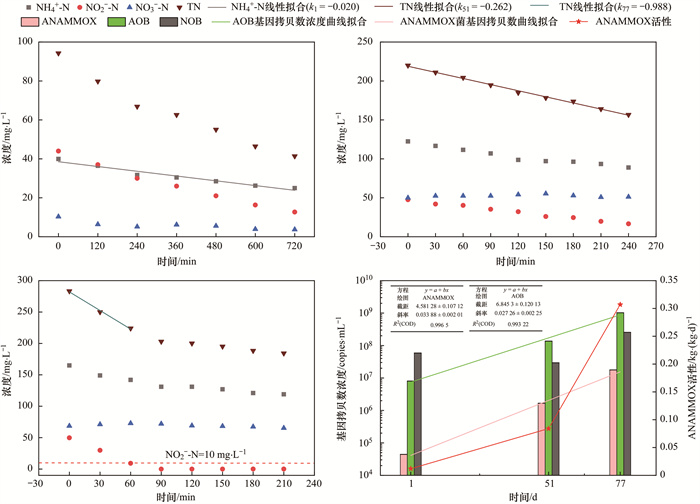
SBR在经过77 d的调试运行成功启动了CPNA工艺, 反应器中第1、51和77 d污泥的ANAMMOX活性及氮转化功能菌基因拷贝浓度的变化趋势如图 5所示.在第1~51 d期间, 通过控制间歇曝气方式、进水NO2--N浓度和DO实现了短程硝化向ANAMMOX反应的转化, 反应器中ANAMMOX菌的活性和基因拷贝数浓度分别从最初的0.012 kg ·(kg ·d)-1和4.42×104 copies ·mL-1升高至0.084 kg ·(kg ·d)-1和1.66×106 copies ·mL-1; 同时, AOB的基因拷贝数浓度从8.06×106 copies ·mL-1增加到1.37×108 copies ·mL-1, 而NOB的基因拷贝数浓度则略有下降, 这表明该阶段的DO控制策略有效促进了SBR中短程硝化的建立以及ANAMMOX菌活性的增长.通过式(2)和式(3)计算得CPNA工艺启动阶段ANAMMOX菌的生长率和倍增时间分别为0.071 d-1和9.74 d.经过26 d的外加亚硝酸盐强化运行后, ANAMMOX菌的活性和基因拷贝数浓度则继续增大至0.307 kg ·(kg ·d)-1和1.77×107 copies ·mL-1, 且该阶段ANAMMOX菌的生长率和倍增时间分别为0.046 d-1和7.62 d, 优于Strous等[29]的研究用SBR富集ANAMMOX菌试验中所得出0.065 d-1的生长率和11 d的倍增时间.这表明在短程硝化向CPNA工艺转化的过程中, 阶段性外加亚硝酸盐的运行策略可有效解决因低DO所导致的NO2--N积累不足的问题, 避免ANAMMOX菌生长受到反应底物不足的限制.通过将不同阶段SBR污泥中AOB、ANAMMOX菌的基因拷贝数浓度曲线进行线性拟合发现, SBR中AOB和ANAMMOX菌的数量浓度均呈几何级数增长趋势, AOB和ANAMMOX菌的基因拷贝数浓度(copies ·mL-1)可分别以下列拟合方程式计算:

|
|
图 5 SBR中ANAMMOX菌活性及氮转化功能菌基因拷贝数浓度的变化 Fig. 5 Variations of the ANAMMOX activities and gene copy concentration of nitrogen-transforming bacteria in the SBR |
这表明在整个CPNA工艺启动过程中, 通过以调控DO和曝气方式为主, 辅以外加NaNO2的亚硝酸盐调控策略可有效保障反应器中AOB和ANAMMOX菌的快速增长, 进而实现CPNA工艺的快速启动.
SBBR经过二次接种后实现了较为稳定的CPNA反应.经过77 d的调试运行, 反应器内AOB、NOB和ANAMMOX菌的基因拷贝数浓度(以MLVSS计)由接种污泥的2.93×109、2.13×1010和1.60×107 copies ·g-1, 分别逐步演变为组合填料上所形成生物膜中的6.98×109、4.94×109和6.53×107 copies ·g-1.AOB基因拷贝数浓度的少量增大和NOB基因拷贝数浓度的明显降低验证了SBBR内存在稳定的短程硝化, 而AOB基因拷贝数浓度只有小幅的增大可能是由于AOB更喜欢在絮状污泥里富集生长[30].而反应器内ANAMMOX菌在遭受到严重的NO2--N抑制后进行二次接种, 稳定运行37 d后所形成生物膜中ANAMMOX菌基因拷贝数浓度有所增长, 这同SBBR在进行二次接种后出现连续稳定的TN去除现象相符.
3 结论(1) 在短程硝化启动过程的相同条件下, 通过调控DO、pH及曝气模式, SBBR的启动时间和NO2--N积累速率均明显优于SBR, 泥膜共生形式更适于短程硝化的快速启动.
(2) 在成功启动短程硝化的基础上, 可逐步降低DO来启动ANAMMOX.SBR经过39 d调试运行成功实现了连续稳定的TN去除, TNRR和TNRE分别稳定在0.069 kg ·(m3 ·d)-1和23.3%; 而经过相同调试运行的SBBR未能实现稳定的TN去除, 这可能是由于长时间、高浓度的NO2--N抑制(129~286 mg ·L-1, 共计17 d)对ANAMMOX菌活性造成了难以恢复的影响.
(3) 合理的NO2--N调控是CPNA工艺快速启动的关键因素.以调控DO、曝气方式为主和辅以外加NaNO2的亚硝酸盐调控策略可有效实现反应器中AOB和ANAMMOX菌的快速增长.经过阶段性外加NaNO2后, SBR在第77 d成功启动了CPNA工艺, TNRR和TNRE分别从第51 d的0.070 kg ·(m3 ·d)-1、16.0%迅速提高至第77 d的0.336 kg ·(m3 ·d)-1、52.2%, ANAMMOX菌的活性和基因拷贝数浓度从最初的0.012 kg ·(kg ·d)-1和4.42×104 copies ·mL-1跃升至0.307 kg ·(kg ·d)-1和1.77×107 copies ·mL-1.
| [1] | Ma B, Wang S Y, Cao S B, et al. Biological nitrogen removal from sewage via anammox: recent advances[J]. Bioresource Technology, 2016, 200: 981-990. DOI:10.1016/j.biortech.2015.10.074 |
| [2] | Mulder A. The quest for sustainable nitrogen removal technologies[J]. Water Science & Technology, 2003, 48(1): 67-75. |
| [3] | Jetten MSM, Cirpus I, Kartal B, et al. 1994-2004:10 years of research on the anaerobic oxidation of ammonium[J]. Biochemical Society Transactions, 2005, 33(1): 119-123. DOI:10.1042/BST0330119 |
| [4] | Zhang F Z, Peng Y Z, Wang S Y, et al. Efficient step-feed partial nitrification, simultaneous Anammox and denitrification(SPNAD) equipped with real-time control parameters treating raw mature landfill leachate[J]. Journal of Hazardous Materials, 2019, 364. DOI:10.1016/j.jhazmat.2018.09.066 |
| [5] | Lackner S, Gilbert E M, Vlaeminck S E, et al. Full-scale partial nitritation/anammox experiences-an application survey[J]. Water Research, 2014, 55: 292-303. DOI:10.1016/j.watres.2014.02.032 |
| [6] | Deng S Y, Peng Y Z, Zhang L, et al. Advanced nitrogen removal from municipal wastewater via two-stage partial nitrification-simultaneous anammox and denitrification(PN-SAD) process[J]. Bioresource Technology, 2020, 304. DOI:10.1016/j.biortech.2020.122955 |
| [7] | Strous M, Kuenen J G, Jetten M S M. Key physiology of anaerobic ammonium oxidation[J]. Applied and Environmental Microbiology, 1999, 65(7): 3248-3250. DOI:10.1128/AEM.65.7.3248-3250.1999 |
| [8] | Peng Y Z, Guo J H, Horn H, et al. Achieving nitrite accumulation in a continuous system treating low-strength domestic wastewater: switchover from batch start-up to continuous operation with process control[J]. Applied Microbiology and Biotechnology, 2012, 94(2): 517-526. DOI:10.1007/s00253-011-3702-8 |
| [9] |
王元月, 魏源送. 新型控制模式下短程硝化/厌氧氨氧化法处理污泥水[J]. 中国给水排水, 2013, 29(17): 24-27. Wang Y Y, Wei Y S. Combined partial nitrification and ANAMMOX process for treating sludge water under new control pattern[J]. China Water & Wastewater, 2013, 29(17): 24-27. DOI:10.3969/j.issn.1000-4602.2013.17.006 |
| [10] | Miao Y Y, Zhang J H, Peng Y Z, et al. An improved start-up strategy for mainstream anammox process through inoculating ordinary nitrification sludge and a small amount of anammox sludge[J]. Journal of Hazardous Materials, 2019, 384. DOI:10.1016/j.jhazmat.2019.121325 |
| [11] |
王元月, 魏源送, 张树军. 厌氧氨氧化技术处理高浓度氨氮工业废水的可行性分析[J]. 环境科学学报, 2013, 33(9): 2359-2368. Wang Y Y, Wei Y S, Zhang S J. Feasibility analysis of anammox for treating high strength ammonia industrial wastewater[J]. Acta Scientiae Circumstantiae, 2013, 33(9): 2359-2368. |
| [12] | Kimura Y, Isaka K, Kazama F, et al. Effects of nitrite inhibition on anaerobic ammonium oxidation[J]. Applied Microbiology and Biotechnology, 2010, 86(1): 359-365. DOI:10.1007/s00253-009-2359-z |
| [13] |
朱强, 王凡, 刘娜, 等. 亚硝酸盐形态对ANAMMOX菌活性的影响及抑制规律[J]. 中国给水排水, 2019, 35(15): 122-127. Zhu Q, Wang F, Liu N, et al. Effect of nitrite form on ANAMMOX bacteria activity and its inhibiting rule[J]. China Water & Wastewater, 2019, 35(15): 122-127. |
| [14] |
付昆明. 全程自养脱氮(CANON)反应器的启动及其脱氮性能[D]. 北京: 北京工业大学, 2010. Fu K M. Start-up and performance of nitrogen removal of CANON reactor[D]. Beijing: Beijing University of Technology, 2010. |
| [15] |
李冬, 何永平, 张肖静, 等. MBR系统CANON工艺的快速启动及微生物种群特征[J]. 中国环境科学, 2014, 34(11): 2788-2795. Li D, He Y P, Zhang X J, et al. The fast start-up of CANON process in MBR system and the characterization of microbes[J]. China Environmental Science, 2014, 34(11): 2788-2795. |
| [16] |
李思敏, 左富民, 吴坤茹. 石英砂-海绵填料CANON反应器的快速启动研究[J]. 中国给水排水, 2018, 34(3): 100-104. Li S M, Zuo F M, Wu K R. Rapid start-up of CANON reactor filled with quartz sand/sponge carrier[J]. China Water & Wastewater, 2018, 34(3): 100-104. |
| [17] |
付昆明, 张杰, 曹相生, 等. 好氧条件下CANON工艺的启动研究[J]. 环境科学, 2009, 30(6): 1689-1694. Fu K M, Zhang J, Cao X S, et al. Study of CANON process start-up under aerobic conditions[J]. Environmental Science, 2009, 30(6): 1689-1694. DOI:10.3321/j.issn:0250-3301.2009.06.022 |
| [18] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002. |
| [19] | Kuenen J G. Anammox bacteria: from discovery to application[J]. Nature Reviews Microbiology, 2008, 6(4): 320-326. DOI:10.1038/nrmicro1857 |
| [20] | Park H, Rosenthal A, Jezek R, et al. Impact of inocula and growth mode on the molecular microbial ecology of anaerobic ammonia oxidation(ANAMMOX) bioreactor communities[J]. Water Research, 2010, 44(17): 5005-5013. DOI:10.1016/j.watres.2010.07.022 |
| [21] | Vadivelu V M, Yuan Z G, Fux C, et al. The inhibitory effects of free nitrous acid on the energy generation and growth processes of an enriched Nitrobacter culture[J]. Environmental Science & Technology, 2006, 40(14): 4442-4448. |
| [22] | Vadivelu V M, Keller J, Yuan Z. Free ammonia and free nitrous acid inhibition on the anabolic and catabolic processes of Nitrosomonas and Nitrobacter[J]. Water Science & Technology, 2007, 56(7): 89-97. |
| [23] |
李亚峰, 秦亚敏, 谢新立, 等. 间歇曝气条件下短程硝化的实现及影响因素研究[J]. 环境工程学报, 2011, 5(7): 1518-1521. Li Y F, Qin Y M, Xie L X, et al. Study on achievement and influencing factors of shortcut nitrification in intermittent aeration[J]. Chinese Journal of Environmental Engineering, 2011, 5(7): 1518-1521. |
| [24] | Laanbroek H J, Gerards S. Competition for limiting amounts of oxygen between Nitrosomonas europaea and Nitrobacter winogradskyi grown in mixed continuous cultures[J]. Archives of Microbiology, 1993, 159(5): 453-459. DOI:10.1007/BF00288593 |
| [25] |
周家中, 吴迪, 韩文杰, 等. 基于MBBR的CANON工艺处理消化液中试启动[J]. 中国环境科学, 2019, 39(6): 2378-2386. Zhou J Z, Wu D, Han W J, et al. Pilot scale start-up of CANON disposal sludge-digestion wastewater treatment based on MBBR[J]. China Environmental Science, 2019, 39(6): 2378-2386. DOI:10.3969/j.issn.1000-6923.2019.06.018 |
| [26] | Dosta J, Fernández I, Vázquez-Padín J R, et al. Short-and long-term effects of temperature on the Anammox process[J]. Journal of Hazardous Materials, 2008, 154(1-3): 688-693. DOI:10.1016/j.jhazmat.2007.10.082 |
| [27] | Egli K, Fanger U, Alvarez P J J, et al. Enrichment and characterization of an anammox bacterium from a rotating biological contactor treating ammonium-rich leachate[J]. Archives of Microbiology, 2001, 175(3): 198-207. DOI:10.1007/s002030100255 |
| [28] | Strous M, van Gerven E, Kuenen J G, et al. Effects of aerobic and microaerobic conditions on anaerobic ammonium-oxidizing(Anammox) sludge[J]. Applied and Environmental Microbiology, 1997, 63(6): 2446-2448. DOI:10.1128/aem.63.6.2446-2448.1997 |
| [29] | Strous M, Heijnen J J, Kuenen J G, et al. The sequencing batch reactor as a powerful tool for the study of slowly growing anaerobic ammonium-oxidizing microorganisms[J]. Applied Microbiology and Biotechnology, 1998, 50(5): 589-596. DOI:10.1007/s002530051340 |
| [30] | Tan H, Wang Y Y, Tang X, et al. Quantitative determination of cavitation formation and sludge flotation in Anammox granules by using a new diffusion-reaction integrated mathematical model[J]. Water Research, 2020, 174. DOI:10.1016/j.watres.2020.115632 |
 2021, Vol. 42
2021, Vol. 42


