2. 农业农村部资源循环利用技术与模式重点实验室, 北京 100125
2. Key Laboratory of Technology and Model for Cyclic Utilization from Agricultural Resources, Ministry of Agriculture and Rural Affairs, Beijing 100125, China
据调查显示, 我国约19.4%的农田土壤受到污染, Cd和Cu点位超标率分别达7.0%和2.1%[1], 其中冶炼厂和矿区周边农田土壤重金属污染更为严重.与单一重金属污染相比, 复合污染土壤中多种重金属之间的相互作用会因为土壤环境、元素种类和浓度而改变其赋存形态、溶解度和生物可利用度, 从而相互抑制或促进彼此的修复效率[2].Cd和Cu复合污染土壤中两种重金属表现出竞争和协同作用, 二者在土壤中均主要以二价离子的形式存在, 其有效性形态与氧化还原电位、有机质和pH等密切相关, 但钝化机制不尽相同[3].原位钝化修复技术由于对土壤环境影响小, 投入成本低等特点, 在农田土壤重金属污染修复中备受关注.研究报道的钝化材料种类较多, 包括化学、生物和微生物等不同类型[4], 其中生物炭由于具有较大的比表面积、丰富的官能团、稳定的有机碳和矿物灰分等特性[5], 能有效地降低土壤中重金属活性, 同时可改善土壤结构和提高土壤有机质含量等, 而广泛应用于重金属污染农田土壤的修复[6].其钝化效果受其粒径分布、孔容、比表面积和表面官能团等表面结构以及pH、挥发分含量、灰分含量和持水性等理化性质影响.为进一步提高生物炭对重金属的钝化效果, 国内外研究学者开发了多种改性方法, 主要分为物理、化学和生物这3类, 相对于物理和生物改性方法, 化学改性方法使生物炭表面化学性质和结构产生显著变化, 获得吸附效果更佳的钝化材料, 且操作简单, 成本较低[7], 一般采用强氧化剂、酸碱和纳米金属负载等方式进行.不同改性方法的适用性主要由重金属类型、污染程度及土壤环境条件等决定.有研究表明, 化学改性生物炭适用于Cd污染土壤的修复[8], 杨兰等[9]采用NaOH、KMnO4和FeCl3改性生物炭对Cd污染土壤进行钝化, 均有效降低了土壤中Cd的有效态含量, 其中KMnO4改性生物炭的钝化效率高达65.1%; Sun等[10]采用KMnO4浸渍处理生物炭, 改性后生物炭孔隙度和比表面积增大, 含氧官能团数量增加, 对Pb和Cd的吸附能力明显增强; Zhang等[11]采用FeCl2和FeCl3对生物炭进行改性, 改性后比表面积增大约50倍, 对土壤中Cd的钝化效率上升了6.81%~25.0%; 陈雪娇等[12]对改性生物炭对重金属吸附的稳定性研究发现, NaOH改性生物炭对Cd的吸附更加稳固, 生物炭含氧官能团的增加更易与Cu产生络合物[13].汪怡等[14]通过KOH对生物炭进行改性, 羟基和氨基等碱性官能团数量增多, 对Cu的最大吸附量提高了14.6%; Li等[15]通过ZnO/ZnS改性后生物炭比表面积从102.96 m2·g-1增至397.45 m2·g-1, 对Cu的最大吸附量可达91.2 mg·g-1; Zhang等[16]制备的K3PO4改性生物炭在重金属复合污染土壤中对Cu和Cd的钝化效率较改性前, 分别提高了14%~24%和19%~33%, 但仍未明确复合污染土壤中Cu和Cd钝化效果较佳的改性方法及主要影响机制.
目前, 我国农田土壤重金属污染逐渐趋于复杂化和多元化, 尤其冶炼厂产生烟尘、尾矿和废水中重金属随大气沉降、废渣渗漏和污水灌溉等途径进入周围农田土壤, 重金属污染物多以复合污染的形式存在[17].现有的生物炭改性研究大多针对单一重金属污染或外源添加重金属, 针对冶炼厂周边复合污染农田土壤的研究较少.因此, 本文把冶炼厂周围Cu和Cd复合污染农田土壤作为研究对象, 以稻壳生物炭为原料, 比较分析K3PO4、KMnO4和NaOH等不同改性方法对生物炭特性及土壤重金属形态的影响, 以期为生物炭修复重金属污染土壤提供理论依据.
1 材料与方法 1.1 改性生物炭制备生物炭(WBC)的制备:以稻壳为原料, 采用外加热式生物质连续热解炭化技术, 在管式炉中进行绝氧保温炭化, 炭化条件为:升温速率20℃·min-1, 炭化终温600℃, 保温时间5 min, 制备过程充氮气以绝氧.
NaOH改性生物炭(NBC)制备方法:配制2 mol·L-1 NaOH溶液, 按质量比为1∶5加入生物炭, 混合均匀搅拌2 h, 浸泡24 h后, 过滤, 用去离子水清洗至滤液呈中性, 100℃烘干至恒重[18].
KMnO4改性生物炭(MBC)制备方法:采用抽滤法将生物炭清洗至中性(pH=7), 于80℃烘干备用.将0.1mol·L-1的KMnO4溶液按质量比为5∶1加入生物炭, 混合均匀搅拌2 h, 浸泡24 h后, 过滤, 清洗至滤液呈中性, 60℃烘干至恒重[18].
K3PO4改性生物炭(PBC)制备方法:配制0.05 mol·L-1 K3PO4溶液, 按质量比5∶1加入生物炭, 混合均匀搅拌2 h; 再加入质量分数为8%的H2O2溶液, 混合均匀搅拌2 h, 浸泡24 h后, 过滤, 清洗至滤液呈中性, 过滤后60℃烘干至恒重.
1.2 供试土壤及土壤培养试验供试土壤为Cu和Cd复合污染土壤, 取自江西省贵溪市贵溪冶炼厂附近农田耕层土壤(0~20 cm), 风干、去除异物, 过筛备用.土壤的基本理化性质及Cu和Cd含量见表 1.
|
|
表 1 土壤基本理化性质及重金属Cu和Cd含量 Table 1 Basic physical and chemical properties of soil as well as copper and cadmium content |
以不添加生物炭、未改性生物炭和3种改性生物炭为钝化材料, 设置添加量分别为0.5%(0.5 g生物炭/100 g土)和2%(2 g生物炭/100 g土), 共9个处理(表 2), 3次重复.将钝化材料与土壤混合均匀, 在25℃、65%的田间持水量条件下培养90 d, 分别在第30 d、90 d时取土样.土壤样品风干后, 研磨过1 mm筛备用.
|
|
表 2 土壤培养试验处理 Table 2 Soil culture experiment treatments |
1.3 测定方法 1.3.1 土壤理化性质测定
土壤pH值采用玻璃电极法(土∶水=1∶2.5)测定, CEC采用乙酸铵交换法测定, 全氮采用凯氏定氮法测定, 全磷、全钾采用碱熔法消解后测定, 有机质采用重铬酸钾容量法测定[19].
1.3.2 生物炭特性表征采用全自动比表面分析仪(美国康塔, NOVAe)分析改性生物炭比表面积、孔容和孔径等; 采用扫描电镜能谱仪(日本电子, JSM-IT500)进行表面形貌分析; 采用傅立叶变换红外光谱仪(美国尼高力, Nicolet 8700)测试生物炭的红外光谱图.
1.3.3 土壤重金属Cu和Cd有效态的测定CaCl2溶液提取的有效态重金属与植物体中重金属的含量均呈极显著相关, 可较好地预测土壤重金属的生物有效性[20], 采用CaCl2(0.01 mol·L-1)为提取剂提取土壤中Cu和Cd有效态, 准确称取土壤样品2.00 g, 置于50 mL离心管中, 取CaCl2溶液(pH=7) 20 mL加入样品中, 20℃振荡提取2 h, 4 000 r·min-1离心15 min, 过0.45 μm滤膜, ICP-MS(美国安捷伦, Agilent-7900)测定, 重复3次.
1.3.4 土壤重金属Cu和Cd形态的测定土壤中Cu和Cd结合形态采用改进的Tessier六步提取法[21]测定(表 3), 每种形态含量以所占质量分数表示, 即由各形态含量与6种形态含量之和的比值计算获得, 采用弱酸提取态(水溶态、可交换态和碳酸盐结合态)培养前后形态变化作为重金属的钝化效果指标, 由公式(1)计算:

|
(1) |
|
|
表 3 改进的Tessier六步提取法 Table 3 Improved Tessier six-step extraction method |
1.4 数据处理
使用Microsoft Excel和Origin9.5对数据进行处理并作图分析, 统计分析采用数据分析软件SPSS21.0, 采用单因素方差分析法(LSD法)检验各处理pH值的差异显著性(P < 0.05), 用Pearson相关分析系数法分析各改性生物炭理化性质与重金属形态间的相关性.所有数据均以3次重复的平均值加减标准差来表示.
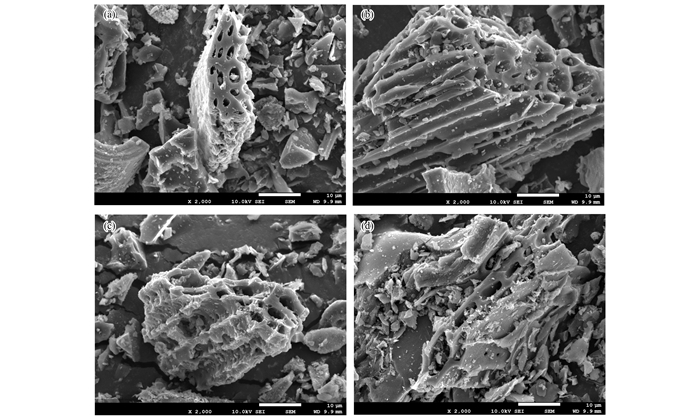
2 结果与讨论 2.1 改性生物炭特性表征 2.1.1 表面结构图 1为不同生物炭的电镜扫描图, 4种生物炭表面均伴有大量无规则的孔隙结构, 有利于重金属离子进入生物炭内层, 并与内层表面吸附位点结合[22].WBC呈筛管状结构、微孔结构大小不一, 表面颗粒物较少; 改性后, PBC仍呈现筛管状结构, 其表面孔隙结构明显缩小; MBC和NBC结构变化较大, MBC呈不规则多孔褶皱结构, 大量的颗粒物聚集表面, 可能是改性后负载的δ-MnO2和MnOx颗粒[23, 24]; NBC表面粗糙, 大量不规则形状颗粒在表面聚集, 导致孔洞堵塞.
|
(a)WBC(未改性), (b)PBC(K3PO4改性), (c)MBC(KMnO4改性), (d)NBC(NaOH改性) 图 1 不同生物炭的SEM图 Fig. 1 SEM images of different biochars |
不同生物炭的比表面积(BET)和孔隙特征见表 4, 可以看出, 改性后其表面孔隙、比表面积和孔容均有较大的变化, MBC和NBC变化较为明显, 比表面积分别增至46.19 m2·g-1和60.79 m2·g-1, 孔容增至0.09 cm3·g-1和0.12 cm3·g-1远高于未改性生物炭. 4种生物炭的比表面积的大小顺序为:WBC < PBC < MBC < NBC.孔容的变化规律与比表面积一致, 改性后均有所增大, 有利于提高对重金属的吸附[25].而平均孔径的变化趋势与之相反, 大小顺序为MBC < NBC < PBC < WBC, 这与SEM观察到的现象一致.孔径大小对吸附重金属效果的影响说法不一, 有研究认为孔径较大的生物炭更加有利于吸附重金属, 但也有研究认为, 孔径变小使部分重金属进入微孔内部难以被溶出解吸, 更利于对重金属的固定[26, 27].
|
|
表 4 不同改性生物炭的BET比表面积、平均孔径和孔容参数表 Table 4 BET specific surface area and pore characteristics of different modified biochars |
2.1.3 元素分析
生物炭的元素组成与其稳定性密切相关[28], 不同改性生物炭的元素含量及pH变化如表 5所示.改性后生物炭C元素含量均有所下降, H和O元素含量有所上升.H/C和O/C比值明显增加, 表明生物炭芳香化程度降低, 表面极性增大, 亲水性增强[29], 其中PBC的H/C比值最大, 为0.69, N含量也明显升高, 说明其表面活性位点和负载的含磷组分更多、官能团更加丰富; MBC的O/C比值最大, 可能是KMnO4强氧化性引起的含氧官能团增多, 与Wang等[30]采用KMnO4改性后生物炭的元素变化基本一致; NBC与改性前相比, N含量略有降低, 可能在NaOH改性过程中生物炭受到强碱物质抑制脱水聚合、增强脱羧等反应作用导致含N官能团损失[31].
|
|
表 5 不同改性生物炭的元素含量和pH Table 5 Element content and pH of different modified biochars |
2.1.4 表面官能团
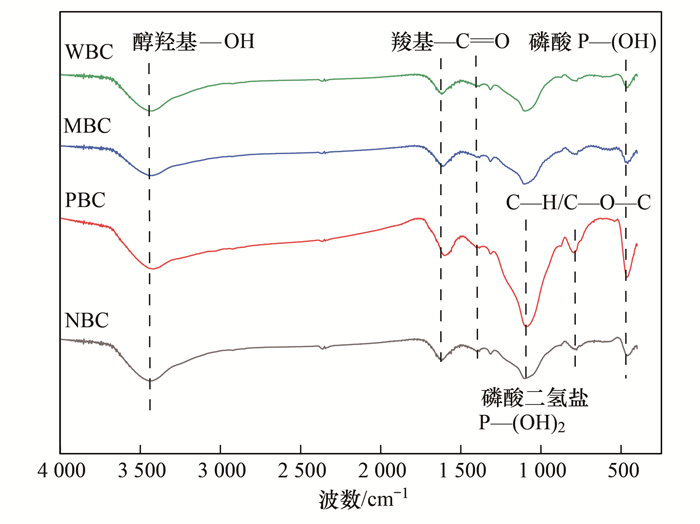
图 2为不同生物炭的傅里叶红外光谱图, 与WBC相比, 改性生物炭在波数为3 455~3 430 cm-1处的醇羟基(—OH)伸缩振动和1 625 cm-1、1 400 cm-1处的羧基(—COO)正反对称伸缩形成的峰值均有不同程度的增强, 表面羟基和羧酸基增多在一定程度上可促进与重金属离子沉淀反应的发生.PBC在波数为1 100 cm-1处的磷酸二氢盐[P—(OH)2]对称伸缩增强最为明显, 这可能是由于改性过程中K3PO4的加入形成较强的含磷官能团, 同时此处与C—O键拉伸、—C键和—OH键变形的峰值重合[32], 各生物炭在此处均有较为明显的峰值.总体来看, 生物炭改性处理使表面官能团种类更加丰富, 官能团数量明显增多, 更利于结合固定重金属.
|
图 2 不同改性生物炭的傅里叶红外光谱图 Fig. 2 FT-IR of different modified biochars |
土壤pH是影响重金属结合形态的重要因素, 增大pH值可以改变土壤中固相物质的表面活性和增强对重金属离子的静电引力, 降低土壤中的重金属活性[6].生物炭本身呈碱性, 且灰分和有机质含量较高, 施入土壤后能有效地提高土壤pH值, 且不同条件改性后生物炭结构、含有的盐类物质以及官能团发生变化[33], 对土壤pH值的影响差异性显著, 总体效果表现为:NBC>PBC>MBC>WBC(图 3).培养30 d时, 与对照组(CK)相比, 添加量为0.5%处理的pH提高6.8%~14.0%, 2%处理的pH提高15.2%~25.49%, 其中P-2和N-2的增幅均达20%以上, 这与李洪达等[34]指出的随着稻壳炭添加量的增大, 土壤pH值不断提高的结果相一致.培养90 d时土壤pH值均有所下降, 这可能是由于土壤具有较强的缓冲性能所导致[35]. P-2和N-2处理的pH增幅仍保持较高水平, 分别为20.5%和19.5%.

|
同一添加量的不同字母表示在P<0.05水平上差异显著 图 3 不同生物炭对土壤pH的影响 Fig. 3 Effect of different modified biochars on soil pH |
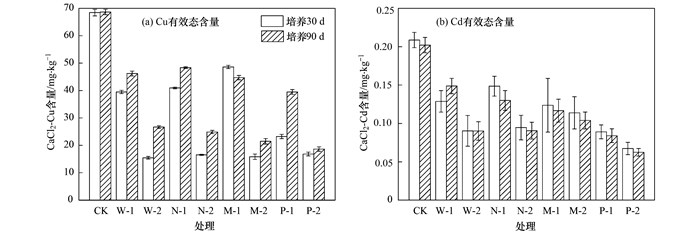
添加不同生物炭后, 土壤中Cu和Cd有效态含量变化如图 4所示.添加量为0.5%, 培养30 d时, 各处理Cu和Cd有效态含量分别降低了28.98%~66.11%和28.81%~57.35%, 其中P-1处理的Cu和Cd钝化效果最好, 分别为66.11%和57.35%.添加量为2%时, 各处理Cu和Cd有效态含量均明显降低, 降低了75.44%~77.44%和45.45%~67.70%, 其中P-2的效果最好, 分别降低77.44%和67.70%.培养90 d后, 土壤中Cu有效态含量整体略有升高, 可能是由于生物炭在土壤中会发生短期缓慢氧化, 将表面吸附的部分重金属重新释放到土壤中[36], 还有部分生物炭表面吸附的重金属发生了解吸[37].土壤中Cd的有效态含量变化受时间影响较小, 与李明遥等[38]通过模拟污染土壤试验中Cd有效态含量随着培养时间的增加而降低相同, 培养90 d后, Cd的有效态整体略有降低, 在短时期内有效态Cd含量相对稳定.
|
图 4 不同处理土壤中Cu和Cd的有效态含量 Fig. 4 Effective content of Cu and Cu in soils after different treatments |
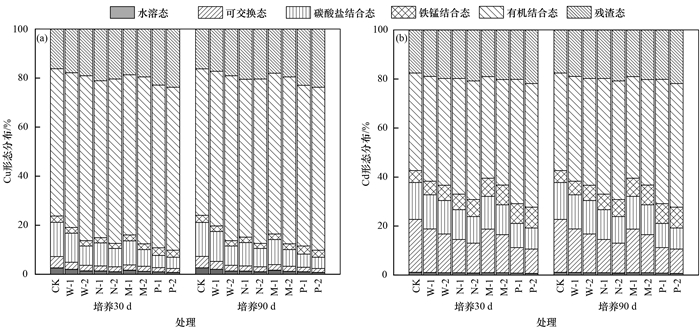
生物炭材料添加后, 土壤中Cu和Cd结合形态的变化如图 5所示.复合污染土壤中Cu和Cd均以有机结合态为主, 添加生物炭有效地促进了弱酸提取态(水溶态、可交换态和碳酸盐结合态)组分向有机结合态和残渣态转化, 与闫翠侠等[39]在Pb和Cd复合污染土中的修复规律一致, 并且随着生物炭的增加, 钝化效果明显提高.当添加量为0.5%, 培养30 d时, W-1、N-1、M-1和P-1处理Cu的钝化效率分别为19.13%、33.43%、29.57%和60.10%, 有机结合态和残渣态比例分别增加了3.11%~6.29%和1.60%~6.67%, 铁锰结合态变化不明显; W-1、N-1、M-1和P-1处理Cd的钝化效率分别为0.98%、2.36%、0.90%和3.91%.当添加量为2%时, 各处理的钝化效率略有上升, 其中PBC对Cu和Cd均有较高的钝化效率, 其次为NBC, MBC和WBC效果差距不大, 这也与上述研究中pH的变化表现一致.与30 d时相比, 培养90 d后Cu和Cd形态均无明显变化, 在短期内其形态较为稳定, 与Jiang等[40]得出的在120 d内秸秆生物炭对Cu的固定作用保持稳定的结果相一致.
|
图 5 不同处理土壤中Cu和Cd的形态分布特征 Fig. 5 Distribution characteristics of Cu and Cd in different treatment soils |
表 6为不同改性方法对生物炭特性以及土壤中重金属的修复效果, 不同原材料、改性方法及土壤环境条件下钝化效果差距较大.在本研究中, 生物炭改性后对复合污染土壤中Cu和Cd的钝化效果明显增强, 但其钝化效率小于其它研究中改性生物炭对外源添加重金属土壤的钝化效率, 这可能是由于外源添加重金属的有效态含量占总量的比值较高, 离子态丰富, 易与生物炭发生吸附反应[41].与单一的Cu和Cd污染土壤相比, 生物炭对复合污染土壤Cu的钝化效率明显高于Cd, 这可能是由于复合污染土壤中Cu的浓度远高于Cd, 并且生物炭对Cu的亲和力更强, 其中MBC对Cu的钝化效率达到Cd的32倍, 这与刘芳等[42]在Cu-Cd二元复合体系中, 氧化石墨烯/聚酰胺对Cu和Cd的亲和力排序一致, 在其它复合污染土壤中, Cd也始终处于较弱的竞争次序[43].通过与其它改性方法的研究结果相比较, PBC对Cu有较高的钝化效率, 分别为61.06%和4.12%, K3PO4改性后引入的含磷基团参与重金属的钝化过程[44], 含磷组分易与重金属离子形成不溶于水的络合物[45]; NBC和MBC与大部分氧化剂或酸碱活化的改性方法对生物炭特性以及土壤中重金属钝化的影响一致, 引入的OH-易与游离的Cu和Cd离子形成Cu(OH)2和Cd(OH)2等物质, 对Cu和Cd的钝化有较为积极的影响.但除此之外, 有研究表明HNO3改性生物炭在外源Cd污染土壤中使可交换态含量增加了7.2%~20.2%, 这可能与HNO3改性后呈酸性, 增加土壤中H+, 导致土壤中CO32-、Fe2+和Mn2+等离子的释放, 碳酸盐和铁锰氧化物与Cd形成的络合物易遭到破坏有关[9].
|
|
表 6 改性生物炭的特性变化及其对重金属污染土壤的修复效果 Table 6 Characteristic changes of modified biochar and its remediation effect on heavy metal contaminated soil |
2.5 相关性分析
对不同生物炭比表面积、孔径、元素组成、pH等与Cu和Cd的形态进行相关性分析, 其相关系数如表 7和表 8所示.比表面积、平均孔径和孔容等表面结构对Cu和Cd的CaCl2提取态和结合形态无明显的相关性, 其相关系数均较低, 尤其是PBC, 其自身孔隙结构相对较差, 但对Cu和Cd的钝化效果远高于其它3种生物炭, 这也反映出生物炭对土壤Cu和Cd的钝化中物理吸附所占的贡献率较小.生物炭pH与Cu和Cd的弱酸提取态均呈负相关, 与有机结合态等相对稳定的形态呈正相关, 相关系数较高, 一方面是由于提高了土壤中pH, 有效地抑制Cu和Cd的生物有效性; 另一方面土壤中有机质含量增加, 使重金属在土壤表面形成有机结合态.H/C与Cu和Cd的弱酸提取态均呈负相关, 与铁锰氧化物结合态和残渣态呈显著正相关, H/C值较低时, 有效地促进Cu和Cd活性较高的形态向相对稳定的形态进行转化, 官能团种类和数量对土壤中Cu和Cd的钝化起到主导作用.根据相关性分析发现, 改性生物炭的pH值增加和芳香化程度的降低是提高土壤中Cu和Cd钝化效率的主要因素.对本研究中的3种改性方法进行比较, K3PO4改性生物炭对Cu和Cd均有较好的钝化效果, 一方面提高环境的pH值, 增强生物炭对土壤重金属的静电吸附作用, 同时引入更多的磷酸盐, 可与重金属结合形成磷酸盐沉淀; 另一方面, H/C增大提高了含氧官能团数量, 增强对重金属的络合能力.因此, 针对Cu和Cd复合污染土壤, 应通过提高生物炭的pH值和提高含氧官能团数量两个主要方面开展生物炭定向改性研究.
|
|
表 7 生物炭理化性质、土壤pH与重金属Cu形态的相关系数1) Table 7 Correlation coefficient of biochar physicochemical properties, soil pH, and heavy metal Cu species |
|
|
表 8 生物炭理化性质、土壤pH与重金属Cd形态的相关系数 Table 8 Correlation coefficient of biochar physicochemical properties, soil pH, and heavy metal Cd species |
2.6 生物炭对土壤重金属的钝化机制
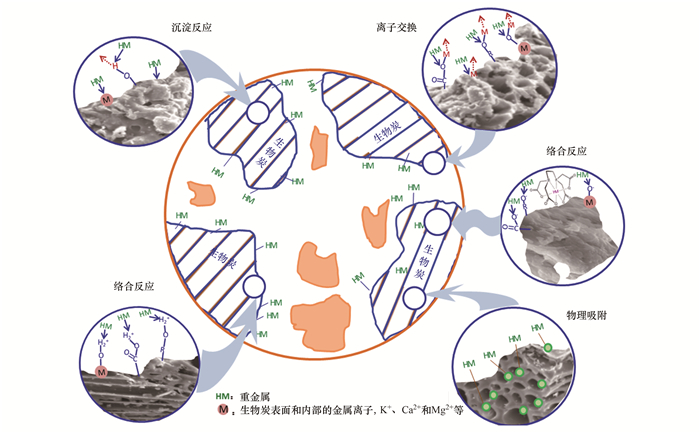
本研究中, 生物炭的钝化效果依次为:PBC>NBC>MBC>WBC, 生物炭改性后比表面积增大, 孔隙更加丰富, 表面的负电荷增加, 能够与土壤中带正电荷的重金属离子产生静电吸引作用[49, 50], 但本研究相关性分析发现, 钝化效果与比表面积和孔隙结构等变化规律并不显著相关, 说明物理吸附反应不是其主要的钝化机制.改性后生物炭表面负载的K+、Ca2+、Na+和Mg2+等盐基离子增多[51], 使土壤中的盐基离子饱和度增加, 能够与土壤中的Cu和Cd进行离子交换[52, 53], 促进了生物炭对重金属的吸附.改性生物炭的羧基、羟基和酚类等表面官能团的增加在钝化土壤重金属方面起着核心作用.相关性分析和FT-IR图谱发现, 改性后生物炭表面具有更加丰富的官能团, 可与重金属离子形成表面络合物或特定的金属配合物[54~56], 其中PBC改性过程中活性位点和官能团数量的增加最为明显, 对土壤中Cu、Cd的钝化效果均最佳.Uchimiya等[57]的研究也表明, 在酸性土壤中改性活性炭对Pb2+、Cd2+和Cu2+的吸附主要作用是表面官能团的络合.NBC和PBC改性过程中引入OH-和PO43-等基团, 易于土壤中与Cu和Cd离子形成氢氧化物和磷酸盐沉淀, 同时矿质灰分参与其中, 与重金属离子或重金属氧化物发生共沉淀[58]. Trakal等[59]的研究也发现生物炭对Cd吸附后引起了CO32-峰的改变, 可能与Cd形成了共沉淀, 与Zhang等[60]的研究利用XRD发现藻类生物炭对Cd的吸附伴随着CdCO3和CdPO4矿物的形成相一致.
综上分析, 改性生物炭对土壤重金属的钝化作用机制以络合反应、离子交换和沉淀反应为主, 物理吸附为辅, 多种作用机制共同主导, 协同进行的(图 6).
|
图 6 生物炭固定重金属的机制 Fig. 6 Mechanism of biochar immobilization of heavy metals |
(1) 改性后生物炭的比表面积和孔容均有不同程度的增大, 其大小顺序为:WBC < PBC < MBC < NBC, 而平均孔径的顺序为:MBC < NBC < PBC < WBC; 表面官能团的种类均无明显变化, 但吸收特征峰值发生改变, 其中PBC的变化最为明显.
(2) 生物炭的添加可显著提高土壤pH值, PBC和NBC的效果较好, 增幅均达到20%以上; 对复合污染土壤中Cu和Cd的有效态含量均明显降低, 其中添加2%PBC时, Cu和Cd有效态含量分别降低75.44%和67.70%, 钝化效率分别为61.06%和4.12%, 其次为NBC, MBC和WBC对Cu和Cd的钝化效果差距不大.
(3) 改性生物炭比表面积和孔隙结构与Cu和Cd的形态变化无显著相关, 与H/C和pH显著相关, 其作用机制以络合反应为主, 多种作用机制协同进行.
| [1] | 环境保护部, 国土资源部. 全国土壤污染状况调查公报[EB/OL]. http://www.gov.cn/foot/site1/20140417/782bcb88840814ba158d01.pdf, 2014-04-17. |
| [2] | Ma J W, Wang F Y, Huang Z H, et al. Simultaneous removal of 2, 4-dichlorophenol and Cd from soils by electrokinetic remediation combined with activated bamboo charcoal[J]. Journal of Hazardous Materials, 2010, 176(1-3): 715-720. DOI:10.1016/j.jhazmat.2009.11.093 |
| [3] |
肖亮亮, 丁园. 药渣生物炭联合麦饭石对铜镉污染土壤修复研究[J]. 环境科学与技术, 2019, 42(2): 145-150. Xiao L L, Ding Y. Study on remediation of Cu and Cd in contaminated soil with the combination of biochar and maifanite[J]. Environmental Science & Technology, 2019, 42(2): 145-150. |
| [4] | Hamid Y, Tang L, Sohail M I, et al. An explanation of soil amendments to reduce cadmium phytoavailability and transfer to food chain[J]. Science of the Total Environment, 2019, 660: 80-96. DOI:10.1016/j.scitotenv.2018.12.419 |
| [5] | Lu H P, Li Z A, Gascó G, et al. Use of magnetic biochars for the immobilization of heavy metals in a multi-contaminated soil[J]. Science of the Total Environment, 2018, 622-623: 892-899. DOI:10.1016/j.scitotenv.2017.12.056 |
| [6] | Jing F, Chen C, Chen X M, et al. Effects of wheat straw derived biochar on cadmium availability in a paddy soil and its accumulation in rice[J]. Environmental Pollution, 2020, 257. DOI:10.1016/j.envpol.2019.113592 |
| [7] | Wang B, Gao B, Fang J E. Recent advances in engineered biochar productions and applications[J]. Critical Reviews in Environmental Science and Technology, 2017, 47(22): 2158-2207. DOI:10.1080/10643389.2017.1418580 |
| [8] |
刘俐, 高新华, 宋存义, 等. 土壤中镉的赋存行为及迁移转化规律研究进展[J]. 能源环境保护, 2006, 20(2): 6-9. Liu L, Gao X H, Song G Y, et al. Progress in the study of cadmium occurrence and transportation in soils[J]. Energy Environmental Protection, 2006, 20(2): 6-9. DOI:10.3969/j.issn.1006-8759.2006.02.002 |
| [9] |
杨兰, 李冰, 王昌全, 等. 改性生物炭材料对稻田原状和外源镉污染土钝化效应[J]. 环境科学, 2016, 37(9): 3562-3574. Yang L, Li B, Wang C Q, et al. Effect of modified biochars on soil cadmium stabilization in paddy soil suffered from original or exogenous contamination[J]. Environmental Science, 2016, 37(9): 3562-3574. |
| [10] | Sun C, Chen T, Huang Q, et al. Enhanced adsorption for Pb(Ⅱ) and Cd(Ⅱ) of magnetic rice husk biochar by KMnO4 modification[J]. Environmental Science and Pollution Research, 2019, 26(9): 8902-8913. DOI:10.1007/s11356-019-04321-z |
| [11] | Zhang J Y, Zhou H, Gu J F, et al. Effects of nano-Fe3O4-modified biochar on iron plaque formation and Cd accumulation in rice (Oryza sativa L.)[J]. Environmental Pollution, 2020, 260. DOI:10.1016/j.envpol.2020.113970 |
| [12] |
陈雪娇, 林启美, 肖弘扬, 等. 改性油菜秸秆生物质炭吸附/解吸Cd2+特征[J]. 农业工程学报, 2019, 35(18): 220-227. Chen X J, Lin Q M, Xiao H Y, et al. Characteristics of Cd2+ sorption/desorption of modified oilrape straw biochar[J]. Transactions of the Chinese Society of Agricultural Engineering, 2019, 35(18): 220-227. DOI:10.11975/j.issn.1002-6819.2019.18.027 |
| [13] | Peng H B, Gao P, Chu G, et al. Enhanced adsorption of Cu(Ⅱ) and Cd(Ⅱ) by phosphoric acid-modified biochars[J]. Environmental Pollution, 2017, 229: 846-853. DOI:10.1016/j.envpol.2017.07.004 |
| [14] |
汪怡, 李莉, 宋豆豆, 等. 玉米秸秆改性生物炭对铜、铅离子的吸附特性[J]. 农业环境科学学报, 2020, 39(6): 1303-1313. Wang Y, Li L, Song D D, et al. Copper and lead ion adsorption characteristics of modified corn stalk biochars[J]. Journal of Agro-Environment Science, 2020, 39(6): 1303-1313. |
| [15] | Li C J, Zhang L, Gao Y, et al. Facile synthesis of nano ZnO/ZnS modified biochar by directly pyrolyzing of zinc contaminated corn stover for Pb(Ⅱ), Cu(Ⅱ) and Cr(Ⅵ) removals[J]. Waste Management, 2018, 79: 625-637. DOI:10.1016/j.wasman.2018.08.035 |
| [16] | Zhang H, Shao J A, Zhang S H, et al. Effect of phosphorus-modified biochars on immobilization of Cu(Ⅱ), Cd(Ⅱ), and As(Ⅴ) in paddy soil[J]. Journal of Hazardous Materials, 2020, 390. DOI:10.1016/j.jhazmat.2019.121349 |
| [17] |
吴志能, 谢苗苗, 王莹莹. 我国复合污染土壤修复研究进展[J]. 农业环境科学学报, 2016, 35(12): 2250-2259. Wu Z N, Xie M M, Wang Y Y. Remediation of soils with combined pollution in China: a review[J]. Journal of Agro-Environment Science, 2016, 35(12): 2250-2259. DOI:10.11654/jaes.2016-0863 |
| [18] | Li B, Yang L, Wang C Q, et al. Adsorption of Cd(Ⅱ) from aqueous solutions by rape straw biochar derived from different modification processes[J]. Chemosphere, 2017, 175: 332-340. DOI:10.1016/j.chemosphere.2017.02.061 |
| [19] | 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. |
| [20] |
章明奎, 方利平, 周翠. 污染土壤重金属的生物有效性和移动性评价: 四种方法比较[J]. 应用生态学报, 2006, 17(8): 1501-1504. Zhang M K, Fang L P, Zhou C. Evaluation of heavy metals bioavailability and mobility in polluted soils: a comparison of four methods[J]. Chinese Journal of Applied Ecology, 2006, 17(8): 1501-1504. DOI:10.3321/j.issn:1001-9332.2006.08.028 |
| [21] | Tessier A, Campbell P G C, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 1979, 51(7): 844-851. DOI:10.1021/ac50043a017 |
| [22] |
陆嫚嫚, 马洁晨, 张学胜, 等. MnOx负载生物质炭对Cu2+、Zn2+的吸附机理研究[J]. 农业环境科学学报, 2018, 37(10): 2297-2303. Lu M M, Ma J C, Zhang X S, et al. The properties and mechanism of Cu2+ and Zn2+ sorption by MnOx-loaded biochar[J]. Journal of Agro-Environment Science, 2018, 37(10): 2297-2303. DOI:10.11654/jaes.2017-1684 |
| [23] | Faheem M, Yu H X, Liu J, et al. Preparation of MnOx-loaded biochar for Pb2+ removal: adsorption performance and possible mechanism[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 66: 313-320. DOI:10.1016/j.jtice.2016.07.010 |
| [24] | Song Z G, Lian F, Yu Z H, et al. Synthesis and characterization of a novel MnOx-loaded biochar and its adsorption properties for Cu2+ in aqueous solution[J]. Chemical Engineering Journal, 2014, 242: 36-42. DOI:10.1016/j.cej.2013.12.061 |
| [25] | Chen T, Zhang Y X, Wang H T, et al. Influence of pyrolysis temperature on characteristics and heavy metal adsorptive performance of biochar derived from municipal sewage sludge[J]. Bioresource Technology, 2014, 164: 47-54. DOI:10.1016/j.biortech.2014.04.048 |
| [26] | Zhu S H, Zhao J J, Zhao N, et al. Goethite modified biochar as a multifunctional amendment for cationic Cd(Ⅱ), anionic As(Ⅲ), roxarsone, and phosphorus in soil and water[J]. Journal of Cleaner Production, 2020, 247. DOI:10.1016/j.jclepro.2019.119579 |
| [27] | Yakout S M, Daifullah A E H M, El-Reefy S A. Pore structure characterization of chemically modified biochar derived from rice straw[J]. Environmental Engineering and Management Journal, 2015, 14(2): 473-480. DOI:10.30638/eemj.2015.049 |
| [28] | Leng L J, Huang H J, Li H, et al. Biochar stability assessment methods: a review[J]. Science of the Total Environment, 2019, 647: 210-222. DOI:10.1016/j.scitotenv.2018.07.402 |
| [29] | Enders A, Hanley K, Whitman T, et al. Characterization of biochars to evaluate recalcitrance and agronomic performance[J]. Bioresource Technology, 2012, 114: 644-653. DOI:10.1016/j.biortech.2012.03.022 |
| [30] | Wang H Y, Gao B, Wang S S, et al. Removal of Pb(Ⅱ), Cu(Ⅱ), and Cd(Ⅱ) from aqueous solutions by biochar derived from KMnO4 treated hickory wood[J]. Bioresource Technology, 2015, 197: 356-362. DOI:10.1016/j.biortech.2015.08.132 |
| [31] | Xia Y, Liu H J, Guo Y C, et al. Immobilization of heavy metals in contaminated soils by modified hydrochar: efficiency, risk assessment and potential mechanisms[J]. Science of the Total Environment, 2019, 685: 1201-1208. DOI:10.1016/j.scitotenv.2019.06.288 |
| [32] | Sevilla M, Fuertes A B. Chemical and structural properties of carbonaceous products obtained by hydrothermal carbonization of saccharides[J]. Chemistry-A European Journal, 2009, 15(16): 4195-4203. DOI:10.1002/chem.200802097 |
| [33] | Yuan J H, Xu R K, Zhang H. The forms of alkalis in the biochar produced from crop residues at different temperatures[J]. Bioresource Technology, 2011, 102(3): 3488-3497. DOI:10.1016/j.biortech.2010.11.018 |
| [34] |
李洪达, 李艳, 周薇, 等. 稻壳生物炭对矿区重金属复合污染土壤中Cd、Zn形态转化的影响[J]. 农业环境科学学报, 2018, 37(9): 1856-1865. Li H D, Li Y, Zhou W, et al. Effects of rice-husk-derived biochar on the morphological transformation of Cd and Zn in mining area soils polluted by heavy metals[J]. Journal of Agro-Environment Science, 2018, 37(9): 1856-1865. |
| [35] |
王俊楠, 程珊珊, 展文豪, 等. 磁性生物炭的合成及对土壤重金属污染的钝化效果[J]. 环境科学, 2020, 41(5): 2381-2389. Wang J N, Cheng S S, Zhan W H, et al. Synthesis of magnetic biochar and its application in the remediation of heavy metal contaminated soils[J]. Environmental Science, 2020, 41(5): 2381-2389. |
| [36] | Beesley L, Moreno-Jiménez E, Gomez-Eyles J L. Effects of biochar and greenwaste compost amendments on mobility, bioavailability and toxicity of inorganic and organic contaminants in a multi-element polluted soil[J]. Environmental Pollution, 2010, 158(6): 2282-2287. DOI:10.1016/j.envpol.2010.02.003 |
| [37] |
张莹, 吴萍, 孙庆业, 等. 长期施用生物炭对土壤中Cd吸附及生物有效性的影响[J]. 农业环境科学学报, 2020, 39(5): 1019-1025. Zhang Y, Wu P, Sun Q Y, et al. Effect of long-term application of biochar on Cd adsorption and bioavailability in farmland soils[J]. Journal of Agro-Environment Science, 2020, 39(5): 1019-1025. |
| [38] |
李明遥, 杜立宇, 张妍, 等. 不同裂解温度水稻秸秆生物炭对土壤Cd形态的影响[J]. 水土保持学报, 2013, 27(6): 261-264. Li M Y, Du L Y, Zhang Y, et al. Influence of pyrolysis temperatures of biochar obtained from the rice straw on cadmium forms[J]. Journal of Soil and Water Conservation, 2013, 27(6): 261-264. DOI:10.3969/j.issn.1009-2242.2013.06.050 |
| [39] |
闫翠侠, 贾宏涛, 孙涛, 等. 鸡粪生物炭表征及其对水和土壤镉铅的修复效果[J]. 农业工程学报, 2019, 35(13): 225-233. Yan C X, Jia H T, Sun T, et al. Characteristics of chicken manure biochars and its effect on Cd and Pb remediation in water and soil[J]. Transactions of the Chinese Society of Agricultural Engineering, 2019, 35(13): 225-233. DOI:10.11975/j.issn.1002-6819.2019.13.027 |
| [40] | Jiang J, Xu R K. Application of crop straw derived biochars to Cu(Ⅱ) contaminated Ultisol: evaluating role of alkali and organic functional groups in Cu(Ⅱ) immobilization[J]. Bioresource Technology, 2013, 133: 537-545. DOI:10.1016/j.biortech.2013.01.161 |
| [41] |
王义祥, 赖永翔, 叶菁, 等. 生物炭对不同镉污染土壤钝化效果和小白菜镉吸收的影响[J]. 土壤通报, 2019, 50(3): 713-718. Wang Y X, Lai Y X, Ye J, et al. Effects of biochar on passivation and uptake of cadmium by brassica chinensis in cadmium-polluted soils[J]. Chinese Journal of Soil Science, 2019, 50(3): 713-718. |
| [42] |
刘芳, 贺盛福, 张帆, 等. Cu(Ⅱ)和Cd(Ⅱ)在氧化石墨烯/聚酰胺-胺复合材料上的竞争吸附[J]. 环境工程学报, 2017, 11(2): 892-898. Liu F, He S F, Zhang F, et al. Competitive adsorption of Cu(Ⅱ) and Cd(Ⅱ) on GO/PAMAMs composites[J]. Chinese Journal of Environmental Engineering, 2017, 11(2): 892-898. |
| [43] | Fan J J, Cai C, Chi H F, et al. Remediation of cadmium and lead polluted soil using thiol-modified biochar[J]. Journal of Hazardous Materials, 2020, 388. DOI:10.1016/j.jhazmat.2020.122037 |
| [44] | 蔡键. 富磷改性毛竹生物炭对水体中重金属镉的吸附研究[D]. 武汉: 华中科技大学, 2018. |
| [45] | Zhang S H, Zhang H, Cai J, et al. Evaluation and prediction of cadmium removal from aqueous solution by phosphate-modified activated bamboo biochar[J]. Energy & Fuels, 2018, 32. DOI:10.1021/acs.energyfuels.7b03159 |
| [46] | Tan X, Wei W X, Xu C B, et al. Manganese-modified biochar for highly efficient sorption of cadmium[J]. Environmental Science and Pollution Research, 2020, 27(9): 9126-9134. DOI:10.1007/s11356-019-07059-w |
| [47] | Wu C, Shi L Z, Xue S G, et al. Effect of sulfur-iron modified biochar on the available cadmium and bacterial community structure in contaminated soils[J]. Science of the Total Environment, 2019, 647: 1158-1168. DOI:10.1016/j.scitotenv.2018.08.087 |
| [48] | Wang Y, Wang L X, Deng X Y, et al. A facile pyrolysis synthesis of biochar/ZnO passivator: immobilization behavior and mechanisms for Cu(Ⅱ) in soil[J]. Environmental Science and Pollution Research, 2020, 27(2): 1888-1897. DOI:10.1007/s11356-019-06888-z |
| [49] | Herath I, Kumarathilaka P, Navaratne A, et al. Immobilization and phytotoxicity reduction of heavy metals in serpentine soil using biochar[J]. Journal of Soils & Sediments, 2015, 15: 126-138. |
| [50] | Liang B Q, Lehmann J, Solomon D, et al. Black carbon increases cation exchange capacity in soils[J]. Soil Science Society of America Journal, 2006, 70(5): 1719-1730. DOI:10.2136/sssaj2005.0383 |
| [51] |
王震宇, 刘国成, Xing M, 等. 不同热解温度生物炭对Cd(Ⅱ)的吸附特性[J]. 环境科学, 2014, 35(12): 4735-4744. Wang Z Y, Liu G C, Xing M, et al. Adsorption of Cd(Ⅱ) varies with biochars derived at different pyrolysis temperatures[J]. Environmental Science, 2014, 35(12): 4735-4744. |
| [52] | Wang M M, Zhu Y, Cheng L R, et al. Review on utilization of biochar for metal-contaminated soil and sediment remediation[J]. Journal of Environmental Sciences, 2018, 63: 156-173. DOI:10.1016/j.jes.2017.08.004 |
| [53] | Zeng Z Z, Wang X L, Gou J F, et al. Effects on Ni and Cd speciation in sewage sludge during composting and co-composting with steel slag[J]. Waste Management & Research, 2014, 32(3): 179-185. |
| [54] | Wang Z Y, Liu G C, Zheng H, et al. Investigating the mechanisms of biochar's removal of lead from solution[J]. Bioresource Technology, 2015, 177: 308-317. DOI:10.1016/j.biortech.2014.11.077 |
| [55] | Mohamed I, Zhang G S, Li Z G, et al. Ecological restoration of an acidic Cd contaminated soil using bamboo biochar application[J]. Ecological Engineering, 2015, 84: 67-76. DOI:10.1016/j.ecoleng.2015.07.009 |
| [56] | Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+ sorption mechanisms by sludge-derived biochar[J]. Water Research, 2012, 46(3): 854-862. DOI:10.1016/j.watres.2011.11.058 |
| [57] | Uchimiya M, Klasson K T, Wartelle L H, et al. Influence of soil properties on heavy metal sequestration by biochar amendment: 1. Copper sorption isotherms and the release of cations[J]. Chemosphere, 2011, 82(10): 1431-1437. DOI:10.1016/j.chemosphere.2010.11.050 |
| [58] | Uchimiya M, Lima I M, Thomas Klasson K, et al. Immobilization of heavy metal ions (CuⅡ, CdⅡ, NiⅡ, and PbⅡ) by broiler litter-derived biochars in water and soil[J]. Journal of Agricultural and Food Chemistry, 2010, 58(9): 5538-5544. DOI:10.1021/jf9044217 |
| [59] | Trakal L, Bingöl D, Poho Dřely M, et al. Geochemical and spectroscopic investigations of Cd and Pb sorption mechanisms on contrasting biochars: engineering implications[J]. Bioresource Technology, 2014, 171: 442-451. DOI:10.1016/j.biortech.2014.08.108 |
| [60] | Zhang F, Wang X, Yin D X, et al. Efficiency and mechanisms of Cd removal from aqueous solution by biochar derived from water hyacinth (Eichornia crassipes)[J]. Journal of Environmental Management, 2015, 153: 68-73. |
 2021, Vol. 42
2021, Vol. 42


