2. 中国科学院大学, 北京 100049;
3. 中国科学院生态环境研究中心饮用水科学与技术重点实验室, 北京 100085
2. University of Chinese Academy of Sciences, Beijing 100049, China;
3. Key Laboratory of Drinking Water Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China
锰(Mn)是地壳中含量仅次于铁的过渡金属元素并广泛分布于自然环境中, 它不仅是生物活动所必需的微量元素, 还是一种活泼的矿物相, 广泛地参与了氧化还原反应, 在元素地球化学循环中发挥着重要的作用[1].而它的氧化物——锰氧化物, 由于具有较强的吸附和氧化能力而被应用于水处理领域[2, 3].有研究发现, 生物介导的锰氧化物——生物锰氧化物具有更高的比表面积, 在吸附性能上远高于化学合成的锰氧化物, 在生物锰氧化物的形成过程中, 微生物可以通过分泌与锰氧化相关的酶或特异性的代谢途径, 将溶解态的Mn(Ⅱ)氧化为不溶性的Mn(Ⅲ/Ⅳ)氧化物[4, 5].
人工湿地是一种经人为设计、建造、运营和管理的污水处理系统, 广泛应用于城镇生活污水、农村废水、养殖废水和工业废水的处理, 具有成本低、能耗低、运行管理方便及环保等特点[6~10].通过基质的吸附、微生物的同化和异化作用以及植物的吸收三者的协同效应, 不仅能够有效去除COD、TN、TP和SS等常规污染物[11], 还能去除一些新型有机污染物, 如有机磷农药[12]和药物及个人护理品[13].湿地中广泛分布着锰氧化微生物, 而在湿地植物根系附近会形成铁锰氧化物胶膜[14].有研究发现, 锰氧化物在模拟人工湿地中氧化污染物后会生成Mn(Ⅱ), 再经过微生物的作用形成生物锰氧化物, Mn(Ⅱ)与生物锰氧化物之间的循环可增强污染物的去除[15].
基于以往发现[15]及前期实验室研究[16], 笔者推测在实际人工湿地中加入锰砂基质, 利用锰氧化物自身的氧化吸附性质强化去除污染物, 同时锰氧化物还原生成的Mn(Ⅱ)又能被土壤及根系锰氧化微生物氧化为Mn(Ⅲ/Ⅳ), 既能防止Mn(Ⅱ)在水中的释放, 又能生成生物锰氧化物进一步去除污染物.而芦苇根系的泌氧功能促进根系微生物的生长, 间接强化了锰氧化的过程.为验证该推测, 本文通过向实际人工湿地中加入锰砂, 研究锰砂填料人工湿地对农村生活污水的强化处理效果, 分析植物根系微生物群落结构以探讨锰砂填料人工湿地对污染物的强化去除机制.本研究将强化锰氧化过程引入到湿地水处理技术中, 以期为人工湿地处理技术改进提供一种新思路.
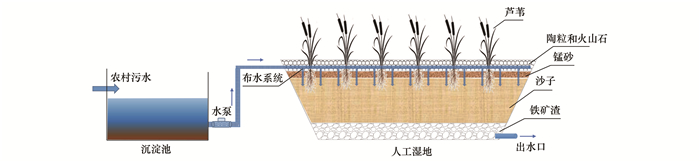
1 材料与方法 1.1 中试研究的建立中试人工湿地位于石家庄市晋州市龙头村(38°03′19.6″N, 115°03′22.3″E), 该地为暖温带大陆性季风气候, 年平均气温14.9℃, 年平均降水量为455.8 mm.中试研究采用2块长12 m, 宽12 m, 深度为1.5 m的人工湿地.湿地内部由下到上分别填充铁矿渣、沙子、陶粒和火山石.一块为填加100 kg锰砂的人工湿地(锰砂约含40% MnO2).而另一块为不填锰砂的人工湿地(对照).水流方向由上到下, 布水层位于陶粒和火山石覆盖层之间.湿地上方种植芦苇, 芦苇来自于当地苗圃市场, 种植密度约为50棵·m-2(图 1).
|
图 1 锰砂人工湿地工艺示意 Fig. 1 Schematic diagram of the constructed wetlands |
人工湿地于2019年5月开始运行, 进水为龙头村生活污水, 由水泵将生活污水从沉淀池泵入布水系统, 采用间歇进水的方式, 平均每块人工湿地的处理负荷为15 t·d-1.待人工湿地达到稳定后开始实验(2019年12月).在不同月份分别对进水和出水进行取样, 使用便携式多参数水质仪(MYRON L Company, 美国)原位测定pH和水温(T), 采用溶解氧仪(哈希HQ30d, 美国)原位测定溶解氧(DO)浓度, 在实验室进行COD、DOC、TN、NO3--N、NH4+-N和TP的测定.
按照等距采样法, 将每块人工湿地设置3个取样点, 对取样点距地面10~20 cm处的芦苇根系土和非根系土进行取样, 将样品密封并冷冻保存(-80℃), 用于测定根系土和非根系土中微生物群落结构.
使用抖落法区分根系土与非根系土, 即挖掘出大体完整的芦苇根系, 将松散的土壤抖落并丢弃, 仍然附在根系上的土壤被称为根系土, 距离植物根系5 cm以外的未附着在根系上的土壤被称为非根系土.采集时避免不同样品之间的交叉污染.
1.3 理化指标测定水质指标的测定参照文献[17], COD采用重铬酸钾法测定, NH4+-N采用纳氏试剂分光光度法测定, NO3--N采用紫外分光光度法测定, TN采用碱性过硫酸钾消解法测定, TP采用过硫酸钾消解-钼锑抗分光光度法测定, DOC使用总有机碳分析仪(Shimadzu TOC-VCPH, 日本)测定.
1.4 DNA提取及16S rRNA数据分析使用土壤DNA提取试剂盒(PowerSoil DNA Kit, QIAGEN, 德国)对土壤样品进行总DNA的提取.样品送至广东美格基因科技有限公司, 通过引物515F(5′-GTGCCAGCMGCCGCGGTAA-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)对16S rRNA基因的V4区进行扩增, 基于NovaSeqPE250测序平台, 对样品进行双末端测序.原始reads经过去杂、去引物、去接头, 以及过滤低质量的reads, 得到clean data.使用QIIME2[18]的pipeline处理过滤后的16S rRNA扩增子序列的clean data, 通过合并双端数据、识别及过滤嵌合子、去噪和冗余, 生成扩增子序列变异(amplicon sequence variants, ASVs).共获得了1 206 144个ASV, 每个样本的ASV数量范围为50 256~62 682.对所有样品进行不放回的重抽样标准化, 使ASV表中每个样本的ASV总数均为50 265.利用QIIME2分析包括Shannon、Chao1和Pielou指数在内的α多样性指数, 使用Bray-Curtis距离矩阵分析β多样性, 并使用R中的vegan程序包(v2.5.2)[19]对距离矩阵进行PCoA分析, 用于表示群落样本的结构分布特征.
1.5 数据统计与分析采用配对样本Wilcoxon符号秩检验对锰砂和对照湿地的水质及微生物相对丰度进行差异性分析.采用皮尔森检验法(检验水平为P<0.05和P<0.01)探讨温度与NH4+-N去除率的相关性.采用ANOSIM相似性分析, 检验2块人工湿地中生物群落结构是否具有显著差异.
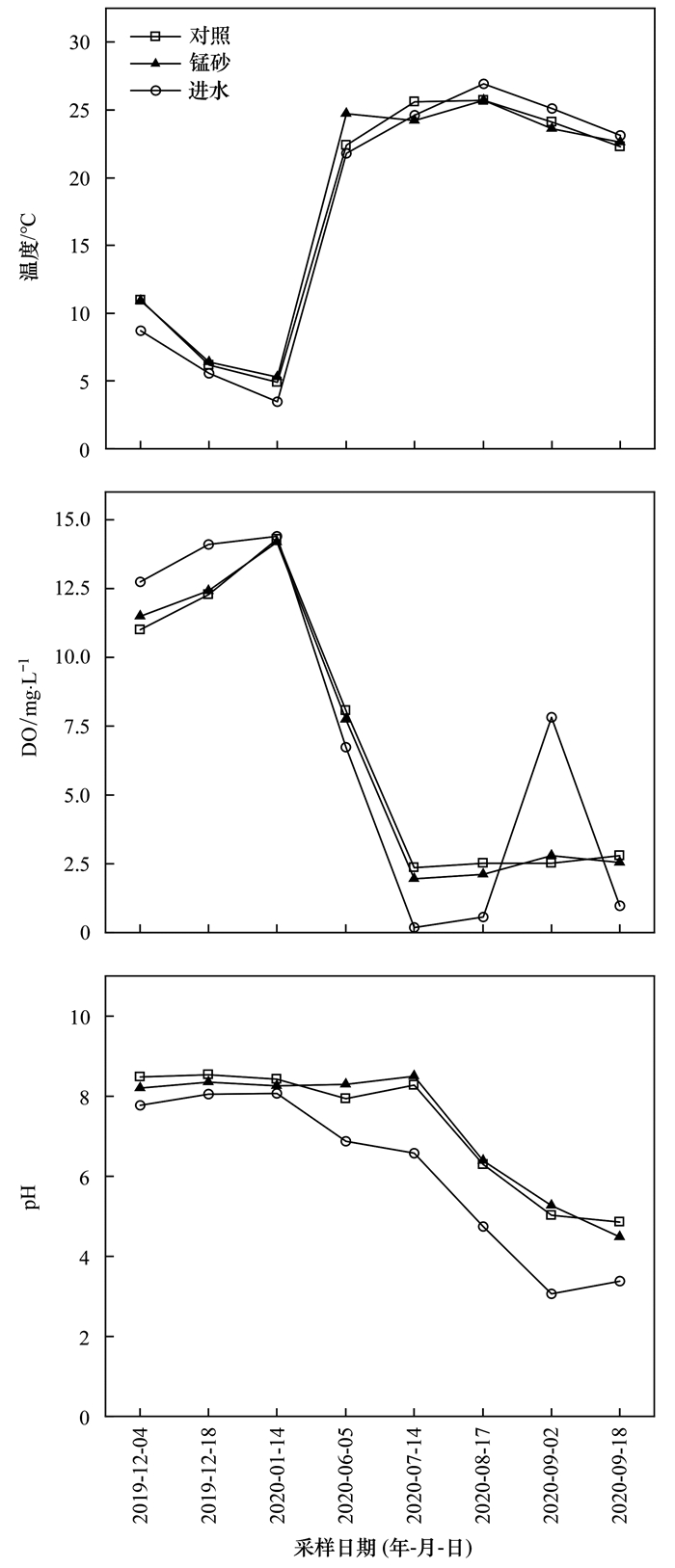
2 结果与讨论 2.1 人工湿地对污染物的去除效果采样期间锰砂及对照人工湿地中水温、pH及DO的变化见图 2.随着季节变化, 湿地进水水温(3.5~26.9℃)及理化性质变化明显.DO从1月最高14.4mg·L-1降低至0.19mg·L-1(7月), 而进水pH逐渐下降, 且经过湿地处理后, pH均显著升高.锰砂人工湿地相比对照未发现水温、pH及DO有明显差异.
|
图 2 采样期间水温、pH及DO变化分析 Fig. 2 Variation of water temperature, pH, and DO during the sampling period |
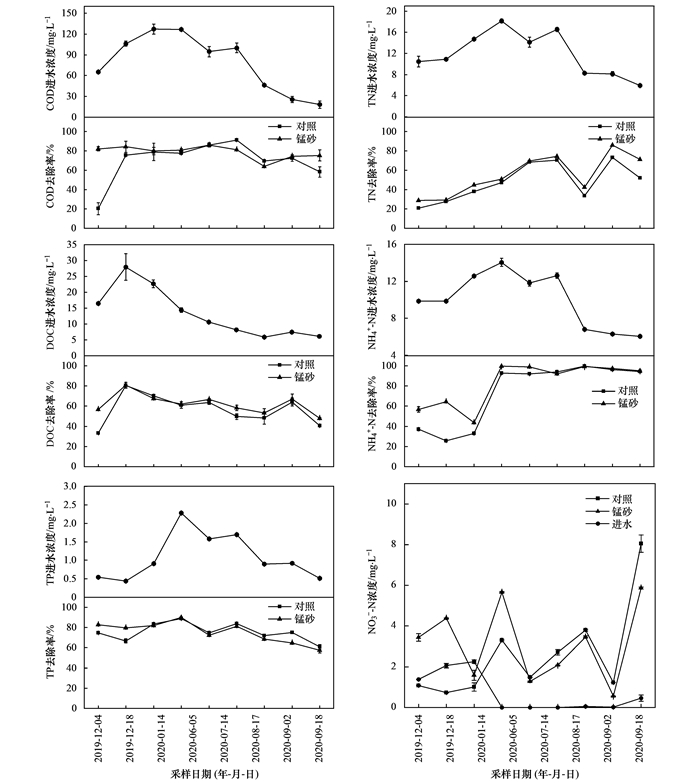
对比锰砂及对照人工湿地的水处理效果(图 3), 发现随着季节变化, 尽管进水浓度发生明显变化, 2块湿地(锰砂及对照)对COD和TP的去除率趋于平稳且两者无显著差异(P>0.05, Wilcoxon符号秩检验).DOC的去除率在20%~80%之间波动, 且锰砂人工湿地的去除率显著高于对照人工湿地(P=0.028).TN的去除率随月份呈波动上升的趋势, 锰砂人工湿地对其的去除率显著高于对照湿地(P=0.008). 2块湿地对NH4+-N的去除率在12月至次年1月(冬季)较低, 8~9月(夏秋季)趋于稳定, 且锰砂人工湿地对其的去除率在冬季显著高于对照湿地(P=0.047), 而在夏秋季无显著差异.此外, 本实验结果发现湿地处理后出水的NO3--N浓度相比于进水有明显上升, 通过分析NH4+-N减少量与NO3--N增加量的相关性(一元回归), 发现约22%的NH4+-N转化为NO3--N.
|
图中误差线为2次测量值的平均偏差 图 3 锰砂及对照人工湿地对污染物的去除 Fig. 3 Pollutant removal in the constructed wetlands with and without manganese oxides |
NH4+-N去除率与水温的皮尔森分析显示两者具有显著正相关(P<0.01), 这表明温度升高可导致湿地微生物硝化作用的显著上升.锰砂湿地相比于对照湿地在冬季去除或转化NH4+-N作用较为明显, 而在夏秋季无明显差异(冬季:P=0.047; 夏秋季:P=0.25), 这可能是由于冬季微生物作用弱, 而锰砂湿地中的锰氧化物可作为电子中介, 催化氧化NH4+-N, 促进了NH4+-N的转化[20].转化途径为MnOx+NH4++H+NO3-+Mn2++H2O或MnOx+NH4++H+N2+Mn2++H2O.而夏秋季2块湿地都以微生物转化去除为主, 去除率均在92%~99%, 导致差异并不明显.
人工湿地上下潜流型的结构以及芦苇根系的泌氧功能, 为进水补充溶解氧提供了条件, 并且在出水中未检测到锰离子析出, 因此笔者推测在人工湿地上层好氧层及植物根系附近发生了锰氧化反应.然而本研究中锰砂与对照人工湿地的COD、TP、NH4+-N和TN的去除率差异相对较小, 可能是由进水浓度较低或湿地锰氧化物加入量较少导致.此外, 有研究表明, 含铁基质的人工湿地对TN和TP具有较高的去除率[21], 而本实验中的人工湿地底部支撑层均为铁矿渣, 这可能是导致锰砂与对照人工湿地污染物去除率差异较小的原因.
2.2 微生物群落结构分析为进一步分析锰砂及对照人工湿地对污染物的微生物去除的机制, 对12月至次年1月以及8~9月的根系土及非根系土(共24个样品)进行了细菌16S rRNA测序与分析.
2.2.1 微生物群落多样性分析16S rRNA测序分析共获得1 206 144个ASV, 对其α多样性分析可以看出(表 1), 锰砂人工湿地中细菌群落的丰富度和多样性指数均显著高于对照湿地(P<0.05, Wilcoxon检验), 这种差异在冬季的根系土中更为明显.这表明锰砂的加入能显著提高冬季时湿地根系中微生物群落的丰富度和多样性.可能是由于加入的锰砂具有疏松多孔的结构特征, 而微生物作用下生成的生物锰氧化物具有更小的粒径和更高的比表面积[5], 便于微生物附着和聚集.而夏秋季锰砂与对照湿地的差异较小可能是由于夏秋季温度高, 便于微生物生长造成两者差异较小, 这与氨氮去除率变化规律相符合.此外, 芦苇根系中微生物群落的丰富度和多样性均高于非根系土(P<0.05, Wilcoxon检验), 这可能是因为植物根系会分泌有机物和氧气, 促进了芦苇根系附近的微生物的生长.
|
|
表 1 人工湿地中微生物群落的多样性指数1) Table 1 Diversity indices of microbial communities in the constructed wetlands |
2.2.2 微生物群落差异性分析
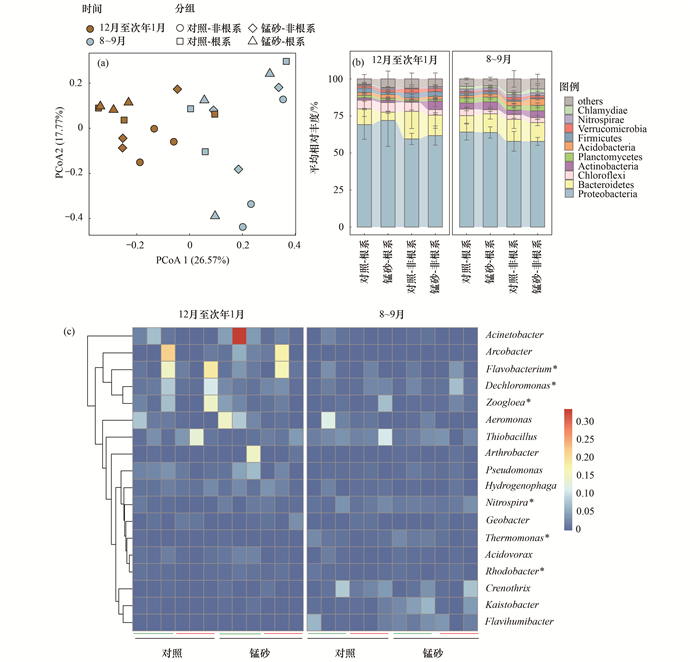
主坐标分析结果表明[图 4(a)], 季节变化是导致微生物群落结构差异的关键因子.通过ANOSIM计算发现锰砂的加入对冬季人工湿地微生物群落结构无明显影响(R=-0.086, P=0.683), 对夏秋季的微生物群落结构也影响较小(R=0.014, P=0.392).
|
图 4 锰砂及对照湿地中微生物群落的PCoA分析及其在门和属水平上的组成 Fig. 4 PCoA analysis, and composition at phylum level and genus level of microbial communities in the constructed wetlands |
对微生物群落在门水平上的组成进行了分析[图 4(b)], 结果表明, 锰砂和对照湿地中变形菌门(Proteobacteria)为相对丰度最高的菌门, 占50.9%~88.16%, 其次是拟杆菌门(Bacteroidetes)、绿弯菌门(Chloroflexi)和放线菌门(Actinobacteria).这些菌门广泛存在于自然界中, 已有研究报道发现这些菌门对污染物的去除具有重要作用[22~25].通过比较分析, 锰砂与对照湿地在群落组成上无显著差异(P>0.05), 表明锰砂的加入对微生物群落结构在门水平上影响较小.
在属水平中选取了丰度前20的菌属(除去2个未能注释的菌属), 样本中丰度前18位菌属的热图如图 4(c)所示, 可以看出, 因季节变化导致的群落结构差异较为明显.对氮转化相关菌属的相对丰度进行差异性分析, 结果显示, Flavobacterium、Dechloromonas和Zoogloea等菌属在低温时期的相对丰度显著高于8~9月(P<0.05), 而Nitrospira和Thermomonas菌属在8~9月的相对丰度显著高于低温时期(P<0.05).Flavobacterium菌属具有较强的硝化能力, 并且可在低温中进行新陈代谢, 与TN的去除有关[26, 27].Zoogloea菌属是一种兼性菌, 既可以分解有机物, 还参与了反硝化作用, 对硝酸盐还原为氮气和固氮有积极作用[28].Nitrospira菌属是典型的氨氧化菌, 可将亚硝酸盐氧化为硝酸盐.Dechloromonas、Thermomonas和Rhodobacter是属于反硝化菌, 都与TN的去除有关.由此可以看出, Flavobacterium、Dechloromonas和Zoogloea等菌属能够适应低温的环境, 促进总氮的去除.而Nitrospira和Thermomonas菌属对温度较为敏感[29], 是8~9月氨氮转化和总氮去除的主要菌属.此外, Thiobacillus、Dechloromonas和Thermomonas等菌属在根系土中的丰度显著高于非根系土(P<0.05), 说明植物根系分泌的有机物和泌氧功能会促进这些根系细菌的生长繁殖, 进一步促进了有机物和TN的去除.
此外, 在优势菌属中包含与铁锰氧化还原相关的菌属.Pseudomonas、Arthrobacter、Acinetobacter和Flavobacterium均被报道具有氧化Mn(Ⅱ)的能力[1, 30, 31].而Crenothrix和Acidovorax为异养铁氧化菌[32].Geobacter为金属还原菌, 可利用多种有机物质作为电子供体, 将高价态的Fe(Ⅲ)和Mn(Ⅳ)还原为Fe(Ⅱ)和Mn(Ⅱ)并从中获得能量[33].对以上菌属进行差异性分析, 结果表明, 季节变化对其相对丰度的影响较为显著, 仅有Geobacter在低温时期的相对丰度显著高于8~9月(P=0.02), 其余菌属在低温时期的相对丰度均显著低于8~9月(P<0.05).此外, Acidovorax和Geobacter在根系土中的相对丰度显著高于非根系(P<0.05), 这可能是由于植物根系分泌的有机物为其提供了生长所必需的碳源和电子供体.然而, 锰砂和对照人工湿地之间的优势菌的丰度均无显著的差别(P>0.05), 这表明填加锰砂对该人工湿地微生物群落结构影响较小, 这在以往研究中也有过报道[34].
综上所述, 填加锰砂会提升人工湿地系统中微生物的丰度和多样性, 但对微生物群落的主要结构特别是丰度较高的细菌影响不大.
3 结论(1) 水质数据分析表明, 填加锰砂可显著提升人工湿地对DOC、TN的去除以及冬季时期氨氮的转化, 但对COD和TP的去除率无显著影响.
(2) 16S rRNA数据分析显示, 锰砂可显著提高冬季时人工湿地中芦苇根系微生物的丰富度和多样性, 但对微生物群落结构影响较小, 这可能与锰砂湿地强化污染物去除能力有关.
(3) 锰砂人工湿地对NH4+-N的去除中, 除相关微生物的作用, 可能还存在锰砂直接催化转化NH4+-N的反应.
| [1] | Tebo B M, Bargar J R, Clement B G, et al. Biogenic manganese oxides: properties and mechanisms of formation[J]. Annual Review of Earth and Planetary Sciences, 2004, 32: 287-328. DOI:10.1146/annurev.earth.32.101802.120213 |
| [2] | Schlosser D, Höfer C. Laccase-catalyzed oxidation of Mn2+ in the presence of natural Mn3+ chelators as a novel source of extracellular H2O2 production and its impact on manganese peroxidase[J]. Applied and Environmental Microbiology, 2002, 68(7): 3514-3521. DOI:10.1128/AEM.68.7.3514-3521.2002 |
| [3] | Bruins J H, Petrusevski B, Slokar Y M, et al. Manganese removal from groundwater: characterization of filter media coating[J]. Desalination and Water Treatment, 2015, 55(7): 1851-1863. DOI:10.1080/19443994.2014.927802 |
| [4] | Katsoyiannis I A, Zouboulis A I, Jekel M. Kinetics of bacterial As(Ⅲ) oxidation and subsequent As(Ⅴ) removal by sorption onto biogenic manganese oxides during groundwater treatment[J]. Industrial & Engineering Chemistry Research, 2004, 43(2): 486-493. |
| [5] | Nelson Y M, Lion L W, Shuler M L, et al. Effect of oxide formation mechanisms on lead adsorption by biogenic manganese (hydr)oxides, iron (hydr)oxides, and their mixtures[J]. Environmental Science & Technology, 2002, 36(3): 421-425. |
| [6] | Carvalho P N, Arias C A, Brix H. Constructed wetlands for water treatment: new developments[J]. Water, 2017, 9(6). DOI:10.3390/w9060397 |
| [7] | Badejo A A, Omole D O, Ndambuki J M, et al. Municipal wastewater treatment using sequential activated sludge reactor and vegetated submerged bed constructed wetland planted with Vetiveria zizanioides[J]. Ecological Engineering, 2017, 99: 525-529. DOI:10.1016/j.ecoleng.2016.11.012 |
| [8] | Lu S B, Zhang X L, Wang J H, et al. Impacts of different media on constructed wetlands for rural household sewage treatment[J]. Journal of Cleaner Production, 2016, 127: 325-330. DOI:10.1016/j.jclepro.2016.03.166 |
| [9] | Huang X, Zheng J L, Liu C X, et al. Removal of antibiotics and resistance genes from swine wastewater using vertical flow constructed wetlands: effect of hydraulic flow direction and substrate type[J]. Chemical Engineering Journal, 2017, 308: 692-699. DOI:10.1016/j.cej.2016.09.110 |
| [10] | Mojiri A, Lou Z Y, Tajuddin R M, et al. Co-treatment of landfill leachate and municipal wastewater using the ZELIAC/zeolite constructed wetland system[J]. Journal of Environmental Management, 2016, 166: 124-130. |
| [11] | Ilyas H, Masih I. The performance of the intensified constructed wetlands for organic matter and nitrogen removal: a review[J]. Journal of Environmental Management, 2017, 198: 372-383. DOI:10.1016/j.jenvman.2017.04.098 |
| [12] | Liu T, Xu S R, Lu S Y, et al. A review on removal of organophosphorus pesticides in constructed wetland: Performance, mechanism and influencing factors[J]. Science of the Total Environment, 2019, 651: 2247-2268. DOI:10.1016/j.scitotenv.2018.10.087 |
| [13] | Delgado N, Bermeo L, Hoyos D A, et al. Occurrence and removal of pharmaceutical and personal care products using subsurface horizontal flow constructed wetlands[J]. Water Research, 2020, 187. DOI:10.1016/j.watres.2020.116448 |
| [14] | 刘文菊, 朱永官. 湿地植物根表的铁锰氧化物膜[J]. 生态学报, 2005, 25(2): 358-363. DOI:10.3321/j.issn:1000-0933.2005.02.027 |
| [15] | Xie H J, Yang Y X, Liu J H, et al. Enhanced triclosan and nutrient removal performance in vertical up-flow constructed wetlands with manganese oxides[J]. Water Research, 2018, 143: 457-466. DOI:10.1016/j.watres.2018.05.061 |
| [16] | Bai Y H, Yang T T, Liang J S, et al. The role of biogenic Fe-Mn oxides formed in situ for arsenic oxidation and adsorption in aquatic ecosystems[J]. Water Research, 2016, 98: 119-127. DOI:10.1016/j.watres.2016.03.068 |
| [17] | 国家环境保护总局. 水和废水监测分析方法[M]. (第四版). 北京: 中国环境科学出版社, 2002. |
| [18] | Bolyen E, Rideout J R, Dillon M R, et al. Reproducible, interactive, scalable and extensible microbiome data science using QⅡME 2[J]. Nature Biotechnology, 2019, 37(8): 852-857. DOI:10.1038/s41587-019-0209-9 |
| [19] | Dixon P. VEGAN, a package of R functions for community ecology[J]. Journal of Vegetation Science, 2003, 14(6): 927-930. DOI:10.1111/j.1654-1103.2003.tb02228.x |
| [20] | 师菊莲, 史昕欣, 黄廷林. 锰氧化物催化氨氮氧化的电子转移路径研究[J]. 水处理技术, 2020, 46(8): 64-68, 73. |
| [21] | Liang Y, Wei D Y, Hu J S, et al. Glyphosate and nutrients removal from simulated agricultural runoff in a pilot pyrrhotite constructed wetland[J]. Water Research, 2020, 168. DOI:10.1016/j.watres.2019.115154 |
| [22] | Zhang T, Shao M F, Ye L. 454 Pyrosequencing reveals bacterial diversity of activated sludge from 14 sewage treatment plants[J]. The ISME Journal, 2012, 6(6): 1137-1147. DOI:10.1038/ismej.2011.188 |
| [23] | Bauer M, Kube M, Teeling H, et al. Whole genome analysis of the marine Bacteroidetes 'Gramella forsetii' reveals adaptations to degradation of polymeric organic matter[J]. Environmental Microbiology, 2006, 8(12): 2201-2213. DOI:10.1111/j.1462-2920.2006.01152.x |
| [24] | Daniel L M C, Pozzi E, Foresti E, et al. Removal of ammonium via simultaneous nitrification-denitrification nitrite-shortcut in a single packed-bed batch reactor[J]. Bioresource Technology, 2009, 100(3): 1100-1107. DOI:10.1016/j.biortech.2008.08.003 |
| [25] | Ansola G, Arroyo P, De Miera L E S. Characterisation of the soil bacterial community structure and composition of natural and constructed wetlands[J]. Science of the Total Environment, 2014, 473-474: 63-71. DOI:10.1016/j.scitotenv.2013.11.125 |
| [26] | 苏金凤, 吕祥, 马传敏, 等. 一株异养硝化细菌的分离培养及鉴定[J]. 生物化工, 2020, 6(4): 79-82. DOI:10.3969/j.issn.2096-0387.2020.04.020 |
| [27] | 李廷梅, 于鲁冀, 刘攀龙, 等. 波流式生态滤床氨氮去除效果及其微生物群落结构分析[J]. 环境科学学报, 2017, 37(10): 3664-3671. |
| [28] | Shao Y Q, Chung B S, Lee S S, et al. Zoogloea caeni sp. nov., a floc-forming bacterium isolated from activated sludge[J]. International Journal of Systematic and Evolutionary Microbiology, 2009, 59(3): 526-530. DOI:10.1099/ijs.0.65670-0 |
| [29] | Alawi M, Off S, Kaya M, et al. Temperature influences the population structure of nitrite-oxidizing bacteria in activated sludge[J]. Environmental Microbiology Reports, 2009, 1(3): 184-190. DOI:10.1111/j.1758-2229.2009.00029.x |
| [30] | An Q, Jin L, Deng S M, et al. Removal of Mn(Ⅱ) by a nitrifying bacterium Acinetobacter sp. AL-6: Efficiency and mechanisms[J]. Environmental Science and Pollution Research, 2021. DOI:10.1007/s11356-021-12764-6 |
| [31] | Carmichael M J, Carmichael S K, Santelli C M, et al. Mn(Ⅱ)-oxidizing bacteria are abundant and environmentally relevant members of ferromanganese deposits in caves of the upper Tennessee River basin[J]. Geomicrobiology Journal, 2013, 30(9): 779-800. DOI:10.1080/01490451.2013.769651 |
| [32] | Ilbert M, Bonnefoy V. Insight into the evolution of the iron oxidation pathways[J]. Biochimica et Biophysica Acta (BBA)-Bioenergetics, 2013, 1827(2): 161-175. DOI:10.1016/j.bbabio.2012.10.001 |
| [33] | Coates J D, Bhupathiraju V K, Achenbach L A, et al. Geobacter hydrogenophilus, Geobacter chapellei and Geobacter grbiciae, three new, strictly anaerobic, dissimilatory Fe(Ⅲ)-reducers[J]. International Journal of Systematic and Evolutionary Microbiology, 2001, 51(2): 581-588. DOI:10.1099/00207713-51-2-581 |
| [34] | 刘俊花. 锰矿物对人工湿地中三氯生及常规污染物强化去除的研究[D]. 济南: 山东大学, 2017. |
 2021, Vol. 42
2021, Vol. 42


