2. 中国科学院南京土壤研究所土壤环境与污染修复重点实验室, 南京 210008;
3. 江苏省建筑设计研究院有限公司, 南京 210000;
4. 甘肃省污水深度处理行业技术中心, 兰州 730070
2. Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China;
3. Jiangsu Provincial Architectural Design & Research Institute Co., Ltd., Nanjing 210000, China;
4. Gansu Province Wastewater Treatment Industry Technology Center, Lanzhou 730070, China
磷(phosphate)在自然水体中的大量排放会造成水体富营养化, 严重威胁水体生态环境. 高浓度的磷会刺激水体中水藻等的疯狂生长, 过度消耗水中溶解氧, 致使鱼虾绝迹, 水质恶化[1, 2]. 并且其自然代谢的归宿通常是沉积在底泥中, 而后会通过各种作用再次释放回水中, 所以自然代谢不能解决磷的过度排放问题. 也因此磷的过度排放对水体的污染目前已成为世界性的环境治理难题.
目前处理磷污染的方法主要有化学法、生物法和物理法[1, 3~5]. 物化方法中, 目前使用较多的方法是吸附法, 其高效环保, 且吸附剂可循环利用, 是处理磷的一种有效的方法. 吸附法的核心是吸附剂, 吸附剂的品质好坏直接关系到吸附效果. 但目前对于除磷吸附剂的开发却研究较少. 剩余污泥(wasted sludge)的处理一直以来是污水与固废处理的一个重要议题. 由于污泥中的重金属以及致病菌的存在, 直接回田施肥可能会污染其上作物进而影响人体健康[6~8]. 而直接填埋则有毒有害物质可能会渗出污染地下水和土地. 厌氧发酵以产沼气的措施可以环保高效地处理剩余污泥, 但是其对污泥日产量要求较高, 一般只适用于大型污水处理厂. 污泥碳化技术是目前新兴的一种污泥处理技术[9, 10]. 有研究发现碳化过程中污泥中的有机质会碳化、造孔和结构蓬松, 成为一种类似于活性炭的材料, 且其中的重金属会在碳化过程中钝化, 毒性降低[8]. 当前污泥碳化技术制备生物炭的研究已有较多报道, 例如阳昕[3, 8]利用剩余污泥碳化制备生物炭吸附水中重金属和四环素均取得了一定的效果. 但是由于污泥中有机质含量相对较少, 所得生物炭孔隙不甚发达, 且表面活性位点也相对较少, 所以对污泥生物炭的改性十分必要. 铁系材料由于价格低廉、来源广泛和无毒无害等特点已开始用于生物炭改性中, 并且已有研究报道了改性后对于水中磷的去除, Yang等[1]以FeCl3作为改性材料改性剩余污泥, 在最佳配比下其对水中磷的去除可达110.0 mg·g-1. 常见的铁系材料包括磁性氧化铁、纳米零价铁和铁硫化合物[11~14]. 其中对磁性氧化铁和纳米零价铁的研究已有大量报道, 其去除的污染物种类包括重金属和有机物等. 对磷的去除也有报道. 铁硫化合物目前应用得较多的是对重金属的去除[11~14], 而对磷的去除却鲜见报道. 另外, 铁硫两种元素因其独特的络合能力和氢键结合能力对磷的吸附在理论上是有一定效果的. N、O、P和S等元素因为电负性较强, 在吸附过程中, 往往会以氢键的形式结合, 氢键结合的作用属于弱作用力至强作用力之间的过渡的一种作用力, 当前众多吸附的研究中均报道了关于氢键结合的作用, 可见氢键结合在设计吸附剂是可以作为一个关键的参考因素. 结合N、O、P和S等元素的氢键结合能力, 引入这些元素进入吸附剂在吸附过程中可能会强化吸附效果, 提升吸附剂活性.
本研究中, 将以剩余污泥为基质材料制备生物炭, 并用铁硫化合物对其改性制备除磷吸附剂. 本研究的主要目的为以下3点:①制备一种新型的除磷吸附剂; ②通过批次实验以及数学模型分析对吸附性能以及过程行为解释; ③通过各类表征手段解释吸附机制. 本研究证明了合成的材料是一种新型的高效除磷吸附剂, 以期为吸附剂设计以及吸附机制的探讨提供借鉴.
1 材料与方法 1.1 实验材料本实验中戊二醛、壳聚糖、乙酸、Na2S·9H2O、FeSO4·7H2O、NaOH、HCl和ZnCl2购自天津富晨化学药品有限公司. KH2PO4购自国药集团试剂有限公司. 所有化学试剂纯度均为分析纯. 市政污泥取自兰州市七里河污水处理厂压缩污泥, 含水率约为75%~80%. 湿污泥在室外自然干燥一周随后在120℃鼓风干燥箱(DHG-9920B, 福絮, 上海)内再次干燥24 h至含水率降至5%以下.
1.2 生物炭(biochar)的制备生物炭的制备参考文献[1]和课题组已有的研究. 由于单纯的碳化污泥不能取得孔隙发达的生物炭, 因此碳化时加入ZnCl2活化剂. 前期小试已选出了最佳控制因素(以磷吸附量为基准), 具体细节在下文中将不再详述. 完全干燥的块状污泥经由粉碎机粉碎, 选择颗粒尺寸在60~80目的颗粒. 将粒径均匀的颗粒置于100 mL 2 mol·L-1的ZnCl2溶液(由体积分数为5%的HCl溶液配制而成)中搅拌一夜. 固液分离后60℃下真空干燥(DZF-6050, 善至, 上海). 干燥后的前体物倒入刚玉舟中压实放于管式炉中(BXG-4-12, 邦世达, 宜兴). 升温速度10℃·min-1; 终温500℃; 终温滞留时间2 h. 自然冷却至室温, 以0.1 mol·L-1 HCl和去离子水洗涤数遍直至上清液pH值不再变化. 固液分离后再次60℃下真空干燥.
1.3 铁硫改性生物炭(BCFe/S)的制备为探究原料的不同投加比例对吸附的影响, 本实验一共研制了7组复合材料以及3组单一材料. 以编号为1的材料为例介绍合成方法:将1 g壳聚糖溶解于100 mL 5%的乙酸溶液中(体积比), 再将1 g生物炭投入, 超声分散直至完全混合. 恒压漏斗滴加50 mL FeSO4溶液(含1 g FeSO4·7H2O), 搅拌、过夜. 第二日, 配制50 mL Na2S溶液(含3 g Na2S·9H2O)并以恒压漏斗滴加, 滴加过程中以纯度为99.9%的N2制造无氧氛围. 完全滴加后, 60℃油浴(602B, 成辉, 常州)老化2 h. 老化完成后加入5 mL 50%戊二醛溶液(体积比), 再次老化一夜, 使戊二醛与壳聚糖完全交联. 第3 d, 以0.1 mol·L-1 NaOH将pH调整为10~11, 60℃油浴3 h(pH全程控制)后即成. 本实验中, 3种原材料的投加总质量控制为3 g, 分别调节生物炭、壳聚糖和FeSO4·7H2O质量比为以下7组:1∶1∶1、1∶3∶5、5∶3∶1、3∶1∶5、3∶5∶1、5∶1∶3和1∶5∶3. 它们分别被标记为BCFe/S/1、BCFe/S/2、BCFe/S/3、BCFe/S/4、BCFe/S/5、BCFe/S/6和BCFe/S/7. 同时也单独探究了生物炭、壳聚糖和硫化亚铁的吸附性能. 其余材料投加量在本实验中均相同, 小试已证明其余材料的投加量均已过量, 可满足要求.
1.4 批次实验批次实验中, 将一定量的磷溶于1 L容量瓶配成1 000 mg·L-1的磷酸储备液(以磷元素计). 取50 mL溶液和25 mg样品加入100 mL锥形瓶中, 加塞, 于298 K的恒温水浴振荡器(SHA-BA, 中贝, 常州)中振荡. 转速定为200 r·min-1. 溶液中磷的含量以钼锑抗分光光度计法在700 nm下测试. 配比优化实验中选择初始浓度(c0)为100 mg·L-1的磷溶液, 吸附时间为24 h. pH影响实验中选择初始浓度为100 mg·L-1的磷溶液, 以0.1 mol·L-1 NaOH和HCl分别调节pH值至2~12, 精度控制在±0.1, 吸附时间为24 h. 实验动力学实验中, 选择初始浓度为100 mg·L-1的磷溶液进行实验, 分别对298、308和318 K这3个温度下的动力学拟合结果. 热力学实验中, 分别选择初始浓度为10、50、100、300、500、700和1 000 mg·L-1的磷溶液、固定溶液体积和吸附剂质量, 在298、308和318 K这3个温度下测试. 共存离子干扰实验中选择初始浓度为100 mg·L-1的磷溶液进行实验, 吸附时间为24 h. 材料的性能以磷的吸附量为指标, 吸附量的计算如式(1)所示:
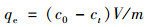
|
(1) |
式中, qe为吸附量, mg·g-1; c0和ct分别为磷溶液的初始浓度和指定时刻磷浓度, mg·L-1; V是溶液体积, L; m为吸附剂的质量, g.
水中COD对磷吸附的影响则通过投加不同来源的COD以及不同初始浓度的COD进行测试, 其余磷酸盐投加量、温度和溶液体积等条件不变. 此外水中COD剩余浓度也将进行测试(哈希COD消解仪, DRB200, 美国), 判断COD与磷之间是否存在竞争吸附.
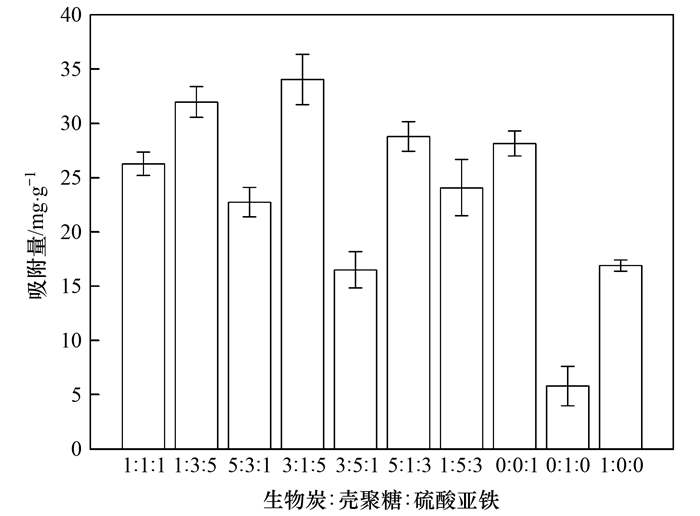
2 结果与讨论 2.1 不同比例(生物炭∶壳聚糖∶硫酸亚铁)对吸附的影响这10种材料对磷的吸附量如图 1所示. 从中可知, 单独的壳聚糖对磷的吸附效果最差, 吸附量仅可达到5.82 mg·g-1, 而单独的生物炭和硫酸亚铁对磷的吸附量相对较高, 分别达到16.90 mg·g-1和28.16 mg·g-1. 这说明在合成的材料中起主要作用的可能是生物炭和硫酸亚铁并非壳聚糖. 这一点通过比较不同配比材料对磷的吸附量也可以看出. 相较于BCFe/S/4(3∶1∶5)和BCFe/S/6(5∶1∶3), 将壳聚糖的添加量提升至BCFe/S/5(3∶5∶1)的水平时, 吸附量下降迅猛, 从34.06 mg·g-1和28.81 mg·g-1降至16.52 mg·g-1. 因此, 壳聚糖在材料中可能主要起分散剂的作用. 对比BCFe/S/1(1∶1∶1)、BCFe/S/2(1∶3∶5)、BCFe/S/3(5∶3∶1)发现, 提升硫酸亚铁的比例明显比提升生物炭的比例更能促进磷的吸附, 说明硫酸亚铁的作用要强于生物炭的作用. 这可能是由于微米/纳米级的FeS颗粒的表面效应在其中起作用. 从单独的硫酸亚铁的吸附量明显优于单独生物炭的吸附量也可以佐证这一观点. 本实验中由于BCFe/S/4对磷的吸附量最高, 因此以BCFe/S/4为接下来的研究对象.
|
图 1 生物炭、壳聚糖与硫酸亚铁投加比例不同对磷吸附的影响 Fig. 1 Effects of the proportions of biochar, chitosan, and FeSO4 on phosphate uptake |
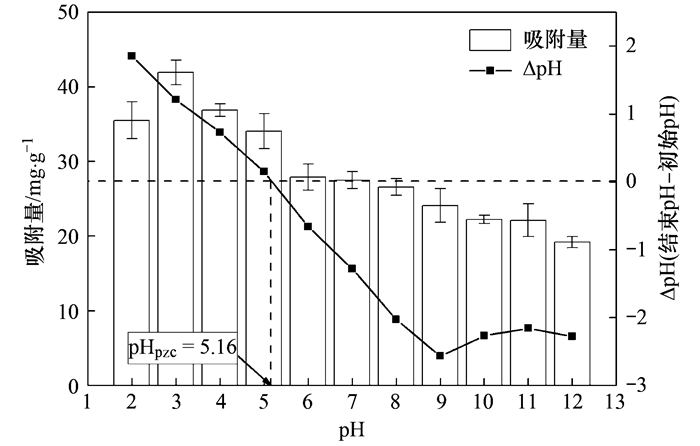
为了探究溶液pH对吸附的影响, 分别用0.1 mol·L-1的NaOH和HCl将100 mg·L-1的含磷溶液的pH调节至2~12, 其吸附量的变化如图 2所示. 从中可知BCFe/S/4对磷的吸附是一个有赖于溶液pH的过程. 对磷的吸附量在pH从2上升到3时逐渐增大, 从3~12时逐渐减小, 在pH等于3时达到最大吸附量. 为了进一步弄清pH对吸附量的影响, 研究中对BCFe/S/4的零点电位(point of zero charge, pHpzc)进行了测量(测定方法:将磷酸盐溶液替换成同体积的初始pH为2~12的去离子水, 25℃振荡48 h后, 再次测定去离子水的pH, pH的差值为0的点即为零点电位), 其值为5.16. 这说明当溶液pH值小于5.16时, BCFe/S/4表面带正电荷, 且随着pH上升带电量减小; 当溶液pH大于5.16时, BCFe/S/4表面带负电, 且随着溶液pH上升带电量增大. 此外, 溶液中的磷也会因溶液pH的变化而以不同的形式存在. 当溶液pH小于2.15时, 此时会以不带电的H3PO4形式存在; 溶液pH在2.15~7.20之间则是以带负电的H2PO4-的形式存在; 在7.20~12.33之间则会以HPO42-的形式存在[1, 3]. 因此当溶液pH小于5.16时, 不带电的H3PO4和带负电的H2PO4-会与带正电的BCFe/S/4之间产生静电吸引, 这将有利于磷吸附到BCFe/S/4表面. 而当溶液pH大于5.16时, 带负电的H2PO4-和HPO42-会与带负电的BCFe/S/4之间产生静电排斥, 磷的吸附受到了抑制. 这也解释了为什么在pH从2上升到3时, 吸附量有一个小的突跃, 正是由于不带电的H3PO4逐渐转变为带负电的H2PO4-, 吸引力增强. 而当pH从5上升6时则产生了一个陡降, 这主要是BCFe/S/4表面由正电转变为负电, 此前的静电引力突然转变为静电斥力.
|
图 2 溶液pH变化对磷吸附的影响以及零点电位 Fig. 2 Effects of solution pH on the phosphate removal and point of zero charge |
吸附动力学是吸附过程中重要的研究内容, 其可以计算出吸附速率, 并且对污染物的扩散机制加以描述. 本研究分别用伪一级动力学模型和伪二级动力学模型对数据进行拟合, 此外以颗粒内扩散模型和膜扩散模型来解释扩散机制, 其公式如下.
伪一级动力学:
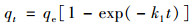
|
(2) |
伪二级动力学:
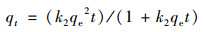
|
(3) |
颗粒内扩散:

|
(4) |
膜扩散:
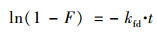
|
(5) |
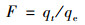
|
(6) |
式中, qt是t时刻下BCFe/S/4对磷的吸附量, mg·g-1; qe是吸附平衡时磷的吸附量, mg·g-1; k1是伪一级动力学的速率常数, min-1; k2是伪二级动力学的速率常数, g·(mg·min)-1; kid[mg·(g·min0.5)-1]和ci(mg·g-1)分别为颗粒内扩散模型常数; kfd为膜扩散模型常数. 动力学模拟曲线如图 3所示, 扩散模拟曲线如图 4所示, 数据总结在表 1中.

|
图 3 BCFe/S/4吸附磷的动力学拟合曲线 Fig. 3 Kinetic plots of phosphate adsorption by BCFe/S/4 |
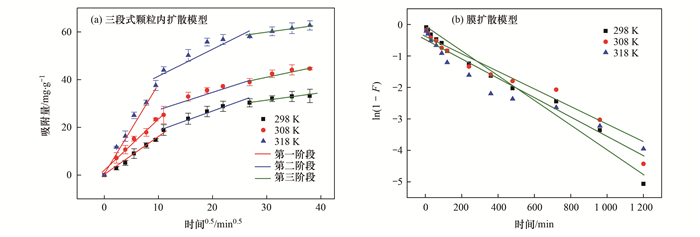
|
图 4 扩散模型拟合 Fig. 4 Diffusion model fitting |
|
|
表 1 BCFe/S/4在不同温度下吸附磷的吸附动力学模型的吸附参数 Table 1 Kinetic parameters of phosphate removal by BCFe/S/4 under different temperatures |
由图 3可知整个吸附过程大致可以分为两个阶段:快速吸附阶段和吸附平衡阶段. 快速吸附阶段约为吸附前480 min, 这一阶段的吸附量约占总吸附量的90%以上. 吸附平衡阶段的吸附量约占吸附总量的10%, 此时, 吸附已经达到平衡. 对比伪一级动力学和伪二级动力学的相关系数(R2), 可以发现不论温度如何伪二级动力学的R2(0.976 0~0.995 5)均大于伪一级动力学的R2(0.939 2~0.977 6). 且伪二级动力学计算得到的qe(35.40~63.62 mg·g-1)比伪一级动力学的qe(31.22~58.32 mg·g-1)更接近实测值qe(33.20~62.76 mg·g-1), 说明伪二级动力学更适合描述磷在BCFe/S/4上的吸附. 有研究报道伪二级动力学模型的拟合度高可归因于化学吸附, 因此可以初步判断BCFe/S/4吸附磷的形式属于化学吸附[1, 11].
为了探究吸附过程中的控制步骤以及最主要的扩散方式, 颗粒内扩散和膜扩散模型被引入用来研究. 由表 1可知, 相较而言颗粒内扩散的R2要大于膜扩散的R2值, 说明整个过程中的决定性控制步骤是颗粒内扩散. 然而颗粒内扩散拟合直线均不过原点, 且温度升高截距越大, 说明颗粒内扩散并非唯一的扩散机制, 膜扩散在其中是起作用的. 一般而言扩散分为3步, 如图 4所示分为3个阶段, 即:①吸附质受浓度梯度差的影响由溶液扩散至颗粒外表面, 这一过程称为膜扩散或外部扩散; ②吸附质从颗粒外表面向颗粒内部孔道扩散, 这一过程包括吸附质在内部孔隙空间的三维扩散和沿内部孔壁的二维扩散, 而后者的吸附速率通常比前者的吸附速率大2~4个数量级, 因此这一过程速率的控制步骤为吸附质在内部孔隙空间的三维扩散; ③吸附质与位点结合, 这一过程十分迅速, 因此通常不认为是速率的限制步骤[15~20]. 3个过程中后面2种扩散统称为颗粒内扩散. 从上述分析可以得知吸附过程的主要控制步骤为颗粒内扩散, 而其中磷在内部孔隙空间三维扩散是最主要的步骤. 同时温度升高, 分子的布朗运动加强, 此时磷在内部孔隙空间三维扩散愈发难以趋于稳定, 因此对整体速率控制的影响会增大. 此外, 升高温度, 会削减固/液界面层阻力[21], 磷在膜界面上扩散更快, 此时膜扩散的速率加大, 越来越不能成为影响整个吸附过程的速率控制步骤, 其R2由298 K下的0.916 2降至318 K时的0.890 8也印证了这一观点.
为了进一步探究BCFe/S/4吸附磷的活化能, 将3个温度下的吸附速率代入Arrhenius方程中, 其式如下:
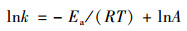
|
(7) |
式中, k为吸附速率[min-1或g·(mg·min)-1]; Ea为吸附活化能, kJ·mol-1; A为指前因子(无量纲). 由于伪二级动力学在拟合过程中表现更好, 因此选择伪二级动力学的速率常数代入计算, 计算结果为Ea=5.710 9 kJ·mol-1, 大于4.2 kJ·mol-1, 说明吸附过程开始由纯物理吸附转变为化学吸附控制的过程[22].
2.4 吸附等温线本研究中, 以常见的Langmuir和Freundlich吸附等温线对数据进行模拟.
Langmuir:
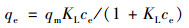
|
(8) |
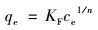
|
(9) |
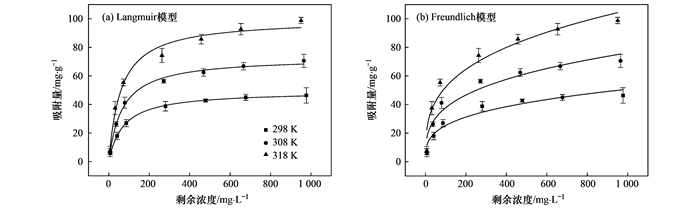
式中, qm为最大吸附量, mg·g-1; ce为吸附平衡时溶液中磷的剩余浓度, mg·L-1; qe为吸附平衡时磷的吸附量, mg·g-1; KL是Langmuir的参数, L·mg-1; KF(mg·g-1)·(L·mg-1)1/n和n是Freundlich的参数.图 5为等温线拟合结果, 表 2对各参数进行了总结.
|
图 5 BCFe/S/4吸附磷的等温拟合曲线 Fig. 5 Isotherm of phosphate adsorption by BCFe/S/4 |
|
|
表 2 BCFe/S/4吸附磷等温线模型的吸附参数 Table 2 Parameters of isotherms for phosphate removal by BCFe/S/4 |
由图 5可知, 随着温度的升高, 吸附量大幅度提升, 说明吸附过程是吸热的过程, 升高温度有利于吸附的进行. 此外对比Langmuir和Freundlich模型, 可以发现Langmuir模型比Freundlich模型能更好地描述磷在BCFe/S/4上的吸附, 这是由于Langmuir的R2(0.982 7~0.997 9)明显高于Freundlich的R2(0.934 9~0.939 9), 这表明BCFe/S/4的表面吸附位点的分布趋于均匀[1, 3, 23]. 为了判断磷在BCFe/S/4上的吸附是否是有利的自发的, RL的值可以作为一个很好的参考, 其式表达如下:
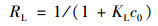
|
(10) |
其中, 当RL=0时此过程不可逆; 0<RL<1时, 此过程是有利的自发的; 当RL=1时, 吸附是线性的过程; 当RL>1时, 吸附过程是无法自发进行的. 由表 2可知, RL的值全部落于0~1之间, 说明磷在BCFe/S/4的吸附是有利的[3, 24]. 且数据发现, 随着c0的增大, RL值不断减小, 说明污染物浓度越高吸附越有利.Langmuir模型是从单分子层吸附的原理出发, 其模型非常适用于表面的化学吸附. 而Freundlich模型则是一个经验公式, 它重点考虑了吸附剂表面吸附位点的不均匀. 由上述可知, 磷在BCFe/S/4上的吸附更倾向于单分子层吸附, 化学吸附起到了主要作用.
2.5 吸附热力学热力学的研究可以帮助研究人员直观地判断吸附过程中的物化作用. 其主要由吉布斯自由能变化(ΔGθ)、熵变(ΔSθ)和焓变(ΔHθ)的数值来表现, 如公式(11)和(12)所示:

|
(11) |
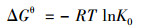
|
(12) |
式中, K0为ln(qe/ce)与吸附量之间的线性关系的截距. 其余符号含义如上文所述. 拟合结果见图 6和表 3. 表 3中的ΔGθ值均小于0, 说明吸附过程是一个自发的过程, 而且温度越高ΔGθ值越小, 说明温度越高越有利于吸附的进行.ΔHθ值均大于0说明吸附是一个吸热的过程, 升温会有利于吸附的进行, 因此温度越高吸附量越大. 通常, ΔHθ的值在0~20 kJ·mol-1之间, 则吸附过程为物理吸附占据主导地位. 当ΔHθ的大于20 kJ·mol-1时, 吸附开始变为物理化学吸附. 由表 3可知ΔHθ值为20.890 1 kJ·mol-1, 因此吸附过程是一个物理化学吸附的过程.ΔSθ值为73.325 1 J·(mol·K)-1为正值, 说明吸附过程是一个趋于混乱的过程[24, 25]. 一般而言, 液相吸附中, 水分子会由于浸润作用先于其他物质进入吸附剂内部占据吸附位点, 此时系统内部趋于稳定, 熵变会呈现负值. 当吸附质进入孔道内部, 水分子会被迫脱附留出吸附点给吸附质, 由于水分子尺寸一般小于吸附质, 因此吸附一个分子的吸附质需要脱附数个分子的水分子, 这会导致体系稳定性的破坏, 混乱程度增加, 熵变为正值. 且吸附剂与吸附质之间的亲和性越强, 这种现象越明显. 因此ΔSθ值为73.325 1 J·(mol·K)-1说明磷分子与BCFe/S/4之间有一定的亲和力[25].

|
图 6 热力学模型 Fig. 6 Thermodynamic model |
|
|
表 3 BCFe/S/4吸附磷的热力学参数 Table 3 Parameters of thermodynamics for phosphate removal by BCFe/S/4 |
2.6 共存离子的影响
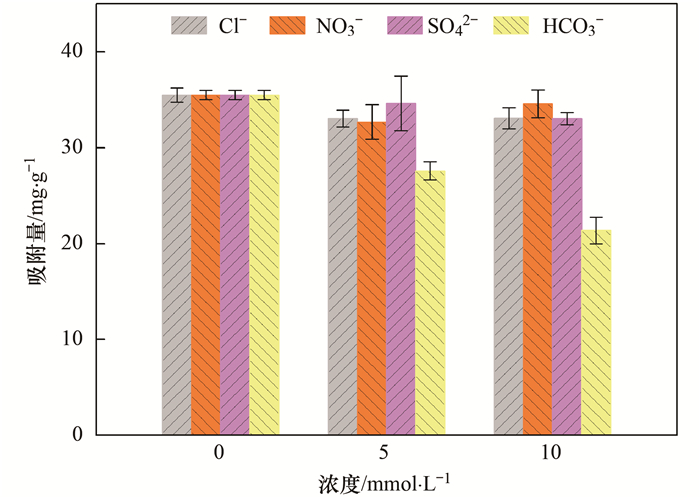
天然水体中除了污染物之外还存在大量的阴阳离子, 它们的存在必然会对水体中磷的吸附产生影响. 由于磷源为磷酸氢二钾, 因此磷在水中是以阴离子的形式存在, 为此选择常见的阴离子Cl-、NO3-、SO42-和HCO3-作为研究对象, 探究阴离子对磷吸附的影响. 结果如图 7所示.
|
图 7 共存离子对磷吸附的影响 Fig. 7 Effects of co-existing ions on phosphate adsorption |
随着阴离子浓度的增加, 它们对磷吸附的影响表现却不同. 可以看出Cl-、NO3-和SO42-这3种离子随着投加量的增加对磷的吸附会产生一定的抑制作用, 但这种抑制作用不明显, 且此时3种离子的含量已经相对较高, 明显高于天然水体中的含量, 说明BCFe/S/4即使运用于天然水体中也不会受到以上3种离子的干扰. 与以上3种离子不同, HCO3-对磷的吸附抑制效果明显, 其抑制效果会随投加量的增大而增大. 这可能是由于HCO3-和H2PO4-的结构相似, 均为四面体结构, 因此二者之间会由于结构类似而对某些特异性吸附位点进行争夺, 所以吸附量会下降. 相似的报道也可见阳昕[3]的研究.
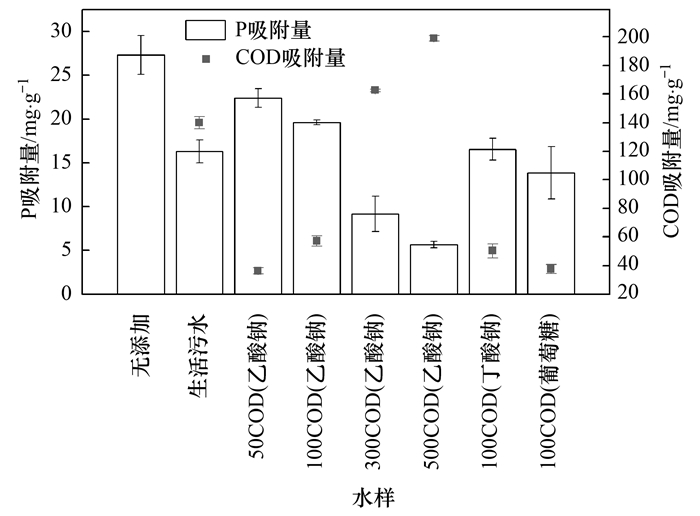
2.7 水中COD的影响污水中的COD通常是主要污染物, 其含量大必然会对吸附剂吸附造成一定影响. 为了探究水中COD对磷吸附的影响, 实验中以生活污水以及多种COD配水共同探究了水中COD对P吸附的影响. 其中生活污水取自北京航空航天大学污水管道(主要指标参考表 4). 在人工配水中以乙酸钠作为COD来源分别配制了50、100、300和500 mg·L-1的溶液(以COD计). 此外为了探究底物不同对吸附的影响, 本实验中还研究了乙酸钠、丁酸钠和葡萄糖作为COD来源对吸附的影响(浓度为100 mg·L-1, 以COD计), 磷浓度仍为100 mg·L-1. 为防止不同基质和生活污水pH不同而造成影响, 所有溶液的初始pH均调整为7.图 8为COD对磷吸附的影响, 从中可以看出, COD确实会抑制磷的吸附, 并且随着COD浓度的增加抑制作用更明显. 这主要是COD也会被材料所吸附, 从图 8中可以看出, COD浓度增大其吸附量也随之增大, 因此二者会存在竞争吸附关系. 此外, 通过改变基质, 磷的吸附和COD的吸附也产生了一定的变化, 当乙酸钠被换成丁酸钠时, 磷的吸附量减小了; 当进一步换成葡萄糖时, 吸附量更进一步减小. 说明COD基质的分子量越大对磷吸附的抑制作用也越强; 而且从COD吸附量来看, 分子量越大COD吸附量也越小.
|
|
表 4 生活污水相关指标 Table 4 Characteristics of the sewage |
|
图 8 COD对磷吸附的影响 Fig. 8 Effect of COD on phosphorus adsorption |
吸附磷前后, BCFe/S/4表面必然会产生明显的物理化学变化, 对于这些变化的解释将有助于研究人员更好地理解吸附机制. 为了探究这些变化, 本文中将对吸附前后材料的比表面积(BET, ASAP, Micromeritics, USA)、表面结构(SEM, JSM-6701F, JEOL, Japan)、晶体类型(XRD, 7000LX, Shimadzu, Japan)以及表面官能团(FTIR, iS20, Thermo Fisher, USA)进行测试.
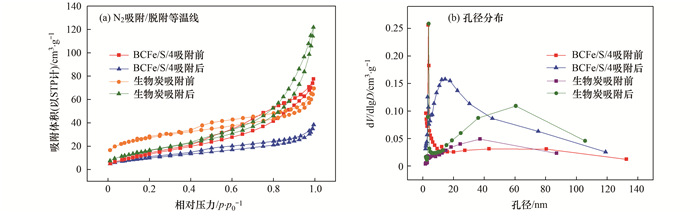
图 9为BET测试结果. 由图 9(a)可知, 无论吸附前后, N2-吸附/脱附等温线均为Ⅳ型. Ⅳ型等温线的存在说明材料键存在介孔分布. 而H3型回滞环的存在说明介孔孔径不均匀. 而吸附体积的相对较小, 说明内部孔隙结构并非十分发达. 从表 5亦可看出, BCFe/S/4的比表面积仅为69.84 m2·g-1, 与活性炭等材料相比其比表面积仍然较小. 从图 10也可以看出材料虽然有一定的孔隙结构, 但远未达到发达水平. 而其对磷的吸附效果十分优异则说明改性剂在吸附过程中起到重要作用.图 9(b)可知, 吸附后孔径分布明显向大尺寸方向偏移, 这可能是由于尺寸较小的介孔与小孔在被磷填充之后, 仅留有部分未被填充的大孔和尺寸较大的介孔, 因此大孔此时所占的比例会上升, 同时平均孔径也会因此而增大. 此现象与表 5中平均孔径由吸附前的5.49 nm上升至吸附后的8.17 nm现象相吻合. 此外, 总容积由吸附前的0.42 cm3·g-1降为吸附后的0.40 cm3·g-1说明磷占据了内部孔隙结构, 因此孔隙填充是磷吸附的一个重要机制[26]. 同样, 对于生物炭吸附前后, 也发生了相似的变化, 具体表现为总比表面积从112.52 m2·g-1减少到109.33 m2·g-1, 总容积由0.75 cm3·g-1减少到0.74 cm3·g-1. 另外一个现象是, 在负载Fe/S颗粒之后, 比表面积和总容积均呈现出减小的趋势, 然而由图 1可知, BCFe/S/4的吸附量是明显大于生物炭的, 因此单纯的较小比表面积和孔隙容积虽然会使孔隙填充的作用减弱, 但是Fe/S的吸附作用是更强的, 并且足以抵消因比表面积和孔隙容积减小带来的作用. 这也从侧面说明了Fe/S改性对吸附性能有极大地提升.
|
图 9 BET分析 Fig. 9 BET analysis |
|
|
表 5 BCFe/S/4吸附磷的BET分析 Table 5 BET analysis of phosphate adsorption by BCFe/S/4 |

|
图 10 BCFe/S/4扫描电镜 Fig. 10 Scanning electron microscopy of BCFe/S/4 |
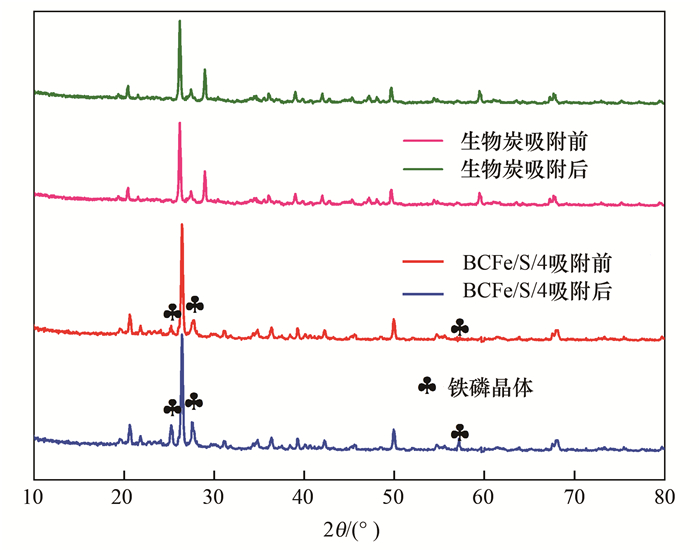
图 11为吸附前后BCFe/S/4的X射线衍射图谱. 从中可知, 吸附后衍射峰在2θ为26.4°和28.2°两处明显增强; 而在2θ=57.5°则出现了一个尖锐的新峰. 这几处峰主要为Fe与磷之间形成的一些晶体造成[3]. 阳昕[3]的研究认为这是磷酸铁盐[Fe5(PO4)4(OH)3·2H2O]的典型衍射峰, 其生成的路径如式(13)和式(14)所示:

|
(13) |
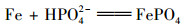
|
(14) |
|
图 11 X射线衍射图谱 Fig. 11 Spectra of X-ray diffraction |
前者一般是在酸性条件(pH为4.0~7.2)下产生, 后者一般在中性碱性条件(pH为7.2~10.0)下产生. 二者主要为白色粉末晶体的形式存在. 因此表面化学沉淀为吸附的一个重要机制. 相比于BCFe/S与磷之间产生的一系列反应, 生物炭与磷之间的反应十分微弱. 由XRD图谱可知, 生物炭在吸附磷之后, 其谱图未有变化, 这表明磷的吸附不会改变生物炭的晶体结构, 也不会在表面以沉淀结晶的形式存在.
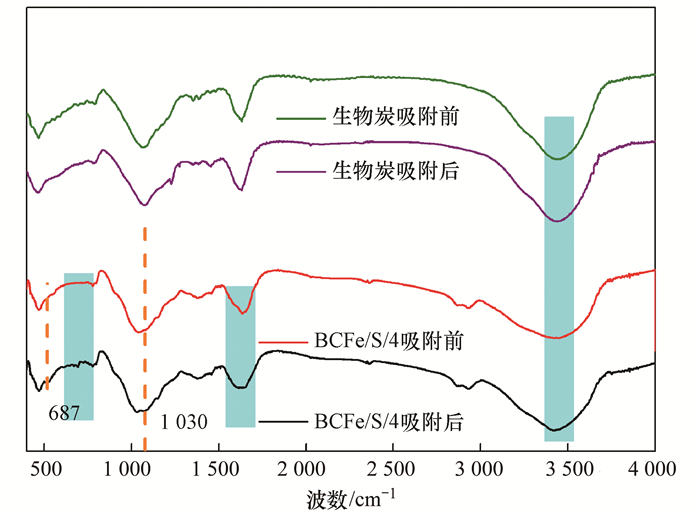
除了BCFe/S/4中的某些晶体在吸附后发生的改变外, 官能团的变化也十分明显.图 12为吸附前后吸附剂的傅里叶变换红外光谱图. 从中可知, 吸附后在687 cm-1和1 030 cm-1处产生了2个新的峰, 它们分别是S—H键和P—O的非对称伸缩振动. 说明磷有效地吸附在BCFe/S/4上, 并且会和S元素产生反应. 通常N、O、S和P这4种原子因电负性较高, 会与H原子形成氢键, 由于P的电负性大于S, 因此二者之间会形成偏向于P的S—H—P这一类型的氢键[1, 3, 27]. 氢键结合的形式在其他波数处也可观察到, 例如在1 550~1 750 cm-1和3 410~3 510 cm-1这2个宽峰带处, 二者分别为—OH的弯曲振动和伸缩振动[3], 它们在磷吸附后强度均有一定的减弱, 说明O—H—P这一类型的氢键的形成, 由于O的电负性高于P, 因此, 这个H会偏向于O原子. 此外在650~750 cm-1的宽峰带在吸附后也发生了明显的变化, 这一处主要为Fe—O和Fe—S等键的变化, 说明Fe可能与磷发生了配位体效应. 磷酸根的络合是通过磷酸根上的O对金属离子配位, 尤其适合与高价(+3价以上)金属离子的配位, 磷酸根对Fe2+的配位效果一般不好. 因此实验中能与磷酸根配位的应是Fe3+, 说明实验过程中Fe2+有部分氧化, 并未完全与S形成FeS沉淀. 与BCFe/s/4相比, 生物炭在吸附磷后官能团会发生明显改变, 但在3 410 cm-1处仍有一定的减弱, 说明氢键结合是生物炭吸附磷的一个重要机制.
|
图 12 傅里叶变换红外光谱图 Fig. 12 Fourier transform infrared spectra |
图 13为BCFe/s/4吸附磷前后的P和Fe的XPS分峰谱, 从中可以看出, 吸附前BCFe/s/4中就已经含有一定量的PO43-, 并且在吸附后, 其位置由134.2 eV偏移到134.7 eV, 这说明磷的吸附可能存在一些化学键之间的反应进而影响了振动峰的位置[28]. 除此之外, Fe和O的XPS变化也充分说明了这一现象, 从图 13可以看出, Fe—O等官能团发生了明显的变化[3, 28], 这可能主要是氢键的生成而导致的, 这与FTIR的结果相一致. 而Fe在吸附磷之后Fe2+的消失表明期间可能存在氧化还原反应, 这也解释了为何FTIR图谱中会产生Fe3+与磷的配位体效应.

|
(a)P的XPS谱图; (b)Fe的XPS谱图; (c)O的XPS谱图 图 13 BCF/S/4对磷的吸附前后XPS Fig. 13 XPS spectra of BCF/S/4 with and |
结合2.2节的分析, BCF/S/4对磷的吸附机制可以归因为: 静电吸引、孔隙填充、表面化学沉淀、氢键结合和配位体效应.
3 结论(1) 以壳聚糖和硫酸亚铁共同改性的污泥生物炭对水中磷的去除效果优异, 在生物炭∶壳聚糖∶硫酸亚铁质量比为5∶1∶3下合成的材料对磷的吸附量最大, 在298 K下吸附量可达49.32 mg·g-1.
(2) 动力学分析结果表明材料对磷的吸附符合伪二级动力学, 且主要速率控制步骤为孔隙内部空间的三维扩散. 热力学结果表明, 其对磷的吸附为物理化学吸附, 吸附符合Langmuir模型.
(3) 离子干扰实验表明, BCFe/S/4吸附磷时不受水中Cl-、NO3-和SO42-干扰, 而HCO3-对其影响较大.
(4) BCFe/S/4对磷的吸附机制为: 静电吸引、孔隙填充、表面化学沉淀、氢键结合和配位体效应.
| [1] | Yang Q, Wang X L, Luo W, et al. Effectiveness and mechanisms of phosphate adsorption on iron-modified biochars derived from waste activated sludge[J]. Bioresource Technology, 2018, 247: 537-544. DOI:10.1016/j.biortech.2017.09.136 |
| [2] |
易蔓, 李婷婷, 李海红, 等. Ca/Mg负载改性沼渣生物炭对水中磷的吸附特性[J]. 环境科学, 2019, 40(3): 1318-1327. Yi M, Li T T, Li H H, et al. Characteristics of phosphorus adsorption in aqueous solution by Ca/Mg-loaded biogas residue biochar[J]. Environmental Science, 2019, 40(3): 1318-1327. |
| [3] |
阳昕. 铁活化污泥基吸附剂的制备及对水中污染物去除效能研究[D]. 哈尔滨: 哈尔滨工业大学, 2016. 62-74. Yang X. Preparation of ferric-activated sluge-based adsorbent and its efficiency on the removal of contaminants from wastewaters[D]. Harbin: Harbin Institute of Technology, 2016. 62-74. |
| [4] | Loganathan P, Vigneswaran S, Kandasamy J, et al. Removal and recovery of phosphate from water using sorption[J]. Critical Reviews in Environmental Science and Technology, 2014, 44(8): 847-907. DOI:10.1080/10643389.2012.741311 |
| [5] |
吴露, 刘锋, 龙睿, 等. 3种吸附剂对污水磷污染去除性能与机制比较[J]. 环境科学, 2019, 40(2): 677-684. Wu L, Liu F, Long R, et al. Removal performance and mechanism for treating phosphorus in agricultural wastewater by three adsorbents[J]. Environmental Science, 2019, 40(2): 677-684. |
| [6] | Pala-Ozkok I, Ubay-Cokgor E, Jonas D, et al. Kinetic and microbial response of activated sludge community to acute and chronic exposure to tetracycline[J]. Journal of Hazardous Materials, 2019, 367: 418-426. DOI:10.1016/j.jhazmat.2018.12.094 |
| [7] | Yin Z H, Liu Y G, Liu S B, et al. Activated magnetic biochar by one-step synthesis: enhanced adsorption and coadsorption for 17β-estradiol and copper[J]. Science of the Total Environment, 2018, 639: 1530-1542. DOI:10.1016/j.scitotenv.2018.05.130 |
| [8] |
阳昕. 铁活化污泥基吸附剂的制备及对水中污染物去除效能研究[D]. 哈尔滨: 哈尔滨工业大学, 2016. 1-2. Yang X. Preparation of ferric-activated sluge-based adsorbent and its efficiency on the removal of contaminants from wastewaters[D]. Harbin: Harbin Institute of Technology, 2016. 1-2. |
| [9] |
赵朔, 裴勇. 氯化锌活化法制备笋壳基活性炭的工艺研究[J]. 材料导报, 2012, 26(4): 87-90. Zhao S, Pei Y. Study of preparation technology of bamboo shoot shell based activated carbon by ZnCl2 activation[J]. Materials Review, 2012, 26(4): 87-90. DOI:10.3969/j.issn.1005-023X.2012.04.024 |
| [10] |
邵瑞华. 泥质活性炭的制备及污泥热解动力学研究[D]. 西安: 西安建筑科技大学, 2011. 1-3. Shao R H. Sewage sludge-based activated carbon preparation and pyrolysis kinetics of sewage sludge from wastewater treatment plant[D]. Xi'an: Xi'an University of Architecture and Technology, 2011. 1-3. |
| [11] | Guo Y G, Huang W L, Chen B, et al. Removal of tetracycline from aqueous solution by MCM-41-zeolite a loaded nano zero valent iron: synthesis, characteristic, adsorption performance and mechanism[J]. Journal of Hazardous Materials, 2017, 339: 22-32. DOI:10.1016/j.jhazmat.2017.06.006 |
| [12] | Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+ sorption mechanisms by sludge-derived biochar[J]. Water Research, 2012, 46(3): 854-862. DOI:10.1016/j.watres.2011.11.058 |
| [13] | Rattanachueskul N, Saning A, Kaowphong S, et al. Magnetic carbon composites with a hierarchical structure for adsorption of tetracycline, prepared from sugarcane bagasse via hydrothermal carbonization coupled with simple heat treatment process[J]. Bioresource Technology, 2017, 226: 164-172. DOI:10.1016/j.biortech.2016.12.024 |
| [14] | Jang H M, Kan E. Engineered biochar from agricultural waste for removal of tetracycline in water[J]. Bioresource Technology, 2019, 284: 437-447. DOI:10.1016/j.biortech.2019.03.131 |
| [15] | Rangabhashiyam S, Anu N, Giri Nandagopal M S, et al. Relevance of isotherm models in biosorption of pollutants by agricultural byproducts[J]. Journal of Environmental Chemical Engineering, 2014, 2(1): 398-414. DOI:10.1016/j.jece.2014.01.014 |
| [16] | Tien C. Introduction to adsorption[M]. Amsterdam: Elsevier, 2019. |
| [17] | Yang G X, Jiang H. Amino modification of biochar for enhanced adsorption of copper ions from synthetic wastewater[J]. Water Research, 2014, 48: 396-405. DOI:10.1016/j.watres.2013.09.050 |
| [18] | Luo J W, Li X, Ge C J, et al. Sorption of norfloxacin, sulfamerazine and oxytetracycline by KOH-modified biochar under single and ternary systems[J]. Bioresource Technology, 2018, 263: 385-392. DOI:10.1016/j.biortech.2018.05.022 |
| [19] | Carter M C, Kilduff J E, Weber W J. Site energy distribution analysis of preloaded adsorbents[J]. Environmental Science & Technology, 1995, 29(7): 1773-1780. |
| [20] |
史月月, 单锐, 袁浩然. 改性稻壳生物炭对水溶液中甲基橙的吸附效果与机制[J]. 环境科学, 2019, 40(6): 2783-2792. Shi Y Y, Shan R, Yuan H R. Effects and mechanisms of methyl orange removal from aqueous solutions by modified rice shell biochar[J]. Environmental Science, 2019, 40(6): 2783-2792. |
| [21] | He J, Guo J S, Zhou Q H, et al. Adsorption characteristics of nitrite on natural filter medium: kinetic, equilibrium, and site energy distribution studies[J]. Ecotoxicology and Environmental Safety, 2019, 169: 435-441. DOI:10.1016/j.ecoenv.2018.11.039 |
| [22] | Zhou Y Y, He Y Z, He Y Z, et al. Analyses of tetracycline adsorption on alkali-acid modified magnetic biochar: site energy distribution consideration[J]. Science of the Total Environment, 2019, 650: 2260-2266. DOI:10.1016/j.scitotenv.2018.09.393 |
| [23] | Jung K W, Hwang M J, Jeong T U, et al. A novel approach for preparation of modified-biochar derived from marine macroalgae: dual purpose electro-modification for improvement of surface area and metal impregnation[J]. Bioresource Technology, 2015, 191: 342-345. DOI:10.1016/j.biortech.2015.05.052 |
| [24] | Yang X, Xu G R, Yu H R, et al. Preparation of ferric-activated sludge-based adsorbent from biological sludge for tetracycline removal[J]. Bioresource Technology, 2016, 211: 566-573. DOI:10.1016/j.biortech.2016.03.140 |
| [25] | Li Y M, Wang S Y, Zhang Y, et al. Enhanced tetracycline adsorption onto hydroxyapatite by Fe(Ⅲ) incorporation[J]. Journal of Molecular Liquids, 2017, 247: 171-181. DOI:10.1016/j.molliq.2017.09.110 |
| [26] | Zeng Z T, Ye S J, Wu H P, et al. Research on the sustainable efficacy of g-MoS2 decorated biochar nanocomposites for removing tetracycline hydrochloride from antibiotic-polluted aqueous solution[J]. Science of the Total Environment, 2019, 648: 206-217. DOI:10.1016/j.scitotenv.2018.08.108 |
| [27] | Lyu H, Tang J C, Huang Y, et al. Removal of hexavalent chromium from aqueous solutions by a novel biochar supported nanoscale iron sulfide composite[J]. Chemical Engineering Journal, 2017, 322: 516-524. DOI:10.1016/j.cej.2017.04.058 |
| [28] |
蒋艳红, 李安玉, 邓华, 等. 载镁香蕉秆基生物炭对养猪废水中磷的吸附性能[J]. 水处理技术, 2020, 46(6): 33-38, 44. Jiang Y H, Li A Y, Deng H, et al. Adsorption property of phosphorus by magnesium-loaded banana stem biochar from swine wastewater[J]. Technology of Water Treatment, 2020, 46(6): 33-38, 44. |
 2021, Vol. 42
2021, Vol. 42


