2. 山东省环境保护科学研究设计院有限公司, 济南 250100
2. Shandong Academy of Environmental Sciences Company Limited, Ji'nan 250100, China
小麦作为现今世界上最重要的粮食作物, 在世界农业生产中占据着极为重要的地位.然而随着现代工业的发展, 我国的土壤重金属污染问题相当严重, 每年因重金属污染而减产的粮食达1000多万t[1], 重金属污染改变土壤质量, 影响作物生长还会通过食物链进入人体, 进而危害人体身体健康[2, 3], 因此如何保障粮食生产和安全问题是制约农业发展的关键因素.
土壤微生物作为农田生态系统的重要组成部分, 其在土壤养分循环和有机质降解等生物化学过程中扮演着重要角色, 对根际土壤有机污染物的自净和重金属的迁移转化等过程发挥重要的作用.目前基于农田土壤微生物的研究, 如开展作物根际与非根际理化性质、作物根际效应、根际微生物组成以及土壤重金属的生物修复研究工作已广泛开展.已有研究发现小麦根际和非根际微生物群落结构差异显著[4], 如华北平原小麦根际土中固氮菌网络结构与非根际环境相比结构相对简单但更加稳定[5].重金属污染会导致土壤中微生物多样性减少[6], Zhang等[7]的研究发现内生细菌可以提高植株抗氧化酶系统的防御能力, 从而有效抵抗重金属引起的氧化胁迫. Wei等[8]的研究发现野生豆类根部的根瘤菌和土壤杆菌对铅、铜、镉和锌重金属都具有抗性.综上表明, 重金属污染条件下根际微生物群落组成会发生显著变化, 而且根际微生物在调控植物抗逆性方面起着非常重要的作用.
因此, 本研究通过高通量测序技术, 开展铜污染胁迫条件下小麦根际微生物群落结构组成, 通过分析铜污染处理组与非污染处理组小麦根际微生物种群变化, 比较非根际、根际以及根内环境中微生物群落结构、丰富度和多样性差异, 深入探究铜胁迫对小麦根际微生物群落的影响作用.
1 材料与方法 1.1 供试材料供试土壤采自山东省滕州市农田的表层土壤(0~20 cm), 土样采集后保存于塑封袋中带回试验室, 置于通风处自然风干后过2 mm筛.供试小麦(Triticum aestivum L.)品种为济麦22, 购买于山东省星科种业有限公司.
污染土壤制备:称取1.00 kg风干过筛土壤置于通风橱中, 将氯化铜粉末(8.44 g)溶于去离子水中后少量多次加入供试土壤中并充分混合均匀, 制备铜污染土壤.将制备完成的铜污染土壤置于无菌塑料袋中平衡7 d后, 通过氢氟酸-高氯酸酸溶法消煮并采用ICP-MS测定污染土壤中铜的含量.经测定, 供试土壤中原始铜含量为0.82 mg·kg-1, 制备所得污染土壤中的铜含量为344 mg·kg-1.
1.2 盆栽培养选择大小一致, 颗粒饱满的小麦种子用无菌水洗净之后依次用75%的乙醇浸种30 s和10%次氯酸钠溶液浸种10 min进行种子表面杀菌, 然后用超纯无菌水彻底清洗.将种子转移至湿润的无菌石英砂上, 于30℃恒温黑暗环境中培养5 d, 待种子萌芽后转移至霍格兰营养液中继续培养1周, 然后转移至土壤中进行盆栽试验.每盆装入供试铜污染土壤约120 g, 选择长势相近的小麦苗2株进行移植.同时以种植小麦的非污染培养和未种植小麦的铜污染培养作为对照, 所有处理设置4个重复.整个小麦生长期间用灭菌蒸馏水浇灌, 保持田间持水量的60%.盆栽放置于温室中, 每10 d将盆栽的位置随机移动一次, 尽量保证盆栽的环境保持一致.
在小麦生长至60 d时进行采样, 分别采集小麦根系和根际土壤, 同时采集未种植小麦的对照处理作为非根际土壤.将整株小麦从盆中取出, 通过抖落摇晃至小麦根部约附着1 mm厚度土壤, 经过涡旋振荡将附着于根系表面的土壤清洗至灭菌的去离子水中, 该部分土样即为根际土壤; 将清洗过的小麦根系继续超声3次后清洗根系表面直至洗净, 保存小麦根系用于提取根内微生物; 而未种植小麦的对照土壤即为非根际土壤.将所得样品置于-20℃保存用于后续DNA样品提取.
1.3 DNA样品提取及高通量测序采用Fast DNA Spin Kit for Soil(MP Biomedicials, LLC)试剂盒分别对根际土、非根际土壤(新鲜土样0.25 g)和小麦根系(新鲜样品0.10 g)样品进行DNA提取[9].采用PCR反应体系对16S rRNA基因的V3~V4区域进行扩增, 引物为338F和806R.同时, 为了区分不同的样品, 在338F前端加入不同barcode序列. PCR的反应条件为:98℃ 30 s; 27个循环×(98℃ 30 s, 50℃ 30 s, 72℃ 30 s); 72℃ 5 min.扩增后DNA经纯化和混匀后上机测定(Illumina MiSeq, USA), 高通量测序由上海美吉生物医药科技有限公司完成.
1.4 统计分析用Majorbio平台(http://www.majorbio.com/)进行小麦不同根系分区(根内、根际、非根际)的微生物群落分析.为了得到每个OTU(operational taxonomic unit)对应的物种分类信息, 采用RDP classifier贝叶斯算法对97%相似水平的OTU序列进行分类学分析, 细菌16S rRNA数据库为Silva(Release132 http://www.arb-silva.de).利用R软件进行物种Venn图、Circos图、热图和PCoA图绘制.
2 结果与分析 2.1 铜污染胁迫下小麦根际微生物群落的α多样性通过表 1可以看出, 在所有处理中根际土与非根际土中微生物群落的均匀度(Shannon)和丰富度(ACE、Chao)远远高于根内微生物, 差异达到极显著水平(P < 0.001).然而, 在非污染处理中, 根际土壤中的微生物多样性与非根际土壤微生物多样性相比, 差异并未达到显著水平(P>0.05).同时比较铜污染与非污染处理中的微生物多样性发现, 铜污染胁迫降低了根际环境中的微生物多样性且差异显著(P < 0.05);在非根际和根内环境中, 尽管铜污染胁迫降低了对应根系分区中的微生物多样性, 但差异并未达到显著水平(P>0.05).
|
|
表 1 小麦根系不同分区微生物群落α多样性指数 Table 1 The α diversity indexes of the microbial communities in different rhizocompartments of wheat |
2.2 铜污染胁迫下小麦根际微生物群落的β多样性
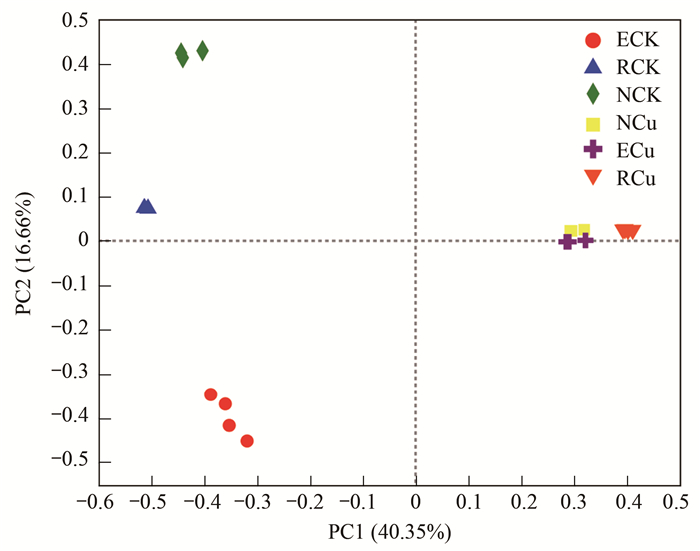
根据各样品的细菌物种组成数据(OTUs)计算bray_curtis距离, 基于bray_curtis距离矩阵进行主坐标分析(PCoA)分析(图 1).从结果可以看出主成分1(PC1)和主成分2(PC2)是共解释了57.01%的微生物结构差异性, 贡献率分别为40.35%和16.66%.基于图 1可知铜污染胁迫处理与非污染对照组微生物群落差异明显.且与对照组小麦根际土、非根际土和根内微生物群落的相对分散程度不同, 铜污染胁迫处理中小麦非根际土、根际土和根内的微生物群落较为集中, 说明铜污染胁迫能够显著改变微生物群落结构, 且能够缩小不同根系分区中的微生物群落差异.
|
图例缩写与表 1相同, 下同 图 1 小麦不同根系分区的微生物群落PCoA分析 Fig. 1 PCoA analysis of microbial communities in different rhizocompartments of wheat |
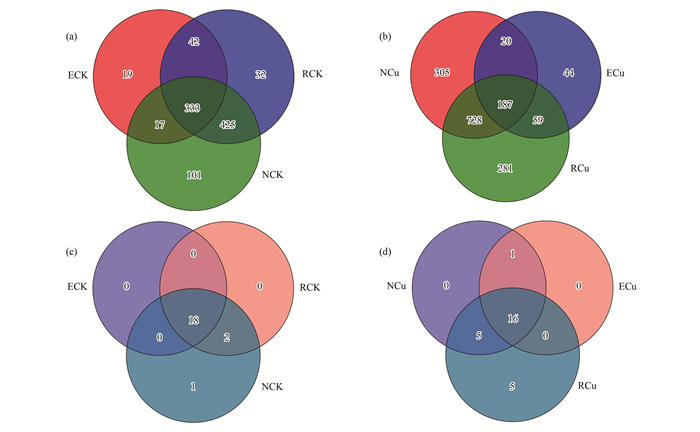
从Venn图(OTU水平)中可以看出在非污染对照组中[图 2(a)], 小麦非根际土(NCK)、根际土(RCK)和根内(ECK)环境中分别测得微生物OTU个数为876、832和411.其中非根际, 根际和根内三者共有的OTU个数为333, 分别占非根际、根际和根内OTU总数的38.01%、40.02%和81.02%.从门水平的Venn图可以看出[图 2(c)], 非污染处理非根际、根际和根内微生物分别包含21、20和18个菌门.根内与根际环境中共有菌门18个.
|
(a)和(b)OTU水平; (e)和(d)门水平 图 2 不同处理中小麦不同根系分区的微生物群落在OTU水平和门水平的Venn图 Fig. 2 Venn diagram of microbial communities in different rhizocompartments of wheat under different treatments at the OTU and phylum level |
从Venn图(OTU水平)中可以看出在铜污染试验组中小麦非根际土(NCu)、根际土(RCu)和根内(ECu)环境中分别测得微生物OTU个数为1240、1255、310 [图 2(b)].其中非根际, 根际和根内环境中共有的OTU个数为187, 分别占非根际、根际和根内OTU总数的15.08%、14.90%和60.32%.从门水平的Venn图可以看出, 铜污染试验组[图 2(d)]非根际、根际和根内微生物分别包含22、26和17个菌门.根内与根际环境中共有菌门16个.从结果中可以看出, 与非污染对照相比, 铜污染试验组中小麦非根际、根际、根内环境中共有OTU的个数降低, 而特有OTU的个数增加, 表明铜污染胁迫改变了小麦根系微域中的微生物组成, 能够显著促进或抑制部分微生物的生长, 而且使得微生物群落差异显著.
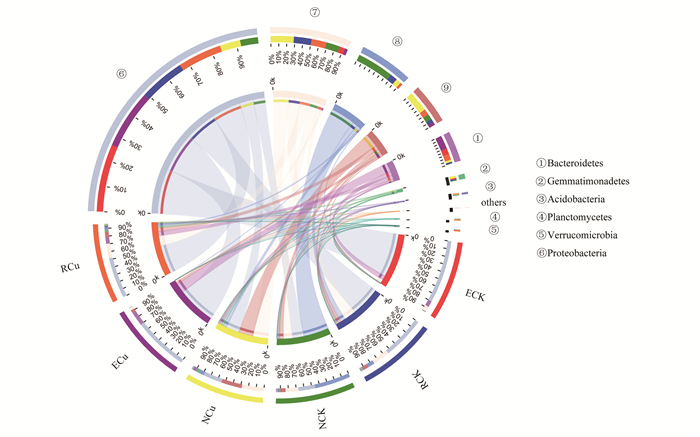
2.4 铜污染胁迫下小麦不同根系分区中微生物菌门组成通过图 3可以看出, 在铜污染处理下, 非根际土环境中变形菌门(Proteobacteria)、放线菌门(Actinobacteria)和厚壁菌门(Firmicutes)是优势菌群, 相对丰度分别为25%、30%和28%;根际土壤中变形菌门和放线菌门是优势菌群, 相对丰度分别为54%和19%;根内组分中的优势菌群则为变形菌门和拟杆菌门(Bacteroidetes)其相对丰度分别为73%和19%.另外, 结果发现厚壁菌门、放线菌门、芽单孢菌门(Gemmatimonadetes)和绿弯菌门(Chloroflexi)的相对丰度沿非根际、根际、根内呈现逐渐递减的趋势, 变形菌门和拟杆菌门的丰度变化趋势则正好相反.在非污染对照组中, 变形菌门、放线菌门和绿弯菌门是非根际土中的优势菌群, 相对丰度分别为22%、17%和48%;变形菌门和放线菌门是根际环境中的优势菌群, 相对丰度分别为57%和23%;而根内组分中的优势菌群为变形菌门, 其相对丰度为84%.绿弯菌门、厚壁菌门、芽单孢菌门、酸杆菌门(Acidobateria)和浮霉菌门(Planctomycetes)相对丰度由非根际、根际和根内呈现出逐渐递减的趋势, 而变形菌门和拟杆菌门与之相反.
|
图 3 不同处理下小麦不同根系分区中的微生物菌门Circos图 Fig. 3 Circos diagram of microbial communities in different rhizocompartments of wheat at the phylum level under different treatments |
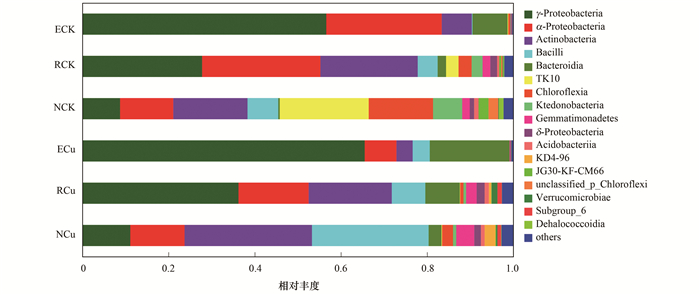
通过柱形图分析小麦不同根系分区(非根际、根际和根内)微生物在纲水平上的组成差异(图 4).其中α变形菌纲(α-Proteobacteria)和γ变形菌纲(γ-Proteobacteria)在铜污染处理和非污染处理中均存在.其中, 铜污染处理中γ变形菌纲在根内(65.55%)和根际(36.24%)环境中的相对丰度远远高于非根际环境(11.11%); 而在非污染处理中, 类似地, 根内(56.62%)和根际(27.80%)环境中的γ变形菌纲相对丰度也远高于根内环境(8.75%).
|
图 4 不同处理小麦不同根系分区中的微生物菌纲柱形图 Fig. 4 Bar chart of microbial communities in different rhizocompartments of wheat at the class level under different treatments |
与非污染处理相比, 在根际环境中, 铜污染处理显著促进了γ变形菌纲、杆菌纲(Bacilli)、拟杆菌纲(Bacteroidia)和芽单孢菌纲(Gemmatimonadetes)相对丰度的增加, 而α变形菌纲、放线菌纲(Actinobacteria)、TK10、绿弯菌纲(Chloroflexia)和纤线杆菌纲(Ktedonobacteria)的相对丰度降低; 在根内环境中, 铜污染处理促进了γ变形菌纲、杆菌纲和拟杆菌纲的生长, 而抑制了α变形菌纲和放线菌纲的生长; 在非根际环境中, 铜污染处理中放线菌纲、杆菌纲、γ变形菌纲和芽单孢菌纲的相对丰度增加, 而TK10、绿弯菌纲和纤线杆菌纲的相对丰度减少.
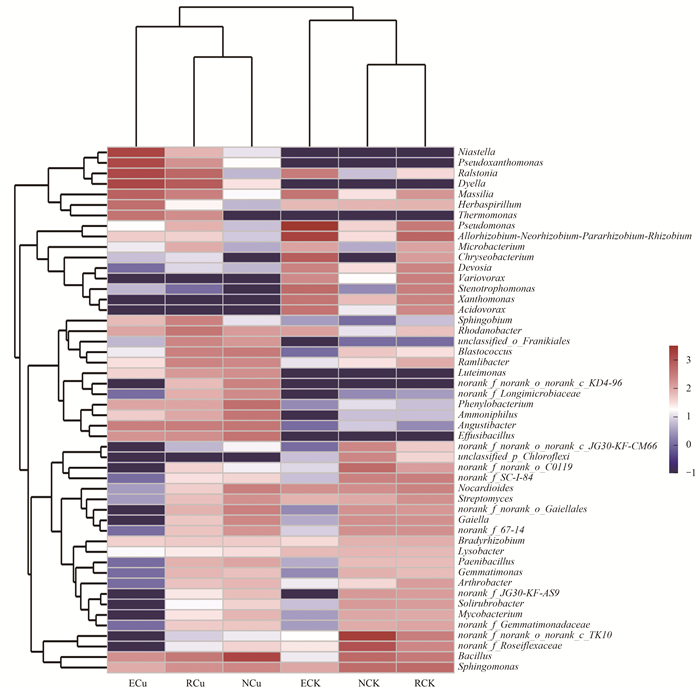
2.6 铜污染胁迫下小麦不同根系分区中微生物菌属组成从图 5结果中可以明显看出小麦不同根系分区(非根际、根际和根内)在不同处理中的微生物群落组成差异显著且区分明显.铜污染处理条件下, 在根内环境中, 相对丰度较高的菌属主要是戴氏菌属(Dyella)、青枯菌属(Ralstonia)、农研丝杆菌属(Niastella)、假黄色单胞菌属(Pseudoxanthomonas)、马赛菌属(Massilia)、热单胞菌属(Thermomonas)和Herbaspirilum; 根际环境中, 相对丰度较高的菌属包括戴氏菌属、青枯菌属、芽孢杆菌属、产黄杆菌属(Rhodanobacter)和Angustibacter; 在非根际环境中, 相对丰度较高的菌属主要包括芽孢杆菌属(Bacillus)、Angustibacter、多变芽孢杆菌属(Effusibacillus)、苯甲基杆菌属(Phenylobacterium)、芽球菌属(Blastococcus)和李斯特氏菌属(Ammoniphilus).非根际群落中的优势属包括芽孢杆菌属、苯甲基杆菌属、李斯特氏菌属、类诺氏菌属(Nocardioides)和多变芽孢杆菌属.
|
图 5 不同处理小麦不同根系分区中的微生物菌属热图 Fig. 5 Heat map of microbial communities in different rhizocompartments of wheat at the genus level under different treatments |
有研究表明, 植物根内微生物群落的结构组成与根际相比具有高度的特异性, 微生物多样性显著降低, 说明植物根系对进入其根内的微生物具有选择作用[10~13]. Bulgarelli等[14]利用木碎片模拟植物根系细胞壁, 结果发现在拟南芥根内微生物组的形成过程中约有60%是宿主植物自身决定的. Lundberg等[15]通过研究600种拟南芥的根际微生物组发现, 拟南芥根内微生物的Shannon多样性远远低于根际和土壤中的群落多样性.本研究结果中发现无论在铜污染胁迫处理中还是非污染处理中, 小麦根内微生物多样性均远低于根际和非根际环境, 说明仅有部分微生物种类能够进入到小麦根内环境中定殖生长. Coleman-Derr等[16]的研究发现绝大部分在根内富集的微生物也同时富集在根际和非根际环境中.本研究发现无论是铜污染处理还是非污染处理, 小麦根内和根际环境中共同包含变形菌门、放线菌门、厚壁菌门和拟杆菌门等多个菌门.此外发现在铜污染处理条件下根内与根际环境中的共有微生物占根内总微生物的79.35%, 而且大部分在根际环境中丰度较低的微生物在根内环境中的丰度也较低.综上说明, 根表作为微生物进入根内环境的门户, 对于根内微生物的定殖起着过滤和筛选的作用.
3.2 铜污染胁迫对小麦根际微生物群落的影响通常情况下, 由于植物根系代谢为根际微生物提供较多的碳源, 使得根际土壤中的微生物数量和多样性高于非根际环境中, 如杨树人工林中的根际细菌多样性高于非根际环境中[17]. Peiffer等[18]通过高通量测序分析发现, 玉米根际与周围土壤中的微生物群落在多样性和丰富度方面存在显著差异, 植物根际区域中的微生物活性更高.而在本研究中, 无论是铜污染处理还是非污染处理中小麦根际环境中的微生物多样性与非根际环境差异未达到显著水平.与非污染处理相比, 铜污染处理中小麦根内、根际和非根际环境中微生物Shannon多样性均有所降低.在根际环境中, 根系分泌物螯合酸类物质能够活化土壤中的重金属, 从而使得重金属对微生物的毒性增强, 部分微生物不能在铜污染的环境下生存, 因此使得其小麦根际土壤微生物的多样性降低, 抵消了根际分泌物对根际微生物的正激发效应.
优势微生物在土壤中相对丰度较高且在生态功能调控中发挥着重要作用[19].变形菌门和放线菌门在根际和非根际环境中富集, 这与其强适应性能力有关.其中变形菌门可以在大多数环境中生存并繁殖成为优势菌是因为其外膜主要由脂多糖组成, 可以保护其内部遗传物质不受外部干扰[20, 21].在非根际环境中, 铜污染处理中厚壁菌门的相对丰度显著高于非污染处理中, 而绿弯菌门在非污染处理中的相对丰度显著高于铜污染处理, 这表明重金属铜对绿弯菌门具有抑制作用, 而厚壁菌门则对铜污染有较好的适应能力.
根系分泌物是根系-微生物相互影响关系的重要媒介, 对根际定殖微生物种类具有选择作用[22~25].铜污染处理中, 在非根际环境中, 厚壁菌门的相对丰度远远高于根际和根内环境; 在非污染处理中, 绿弯菌门在非根际环境中的相对丰度远远高于根际和根内环境, 而在两组处理中, 变形菌门(Proteobacteria)在根际土中的相对丰度均远高于非根际土, 这可能是由于小麦根系分泌物产生的根际效应所导致.铜污染胁迫条件下, 杆菌纲和γ变形菌纲在根内、根际、非根际环境中的丰度显著提高, 表明这些菌群在铜污染环境中更具竞争力, 可以在铜污染环境中较好地生存.
与非污染处理相比, 铜污染处理中丰度较高的菌属包括芽孢杆菌属、假黄色单胞菌属、多变芽孢杆菌属、Angustibacter、苯甲基杆菌属、Ammoniphilus、藤黄色单胞菌属(Luteimonas)、芽球菌属、Ramlibacter和罗河杆菌属(Rhodanobacter).其中芽孢杆菌属能够形成高抗性芽孢, 定殖能力和抗逆性能力非常强; 假黄色单胞菌属和鞘氨醇单胞菌属(Sphingomonas)对土壤中的有毒物质具有一定的降解能力, 且与植物联系非常密切, 在根际环境中可以分泌糖类营养物促进植物生长[26, 27].以上说明这些菌属具有较强的抗逆性, 能够在铜污染胁迫下存活且能够为植物提供营养物质.
4 结论(1) 根表作为微生物进入根内环境的门户, 对于根内微生物的定殖起着过滤和筛选的作用.
(2) 与非污染对照相比, 在铜污染胁迫条件下, 小麦非根际土和根际土中的优势菌门为变形菌门和放线菌门, 这与其强环境适应能力有关.
(3) 芽孢杆菌属、假黄色单胞菌属、多变芽孢杆菌属、Angustibacter、苯甲基杆菌属、Ammoniphilus、藤黄色单胞菌属、芽球菌属、Ramlibacter和罗河杆菌属具有较强的耐铜能力.
| [1] |
贾夏, 周春娟, 董岁明. Pb2+/Cd2+处理对冬小麦幼苗根际微生物种群数量的影响[J]. 沈阳农业大学学报, 2011, 42(4): 443-448. Jia X, Zhou C J, Dong S M. Effects of Pb2+/Cd2+ on the number of microorganisms in the rhizosphere of winter wheat seedlings[J]. Journal of Shenyang Agricultural University, 2011, 42(4): 443-448. DOI:10.3969/j.issn.1000-1700.2011.04.011 |
| [2] | Mahar A, Wang P, Ali A, et al. Challenges and opportunities in the phytoremediation of heavy metals contaminated soils:a review[J]. Ecotoxicology and Environmental Safety, 2016, 126: 111-121. DOI:10.1016/j.ecoenv.2015.12.023 |
| [3] |
黄健, 朱旭炎, 陆金, 等. 狮子山矿区不同土地利用类型对土壤微生物群落多样性的影响[J]. 环境科学, 2019, 40(12): 5550-5560. Huang J, Zhu X Y, Lu J, et al. Effects of different land use types on microbial community diversity in the Shizishan mining area[J]. Environmental Science, 2019, 40(12): 5550-5560. |
| [4] |
王晓婷, 陈瑞蕊, 井忠旺, 等. 水稻和小麦根际效应及细菌群落特征的比较研究[J]. 土壤学报, 2019, 56(2): 443-453. Wang X T, Chen R R, Jing Z W, et al. Comparative study on rhizosphere effects and bacterial communities in the rhizospheres of rice and wheat[J]. Acta Pedologica Sinica, 2019, 56(2): 443-453. |
| [5] | Fan K K, Weisenhorn P, Gilbert J A, et al. Soil pH correlates with the co-occurrence and assemblage process of diazotrophic communities in rhizosphere and bulk soils of wheat fields[J]. Soil Biology and Biochemistry, 2018, 121: 185-192. DOI:10.1016/j.soilbio.2018.03.017 |
| [6] | Khan S, Hesham A E L, Qiao M, et al. Effects of Cd and Pb on soil microbial community structure and activities[J]. Environmental Science and Pollution Research, 2010, 17(2): 288-296. DOI:10.1007/s11356-009-0134-4 |
| [7] | Zhang X X, Li C J, Nan Z B. Effects of cadmium stress on growth and anti-oxidative systems in Achnatherum inebrians symbiotic with Neotyphodium gansuense[J]. Journal of Hazardous Materials, 2010, 175(1-3): 703-709. DOI:10.1016/j.jhazmat.2009.10.066 |
| [8] | Wei G H, Fan L M, Zhu W F, et al. Isolation and characterization of the heavy metal resistant bacteria CCNWRS33-2 isolated from root nodule of Lespedeza cuneata in gold mine tailings in China[J]. Journal of Hazardous Materials, 2009, 162(1): 50-56. DOI:10.1016/j.jhazmat.2008.05.040 |
| [9] | Xu Y, Ge Y, Song J X, et al. Assembly of root-associated microbial community of typical rice cultivars in different soil types[J]. Biology and Fertility of Soils, 2020, 56(2): 249-260. DOI:10.1007/s00374-019-01406-2 |
| [10] | Edwards J, Johnson C, Santos-Medellin C, et al. Structure, variation, and assembly of the root-associated microbiomes of rice[J]. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(8): E911-E920. DOI:10.1073/pnas.1414592112 |
| [11] | Vandenkoornhuyse P, Quaiser A, Duhamel M, et al. The importance of the microbiome of the plant holobiont[J]. New Phytologist, 2015, 206(4): 1196-1206. DOI:10.1111/nph.13312 |
| [12] | Philippot L, Raaijmakers J M, Lemanceau P, et al. Going back to the roots:the microbial ecology of the rhizosphere[J]. Nature Reviews Microbiology, 2013, 11(11): 789-799. DOI:10.1038/nrmicro3109 |
| [13] | Hardoim P R, van Overbeek L S, van Elsas J D. Properties of bacterial endophytes and their proposed role in plant growth[J]. Trends in Microbiology, 2008, 16(10): 463-471. DOI:10.1016/j.tim.2008.07.008 |
| [14] | Bulgarelli D, Rott M, Schlaeppi K, et al. Revealing structure and assembly cues for Arabidopsis root-inhabiting bacterial microbiota[J]. Nature, 2012, 488(7409): 91-95. DOI:10.1038/nature11336 |
| [15] | Lundberg D S, Lebeis S L, Paredes S H, et al. Defining the core Arabidopsis thaliana root microbiome[J]. Nature, 2012, 488(7409): 86-90. DOI:10.1038/nature11237 |
| [16] | Coleman-Derr D, Desgarennes D, Fonseca-Garcia C, et al. Plant compartment and biogeography affect microbiome composition in cultivated and native Agave species[J]. New Phytologist, 2016, 209(2): 798-811. DOI:10.1111/nph.13697 |
| [17] |
汪其同, 朱婉芮, 刘梦玲, 等. 基于高通量测序的杨树人工林根际和非根际细菌群落结构比较[J]. 应用与环境生物学报, 2015, 21(5): 967-973. Wang Q T, Zhu W R, Liu M L, et al. Comparison on bacterial community of rhizosphere and bulk soil of poplar plantation based on pyrosequencing[J]. Chinese Journal of Applied and Environmental Biology, 2015, 21(5): 967-973. |
| [18] | Peiffer J A, Spor A, Koren O, et al. Diversity and heritability of the maize rhizosphere microbiome under field conditions[J]. Proceedings of the National Academy of Sciences of the United States of America, 2013, 110(16): 6548-6553. DOI:10.1073/pnas.1302837110 |
| [19] |
王燕, 程东会, 檀文炳, 等. 土壤微生物群落结构对生活源和工业源再生水灌溉的差异化响应[J]. 环境科学, 2020, 41(9): 4253-4261. Wang Y, Cheng D H, Tan W B, et al. Different responses of soil microbial community structure to irrigation with treated wastewater from domestic and industrial sources[J]. Environmental Science, 2020, 41(9): 4253-4261. |
| [20] | Song H G, Kim O S, Yoo J J, et al. Monitoring of soil bacterial community and some inoculated bacteria after prescribed fire in microcosm[J]. Journal of Microbiology, 2004, 42(4): 285-291. |
| [21] | Whalley W R, Riseley B, Leeds-Harrison P B, et al. Structural differences between bulk and rhizosphere soil[J]. European Journal of Soil Science, 2005, 56(3): 353-360. DOI:10.1111/j.1365-2389.2004.00670.x |
| [22] | Haichar F E Z, Marol C, Berge O, et al. Plant host habitat and root exudates shape soil bacterial community structure[J]. The ISME Journal, 2008, 2(12): 1221-1230. DOI:10.1038/ismej.2008.80 |
| [23] | Berg G, Smalla K. Plant species and soil type cooperatively shape the structure and function of microbial communities in the rhizosphere[J]. FEMS Microbiology Ecology, 2009, 68(1): 1-13. DOI:10.1111/j.1574-6941.2009.00654.x |
| [24] | Grayston S J, Wang S, Campbell C D, et al. Selective influence of plant species on microbial diversity in the rhizosphere[J]. Soil Biology and Biochemistry, 1998, 30(3): 369-378. DOI:10.1016/S0038-0717(97)00124-7 |
| [25] | Grayston S J, Griffith G S, Mawdsley J L, et al. Accounting for variability in soil microbial communities of temperate upland grassland ecosystems[J]. Soil Biology and Biochemistry, 2001, 33(4-5): 533-551. DOI:10.1016/S0038-0717(00)00194-2 |
| [26] |
汪娅婷, 付丽娜, 姬广海, 等. 基于高通量测序技术研究云南玉米根际微生物群落多样性[J]. 江西农业大学学报, 2019, 41(3): 491-500. Wang Y T, Fu L N, Ji G H, et al. A study of the microbial community diversity of corn rhizosphere in Yunnan Province based on high-throughput sequencing technique[J]. Acta Agriculturae Universitatis Jiangxiensis, 2019, 41(3): 491-500. |
| [27] |
胡杰, 何晓红, 李大平, 等. 鞘氨醇单胞菌研究进展[J]. 应用与环境生物学报, 2007, 13(3): 431-437. Hu J, He X H, Li D P, et al. Progress in research of Sphingomonas[J]. Chinese Journal of Applied & Environmental Biology, 2007, 13(3): 431-437. DOI:10.3321/j.issn:1006-687X.2007.03.030 |
 2021, Vol. 42
2021, Vol. 42


