2. 中国环境科学研究院, 国家环境保护化学品生态效应与风险评估重点实验室, 北京 100012;
3. 江西理工大学资源与环境工程学院, 赣州 341000;
4. 中北大学理学院, 太原 030051
2. State Environmental Protection Key Laboratory of Ecological Effect and Risk Assessment of Chemicals, Chinese Research Academy of Environmental Sciences, Beijing 100012, China;
3. College of Resources and Environmental Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, China;
4. College of Science, North University of China, Taiyuan 030051, China
溴代阻燃剂在20世纪60年代成为使用最广泛的有机阻燃剂, 但由于其在环境中的持久性、生物累积性和生物毒性, 逐步在世界范围内被禁止使用.有机磷酸酯(organophosphate esters, OPEs)作为溴代阻燃剂的替代品, 具有良好的阻燃作用和增塑效果, 目前已经被普遍应用在食品包装、建筑材料、电子设备和纺织品等产品中[1].根据IHS咨询公司2017年的市场研究, 2016年世界范围内阻燃剂的消耗量已超过225万t·a-1, 且年消费量将继续以3.1%的速度增长.其中, 亚洲的阻燃剂消耗量最大, 占50%.而中国是最大的阻燃剂消费国, 占26%. OPEs的消费比例越来越高, 2008年占全球阻燃剂消费比例的11%, 2016年占比18%, 消费量达40.5万t[2].由于OPEs是以物理的方式添加到材料中, 很容易通过挥发、产品磨损、泄漏等方式进入环境[3].目前, 已在水体、沉积物、大气和室内灰尘等环境介质[3~6], 甚至在蔬菜、动物体内及人类血液、尿液、母乳中检测到OPEs[7~9].有研究表明OPEs具有细胞毒性、遗传毒性、发育毒性、内分泌干扰效应和神经毒性等[4], 如磷酸三(2-氯乙基)酯(TCEP)可以破坏甲状腺内分泌系统并具有神经毒性; 磷酸三苯酯(TPhP)会降低神经突触和羧酸酯酶活动, 表现出神经毒性、接触过敏和影响生育能力.
地表水中OPEs主要来自于OPEs产品泄漏和挥发、污水排放和大气沉降等.如工业企业生产过程中排放的废水, 液压油和润滑油的损耗和泄漏, 产品中的OPEs会挥发进入大气, 通过沉降和地表径流直接或间接进入水体.污水中普遍含有较高浓度的OPEs, 且被认为是地表水中OPEs的主要来源.有研究表明污水处理厂中仅有50%的OPEs被有效去除, 剩余的OPEs会随出水直接和间接排放到地表水中[10].世界各地污水处理厂进出水中都检测到较高浓度的OPEs, 由于OPEs在不同国家和地区使用类型和使用量不同, 在环境中的含量也略有差异[11~13].本课题组前期对北京某污水处理厂不同工艺和污水受纳河流水体上下游取样检测, 污水厂出水中∑OPEs浓度为162.5 ng·L-1, 主要以磷酸二(2-乙基)己基二苯酯(EHDPP)和磷酸三(2-乙基己基)酯(TEHP)为主, 受纳河流下游的∑OPEs平均浓度虽低于污水处理厂出水总浓度, 但明显高于上游来水浓度, 可推断河流受到污水处理厂出水的影响[14].此外, 受工业出水影响的河流中OPEs的污染水平相对较高, 如Cristale等[15]在英国接收工业废水的埃尔河中检出∑OPEs浓度范围为113~26 050 ng·L-1. Wang等[3]在太湖水体和沉积物中均检测出OPEs, 其中TCEP和磷酸三(1-氯-2-丙基)酯(TCPP)占主要成分, 并推断其与电器、纺织、机械和塑料等生产企业排放有关.Xu等[16]对珠三角地区不同类型企业废水处理厂进出水中OPEs进行调查研究, 发现印刷电路板废水处理厂进出水中∑OPEs浓度最高, 主要以磷酸三正丁酯(TnBP)、TCPP和TCEP为主; 汽车零配件加工企业浓度相对较低, 进出水浓度分别为65.8 ng·L-1和37.2 ng·L-1; 纸箱生产企业进水中主要成分为TCPP、TPhP和TCEP.可见不同地区和不同类型企业废水中OPEs浓度水平及组成略有不同.由于OPEs为工业产品, 无自然排放源, 因而研究污水处理厂进出水和企业废水中OPEs的分布特征对水环境中OPEs的来源解析有重要意义.
太湖是我国第二大淡水湖泊, 地处长三角经济发达区, 为苏州、无锡、常州和湖州所包围, 经济发达, 是流域内主要城市的最主要的供水水源地和重要的淡水生态系统.丹金溧漕河经京杭大运河与长江相连, 是太湖西部地区主要水运干线, 此外还承担洪水调蓄和纳污等功能[17].受周围人类活动的影响, 丹金溧漕河和京杭大运河水质较差, 水生态系统遭到破坏, 且流域内主导经济是工业, 主要有纺织、印染、电镀、医药和化工等企业, 均是与OPEs相关的主导产业, 可能存在风险.本文对流域内典型行业废水、污水处理厂进出水以及地表水中13种OPEs进行检测, 分析其污染水平及组成特征, 判别地表水中OPEs的来源, 并评估其可能造成的生态风险, 以期为深入了解水环境中OPEs的来源及归趋提供科学依据, 也为流域环境管理和污染防治提供基础数据.
1 材料与方法 1.1 仪器与试剂电喷雾电离(ESI)串联三重四级杆质谱仪(Xevo T-QS, Waters, MA, USA); LabTech-MV5氮吹浓缩仪; 超纯水由Mili-Q系统(Millipore, MA, 美国)制备.玻璃纤维滤膜(直径47 mm, 孔径0.45 μm)与ENVI-18柱(6 mL, 500 mg, Supelclean)购自美国Waters公司.
磷酸三甲酯(TMP)、磷酸三乙酯(TEP)、TPhP、磷酸三丁氧基乙酯(TBEP)、磷酸三丙酯(TPrP)、TCEP、TCPP、磷酸三(1, 3-二氯-2-丙基)酯(TDCP)、TEHP、磷酸三甲苯酯(TCrP)、磷酸甲苯二甲苯酯(CDPP)和EHDPP购自德国Dr. Ehremstorfer公司(纯度均大于98%).TnBP-d27、TCPP-d18和TiBP购自Toronto Research Chemicals Inc.公司.TPrP-d21购自挪威Chiron AS公司.分析纯氨水(25%~28%)与浓盐酸购自国药集团化学试剂有限公司(北京), 色谱纯甲醇、乙腈购自Fisher公司(Poole, 英国), 甲酸(FA)购自Sigma-Aldrich公司(Bellefonte, 美国).OPEs的理化性质如表 1所示.
|
|
表 1 OPEs化合物名称及理化性质[18] Table 1 Physicochemical properties of the OPEs |
1.2 样品采集
在2019年6月对流域内7家企业(Q1~Q7)进行调研, 在生产企业排水口取样.采集2家污水处理厂W1、W2进水(W1-1、W2-1)和出水(W1-2、W2-2).在丹金溧漕河(S1~S9)和京杭大运河(S10~S14)采集地表水.每个点位取水样1 L, 置于棕色玻璃瓶中, 冷藏运回实验室并在24 h内处理完.采样点位如图 1所示.
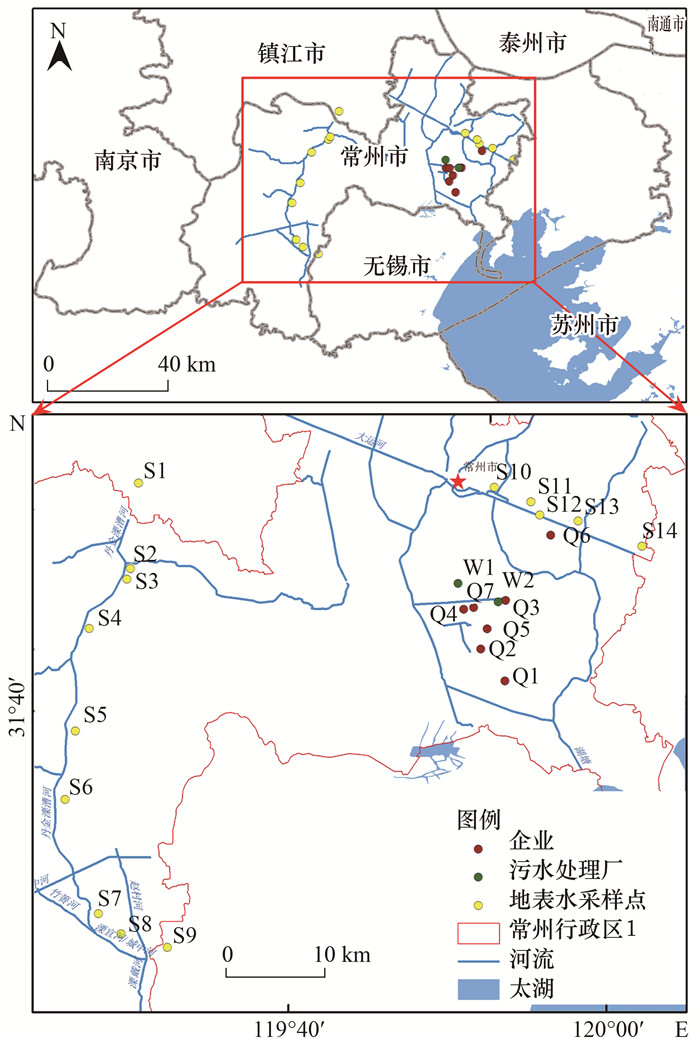
|
图 1 采样点位示意 Fig. 1 Location of sampling sites |
量取1 L水样, 经0.45 μm玻璃纤维滤膜过滤, 加入50 μL浓度为100 μg·L-1的混合内标(TnBP-d27、TCPP-d18和TPrP-d21), 用ENVI-18柱进行富集, 1 mL·min-1的流速上样, 上样前ENVI-18柱用5 mL二氯甲烷、5 mL乙腈和10 mL水活化; 样品加载完后, 抽干10 min, 再用10 mL超纯水淋洗SPE柱, 继续真空抽提1 h以除去萃取柱中多余水分; 用8 mL 25%二氯甲烷的乙腈洗脱, 收集洗脱液在40℃水浴中, 氮气吹至近干, 初始流动相比例定容至1 mL, 过0.22 μm的尼龙膜, 用UPLC-MS/MS分析.
1.4 仪器分析液相色谱柱为ACQUITY UPLC® BEH C18(1.7 μm, 50×2.1 mm, Waters, MA, 美国), 柱温40℃, 进样量5 μL, 流动相采用水/乙腈(A:水相含0.1%甲酸, B:乙腈), 流速0.4 mL·min-1, 梯度洗脱程序为:0~1 min 2% B, 1.1 min 30% B, 2.5 min 55% B, 6.5 min 65% B, 7.2~8.9 min 98% B, 9~10 min 2% B.质谱运行模式为正电离模式ESI+、多反应选择离子监测(multiple reaction monitoring, MRM).电喷雾电离, 氮气作为脱溶剂和雾化气体, 毛细管电压为0.5 kV, 离子源和脱溶温度分别为150℃和400℃.氩气为碰撞气, 仪器工作软件为Masslynx 4.2.目标物质谱参数见表 2.
|
|
表 2 目标物离子对及相应质谱参数1) Table 2 Analyte ions and MS parameters of the target OPEs |
1.5 质量控制与质量保证
采用内标法定量, 线性范围为0.1~200 μg·L-1, 相关系数均大于0.99(表 3).分别以高纯水、地表水和污水作为基质进行加标回收率实验, 加标水平为10 ng·L-1(n=5), 对应回收率分别为83.7%~108.5%、73.8%~103.6%和84.5%~116.1%, 相对标准偏差均低于10%, 重现性良好.方法检出限(信噪比LOD, S/N=3)在0.1~0.7 ng·L-1之间, 方法定量限(S/N=10)在0.3~2.5 ng·L-1之间.
|
|
表 3 方法的线性范围、相关系数(R2)、检出限及加标回收率 Table 3 Linear range, correlation coefficient (R2), detection limit, and recovery rate of the method |
2 结果与讨论 2.1 企业废水中OPEs的污染特征
企业废水中13种OPEs浓度水平及组成特征如图 2所示.Q1为制药企业, 废水中∑OPEs浓度相对较低, 为114.35 ng·L-1, 共检出10种OPEs, 其中TCPP、TBEP和TDCP占比较高.两家电镀企业Q2和Q3浓度水平虽有差异, 但组成上均以TEP和TCPP为主, 两者占OPEs的质量分数为76.51%~83.59%. Q4(电子元件加工企业)废水中TCPP占主要成分, 浓度为452.57 ng·L-1; 其次为TBEP, 浓度为218.52 ng·L-1.Q5热电企业废水中∑OPEs浓度为159.94 ng·L-1, TCPP和TCEP占OPEs的70.50%.该企业主要是焚烧处理城市生活垃圾, 因为TCPP和TCEP是目前最常用的OPEs, 被广泛应用于各个行业, 所以在生活垃圾焚烧处理产生的废水中浓度也较高.Q6纺织企业废水中OPEs浓度最低为91.70 ng·L-1, 其中TCPP和TEP为主要单体, 浓度分别为25.26 ng·L-1和24.86 ng·L-1.Q7五金企业废水中∑OPEs浓度为326.12 ng·L-1, 以TEP和TCPP为主.不同行业废水中OPEs污染特征不同, 如珠三角地区地区印刷电路板污水处理厂进水中∑OPEs浓度最高, 分别为2 842 ng·L-1和2 710 ng·L-1, 主要以TnBP、TCPP和TCEP为主; 汽车零配件加工企业浓度相对较低, 以TDCP和TnBP为主; 纸箱生产企业进水中浓度略高, 为1 065 ng·L-1, 主要成分为TCPP、TPhP和TCEP; 乳胶漆企业主要以TPhP、TCPP和TCEP为主[16].即使相同行业在不同地区OPEs排放特征也不同, 如珠三角地区纺织企业只检出TnBP、TPhP和TCPP, 总浓度达361 ng·L-1, 与本文中纺织企业组成略有差异, 这可能与企业生产工艺与污水处理工艺等有关.
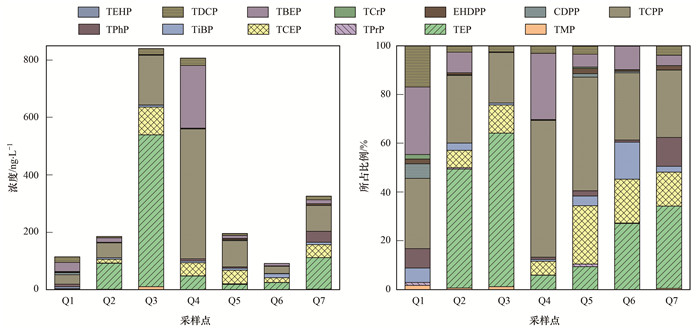
|
图 2 企业废水OPEs浓度水平及组成特征 Fig. 2 Concentration and composition of the OPEs in industrial wastewater |
虽然各企业污水中OPEs浓度和组成各有差异, 但总体来说以氯代OPEs为主, 这是因为氯代OPEs具有较强的稳定性, 被大量应用于电子、纺织、建材和化工等行业中[19].尽管20世纪90年代中期TCEP在西欧国家被禁用, 但本研究的企业废水中仍检出高浓度的TCEP, 可见TCEP在我国仍然被广泛使用.
2.2 污水处理厂中OPEs的污染特征本文分析了丹金溧漕河下游两家集中处理电子企业废水和少量生活污水的污水处理厂进出水中OPEs情况, 浓度水平及组成特征如图 3所示.除TPrP和TEHP检出率为50%外, 其他污染物检出率均为100%.污水处理厂W1进水中∑OPEs的浓度为2 186.96 ng·L-1, 以TCPP、TBEP和TCEP为主; 出水中总浓度为1 859.59 ng·L-1, 主要污染物TCPP、TCEP和TEP浓度分别为907.30、416.48和267.77 ng·L-1.W2进水中∑OPEs的浓度与W1相当, 为2 778.57 ng·L-1, 主要污染物为TCPP、TiBP和TCEP; 出水中∑OPEs的浓度为2 297.37 ng·L-1, 以TCPP、TEP和TCEP为主.两家污水处理厂进出水中OPEs浓度高于周边企业污水中OPEs浓度, 是因为OPEs在生产、使用过程中很容易释放到环境中, 并随着生活污水和工业废水等的排放进入污水处理厂, 因而污水处理厂成为环境中OPEs的“汇”.
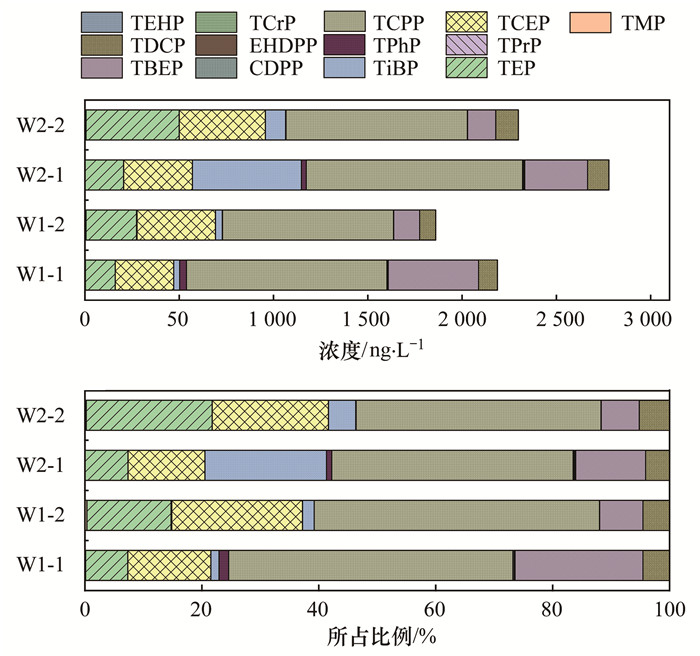
|
图 3 污水处理厂进出水中OPEs浓度水平及组成特征 Fig. 3 Concentration and composition of the OPEs in influents and effluents of the wastewater treatment plant |
与其他污水处理厂相比, 本文中污水处理厂中∑OPEs浓度略高于北京[14](0.5~121.8 ng·L-1)、合肥[20](676.80~1 102.24 ng·L-1)和美国、欧洲、澳洲及亚洲其他国家的生活污水处理厂[19]以及珠三角地区乳胶漆、纺织、汽车零配件、纸箱、黏合剂等企业污水处理厂中OPEs浓度(37.2~1 065 ng·L-1), 与珠三角地区印刷电路板(245~2 842 ng·L-1)污水处理厂中OPEs浓度水平相当[16].这是由于各污水厂所接纳的废水来源、处理水量及处理工艺不同, 导致各污水厂中各种OPEs的浓度和组成存在差异.
W1和W2均采用氧化沟处理方式, 对OPEs的总去除率分别为14.97%和17.32%, 与A/O处理工艺(总去除率为50%)[14]和改良型氧化沟联合紫外处理工艺(总去除率为27.69%)[20]相比去除效果相对较差.W1和W2对烷基OPEs的去除率分别为32.83%和32.24%, 对芳香基OPEs的去除率分别为97.91%和90.83%.而对氯代OPEs去除极其有限, 去除率分别为4.37%和5.40%.可见, 烷基和芳基OPEs经过处理后浓度都有明显地降低, 氯代OPEs没有得到有效地去除, 这与国内外的研究结果一致[10].烷基和芳香基OPEs在微生物作用下可降解, 而芳香基OPEs在自然光下可发生降解, 同时氯代OPEs因为自身位阻效应的影响, 很难发生降解和被传统的污水处理工艺去除, 因此需要开发新的污水处理工艺提高氯代OPEs的去除率.污水处理厂W1和W2对TMP、TEP、TPrP和TCEP均存在负去除的现象, 这可能是因为污水处理设施、管道和污泥中释放该类物质, 可见, 污水处理厂出水可能是地表水环境中OPEs的重要污染“源”.
2.3 地表水中OPEs的污染特征OPEs在地表水中的浓度水平和组成情况如图 4所示, 除TPrP外, 其他所有OPEs均有检出.推断是由于TPrP在该地区使用较少, 这与企业废水和污水处理厂检出情况一致.地表水中∑OPEs的浓度为219.47~689.85 ng·L-1, 平均浓度为499.74 ng·L-1, 与太湖(166~1 530 ng·L-1)、松花江(5~3 700 ng·L-1)、北京城市河流(954~10 945 ng·L-1)以及环渤海河流(9.6~1 549 ng·L-1)[3, 18, 21]等国内水体相比, 浓度水平较低.OPEs在丹金溧漕河和京杭大运河中的浓度水平无明显差异(P>0.05).
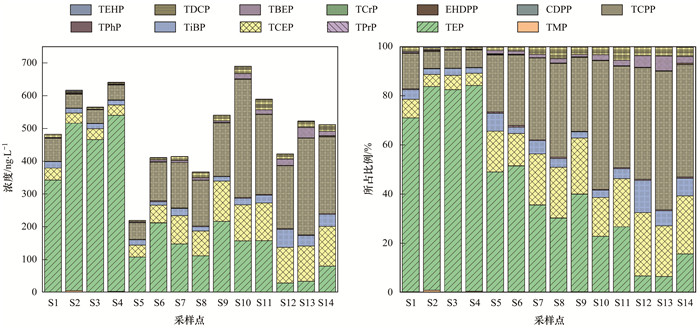
|
图 4 地表水中OPEs浓度水平及组成特征 Fig. 4 Concentration and composition of the OPEs in the surface water |
地表水中OPEs以烷基和氯代OPEs为主, 分别占∑OPEs总浓度的49.92%和49.37%.TEP浓度最高, 为27.63~537.35 ng·L-1, 这与TEP在流域周边的广泛使用有关, 另一方面是由于TEP属于极性和亲水性较强的化合物, lgKow为0.8(表 1), 容易存在于水相中.其次, TCPP、TCEP浓度范围分别为41.14~361.04 ng·L-1和30.72~123.27 ng·L-1.这两种物质是OPEs产品中应用较广泛的化合物, 这主要是因为氯代OPEs具有较强的稳定性而被广泛应用各行业中; 此外, 由于传统的污水处理工艺难以去除氯代OPEs, 导致其在水体中大量存在[16].芳香基OPEs检出浓度均较低, 浓度为1.71~6.37 ng·L-1, 以TPhP为主, 是我国地表水中检出频率最高的OPEs之一[22].
2.4 地表水中OPEs来源解析本研究运用SPSS 20.0对地表水中OPEs浓度进行Spearman相关性分析和主成分分析(principal component analysis, PCA), 因为TPrP的检出率较低(为40%), 故在统计分析时将其剔除, 分析结果如表 4和图 5所示.表 4显示TCPP、TCEP、TBEP和TDCP之间显著相关, 表明具有同源性; TCrP与TEHP之间相关性较强, 说明可能来自同一种源; CDPP、EHDPP与其他OPEs之间均无相关性, 表明它们可能来自不同的其他的源.
|
|
表 4 地表水中OPEs的相关性分析1) Table 4 Correlation analysis among the OPEs in surface water |
|
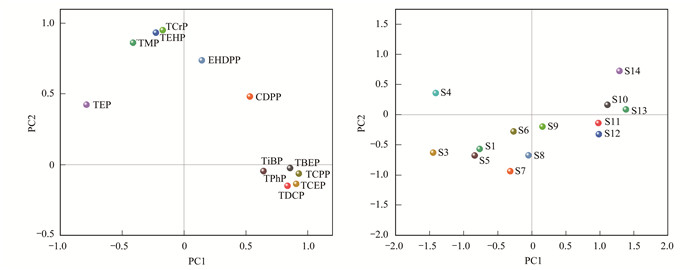
图 5 主成分分析因子载荷与得分图 Fig. 5 Loading and score plot of the PCA |
主成分分析结果显示影响地表水中OPEs分布的主成分有2个, 总贡献率为72.10%, 能够反映检测数据的大部分信息.根据因子载荷矩阵, 可以进行源类识别, 旋转的因子载荷和点位得分见图 5.
PC1的特征值为5.68, 方差贡献率为47.30%, 包括TCPP、TCEP、TBEP和TDCP, 表明这几种污染物可能来自同一种源, 这与相关性分析结果一致.已知这些物质常因其特殊的理化性质被作为阻燃剂广泛应用到塑料制品、纺织品、电子设备以及建筑材料中, 在地表水中浓度相对较高, 因此推测水环境中OPEs的大量存在与这些生产活动有关.如图 5所示, S10~S14在PC1上具有较高的得分, 可见受PC1影响较大.这些点位均位于京杭大运河下游(见图 1), 地处常州市武进区、天宁区, 根据环境统计数据显示, 2018年武进区和天宁区纺织企业废水排放量最大, 142家企业排放废水共计2874万t, 因此推测PC1可能为该区域内纺织类企业生产活动.
PC2的特征值为2.98, 方差贡献率为24.80%, TCrP和TEHP具有较高的载荷, 两者在地表水中的浓度水平很低.TCrP通常作为阻燃剂和润滑剂被广泛应用于机械或车辆液压油和润滑油中, 它们在车辆行驶过程中可通过损耗和渗漏行为释放到路面上, 在道路灰尘、地表径流中有较高的检出率和浓度[23].TEHP多用于聚氯乙烯及涂料等产品中, 在大气环境中有相对较高的检出量和检出率, 而研究区域内企业废水和污水处理厂中并未检出较高浓度的TCrP和TEHP, 可见并无明显的点源, 推测水环境中OPEs可能与废油废气的排放和涂料等建筑材料的释放有关.由于OPEs的理化性质差异和来源广泛, 因而对OPEs的来源的识别有待进一步的研究.
2.5 水体中OPEs生态风险评估采用风险商(risk quotient, RQ)评价OPEs的潜在环境风险, 计算如式(1)和式(2)所示:
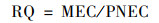
|
(1) |
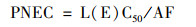
|
(2) |
式中, MEC为污染物环境实测浓度, mg·L-1; PNEC为污染物的预测无效应浓度, mg·L-1; L(E)C50为引起50%的供试生物的某种效应变化的受试物浓度, mg·L-1, 通过文献[24~26]获得; AF为评价因子, 采用欧盟水框架指令的推荐值10~1 000. RQ≥1.00表示风险较高, 0.10≤RQ < 1.00表示为中等风险, RQ < 0.1表示风险较低.
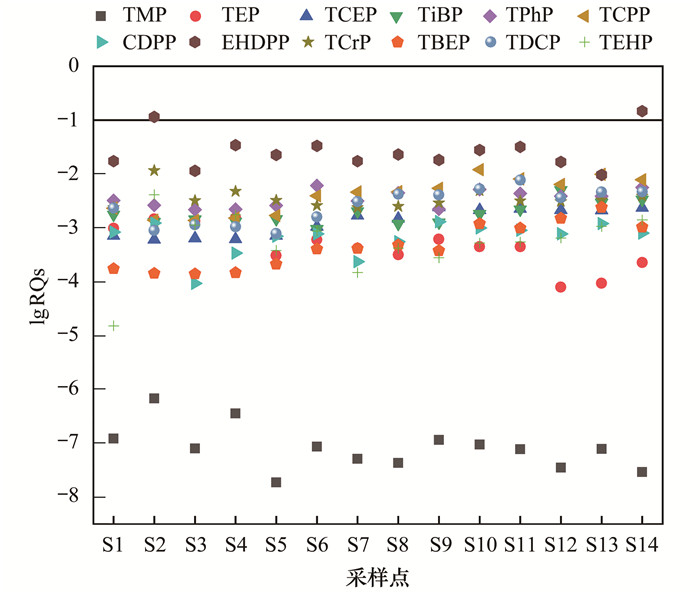
OPEs对不同水生生物(藻类、水蚤和鱼)的急性毒性浓度(LC50)或半数效应浓度(EC50)如表 5所示.从中筛选出最低的急性毒性数据, 利用相应的评价因子推导PNEC值, 计算地表水中OPEs的RQ值.由图 6可以看出, 在大多数样品中OPEs的RQ值小于0.1, 表示对水生生物具有较低的风险.值得注意的是, 尽管EHDPP在水环境中的检出浓度较低, 但因为水生生物对其较为敏感, 在部分点位(S2和S14)处EHDPP呈现中等风险.
|
|
表 5 有机磷酸酯的半数效应浓度L(E)C50和PNECs值1) Table 5 Half effect concentration L(E)C50 and PNEC values of OPEs |
|
图 6 地表水中OPEs的风险商值 Fig. 6 RQs of the OPEs in the surface water |
由于目前关于OPEs对水生态环境效应的报道多集中在水生生物的急性毒性, 缺乏对低剂量长期暴露下的生物毒性效应研究[27].且尽管有部分OPEs对水生生物慢性效应的研究, 却没有基于慢性毒性推导PNEC值的报道, 本文中基于评价因子推导的PNEC值具有不确定性, 不能为水生生物提供充足的保护.因此, OPEs对水生生物的长期慢性毒性效应有待于进一步研究.
3 结论(1) 太湖流域重点地区企业废水、污水处理厂进出水以及地表水中均检出OPEs, 污水处理厂进出水中13种OPEs总浓度高于企业废水和地表水.不同水体中OPEs浓度水平各有差异, 但从组成上看主要以氯代OPEs为主.
(2) 相关性分析判定TCPP、TCEP、TBEP和TDCP之间显著相关, 同源性较强; TCrP和TEHP可能来自同一种源.主成分分析方法识别地表水中OPEs的来源可能有纺织企业废水排放、废油废气的排放以及建筑材料的释放等.
(3) 风险评估结果显示多数地表水中OPEs对水生生物具有较低的风险, 但部分点位处EHDPP呈现中等风险.考虑到OPEs对水生生物具有慢性毒性, 长期暴露对水生生物的潜在影响值得关注.
(4) 目前关于水环境受体中OPEs来源的研究较少, 有必要尽快开展不同源类的标识组分识别工作并建立详细的源成分谱数据库, 利用大数据和相关模型建立OPEs源解析方法, 更加科学地判定各污染源的贡献率, 这对水环境中OPEs的污染控制和预防具有重要意义.
| [1] | Su G Y, Letcher R J, Yu H X. Organophosphate flame retardants and plasticizers in aqueous solution: pH-dependent hydrolysis, kinetics, and pathways[J]. Environmental Science & Technology, 2016, 50(15): 8103-8111. |
| [2] | HIS Markit. Flame retardants[EB/OL]. https://ihsmarkit.com/products/chemical-flame-retardants-scup.html, 2020-06-30. |
| [3] | Wang X L, Zhu L Y, Zhong W J, et al. Partition and source identification of organophosphate esters in the water and sediment of Taihu Lake, China[J]. Journal of Hazardous Materials, 2018, 360: 43-50. DOI:10.1016/j.jhazmat.2018.07.082 |
| [4] | Xing L Q, Zhang Q, Sun X, et al. Occurrence, distribution and risk assessment of organophosphate esters in surface water and sediment from a shallow freshwater Lake, China[J]. Science of the Total Environment, 2018, 636: 632-640. DOI:10.1016/j.scitotenv.2018.04.320 |
| [5] | Castro-Jiménez J, González-Gaya B, Pizarro M, et al. Organophosphate ester flame retardants and plasticizers in the global oceanic atmosphere[J]. Environmental Science & Technology, 2016, 50(23): 12831-12839. |
| [6] | Kurt-Karakus P, Alegria H, Birgul A, et al. Organophosphate ester (OPEs) flame retardants and plasticizers in air and soil from a highly industrialized city in Turkey[J]. Science of the Total Environment, 2018, 625: 555-565. DOI:10.1016/j.scitotenv.2017.12.307 |
| [7] | Hou R, Xu Y P, Wang Z J. Review of OPFRs in animals and humans: Absorption, bioaccumulation, metabolism, and internal exposure research[J]. Chemosphere, 2016, 153: 78-90. DOI:10.1016/j.chemosphere.2016.03.003 |
| [8] | Van den Eede N, Erratico C, Exarchou V, et al. In vitro biotransformation of tris(2-butoxyethyl) phosphate (TBOEP) in human liver and serum[J]. Toxicology and Applied Pharmacology, 2015, 284(2): 246-253. DOI:10.1016/j.taap.2015.01.021 |
| [9] | Zhao F R, Wan Y, Zhao H Q, et al. Levels of blood organophosphorus flame retardants and association with changes in human sphingolipid homeostasis[J]. Environmental Science & Technology, 2016, 50(16): 8896-8903. |
| [10] | Marklund A, Andersson B, Haglund P. Organophosphorus flame retardants and plasticizers in Swedish sewage treatment plants[J]. Environmental Science & Technology, 2005, 39(19): 7423-7429. |
| [11] | Loos R, Carvalho R, Comero S, et al. EU wide monitoring survey on waste water treatment plant effluents[R]. EU: European Commission, Joint Research Centre, Institute for Environment and Sustainability, 2012. |
| [12] | O'Brien J W, Thai P K, Brandsma S H, et al. Wastewater analysis of Census day samples to investigate per capita input of organophosphorus flame retardants and plasticizers into wastewater[J]. Chemosphere, 2015, 138: 328-334. DOI:10.1016/j.chemosphere.2015.06.014 |
| [13] | Hao C Y, Helm P A, Morse D, et al. Liquid chromatography-tandem mass spectrometry direct injection analysis of organophosphorus flame retardants in Ontario surface water and wastewater effluent[J]. Chemosphere, 2018, 191: 288-295. DOI:10.1016/j.chemosphere.2017.10.060 |
| [14] |
张振飞, 吕佳佩, 裴莹莹, 等. 北京某污水处理厂及受纳水体中典型有机磷酸酯的污染特征和风险评估[J]. 环境科学, 2020, 41(3): 1368-1376. Zhang Z F, Lü J P, Pei Y Y, et al. Pollution characteristics and risk assessment of typical organophosphate esters in Beijing municipal wastewater treatment plant and the receiving water[J]. Environmental Science, 2020, 41(3): 1368-1376. |
| [15] | Cristale J, Katsoyiannis A, Sweetman A J, et al. Occurrence and risk assessment of organophosphorus and brominated flame retardants in the River Aire (UK)[J]. Environmental Pollution, 2013, 179: 194-200. DOI:10.1016/j.envpol.2013.04.001 |
| [16] | Xu L, Hu Q P, Liu J, et al. Occurrence of organophosphate esters and their diesters degradation products in industrial wastewater treatment plants in China: Implication for the usage and potential degradation during production processing[J]. Environmental Pollution, 2019, 250: 559-566. DOI:10.1016/j.envpol.2019.04.058 |
| [17] | 唐国平, 陈德超, 周涛, 等. 丹金溧漕河(溧阳段)水质特征分析[J]. 农村经济与科技, 2016, 37(6): 1-2. |
| [18] |
高立红.北京市城市环境有机磷酸酯污染水平和分布特征研究[D].北京: 北京科技大学, 2016. Gao L H. Occurrence and distribution of organophosphate esters in the urban area of Beijing[D]. Beijing: University of Science and Technology Beijing, 2016. |
| [19] | Wei G L, Li D Q, Zhuo M N, et al. Organophosphorus flame retardants and plasticizers: Sources, occurrence, toxicity and human exposure[J]. Environmental Pollution, 2015, 196: 29-46. DOI:10.1016/j.envpol.2014.09.012 |
| [20] |
赵赛, 刘世龙, 张华, 等. 污水处理工艺对有机磷酸酯的去除效果[J]. 中国给水排水, 2018, 34(5): 88-91. Zhao S, Liu S L, Zhang H, et al. Removal efficiency of organophosphate esters in wastewater treatment processes[J]. China Water & Wastewater, 2018, 34(5): 88-91. |
| [21] | Wang R M, Tang J H, Xie Z Y, et al. Occurrence and spatial distribution of organophosphate ester flame retardants and plasticizers in 40 rivers draining into the Bohai Sea, North China[J]. Environmental Pollution, 2015, 198: 172-178. DOI:10.1016/j.envpol.2014.12.037 |
| [22] | Yuan S L, Li H, Dang Y, et al. Effects of triphenyl phosphate on growth, reproduction and transcription of genes of Daphnia magna[J]. Aquatic Toxicology, 2018, 195: 58-66. DOI:10.1016/j.aquatox.2017.12.009 |
| [23] | Shi Y L, Gao L H, Li W H, et al. Occurrence, distribution and seasonal variation of organophosphate flame retardants and plasticizers in urban surface water in Beijing, China[J]. Environmental Pollution, 2016, 209: 1-10. DOI:10.1016/j.envpol.2015.11.008 |
| [24] | Verbruggen E M J, Rila J P, Traas T P, et al. Environmental risk limits for several phosphate esters, with possible application as flame retardant[R]. RIVM Report 601501024, 2005. |
| [25] | Wong P T S, Chau Y K. Structure-toxicity of triaryl phosphates in freshwater algae[J]. Science of the Total Environment, 1984, 32(2): 157-165. DOI:10.1016/0048-9697(84)90128-1 |
| [26] | Hanna P J. Effects on spermatogenesis in the guppy Poecilia reticulata by prolonged exposure to trimethylphosphate[J]. Bulletin of Environmental Contamination and Toxicology, 1982, 28(1): 28-32. |
| [27] | Cristale J, García Vázquez A, Barata C, et al. Priority and emerging flame retardants in rivers: Occurrence in water and sediment, Daphnia magna toxicity and risk assessment[J]. Environment International, 2013, 59: 232-243. DOI:10.1016/j.envint.2013.06.011 |
 2020, Vol. 41
2020, Vol. 41


