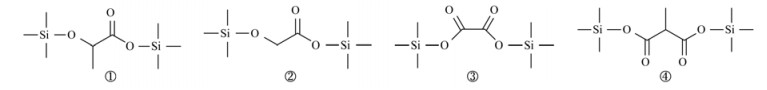2. 常州市排水管理处, 常州 213016
2. Office of Drainage Management, Changzhou 213016, China
人工甜味剂(artificial sweeteners, Ass)是一类人工合成或半合成物质, 作为蔗糖替代品而广泛用于食品、饮料、个人护理、药物及动物饲料中.其中三氯蔗糖(sucralose, SUC)是一种氯原子选择性取代蔗糖分子中3个羟基而生成的氯化碳水化合物, 由于结构与蔗糖相似, 甜度高于蔗糖600~800倍, 成为广泛应用的商业甜味剂[1, 2].三氯蔗糖化学性质稳定, 常规废水处理工艺(如生物降解、絮凝和紫外消毒)对其去除效果有限[3, 4].由于其广泛存在性和显著持久性, 三氯蔗糖被美国环境保护局(USEPA)列为一种新兴污染物(emerging contaminant, EC)[5].Wiklund等[6]的研究发现, 三氯蔗糖会明显抑制大型蚤的运动速度与摄取食物等行为, 此外三氯蔗糖还会通过改变肠道菌群来诱导对葡萄糖的不良耐受性[7].据报道, 全球每年大概有10 000 t三氯蔗糖进入水环境中[8].随着三氯蔗糖不断进入水体, 并在水环境中产生浓度积累效应, 可能对生态系统和人类健康构成潜在威胁[9, 10].因此三氯蔗糖所带来的环境问题不容忽视.
高级氧化工艺(advanced oxidation processes, AOPs)是一类能有效去除水中难生物降解污染物的水处理技术.其中基于硫酸根自由基(SO4-·)的活化过硫酸盐(persulfate, PS)高级氧化工艺备受关注.由于SO4-·半衰期较长, 可与有机污染物充分接触, 与基于羟基自由基(·OH)的传统氧化方法相比, 活化过硫酸盐(UV/PS)氧化能力更为显著[11, 12], 可有效去除水中卡磺胺甲唑[13]、苯胺[14]和双氯芬酸[15]等污染物.
本研究以典型人工甜味剂SUC为目标污染物, 建立UV/PS降解SUC的动力学模型, 考察UV光强、PS投加量、溶液初始pH值及阴离子等因素对SUC降解效果的影响, 解析降解过程中产生的中间产物, 并评估其生态风险, 以期为UV/PS去除含SUC废水或环境水体提供理论依据和技术支持.
1 材料与方法 1.1 实验试剂SUC购于Aladdin公司(中国), 甲醇(HPLC级)购于Sigma公司(美国), 衍生剂BSTFA/TMCS(99:1)购于Aladdin公司(中国), CH2Cl2购于永华化学科技(江苏)公司, 其他试剂Na2S2O8、HCl、NaOH、Na2HPO4·12H2 O、KH2PO4、Na2SO3、NaHCO3、NaCl、NaNO3、Na2SO4均为分析纯, 购自上海国药集团.本实验用水均为超纯水(电阻率18.3 MΩ·cm).
1.2 实验装置降解过程在光反应装置中进行.波长254 nm低压汞灯(Philips, 上海)悬挂于50 mL玻璃反应皿上方, 采用磁力搅拌器(HJ-6, 江苏金怡)确保反应体系均匀, 通过改变反应皿与汞灯的距离来调节UV强度, 采用紫外辐射计(UV-B, 北师大光电仪器厂)来测定UV光强.
1.3 实验方法与过程取一定体积SUC(0.01 mmol·L-1)溶液于反应皿中, 使用磷酸盐缓冲溶液(0.20 mol·L-1)、稀盐酸(0.10 mol·L-1)或氢氧化钠(0.10 mol·L-1)调节溶液pH值, 加入一定体积的PS(0.10 mol·L-1).打开UV汞灯, 开始降解反应.每隔一段时间取样, 加入Na2SO3(5 g·L-1)淬灭降解反应.采用HPLC-MS/MS测定剩余SUC浓度.所有条件下的反应均重复3次, 取平均值.
1.4 SUC及其中间产物分析使用HPLC-MS/MS(Thermo TSQ quantum Access Max)测定SUC浓度, 色谱条件:Thermo Accucore C18色谱柱(3 mm×50 mm, 2.6 μm); 流动相为水和甲醇, 梯度洗脱; 流速0.2 mL·min-1, 柱温25℃.质谱条件:SRM, 负离子扫描, 子母离子对m/z:394.8/394.0, 碎裂电压10 eV.
根据美国EPA1694标准方法[16], 采用全自动固相萃取仪SPE(432-EVA32)对SUC降解液进行固相萃取.随后采用高分辨率液相质谱HRMS Orbitrap(Q-E Plus)对SUC降解中间产物进行定性分析, 色谱条件为:Waters HSS T3色谱柱(2.1 mm×50 mm, 1.7 μm); 流动相为甲醇和水.正负离子同时扫描.离子源参数:鞘气流速12 mL·min-1, 毛细管温度32℃, 喷雾电压4 kV, S透镜射频能级50.其他MS条件包括:扫描范围70~600 m/z, 动态排除5 s, HCD碰撞能量值(CE%)35, 质量分辨率为70 000.数据分析采用Xcalibur 4.1软件.
使用GC-MS(Thermo Trace ISQLT)鉴定SUC降解末期生成的小分子有机酸.降解液经旋转蒸发器(XD-5000ADQ上海贤德)蒸干后, 以CH2Cl2为萃取剂, BSTFA/TMCS(99:1)为硅烷化试剂, 70℃下硅烷化衍生60 min.GC-MS进样分析条件为:Thermo TG-624色谱柱(30 m×0.25 mm×1.4 μm); 载气流量1.0 mL·min-1, 进样体积1 μL, 进样口温度280℃, 无分流进样; 升温程序:50℃保持3 min, 50~150℃(20℃·min-1)保持0 min, 150~280℃(10℃·min-1)保持3 min.采用全扫模式, 范围50~500 m/z.
1.5 生态毒性风险评价选用海洋发光细菌——费氏弧菌(Vibrio fischeri)作为指示细菌测定UV/PS降解SUC过程中反应液的毒性变化.采用生物毒性检测仪(ATD-P1, 北京金达清创)测定发光细菌的发光强度, 通过水样对发光细菌的相对抑制率来反映毒性的强弱.每个样品测定3次作为平行数据, 并在前后设置两组空白对照, 发光细菌的相对抑制率(I)见式(1).

|
(1) |
式中, Lt为样品发光强度, L0为阴性对照发光强度.
2 结果与讨论 2.1 单一UV、单一PS及UV/PS反应条件比较在UV光强0.8 mW·cm-2, PS浓度1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1, 溶液pH值为7.0的实验条件下, 分别考察了SUC在单一UV、单一PS及UV/PS反应条件下的降解情况, 并用准一级动力学方程拟合实验数据[式(2)、式(3)], 结果见图 1.
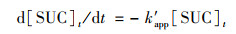
|
(2) |
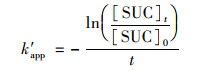
|
(3) |

|
图 1 单一UV、单一PS和UV/PS对SUC降解的影响 Fig. 1 Effect of single UV photolysis, single PS, and UV/PS on SUC degradation |
式中, [SUC]t表示t时刻该反应体系中SUC的浓度, mmol·L-1; [SUC]0表示SUC初始浓度, mmol·L-1; k′ app为一级动力学速率常数, min-1.
图 1表明, SUC在单一UV和单一PS两种反应条件下15 min时降解率仅为7.2%和3.3%, 基本没有去除.而在UV/PS反应条件下降解率可达98.6%, 与单一UV和单一PS两种反应条件相比, SUC在UV/PS反应条件下的降解率有显著提高.数据拟合结果表明, SUC在3种反应条件下的降解反应均符合准一级反应动力学, 反应速率常数分别为0.005 1、0.002 6和0.285 6 min-1. UV和PS的结合, 明显提升了SUC降解效果.
|
(4) |

|
(5) |
水溶液中Na2S2O8在紫外线UV激发下, S2O82-离子会生成SO4-·和·OH[17] [式(4)、式(5)], 而SO4-·具有较高的氧化能力, 可快速氧化有机污染物[18].因此UV和PS协同作用加速了SUC的降解.
2.2 UV光强对SUC降解反应的影响在PS浓度为1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1, 溶液pH值为7的条件下, 考察不同光强对SUC降解反应的影响, 结果见图 2.
|
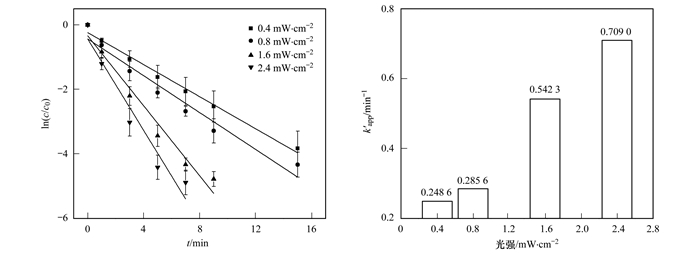
图 2 UV光强对UV/PS降解SUC的影响 Fig. 2 Effect of UV intensity on SUC degradation using UV/PS |
由图 2可知, 随着光强增加, 反应速率常数逐渐增加, SUC降解效果显著.当光强从0.4 mW·cm-2增大到2.4 mW·cm-2时, 反应速率常数由0.248 6 min-1上升至0.709 0 min-1.由于光强大小会影响SO4-·的生成, 因此随着光强的增加, 产生的SO4-·增多. PS初始浓度保持不变, 增大UV光强, 单位时间内产生的SO4-·增多, 从而加快SUC的降解速率.
2.3 PS浓度对SUC降解反应的影响PS浓度是影响有机物降解效率的主要因素之一.在UV光强0.8 mW·cm-2, SUC初始浓度0.01 mmol·L-1, 溶液初始pH值为7的实验条件下, 考察不同PS浓度对SUC降解反应的影响, 结果见图 3.
|
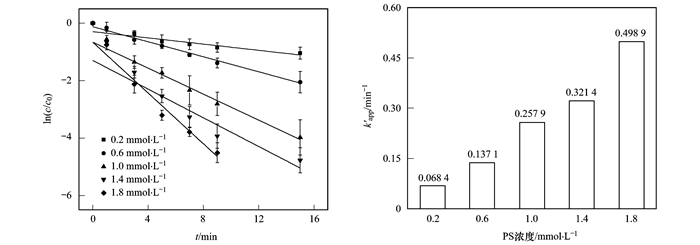
图 3 PS浓度对UV/PS降解SUC的影响 Fig. 3 Effect of PS doses on SUC degradation using UV/PS |
由图 3可知, 当氧化剂PS浓度从0.2 mmol·L-1增加到1.8 mmol·L-1时, 反应速率常数由0.068 4 min-1上升至0.498 9 min-1, 结果表明SUC降解速率随氧化剂PS浓度的增加而提高.这是因为在SUC初始浓度一定时, 增加PS的浓度会产生更多SO4-·, 从而有效促进SUC的降解反应.有研究表明[19]过量浓度的PS会和生成的SO4-·进一步反应, 导致SO4-·浓度下降, 从而抑制目标污染物的降解.本研究中PS浓度为0.2~1.8 mmol·L-1, 尚未观察到抑制SUC降解现象.
2.4 溶液初始pH值对SUC降解反应的影响在UV光强0.8 mW·cm-2, PS浓度为1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1的条件下, 考察了不同溶液初始pH值对SUC降解反应的影响, 结果见图 4.
|
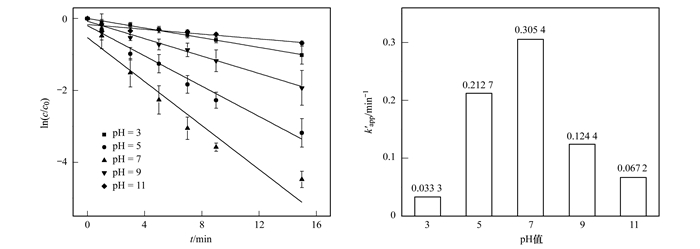
图 4 溶液初始pH值对UV/PS降解SUC反应的影响 Fig. 4 Effect of pH value on SUC degradation using UV/PS |
由图 4可知, 在溶液初始pH值为3、5、7、9和11时对应的反应速率常数分别为0.033 3、0.212 7、0.305 4、0.124 4和0.067 2 min-1, 在酸性和碱性条件下SUC降解速率常数明显下降, 中性条件下SUC降解速率常数达到最大.酸性条件下, 溶液中H+与SO4-·反应会生成活性较弱的HSO4·和HSO4-[式(6)~(8)], 而HSO4·和HSO4-会同SO4-·争夺SUC, 抑制SUC的降解[20].碱性条件下, 溶液中部分SO4-·会与OH-反应生成·OH[21] [式(9)], 当溶液pH值由9上升至11时, 溶液中·OH不断增加, SO4-·减少, 由于·OH的氧化还原电位(1.8~2.4 V)低于SO4-·的氧化还原电位(2.5~3.1 V), 因此碱性条件下反应速率会明显降低[22].

|
(6) |
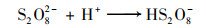
|
(7) |
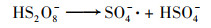
|
(8) |

|
(9) |
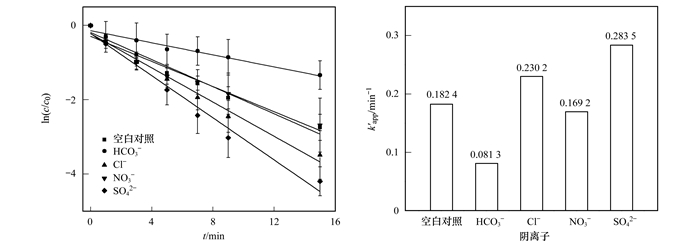
环境水体中广泛存在大量阴离子, 为考察常见阴离子对UV/PS降解SUC的影响, 在UV光强0.8 mW·cm-2, PS浓度为1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1的条件下, 考察HCO3-、Cl-、NO3-和SO42-这4种阴离子对SUC降解的影响.阴离子浓度均为10 mmol·L-1, 结果见图 5所示.
|
图 5 阴离子对UV/PS降解SUC反应的影响 Fig. 5 Effect of different anions on SUC degradation using UV/PS |
从图 5可知, 未投加阴离子时, UV/PS降解SUC的反应速率常数为0.182 4 min-1, 投加阴离子HCO3-、Cl-、NO3-和SO42-后的反应速率常数分别为0.081 3、0.230 2、0.169 2和0.283 5 min-1.结果表明, HCO3-、NO3-对SUC的降解反应有一定抑制作用, Cl-、SO42-对SUC的降解反应有一定促进作用, 其中HCO3-和SO42-对SUC降解反应的影响较显著.由于部分SO4-·会与Cl-反应生成Cl·、Cl2-·、Cl2、HOCl和ClHO-·等活性氯成分, 其中Cl·具有强氧化性, 在SO4-·与主要活性氯成分Cl·、Cl2和HOCl的双重作用下, 加速了SUC的降解[23, 24].研究表明[25, 26]NO3-在光强激发作用下会产生NO2-、O2、NO2·、和O-·, 其中NO3-、NO2-会迅速与SO4-·发生反应生成NO3·、NO2·, 消耗了反应体系内的SO4-·, 从而导致SUC降解效率的降低.
2.5.1 HCO3-浓度对降解SUC的影响碳酸氢根离子(HCO3-)是一种广泛存在于环境水体中的阴离子, 因此考察HCO3-对UV/PS降解SUC的影响具有重大意义.在UV光强0.8 mW·cm-2, PS浓度1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1的条件下, 考察在不同HCO3-浓度条件下SUC的降解情况, 结果见图 6.

|
图 6 HCO3-浓度对UV/PS降解SUC反应的影响 Fig. 6 Effect of HCO3- on SUC degradation using UV/PS |
由图 6可知, 随着HCO3-浓度的增加, SUC的降解速率逐渐降低.当HCO3-浓度从0上升至14 mmol·L-1时, 反应速率常数从0.173 9 min-1下降至0.050 7 min-1, 表明随着HCO3-浓度的增加, HCO3-对UV/PS降解SUC有明显抑制作用.体系中的HCO3-以及电离产生的CO32-均会与SO4-·反应产生SO42-, 消耗体系内的SO4-·浓度, 从而抑制SUC的降解[27, 28] [式(10)~(12)].

|
(10) |

|
(11) |

|
(12) |
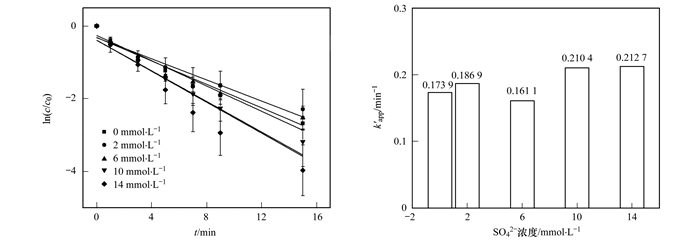
鉴于上述实验中背景离子SO42-对SUC的降解有一定影响, 因此在UV光强0.8 mW·cm-2, PS浓度1.0 mmol·L-1, SUC初始浓度0.01 mmol·L-1的中性实验条件下, 进一步考察在不同SO42-浓度下SUC的降解情况, 结果见图 7.
|
图 7 SO42-浓度对UV/PS降解SUC反应的影响 Fig. 7 Effect of SO42- on SUC degradation using UV/PS |
由图 7可知, 当SO42-浓度从0上升至14 mmol·L-1时, 反应速率常数由0.173 9 min-1上升至0.212 7 min-1, 表明随着SO42-浓度的增加, 对UV/PS降解SUC起到一定的促进作用.研究表明[29] SO42-与SO4-·反应会生成S2O82-和具有强还原性的水合电子eaq-(还原电位为-2.9 V), 而eaq-会与污染物快速反应从而加快SUC的降解[式(13)].

|
(13) |
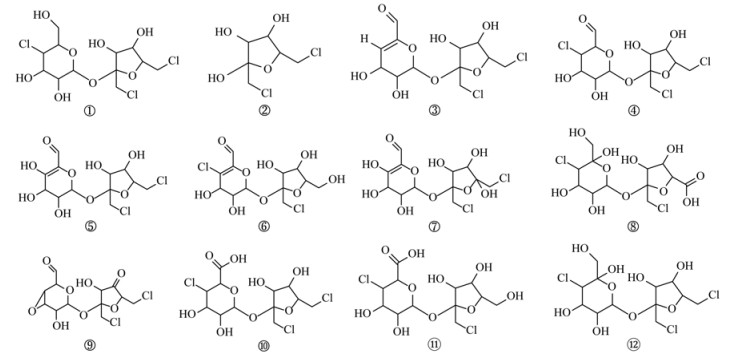
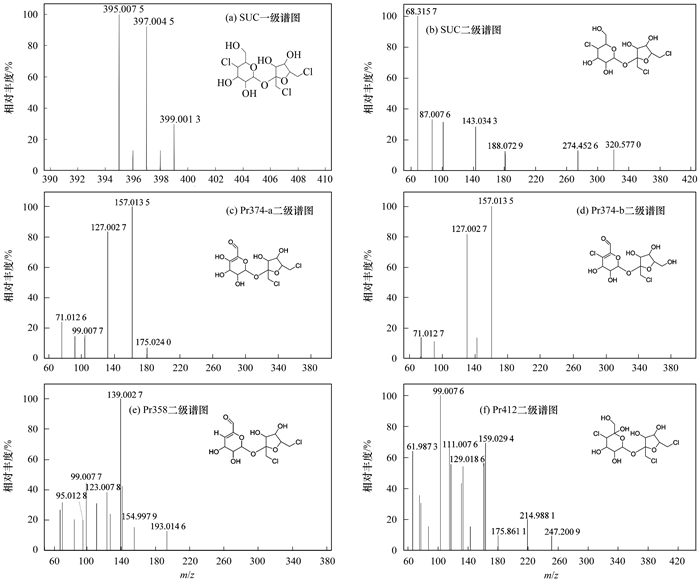
使用HRMS、GC-MS进行质谱分析, 解析出16种SUC降解中间产物(HRMS检测出12种, GC-MS检测出4种), 结果见图 8、表 1及表 2. SUC受氯同位素影响有3个分子离子峰, 质荷比m/z分别是395.007 5、397.004 5和399.001 3[图 8(a)], 二级谱图中存在m/z 68.315 7、87.007 6和143.034 3等3个主要碎片离子[图 8(b)].
|
图 8 SUC和部分降解产物质谱图 Fig. 8 Mass spectrum of SUC and several products |
|
|
表 1 HRMS检测下SUC及中间产物质谱参数1) Table 1 Mass spectroscopy paramaters of SUC and its intermediates detected using HRMS |
|
|
表 2 GC-MS检测下SUC中间产物质谱参数 Table 2 Mass spectroscopy paramaters of SUC intermediates detected using GC-MS |
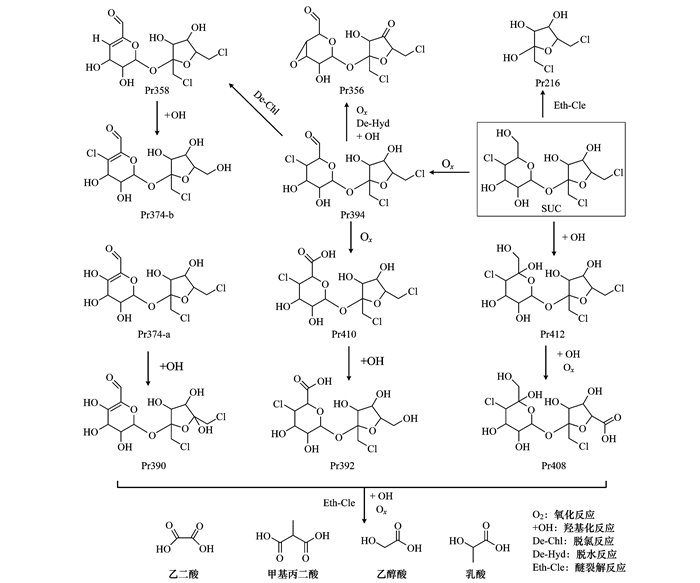
基于SUC与产物结构探索反应路径.在降解过程中, 主要发生羟基化、氧化和醚裂解等反应.在UV照射和SO4-·的联合作用下, ·OH诱导SUC经羟基化反应生成Pr412[图 8(f)], Pr412经羟基化和氧化反应后生成Pr408[30].SUC经醚裂解反应可直接生成Pr216. SUC六元环上的醇羟基被氧化成醛结构产物Pr394, Pr394经羟基化、脱水和氧化等反应生成Pr356[31], 经氧化反应生成Pr410.此外, Pr394经脱氯反应脱去六元环上的HCl生成Pr358[图 8(e)][32], 继而Pr358经羟基化反应生成同分异构体Pr374-a[图 8(c)]和Pr374-b[图 8(d)][33].Pr394-a和Pr410分别经羟基化反应后生成羟基化产物Pr390和Pr392.随后以上产物进一步发生醚裂解、羟基化和氧化反应生成产物乳酸、乙醇酸、甲基丙二酸和乙二酸等小分子有机酸(表 2).基于以上分析, 提出SUC可能的降解反应路径, 见图 9.
|
图 9 SUC在UV/PS降解过程中的反应路径 Fig. 9 Proposed degradation mechanism of SUC degradation using UV/PS |
在SUC初始浓度0.01 mmol·L-1, UV光强0.8 mW·cm-2, PS投加量为1.0 mmol·L-1, 溶液初始pH值为7的条件下进行降解反应.利用费氏弧菌的发光强度来指示反应液的急性毒性, 毒性强弱通过抑制率体现, 结果见图 10.降解反应进行前, 溶液对发光细菌的相对抑制率为17.3%, 随着降解进行, 抑制率显著提升.降解15 min时, SUC基本完全降解, 去除率为98.4%, 此时抑制率高达73.4%, 降解45 min时, 抑制率逐渐下降至46.1%.反应前期相对抑制率并未随SUC的降解而逐步降低.至反应中后期, SUC去除率近100%, 相对抑制率略有降低但仍高达46.1%.在降解反应过程中SUC的去除并不代表着降解液毒性效应的降低, 表明UV/PS降解SUC过程中产生了毒性高于SUC毒性的中间产物.

|
图 10 UV/PS降解SUC过程中对发光细菌的发光抑制率 Fig. 10 Inhibition rate of SUC degradation using UV/PS on luminescent bacteria |
使用ECOSAR软件, 预测SUC及其中间产物对鱼类、水蚤和绿藻的生态环境风险, 结果见表 3, SUC的EC50(绿藻96 h)为44 337 mg·L-1, 而中间产物Pr216、Pr356和Pr410的EC50分别为7 382.2、162.1和29 947.9 mg·L-1, 均明显低于母物质SUC.此外LC50(鱼96 h)和LC50(水蚤48 h)这两个指标均表现出相似的分布特征.这说明SUC在降解过程中产生了具有更高生态风险的中间产物, 与发光细菌急性毒性实验所得结论相符.因此活化过硫酸盐降解三氯蔗糖过程中毒性中间产物及其生态风险仍需进一步深入研究, 以保证水质安全.
|
|
表 3 利用ECOSAR预测SUC及其中间产物的急性毒性/mg·L-1 Table 3 Estimated acute toxicity of SUC and its intermediates using ECOSAR software/mg·L-1 |
4 结论
(1) UV/PS体系可高效去除SUC, 降解过程符合准一级反应动力学.
(2) SUC降解速率常数随着UV光强、PS投加量增大而增大, 在中性条件下降解效果最好.阴离子HCO3-和NO3-有一定抑制作用, 而SO42-和Cl-促进降解过程, 其中HCO3-的抑制作用和SO42-的促进作用较明显.
(3) 通过HRMS和GC-MS共解析出16种中间产物, 在UV/PS降解SUC过程中主要涉及羟基化、氧化和醚裂解等反应.
(4) 发光细菌毒性实验和ECOSAR预测结果表明, UV/PS降解SUC过程中会产生急性毒性高于母物质的中间产物, 对生态环境存在潜在威胁.
| [1] | Sharma V K, Oturan M, Kim H. Oxidation of artificial sweetener sucralose by advanced oxidation processes:a review[J]. Environmental Science and Pollution Research, 2014, 21(14): 8525-8533. DOI:10.1007/s11356-014-2786-y |
| [2] |
马晓雁, 余齐, 黄富, 等. 水环境中新兴污染物三氯蔗糖的研究进展[J]. 环境科学研究, 2018, 31(9): 1495-1503. Ma X Y, Yu Q, Huang F, et al. Research advances on the emerging contaminants sucralose in aqueous system[J]. Research of Environmental Sciences, 2018, 31(9): 1495-1503. |
| [3] | Scheurer M, Storck F R, Brauch H J, et al. Performance of conventional multi-barrier drinking water treatment plants for the removal of four artificial sweeteners[J]. Water Research, 2010, 44(12): 3573-3584. DOI:10.1016/j.watres.2010.04.005 |
| [4] | Keen O S, Linden K G. Re-engineering an artificial sweetener:transforming sucralose residuals in water via advanced oxidation[J]. Environmental Science & Technology, 2013, 47(13): 6799-6805. |
| [5] | Richardson S D, Ternes T A. Water analysis:emerging contaminants and current issues[J]. Analytical Chemistry, 2011, 83(12): 4614-4648. DOI:10.1021/ac200915r |
| [6] | Wiklund A K, Breitholtz M, Bengtsson B E, et al. Sucralose-An ecotoxicological challenger?[J]. Chemosphere, 2012, 86(1): 50-55. DOI:10.1016/j.chemosphere.2011.08.049 |
| [7] | Suez J, Korem T, Zeevi D, et al. Artificial sweeteners induce glucose intolerance by altering the gut microbiota[J]. Nature, 2014, 514(7521): 181-186. DOI:10.1038/nature13793 |
| [8] | Toth J E, Rickman K A, Venter A R, et al. Reaction kinetics and efficiencies for the hydroxyl and sulfate radical based oxidation of artificial sweeteners in water[J]. The Journal of Physical Chemistry A, 2012, 116(40): 9819-9824. DOI:10.1021/jp3047246 |
| [9] | Lillicrap A, Langford K, Tollefsen K E. Bioconcentration of the intense sweetener sucralose in a multitrophic battery of aquatic organisms[J]. Environmental Toxicology and Chemistry, 2011, 30(3): 673-681. DOI:10.1002/etc.433 |
| [10] | Luo J Y, Zhang Q, Cao M, et al. Ecotoxicity and environmental fates of newly recognized contaminants-artificial sweeteners:A review[J]. Science of the Total Environment, 2019, 653: 1149-1160. DOI:10.1016/j.scitotenv.2018.10.445 |
| [11] | Shukla P, Wang S B, Singh K, et al. Cobalt exchanged zeolites for heterogeneous catalytic oxidation of phenol in the presence of peroxymonosulphate[J]. Applied Catalysis B:Environmental, 2010, 99(1-2): 163-169. DOI:10.1016/j.apcatb.2010.06.013 |
| [12] | Wang J L, Wang S Z. Activation of persulfate (PS) and peroxymonosulfate (PMS) and application for the degradation of emerging contaminants[J]. Chemical Engineering Journal, 2018, 334: 1502-1517. DOI:10.1016/j.cej.2017.11.059 |
| [13] | Zhang Y Y, Li L Y, Pan Z H, et al. Degradation of sulfamethoxazole by UV/persulfate in different water samples:influential factors, transformation products and toxicity[J]. Chemical Engineering Journal, 2020, 379: 122354. DOI:10.1016/j.cej.2019.122354 |
| [14] |
韩东晖, 李瑛, 李开明, 等. UV强化草酸络合Fe3+活化过硫酸盐氧化降解苯胺[J]. 环境科学, 2018, 39(9): 4257-4264. Han D H, Li Y, Li K M, et al. Enhanced degradation of aniline by PS oxidation in the presence of UV and ferric oxalate[J]. Environmental Science, 2018, 39(9): 4257-4264. |
| [15] | Fu Y Y, Gao X S, Geng J J, et al. Degradation of three nonsteroidal anti-inflammatory drugs by UV/persulfate:degradation mechanisms, efficiency in effluents disposal[J]. Chemical Engineering Journal, 2019, 356: 1032-1041. DOI:10.1016/j.cej.2018.08.013 |
| [16] | Sapozhnikova Y, Hedgespeth M, Wirth E, et al. Analysis of selected natural and synthetic hormones by LC-MS-MS using the US EPA method 1694[J]. Analytical Methods, 2011, 3(5): 1079-1086. DOI:10.1039/c0ay00748j |
| [17] | Acero J L, Benítez F J, Real F J, et al. Degradation of selected emerging contaminants by UV-activated persulfate:Kinetics and influence of matrix constituents[J]. Separation and Purification Technology, 2018, 201: 41-50. DOI:10.1016/j.seppur.2018.02.055 |
| [18] | Brienza M, Katsoyiannis I A. Sulfate radical technologies as tertiary treatment for the removal of emerging contaminants from wastewater[J]. Sustainability, 2017, 9(9): 1604. DOI:10.3390/su9091604 |
| [19] | Liu Y Q, He X X, Fu Y S, et al. Kinetics and mechanism investigation on the destruction of oxytetracycline by UV-254 nm activation of persulfate[J]. Journal of Hazardous Materials, 2016, 305: 229-239. DOI:10.1016/j.jhazmat.2015.11.043 |
| [20] |
朱思瑞, 高乃云, 鲁仙, 等. 热激活过硫酸盐氧化降解水中双酚A[J]. 中国环境科学, 2017, 37(1): 188-194. Zhu S R, Gao N Y, Lu X, et al. Degradation of bisphenol A in aqueous solution by thermally activated sulfate oxidation[J]. China Environmental Science, 2017, 37(1): 188-194. |
| [21] | Gao Y Q, Gao N Y, Yin D Q, et al. Oxidation of the β-blocker propranolol by UV/persulfate:effect, mechanism and toxicity investigation[J]. Chemosphere, 2018, 201: 50-58. DOI:10.1016/j.chemosphere.2018.02.158 |
| [22] |
高乃云, 胡栩豪, 邓靖, 等. 紫外激活过硫酸盐降解水中卡马西平研究[J]. 华中科技大学学报:自然科学版, 2013, 41(12): 117-122. Gao N Y, Hu X H, Deng J, et al. Study on UV-activated persulfate oxidation of carbamazepine in water[J]. Journal of Huazhong University of Science and Technology (Natural Science Edition), 2013, 41(12): 117-122. |
| [23] | Zhang W Q, Zhou S Q, Sun J L, et al. Impact of chloride ions on UV/H2 O2 and UV/persulfate advanced oxidation processes[J]. Environmental Science & Technology, 2018, 52(13): 7380-7389. |
| [24] |
蒋梦迪, 张清越, 季跃飞, 等. 热活化过硫酸盐降解三氯生[J]. 环境科学, 2018, 39(4): 1661-1667. Jiang M D, Zhang Q Y, Ji Y F, et al. Degradation of triclosan by heat activated persulfate oxidation[J]. Environmental Science, 2018, 39(4): 1661-1667. |
| [25] | Gu D M, Guo C S, Lv J P, et al. Removal of methamphetamine by UV-activated persulfate:Kinetics and mechanisms[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2019, 379: 32-38. DOI:10.1016/j.jphotochem.2019.05.009 |
| [26] | Keen O S, Love N G, Linden K G. The role of effluent nitrate in trace organic chemical oxidation during UV disinfection[J]. Water Research, 2012, 46(16): 5224-5234. DOI:10.1016/j.watres.2012.06.052 |
| [27] | Deng J, Shao Y S, Gao N Y, et al. Degradation of the antiepileptic drug carbamazepine upon different UV-based advanced oxidation processes in water[J]. Chemical Engineering Journal, 2013, 222: 150-158. DOI:10.1016/j.cej.2013.02.045 |
| [28] |
孙昕, 史路肖, 张燚, 等. 真空紫外/过二硫酸盐去除饮用水中嗅味物质[J]. 环境科学, 2018, 39(5): 2195-2201. Sun X, Shi L X, Zhang Y, et al. Removal of odorants in drinking water using VUV/persulfate[J]. Environmental Science, 2018, 39(5): 2195-2201. |
| [29] | Shah N S, He X X, Khan H M, et al. Efficient removal of endosulfan from aqueous solution by UV-C/peroxides:a comparative study[J]. Journal of Hazardous Materials, 2013, 263: 584-592. DOI:10.1016/j.jhazmat.2013.10.019 |
| [30] | Hu R K, Zhang L F, Hu J Y. Investigation of ozonation kinetics and transformation products of sucralose[J]. Science of the Total Environment, 2017, 603-604:8-17. |
| [31] | Xu Y, Wu Y, Zhang W, et al. Performance of artificial sweetener sucralose mineralization via UV/O3 process:Kinetics, toxicity and intermediates[J]. Chemical Engineering Journal, 2018, 353: 626-634. DOI:10.1016/j.cej.2018.07.090 |
| [32] | Fu Y Y, Wu G, Geng J J, et al. Kinetics and modeling of artificial sweeteners degradation in wastewater by the UV/persulfate process[J]. Water Research, 2019, 150: 12-20. DOI:10.1016/j.watres.2018.11.051 |
| [33] | Fu Y Y, Li S N, Shi Y F, et al. Removal of artificial sweeteners using UV/persulfate:Radical-based degradation kinetic model in wastewater, pathways and toxicity[J]. Water Research, 2019, 167: 115102. DOI:10.1016/j.watres.2019.115102 |
 2020, Vol. 41
2020, Vol. 41